0 引言
【研究意义】禽流感是由A型流感病毒引起的一种禽类感染或疾病综合症,A型流感病毒不仅对养殖业造成严重的危害[1],同时具有直接感染人的能力,也给人类心理和身体健康造成巨大威胁[2]。为有效防控高致病性禽流感,我国采取对全国所有家禽进行强制免疫的政策[3]。【前人研究进展】目前国内的禽流感疫苗生产工艺主要采用鸡胚进行接种增殖,但这种生产工艺中,病毒连续传代可能导致抗原性变异、鸡胚存在可能的外源因子污染、尿囊液中杂质多、鸡胚残体无害化处理成本高,如果禽流感暴发,鸡群大量死亡,鸡胚供应会成为瓶颈[4],这种工艺将逐渐被基于动物细胞培养的生产工艺淘汰[5]。一些欧美国家,已经批准基于动物细胞培养生产的流感疫苗上市[6,7,8]。以哺乳动物细胞作为流感病毒增殖的基质生产疫苗,具有重复性高、生产稳定、抗原特性更接近自然株、变态反应少等优势[9]。成熟的动物细胞规模化培养技术采用“细胞工厂”或微载体悬浮培养技术,其原理是增加细胞黏附生长的表面积来增加细胞密度[10],虽然微载体悬浮培养能使细胞获得较高的细胞密度,但其操作工艺繁琐,增加了生产时间与生产成本[11],应用具有局限性。【本研究切入点】MDCK细胞是最适于生产甲型流感病毒和乙型流感病毒的三种细胞之一[12,13],可以生产安全有效的人用和兽用疫苗,产毒能力高。采用可连续培养传代的MDCK悬浮细胞在生物反应器中进行禽流感病毒的大规模增殖制备,不但可以突破了各种限制,节约成本,还可大大提高培养密度和产物制备效率[14],经逐级放大培养后可以制备出有效、安全和高产量的流感病毒疫苗,是目前兽用疫苗生产领域的前沿技术。【拟解决的关键问题】本试验中以驯化成功的悬浮MDCK细胞为基质,增殖重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株、H5N1 Re-8株,制备成三价灭活疫苗,免疫海兰褐商品蛋鸡和长白飞鸭,检测血清中的HI抗体效价,评估细胞源三价灭活疫苗的免疫效果。1 材料与方法
本研究于2017年1—12月进行,商品蛋鸡试验在吉林省梅河口市得利鸡场;商品鸭试验在梅河口市方正鸭场。1.1 材料
1.1.1 细胞株及病毒株 贴壁MDCK细胞由西北民族大学甘肃省动物细胞工程技术研究中心从ATCC引进,引进时间:2011年2月,ATCC编号:CCL-34,代次:P56,保存号:58860056。重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株、H5N1 Re-8株购自中国农业科学院哈尔滨兽医研究所。
1.1.2 主要试剂
1.1.2.1 胎牛血清(FBS)、新生牛血清(NBS)购自兰州民海生物工程有限公司;DMEM、DMEM/F12(1﹕1)购自HyClone公司;生物素、氯化胆碱、维生素、葡萄糖、氨基酸等成分配制而成的MDCK无血清培养基,1%鸡红细胞悬液由吉林冠界生物技术有限公司制备;SPF鸡胚购自梅里亚公司。
1.1.2.2 禽流感病毒H5亚型Re-6株、Re-7株和Re-8株HI试验抗原及阳性血清,均购自哈尔滨维科生物技术开发公司。
1.1.3 仪器设备 细胞摇床购自德国Eppendorf公司,倒置显微镜购自Olympus公司,5 L生物反应器购自艾贝泰公司,计数仪为Count star全自动细胞计数仪。
1.1.4 试验动物 海兰褐蛋鸡[15]6 050只;长白飞鸭[16]220只。
1.2 方法
1.2.1 悬浮MDCK细胞的驯化及生物学特性[17]。1.2.1.1 驯化MDCK细胞适应低血清培养 在静置培养的条件下,用含8% FBS的培养液培养MDCK细胞,逐步降低培养液中FBS的含量,至细胞适应含2% FBS的培养液。用NBS替代FBS,适应后将细胞消化转移至摇床上培养(30 mL,30 r/min),每天测定葡萄糖含量,低于1 g·L-1进行换液。待细胞比生长速率稳定后,每次传代前密度调整为约5.0×105cells/mL,并逐步提高摇床转速。直至细胞完全失去黏附瓶壁的能力,以悬浮方式稳定增殖。
1.2.1.2 驯化MDCK细胞适应无血清悬浮培养 以适应了2% NBS的MDCK细胞为基础,逐步调整MDCK无血清培养基配方成分,直至完全适应MDCK无血清培养基。
1.2.1.3 无血清适应及在摇瓶中的生长情况 将MDCK细胞以1.5×106 cells/mL的密度接种至250 mL Corning摇瓶中,培养体积为80 mL,转速120 r/min,培养基为MDCK无血清培养基。每24 h取样监测培养液中的葡萄糖含量并进行计数,绘制生长曲线。
1.2.1.4 在5L反应器中的生长情况 将MDCK细胞以1.5×106 cells/mL的密度放大至5L反应器,有效培养体积为4 L,控制关键参数(温度为(37±0.5)℃,pH 7.0±0.1,溶氧30%—50%,搅拌转速150 r/min),每24 h取样监测培养液中的葡萄糖含量并进行计数,绘制生长曲线。
1.2.2 重组禽流感病毒的增殖
1.2.2.1 在悬浮MDCK细胞中的增殖 分别将重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株和H5N1 Re-8株按MOI为10-2接种至细胞密度为4.5—5.0×106 cells/mL,有效培养体积为4 L生物反应器,培养条件为温度(34±0.5)℃,pH 7.3±0.1,溶氧30%—50%,搅拌转速150 r/min,TPCK-胰酶终浓度为5 μg·mL-1。
1.2.2.2 在贴壁MDCK细胞中的增殖 分别将重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株和H5N1 Re-8株按MOI为10-2接种至生长良好的MDCK细胞单层,培养条件为温度34℃,TPCK-胰酶终浓度为2 μg·mL-1。
1.2.3 病毒HA效价、TCID50、EID50的测定
1.2.3.1 HA效价测定 测定方法参照文献[18]进行。
1.2.3.2 TCID50测定 将收获的各重组禽流感病毒用DMEM培养基作10倍系列稀释,取10-5、10-6、10-7、10-8 4个稀释度,接种生长良好的MDCK细胞单层96孔培养板,每个稀释度接种4孔,0.1 mL/孔,同时设正常细胞对照,置37℃、5% CO2培养箱中培养3—4 d,逐日观察并记录CPE,按Reed- Muench法计算TCID50。
1.2.3.3 EID50测定 将收获的各重组禽流感病毒用灭菌生理盐水作10倍系列稀释,取10-6、10-7、10-8 3个稀释度,各尿囊腔内接种10日龄SPF鸡胚5枚,每胚0.1 mL,置36℃孵育72 h,逐个收获鸡胚液,分别测定HA效价,HA效价不低于1﹕16判为感染,按Reed-Muench法计算EID50。
1.2.4 灭活疫苗的免疫 将上述以悬浮MDCK细胞为基质生产的毒液制备成重组禽流感病毒(H5亚型)三价灭活疫苗(细胞源,Re-6株+ Re-7株+Re-8株),与鸡胚源重组禽流感病毒(H5亚型)三价灭活疫苗(Re-6株+ Re-7株+Re-8株)分别在商品鸡场与商品鸭场同时免疫,检测禽流感HI抗体效价。
1.2.4.1 商品鸡场 品种为海兰褐商品蛋鸡:6 050只,分为3组,2组为免疫组,每组3 000只,50只不免疫作为对照组,首次免疫:28日龄,0.5 mL/只;二次免疫:80日龄,0.5 mL/只;采血[19]时蛋鸡日龄分别为49日龄、110日龄、210日龄,免疫组随机采集50只血清样本,对照组随机采取10只,进行血凝抑制试验,计算每组鸡HI抗体效价几何平均值(GMT)。
1.2.4.2 商品鸭场 品种为长白飞鸭,220只,分为3组,2组为免疫组,每组100只,不免疫对照组20只,同等条件下隔离饲养。首次免疫:10日龄,0.5 mL/只;二次免疫:24日龄,1.0 mL/只;采血时鸭日龄分别为24、38、52日龄,免疫组随机采集20只血清样本,对照组随机采取10只血清样本,每份血清样本采用20%鸡红细胞吸附处理,本法采用0.5 mL血清与0.5 mL 20%鸡红细胞混合,轻振后,静置60 min,吸取上清0.5 mL备用,进行血凝抑制试验,计算每组HI抗体效价几何平均值(GMT)
2 结果
2.1 驯化过程中MDCK细胞生长性能的比较
2.1.1 静置培养条件下生长情况的比较 从最初培养液中血清浓度为8% FBS,逐步降低至2% NBS,培养液使用量均为10 mL,其细胞状态见图1-A和B,生长曲线比较见图1-C。经长时间的驯化,细胞已适应低血清环境,生长速度虽比8% FBS组稍慢,但细胞状态良好,活率(活细胞数/总细胞数)较高。 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图1静置培养条件下生长情况的比较
A血清浓度为8%FBS;B血清浓度为2%NBS;C生长曲线
-->Fig. 1Comparison of growth under the condition of static
A: Serum concentration is 8% FBS; B: Serum concentration is 2% NBS; C: Growth curve
-->
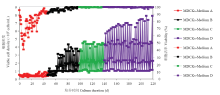
2.1.2 MDCK细胞驯化悬浮过程 细胞无血清全悬浮驯化初期,细胞几乎不生长,活率也维持在一个较低的水平,经过一段时间的适应传代以及培养基组份的不断调整,经过4个不同培养体系,细胞逐渐适应并开始生长,细胞密度由(3.0—4.0)×106 cells/mL,活率保持在90%以上;最终稳定至细胞生长第3天时密度可达(7.0—8.0)×106 cells/mL,活率保持在99%以上。MDCK细胞悬浮驯化过程细胞密度和细胞活率变化见图2。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图2MDCK细胞悬浮驯化过程细胞密度和细胞活率图谱
-->Fig. 2Map of cell density and cell viability during MDCK cell acclimation and suspension
-->
2.1.3 悬浮细胞传代数据 驯化后的悬浮细胞冻存
建库保存,复苏以后,通常第3天就可恢复生长,细胞密度(8.0—9.0)×106 cells/mL,活率保持在99%以上。悬浮MDCK细胞复苏后的细胞密度和细胞活率见图3。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图3悬浮MDCK细胞复苏后的细胞密度和细胞活率图谱
-->Fig. 3Cell density and cell viability map after the recovery of suspension MDCK cells
-->
2.1.4 悬浮培养条件下的生长特性 在2% NBS静置培养的基础上,不断调整MDCK无血清培养基成分,驯化出可高密度无血清悬浮培养的MDCK细胞,细胞倍增时间明显缩短,形态近圆形、大小基本均一、单个悬浮于培养液中。以1.5×106 cells/mL的细胞密度分别接种摇瓶和5 L反应器,每隔24 h取样计数,绘制生长曲线,比较两者的差异,见图4。5 L反应器中增殖速度高于摇瓶,这是由于反应器的培养条件更为恒定,能为细胞的生长代谢提供更充分的氧并有效排除二氧化碳[20]。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图4摇瓶及5 L反应器中生长情况
A.摇瓶中的细胞状态;B. 5 L反应器中的细胞状态;C.生长曲线
-->Fig. 4Growth in a shaker and 5 L reactor
A. Cell state in a shaker; B. Cell state in 5 L reactor; C. Growth curve
-->
2.2 H5亚型重组禽流感病毒含量的比较
分别以贴壁及悬浮MDCK细胞为基质制备重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株和H5N1 Re-8株,病毒含量的结果比较见表1。经分析,两种细胞制备的禽流感病毒含量相当,说明驯化的悬浮MDCK细胞对病毒的敏感性与贴壁细胞一致,适用于病毒的增殖。Table 1
表1
表1不同细胞制备的重组禽流感病毒含量比较
Table 1Comparison of the price of reassortant avian influenza virus produced by different cells
| 毒株 Strain | 细胞 Cell | HA | TCID50 /mL | EID50/0.1 mL |
|---|---|---|---|---|
| H5N1 Re-6株 H5N1 Re-6 strain | 贴壁MDCK细胞Adherent MDCK cell | 1﹕512 | 108.0 | 107.83 |
| 悬浮MDCK细胞Suspended MDCK cell | 1﹕1024 | 107.67 | 107.83 | |
| H5N1 Re-7株 H5N1 Re-7 strain | 贴壁MDCK细胞Adherent MDCK cell | 1﹕256 | 107.33 | 107.375 |
| 悬浮MDCK细胞Suspended MDCK cell | 1﹕512 | 107.33 | 107.17 | |
| H5N1 Re-8株 H5N1 Re-8 strain | 贴壁MDCK细胞Adherent MDCK cell | 1﹕512 | 108.33 | 108.5 |
| 悬浮MDCK细胞Suspended MDCK cell | 1﹕1024 | 108.5 | 108.38 |
新窗口打开
2.3 HI抗体测定结果
2.3.1 海兰褐商品蛋鸡HI抗体结果 细胞源禽流感病毒灭活疫苗在商品鸡场进行免疫试验,免疫21天后禽流感H5亚型 Re-6株、Re-7株、Re-8株平均抗体效价(GMT)分别为1﹕446、1﹕111、1﹕416,首免后60 d鸡群抗体有所下降,选择在鸡群80日龄进行二次免疫,二免后30 d HI抗体效价均能达到1﹕588、1﹕362、1﹕776,210日龄三者平均抗体效价(GMT)分别为1﹕239、1﹕128、1﹕223,维持了较高的抗体水平(表2)。2.3.2 长白飞鸭HI抗体结果 细胞源禽流感病毒灭活疫苗在商品鸭场进行免疫试验,经过两次免疫,2周后禽流感H5亚型 Re-6株、Re-7株、Re-8株平均抗体效价(GMT)分别为1﹕194、1﹕91、1﹕137,4周后平均抗体效价(GMT)可达到1﹕416、1﹕128、1﹕239。可对鸭群产生保护(表3)。
Table 2
表2
表2海兰褐商品蛋鸡血清HI抗体结果
Table 2Results of Hy-line brown laying hens antibody(GMT)
| 日龄 Day age | 来源 Source | Re-6株HI抗体效价 antibody titer of strain Re-6 | Re-7株HI抗体效价 antibody titer of strain Re-7 | Re-8株HI抗体效价 antibody titer of strain Re-8 |
|---|---|---|---|---|
| 49 | 细胞源Cell source | 1﹕446 | 1﹕111 | 1﹕416 |
| 鸡胚源Chicken embryos source | 1﹕478 | 1﹕147 | 1﹕512 | |
| 对照组Control group | <1﹕2 | <1﹕2 | <1﹕2 | |
| 110 | 细胞源Cell source | 1﹕1261 | 1﹕362 | 1﹕1783 |
| 鸡胚源Chicken embryos source | 1﹕1176 | 1﹕446 | 1﹕1783 | |
| 对照组Control group | 1﹕1.7 | 1﹕1.2 | 1﹕1.4 | |
| 210 | 细胞源Cell source | 1﹕239 | 1﹕128 | 1﹕223 |
| 鸡胚源Chicken embryos source | 1﹕274 | 1﹕194 | 1﹕294 | |
| 对照组Control group | <1﹕2 | <1﹕2 | <1﹕2 |
新窗口打开
Table 3
表3
表3长白飞鸭血清HI抗体结果
Table 3Results of Changbai flying duck HI antibody (GMT)
| 日龄 Day age | 来源 Source | Re-6株HI抗体效价 HI antibody titer of strain Re-6 | Re-7株HI抗体效价 HI antibody titer of strain Re-7 | Re-8株HI抗体效价 HI antibody titer of strain Re-8 |
|---|---|---|---|---|
| 24 | 细胞源Cell source | 1﹕30 | 1﹕17 | 1﹕64 |
| 鸡胚源Chicken embryos source | 1﹕37 | 1﹕18 | 1﹕52 | |
| 对照组Control group | <1﹕2 | <1﹕2 | <1﹕2 | |
| 38 | 细胞源Cell source | 1﹕588 | 1﹕91 | 1﹕776 |
| 鸡胚源Chicken embryos source | 1﹕630 | 1﹕74 | 1﹕724 | |
| 对照组Control group | <1﹕2 | <1﹕2 | <1﹕2 | |
| 52 | 细胞源Cell source | 1﹕416 | 1﹕128 | 1﹕239 |
| 鸡胚源Chicken embryos source | 1﹕416 | 1﹕119 | 1﹕256 | |
| 对照组Control group | <1﹕2 | <1﹕2 | <1﹕2 |
新窗口打开
3 讨论
利用动物传代细胞生产禽流感疫苗,可在短期内大规模增殖病毒,在疫病爆发时提供足够的疫苗产品,降低了病毒在鸡胚中连续传代而引起HA基因发生变异的概率,使疫苗的免疫效果更可靠。MDCK悬浮细胞的大规模培养,可以有效扩大细胞的生长密度,既保留禽流感病毒在其中的增殖优势,又克服其产量低的缺点[21]。试验中采用逐步降低血清含量并调整无血清培养基配方的方法,在整个驯化过程中经过了4种体系的逐步适应,最终获得可无血清悬浮培养的MDCK细胞,此株细胞能够稳定连续传代,适应高密度生长,细胞保持较高的活力,从摇瓶放大至5L反应器,生长稳定。此研究掌握了一种MDCK悬浮细胞驯化的方法,其他贴壁细胞的驯化也可借鉴此类方法。此细胞株对重组禽流感病毒H5N1 Re-6株、H5N1 Re-7株、H5N1 Re-8株均敏感,病毒在其上的增殖能力与贴壁型MDCK相当,可获得较高的病毒滴度;但贴壁型MDCK增殖病毒的操作过程繁琐、同一批次不同细胞瓶中病毒的滴度也存在差异、时间成本大。利用MDCK悬浮细胞生产的病毒产量远远高于贴壁培养,且同一批次的病毒质量更均一稳定,为后续逐级放大至6000L反应器奠定了基础。
家禽的日龄、品种及饲养管理条件不同,对疫苗免疫的敏感性也不一致,HI抗体效价产生的时间和所能达到的HI抗体水平及维持时间也存在相应的差别[22]。以此株悬浮细胞为基础制备禽流感灭活疫苗,在商品鸡场进行免疫试验,28日龄首次免疫,21天后禽流感H5亚型 Re-6株、Re-7株、Re-8株平均抗体效价(GMT)分别为1﹕446、1﹕111、1﹕416,首免后50—60 d抗体有所下降,因此选择在80日龄进行二免,210日龄三者平均抗体效价(GMT)分别为1﹕239、1﹕128、1﹕223,维持了较高的抗体水平。鸭的高致病性禽流感免疫一般需要二次接种才能产生较高的抗体水平[23]。不同日龄的蛋鸭经免疫接种后抗体效价并不一致[24],如果血清抗体效价在免疫接种临界值1﹕32—1﹕64之间,就需要接种免疫;如果血清抗体效价在1﹕64以上,可以不接种免疫[25]。商品鸭场进行的免疫试验,52 d时禽流感H5亚型 Re-6株、Re-7株、Re-8株平均抗体效价(GMT)分别为1﹕416、1﹕128、1﹕239,从这个试验可以看出试验结果与鸡胚源重组禽流感灭活疫苗免疫后诱导产生的HI抗体效价相当。
对于疫苗质量,国家高度重视,农业部颁布了疫苗制造规程和质量标准,并对疫苗生产企业采取了严格的管理措施和市场准入制度,为疫病的防控起到了重要作用[26]。对于重组禽流感病毒灭活疫苗的生产,凡是采用浓缩工艺的,疫苗的效力明显好于非浓缩工艺。因此当抗原的血凝价达不到配制三价疫苗的要求时,需要进行适当的浓缩[27]。鸡胚作为疫苗的生产基质,还存在大规模生产时供给困难、潜在的外源病毒污染以及批间差异较大的问题[28],相信随着生物技术的不断进步,新的技术将会不断的用于禽流感疫苗的生产,新型禽流感疫苗将会不断推出[29]。利用连续细胞培养系统生产流感疫苗其优点为可规模化快速大量生产,易于质量控制,纯度高,稳定性好[30],将会成为未来的禽流感灭活疫苗生产的主要工艺。
4 结论
以本文所述方法驯化的MDCK悬浮细胞为基础制备禽流感灭活疫苗,商品鸡在免疫后21 d禽流感H5亚型Re-6株、Re-7株、Re-8株平均抗体效价(GMT)均达到或高于国家标准。在80日龄进行二免,210日龄后测定三者平均抗体效价均超过国家标准维持较高的抗体水平。长白飞鸭二次 免疫后平均抗体效价也均达到或是超过国家标准。因此该生产工艺可用于禽流感灭活疫苗的大规模生产。The authors have declared that no competing interests exist.
