 ,1
,1Effects of LED Light Withering at Different Temperatures on Expression of Key Genes in the Upstream of MEP and Formation of Volatiles in Tieguanyin Tea
YOU FangNing1, DENG HuiLi1, HU Juan1, YAO ZhiLing1, WU ShuaiQiang1, QIN YiJia1, TANG TongHua2, SUN Yun ,1
,1通讯作者:
责任编辑: 赵伶俐
收稿日期:2019-02-28接受日期:2019-06-5网络出版日期:2020-01-16
| 基金资助: |
Received:2019-02-28Accepted:2019-06-5Online:2020-01-16
作者简介 About authors
游芳宁,E-mail:youfangning123@163.com。

摘要
关键词:
Abstract
Keywords:
PDF (515KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
游芳宁, 邓慧莉, 胡娟, 姚知灵, 武帅强, 秦艺嘉, 汤铜华, 孙云. 不同温度LED光萎凋对铁观音MEP上游关键基因和香气的影响[J]. 中国农业科学, 2020, 53(2): 346-356 doi:10.3864/j.issn.0578-1752.2020.02.009
YOU FangNing, DENG HuiLi, HU Juan, YAO ZhiLing, WU ShuaiQiang, QIN YiJia, TANG TongHua, SUN Yun.
0 引言
【研究意义】萜类化合物是乌龙茶挥发性芳香物质的重要组分,芳香物质主要通过2-C-甲基-D-赤藓醇-4-磷酸途径(MEP)上游关键基因(DXS、DXR、HDS、HDR)直接参与调控合成。1-脱氧-D-木酮糖-5-磷酸合成酶(DXS)和脱氧木酮糖-5-磷酸还原异构酶(DXR)是MEP途径的第一、第二个限速酶,调控单萜、双萜类香气化合物以及类胡萝卜素等重要物质的合成,研究表明UV-B[1]、日光[2]和虫害[3]等均等促进DXR的相对表达量。4-羟基-2-甲基-2-E-丁烯基-4-焦磷酸合酶(HDS)和4-羟基-2-甲基-2-E-丁烯基-4-焦磷酸还原酶(HDR)是MEP途径的最后一步反应所需要的酶,能催化1-羟基-2-甲基-2-(E)-丁烯基?4-二磷酸HMBPP 转化为异戊烯基焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP)的混合物,其表达量的变化直接影响萜类代谢物的产量[1,4]。光照是一种重要的植物外源调控因子,与茶鲜叶和萎凋叶内香气成分的生物合成有重要关联[5,6,7]。铁观音有“七泡有余香”之誉,其馥郁的兰花香与萎凋工序密切相关。因此,以铁观音为试验材料开展不同温度LED光萎凋研究,探明温度与光对萎凋叶萜类上游关键基因表达量和香气含量的影响,对于提高乌龙茶萎凋叶香气含量具有重要意义。【前人研究进展】研究表明,铁观音日光萎凋的时间过长或过短,均会导致毛茶花果香味不明显,夹带杂味[8]。FU等[9]研究发现短时(3 d)LED补光栽培‘金萱’品种鲜叶的萜类化合物含量比长时处理(14 d)高;陈寿松等[10,11]对铁观音萎凋和摇青过程进行补光试验,得出经LED处理后,毛茶中的橙花叔醇和α-法呢烯等主要呈香物质含量较全程无光显著提升;可见光照对乌龙茶萜类化合物的形成具有显著调控作用。目前,前人大多把光和温度作为统一的外在胁迫因子来研究其对茶叶生理生化的影响[12,13,14]。【本研究切入点】温度对萎凋工序的影响至关重要,温度过高过低均影响茶叶的香气品质。在茶叶萎凋过程中,尚未见到将光照系统区分为光与温度两个影响因子的报道。【拟解决的关键问题】本研究利用自主研制的乌龙茶调温排湿LED光补偿萎凋装置(Oolong tea LED withering equipment,OLW),简称“LED光萎凋装置”[10],系统研究不同光和温度对乌龙茶香气组分的影响。由于LED是冷光源,光谱中不存在紫外线和红外线,因此不具有热量和辐射,与温度共同试验处理研究,更为贴近生产实际。基于这一原理,从笔者课题组转录组数据筛选出响应光照的萜类上游关键基因(DXS、DXR、HDS、HDR),以铁观音为供试材料,设计不同LED加温度的萎凋处理试验,分别测定各铁观音萎凋叶的香气组分和MEP上游关键基因的相对表达量。结合分子和代谢水平研究,综合评价和总结不同温度和LED光萎凋处理对乌龙茶香气品质形成的工艺特点及变化规律,为乌龙茶人工光源萎凋提供理论依据。1 材料与方法
1.1 试验材料和设备
1.1.1 试验材料 品种为铁观音,2018年5月采摘一芽三叶铁观音鲜叶,经3次重复测定,鲜叶含水率为(74.2±1.0)%。1.1.2 试验装置 自主研制的乌龙茶调温排湿LED光补偿萎凋装置。主要由箱体、LED灯源、增湿装置等构成,箱体四壁安装匀光板,以消除光边界效应,控制各点光强在(400±10)μmol∙m-2·s-1;热泵机组春季制热夏季制冷,控制萎凋温度(20—50℃);排湿风扇和气流循环通道及时排除萎凋过程的水蒸汽。
1.1.3 试验仪器 Agilent 6890N-5975B气相色谱—质谱联用仪,安捷伦科技有限公司;BAS124S型电子天平(精度0.0001 g),梅特勒-托利多仪器有限公司;Allegra 64R台式高速冷冻离心机,美国贝克曼库尔特有限公公司;Agilent 6890N-5975B气相色谱—质谱联用仪,安捷伦科技有限公司;IMS-70全自动雪花制冰机,上海声裕生物科技有限公司;超微量分光光度计(Thermo Electron corp.USA);罗氏LightCycler480,天津津立仪器设备科技发展有限公司(天津),荧光共聚焦显微镜FV1000,OLYMPUS公司;LED白光灯源,深圳拓邦股份有限公司;其他常规检测仪器等。
1.2 试验方法
1.2.1 试验方案设计 设计LED与温度共同作用和单独温度作用的萎凋处理,以鲜叶为对照,其中Dark组处理为黑暗条件处理,详情见表1。LED光萎凋装置参数:光照强度(400±5)μmol∙m-2·s-1,相对湿度(60±2)%;LED距萎凋叶15 cm,摊叶厚度10 mm;取样时,萎凋叶含水率经3次重复测定,为(68.4±1.3)%。Table 1
表1
表1不同温度LED光萎凋条件下铁观音的处理方法
Table 1
| 处理名称 Treatment name | 样品处理方法 Sample processing method |
|---|---|
| XY | 铁观音鲜叶 Fresh leaves |
| L20 | LED白光+20℃条件下萎凋60 min Withered 60 min at condition of LED white light and 20℃ |
| L25 | LED白光+25℃条件下萎凋60 min Withered 60 min at condition of LED white light and 25℃ |
| L30 | LED白光+30℃条件下萎凋60 min Withered 60 min at condition of LED white light and 30℃ |
| L35 | LED白光+35℃条件下萎凋60 min withered 60 min at condition of LED white light and 35℃ |
| L40 | LED白光+40℃条件下萎凋60 min Withered 60 min at condition of LED white light and 40℃ |
| D20 | 20℃无光条件下萎凋60 min Withered 60 min at condition of dark and 20℃ |
| D25 | 25℃无光条件下萎凋60 min Withered 60 min at condition of dark and 25℃ |
| D30 | 30℃无光条件下萎凋60 min Withered 60 min at condition of dark and 30℃ |
| D35 | 35℃无光条件下萎凋60 min withered 60min at condition of dark and 35℃ |
| D40 | 40℃无光条件下萎凋60 min withered 60 min at condition of dark and 40℃ |
新窗口打开|下载CSV
1.2.2 样品取样方法 铁观音鲜叶和各处理萎凋叶分别取30 g,称样结束立刻用液氮冷冻固样,后置于-80℃超低温保存箱冻存。主要用于总RNA提取,qRT-PCR及香气测定。
1.2.3 测定项目与方法
1.2.3.1 茶树总RNA的提取及cDNA的合成方法 试验使用天根多糖多酚植物试剂盒,参考说明书操作步骤提取茶树总RNA,通过超微量分光光度计测定RNA浓度及OD值,最后采用1%琼脂糖凝胶电泳检测其完整性。按照TaKaRa的PrimeScriptTM 1st strand cDNA Synthesis Kit试剂盒合成cDNA,用于后续的qRT-PCR测定。
1.2.3.2 萜类上游关键基因实时荧光定量PCR分析 根据DXS、DXR、HDS和HDR全长cDNA序列设计实时荧光定量PCR特异性引物,详见表2,采用TaKaRa公司提供的SYBR Ex-ScriptTM试剂盒,按照说明书进行试验操作,具体情况参照LIN和LAI[15]的操作步骤,以20 μL反应体系进行qRT-PCR测定,采用GDPDH为内参基因,通过罗氏Light cyclers480荧光定量PCR仪,采用qRT-PCR检测铁观音鲜叶的DXS、DXR、HDS和HDR在不同温度和光照萎凋处理下的表达情况。采用2-ΔΔCt方法对试验数据进行计算分析。
Table 2
表2
表2引物序列
Table 2
| 引物名称 Primer name | 序列 Sequence (5'→3') | 用途 Function |
|---|---|---|
| DXS-qF | GGATGGTGGGTGGTTCAG | 实时荧光定量PCR qRT-PCR |
| DXS-qR | ATGAGAACAGGTCCAGGTGC | 实时荧光定量PCR qRT-PCR |
| DXR-qF | CGGGATAAACTACCTTGACATT | 实时荧光定量PCR qRT-PCR |
| DXR-qR | TTCCTCGCCCACAAGTCAT | 实时荧光定量PCR qRT-PCR |
| HDS-qF | AACCCTCTCTTTCTCTCTCTCG | 实时荧光定量PCR qRT-PCR |
| HDS-qR | TCTGTTGTGGTCATCGTTTG | 实时荧光定量PCR qRT-PCR |
| HDR-qF | GTGTTGAGAGGGCAGTCCA | 实时荧光定量PCR qRT-PCR |
| HDR-qR | AGCAGGCAGAACCACGACA | 实时荧光定量PCR qRT-PCR |
| GDPDH-qF | TTTGGTGAGAAAGCAGTAG | 内参基因Reference gene |
| GDPDH-qR | TGGGCAGCAGCCTTATCCT | 内参基因Reference gene |
新窗口打开|下载CSV
1.2.3.3 HS-SPME-GC-MS香气组分测定 采用顶空固相微萃取HS-SPME提取香气,称取10.0 g磨碎茶样加入2 mg∙mL-1癸酸乙酯(内标)25 μL,100 mL沸腾蒸馏水,放于磁力搅拌器上(转速450 r/min),在50℃干燥箱中平衡5 min后再吸附40 min,最后在GC-MS进样口于230℃下解析5 min。GC-MS条件:色谱柱:HP-5MS(30 m×0.25 mm ID×0.25 μm膜厚);载气为高纯氮气,99.999%;进样口温度:230℃;脉冲不分流,进样1 μL,柱流速:1 mL∙min-1;色谱-质谱接口温度:250℃。离子源温度:230℃;离子化学式:EI;电子能量:70 eV;程序升温参数:50℃保持2 min,以5 ℃∙min-1升至180℃,保持2 min,再以10 ℃∙min-1升到230℃,保持5 min,最后进行NIST数据库匹配质谱定性和峰面积归一法相对定量分析。
1.3 数据处理
采用Microsoft Office Excel和SPSS19.0软件进行数据分析,单因素方差(one-way ANOVA)和Duncan’s test、LSD显著性分析。2 结果
2.1 不同温度LED光萎凋对MEP途径上游关键基因表达量的影响
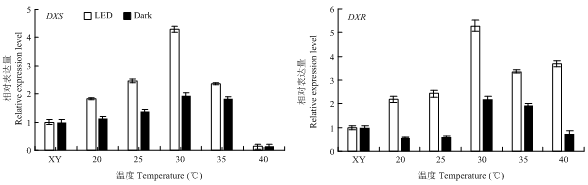
2.1.1 DXS和DXR相对表达量 如图1所示,经LED光照萎凋后,各温度处理萎凋叶DXS和DXR相对表达量均有所提高;其中LED组(L20、L25、L30、L35、L40)萎凋叶DXS表达量分别是无光处理温度组(D20、D25、D30、D35、D40)的1.61、1.82、2.24、1.29和0.96倍;L30和D30分别为LED组和黑暗组的最大值,表达量为4.31和1.92;各处理萎凋叶DXR相对表达量变化趋势和DXS基本一致,经光照处理萎凋叶DXR含量依次为无光处理的3.81、4.04、2.39、1.74和4.97倍;其中L30和D30含量分别为5.28和2.21,为各自处理组的最大值。结果表明,光照可以大幅度增加DXS和DXR的相对表达量,两基因的最适表达温度为30℃,且光照对DXR表达量的提升更显著。图1
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图1DXS和DXR在不同温度LED光萎凋过程中的相对表达量
Fig. 1Relative expression of DXS and DXR during LED light withering process under different temperatures
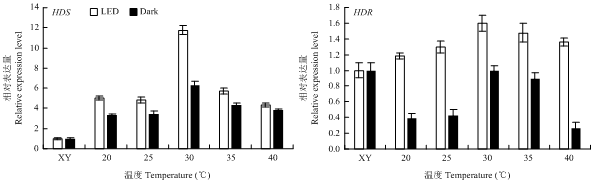
2.1.2 HDS和HDR相对表达量 不同处理萎凋叶HDS和HDR相对表达量如图2所示。经LED光照处理后,LED组萎凋叶HDS表达量依次是Dark组的1.51、1.40、1.86、1.33和1.13倍;LED组HDR表达量按序依次是Dark组的3.03、3.00、1.60、1.65和5.22倍;无论是HDS还是HDR的表达量均在30℃处理时达到最大值,其中L30的HDS和HDR表达量为11.77和1.59,D30的HDS和HDR表达量为6.34和0.99。结果证明,光照和温度对HDS和HDR的表达均有调控作用,光能大幅度提高两基因的表达量,30℃是其最适表达温度。
图2
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2HDS和HDR在不同温度LED光萎凋过程中的相对含量
Fig. 2Relative expression of HDS and HDR during LED light withering process under different temperatures
2.2 不同温度LED光萎凋对铁观音萎凋叶香气的影响
乌龙茶感官审评中,香气占35%的权重,是评判乌龙茶品质的重要因子之一[6,7,8,9,10,11,12,13,14,15,16,17,18]。经HS-SPME结合GC-MS对不同温度处理的铁观音萎凋叶进行香气组分检测(表3)可知,鲜叶(对照)和10个处理测出的相对含量最高的前10位香气组分分别为:芳樟醇氧化物II(0.06%—15.19%)、α-法呢烯(0.08%—15.13%)、香叶醇(2.38%—17.66%)乙酸叶醇酯(2.32%—15.18%)、芳樟醇(4.32%—10.46%)、芳樟醇氧化物I(2.33%—7.25%)、顺式-己酸-3-己烯酯(0.12%—7.05%)、苯乙醇(0.48%—3.57%)、橙花叔醇(0.33%—4.04%)和脱氢芳樟醇(0.95%—4.11%)。本研究筛选出相对含量前25的香气组分(除对照外,各萎凋叶香气组分含量均大于0.1%),差异性分析得出,与铁观音毛茶不同,毛茶中的橙花叔醇、α-法呢烯和吲哚的相对含量占极大比重[19,20,21],在萎凋叶中,萜类化合物中的芳樟醇(铃兰香)、芳樟醇氧化物I(淡花香)[22]、芳樟醇氧化物II(弱木香)、α-法呢烯(花香)、香叶醇(玫瑰花香)和乙酸叶醇酯(香蕉香)相对含量总量达到55.25%—69.01%,占铁观音萎凋叶的香气比重最高。Table 3
表3
表3不同温度LED光照处理铁观音萎凋叶主要香气组分的相对含量
Table 3
| 香气组分 Volatile compounds | 处理 Treatment | 处理 Treatment | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| XY | D20 | D25 | D30 | D35 | D40 | XY | L20 | L25 | L30 | L35 | L40 | |
| 芳醇氧化物II Linalool oxide II (X1) | 0.06 | 7.93 | 10.00 | 10.20 | 9.09 | 8.64 | 0.06 | 15.19 | 11.14 | 13.44 | 8.95 | 9.68 |
| α-法呢烯 α-Farnesene (X2) | 0.08 | 7.15 | 4.83 | 6.24 | 6.69 | 3.54 | 0.08 | 15.13 | 5.14 | 8.56 | 6.99 | 4.18 |
| 香叶醇 Geraniol (X3) | 2.38 | 11.51 | 11.10 | 16.50 | 10.42 | 9.70 | 2.38 | 16.34 | 11.58 | 17.66 | 13.08 | 12.37 |
| 乙酸叶醇酯 3-Hexen-1-ol,acetate,(Z) (X4) | 2.32 | 12.58 | 8.15 | 14.44 | 5.79 | 4.76 | 2.32 | 15.18 | 10.28 | 13.57 | 12.51 | 10.41 |
| 芳樟醇 Linalool (X5) | 4.32 | 8.88 | 8.29 | 9.83 | 8.84 | 7.88 | 4.32 | 9.45 | 9.33 | 10.46 | 9.01 | 8.60 |
| 芳醇氧化物I Linalool oxide I (X6) | 2.33 | 4.32 | 5.33 | 4.51 | 4.96 | 4.91 | 2.33 | 7.25 | 6.99 | 6.43 | 5.63 | 5.39 |
| 顺式-己酸-3-己烯酯 Hexanoic acid,3-hexenyl ester,(Z) (X7) | 0.12 | 3.11 | 2.33 | 3.13 | 4.28 | 3.78 | 0.12 | 7.05 | 2.33 | 3.13 | 4.17 | 3.05 |
| 苯乙醇 Phenylethyl Alcohol (X8) | 0.48 | 0.92 | 2.56 | 2.24 | 1.45 | 2.29 | 0.48 | 3.57 | 2.60 | 3.15 | 1.62 | 1.87 |
| 橙花叔醇 Nerolidol (X9) | 0.33 | 2.53 | 2.93 | 3.56 | 3.36 | 2.40 | 0.33 | 3.54 | 3.40 | 4.04 | 3.51 | 2.96 |
| 脱氢芳樟醇 1,5,7-Octatrien-3-ol,3,7-dimethyl (X10) | 0.95 | 3.39 | 2.89 | 2.79 | 3.69 | 2.29 | 0.95 | 3.49 | 3.92 | 4.11 | 3.82 | 1.40 |
| 吲哚 Indole (X11) | 1.20 | 1.76 | 2.37 | 2.13 | 3.23 | 2.36 | 1.20 | 3.12 | 3.02 | 3.39 | 3.50 | 2.59 |
| 叶醇 3-Hexen-1-ol (X12) | 0.87 | 1.09 | 1.01 | 0.80 | 2.17 | 2.01 | 0.87 | 2.99 | 2.05 | 2.04 | 3.97 | 3.47 |
| 水杨酸甲酯 Methyl salicylate (X13) | 0.14 | 1.86 | 1.99 | 2.54 | 2.66 | 2.81 | 0.14 | 2.36 | 2.81 | 3.01 | 3.42 | 3.83 |
| 丁酸-3-己烯酯 Butanoic acid,3-hexenyl ester,(E) (X14) | 0.05 | 0.80 | 1.40 | 0.91 | 2.38 | 2.22 | 0.05 | 1.69 | 1.15 | 1.66 | 2.12 | 2.35 |
| 香叶基丙酮 5,9-Undecadien-2-one,6,10-dimethyl-,(E) (X15) | 0.66 | 1.20 | 0.96 | 0.77 | 0.67 | 1.18 | 0.66 | 1.33 | 0.99 | 0.81 | 0.70 | 0.68 |
| 2-庚醇 2-Heptanol (X16) | 0.08 | 1.31 | 2.63 | 1.45 | 1.40 | 1.87 | 0.08 | 1.08 | 2.12 | 1.23 | 1.29 | 1.24 |
| 己酸己酯 Hexanoic acid,hexyl ester (X17) | 0.15 | 0.36 | 0.30 | 0.51 | 0.39 | 0.25 | 0.15 | 0.92 | 0.21 | 0.26 | 0.31 | 0.15 |
| 顺-3-己烯酸顺-3-己烯酯 cis-3-Hexenyl, cis-3-hexenoate (X18) | 0.19 | 0.45 | 0.35 | 0.37 | 0.44 | 0.44 | 0.19 | 0.85 | 0.30 | 0.36 | 0.47 | 0.41 |
| 2-甲基丁酸顺-3-己烯酯cis-3-Hexenyl-2-methylbutyrate (X19) | 0.28 | 0.47 | 0.23 | 0.33 | 0.36 | 0.18 | 0.28 | 0.64 | 0.24 | 0.30 | 0.35 | 0.15 |
| 苯甲醇 Benzyl alcohol (X20) | 1.33 | 1.00 | 0.52 | 0.71 | 0.55 | 0.53 | 1.33 | 0.63 | 0.67 | 0.47 | 0.54 | 0.61 |
| 1,2-苯二甲酸双(2-甲基丙基)酯 1,2-Benzenedicarboxylic acid, bis (2-methylpropyl) ester (X21) | 0.87 | 0.29 | 0.45 | 0.39 | 0.29 | 0.43 | 0.87 | 0.58 | 0.26 | 0.27 | 0.26 | 0.16 |
| 十四烷 Tetradecane (X22) | 0.17 | 0.38 | 0.35 | 0.29 | 0.24 | 0.30 | 0.17 | 0.47 | 0.24 | 0.19 | 0.20 | 0.31 |
| 反式2-己烯基己酸 Hexanoic acid,2-hexenyl ester,(E) (X23) | 0.17 | 0.17 | 0.15 | 0.26 | 0.22 | 0.15 | 0.17 | 0.43 | 0.11 | 0.15 | 0.17 | 0.10 |
| 2-硝基乙基苯 Benzene,(2-nitroethyl) (X24) | 0.04 | 0.31 | 0.35 | 0.42 | 0.47 | 0.27 | 0.04 | 0.43 | 0.38 | 0.47 | 0.44 | 0.34 |
| 2,2,3,3-四甲基丁烷 2,2,3,3-tetramethyl butane (X25) | 0.28 | 0.42 | 0.23 | 0.38 | 0.19 | 0.36 | 0.28 | 0.22 | 0.05 | 0.01 | 0.17 | 0.02 |
新窗口打开|下载CSV
2.2.1 对萎凋叶香气组分的影响 如表3所示,不同温度处理下铁观音萎凋叶的α-法呢烯相对含量按序依次为:D20>D30>D35>D25>D40,D20比D40提高3.61%;与对照相比,D20的相对含量增长了7.07%,D40增长了3.46%。香叶醇的含量按序排列依次为:D30>D20>D25>D35>D40;D30比D40提高6.80%;与对照相比,D30的相对含量增长了14.12%,D40增长了7.32%。各萎凋叶橙花叔醇的相对含量按序依次为:D30>D35>D25>D20>D40,D30比D40提高1.16%;与对照相比,D30增长了3.23%,D40增长了2.07%。同样,D30萎凋叶芳樟醇的相对含量最高,D40含量最低,二者相差约1.95%,其中D30较对照增长了5.51%,D40较对照增长了3.56%。芳樟醇氧化物I和芳樟醇氧化物II的相对含量均在D25达到最大值,在D40达到最小值。
LED光照处理下,α-法呢烯的相对含量按序依次为:L20>L30>L35>L25>L40,L20比L40提高10.95%;与对照相比,L20增长了15.05%,L40增长了4.10%。香叶醇的含量按序依次为:L30>L25>L35>L40>L20,L30比L20提高6.08%,L30较对照增长了15.28%,L20较对照增长了9.20%。芳樟醇的含量按序依次为:L30>L20>L25>L35>L40,L30比L40提高1.86%;L30较对照增长了6.14%,L40较对照增长4.28%。橙花叔醇也在L30达到最大值,而在L40为最小值,其相对含量按序依次为:L30>L20>L35>L25>L40,L30较L40提高了1.08%;与对照相比,L30增长了3.71%,L40增长了2.63%。芳樟醇氧化物I和芳樟醇氧化物II均在L20达到最大值,分别为15.19%和7.25%,最小值则不同,芳樟醇氧化物II在L35为最小值,而芳樟醇氧化物I在L40为最小值,二者较对照分别增长了8.89% 和3.06%。剩余香气组分中,酯类物质占8种,总相对含量为4.12%—29.27%;醇类物质占5种,总相对含量为3.71%—11.76%;烷烃类物质占3种,总相对含量占0.49%—1.12%;酸类、酮类和其他物质各为1种。
2.2.2 对萎凋叶主要萜类香气组分的影响 由图3可知,LED组萎凋叶中主要萜类化合物的相对含量较Dark组均有不同程度的增长,其中L30和D30处理的橙花叔醇、香叶醇和芳樟醇的相对含量均为各自处理组的最大值;α-法呢烯和芳樟醇氧化物(I、II)则在L20处理为所有处理组的最大值;除芳樟醇外,L20橙花叔醇、香叶醇、α-法呢烯和芳樟醇氧化物(I、II)的相对含量较D20的提升幅度最大,按序依次增加了1.01%、4.83%、7.98%、2.93%和7.26%;L25的芳樟醇、芳樟醇氧化物(I、II)较D25依次分别增长1.04%、1.66%和1.14%;L30的香叶醇、α-法呢烯和芳樟醇氧化物(I、II)较D30依次分别增长了1.16%、2.32%、1.92%和3.24%;L35和L40的其他香气组分较D35和D40增长不多,而香叶醇的增长幅度较大,依次为2.66%和2.67%。
图3
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图3不同温度LED光照处理铁观音萎凋叶主要香气组分含量
Fig. 3Aroma components of Tieguanyin withered leaves treated with different temperatures and LED light
2.3 基于主成分分析温度和LED光照共同处理对萎凋叶香气组分的影响
为了客观评估不同温度LED光萎凋叶的香气质量,本研究采用顶空固相微萃取-气相色谱-质谱联用(HS-SPME-GC-MS)技术对对照鲜叶和10个萎凋叶进行分析,得到123种共有香气组分。通过阅读国内外与铁观音香气组分相关的报道,结合已检测出的香气数据,筛选出25种达到人体嗅觉阈值的主要香气组分(相对含量基本高于0.1%),25种香气组分总相对含量占各萎凋叶香气总含量的50%以上,因此,选择前25种香气成分进行主成分分析具有一定代表性。利用SPSS19.0对筛选出的25种香气组分进行主成分分析,标准化处理后得到各主成分的特征值和累计贡献率,具体如表4。对25个香气组分进行主成分分析处理后,转化为F1、F2、F3、F4、F5 5个主成分。其方差贡献率按序为51.367%、21.379%、7.968%、6.586%和4.408%,累计贡献率达到91.708%;且F1—F5的特征根λ>1.000,能较为全面反映铁观音萎凋叶香气品质的综合特点,因此选择F1—F5进行主成分分析能较为客观、全面的解释和评价不同温度LED光萎凋叶香气质量的全部信息。不同香气组分对应F1—F5的载荷系数如表5所示,其中Xi(i=1—25)分别代表铁观音香气组分,详见表3。Table 4
表4
表4主成分特征值与累积贡献率
Table 4
| 主成分 Principal component | 特征值 Eigenvalue | 方差贡献率 Variance contribution rate (%) | 累计贡献率 Cumulative contribution rate (%) |
|---|---|---|---|
| F1 | 12.842 | 51.367 | 51.367 |
| F2 | 5.345 | 21.379 | 72.746 |
| F3 | 1.992 | 7.968 | 80.714 |
| F4 | 1.646 | 6.586 | 87.300 |
| F5 | 1.102 | 4.408 | 91.708 |
新窗口打开|下载CSV
Table 5
表5
表5主成分对应的载荷矩阵
Table 5
| 主成分 Principal component | X1 | X2 | X3 | X4 | X5 | X6 | X7 | X8 | X9 | X10 | X11 | X12 | X13 | X14 | X15 | X16 | X17 | X18 | X19 | X20 | X21 | X22 | X23 | X24 | X25 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| F1 | 0.96 | 0.85 | 0.89 | 0.76 | 0.90 | 0.89 | 0.84 | 0.78 | 0.93 | 0.73 | 0.83 | 0.54 | 0.73 | 0.61 | 0.35 | 0.41 | 0.60 | 0.72 | 0.41 | -0.80 | -0.58 | 0.43 | 0.42 | 0.91 | -0.34 |
| F2 | 0.01 | 0.47 | 0.00 | 0.18 | -0.17 | -0.12 | 0.37 | 0.05 | -0.25 | -0.06 | -0.37 | -0.29 | -0.57 | -0.44 | 0.60 | -0.34 | 0.76 | 0.57 | 0.81 | 0.44 | 0.63 | 0.63 | 0.82 | -0.21 | 0.62 |
| F3 | 0.16 | -0.11 | 0.17 | 0.13 | 0.26 | 0.05 | -0.28 | 0.21 | 0.13 | 0.20 | -0.29 | -0.69 | -0.13 | -0.36 | 0.38 | 0.67 | -0.08 | -0.29 | -0.18 | -0.07 | -0.13 | 0.23 | -0.22 | 0.04 | 0.32 |
| F4 | 0.02 | -0.13 | -0.26 | -0.41 | -0.22 | 0.07 | 0.22 | 0.12 | -0.19 | -0.36 | -0.07 | 0.20 | 0.16 | 0.47 | 0.42 | 0.40 | -0.03 | 0.26 | -0.28 | -0.27 | 0.03 | 0.45 | -0.07 | -0.21 | 0.14 |
| F5 | -0.16 | -0.05 | 0.07 | 0.15 | 0.16 | -0.35 | 0.14 | -0.51 | 0.07 | -0.01 | -0.16 | 0.04 | 0.23 | 0.19 | -0.09 | -0.03 | -0.01 | 0.07 | 0.09 | 0.04 | -0.42 | 0.14 | -0.07 | 0.15 | 0.51 |
新窗口打开|下载CSV
综合表4和表5可知,F1的累计贡献率达到51.367%,包含了50%以上的香气信息,且铁观音萎凋叶香气相对含量占大部分比重的α-法呢烯(X2)、橙花叔醇(X9)、芳樟醇及其氧化物(I、II)(X5、X6、X1)和香叶醇(X3)的载荷系数为0.85、0.93、0.90、0.89、0.96和0.89,与主成分方程F1呈高度正相关,而呈青香、刺激性味的邻苯二甲酸酯和2,2,3,3-四甲基丁烷等成分载荷系数与主成分方程F1呈高度负相关。
以不同特征值的F1、F2、F3、F4、F5方差贡献率作为加权系数,由F1—F5对应的不同特征值的方差贡献率为权重相乘再求和建立香气的综合评估数学模型:F=0.514F1+0.214F2+0.08F3+0.066F4+0.044F5,通过数学模型F对不同温度LED光萎凋叶进行香气质量评估,并按F值大小排序。根据方差贡献率最大的F1分析可知,F值越大,萎凋叶的主要香气主要组分含量越高,综合评价结果如表6所示。通过主成分分析得出不同光照和温度共同处理铁观音萎凋叶的香气质量综合得分F由高到低依次为:L20、L30、D30、L35、L25、L40、D20、D35、D25和D40;由于F越大,萎凋叶香气综合质量越好,因此可知L20萎凋叶的各主要香气组分含量的综合得分最高,L30处理次之;D30在无光处理组中得分最高;L40和D40在各自处理组得分最低,但各萎凋叶主要香气组分的含量均高于对照,这与萎凋叶香气组分分析所得的结果基本一致。
Table 6
表6
表6香气质量综合评价结果
Table 6
| 处理 Treatment | F1 | F2 | F3 | F4 | F5 | F | 排序Ranking |
|---|---|---|---|---|---|---|---|
| L20 | 92.18 | 8.57 | 5.16 | -11.13 | -0.98 | 48.85 | 1 |
| L30 | 81.68 | 1.06 | 7.69 | -11.91 | -0.33 | 42.02 | 2 |
| D30 | 69.21 | 2.70 | 8.30 | -11.75 | 1.42 | 36.10 | 3 |
| L35 | 69.82 | 0.06 | 3.48 | -8.99 | 1.28 | 35.64 | 4 |
| L25 | 65.62 | -0.91 | 6.98 | -8.16 | -1.06 | 33.51 | 5 |
| L40 | 61.44 | -1.91 | 3.70 | -6.54 | 0.87 | 31.07 | 6 |
| D20 | 58.48 | 4.04 | 6.32 | -9.82 | 1.57 | 30.85 | 7 |
| D35 | 59.71 | -0.07 | 3.41 | -5.74 | 0.22 | 30.58 | 8 |
| D25 | 57.31 | 0.17 | 7.13 | -6.42 | -0.88 | 29.60 | 9 |
| D40 | 51.69 | -0.94 | 4.10 | -3.31 | -0.37 | 26.46 | 10 |
| 对照 XY | 12.17 | 0.94 | 1.34 | -2.51 | -0.13 | 6.39 | 11 |
新窗口打开|下载CSV
3 讨论
综合本研究结果可知,不同温度处理的铁观音萎凋叶的DXS、DXR、HDS、HDR相对表达量均在30℃和35℃处理时达到较大值,而温度过高或过低均会抑制其表达量,得出各基因的最适表达温度为30℃—35℃。前人研究表明,改变萎凋温度能增加红茶的花香[24]。萎凋叶不同香气组分的最大值分布在不同温度处理,D20处理的α-法呢烯含量最高,D30的橙花叔醇、香叶醇、芳樟醇和芳樟醇氧化物I含量最高,D25的芳樟醇氧化物II的含量最高;但各主要香气组分的含量基本在D40处理达到最小值,这与主成分分析得出的D30在无光处理组香气综合得分最高,D40得分最低这一结论一致。此外,在不同温度萎凋处理下,萜类代谢途径上游基因相对含量与主要萜类芳香物质的含量变化不具有同步性;但均在30℃左右达到最大值,40℃处理最低;推测这与茶叶中各种酶的最适温度有关,尤其是多酚氧化酶(PPO)和过氧化氢酶(POD)。有研究表明[25,26],茶叶中的主要芳香物质如芳樟醇及其氧化物、香叶醇等,都与β-糖苷酶酶促水解作用所形成大量香气前体物,特别是多酚类物质与PPO、POD的接触氧化密切相关;滑金杰等[27]设计20℃、28℃、36℃ 3个萎凋温度梯度处理鲜叶,得出在28℃处理的多酚氧化酶PPO、POD酶活性最高,这与本研究30℃萎凋处理主要萜类芳香物质含量最高这一结论基本一致。LED组铁观音萎凋叶DXS、DXR、HDS、HDR的相对表达量均高于对应的Dark组,与鲜叶相比,LED组萎凋叶较Dark组提升更显著;Dark组的DXR、HDR相对表达量均低于XY;经LED处理后,DXR、HDR表达量均显著高于XY;推测与温度因子相比,LED光因子对DXR、HDR调控更显著。可见,光与温度同时对萎凋叶DXS、DXR、HDS、HDR表达具有调控作用;在一定温度范围内,两者组合对萎凋叶的DXS、DXR、HDS、HDR表达具有正向调控作用;项丽慧等[28]研究得出红茶萎凋过程中经LED黄光处理,毛茶中萜类挥发性物质大幅度增加。本研究结果表明,在乌龙茶萎凋过程中,增加LED光照可显著提高萎凋叶主要萜烯类组分的含量,这与FU等[9]的研究结果基本一致;在同温度梯度处理下,L20萎凋叶的主要香气组分含量较D20提升最显著,其次是L30;而L35、L40较D35、D40涨幅不大;其中L20、L25、L30主要萜类芳香物质的含量较D20、D25、D30增长幅度较大,最显著的为L20处理,而L35、L40处理,各香气组分含量较D35、D40增长幅度不大;这与主成分分析得出的结论基本一致。
L20与D20主要香气组分的含量在各自处理组中均占较高比例;L20的芳醇氧化物(I、II)、α-法呢烯、乙酸叶醇酯、芳醇氧化物的相对含量为所有处理组的最大值;其香叶醇、芳樟醇、橙花叔醇的含量也仅次于L30,与主成分分析得出的结论一致。朱宏凯等[29]设计红茶低温(20±2℃)、中温(30±2℃)、高温(40±2℃)揉捻试验,得出在低温揉捻条件下酶活性保留相对较高,这可能与低温条件减少了酶与邻醌等物质的结合有关[30]。因此,推测低温条件有利萎凋和揉捻处理过程中鲜叶PPO和POD酶活性的保留,而PPO和POD酶活性与茶叶芳香物质含量的累加直接相关,所以,L20和D20处理萎凋叶的主要香气组分含量较高;此外,L30萎凋叶的香气组分含量仅次于L20。
而L20、D20处理萎凋叶DXS、DXR、HDS、HDR的相对表达量却较低,与其香气总相对含量最高的结果相反;推测可能是MEP下游某些香气合成基因受低温诱导,在20℃处理显著表达,直接提高萜类化合物的含量,进而使L20、D20萎凋叶香气主要组分综合含量最高,还有待更深入的研究。
4 结论
在LED光萎凋过程中各香气组分形成的最适温度并不一致,L20处理萎凋叶α-法呢烯和芳樟醇氧化物(I、II)含量较高,L30处理萎凋叶橙花叔醇、芳樟醇和香叶醇含量较高;生产上可根据萎凋叶所需不同香气类型来选择不同的LED光萎凋温度。D40处理不利于萎凋叶萜类关键基因(DXS、DXR、HDS、HDR)的表达,同时不利于萜类主要芳香物质的合成;生产上应注意萎凋时的通风状况及其萎凋环境温度的调控,摊叶不能太厚,避免叶温上升过快。乌龙茶萎凋过程中温度参数的改变能影响MEP上游关键基因的表达量和萜类香气组分相对含量;在温度一致的条件下,单独的光因子对MEP上游关键基因的表达和主要萜类香气组分的生成具有调控作用。L30光照萎凋处理的萎凋叶MEP途径上游关键基因相对表达量最高,同时橙花叔醇、芳樟醇和香叶醇含量最高,这与生产上的萎凋温度一致。因此,乌龙茶萎凋过程中香气组分积累、4个关键基因的表达量与光和温度处理三者间不存在线性相关关系,调控好合适的光萎凋温度有利于促进铁观音萎凋叶香气的形成。参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[D].
[本文引用: 2]
[D].
[本文引用: 2]
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 3]
[本文引用: 3]
[本文引用: 3]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
