全文HTML
--> --> -->火星稀薄的大气在光照等因素的作用下携带沙尘形成强烈的尘暴, 沙尘颗粒在通过摩擦与碰撞等过程携带电荷后, 最终可以形成几十到几百千伏每米的沙尘电场, 可能使火星大气发生CO2击穿放电现象[2-9], 目前人们正对火星沙尘放电中独特的自激发与自熄灭等现象进行深入的研究[10-13]. 从另一个角度来看, 火星大气中丰富的CO2资源为人类空间探索进行火星原位制氧提供了可能. 2021年2月登陆的美国毅力号火星探测器已经携带基于热催化的CO2制氧装置, 针对火星原位制氧进行了实地探索, 预计能以6 g/h的速率产生纯度高于98%的氧气[14], 这意味着火星原位制氧问题的研究开始进入新的阶段. 由于等离子体低能耗、高效率的特点, 采用CO2放电的方式进行火星原位制氧也成为人们关注的主要方向之一[15]. 一方面, 借助于CO2放电等离子体技术在火星上实现原位制氧有其独特的优势, 首先火星大气中的压力和温度范围有利于CO2分子不对称拉伸模式的振动激发和随后的振动上移, 这可使更多的能量储存在CO2的振动模式中, 有利于CO2分解[16]; 此外, CO2通过振动激发解离比电子碰撞激发解离需要更少的能量, 因此在火星上采用CO2的逐步振动激发方式能更有效地分解CO2, 并提高能量利用效率[17]. 另一方面, 由于CO2是地球上主要的温室气体, 它经过转化的产物作为增值化学品和新燃料具有独特的优势, 因此人们对地球大气压下的CO2放电已开展深入的研究, 并对脉冲介质阻挡放电(DBD)、微波放电、滑动弧放电等不同模式下的CO2放电行为得到了一定的认识[18-21]. 这些成果将有助于人们更深刻地理解火星环境中的CO2放电.
进行火星上CO2放电研究首先面临的一个重要问题是放电反应集合的确定, 由于火星上的放电环境与地球大气环境及实验室环境差别很大, 寻找完整的反应集合是火星原位制氧及火星沙尘放电等研究的重要前提, 这同时也涉及到对火星CO2放电中主要与本质放电过程的认识. 一般来说, 出于计算的难易程度考虑, 首先选择零维模型[22]或一维模型[23,24]进行反应集合的分析, 并在将其应用于高维模型[25-28]之前进行反应集合的简化, 此过程被称为骨架还原[29]. 反应集合的主要分析方法有灵敏度分析(SA)、不确定性分析(UA)、主成分分析(PCA)和通径分析(PWA), SA与UA通过分析系统受到扰动后的响应来实现集合的化简, PCA着重于研究集合解耦后各粒子之间的耦合关系, PWA则以各路径的速率大小作为选择的标准[30-33].
然而, 对于火星条件下CO2放电这种复杂的反应过程而言, 上述方法通常非常耗时. 在实际研究中, 可以首先应用图形理论对初始集合进行预处理. 它通过构造数学图形的方式对节点间关系进行分析, 已被广泛用于各种复杂系统和多种领域[34-38]. 在反应种类繁多、粒子间相互关系复杂的情况下, 图论方法能够确定在后续模拟中扮演中心角色的粒子, 并对等离子体化学过程做到迅速而准确的分类[39,40]. 对于图论方法的处理结果, 可以在数值模拟之后, 借助粒子间依赖关系分析进行深入的探讨与验证, 它能够定量地求解粒子重要程度, 运用有向图对可以保留在简化集中的粒子进行标记, 从而产生还原骨架, 以一定的精度预测简化集中粒子的表现[41,42]. 由于粒子间通过反应耦合, 因此依赖关系分析法需着重考虑粒子和反应的速率表达式. 在分析过程中, 它计算粒子间相互关系占用的时间只是进行常微分方程积分所需时间的一部分, 速度较快, 因此已被用于等离子体方面的研究[21].
DBD是进行CO2转化最常用的非热等离子体类型, 其设计简单, 并有利于在应用中扩大规模[17,43]. 虽然振动激发能级在微波和滑动弧放电中对CO2转化起到关键作用, 但在DBD大于200 Td (1 Td = 10–17 V·cm2)的约化场范围下, 高能级振动态粒子的存在显得没那么重要, 电子在激发粒子的过程中造成的能量损失也可通过引入不会造成粒子变化的虚拟反应进行弥补[17,19,4344]. 因此本文不考虑振动激发态粒子, 采用图论分析法与粒子依赖性分析法, 结合基于反应速率的反应比重分析, 致力于获得可应用于DBD形式下的基态CO2放电简化集合.
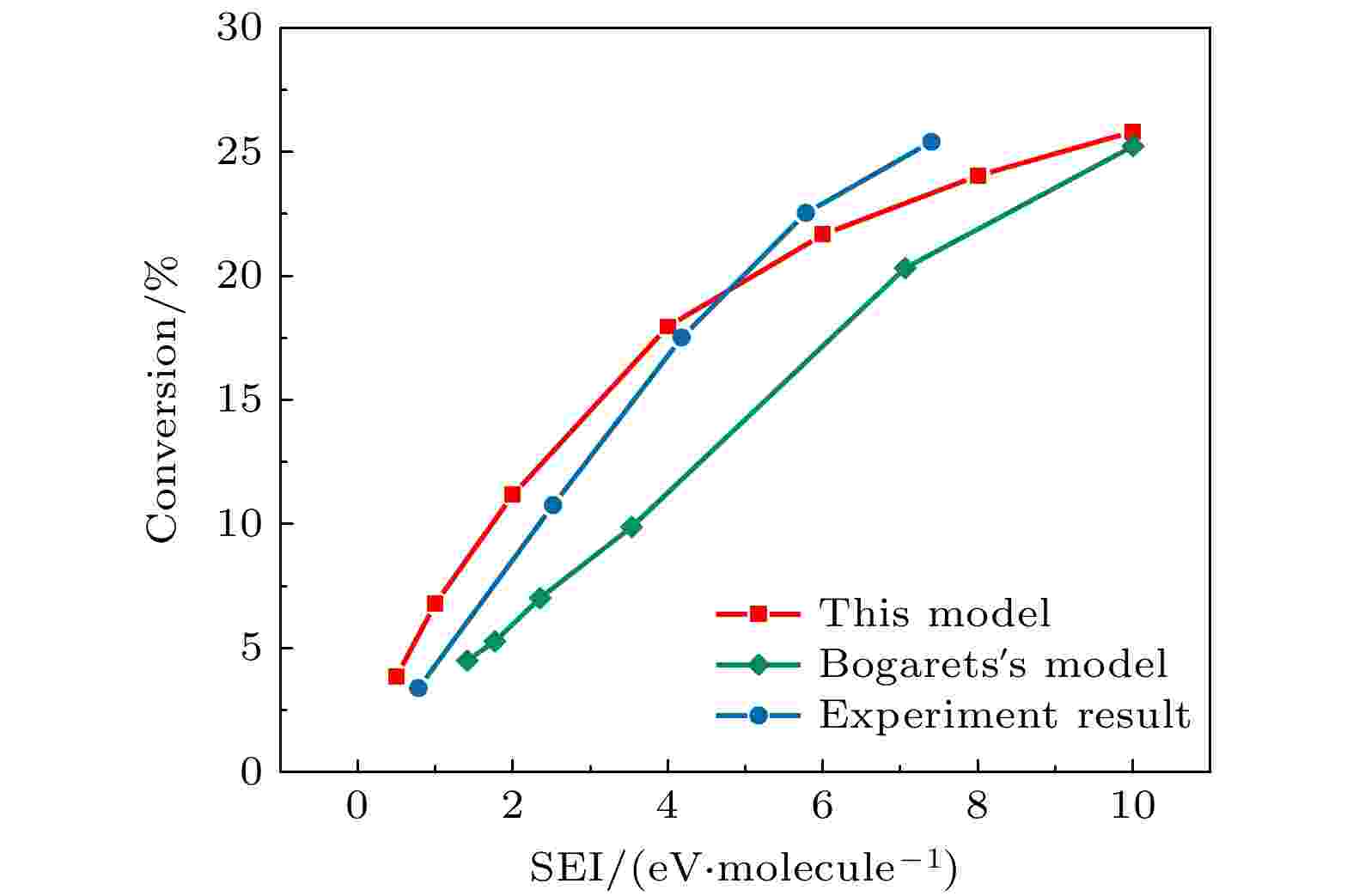 图 1 地球大气环境下CO2放电转化率对比
图 1 地球大气环境下CO2放电转化率对比Figure1. Comparations of CO2 discharge conversion in the earth atmosphere.
本文采用等离子体整体模型, 借助粒子平衡方程和能量平衡方程, 求解物质浓度及能量随时间的演化过程. 运用自编Matlab程序, 采用局部能量近似的方法, 耦合Bolsig+程序, 通过计算各粒子的浓度变化与能量的散失过程, 得出各反应间的相互关系; 运用Zdplaskin程序, 查看CO2转化率与能量效率、能量损耗随比能量输入的变化, 并将粒子浓度变化与自编Matlab程序中的结果形成对照.
放电数值模拟中取火星气压为700 Pa, 火星表面平均温度为218 K, 并设置功率密度为20 W/cm3, 忽略背景气体CO2及其产物O2和CO的振动态与激发态形式, CO2初始浓度与火星条件下保持一致, 初始的放电反应集合在借鉴Kozák和Bogaerts[18]的研究后进行一定的补充, 定义粒子M为过渡粒子, 在本模型中可由CO2, O2, CO等中性粒子替代. 详情见附录A的表A1.
| 初始集合粒子构成 | |
| 中性粒子 | CO2, CO, C, O, O2, O3, C2O |
| 正离子 | $ {\mathrm{C}\mathrm{O}}_{4}^{+} $, $ {\mathrm{C}\mathrm{O}}_{2}^{+} $, CO+, C+, O+, $ {\mathrm{O}}_{2}^{+} $, $ {\mathrm{O}}_{4}^{+} $, $ {\mathrm{O}}_{5}^{+} $, $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $, $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $, $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ |
| 负离子 | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $, $ {\mathrm{C}\mathrm{O}}_{3}^{-} $, O–, $ {\mathrm{O}}_{2}^{-} $, $ {\mathrm{O}}_{3}^{-} $, $ {\mathrm{O}}_{4}^{-} $ |
表A1初始反应集合中的粒子构成
TableA1.Composition of particles in the original model.
数值模拟中的反应速率v定义为单位时间单位体积内各反应中化学计量数为1的粒子的浓度变化量:


比能量输入







在简化集合的构建过程中, 首先运用图论对初始集合进行预处理, 将各粒子视为节点, 粒子间的碰撞反应由节点间的有向边表示, 并寻找节点间连通的最短路径, 从粒子间连通性、临近中心性、相间中心性、网络集聚度等方面共同分析反应集合特征. 在进行数值模拟之后, 采用粒子依赖性分析法, 探究不同粒子之间的相互关系, 定量地判断各粒子的重要程度, 并结合图论分析的相关结论确定粒子简化集. 最后对粒子简化集所涉及的各项反应基于反应速率进行反应比重分析, 化简反应种类, 形成最终的完整简化集. 具体的分析过程见第3节, 特别需要指出的是, 该分析方法在包含振动激发能级粒子种类的集合中同样具备可行性.
3.1.图论分析
33.1.1.粒子间连通性分析
由于不同粒子(即节点)间的碰撞反应类型存在差异, 因此首先统计各粒子参与反应的数目, 确定初始集合总体的反应构成情况, 如图2所示. 图 2 各粒子所参与的反应数目
图 2 各粒子所参与的反应数目Figure2. Number of reactions that each species participates in
背景气体分子CO2参与了超过1/3的碰撞反应, CO, O2和O是其放电的主要产物, 其中CO的碳氧成键较为稳定, 与之相比, O2和O更具活泼性, 它们参与的反应数目已远超CO2, 是初始集合中参与反应构成最多的粒子.
另一方面, 通过检索反应类型可以发现, 相比于其他正离子,




图3描述了各粒子与其他粒子间可通过反应建立联系的数目. 在共25种粒子中, O2可与23种粒子直接连通; 作为基本粒子的CO2也具备显著的表现, 它可以通过碰撞反应生成其他粒子, 或由其他粒子经过逆反应补偿. 通过图2与图3的对比可以发现, 参与反应种类较少的





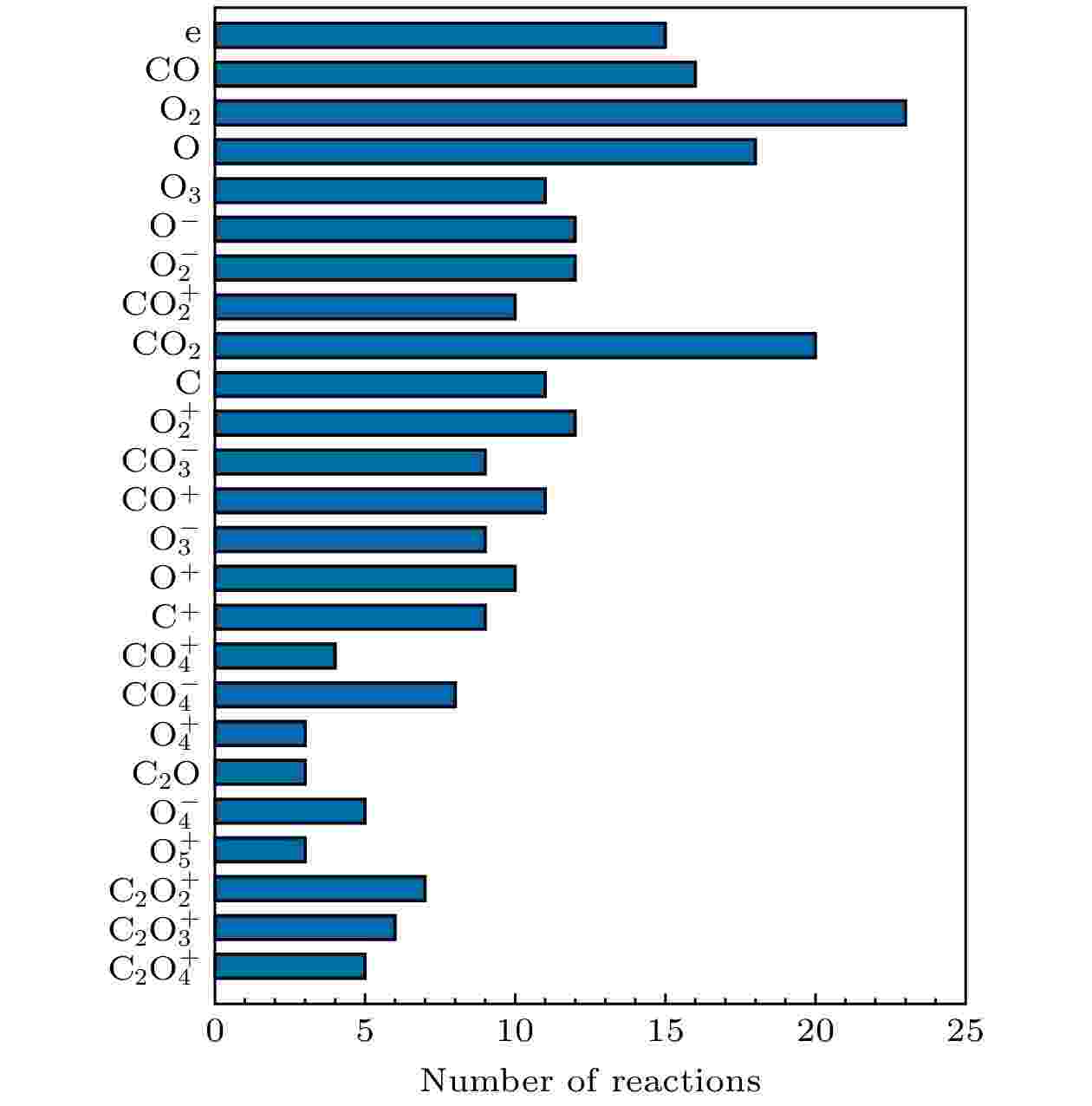 图 3 可通过反应直接建立联系的粒子种类数目
图 3 可通过反应直接建立联系的粒子种类数目Figure3. Number of species that can be directly connected by reactions.
为了更好地预测各粒子在放电行为中的实际参与情况, 研究了它们在反应中分别作为反应物与生成物出现时与其他粒子相沟通的频数, 如图4所示. 在这里, 引入了度(Degree)的概念, 定义汇入节点的边的总数为入度(In-degree), 背离节点的边的总数为出度(Out-degree). 比如, e, O–,

 图 4 各粒子度数 (a)出度、入度的条形堆积图; (b)粒子在出度-入度空间的分布情况
图 4 各粒子度数 (a)出度、入度的条形堆积图; (b)粒子在出度-入度空间的分布情况Figure4. Degrees of species: (a) Stacked bars of in-degree and out-degrees; (b) distribution of species in the out-degree-in-degree space.
电子和O2在度数图中均有显著的表现. 由于电子大量参与了与中性粒子间的碰撞反应(电子碰撞电离反应、电子碰撞解离反应、电子解离附着反应等), 因此出度值最高, 为114; O2是CO2放电的气体产物之一, 也是多种重粒子反应的主要生成物, 由于化学性质活泼, 它常在三体反应过程中作为中间粒子催化反应进行, 不发生浓度的改变. 在169个反应构成的初始集合中, O2的入度和出度分别为159与86, 平均在每个反应中都能与至少一个粒子建立联系.
离子方面, O–和




3
3.1.2.粒子间信息传递速度分析
放电过程中, 某粒子浓度发生变化时, 其他粒子做出响应的快慢在拓扑网络中表现为信息的传递速度, 途经的过渡粒子越多, 则信息的传递速度越慢, 传递速度与路径长度成反比. 可以运用临近中心性


 图 5 粒子网络拓扑图
图 5 粒子网络拓扑图Figure5. Species network topology.
该网络将各粒子按临近中心性数值大致分为三类: 以O2为代表的高临近中心性粒子群置于网络中心, 以表示其在信息传递过程中的高效性; C2O等边缘粒子数值较低, 被置于最外围; 数值居中的

CO2虽是火星大气条件下放电过程中的背景气体粒子, 但其临近中心性弱于O2, 在网络中并不位于正中位置. 这是因为在担任过渡粒子催化三体反应这方面, CO2远没有O2表现得更为活泼. 结合图3可以看出, 在25种粒子中, O2只与C2O无法直接连通, 而CO2与







在计算中发现, C2O十分特殊. 其他粒子在相互建立联系的过程中, 最多只需途经一个过渡粒子, 而C2O与




针对各粒子建立联系的方式, 引入了相间中心性



 图 6 粒子在临近-相间中心性空间的分布图
图 6 粒子在临近-相间中心性空间的分布图Figure6. Distribution of species in the closeness-betweenness centrality space.
值得注意的是, C2O与











































3
3.1.3.集聚度分析
在多数社会网络中, 各节点易与周围节点形成紧密的团状结构, 并倾向于向中心节点攀附. 在这里, 运用集聚系数





 图 7 粒子在集聚系数-度数空间的分布
图 7 粒子在集聚系数-度数空间的分布Figure7. Distribution of species in the clustering coefficient-degree space.
这种稠密的网络反过来印证了这些粒子的低活跃性与低影响度. 比如,




2
3.2.粒子种类筛选
前面通过粒子的度数与中心性, 分析初始集合中各粒子的活跃水平、粒子间信息的传递速度, 并借助集聚系数探讨网络构成, 最终初步得出


| 序号 | 反应 | 文献 |
| (X01) | e + CO2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + 2e | [50] |
| (X02) | e + CO2 $ \Rightarrow $ CO + O + e | [50] |
| (X03) | e + CO2 $ \Rightarrow $ CO + O– | [50] |
| (X04) | e + CO2 $ \Rightarrow $ 2e + O + CO+ | [50] |
| (X05) | e + CO2 $ \Rightarrow $ 2e + CO + O+ | [50] |
| (X06) | e + CO2 $ \Rightarrow $ 2e + C+ + O2 | [50] |
| (X07) | e + CO2 $ \Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + C + 2e | [51, 52] |
| (X08) | e + CO $ \Rightarrow $ C + O– | [50] |
| (X09) | e + CO $ \Rightarrow $ e + C + O | [50] |
| (X10) | e + CO $ \Rightarrow $ 2e + CO+ | [50] |
| (X11) | e + CO $ \Rightarrow $ 2e + C + O+ | [50] |
| (X12) | e + CO $ \Rightarrow $ 2e + C+ + O | [50] |
| (X13) | e + O3 $ \Rightarrow $ $ {{\mathrm{O}}_{2}^{-}}^{-} $ + O | [50] |
| (X14) | e + O3 $ \Rightarrow $ O2 + O– | [50] |
| (X15) | e + O3 $ \Rightarrow $ O + O2 + e | [53] |
| (X16) | e + O3 $ \Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + O + 2e | [53] |
| (X17) | e + O3 $ \Rightarrow $ O+ + O– + O + e | [53] |
| (X18) | e + O2 $ \Rightarrow $ 2 O + e | [50] |
| (X19) | e + O2 $ \Rightarrow $ O + O– | [50] |
| (X20) | e + O2 $ \Rightarrow $ 2e + $ {\mathrm{O}}_{2}^{+} $ | [50] |
| (X21) | e + O2 $ \Rightarrow $ 2e + O + O+ | [50] |
| (X22) | e + O2 $ \Rightarrow $ e + O+ + O– | [50, 54] |
| (X23) | e + O $ \Rightarrow $ 2e + O+ | [50] |
| (X24) | e + C $ \Rightarrow $ 2e + C+ | [50] |
表A2初始集合中由碰撞截面描述的电子碰撞反应
TableA2.Electron impact reactions described by collision cross sections in the original model.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (I01) | O– + CO2 $ \Rightarrow$ O + CO2 + e | 4.0 × 10–18 | [48] |
| (I02) | O– + CO2 + CO $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO | 1.5 × 10–40 | [61] |
| (I03) | O– + CO2 + O2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 3.1 × 10–40 | [61] |
| (I04) | O– + CO2 + CO2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO2 | 9.0 × 10–41 | [52] |
| (I05) | $ {\mathrm{O}}_{2}^{-} $ + CO2 + O2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O2 | 4.7 × 10–41 | [52] |
| (I06) | $ {\mathrm{O}}_{3}^{-} $+ CO2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 5.5 × 10–16 | [18] |
| (I07) | $ {\mathrm{O}}_{4}^{-} $ + CO2 $ \Rightarrow$ O2 + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ | 4.8 × 10–16 | [18] |
| (I08) | O+ + CO2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + CO | 9.4 × 10–16 | [18] |
| (I09) | O+ + CO2 $ \Rightarrow$ O + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ | 4.5 × 10–16 | [18] |
| (I10) | C+ + CO2 $ \Rightarrow$ CO+ + CO | 1.1 × 10–15 | [18] |
| (I11) | $ {\mathrm{O}}_{2}^{+} $ + CO2 + M $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{4}^{+} $ + M | 2.3 × 10–41 | [18] |
| (I12) | $ {\mathrm{O}}_{5}^{+} $ + CO2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{4}^{+} $ + O3 | 1.0 × 10–17 | [52] |
| (I13) | CO+ + CO2 $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + CO | 1.0 × 10–15 | [56] |
| (I14) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + CO2 + M $ \Rightarrow$ $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + M | 3.0 × 10–40 | [18] |
| (I15) | O+ + CO $ \Rightarrow$ O + CO+ | 4.9 × 10–18(Tg/298)0.5exp(–4580/Tg) | [18] |
| (I16) | C+ + CO $ \Rightarrow$ CO+ + C | 5.0 × 10–19 | [18] |
| (I17) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + CO $ \Rightarrow$ CO2 + $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ | 1.1 × 10–15 | [18] |
| (I18) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + CO $ \Rightarrow$ CO2 + $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ | 9.0 × 10–16 | [18] |
| (I19) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + CO + M $ \Rightarrow$ CO2 + $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + M | 2.6 × 10–38 | [18] |
| (I20) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + CO + M $ \Rightarrow$ CO2 + $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + M | 4.2 × 10–38 | [18] |
| (I21) | O– + CO $ \Rightarrow$ CO2 + e | 5.5 × 10–16 | [44] |
| (I22) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO $ \Rightarrow$ 2CO2 + e | 5.0 × 10–19 | [58] |
| (I23) | $ {\mathrm{O}}_{2}^{+} $ + C $ \Rightarrow$ CO+ + O | 5.2 × 10–17 | [18] |
| (I24) | $ {\mathrm{O}}_{2}^{+} $ + C $ \Rightarrow$ C+ + O2 | 5.2 × 10–17 | [18] |
| (I25) | CO+ + C $ \Rightarrow$ CO + C+ | 1.1 × 10–16 | [18] |
| (I26) | O– + C $ \Rightarrow$ CO + e | 5.0 × 10–16 | [57] |
| (I27) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + CO | 1.638 × 10–16 | [52] |
| (I28) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O $ \Rightarrow$ CO2 + O+ | 9.62 × 10–17 | [18] |
| (I29) | CO+ + O $ \Rightarrow$ CO + O+ | 1.4 × 10–16 | [18] |
| (I30) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 1.1 × 10–16 | [18] |
| (I31) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow$ CO2 + O2 + O– | 1.4 × 10–17 | [18] |
| (I32) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow$ CO2 + $ {\mathrm{O}}_{3}^{-} $ | 1.4 × 10–16 | [18] |
| (I33) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow$ CO2 + $ {\mathrm{O}}_{2}^{-} $ | 8.0 × 10–17 | [58] |
| (I34) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + CO2 | 6.4 × 10–17 | [52] |
| (I35) | CO+ + O2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + CO | 1.2 × 10–16 | [18] |
| (I36) | C+ + O2 $ \Rightarrow$ CO + O+ | 6.2 × 10–16 | [18] |
| (I37) | C+ + O2 $ \Rightarrow$ CO+ + O | 3.8 × 10–16 | [18] |
| (I38) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + O2 $ \Rightarrow$ 2CO + $ {\mathrm{O}}_{2}^{+} $ | 5.0 × 10–18 | [18] |
| (I39) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O3 $ \Rightarrow$ CO2 + $ {\mathrm{O}}_{3}^{-} $ + O2 | 1.3 × 10–16 | [18] |
| (I40) | $ {\mathrm{C}\mathrm{O}}_{4}^{+} $ + O3 $ \Rightarrow$ $ {\mathrm{O}}_{5}^{+} $ + CO2 | 1.0 × 10–16 | [52] |
| (I41) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O– $ \Rightarrow$ O + CO2 | 1.0 × 10–13 | [62] |
| (I42) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow$ CO + O2 + O | 6.0 × 10–13 | [44] |
| (I43) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ $ \Rightarrow$ 2CO2 + O | 5.0 × 10–13 | [58] |
| (I44) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow$ 2CO2 + O2 | 5.0 × 10–13 | [18] |
| (I45) | CO+ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow$ CO + O2 | 2.0 × 10–13 | [55] |
| (I46) | C+ + O– $ \Rightarrow$ C + O | 5.0 × 10–14 | [55] |
| (I47) | C+ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow$ C + O2 | 5.0 × 10–14 | [55] |
| (I48) | O–+ CO+ $ \Rightarrow$ CO + O | 1.0 × 10–13 | [62] |
| (I49) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ CO2 + O2 + O | 3.0 × 10–13 | [18] |
| (I50) | $ {\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow$ CO2 + 2O2 | 3.0 × 10–13 | [18] |
| (I51) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + M $ \Rightarrow$ CO+ + CO + M | 1.0 × 10–18 | [18] |
| (I52) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{3}^{-} $$ \Rightarrow$ CO2 + 2CO + O | 5.0 × 10–13 | [18] |
| (I53) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow$ CO2 + 2CO + O2 | 5.0 × 10–13 | [18] |
| (I54) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ + $ {\mathrm{O}}_{2}^{-} $$ \Rightarrow$ 2CO + O2 | 6.0 × 10–13 | [18] |
| (I55) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ $ \Rightarrow$ 2CO2 + CO + O | 5.0 × 10–13 | [18] |
| (I56) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow$ 2CO2 + CO + O2 | 5.0 × 10–13 | [18] |
| (I57) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow$ CO2 + CO + O2 | 6.0 × 10–13 | [18] |
| (I58) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + M $ \Rightarrow$ $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + CO2 + M | 1.0 × 10–20 | [18] |
| (I59) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{3}^{-} $$ \Rightarrow$ 3CO2 + O | 5.0 × 10–13 | [18] |
| (I60) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow$ 3CO2 + O2 | 5.0 × 10–13 | [18] |
| (I61) | $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow$ 2CO2 + O2 | 6.0 × 10–13 | [18] |
| (I62) | O–+ O3 $ \Rightarrow$ 2O2 + e | 3.0 × 10–16 | [44] |
| (I63) | O–+ O3 $ \Rightarrow$ $ {\mathrm{O}}_{3}^{-} $ + O | 8.0 × 10–16 | [18] |
| (I64) | $ {\mathrm{O}}_{2}^{-} $ + O3 $ \Rightarrow$ $ {\mathrm{O}}_{3}^{-} $ + O2 | 4.0 × 10–16 | [18] |
| (I65) | $ {\mathrm{O}}_{3}^{-} $ + O3 $ \Rightarrow$ 3O2 + e | 3.0 × 10–16 | [18] |
| (I66) | O+ + O3 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + O2 | 1.0 × 10–16 | [18] |
| (I67) | O– + O2 $ \Rightarrow$ O3 + e | 1.0 × 10–18 | [44] |
| (I68) | O– + O2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{-} $ + O | 1.5 × 10–18 | [55] |
| (I69) | O– + O2 $ \Rightarrow$ O + e + O2 | 6.9 × 10–16 | [52] |
| (I70) | O– + O2 + O2 $ \Rightarrow$ $ {\mathrm{O}}_{3}^{-} $ + O2 | 1.1 × 10–42(Tg/300) | [52] |
| (I71) | $ {\mathrm{O}}_{2}^{-} $ + O2 $ \Rightarrow$ 2O2 + e | 2.7 × 10–16(Tg/300)0.5exp(–5590/Tg) | [52] |
| (I72) | $ {\mathrm{O}}_{2}^{-} $ + O2 + M $ \Rightarrow$ $ {\mathrm{O}}_{4}^{-} $ + M | 3.5 × 10–43 | [18] |
| (I73) | $ {\mathrm{O}}_{3}^{-} $ + O2 $ \Rightarrow$ O2 + O3 + e | 2.3 × 10–17 | [18] |
| (I74) | O+ + O2 $ \Rightarrow$ O + $ {\mathrm{O}}_{2}^{+} $ | 1.9 × 10–17(Tg/298)–0.5 | [18] |
| (I75) | $ {\mathrm{O}}_{2}^{+} $ + O2 + O2 $ \Rightarrow$ $ {\mathrm{O}}_{4}^{+} $ + O2 | 4.0 × 10–42(Tg/300)–2.93 | [52] |
| (I76) | $ {\mathrm{O}}_{4}^{+} $ + O2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + O2 + O2 | 1.8 × 10–19 | [52] |
| (I77) | O+ + O + O2 $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + O2 | 1.0 × 10–41 | [52] |
| (I78) | O– + O $ \Rightarrow$ O2 + e | 2.3 × 10–16 | [21] |
| (I79) | $ {\mathrm{O}}_{2}^{-} $ + O $ \Rightarrow$ O2 + O– | 3.31 × 10–16 | [21] |
| (I80) | $ {\mathrm{O}}_{2}^{-} $ + O $ \Rightarrow$ O3 + e | 3.3 × 10–16 | [18] |
| (I81) | $ {\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow$ O3 + O– | 1.0 × 10–19 | [18] |
| (I82) | $ {\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow$ 2O2 + e | 1.0 × 10–19 | [18] |
| (I83) | $ {\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow$ $ {\mathrm{O}}_{2}^{-} $ + O2 | 2.5 × 10–16 | [18] |
| (I84) | $ {\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow$ $ {\mathrm{O}}_{3}^{-} $ + O2 | 4.0 × 10–16 | [18] |
| (I85) | $ {\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow$ O– + 2O2 | 3.0 × 10–16 | [18] |
| (I86) | $ {\mathrm{O}}_{4}^{+} $ + O $ \Rightarrow$ $ {\mathrm{O}}_{2}^{+} $ + O3 | 3.0 × 10–16 | [18] |
| (I87) | O– + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ O2 + O | 2.6 × 10–14(300/Tg)0.44 | [21] |
| (I88) | O– + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ 3O | 4.2 × 10–13(300/Tg)0.44 | [21] |
| (I89) | O– + $ {\mathrm{O}}_{2}^{+} $ + O2 $ \Rightarrow$ O3 + O2 | 2.0 × 10–37 | [57] |
| (I90) | O– + O+ + O $ \Rightarrow$ O2 + O | 2.0 × 10–37 | [57] |
| (I91) | O– + O+ + O2 $ \Rightarrow$ 2O2 | 2.0 × 10–37 | [57] |
| (I92) | O– + O+ $ \Rightarrow$ 2O | 4.0 × 10–14 | [18] |
| (I93) | $ {\mathrm{O}}_{2}^{-} $ + O+ $ \Rightarrow$ O + O2 | 2.7 × 10–13 | [18] |
| (I94) | $ {\mathrm{O}}_{2}^{-} $ + O+ + O2 $ \Rightarrow$ O3 + O2 | 2.0 × 10–37 | [57] |
| (I95) | $ {\mathrm{O}}_{2}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ 2O2 | 2.01 × 10–13(300/Tg)0.5 | [21] |
| (I96) | $ {\mathrm{O}}_{2}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ O2 + 2O | 4.2 × 10–13 | [21] |
| (I97) | $ {\mathrm{O}}_{2}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ + O2 $ \Rightarrow$ 3O2 | 2.0 × 10–37 | [57] |
| (I98) | $ {\mathrm{O}}_{3}^{-} $ + O + M $ \Rightarrow$ O3 + O + M | 2.0 × 10–37(Tg/300)–2.5 | [57] |
| (I99) | $ {\mathrm{O}}_{3}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ + M $ \Rightarrow$ O3 + O2 + M | 2.0 × 10–37(Tg/300)–2.5 | [57] |
| (I100) | $ {\mathrm{O}}_{3}^{-} $ + O+ $ \Rightarrow$ O3 + O | 1.0 × 10–13 | [18] |
| (I101) | $ {\mathrm{O}}_{3}^{-} $+ $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ O2 + O3 | 2.0 × 10–13 | [18] |
| (I102) | $ {\mathrm{O}}_{3}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow$ 2O + O3 | 1.0 × 10–13 | [18] |
| (I103) | $ {\mathrm{O}}_{4}^{-} $ + M $ \Rightarrow$ $ {\mathrm{O}}_{2}^{-} $ + O2 + M | 4.0 × 10–18 | [18] |
表A5初始集合中的离子-中性和离子-离子反应, 其中Tg为气体温度, 单位是K, 速率系数的单位在二体或三体反应中分别是m3/s或m6/s
TableA5.Ion-neutral and ion-ion reactions in the original model. Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.
对集合中不同的粒子A与B, 粒子A对粒子B的依赖性




首先关注在CO2的产生与损耗过程中, 其他中性粒子的表现. 图8中, 除O3经由O受到CO2的影响外, 其他中性粒子均直接依赖于CO2, 而CO2可通过CO与O之间的逆反应产生. 对于无有向边汇入的粒子节点, 如O3与C2O, 可以认为它们对其他中性粒子的数值影响极其微弱; 此外, C2O对CO, C, CO2的依赖作用为1, 通过检索反应构成, 发现C2O只通过反应N09产生, 涉及的反应数目极少, 可作为边缘粒子删除.
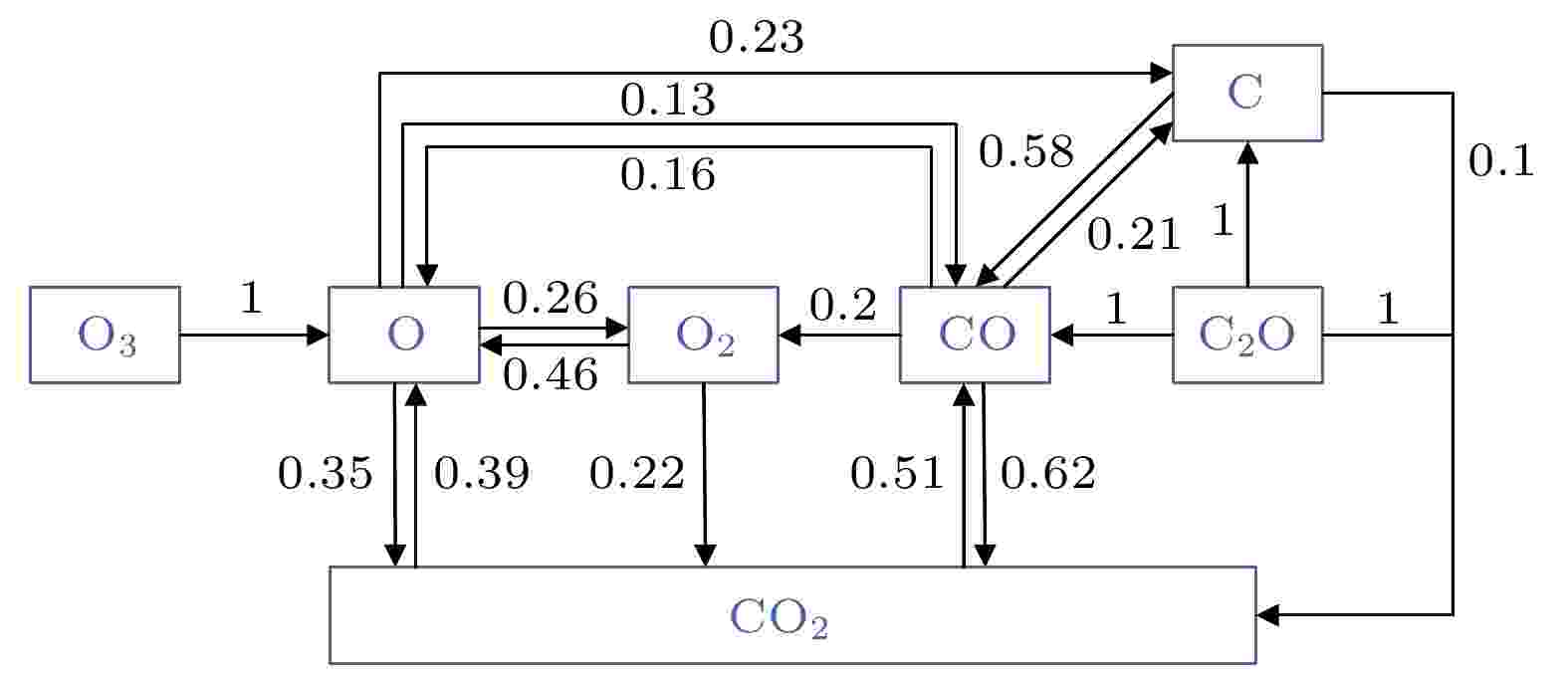 图 8 基于CO2的各中性粒子间的相互关系有向图
图 8 基于CO2的各中性粒子间的相互关系有向图Figure8. Directed relation graph among neutral species based on CO2.
在整体模型中, 认为外部能量首先传递于电子, 并通过电子与重粒子间发生碰撞进行能量传递. 因此, 研究电子与各离子的相互关系能明确具体的放电过程和电荷转移行为. 图9是基于电子的各带电粒子之间的有向关系图. 可以看到,










 图 9 基于e的各带电粒子间的相互关系有向图
图 9 基于e的各带电粒子间的相互关系有向图Figure9. Directed relation graph among charged species based on electrons.
























 图 10 初始集合所有粒子间相互关系有向图
图 10 初始集合所有粒子间相互关系有向图Figure10. Directed relation graph of the original model among all species.
在前面的连通性分析中,











































对于




































































2
3.3.反应集合的最终简化
在前面, 针对初始粒子集合, 已从图形理论与粒子间依赖性两个角度进行了完整的分析, 对粒子在集合中的重要程度得到了明确的认识, 把






反应速率是衡量一个反应重要性最基本的指标. 下面以CO2与电子发生碰撞电离反应的生成粒子

如图11所示, 反应X1, 即电子与CO2的碰撞电离反应, 是

























 图 11
图 11 
Figure11. Reaction rates of

仅比较不同反应对单一粒子浓度的影响是不够的, 由于各粒子浓度不同, 不同粒子在同一反应中的化学计量数也可能存在差异, 所以需要分析各反应在整个放电过程中的参与. 对此, 引入了各反应的相对贡献




图12以初始集合中由碰撞截面描述的电子碰撞电离反应子集为例, 给出了各反应的贡献比重. 其中, 反应X01, X02, X03是造成CO2损耗的主要反应, CO2具备的高粒子浓度, 会使这些反应具有极高的反应速率, 为整个数值模拟带来足够的粒子浓度变化, 从而本身具有较高的绝对贡献比重与相对贡献比重.
 图 12 初始集合中由碰撞截面描述的电子碰撞电离反应的比重
图 12 初始集合中由碰撞截面描述的电子碰撞电离反应的比重Figure12. Proportion of electron impact ionization reactions described by collision cross sections in the original model.
对于反应X13, X14, X15而言, 它们是消耗O3的主要反应, 相对贡献会呈现较高的数值; 而由于速率系数相对较小、反应中所涉及的各反应物浓度偏低, 它们对粒子总浓度的数值影响并不大, 因此会表现出极小的绝对贡献. 这在已舍弃的

在反应集合的筛选中, 应主要针对相对贡献和绝对贡献均较低的反应, 因为它们无论对单一粒子还是集合整体而言, 均具有极低的影响. 需要注意的是, 虽然用户可根据自身的情况选择简化集的精简度, 但仍需要保证每个粒子在反应中均包含足够的生成与损耗反应, 以大体符合实际的放电过程, 同时提高数值模拟的稳定性, 尽量避免因为单个反应的问题带来整个反应过程的不确定性. 最终, 本文在对简化粒子集合中相对贡献比重小于0.2, 绝对贡献比重小于0.002的反应去除后, 又补充了E11, I30, I44, I83等反应以使


| 简化集合粒子构成 | |
| 中性粒子 | CO2, CO, C, O, O2, O3 |
| 正离子 | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $, CO+, C+, O+, $ {\mathrm{O}}_{2}^{+} $ |
| 负离子 | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $, $ {\mathrm{C}\mathrm{O}}_{3}^{-} $, O–, $ {\mathrm{O}}_{2}^{-} $, $ {\mathrm{O}}_{3}^{-} $ |
表B1简化集合中的粒子构成
TableB1.Composition of particles in the simplified model.
图13给出了简化集与初始集合的粒子浓度变化情况. 反应初期, 电子浓度较低, 平均电子能量较高, 电子雪崩不断发展, 大量电子同高浓度的CO2发生电子碰撞反应, 在进行能量传递的同时, 伴随着CO2的电离与解离过程, 产生大量电子与其他重粒子. 之后随着电子温度的下降与放电产物浓度的升高, 除电子碰撞反应外, 重粒子间的碰撞反应速率开始加快, 各粒子浓度在0.1 ms后开始趋于较稳定的状态, 简化集与初始集合的粒子浓度表现基本一致.
 图 13 初始集合(实线)与简化集(虚线)关于粒子浓度的数值模拟结果比较 (a)中性粒子; (b)正离子; (c)电子与负离子
图 13 初始集合(实线)与简化集(虚线)关于粒子浓度的数值模拟结果比较 (a)中性粒子; (b)正离子; (c)电子与负离子Figure13. Comparison of the numerical simulation results of particle concentration between the original model (solid line) and the simplified model (dashed line): (a) Neutrals; (b) positive ions; (c) electron and negative ions.
中性粒子方面, CO和O是电子与CO2发生碰撞反应的主要产物, 浓度上升迅速, 与此同时, 大量的O会发生复合反应生成O2, 导致O2的浓度升高; C是CO2不完全反应的产物, 在将来的实验过程中, 应尽量抑制生成C的副反应的发生, 以防颗粒物对装置造成损坏; O3则是由于与CO2的直接联系较少, 因此会呈现相对更少的变化.
离子方面,



























作为火星环境下CO2放电的主要产物, CO可以用作燃料, O2是生命所需, 同时也可以液氧的形式用于火箭推动. 图14已列出影响它们浓度变化的主要反应. 对于CO, 主要通过电子与CO2的碰撞解离反应Y02、电子附着反应Y03、C与O2间的中性粒子碰撞反应M02及




 图 14 3 ms时引起(a) CO和(b) O2浓度变化的主要反应
图 14 3 ms时引起(a) CO和(b) O2浓度变化的主要反应Figure14. Main reactions at 3 ms which cause density changes of (a) CO and (b) O2.
图15给出了简化集合与初始集合在CO2转化率、能量效率和能量损耗方面的比较. 可以看到, 各曲线基本重合, 这证明了所构建的简化集的合理性. 图15(a)中, 随着反应进行, SEI提高, CO2转化率也相应提高, 但上升率逐渐降低. 这是因为, CO2分解产生的相对稳定的CO在足够长的反应时间后可以与O–和O重新结合, 形成CO2, 起到一定的逆补偿作用[17]. 另一方面, 由(4)式和(5)式可以看到, 能量效率与能量损耗的变化也是合理的, 实际上, 当转化率不具备与SEI同速上升的能力时, 能量效率总是下降、能量损耗量总是上升的[17]. 从反应速率的角度, 由于SEI的升高会使粒子温度增加, 进而导致部分反应的速率系数增加, 意味着更多的能量损失于各种重粒子的碰撞反应中, 进而导致能量效率与能量损耗产生相应的表现. 总的来说, 转化率与能量效率是无法同时兼顾的, 因此, 确定合适的放电条件, 使放电在保证CO2转化率的基础上尽可能提高能量转化效率, 将会是下一步的目标.
 图 15 作为比能量输入的函数, 简化集合与初始集合关于转化率与能量方面的比较 (a) CO2转化率; (b)能量效率; (c)能量损耗
图 15 作为比能量输入的函数, 简化集合与初始集合关于转化率与能量方面的比较 (a) CO2转化率; (b)能量效率; (c)能量损耗Figure15. As a function of SEI, comparations of original and simplified model on (a) conversion of CO2, (b) energy efficiency, (c) energy cost.
首先通过图论的方法, 寻找各目标粒子直接参与的反应数目和直接相关的粒子种类, 从入度与出度方面分析粒子对整个放电过程的参与程度与粒子间建立联系的方式. 在对粒子中心性的考察中, 发现O2与其他绝大多数粒子具备直接相关性, 于是以O2为中心粒子构建基于临近中心性的粒子间网络拓扑图, 并结合网络的紧密程度, 分析过渡粒子在其他粒子对连接中的关键作用, 通过粒子间信息流的传递速度推断各粒子的重要程度, 把













通过分别基于简化集合与初始集合进行数值模拟, 发现相应的粒子浓度、转化率、能量效率等数据的高度一致性, 从而对火星大气CO2放电的具体过程得到了更深入的了解. 同时, 用简化集代替初始集合进行数值模拟工作, 能够极大地降低计算工作量. 由于包含振动能级的粒子集合与基态粒子集合相似, 均是通过粒子间的碰撞反应实现相互作用, 因此, 本文构建简化集的思路对于振动激发态集合同样适用. 下一步, 将纳入振动态集合, 并考虑火星沙尘颗粒的影响, 与类火星大气条件下的实验探究结果进行对比, 对反应集合进行进一步的完善与改进, 揭示火星CO2放电中主要与本质的反应过程, 深化对火星大气的认识, 为火星CO2放电及原位制氧的研究提供理论基础.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (E01) | e + e + C+ $\Rightarrow $ C + e | 5.0 × 10–39 | [55] |
| (E02) | e + CO+ $\Rightarrow $ C + O | 3.46 × 10–14Te–0.48 | [56] |
| (E03) | e + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ $\Rightarrow $ C + O2 | 3.94 × 10–13Te–0.4 | [21] |
| (E04) | e + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ $\Rightarrow $ CO + O | 2.0 × 10–11Te–0.5Tg–1 | [18] |
| (E05) | e + $ {\mathrm{C}\mathrm{O}}_{4}^{+} $ $\Rightarrow $ CO2 + O2 | 1.61 × 10–13Te–0.5 | [18] |
| (E06) | e + $ {\mathrm{C}}_{2}{\mathrm{O}}_{2}^{+} $ $\Rightarrow $ 2CO | 4.0 × 10–13Te–0.34 | [18] |
| (E07) | e + $ {\mathrm{C}}_{2}{\mathrm{O}}_{3}^{+} $ $\Rightarrow $ CO2 + CO | 5.4 × 10–14Te–0.7 | [18] |
| (E08) | e + $ {\mathrm{C}}_{2}{\mathrm{O}}_{4}^{+} $ $\Rightarrow $ 2CO2 | 2.0 × 10–11Te–0.5Tg–1 | [18] |
| (E09) | e + O2 + O2 $\Rightarrow $ $ {\mathrm{O}}_{2}^{-} $ + O2 | 2.2 × 10–41(300/Tg)1.5exp(-600/Tg) | [52] |
| (E10) | e + O + O2 $\Rightarrow $ O– + O2 | 1.0 × 10–43exp(300/Tg) | [52] |
| (E11) | e + O3 + O2 $\Rightarrow $ $ {\mathrm{O}}_{3}^{-} $ + O2 | 4.6 × 10–40 | [52] |
| (E12) | e + O+ + M $\Rightarrow $ O + M | 6.0 × 10–39(Te × 38.67)–1.5 | [57] |
| (E13) | e + $ {\mathrm{O}}_{2}^{+} $ $\Rightarrow $ 2O | 6.0 × 10–13Te–0.5(1/Tg)0.5 | [21] |
| (E14) | e + $ {\mathrm{O}}_{2}^{+} $ + M $\Rightarrow $ O2 + M | 6.0 × 10–39(Te × 38.67)–1.5 | [57] |
| (E15) | e + $ {\mathrm{O}}_{2}^{+} $ + e $\Rightarrow $ O2 + e | 1.0 × 10–31(Te × 38.67)–4.5 | [57] |
| (E16) | e + O+ + e $\Rightarrow $ O + e | 7.2 × 10–32(Te × 38.67)–4.5 | [57] |
| (E17) | e + $ {\mathrm{O}}_{4}^{+} $ $\Rightarrow $ 2O2 | 2.25 × 10–13Te–0.5 | [18] |
| (E18) | e + $ {\mathrm{O}}_{5}^{+} $ $\Rightarrow $ O2 + O3 | 5.0 × 10–12(Te × 38.67)–0.6 | [52] |
表A3初始集合中由反应速率系数描述的电子碰撞反应, 其中Te为电子温度, 单位是eV; Tg为气体温度, 单位是K; 速率系数的单位在二体或三体反应中分别是m3/s或m6/s
TableA3.Electron impact reactions described by rate coefficients in the original model. Te is the electron temperature in eV and Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (N01) | CO2 + O $ \Rightarrow$ CO + O2 | 2.8 × 10–17exp(–26500/Tg) | [21] |
| (N02) | CO + O2 $ \Rightarrow$ CO2 + O | 4.2 × 10–18exp(–24000/Tg) | [21] |
| (N03) | CO2 + C $ \Rightarrow$ 2CO | 1.0 × 10–21 | [21] |
| (N04) | C + O2 $ \Rightarrow$ O + CO | 3.0 × 10–17 | [21] |
| (N05) | C + O + M $ \Rightarrow$ M + CO | 2.14 × 10–41(Tg/300)–3.08exp(–2114/Tg) | [21] |
| (N06) | CO + M $ \Rightarrow$ O + C + M | 1.52 × 10–10(Tg/298)–3.1exp(–129000/Tg) | [58] |
| (N07) | CO + O3 $ \Rightarrow$ CO2 + O2 | 4.0 × 10–31 | [52] |
| (N08) | CO2 + CO2 $ \Rightarrow$ CO + O + CO2 | 3.91 × 10–16exp(–49430/Tg) | [59] |
| (N09) | C + CO + CO2 $ \Rightarrow$ C2O + CO2 | 6.3 × 10–44 | [59] |
| (N10) | C2O + O $ \Rightarrow$ 2CO | 5.0 × 10–17 | [18] |
| (N11) | C2O + O2 $ \Rightarrow$ CO2 + CO | 3.3 × 10–19 | [18] |
| (N12) | O + O2 + CO2 $ \Rightarrow$ O3 + CO2 | 1.7 × 10–42Tg–1.2 | [48] |
| (N13) | O + O + CO2 $ \Rightarrow$ O2 + CO2 | 3.81 × 10–42Tg–1exp(–170/Tg) | [48] |
| (N14) | O + CO + CO2 $ \Rightarrow$ 2CO2 | 1.6 × 10–45exp(–1510/Tg) | [48] |
| (N15) | O + CO + CO $ \Rightarrow$ CO2 + CO | 6.54 × 10–45 | [60] |
| (N16) | O + O2 + CO $ \Rightarrow$ CO2 + O2 | 6.51 × 10–48 | [60] |
| (N17) | O + O + CO $ \Rightarrow$ O2 + CO | 2.76 × 10–46 | [60] |
| (N18) | O + O + O $ \Rightarrow$ O2 + O | 6.2 × 10–44exp(–750/Tg) | [52] |
| (N19) | O + O + O2 $ \Rightarrow$ 2O2 | 1.3 × 10–44(Tg/300)–1exp(–170/Tg) | [52] |
| (N20) | O + O3 $ \Rightarrow$ 2O2 | 3.1 × 10–20Tg0.75exp(–1575/Tg) | [18] |
| (N21) | O2 + O3 $ \Rightarrow$ 2O2 + O | 7.26 × 10–16exp(–11400/Tg) | [48] |
| (N22) | O2 + O + O2 $ \Rightarrow$ O3 + O2 | 8.61 × 10–43Tg–1.25 | [48] |
| (N23) | O2 + O2 $ \Rightarrow$ O + O3 | 2.1 × 10–17exp(–498000/Tg) | [57] |
| (N24) | O2 + M $ \Rightarrow$ O + O + M | 3.0 × 10–12Tg–1exp(–59380/Tg) | [57] |
表A4初始集合中的中性粒子反应, 其中 Tg 为气体温度, 单位是 K; 速率系数的单位在二体或三体反应中分别是 m3/s 或 m6/s
TableA4.Reaction of neutrals in the original model. Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.
| 序号 | 反应 | 文献 | 序号 | 反应 | 文献 | |
| (Y01) | e + CO2 $\Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + 2e | [50] | (Y11) | e + O3 $\Rightarrow $ $ {\mathrm{O}}_{2}^{-} $ + O | [50] | |
| (Y02) | e + CO2 $\Rightarrow $ CO + O + e | [50] | (Y12) | e + O3 $\Rightarrow $ O2 + O– | [50] | |
| (Y03) | e + CO2 $\Rightarrow $ CO + O– | [50] | (Y13) | e + O3 $\Rightarrow $ O + O2 + e | [53] | |
| (Y04) | e + CO2 $\Rightarrow $ 2e + O + CO+ | [50] | (Y14) | e + O3 $\Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + O + 2e | [53] | |
| (Y05) | e + CO2 $\Rightarrow $ 2e + CO + O+ | [50] | (Y15) | e + O2 $\Rightarrow $ 2 O + e | [50] | |
| (Y06) | e + CO2 $\Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + C + 2e | [51, 52] | (Y16) | e + O2 $\Rightarrow $ O + O– | [50] | |
| (Y07) | e + CO $\Rightarrow $ C + O– | [50] | (Y17) | e + O2 $\Rightarrow $ 2e + $ {\mathrm{O}}_{2}^{+} $ | [50] | |
| (Y08) | e + CO $\Rightarrow $ e + C + O | [50] | (Y18) | e + O $\Rightarrow $ 2e + O+ | [50] | |
| (Y09) | e + CO $\Rightarrow $ 2e + CO+ | [50] | (Y19) | e + C $\Rightarrow $ 2e + C+ | [50] | |
| (Y10) | e + CO $\Rightarrow $ 2e + C+ + O | [50] |
表B2简化集合中由碰撞截面描述的电子碰撞反应
TableB2.Electron impact reactions described by collision cross sections in the simplified model.
简化集合包含的粒子种类如表B1所列, 考虑到碰撞种类和反应速率系数计算方式的差异, 这些粒子构成的反应被划分为不同的碰撞反应子集, 如表B2—B5所列.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (F01) | e + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ $\Rightarrow $ C + O2 | 3.94 × 10–13Te–0.4 | [21] |
| (F02) | e + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ $\Rightarrow $ CO + O | 2.0 × 10–11Te–0.5Tg–1 | [18] |
| (F03) | e + O3 + O2 $\Rightarrow $ $ {\mathrm{O}}_{3}^{-} $ + O2 | 4.6 × 10–40 | [52] |
| (F04) | e + $ {\mathrm{O}}_{2}^{+} $ $\Rightarrow $ 2O | 6.0 × 10–13Te–0.5(1/Tg)0.5 | [21] |
表B3简化集合中由反应速率系数描述的电子碰撞反应, 其中Te为电子温度, 单位是eV; Tg为气体温度, 单位是K; 速率系数的单位在二体或三体反应中分别是m3/s或m6/s
TableB3.Electron impact reactions described by rate coefficients in the simplified model. Te is the electron temperature in eV and Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (M01) | CO2 + C $ \Rightarrow$ 2 CO | 1.0 × 10–21 | [21] |
| (M02) | C + O2 $\Rightarrow $ O + CO | 3.0 × 10–17 | [21] |
| (M03) | O + O2 + CO2 $\Rightarrow $ O3 + CO2 | 1.7 × 10–42Tg–1.2 | [48] |
| (M04) | O + O + CO2 $\Rightarrow $ O2 + CO2 | 3.81 × 10–42Tg–1exp(–170/Tg) | [48] |
表B4简化集合中的中性粒子反应, 其中, Tg 为气体温度, 单位是 K; 速率系数的单位在二体或三体反应中分别是 m3/s 或 m6/s
TableB4.Reaction of neutrals in the simplified model. Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.
| 序号 | 反应 | 反应速率系数 | 文献 |
| (H01) | O– + CO2 $ \Rightarrow $ O + CO2 + e | 4.0 × 10–18 | [48] |
| (H02) | O– + CO2 + CO $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO | 1.5 × 10–40 | [61] |
| (H03) | O– + CO2 + O2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 3.1 × 10–40 | [61] |
| (H04) | O– + CO2 + CO2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO2 | 9.0 × 10–41 | [52] |
| (H05) | $ {\mathrm{O}}_{2}^{-} $ + CO2 + O2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O2 | 4.7 × 10–41 | [52] |
| (H06) | $ {\mathrm{O}}_{3}^{-} $ + CO2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 5.5 × 10–16 | [18] |
| (H07) | O+ + CO2 $ \Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + CO | 9.4 × 10–16 | [18] |
| (H08) | O+ + CO2 $ \Rightarrow $ O + $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ | 4.5 × 10–16 | [18] |
| (H09) | C+ + CO2 $ \Rightarrow $ CO+ + CO | 1.1 × 10–15 | [18] |
| (H10) | CO+ + CO2 $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + CO | 1.0 × 10–15 | [56] |
| (H11) | O– + CO $ \Rightarrow $ CO2 + e | 5.5 × 10–16 | [44] |
| (H12) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + CO $ \Rightarrow $ 2CO2 + e | 5.0 × 10–19 | [58] |
| (H13) | $ {\mathrm{O}}_{2}^{+} $ + C $ \Rightarrow $ CO+ + O | 5.2 × 10–17 | [18] |
| (H14) | $ {\mathrm{O}}_{2}^{+} $ + C $ \Rightarrow $ C+ + O2 | 5.2 × 10–17 | [18] |
| (H15) | O– + C $ \Rightarrow $ CO + e | 5.0 × 10–16 | [57] |
| (H16) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O $ \Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + CO | 1.638 × 10–16 | [52] |
| (H17) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O $ \Rightarrow $ CO2 + O+ | 9.62 × 10–17 | [18] |
| (H18) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow $ $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O2 | 1.1 × 10–16 | [18] |
| (H19) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow $ CO2 + O2 + O– | 1.4 × 10–17 | [18] |
| (H20) | $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ + O $ \Rightarrow $ CO2 + $ {\mathrm{O}}_{3}^{-} $ | 1.4 × 10–16 | [18] |
| (H21) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow $ CO2 + $ {\mathrm{O}}_{2}^{-} $ | 8.0 × 10–17 | [58] |
| (H22) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O2 $ \Rightarrow $ $ {\mathrm{O}}_{2}^{+} $ + CO2 | 6.4 × 10–17 | [52] |
| (H23) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + O– $ \Rightarrow $ O + CO2 | 1.0 × 10–13 | [62] |
| (H24) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{O}}_{2}^{-} $ $ \Rightarrow $ CO + O2 + O | 6.0 × 10–13 | [44] |
| (H25) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ $ \Rightarrow $ 2CO2 + O | 5.0 × 10–13 | [58] |
| (H26) | $ {\mathrm{C}\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow $ 2CO2 + O2 | 5.0 × 10–13 | [18] |
| (H27) | $ {\mathrm{C}\mathrm{O}}_{3}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow $ CO2 + O2 + O | 3.0 × 10–13 | [18] |
| (H28) | $ {\mathrm{O}}_{2}^{+} $ + $ {\mathrm{C}\mathrm{O}}_{4}^{-} $ $ \Rightarrow $ CO2 + 2O2 | 3.0 × 10–13 | [18] |
| (H29) | O– + O3 $ \Rightarrow $ 2O2 + e | 3.0 × 10–16 | [44] |
| (H30) | O– + O3 $ \Rightarrow $ $ {\mathrm{O}}_{3}^{-} $ + O | 8.0 × 10–16 | [18] |
| (H31) | $ {\mathrm{O}}_{2}^{-} $ + O3 $ \Rightarrow $ $ {\mathrm{O}}_{3}^{-} $ + O2 | 4.0 × 10–16 | [18] |
| (H32) | O– + O2 $ \Rightarrow $ O + e + O2 | 6.9 × 10–16 | [52] |
| (H33) | O– + O $ \Rightarrow $ O2 + e | 2.3 × 10–16 | [21] |
| (H34) | $ {\mathrm{O}}_{2}^{-} $ + O $ \Rightarrow $ O2 + O– | 3.31 × 10–16 | [21] |
| (H35) | $ {\mathrm{O}}_{2}^{-} $ + O $ \Rightarrow $ O3 + e | 3.3 × 10–16 | [18] |
| (H36) | $ {\mathrm{O}}_{3}^{-} $ + O $ \Rightarrow $ $ {\mathrm{O}}_{2}^{-} $ + O2 | 2.5 × 10–16 | [18] |
| (H37) | O–+ $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow $ O2 + O | 2.6 × 10–14(300/Tg)0.44 | [21] |
| (H38) | O– + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow $ 3O | 4.2 × 10–13(300/Tg)0.44 | [21] |
| (H39) | $ {\mathrm{O}}_{2}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow $ 2O2 | 2.01 × 10–13(300/Tg)0.5 | [21] |
| (H40) | $ {\mathrm{O}}_{2}^{-} $ + $ {\mathrm{O}}_{2}^{+} $ $ \Rightarrow $ O2 + 2O | 4.2 × 10–13 | [21] |
表B5简化集合中的离子-中性和离子-离子反应, 其中Tg为气体温度, 单位是K; 速率系数的单位在二体或三体反应中分别是m3/s或m6/s
TableB5.Ion-neutral and ion-ion reactions in the simplified model. Tg is the gas temperature in K. The rate coefficients are in m3/s or m6/s for binary or ternary reactions.








