 ,1, 尹玉和2, 王琼
,1, 尹玉和2, 王琼 ,1, 林团荣2, 郭华春
,1, 林团荣2, 郭华春 ,1
,1Correlation Analysis of Volatile Flavor Components and Metabolites Among Potato Varieties
LI KaiFeng ,1, YIN YuHe2, WANG Qiong
,1, YIN YuHe2, WANG Qiong ,1, LIN TuanRong2, GUO HuaChun
,1, LIN TuanRong2, GUO HuaChun ,1
,1通讯作者:
责任编辑: 赵伶俐
收稿日期:2020-04-15接受日期:2020-09-23网络出版日期:2021-02-16
| 基金资助: |
Received:2020-04-15Accepted:2020-09-23Online:2021-02-16
作者简介 About authors
李凯峰,E-mail:

摘要
关键词:
Abstract
Keywords:
PDF (3202KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
李凯峰, 尹玉和, 王琼, 林团荣, 郭华春. 不同马铃薯品种挥发性风味成分及代谢产物相关性分析[J]. 中国农业科学, 2021, 54(4): 792-803 doi:10.3864/j.issn.0578-1752.2021.04.011
LI KaiFeng, YIN YuHe, WANG Qiong, LIN TuanRong, GUO HuaChun.
开放科学(资源服务)标识码(OSID):

0 引言
【研究意义】马铃薯在投放鲜食消费市场后,风味品质是决定其能否被消费者接纳的主要因素之一。中国马铃薯50%以上为鲜食消费,需求巨大。市场对风味品质不佳的品种接受程度低,影响新育成品种的种植和推广[1]。香味是影响马铃薯整体风味品质的重要因素,而挥发性风味化合物则是构成食品香味的物质基础。其主要为一类具有特殊嗅味特征的有机化合物,包括醛、酯、酮和吡嗪等其他杂环化合物[2]。考察挥发性风味化合物构成规律,有助于寻找改良风味品质的新途径,对提高消费者接受程度也具有重要意义[1]。【前人研究进展】马铃薯中的挥发性风味化合物共检出300余种[3]。不同烹饪方式下,风味化合物的结构和组成差别明显[4]。影响感官评价的主要成分是由脂类降解产生的醛类化合物[5],以及美拉德反应下,氨基酸和糖类反应生成的呋喃[6]、吡嗪类物质组成[7,8]。环境因素,包括栽培条件、采收贮藏[9]以及加工预处理条件[10]等均会影响马铃薯风味的构成。除烹饪方式外,风味化合物的构成在品种间也存在差异[11];马铃薯富利加亚种(S. phureja)中富含阿尔法古巴烯且风味独特,在品尝试验中获得比普通栽培种(Solanum tuberosum)更高的分数。甲硫基丙醛是重要的挥发性化合物,其含量在品种间存在差异[11]。虽然通过基因编辑可间接增加含硫氨基酸的含量[12],但是对多倍体材料进行基因编辑的难度相对较高。而MORRIS等[13]发现对单一化合物含量的添加无法显著提高整体的风味品质。目前,国内外的相关报道聚焦于环境因素对风味成分构成的影响分析,以及风味相关“标志化合物”的筛选[8]。【本研究切入点】虽然代谢化合物是挥发性风味化合物构成的基础,但鲜有将两者进行联合分析的报告。此外,与组学快捷、高通量的特性相比,传统的营养成分检测手段仅着重于某几个或某一类化合物的检测,无法从整体上有效地反映块茎熟化前较短一段时间内,组织中代谢化合物的全貌。【拟解决的关键问题】本研究对挥发性化合物和烹饪前短时间内块茎主要代谢产物进行代谢组检测,初步挖掘与挥发性风味组分相关的代谢化合物,为品种品质改良提供参考。1 材料与方法
试验于2019年在云南农业大学农学与生物技术学院进行。1.1 试验材料
本试验所用的7个马铃薯品种(系),包括希森6号、后旗红、华颂7号、冀张薯12号、青薯9号、D545和D727,由内蒙古乌兰察布市农牧业科学研究院提供,采收后于4℃下统一贮藏并在20 d内完成测试。1.2 试验试剂与设备
2-甲基-3-庚酮(0.163 μg?μL-1)、正构烷烃(C7-C40)、核糖醇、2%甲氧胺盐酸盐吡啶(MOX)、(三甲基硅烷基)三氟乙酰胺(BSTFA)以及其他色谱纯化合物标准品均购自Sigma-Aldrich Chemical公司。NaCl为分析纯,购自天津科密欧公司。顶空固相微萃取纤维头75 μm CAR/PDMS 100 μm PDMS(Sigma-Aldrich Chemical公司),气相色谱-质谱联用仪(型号7890A\5970B,安捷伦公司),去离子水处理机(北京厉元),电空气炸锅(苏泊尔公司),红外线测温仪(深圳标智仪表公司),恒温水浴锅(金城致杰公司)。
1.3 试验方法
1.3.1 挥发性风味化合物测定(1)样品前处理
马铃薯洗净,晾干,切块(9 cm×5 cm×3 cm),取200 g。空气炸锅通电100℃预热10 min后放入马铃薯块,并于150℃下恒温加热30 min,剪取表面1—1.5 mm厚样品,充分剪碎后混合。萃取纤维头在第一次使用前,于气相色谱的进样口老化,老化温度为250℃,时间30 min,每次进样后,再于进样口老化10 min。
经预处理后的材料,取3 g NaCl加入1 μL浓度为0.163 μg?μL-1的2-甲基-3-庚酮作为内标物质于25 mL顶空瓶中,用聚四氟乙烯隔垫密封后,于50℃水浴平衡30 min,萃取40 min。每个组合进行3次重复,各重复所用材料独立重新制备。萃取后的纤维头在温度为250℃的气相色谱-质谱联用仪进样口中解吸附5 min,进行GC-MS分析。
(2)GC-MS条件
参考龚兴旺等[14]的方法,并作适当调整。色谱柱为HP-5 ms(30 m×0.25 mm×0.25 μm)毛细管柱,载气为氦气,不分流进样,流速为1.2 mL?min-1。升温条件:初始温度40℃,保持3 min,以5℃?min-1升温至200℃,再以10℃?min-1升至230℃,保持5 min。
质谱条件:电子轰击离子源(EI),电子能量70 eV,传输线温度280℃,离子源温度230℃,四级杆温度150℃,质量扫描范围(m/z)33—550,溶剂延迟1 min。
(3)定性定量方法
化合物定性:分别使用Agilent ChemStation软件以及XCMS完成峰对齐和矫正,对利用metGC和ChemStation识别到的潜在峰经过NIST14比对,过滤并保留正反匹配均大于800的峰,对过滤后的结果使用保留指数法(RI)进行筛选,对筛选后的结果结合人工谱图解析和标样质谱图比对进行化合物定性。
化合物定量:挥发性化合物参考公式[5]:
式中,C为未知化合物浓度(μg?g-1),Ci为内标物质含量(μg),S为未知化合物定量离子峰面积,Si为内标物定量离子峰面积,m为样品质量(g)。
1.3.2 代谢化合物测定
(1)样品前处理
样品前处理及升温条件参考ZHANG等[15]的方法,并做适当调整。取做风味化合物测定时切好的新鲜块茎小块(9 cm×5 cm×3 cm),每块茎取3块,快速切成1 cm3左右的小块,混匀后在液氮下冻干,并于-80℃冰箱保存。样品检测时,于材料未溶解前快速打粉混匀。取样400 mg,移入10 mL离心管中。加入100 μL核糖醇水溶液(2 mg?mL-1)作为极性内标。加入甲醇1.36 mL,漩涡振荡1 min。冰水超声2 min、手摇1 min,循环10次。4℃下12 000 r/min离心10 min。吸取上清液250 μL,氮气吹干。加入MOX吡啶溶液(20 mg?mL-1)50 μL后旋转振荡30 s,于50℃下肟化孵育4 h。加入40 μL的BSTFA后,充入氮气。旋转振荡30 s后,在50℃下衍生化60 min。
(2)GC-MS条件
色谱条件:色谱柱为HP-5 ms(30 m×0.25 mm×0.25 μm)毛细管柱,载气为氦气,进样量为1 μL,分流流量10 mL?min-1,分流比20﹕1,隔垫吹扫3 mL?min-1。进样口温度:280℃,柱流量2 mL?min-1。初始温度80℃保持2 min,随后以10℃?min-1升温至310℃,保持6 min。
质谱条件:电子轰击离子源(EI),电子能量70 eV。传输线温度:250℃,离子源温度230℃,四极杆温度150℃。扫描范围(m/z)50—600,后于70℃下运行6 min,溶剂延迟3 min。
(3)定性定量方法
化合物定性:使用Mzmine2完成峰检测、对齐和矫正,随后利用AMDIS对潜在化合物峰进行解卷积。使用Agilent ChemStation软件完成自动峰识别,对利用AMDIS和ChemStation识别到的潜在峰经过NIST14比对,过滤并保留正向匹配大于800、反向匹配大于700的峰,筛选峰宽±5%时间窗口内用两种方法鉴定一致的化合物,对经过软件鉴定的结果使用保留指数法(RI)进行二次筛选,筛选后的结果结合人工谱图解析和标样质谱图比对进行化合物定性。
化合物定量:参考GAO等[16]使用面积归一化法进行定量
1.4 数据分析
数据采用SPSS软件进行单因素方差分析,对F值显著(P<0.05)的成分使用Fisher检验法进行处理间的两两比较,随后使用R和基于R的MetaboAnalyst平台进行数据归一化及PLS-DA、聚类分析。各品种风味强度值计算:
式中,Ci:各品种挥发性组分含量(μg?g-1),a:2-甲基呋喃,b:1-辛烯-3-醇,c:反,顺-2,6-壬二烯醛,d:癸醛,e:2,3-辛二酮,f:甲硫基丙醛,g:反,反-2,6-壬二烯醛,h:反-2-癸烯醛。
2 结果
2.1 挥发性风味化合物测定及品种聚类
表1所示为品种间差异的22种挥发性化合物。品种冀张薯12号中,反-2-辛烯醛含量显著高于品种华颂7号、希森6号和青薯9号(P<0.05),反,顺-2, 6-壬二烯醛含量极显著高于其他品种(P< 0.01),苯乙醛含量显著高于希森6号和华颂7号(P<0.05)。青薯9号中,反,反-2,4-癸二烯醛含量显著高于品种D727(P<0.05),3-辛烯-2-酮含量显著高于品种希森6号、华颂7号和D727(P0.05),而2-甲氧基苯酚含量极显著高于所有其他品种(P<0.01)。D548中,反,反-2,6-壬二烯醛含量极显著高于除D727和冀张薯12号外的其他品种(P<0.01),甲硫基丙醛含量极显著高于品种华颂7号(P<0.01)。Table 1
表1
表1六个马铃薯品种中差异挥发性化合物
Table 1
| 化合物 Compound | 品种 Variety | ||||||
|---|---|---|---|---|---|---|---|
| 希森6号 Xisen No.6 | 冀张薯12号 Jizhangshu No.12 | 后旗红 Houqihong | 华颂7号 Huasong No.7 | D548 | D727 | 青薯9号 Qingshu No.9 | |
| 反-2-癸烯醛(E)-2-Decenal | 0.01±0.01A | 0.08±0.02C | 0.01±0.01A | — | 0.03±0.01AB | 0.04±0.02B | 0.03±0.02AB |
| 反-十二烯醛(E)-2-Dodecenal | 0.03±0.01a | 0.67±0.38b | 0.27±0.14a | 0.03±0.03a | 0.13±0.01a | 0.24±0.37a | 0.09±0.02a |
| 2-庚酮 2-Heptanone | 0.06±0.02D | 0.01±0.01A | 0.01±0.01A | 0.03±0.01C | 0.01±0.01A | — | 0.02±0.01AB |
| 反-2-庚烯醛(E)-2-Heptenal | 0.02±0.02A | 2.03±1.07B | 0.36±0.48A | 0.04±0.03A | 0.26±0.38A | 0.25±0.27A | 0.06±0.02A |
| 反-2-辛烯醛(E)-2-Octenal | 0.22±0.04a | 0.75±0.36b | 0.4±0.11ab | 0.21±0.06a | 0.41±0.09ab | 0.55±0.29ab | 0.19±0.16a |
| 2-十一烯醛 2-Undecenal | 0.03±0.01A | 0.26±0.15B | 0.07±0.03A | 0.03±0.01A | 0.08±0.03A | 0.11±0.08A | 0.06±0.01A |
| 反,反-2,4-癸二烯醛 (E,E)-2,4-Decadienal | 2.12±0.49bc | 1.08±1.28ab | 2.95±0.16c | 2.21±1.01bc | 1.85±0.61abc | 0.56±0.48a | 2.54±0.28c |
| 反,反-2,6-壬二烯醛 (E,E)-2,6-Nonadienal | 0.38±0.07AB | 0.87±0.21CD | 0.28±0.1A | 0.32±0.07A | 1.17±0.32D | 0.78±0.29BCD | 0.67±0.28ABC |
| 反,顺-2,6-壬二烯醛 (E,Z)-2,6-Nonadienal | 0.06±0.02A | 2.26±0.88B | 0.16±0.1A | 0.03±0.1A | 0.72±0.65A | 0.74±0.21A | 0.08±0.03A |
| 3-辛烯-2-酮 3-Octen-2-one | 0.01±0.01a | 0.03±0.01b | — | 0.01±0.01a | 0.02±0.01ab | 0.01±0.01a | 0.03±0.02b |
| 3,5-辛二烯-2-醇 3,5-Octadien-2-ol | 0.02±0.01A | 0.22±0.15B | 0.07±0.04A | 0.01±0.01A | 0.13±0.05AB | 0.11±0.01A | 0.04±0.02A |
| 1-辛醇 1-Octanol | 0.04±0.04A | 0.33±0.17B | 0.04±0.04A | 0.09±0.02A | 0.14±0.06A | 0.16±0.04A | 0.09±0.04A |
| 苯乙醛Benzeneacetaldehyde | 31.4±9.36a | 66.11±19.06b | 51.71±17.02ab | 33.13±1.43a | 66.54±19.91b | 51.7±13.9ab | 54.4±2ab |
| 异戊醛3-Methylbutanal | 7.26±4.18A | 31.7±5.41B | 12.48±3.32A | 7.07±0.1A | 10.54±3.42A | 15.17±7.2A | 9.81±0.22A |
| 2-甲基呋喃2-Methylfuran | 0.28±0.2A | 7.41±5.09B | 0.6±0.21A | 0.12±0.04A | 1.43±0.99A | 2.18±1.4A | 0.09±0.06A |
| 2-甲基丙醛2-Methylpropanal | 9.39±3.79A | 148.69±77.63B | 41.5±16.95A | 14.52±2.22A | 33.49±36.19A | 52.79±21.74A | 15.13±7.3A |
| 2,6-二甲基吡嗪 2,6-Dimethylpyrazine | 0.34±0.09a | 2.25±1.84b | 0.42±0.06a | 0.24±0.01a | 0.41±0.06a | 0.54±0.1a | 0.22±0.15a |
| 2,3,5-三甲基吡嗪 2,3,5-Trimethylpyrazine | 34.77±9.95c | 21.08±13.76abc | 28.52±4.03bc | 27.26±7.55abc | 16.69±4.49ab | 12.77±7.07a | 30.74±5.07bc |
| 2,5-二甲基吡嗪 2,5-Dimethylpyrazine | 103.87±33.75C | 12.16±9.72A | 28.64±49.61AB | 74.26±13.02BC | 5.27±4.32A | 8.27±10.04A | 43.43±43.43AB |
| 甲硫基丙醛Methional | 6.76±1.19AB | 16.68±4.22D | 8.5±0.8ABC | 6.05±0.53A | 12.71±5.92BCD | 13.83±3.74CD | 11.74±1.56ABCD |
| 2-甲氧基苯酚 2-Methoxyphenol | 0.52±0.19BC | 0.25±0.1AB | 0.73±0.38C | 1.23±0.06D | 0.14±0.05A | 0.44±0.19ABC | 2.25±0.17E |
| 1,6-二甲基萘 1,6-Dimethylnaphthalene | — | 0.03±0.02b | 0.01±0.01a | 0.01±0.01a | 0.01±0.01a | 0.01±0.01a | 0.01±0.01a |
新窗口打开|下载CSV
马铃薯熟化后产生的挥发性化合物与消费者对其感官评价的优劣存在一定的相关性,这些差异显著的挥发性化合物,可能是导致不同品种间存在风味差异的潜在原因。因此,使用筛选出的22种化合物对品种进行聚类,探索品种风味相似性。
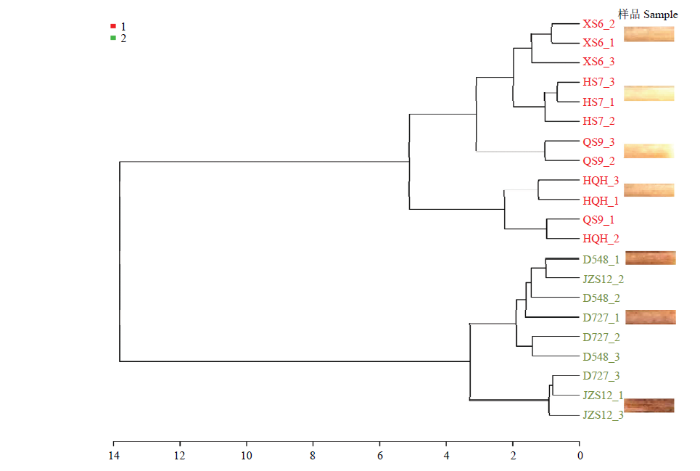
计算样品间的欧氏距离(Euclidean Distance)后,使用Ward法对7个马铃薯品种进行聚类的结果如图1所示。结合对熟化后样品色泽的比较,本试验将7个品种聚为两类。类1包括品种希森6号、华颂7号、青薯9号和后旗红4个品种,类2包括冀张薯12号、D548和D727 3个品种(系)。类1品种与类2品种相比,经过熟化后的材料颜色更深,可能暗示着类2品种具有更高的还原糖含量。而还原糖在熟化过程中参与的美拉德反应,则是挥发性风味物质的主要来源之一。
图1
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图17个马铃薯品种Ward法聚类
Fig. 1Cluster diagram of seven potato varieties
XS6:希森6号 Xisen No. 6;HQH:后旗红 Houqihong;HS7:华颂7号 Huasong No. 7;JZS12:冀张薯12号 Jizhangshu No. 12,QS9:青薯9号 Qingshu No. 9。下同 The same as below
为了进一步验证品种间的差异化合物对不同风味特征群体的代表性,利用全部检出化合物作为指标对7个品种进行偏最小二乘法判别分析,分析结果如图2所示。偏最小二乘法判别分析表明,类1品种与类2品种之间确实存在挥发性化合物构成上的差异。以VIP>1为标准,共筛选出差异组分19种(图2-B)。分别计算各品种的风味强度值(式2),类1的4个品种分别为:希森6号(4.15)、后旗红(3.44)、华颂7号(5.07)、青薯9号(2.32)。其中华颂7号风味强度值最高,且负向风味相关的挥发性化合物含量最低。类2的3个品种风味强度值分别为冀张薯12号(3.49)、D548(1.49)、D727(2.09),其中冀张薯12号风味强度值最高,因此,该品种在空气炸制烹饪方式下,马铃薯烘烤风味最为明显[8]。
图2
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2两个聚类分组下7个马铃薯品种PDLS-DA得分图
Fig. 2PDLS-DA scores of seven potato varieties under two cluster groups
2.2 代谢化合物差异检测及相关性分析
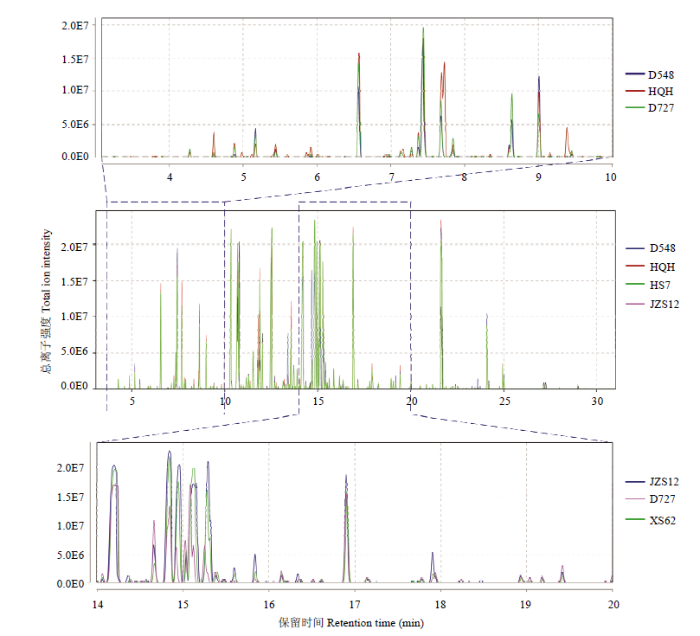
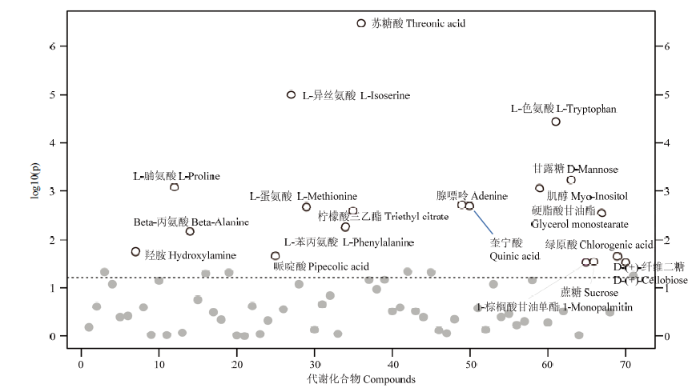
7个马铃薯品种(系)块茎代谢物TIC如图3所示,以品种希森6号、华颂7号、青薯9号和后旗红为类别1,以品种冀张薯1号、D548、D727为类别2;所有参试材料新鲜块茎组织中共检出代谢化合物69种,经非平衡条件T检验后,共筛选出在分类1和分类2间差异显著(P<0.05)的代谢化合物19种(图4)。图3
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图37个马铃薯品种(系)块茎检出代谢物总离子流图
Fig. 3Total ion current map of metabolites detected in tubers of seven potato cultivars (lines)
图4
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图4主要代谢化合Fisher检验P值
Fig. 4P-value diagram of Fisher test for major metabolites
图5所示为19种差异代谢化合物在两个类别中的含量分布,其中检出的3种脂类,5种氨基酸和其他化合物,如奎宁酸(Quinic acid)等共14种均在类2的品种中较高(P<0.05)。而剩下的包括腺嘌呤(Adenine)、脯氨酸(L-Proline)、哌啶酸(Pipecolic acid)、D-(+)-纤维二糖(D-(+)-Cellobiose)和L-异丝氨酸(L-Isoserine)这5种化合物在类1的品种中含量较高(P<0.05)。
图5
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图5显著差异代谢产物含量分布
Fig. 5Distribution of metabolites with significant difference
差异代谢化合物可能是影响风味特征差异的潜在原因,所以将各品种经熟化处理后筛选出的19个主要差异挥发性化合物与筛选出的19个主要差异代谢化合物,使用parson法进行联合相关性分析。原始数据使用R语言经Log转换且Pareto法归一化后,进行分析。
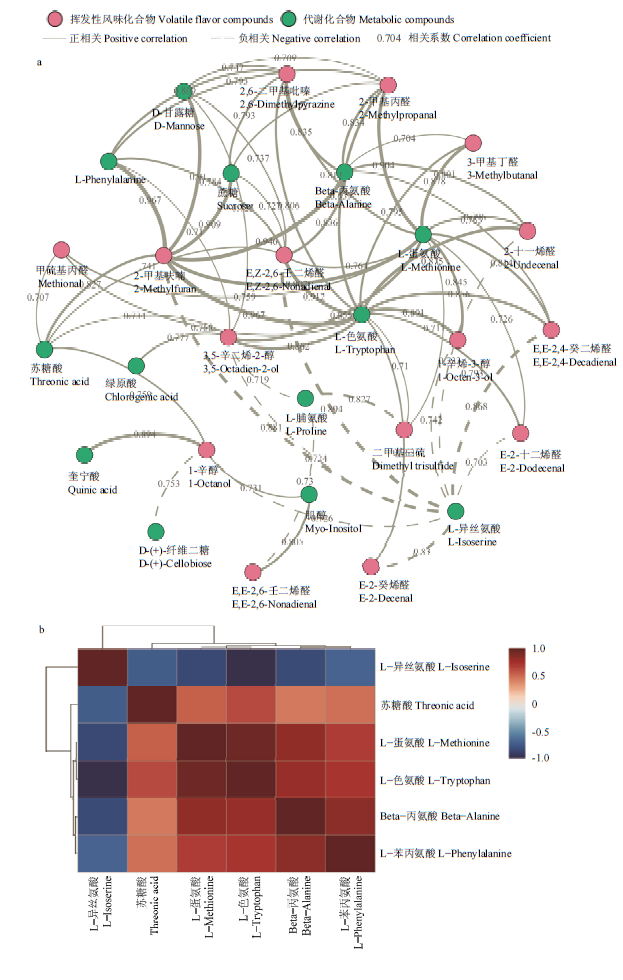
图6-a所示为相关性显著(P<0.05),且相关性系数绝对值大于0.6的风味组分和代谢化合物间的相关性网络;剔除相关性相对较弱的化合物后,19种差异挥发性风味化合物中的15种与块茎代谢化合物存在较强的相关性,相关系数均达到0.7以上。
图6
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图6挥发性风味组分和代谢化合物间相关性网络及热图
Fig. 6Correlation network of volatile flavor components and metabolic compounds in potato
与5种以上代谢化合物存在较强相关联系的风味化合物有2-甲基呋喃(2-Methylfuran)、3,5-辛二烯-2-醇(3,5-Octadien-2-ol)、反,顺-2,6-壬二烯醛(E,Z-2,6- Nonadienal)、2,6-二甲基吡嗪(2,6-Dimethylpyrazine)和2-甲基丙醛(2-Methylpropanal)。此类风味化合物占总检出挥发性化合物的9.1%。其中2-甲基呋喃与8种代谢物相关性显著,并和β-丙氨酸(Beta-Alanine)的相关程度最高。从代谢化合物的角度统计,5种代谢化合物与多个挥发性组分存在较强的显著相关,占总检出代谢化合物的7%;L-色氨酸(L-Tryptophan)与13种挥发性风味化合物呈显著的相关性,其与2-甲基呋喃(2-methylfuran)的相关最强,与反,反-2,4-癸二烯醛(E,E-2,4-Decadienal)、反,顺-2,6-壬二烯醛(E,Z-2,6-Nonadienal)这类脂类降解产生的醛类化合物也表现出了较强的相关性;除L-色氨酸(L-Tryptophan)外,蛋氨酸(L-methionine)、L-异丝氨酸(L-Isoserine)、β-丙氨酸(Beta-Alanine)、苯丙氨酸(L-Phenylalanine)等也与多个风味化合物显著相关(图6-b)。
3 讨论
空气炸制条件下,醛类和吡嗪类化合物是主要的挥发性风味化合物。代表性醛类化合物为反-2-己烯醛、反,顺-2,6-壬二烯醛等,与曾著莉等[17]对蒸煮烹饪方式下的检测结果一致;这些醛类化合物可能是在烹饪升温过程中,由依然保持活性的脂氧合酶(Lox)催化的前体物质裂解产生;构建风味指纹图谱并对食品材料进行鉴定分类的方法已经被广泛应用[18,19]。本研究根据风味化合物存在的差异程度,将7个马铃薯品种聚为两类。类1品种中共3种化合物在该分类的品种中含量较高,其中反,反-2,4-癸二烯醛(E,E-2,4-Decadienal)具有油和脂肪味;2-甲氧基苯酚(2-Methoxy-phenol)具有木香味,可能是由纤维素、半纤维素在高温下裂解产生;2-庚酮(2- Heptanone)则具有典型的蔬果香味,与香味特征呈正相关。但甲硫基丙醛(Methional)、二甲基三硫醚(Dimethyl trisulfide)和其他吡嗪类化合含量均较少,可能导致该类品种的马铃薯特征风味较类2品种弱,其中硫基丙醛(Methional)与整体的风味强度呈负相关,当其他风味化合物含量过低时,会呈现刺激性气味。反观类2品种,大部分差异风味化合物均在该分类下含量较高,其中2-甲基呋喃(2-Methylfuran)有香草味,与风味强度呈正相关;反,顺-2,6-壬二烯醛(E,Z-2,6-Nonadienal)是黄瓜的特征风味化合物,类似具有顺式结构的醛类能增加清爽的气味[20],但是,反,反-2,6-壬二烯醛(E,E-2,6-Nonadienal)、反-2-癸烯醛(E-2-Decenal)等一类具有反式结构的醛类产生油脂味,在浓度较高时,则有可能产生不良风味。2,3,5-三甲基吡嗪(2,3,5-Trimethylpyrazine)具有烤土豆味和可可味,吡嗪类物质往往与令人愉悦的气味特征有关。3,5-三甲基吡嗪、甲硫基丙醛等吡嗪类和醛类物质在两个类别中整体差异显著,会对品种在空气炸制条件下的风味构成影响。所以类2和类1品种在空气炸制的烹饪方式下,可能分别代表两种特点鲜明的风味特征。
使用GC-MS是鉴定和分离主要代谢化合物的经典方法[21],这种高通量无偏检测常被用于对生物和非生物胁迫的研究[16]。试验中主要检出的代谢化合物为氨基酸类、糖类和少量有机酸酸类。仅有L-异丝氨酸等11种化合物在两个类别中表现显著差异,说明分组内品种间化合物含量波动变化较大,暗示了代谢化合物存在一定程度的品种特异性,材料具有一定代表性。检出化合物在种类上,与ZHANG等[15]对东北地区几个主栽品种的检测结果一致,而与ROESSNER等[21]结果相比,少部分未检出,这可能是由于部分化合物在材料中的含量低于检出阈值所致。部分检出但无法鉴定的化合物可能为与次生代谢相关的次生代谢产物,需要进一步研究确认。
代谢组学可以反映某一阶段或某一时刻内代谢化合物特征的全貌,有助于从整体角度上讨论物质间的相关关系。块茎组织中游离态的代谢化合物是影响风味形成的原因之一[22],大部分研究者采用相关分析法来发现感官特征和风味化合物之间的联系,但风味化合物与代谢前体之间的相关性,则鲜有报道。本试验发现检出的挥发性组分中,与代谢化合物呈显著相关的物质相对较少,仅占总检出风味化合物的27.3%,这可能是由于受试验方法所限。脂类-氨基酸-糖类反应体系是构成马铃薯挥发性风味化合物的重要体系[23],试验中检出的氨基酸和糖类占检测化合物总数的47%,但与醛类风味组分合成相关的非极性化合物(如脂类)未检出,未来可以通过改进试验方法进一步扩大检出化合物种类。
具有显著相关性的化合物中,单个挥发性组分与多个代谢化组分呈较高相关性,这是因为在热化学作用下产生的风味化合物,往往由多个代谢化合物参与合成;2-甲基呋喃是丙氨酸、苏氨基酸和果糖以及葡萄糖通过热化学作用产生[24],且2-甲基呋喃与其含量间表现出较强的正相关。此外,热化学反应产生的风味化合物,易受块茎含水量、烹饪环境等多因素波动的影响,导致试验结果中大部分风味组分和其理论上的代谢底物相关性并不显著;但从应用价值角度看,本试验发现包括2,6-二甲基吡嗪、反,反-2,6-壬二烯醛在内的5种风味化合物,即使受到较多环境因素的影响,仍表现出与代谢化合物显著相关。此类具有稳定相关联系的化合物,具有进一步深入研究的价值[25]。
蔗糖可在植物体内被催化水解为果糖及葡萄糖,这些游离态的还原性糖参与美拉德反应生成多种化合物如呋喃类、吡嗪类和醛类等,相关分析发现蔗糖与2-甲基呋喃、2-甲基丙醛存在显著的相关性。除蔗糖外,共有13种检出化合物与2种以上的挥发性风味化合物高度相关,占总检出化合物的12.7 %,其中大部分为氨基酸。试验发现色氨酸和苯丙氨酸等均与2,6-二甲基吡嗪正相关,但相关性相对较弱,这可能是由于小分子的肽链在样品处理过程中发生了水解,导致检测到的游离氨基酸含量上升,而分子质量在500 Da以下的多肽是吡嗪化合物形成的主要来源[26]。苯丙氨酸还参与了丙氨酸、苏氨基酸和糖分子碎片的重组,促进了2-甲基呋喃的合成[24]。因此,未来可以尝试挖掘关键氨基酸,如苯丙氨酸和色氨酸相关的基因,调控其表达,影响其在块茎组织中的含量,进而间接达到调控相关挥发性风味组分的目的。另外,异丝氨酸与多数挥发性化合物呈负相关,与丙氨酸、色氨酸和苏氨酸等氨基酸呈显著负相关(图6-b)。陈佳华[27]发现甘薯块根在受到镰刀菌侵染后,氨基酸类代谢化合物含量会显著增加。而异丝氨酸本身具有一定的药理活性,构成的抗生素具有强烈的抗菌活性。因此,推测来源于土壤微生物中的含有异丝氨酸的生物活性物质[28,29],抑制了附着并侵染马铃薯块茎的相关病原菌,使块茎组织应答侵染胁迫而产生的游离氨基酸含量降低[30],进而影响了挥发性风味化合物的含量,其相关机制还需进一步深入研究。
4 结论
挥发性风味化合物含量变化受品种因素影响;甲硫基丙醛、2-甲基呋喃和2-甲基吡嗪等是品种间主要的差异挥发性化合物;蛋氨酸、丙氨酸、苏氨基酸和果糖等,是最有可能影响马铃薯特征风味构成的代谢化合物;使用相关性分析方法可以为寻找挥发性组分的潜在代谢途径提供参考。参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 3]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
