 ,1, 吴悠1, 肖妍1, 赵武奇1, 雷玉山2
,1, 吴悠1, 肖妍1, 赵武奇1, 雷玉山2Influence of Three Enzymes on Oxidation of Ascorbic Acid in Postharvest 'Hayward' and 'Huate' Kiwifruit
FENG Qi1, LI ChaoZheng1, GAO GuiTian ,1, WU You1, XIAO Yan1, ZHAO WuQi1, LEI YuShan2
,1, WU You1, XIAO Yan1, ZHAO WuQi1, LEI YuShan2通讯作者:
责任编辑: 赵伶俐
收稿日期:2019-07-9接受日期:2019-11-30网络出版日期:2020-02-16
| 基金资助: |
Received:2019-07-9Accepted:2019-11-30Online:2020-02-16
作者简介 About authors
封琦,E-mail:fengqi19970101@snnu.edu.cn。

摘要
关键词:
Abstract
Keywords:
PDF (450KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
封琦, 李朝政, 高贵田, 吴悠, 肖妍, 赵武奇, 雷玉山. 三种酶对采后‘海沃德’和‘华特’猕猴桃 AsA的氧化作用[J]. 中国农业科学, 2020, 53(4): 811-822 doi:10.3864/j.issn.0578-1752.2020.04.013
FENG Qi, LI ChaoZheng, GAO GuiTian, WU You, XIAO Yan, ZHAO WuQi, LEI YuShan.
0 引言
【研究意义】抗坏血酸(ascorbic acid,AsA),又称维生素C(Vc),是广泛存在于植物中的抗氧化剂主要清除细胞内的氧化物和超氧化物,或作为某些还原酶的辅因子参与还原反应[1]。AsA还参与植物的衰老调控[2]。另一方面,AsA是人体不可缺少但无法自身合成,必须从食物中获取的营养物质。猕猴桃(Actinidia)果实AsA含量高于大多数水果,享有“Vc之王”的美称。深入了解猕猴桃果实采后AsA的变化规律及影响因素,AsA在成熟与衰老中的作用及其机制,对调控果实成熟和衰老进程并有效保持果实采后品质和延长贮藏时间具有重要意义。【前人研究进展】植物中AsA的含量由合成途径和循环再生途径综合调节[3]。AsA主要合成途径为L-半乳糖途径[4],循环再生途径主要为抗坏血酸-谷胱甘肽循环(AsA-GSH)[5],是氧化态AsA再生的主要途径。在该途径中,AsA通过APX[6]或AO[7,8],将AsA氧化成单脱氢抗坏血酸(monodehydroascorbate,MDHA),同时AsA作为电子供体在APX清除H2O2的过程中被氧化成MDHA[6],部分MDHA发生非酶促歧化反应后得到DHA,生成的DHA借助AsA-GSH循环还原成最初的AsA[9],APX对AsA的积累有调节作用[10]。MA等[11]研究表明不同品种猕猴桃果实AsA含量存在较大差异。原玉林等[3]研究发现猕猴桃果实生长发育过程中AsA含量受合成和再生的共同调控,不同基因型猕猴桃果实中AsA和AsA相关氧化物水平存在明显的多样性,并且L-半乳糖1,4-内酯脱氢酶(GalLDH)、脱氢抗坏血酸还原酶(DHAR)和单脱氢抗坏血酸还原酶(MDHAR)的活性均与AsA含量存在极显著相关性,并且MDHAR活性与AsA含量和APX都有较高的相关性。目前,植物AsA合成与氧化的研究主要集中在AsA生物合成途径方面[12],对果蔬采后AsA分解氧化及其机理鲜有报道。薛敏等[13]研究发现‘海沃德’猕猴桃果实在贮藏期AsA氧化率高达61.5%,另有研究表明,‘华特’猕猴桃在采后AsA含量始终保持较高水平,在贮藏末期AsA的氧化率只有10%[14]。【本研究切入点】笔者课题组前期采用转录组测序技术,发现‘海沃德’猕猴桃采后AsA氧化通路中AO、漆酶基因家族中存在表达差异[15],并用实时荧光定量PCR进行了验证,为从基因水平研究猕猴桃采后AsA分解氧化奠定了基础。【拟解决的关键问题】本研究以AsA含量较低、采后流失严重的‘海沃德’猕猴桃和AsA含量高、采后流失少的‘华特’猕猴桃作为试验材料,通过研究两个品种的猕猴桃在采后25℃贮藏条件下AsA含量和相关酶活性及其基因表达的变化差异,以期探明影响猕猴桃AsA含量变化的相关机制,为今后通过基因层面维持和减少猕猴桃果实采后AsA的损失提供理论依据。1 材料与方法
1.1 试验材料
‘华特’猕猴桃、‘海沃德’猕猴桃,于2017年10月21号采于周至县虎峰村的陕西佰瑞猕猴桃研究院有限公司实验基地。挑选果型大小均匀、完整、无病虫害的果实于采后当天运回实验室。‘华特’猕猴桃、‘海沃德’猕猴桃分别按每30个一组放入已消毒的筐中,框外侧套厚度为0.05 mm的聚乙烯薄膜袋,让袋口处于自然合拢状态,置于(25±0.5)℃的恒温箱贮藏;每隔5 d分别选‘华特’猕猴桃30个和‘海沃德’猕猴桃30个,取果实果肉、中轴部分将其切碎混合后用液氮速冻,用锡箔纸把样品包好后存放在-80℃冰箱,用于酶活测定及基因表达研究。
1.2 主要仪器与试剂
仪器:pH计,北京科伟永兴仪器公司;超高速低温离心机,美国Sigma公司;紫外分光光度计,瑞典福斯公司;全波长酶标仪,美国热电公司;BIO-RAD梯度PCR仪,北京元业伯乐科技发展有限公司;DYY-4C型电泳仪,北京市六一仪器厂;格兰仕微波炉,格兰仕微波炉电器有限公司;XW-80A漩涡混合仪,海门市其林贝尔仪器制造有限公司;JY02G型凝胶成像仪,北京君意东方电泳设备有限公司;NanoDrop 2000微量快速核酸定量仪,赛默飞尔公司;RF-6000荧光定量PCR仪,美国热力公司。分析纯化学试剂:BP(纯度>97.0%),磷酸,无水乙醇,标准抗坏血酸,氯化铁(FeCl3),三氯乙酸(TCA)购于天津天力化学试剂有限公司;HiPure Plant RNA Mini Kit,美基生物工程有限公司;Light cycler RNA SYBR green I,Sigma生物工程有限公司;TRUEscript 1st Strand cDNA Synthesis Kit,北京艾德莱生物科技有限公司;DNA Marker-D、6×Loading Buffer、EDTA、Tris-HCl、琼脂糖,TaKaRa(大连)生物工程有限公司。
1.3 试验方法
1.3.1 T-AsA、AsA、DHA含量测定 参考赵玉梅等[16]的方法测定。标准曲线制备:在波长534 nm处测定吸光值,将AsA质量设置为横坐标,吸光度值设置为纵坐标,绘制标准曲线,并求线性回归方程。
样品提取:准确称4.0 g猕猴桃果实样品,放入已加5 mL 50 g∙L-1 TCA溶液的研钵中,冰浴条件下将样品研磨成匀浆后转移到25 mL的容量瓶,用TCA溶液冲洗研钵一并转移到容量瓶后定容至刻度,摇匀,冰浴条件下提取10 min后过滤,将滤液4℃、12 000×g离心10 min后收集上清液,即样品提取液。低温备用(‘华特’猕猴桃果实上清液需稀释10倍备用)。
T-AsA测定:取1.0 mL样品提取液,加0.5 mL浓度为60 mmol∙L-1的DTT-乙醇溶液,用Na2HPO4-NaOH溶液将pH调至7—8,室温下静置10 min,加0.5 mL的TCA溶液。按照制作标准曲线同样的方法进行测定。记录波长534 nm处的吸光值。重复3次。
AsA测定:取1.0 mL样品提取液,加1.0 mL的TCA溶液,按照制作标准曲线同样的方法进行测定。记录波长534 nm处的吸光值。重复3次。
DHA含量等于样品中T-AsA的含量减去原有的AsA的含量。
1.3.2 漆酶、AO、APX活性的测定 漆酶、AO、APX活性测定用Mlbio酶联免疫分析试剂盒(分别为Plant Laccase ELISA KIT、Plant AO ELISA KIT、Plant APX ELISA KIT)进行测定。
1.3.3 RNA的提取及质检 裂解液加入浓度为2%(w/v)的PVP-40,其余步骤按照植物RNA小提试剂盒说明书(HiPure Plant RNA Mini Kit)进行;通过2%的琼脂糖凝胶电泳和微量快速核酸定量仪检测RNA的纯度、浓度。
1.3.4 单链cDNA的合成 将检测合格的RNA使用第一链反转录试剂盒(TRUEscript 1st Strand cDNA Synthesis Kit)进行单链cDNA合成。
1.3.5 荧光定量PCR 用Gene ID在猕猴桃数据库(http://bioinfo.bti.cornell.edu/cgi-bin/kiwi/home.cgi)检索并获得相应基因的CDS区[17],通过Primer 6.0软件,在NCBI上使用Primer-BLAST程序将设计的引物进行模拟扩增,通过比对引物扩增的特异性,筛选出特异性最强的荧光定量PCR引物对,引物见表1。
Table 1
表1
表1实时荧光定量PCR分析使用的引物
Table 1
| 酶名称 Enzyme name | 基因名称 Gene name | 上游引物 Forward primer | 下游引物 Reverse primer |
|---|---|---|---|
| 抗坏血酸氧化酶 AO | Achn020161 | CGGGTCCTGAACTCTACTGC | GCAAGGTAGTCCTGTTTGGA |
| Achn230551 | CCTGTGTGGAACGATGTGGA | GCGAGGTAAAGGACAGCGTA | |
| Achn316521 | CCAAGTACTCACGGCCACAT | AGTGTCTGCTGGGATGAACG | |
| 漆酶Laccase | Achn007661 | CAGTTGTTGCTGTGGATGCT | TGAGAAGTGTCGGCTGGTTA |
| Achn191341 | GGTGAAATCTGGGGAGACAA | GACTACGACGGATGTGGTTC | |
| Achn163871 | CCCAACAAGTGGACAAACATT | CCACTTTGGTTGGAGTAAGC | |
| 抗坏血酸过氧化物酶 APX | Achn123021 | CAACTGAAGAGTGCCCGAGA | GAATCACCAGCAGCATTGGC |
| Achn082241 | TCCCGGTACTTTCAGAGGTG | ACCACAACGACCTCAAGTTC | |
| Achn187071 | GGTGGAATGAATGGCTCAAT | CACACGCCTCCAGGTTTATA |
新窗口打开|下载CSV
按照Light cycler RNA SYBR green I试剂盒操作,以18s RNA基因为内参基因进行qRT-PCR反应。反应程序为95℃预变性10 min,90℃变性20 s、61℃退火20 s,40个循环,熔解曲线温度范围为55—95℃。分析荧光值变化曲线及熔解曲线,用2-△△Ct法计算两个品种猕猴桃在不同的贮藏天数时AO、漆酶、APX相关基因的相对表达量。
1.3.6 数据处理 样品进行3次生物学重复取平均值,运用SPSS 17.0进行数据统计和差异性分析,取P<0.05为显著相关,P<0.01为极显著相关,采用Origin 8.6绘图。
2 结果
2.1 猕猴桃中T-AsA、AsA、DHA含量
‘海沃德’和‘华特’猕猴桃在采后贮藏期AsA含量存在显著差异(图1-A)。‘海沃德’猕猴桃果实采后第1天AsA含量只有‘华特’猕猴桃的14%,在第6—11天下降速度加快,在第11—21天下降速度又趋于平缓,在贮藏末期,AsA含量下降了约45%,损失严重。‘华特’猕猴桃采后贮藏期AsA含量远高于‘海沃德’猕猴桃,含量呈现先下降后上升的趋势;在第6—11天AsA含量急剧上升并达到峰值,从第11天到贮藏末期,AsA含量缓慢下降,仍高于采后第1天AsA含量,整体呈上升趋势。图1
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图1两个品种猕猴桃采后AsA(A)、DHA(B)、T-AsA(C)含量变化
“*”和“**”分别表示在两品种差异显著(P<0.05)和极显著(P<0.01)水平。下同
Fig. 1Changes of AsA (A), DHA (B), and T-AsA (C) contents of two varieties of kiwifruit during storage
“*” and “**” indicate significant differences (P<0.05) and extremely significant (P<0.01) between the two varieties. The same as below
‘海沃德’猕猴桃DHA含量在整个贮藏期都低于‘华特’猕猴桃,两个品种都呈现先下降后上升的变化趋势(图1-B)。‘海沃德’猕猴桃第1—16天DHA含量处于缓慢下降的趋势,在第16—21天含量略有回升,在第21天仍低于初期含量。‘华特’猕猴桃在采后第1—16天,DHA含量处于较快下降的趋势且达到最低点,16 d之后含量开始回升,但仍远低于初期含量。
‘海沃德’和‘华特’猕猴桃的T-AsA含量与其AsA含量的变化趋势接近(图1-C)。T-AsA是AsA与DHA之和,由于两个品种的猕猴桃果实中AsA含量远远大于DHA含量,因此,AsA含量的变化直接影响T-AsA的变化趋势。
2.2 猕猴桃AsA/DHA比值的变化
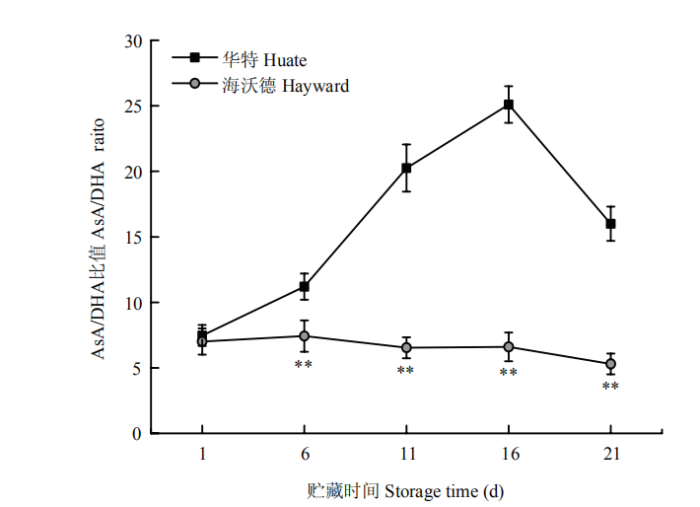
AsA/DHA的比值反应果实中AsA的氧化还原状态和程度。如图2,‘海沃德’和‘华特’猕猴桃在采后初期AsA/DHA比值接近,‘海沃德’AsA/DHA比值整体缓慢波动呈下降趋势,而‘华特’呈先上升后下降趋势。在贮藏第1—6天,两个品种的AsA/DHA比值都略微上升,‘华特’上升较快。‘海沃德’在第6—11天,AsA/DHA比值呈下降趋势。‘华特’在第6—16天,比值急剧上升且达到顶峰。在整个贮藏后期,‘海沃德’猕猴桃的AsA/DHA比值远低于‘华特’。图2
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2两个品种猕猴桃采后AsA/DHA比值变化
Fig. 2Changes of AsA/DHA ratio of two varieties of kiwifruit during storage
2.3 猕猴桃AO、漆酶、APX活性的变化
‘海沃德’猕猴桃在贮藏期AO活性呈先上升后下降的趋势,且在采后初期低于‘华特’,第1—16天缓慢上升,在第16天达到最高值后呈下降趋势。‘华特’猕猴桃在贮藏期AO活性呈现先下降后上升的趋势,第11天到达最低值,之后活性上升,但仍低于‘海沃德’(图3-A)。图3
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图3两个品种猕猴桃采后AO(A)、漆酶(B)、APX(C)活性变化
Fig. 3Changes of AO (A), laccase (B) and APX (C) activities of two varieties of kiwifruit during storage
在整个采后贮藏期,‘海沃德’猕猴桃的漆酶活性始终高于‘华特’,但两者变化趋势相似,均表现为先下降后上升再下降的趋势。‘海沃德’猕猴桃漆酶活性在第16天达到峰值后开始下降,在贮藏末期活性仍高于‘华特’;‘华特’猕猴桃在贮藏第1—11天时漆酶活性呈快速下降趋势,在第11天达到最低值,贮藏末期的活性只有‘海沃德’的一半(图3-B)。
‘华特’猕猴桃在贮藏期APX活性始终高于‘海沃德’,且在第1天远高于‘海沃德’,在采后第1—6天,‘华特’APX活性迅速下降,在贮藏后期,呈现波动变化趋势,但始终维持在20 U∙g-1 FW以上。‘海沃德’猕猴桃APX活性在贮藏过程中呈先上升后下降的趋势,在第11天达到峰值,随后开始下降,贮藏后期活性始终维持在14.5 U∙g-1 FW左右(图3-C)。
2.4 猕猴桃AsA含量与T-AsA、AsA/DHA及3个酶的相关性分析
如表2,‘海沃德’猕猴桃中AsA含量与T-AsA含量呈极显著正相关(P<0.01),且相关系数为0.999,与AO活性呈显著负相关性且相关系数为0.910;‘华特’猕猴桃AsA含量与T-AsA含量呈极显著正相关(P<0.01),且相关系数为0.993,与AO活性呈显著负相关(P<0.05),且相关系数为0.958。Table 2
表2
表2两个品种猕猴桃AsA含量与相关指标的相关系数
Table 2
| 总抗坏血酸 T-AsA | 抗坏血酸/脱氢抗坏血酸 AsA/DHA | 抗坏血酸氧化酶 AO | 漆酶 Laccase | 抗坏血酸过氧化物酶 APX | |
|---|---|---|---|---|---|
| 海沃德 Hayward | 0.999** | 0.839 | -0.910* | -0.875 | 0.253 |
| 华特 Huate | 0.993** | 0.834 | -0.958* | -0.803 | -0.500 |
新窗口打开|下载CSV
2.5 两个品种猕猴桃AsA氧化相关酶基因相对表达量的变化
Achn020161、Achn230551和Achn316521是猕猴桃AO基因家族中的3个基因。两个品种的猕猴桃采后贮藏期内,Achn020161的表达变化趋势如图4-A所示,在‘海沃德’中的表达量在第16天达到峰值;‘华特’猕猴桃的表达量没有明显变化,且整个贮藏期表达量都明显低于‘海沃德’。从图4-B可以看出,‘海沃德’猕猴桃Achn230551处于表达量较低的状态,且始终低于‘华特’;在‘华特’中,其表达量在第16天达到峰值,第21天时与最初表达量持平。由图4-C可知,‘海沃德’猕猴桃Achn316521表达量在第6天达到最高表达量后急剧下降,第11天后开始上升;‘华特’猕猴桃其基因表达量呈波动变化,贮藏末期与最初表达量没有明显差异。图4
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图4两个品种猕猴桃AsA氧化相关酶基因相对表达量的变化
Fig. 4Changes of expression levels of related enzyme genes of two varieties of kiwifruit during storage
Achn007661、Achn191341、Achn163871是猕猴桃漆酶基因家族中的3个基因。由图4-D可见,在猕猴桃整个采后贮藏期内,‘海沃德’Achn007661表达量在第16天最高,‘华特’的表达量一直明显低于‘海沃德’。Achn191341在‘海沃德’猕猴桃中表达量总体呈上升的趋势,第16天表达量达到峰值且是第1天的5倍;‘华特’猕猴桃表达量变化趋势不明显,且第6天后明显低于‘海沃德’(图4-E)。‘海沃德’猕猴桃Achn163871表达量在第11天达到最高;‘华特’猕猴桃其表达量呈持续上升趋势,且贮藏末期高于‘海沃德’(图4-F)。
Achn123021、Achn082241、Achn187071是猕猴桃APX基因家族中的3个基因。‘海沃德’猕猴桃Achn123021表达量在第16天达到峰值;‘华特’猕猴桃其表达量在第1—6天急剧上升,到贮藏末期相比于第1天上升了约4倍(图4-G)。‘海沃德’中Achn082241表达量始终高于‘华特’,第11天表达量达到峰值;在‘华特’中的表达量变化整体差异不明显(图4-H)。‘海沃德’猕猴桃中Achn187071表达量在第11天表达量开始急剧上升;‘华特’猕猴桃的表达量在前期稍有下降,但整体变化趋势不明显(图4-I)。
2.6 猕猴桃AsA含量与AsA氧化相关酶基因相对表达量的相关性
如表3所示,AO基因家族中,Achn020161表达量与‘海沃德’‘华特’猕猴桃果实中AsA含量的变化具有显著负相关性,相关系数分别为0.922、0.920;Achn191341表达量与‘海沃德’猕猴桃中的AsA含量变化正相关,与‘华特’没有显著相关性;Achn316521表达量与‘海沃德’‘华特’猕猴桃的AsA含量无显著相关性。Table 3
表3
表3两个品种猕猴桃AsA含量与相关基因表达量的相关系数
Table 3
| 海沃德 Hayward | 华特 Huate | |
|---|---|---|
| Achn020161 | -0.922* | -0.920* |
| Achn191341 | 0.769 | 0.494 |
| Achn316521 | 0.02 | 0.494 |
| Achn007661 | -0.947* | -0.950* |
| Achn191341 | -0.852 | -0.423 |
| Achn163871 | -0.325 | 0.599 |
| Achn123021 | -0.84 | 0.536 |
| Achn082241 | -0.390 | 0.246 |
| Achn187071 | -0.803 | -0.517 |
新窗口打开|下载CSV
漆酶基因家族中,Achn007661表达量与‘海沃德’‘华特’猕猴桃贮藏期AsA含量的变化呈显著负相关,相关系数分别为0.947、0.950;Achn191341表达量与‘海沃德’猕猴桃中的AsA含量的变化呈负相关,与‘华特’没有显著相关性;Achn163871表达量与‘海沃德’‘华特’猕猴桃中AsA含量的变化没有显著相关性。
APX基因家族中,Achn123021表达量与‘海沃德’猕猴桃中AsA的含量变化呈负相关性,与‘华特’没有显著相关性;Achn082241表达量与‘海沃德’‘华特’猕猴桃中的AsA含量变化无显著相关性;Achn187071表达量与‘海沃德’猕猴桃中AsA含量呈负相关,与‘华特’无显著相关性。
3 讨论
3.1 AsA/DHA对猕猴桃采后AsA氧化的影响
猕猴桃以富含高AsA而著名,但在贮藏后期,不同品种的猕猴桃果实AsA的损失情况有显著差异。‘华特’猕猴桃具有较高的AsA含量且在采后贮藏期流失较少[14]。而‘海沃德’猕猴桃与‘华特’相比,AsA在采后贮藏期损失很大[18]。DHA是AsA中的一种氧化产物,AsA很容易在酶的作用下氧化,同时在脱氢抗坏血酸还原酶的作用下,DHA还可以转化为AsA以维持较高水平。本试验发现,‘华特’猕猴桃AsA含量是‘海沃德’的8—10倍,与原玉林等[3]的研究结果一致;造成AsA含量差异的主要因素为AsA合成和循环再生机制,‘华特’贮藏前期出现AsA含量的上升现象,说明果实中的AsA合成和再生的协作速率大于氧化速率。有研究表明,‘华特’贮藏前期DHAR活性上升,后期受到反馈抑制活性下降[19],因此,DHAR以DHA为底物会促进果实贮藏前期AsA含量的积累;‘海沃德’猕猴桃刚好与其相反,说明‘海沃德’AsA氧化速度大于再生合成的速度。‘华特’猕猴桃DHA含量远远高于‘海沃德’,两者变化趋势一致,DHA除自身氧化外还参与AsA再生循环。由于猕猴桃中AsA含量远高于DHA含量,所以,‘华特’和‘海沃德’的T-AsA含量变化趋势与AsA基本保持一致,受DHA变化影响很小。AsA/DHA的比值反映的是果实中AsA的氧化还原状态[18],比值越大,说明抗氧化能力越高[20],越有利于维持果实中T-AsA的含量。AsA/DHA的高比值可以阻止AsA的降解,‘华特’在贮藏期内AsA含量整体上升而DHA下降,保持着较高的AsA再生能力,AsA再生酶可能对其后期可以保持较高的抗氧化能力也起到一定作用[21]。‘华特’猕猴桃和‘海沃德’猕猴桃在贮藏过程中AsA/DHA的比值存在显著差异,较高含量的DHA还原以及AsA/DHA的高比值对AsA的积累起到重要作用。3.2 3种酶对猕猴桃采后AsA氧化的影响
通过AsA-GSH循环,植物有清除活性氧(ROS)的能力,同时,AsA会被氧化为单脱氢抗坏血酸(MDAH),这种能力在酶的催化下会增强。前人研究表明,在AsA-GSH循环中,AO在有氧情况下,APX提供电子供体是AsA分解氧化的主要途径,植物APX表达受生物和非生物胁迫以及植物发育期间的调节[22,23,24]。漆酶是一种含铜多酚氧化酶[25],作为催化剂可清除ROS,也可与抗坏血酸、胺类等物质反应[26,27]。本研究发现,AO活性与两个品种猕猴桃AsA含量呈显著负相关性;漆酶活性与两个品种猕猴桃AsA含量呈负相关性,与笔者课题组前期基于转录组测序分析发现漆酶可能是‘海沃德’采后氧化AsA酶的结论一致[15]。猕猴桃AO和漆酶活性在‘华特’采后第11天达到最低值,在‘海沃德’采后第16天达到最高值,而在采后第11天‘华特’猕猴桃的AsA含量上升到峰值,DHA的含量接近最低值,推测这是导致‘华特’猕猴桃AsA含量在贮藏后期始终维持较高含量而‘海沃德’AsA含量呈下降趋势的主要原因。进一步比较AO与漆酶的活力,发现AO是漆酶活力的3—4倍,据此推测,AO是导致两个品种猕猴桃采后氧化的关键酶,漆酶对猕猴桃采后AsA的氧化有一定的作用。而APX的活力变化趋势在两个品种之间差异较大,在采收当天,‘华特’猕猴桃是‘海沃德’的2倍多,在采后第7—21天,‘华特’始终高于‘海沃德’;在采后第1—6天,‘华特’APX活力剧增,与其采后1—6天的AsA升高及DHA降低的变化吻合,但采后第7—21天,APX活力变化与AsA及DHA变化吻合度较低。而‘海沃德’APX活力与其采后AsA含量的相关系数仅为0.253,因此,APX不是两个品种氧化AsA的主要酶,这与钟雨[28]在‘华特’猕猴桃中的研究结果一致。植物中AsA-GSH循环途径需要多个同工酶共同参与[29],这3种酶对于ROS的清除应该都有一定的作用,但具体如何参与ASA的氧化并不清楚,还需要进一步探究验证。3.3 相关基因对猕猴桃采后AsA氧化的影响
AO基因家族中,Achn020161在两个品种猕猴桃中的表达变化趋势与其对应的酶活性变化趋势相近,与其AsA含量呈显著负相关,推测该基因是导致两个品种猕猴桃AsA氧化的关键基因之一。Achn230551、Achn316521表达量与AsA含量无显著相关性,推断这两个基因可能并不参与调控AO氧化AsA的过程。漆酶基因家族的Achn007661与Achn191341在‘海沃德’猕猴桃中表达量显著高于‘华特’;‘华特’猕猴桃Achn007661与Achn191341在采后平稳下降,与其对应品种的漆酶活性变化趋势基本一致,相关分析表明Achn007661与Achn19134与两个品种AsA变化分别为极显著相关与负相关,推测Achn007661与Achn19134对氧化AsA有一定影响。Achn163871表达量在‘海沃德’猕猴桃中为先上升后下降的趋势,第11天表达量达到最高,与漆酶活力变化趋势一致;但在‘华特’猕猴桃中的表达量持续上升,且贮藏末期高于‘海沃 德’,与漆酶活力变化趋势相反,表明Achn163871与两个品种猕猴桃氧化AsA无相关性,也暗示Achn163871可能存在转录后调控,其机理有待进一步研究。
APX基因家族的Achn123021在‘海沃德’猕猴桃中表达量与APX活力的变化趋势一致,与AsA含量呈负相关性;但在‘华特’中采后第1—6天APX活力下降一半,其表达量反而上升,采后第11天,Achn123021表达量是采收当天的4.5倍,与AsA含量上升的表型相反。在两个品种中,Achn082241、Achn187071表达量变化与APX活力变化趋势相近,但两个基因的表达量在‘海沃德’中显著高于‘华特’,与‘华特’APX活性整体高于‘海沃德’的结果相反。其原因可能是由于本研究中APX基因家族Achn082241、Achn187071的CDS序列来自中华猕猴桃‘红阳’基因组数据库[17],而本研究所用的材料是美味猕猴桃‘海沃德’与毛花猕猴桃‘华特’,与中华猕猴桃‘红阳’存在较大的遗传差异[30,31],APX基因编码区的序列也可能存在一定的多态性。另一方面,较多的研究表明APX
在植物生长发育和逆境胁迫响应等生理过程中都发挥着非常重要的作用,它催化H2O2依赖的L-抗坏血酸发生氧化作用,对AsA表现出高度的专一性[23,32-33]。本研究不论从酶学层面,还是基因层面均表明APX与两个品种采后AsA氧化相关性低,其原因有待进一步研究。
4 结论
较高含量的脱氢抗坏血酸还原以及AsA/DHA的高比值对抗坏血酸(AsA)的积累起重要作用。抗坏血酸氧化酶(AO)是氧化AsA的关键酶,漆酶对氧化AsA有一定作用,抗坏血酸过氧化物酶(APX)不是主要氧化AsA的酶。推测AO基因家族中的基因Achn020161是导致AO氧化AsA的关键基因,而Achn191341和Achn316521则与AsA氧化相关性不明显;漆酶基因家族中的基因Achn007661对AsA氧化有一定作用,Achn191341、Achn163871与AsA的氧化没有显著相关性;APX基因家族中的3个基因Achn123021、Achn082241、Achn187071不是氧化AsA的关键基因。参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 3]
[本文引用: 3]
[本文引用: 1]
URL [本文引用: 1]
URL [本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
URL [本文引用: 1]
URL [本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[D].
[本文引用: 2]
[D].
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 2]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[D].
[本文引用: 1]
[D].
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
