 ,2,*
,2,*Molecular identification and chromosomal mapping of exogenous Bt gene in two insect-resistant cotton varieties
ZHOU Xiang-Yang1, ZHAO Liang2, DI Jia-Chun2, CHEN Xu-Sheng ,2,*
,2,*通讯作者:
收稿日期:2018-12-12接受日期:2019-04-15网络出版日期:2019-05-14
| 基金资助: |
Received:2018-12-12Accepted:2019-04-15Online:2019-05-14
| Fund supported: |
作者简介 About authors
E-mail:xiangyzhou@126.com。

摘要
关键词:
Abstract
Keywords:
PDF (1651KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
周向阳, 赵亮, 狄佳春, 陈旭升. 2个抗虫棉的外源Bt基因分子鉴定及其染色体定位[J]. 作物学报, 2019, 45(9): 1440-1445. doi:10.3724/SP.J.1006.2019.84167
ZHOU Xiang-Yang, ZHAO Liang, DI Jia-Chun, CHEN Xu-Sheng.
国外转Bt基因抗虫棉的研究较早。1981年, Schnepfh等[1]首次从菌株HD-1中克隆出苏云金芽孢杆菌的杀虫晶体蛋白基因, 并证明其抗虫能力。1987年美国Agrocetus公司对Bt基因有关的DNA序列片段进行了必要的修饰, 然后利用农杆菌转化法将其导入并整合到棉株的基因组中, 使棉株成功地表达出抗虫性状, 但其抗虫能力不高, 主要因为Bt基因来源于原核生物, 序列富含A、T碱基, 在棉花植株中不易表达[2]。1989年, Monsanto公司对单价Bt基因进行改造, 即在不改变杀虫晶体蛋白氨基酸序列的情况下, 采用人工合成和点突变的方法, 对Bt基因的特定位点进行改造, 把序列中的A、T碱基换成G、C碱基, 选取了适于棉花的启动子, 并在Bt基因所在位置的上游增加了增强子, 然后把改造的Bt基因导入棉株。结果发现, 与Bt基因未改造之前相比, 杀虫晶体蛋白在棉花植株中的表达量由原来的0.001%提高到0.05%~0.10%, 抗虫能力达70%以上[3]。1995年, 美国农业部(USDA)首次通过了转Bt基因棉的种植申请, 并开始在美国国内大面积推广生产转Bt基因棉。1996年, Monsanto公司与岱字棉公司首次合作, 开展转Bt 基因抗虫棉的选育和商业化工作, 保铃棉33B是其代表性品种[4,5]。
我国对转基因抗虫棉的研究较晚, 但进展迅速。1991年, 谢道昕等[6]首次报道将Bt基因利用花粉管通道法导入本土棉花品种之中, 获得具有外源Bt基因的转基因棉花植株, 但抗虫性能较差。1992年, 郭三堆等[7]首先设计并人工合成了具有高效杀虫活性的GFM Cry1A杀虫晶体蛋白结构基因, 并于1994年导入棉花植株, 经过鉴定确认外源Bt基因已整合到棉花基因组中。在此基础上与育种单位合作, 成功选育出GK1、GK12、GK19、GKZ1和晋棉26等中国转基因抗虫棉品种, 使中国成为继美国之后的第二个能自主研发利用转Bt基因抗虫棉的国家[8]。
本研究以中国和美国的2个主要抗虫棉品种GK19与33B为试验材料, 通过PCR检测技术对中美Bt基因进行分子鉴定, 进一步通过SSR分子标记技术对Bt基因进行染色体定位, 旨在从外源基因转化事件的视角探究中美转基因抗虫棉差异的分子基础。
1 材料与方法
1.1 试验材料
选取中国抗虫棉GK19、美国抗虫棉33B, 以及非转基因海岛棉“胜利1号”、陆地棉“泗棉3号”为试验材料。在江苏省农科院南京试验田种植杂交F1代(GK19×胜利1号、33B×胜利1号), 开花期做自交、吐絮期收自交铃, 而后室内轧花获得的种子即为F2代分离群体。将以上2个海陆杂交F2代分离群体作为Bt基因的定位群体, 其中[GK19×胜利1号] F2代群体的个体数为184粒种子, [33B×胜利1号] F2代群体的个体数为185粒种子。1.2 试验方法
1.2.1 种子DNA的提取 取亲本以及杂交F1、F2的种子, 每粒种子即为1个个体。剥种壳得种仁, 采用匡猛等[9]的方法提取单粒种子DNA。1.2.2 Bt基因来源的分子检测 中美Bt基因PCR扩增检测的特异性引物序列来自王奕海等[10]的报道, 中国Bt基因的扩增片段大小为456 bp, 美国Bt基因的扩增片段大小为310 bp。特征引物序列为: F-1: 5°-CATCTTCACTC GGTAACATCG-3° (456 bp); F-2: 5°-AGGGAACCTTCATC GTGG-3° (310 bp); R: 5°-ATACGTGCCAAGTGCCAACC-3°。
利用检测Bt基因的特异性引物分别对抗虫棉GK19、33B、清水、非抗虫棉对照“泗棉3号”进行PCR扩增。PCR扩增产物在恒压90V条件下, 经1%琼脂糖凝胶电泳, 在凝胶成像系统中观察目的基因片段。
1.2.3 多态性标记筛选 SSR引物系列来自Cotton Marker Database (网址http://www.cottonmarker.org/)。从F2代分离群体, 选取含Bt基因的个体10个, 不含Bt基因的个体10个, “有”、“无”个体特征条带清晰明显。然后用scandrop250超微量核酸蛋白测定仪测定选取个体的DNA浓度, 统一稀释成40 ng μL-1后, 吸取等体积的DNA溶液, 构建近等基因混池。
利用本实验室自主筛选获得的234对核心引物(它们相对均匀地分布于棉花26对染色体上, 每对染色体上平均分布9对核心引物)[11], 对双亲以及近等基因混池进行PCR扩增, 筛选多态性SSR引物。
1.2.4 Bt基因的染色体定位 用筛选获得的多态性引物对F2群体的各个体DNA进行PCR扩增; 而后经非变性PAGE凝胶电泳, 通过银染检测[12], 得F2代各个体的标记基因型。在灯箱上观察多态性条带, 统计F2代各个体的标记基因型, 将与母本带型相同的个体基因型记为“1”; 与父本带型相同的个体基因型记为“2”; 共显性杂合带型记为“3”; 缺失或无法辨别的带型记为“0”。进行卡方适应性检测, 并验证标记分离比例是否符合3∶1的孟德尔遗传规律。再利用JoinMap 4.0软件进行分子标记的连锁分析, 以锁定目的引物与染色体; 然后合成目的染色体上的SSR引物进行图谱加密, 实现Bt基因的染色体定位。
2 结果与分析
2.1 转Bt抗虫基因的PCR检测结果
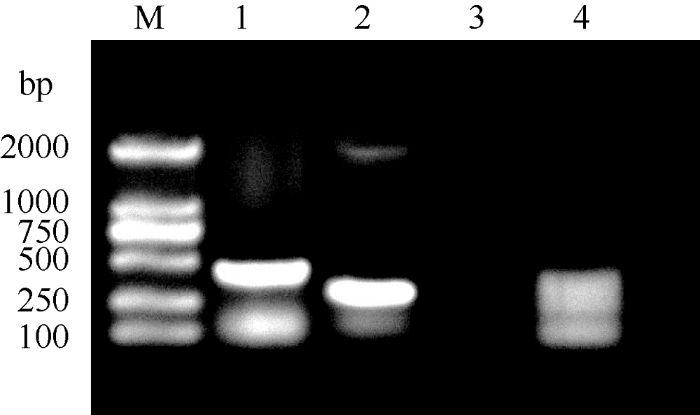
利用检测中美Bt基因的特异性引物, 分别对抗虫棉亲本GK19和33B进行PCR扩增, 并以清水、非抗虫棉品种“泗棉3号”作为对照。通过PCR扩增, 依据扩增条带大小进行分子鉴定。由图1可以看出, 抗虫棉品种GK19的PCR扩增条带, 符合中国Bt抗虫基因设计引物的特征片段长度456 bp (泳道1), 显示GK19为中国转Bt基因抗虫棉。而抗虫棉33B的PCR扩增条带, 则拟合美国Bt抗虫基因设计引物的特征片段长度310 bp (泳道2), 显示33B为美国转Bt基因抗虫棉。清水(泳道3)与对照品种“泗棉3号”(泳道4)则无特征扩增条带。图1
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图1Bt基因类型鉴定
M: DNA marker; 1: GK19; 2: 33B; 3: 清水; 4: 泗棉3号。
Fig. 1Identification of exogenous Bt genes
M: DNA marker; 1: GK19; 2: 33B; 3: Water; 4: Simian 3.
2.2 Bt基因在海陆杂交F2代群体的分离规律
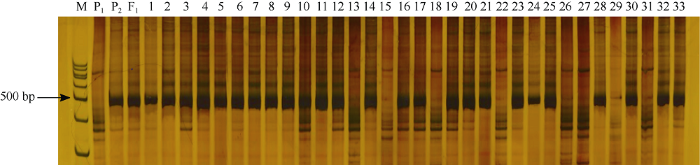
父本GK19全部个体均含有中国Bt基因, 母本“胜利1号”全部个体均不含Bt基因。F1代全部个体均有中国Bt基因, F2代分离群体中含Bt基因和不含Bt基因的个体数目拟合3∶1的分离比例(图2和表1)。结果表明, 该Bt基因为单位点插入, 符合由一对显性基因控制的孟德尔分离规律。图2
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2中国产Bt基因的PCR扩增
M: DNA marker; P1: 胜利1号; P2: GK19; F1为杂交一代, 1至33为F2代分离群体的部分单株。
Fig. 2PCR amplification of Bt gene from China
M: DNA marker; P1: V-1; P2: GK19; F1 for hybrid generation, 1 to 33 for partial plants in F2 segregation population.
Table 1
表1
表1GK19和胜利1号杂交后代Bt基因的分离情况
Table 1
| 世代 Generation | 亲本及组合 Parent and combination | 含Bt基因个体数 Number of individuals with Bt genes | 不含Bt基因个体数 Number of individuals without Bt gene | χ2值 χ2 value |
|---|---|---|---|---|
| P1 | V-1 | 0 | 83 | — |
| P2 | GK19 | 91 | 0 | — |
| F1 | P2×P1 | 80 | 0 | — |
| F2 | F1代自交 Self-crossing F1 | 133 | 51 | 0.72 |
新窗口打开|下载CSV
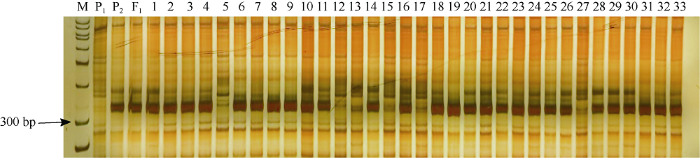
父本33B及其F1代全部个体均含有美国Bt基因, 母本“胜利1号”全部个体均不含美国Bt基因。F2代分离群体中“有”与“没有”Bt基因的个体数目拟合3∶1的分离比例(图3和表2)。表明该Bt基因也是单位点插入, 符合由1对显性基因控制的孟德尔分离规律。
图3
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图3美国Bt基因的PCR扩增
M: DNA marker; P1: 胜利1号; P2: 33B; F1为杂交一代, 1至33为F2代分离群体的部分单株。
Fig. 3PCR amplification of Bt gene from USA
M: DNA marker; P1: V-1; P2 : 33B; F1 for hybrid generation, 1 to 33 for partial plants in F2 segregation population.
Table 2
表2
表233B×胜利1号杂交后代Bt基因的分离情况
Table 2
| 世代 Generation | 亲本及组合 Parent and combination | 含Bt基因单株数 Number of individuals with Bt gene | 不含Bt基因单株数 Number of individuals without Bt gene | χ2值 χ2 value |
|---|---|---|---|---|
| P1 | V-1 | 0 | 84 | — |
| P2 | 33B | 90 | 0 | — |
| F1 | P2×P1 | 76 | 0 | — |
| F2 | F1代自交 Self-crossing F1 | 148 | 37 | 2.47 |
新窗口打开|下载CSV
2.3 中美抗虫棉Bt基因染色体定位
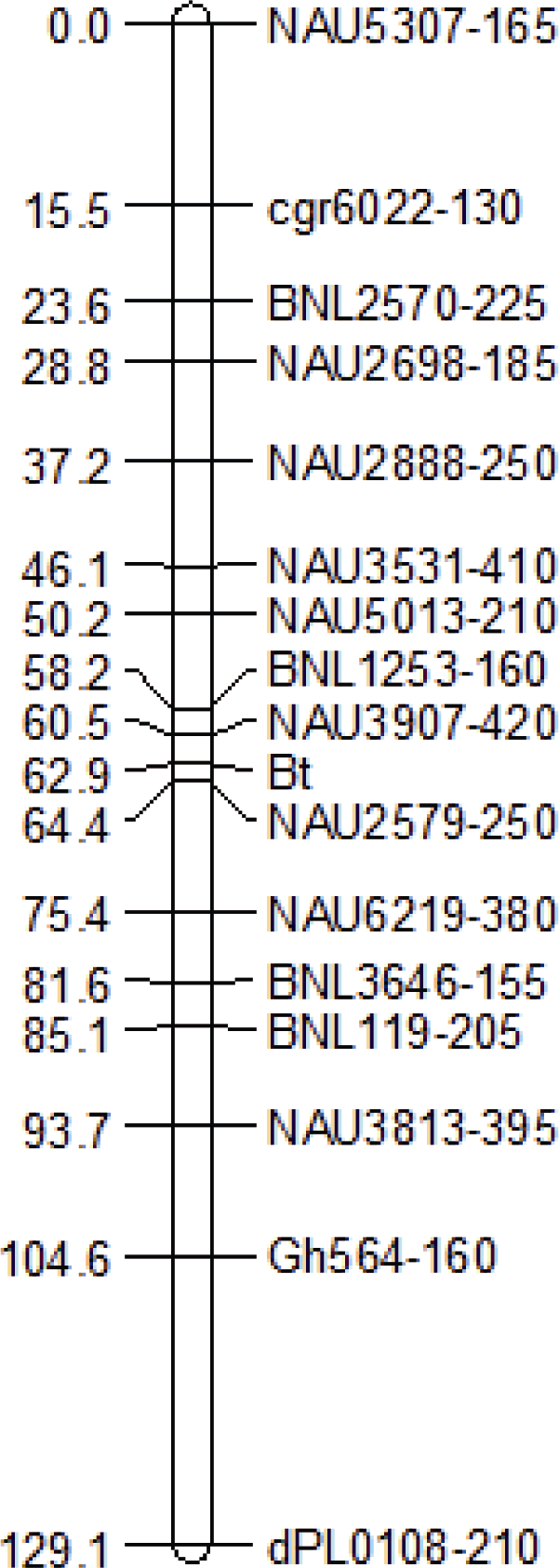
2.3.1 GK19中Bt基因的连锁遗传图谱 对海陆杂交组合“GK19×胜利1号”的亲本及F2近等基因池进行差异性筛选, 共得到22对多态性引物。以这22对多态性引物检测F2代作图群体每个单株的标记基因型。通过连锁软件分析, 发现SSR标记 NAU2579与Bt抗虫基因连锁, 且为共显性标记, 两者的初始遗传距离为3.3 cM。由于标记NAU2579位于第20染色体, 据此初步推断该Bt基因位于第20染色体。查阅棉花最新遗传图谱, 合成位于该SSR标记上下遗传距离50 cM区间的83对引物, 通过对双亲筛选得到20对多态性引物。用这些引物检测F2代群体每个单株的标记基因型, 然后通过JoinMap 4.0软件进行遗传连锁分析。结果表明, 共有NAU2579、NAU2698、NAU2888、NAU3531、NAU3813、NAU3907、NAU5013、NAU5307、NAU6219、BNL119、BNL1253、BNL2570、BNL3646、dPL0108、Gh564、cgr6022这16对标记与Bt基因连锁。位于Bt基因两侧的分子标记分别为NAU3907和NAU2579, 遗传距离分别为2.4 cM和1.5 cM。由此将抗虫棉品种GK19所含的中国Bt基因定位在棉花第20染色体上(图4)。图4
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图4抗虫棉GK19的外源Bt基因连锁遗传图谱
Fig. 4Exogenous Bt gene linkage map of insect-resistant cotton GK19
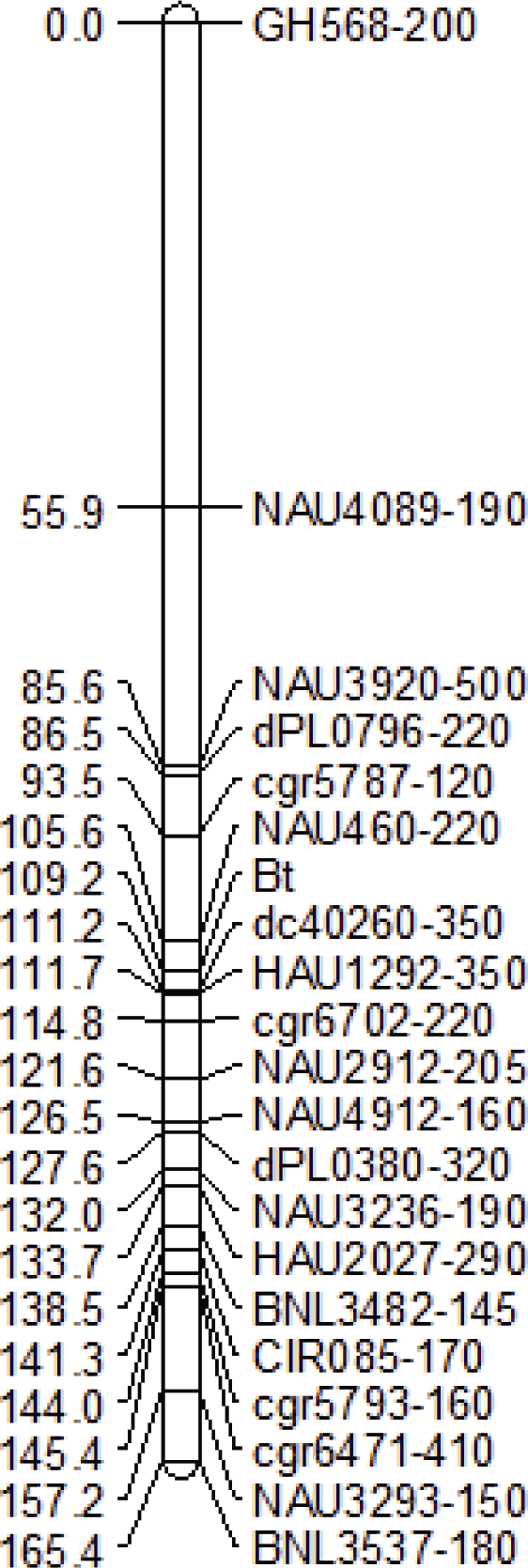
2.3.2 33B中的Bt基因的连锁遗传图谱 对海陆杂交组合“33B×胜利1号”的亲本及其F2近等基因池进行筛选, 共得到37对多态性引物。以这37对多态性引物检测F2代作图群体每个单株的标记基因型, 通过连锁软件分析发现, 多态性标记NAU2912和Bt抗虫基因连锁, 且为共显性标记, 两者的初始遗传距离约为29.5 cM。由于标记NAU2912位于第26染色体, 由此初步推断该Bt基因位于第26染色体。查阅最新棉花遗传图谱, 合成位于该标记上下遗传距离50 cM区间的111对引物, 通过对双亲及F1代和近等基因池筛选得到23对多态性引物。用这些引物检测F2代群体每个单株的标记基因型, 然后通过JoinMap 4.0软件进行遗传连锁分析。结果表明, 共有20对标记与Bt基因连锁, 它们分别是标记NAU460、NAU2912、NAU3236、NAU3293、NAU3920、NAU4089、NAU4912、HAU1292、HAU2027、BNL3482、BNL3537、cgr5787、cgr5793、cgr6471、cgr6702、CIR085、dPL0380、dPL0796、dc40260、Gh568。位于Bt基因两侧的分子标记分别为NAU460和dc40260, 遗传距离分别为3.6 cM和2.0 cM (图5)。由此, 将抗虫棉种质系33B所含的美国Bt基因定位在棉花第26染色体上。
图5
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图5抗虫亲本33B的外源Bt基因连锁遗传图谱
Fig. 5Exogenous Bt gene linkage map of insect-resistant cotton 33B
3 讨论
3.1 外源基因导入与遗传转化事件
外源基因导入棉花会产生不同的遗传转化事件。燕树锋等[13]分析转基因抗草甘膦棉花的遗传情况, 检测26个抗草甘膦棉花转化事件, 只有20个转化事件分离符合3∶1的分离规律, 其他6个转化事件出现了偏分离, 显示转基因植株中外源基因的整合和遗传机制相当复杂, 并非完全遵从经典的孟德尔遗传规律。不同转化方法导入外源基因, 其获得遗传转化事件的拷贝数也不尽相同[14]。转基因作物的育种研发涉及多个环节, 最关键的技术环节是如何把外源基因成功导入受体材料, 最终筛选出结构完整、表达良好的转基因品系, 从而形成具有商业推广价值的“转化事件”(Transgenic event)[15]。目前的生物技术仍无法实现外源基因的定点整合, 外源基因在受体基因组中的插入位点具有一定的随机性, 插入受体的染色体位置不同, 其侧翼序列也将表现不同; 因此将产生不同的转化事件。本研究显示, 外源Bt抗虫基因导入陆地棉, 既可以获得插入棉花第20染色体转化事件, 育成商业化品种GK19; 也可以获得插入棉花第26染色体的转化事件, 育成商业化品种33B。
3.2 不同基因定位方法的特色
棉花经典遗传学的定位方法是使用显性遗传多基因系T586和隐性遗传多基因系T582, 通过配置杂交组合, 对杂交后代目标性状的连锁关系进行分析, 以实现突变基因(或外源基因)的染色体定位。由于以上2个遗传系连锁的形态标记基因数太少, 未能覆盖陆地棉所有染色体, 因此连锁定位成功的几率极低。利用目标基因组步行PCR[16]、TAIL-PCR[17]、hiTAIL- PCR[18]等结合全基因组序列对外源目的基因进行测序定位, 从理论上说是比较容易获得特定外源基因插入染色体的精确位置, 从而实现对外源基因的染色体定位[19]。但实际上, 外源基因导入棉花受体后, 其旁侧翼序列会产生一些不可预知的DNA序列结构变化[20]; 尤其是陆地棉基因组大而复杂, 不同陆地棉材料的基因序列也不尽相同。因此, 尽管在陆地棉中获得许多转基因事件, 但利用测序方法获得棉花外源基因准确定位的公开报道并不多见。比如西南大学2012年对外公开发放了中国转iaaM基因棉花, 棉花全基因组测序结果也相继公布[21,22]; 但迄今未见iaaM基因被测序定位的公开报道。这显示利用TAIL-PCR等方法结合棉花全基因组序列对外源目的基因进行测序定位, 在实际应用中仍有很大的复杂性。
董志强等[23]对转Bt基因抗虫棉GK-12的Bt毒蛋白进行亚细胞结构的定位试验显示, 转Bt基因抗虫棉的外源晶体毒蛋白取向性定位在细胞器叶绿体以及前体中。至于Bt基因的染色体定位, 肖松华等[24]使用经典遗传学的方法, 试图对中国抗虫棉GK-12与美国抗虫棉33B的Bt基因进行基因定位, 但均未成功。近年来, 本实验室依据Guo等[25]、Zhao等[26]公布的四倍体棉花分子标记遗传图谱, 并利用自主筛选的相对均匀分布于棉花26对染色体上的234对SSR核心引物, 已成功对多个外源基因进行染色体定位[27,28,29]。这一定位方法是通过目的基因与特定染色体的多个SSR分子标记连锁关联分析, 其定位结果相当于多次连锁重复验证, 具有极高的可靠性。对于棉花育种的应用者来说, 这种定位结果可以有效指导育种者根据孟德尔的基因独立遗传或连锁遗传规律, 依据育种目标来配置不同的杂交组合, 从而有目的地实现不同外源基因的互补与整合。
参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
DOI:10.7668/hbnxb.2015.03.010Magsci [本文引用: 1]

为分析转基因抗草甘膦棉花早代遗传情况,以花粉管通道法获得的26个转5-烯醇式丙酮酰莽草酸-3-磷酸合酶基因(<em>EPSPS</em>)抗草甘膦棉花转化事件为材料,以其背景亲本中棉所49为对照,喷施草甘膦后对转基因棉T<sub>1</sub>、T<sub>2</sub>分离比例进行考察。T<sub>1</sub>田间抗性鉴定结果表明,经卡方检测20个转化事件T<sub>1</sub>分离符合3: 1的分离规律,即外源基因插入1个位点;6个转化事件不符合1对基因的分离规律,出现了偏分离。T<sub>2</sub>田间抗性鉴定结果表明,通过花粉通管法共获得152个纯合株系,分别来源于25个转化事件;对T<sub>2</sub>不纯合株系继续进行分离比例的考察,发现来源于15个转化事件的57个株系符合3: 1的分离规律;此外卡方检测结果表明,每个转化事件都有不符合3: 1分离规律的株系,且其中10个转化事件没有符合3: 1分离规律的株系。表明通过花粉管通道法获得的转基因植株中外源基因的整合和遗传均较复杂。
DOI:10.7668/hbnxb.2015.03.010Magsci [本文引用: 1]

为分析转基因抗草甘膦棉花早代遗传情况,以花粉管通道法获得的26个转5-烯醇式丙酮酰莽草酸-3-磷酸合酶基因(<em>EPSPS</em>)抗草甘膦棉花转化事件为材料,以其背景亲本中棉所49为对照,喷施草甘膦后对转基因棉T<sub>1</sub>、T<sub>2</sub>分离比例进行考察。T<sub>1</sub>田间抗性鉴定结果表明,经卡方检测20个转化事件T<sub>1</sub>分离符合3: 1的分离规律,即外源基因插入1个位点;6个转化事件不符合1对基因的分离规律,出现了偏分离。T<sub>2</sub>田间抗性鉴定结果表明,通过花粉通管法共获得152个纯合株系,分别来源于25个转化事件;对T<sub>2</sub>不纯合株系继续进行分离比例的考察,发现来源于15个转化事件的57个株系符合3: 1的分离规律;此外卡方检测结果表明,每个转化事件都有不符合3: 1分离规律的株系,且其中10个转化事件没有符合3: 1分离规律的株系。表明通过花粉管通道法获得的转基因植株中外源基因的整合和遗传均较复杂。
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
