全文HTML
--> --> -->值得注意的是, Molina和Rowland[2]提出关于氟利昂破坏大气地球平流层内臭氧层的观点. CFC-11会破坏大气地球平流层内臭氧层, 是全球气候变暖的罪魁祸首之一. 地球上大气臭氧层能够吸收大多数来自太阳的有害辐射, 能有效保护地球生物, 对人类生存及家园至关重要. 自1985年正式发现臭氧破洞后[3], 根据《蒙特利尔议定书修正案》规定, 在2000年前停止生产和使用氟利昂. 但有关CFC-11物质的控制和降解仍然是人们关注的焦点, 如Vollmer等[4]报道了至今近80年来大气对流层中CFC-11分子的排放情况, Schuck等[5]提出在Taunus天文台建立监测氯氟烃的长期方法, LeedhamElvidge等[6]分析了包含CFC-11在内的氟利昂物质的测量, 并估算氯氟烃在大气中的生命周期. 对CFC-11的研究主要集中于大气环境污染监测[4-8]、高温降解[9-11]、激光解离动力学[12]、介质阻挡放电[13]等方面.
辐射场本质上是一种电磁波, 90%以上是电场对该分子的作用, 电场作用下会产生分子的高能激发态及次级电子、改变分子的电子结构、发生键的碎裂及新自由基生成等一系列的化学变化, 且关于分子外电场效应的研究得到了许多研究者的密切关注[14-19]. 谢安东等[14]计算了UO3分子在自辐射场下的光谱性质, 结果显示分子能级对自辐射场有强依赖性, 尹文怡等[15]对GaN在辐射场中的物理特性和光谱进行了计算研究, 结果表明电场可对其光谱进行调控. 李亚莎等[16]研究绝缘材料盐交联聚乙烯分子(XLPE)在外电场下的特性, 得到临界击穿场强为11.16 GV/m, 电场可导致XLPE中C—C键断裂、载流子浓度升高、导电性能提升等现象, 从而降低了XLPE的绝缘性能. 基于此, 有必要对CFC-11分子在辐射场中的光谱与解离特性进行理论计算. 目前尚未见关于CFC-11分子在辐射场中的研究报道.
本文选用B3LYP/6-311++g(3df, 3pd)方法及基组, 对CFC-11分子进行优化来获取该分子的基态稳定构型, 再探索外加电场对CFC-11分子的轨道能级、能隙、偶极矩、红外与拉曼光谱的影响, 最后探究外电场中CFC-11的解离特性. 通过本研究可进一步认识在辐射场作用下CFC-11分子的光谱特征和解离特性, 为降解该污染物提供理论依据.

本文选B3LYP/6-311++g(3df, 3pd)方法沿z轴方向加不同强度的静态偶极电场(其强度为–0.04, –0.03, –0.02, –0.01, 0.01, 0.02, 0.03, 0.04 a.u., 相当于–2.057—2.057 V/?)来考察该分子的红外与拉曼光谱特性, 在不同场强度下优化得到的CFC-11基态分子结构基础上, 计算场对C—F键解离的影响.
3.1.CFC-11分子的基态结构
采用B3LYP/6-311++g(3df, 3pd)方法和基组对CFC-11分子结构进行优化计算, 分子结构如图1所示. 所有频率均为正值, 表明该分子结构是稳定的. 该分子属于C3V点群, R(C—F)和R(C—Cl)键长分别为0.1338, 0.1775 nm, ∠ClCCl键角为110.57°, 文献[20]R(C—F)和R(C—Cl)键长分别为0.1362, 0.1754 nm, 相差0.0024, 0.0021 nm, 误差分别为1.7%, 1.19%; 键角∠ClCCl为111°, 相差0.43°, 误差仅为0.38%. 表明本文的计算与实验值吻合, 方法选取合理. 图 1 CFC-11分子的几何结构
图 1 CFC-11分子的几何结构Figure1. Equilibrium structure of CFC-11 molecule.
2
3.2.辐射场中CFC-11分子的基本性质
沿主轴z方向(即C—F连线)外加电偶极化电场, 选用B3LYP/6-311++g(3df, 3pd)方法和基组探究电场对CFC-11分子结构及特性的影响, 计算结果列入表1中. 从表1和图2可知, 沿着z的正向加大电场时, Cl原子受电场作用向C原子方向移动, F原子则向C原子方向远离, C—F键长的变化比C—Cl键的变化更明显. 从图1可知, 外加电场正是C—F连线的z方向, C—F键受到电场作用力强于C—Cl键, 变化程度大于C—Cl键. 此外, C—F键随电场的增加逐渐增大, 表示化学键因电场强度的增加而变得脆弱. 如此, 电场增大可使化学键越容易发生解离.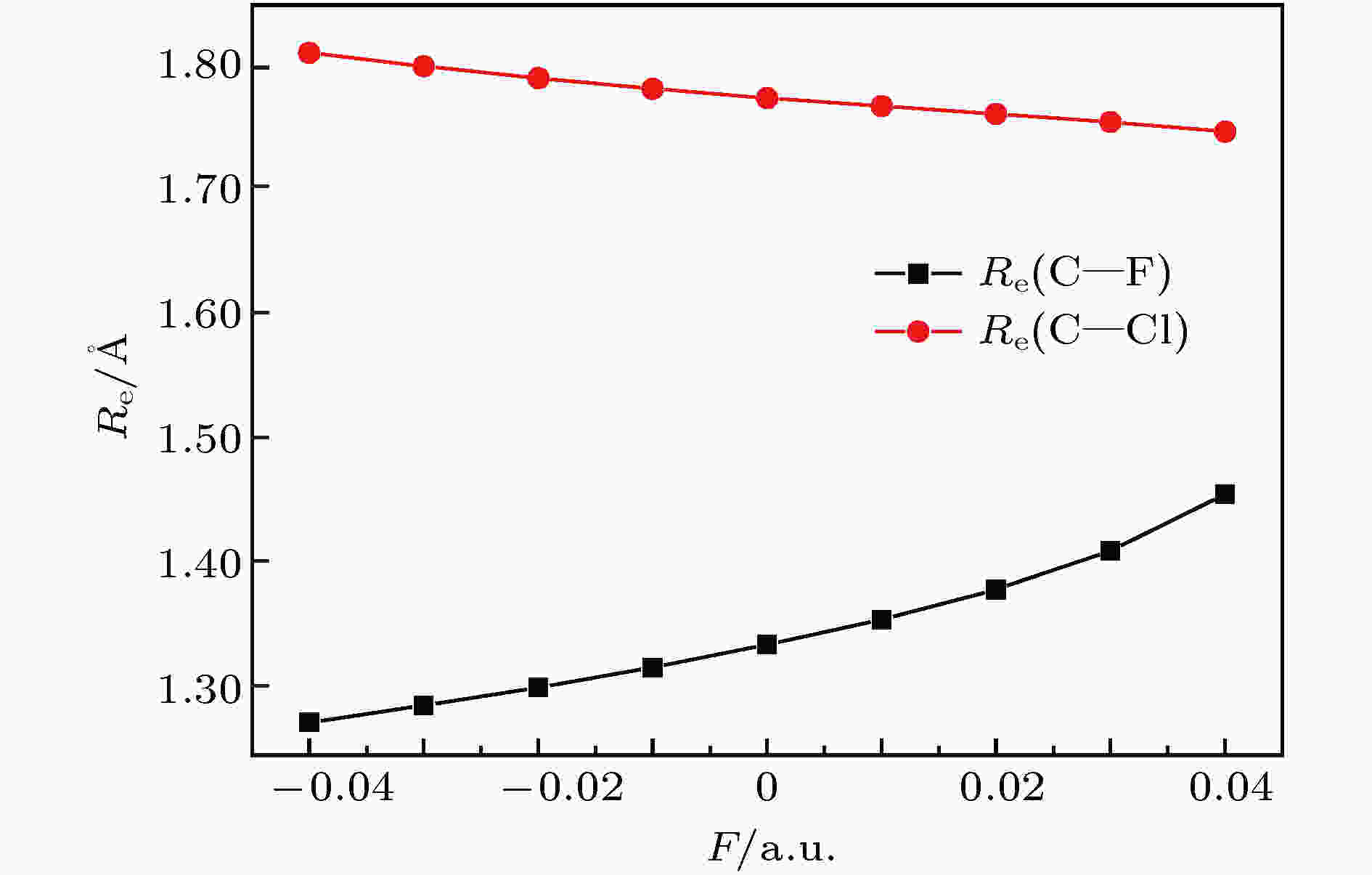 图 2 键长随电场的变化
图 2 键长随电场的变化Figure2. Bond length variation with external electric field.
| F/a.u. | Re(C—F)/? | Re(C—Cl)/nm | E/hartree | $\mu$/Debye |
| –0.04 | 1.2764 | 1.8118 | –1518.7025 | 5.0491 |
| –0.03 | 1.2898 | 1.8010 | –1518.6855 | 3.6168 |
| –0.02 | 1.3043 | 1.7916 | –1518.6740 | 2.2462 |
| –0.01 | 1.3199 | 1.7830 | –1518.6678 | 0.9145 |
| 0.00 | 1.3385 | 1.7757 | –1518.6668 | 0.4044 |
| 0.01 | 1.3582 | 1.7692 | –1518.6710 | 1.7191 |
| 0.02 | 1.3825 | 1.7628 | –1518.6803 | 3.0657 |
| 0.03 | 1.4135 | 1.7563 | –1518.6952 | 4.4805 |
| 0.04 | 1.4587 | 1.7486 | –1518.7158 | 6.0486 |
表1不同电场下计算得到的CFC-11分子参数(1 hartree = 110.5 × 10–21 J)
Table1.Calculated parameters of CFC-11 molecule under different external electric field.
表1还列出了不同电场强度下优化得到的CFC-11分子的电偶极矩







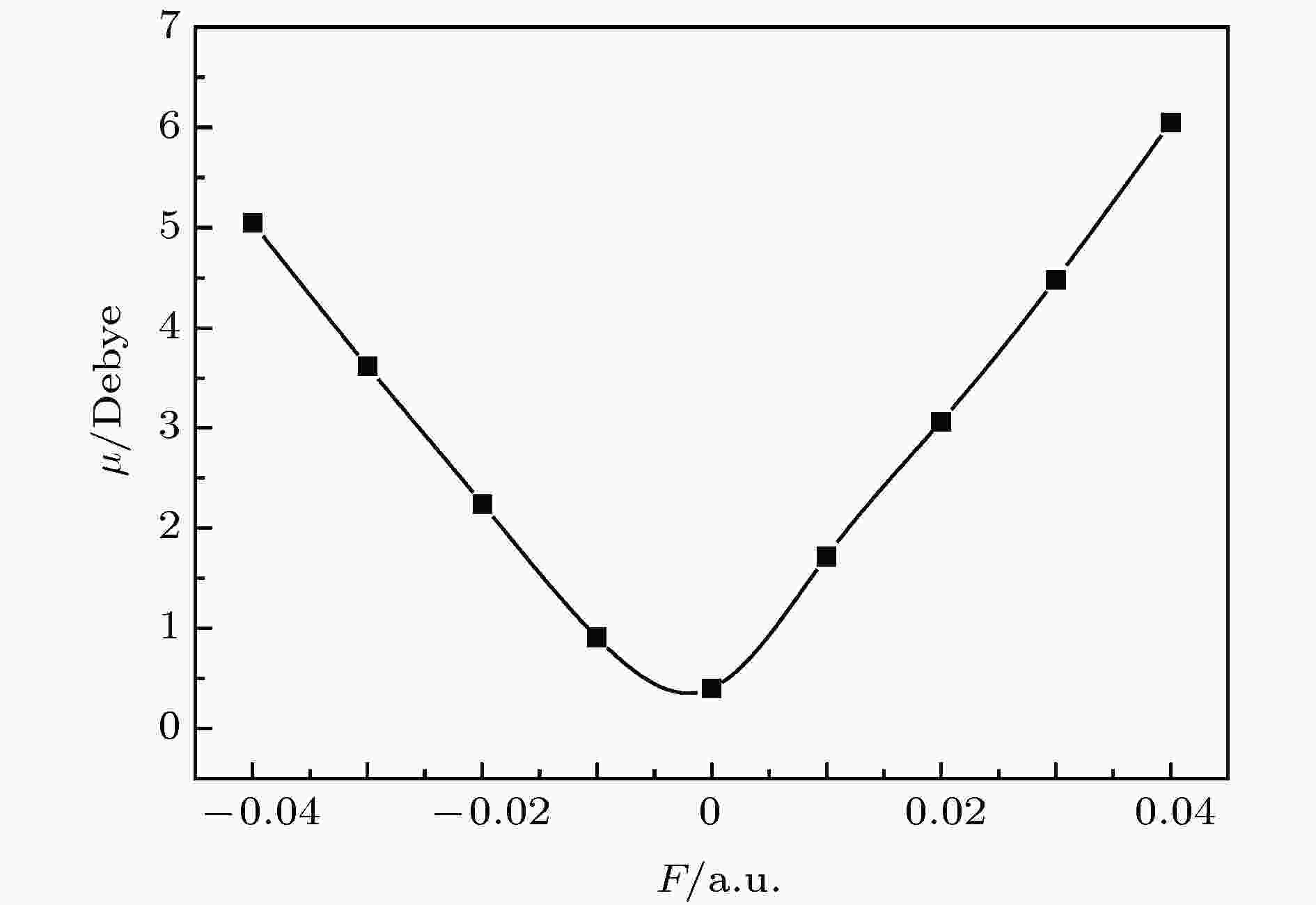 图 3 偶极矩随电场的变化
图 3 偶极矩随电场的变化Figure3. Dipole moment variation with external electric field.
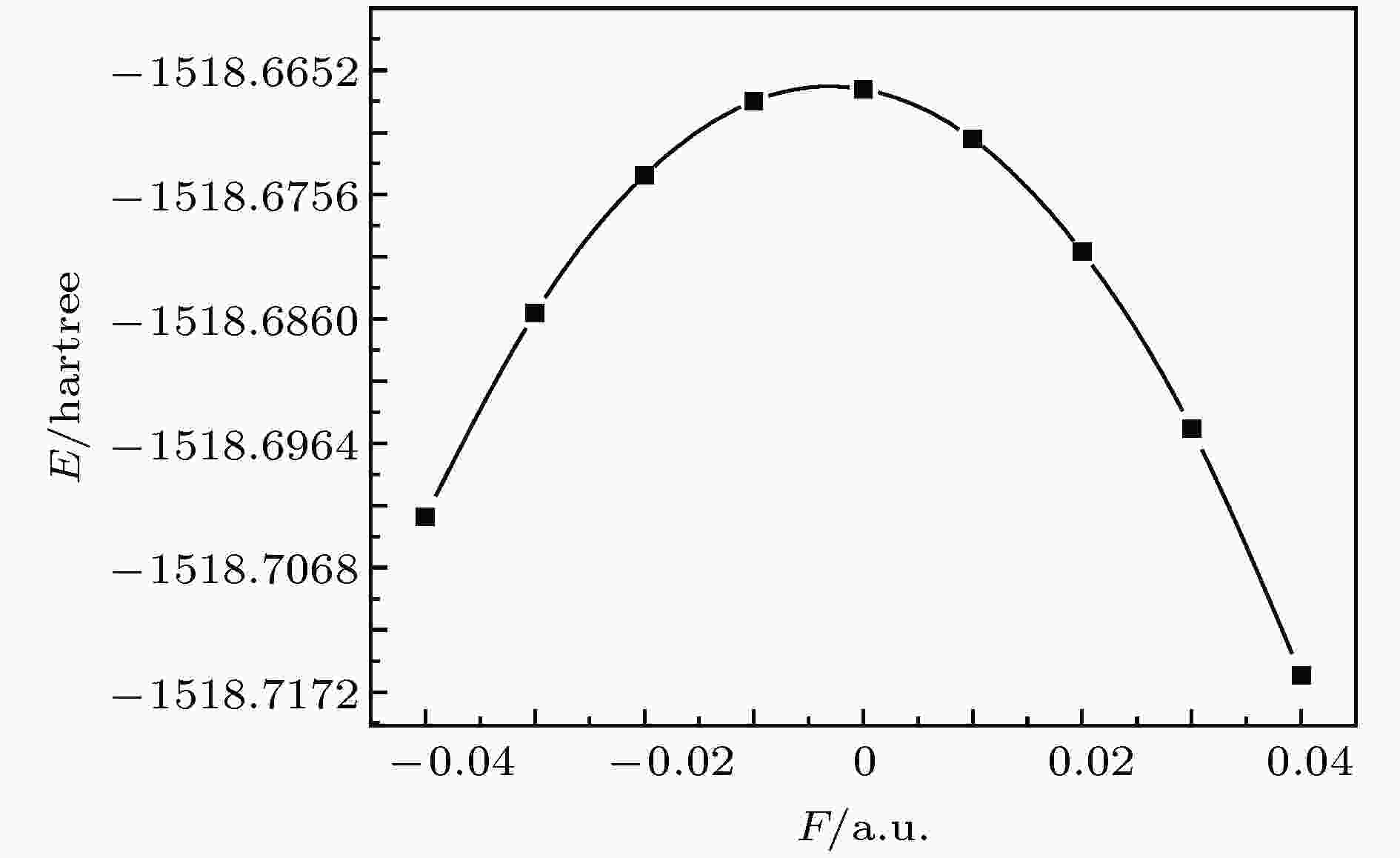 图 4 总能量随电场变化
图 4 总能量随电场变化Figure4. Total energy variation with external electric field.
2
3.3.辐射场中CFC-11分子的轨道能级分布特征
前线轨道理论认为[17,18]分子参与化学反应, 优先起作用的是最低未占据分子轨道(LUMO)和最高占据分子轨道(HOMO), 其中LUMO能级EL在数值上相当于分子的电子亲和势, 能级越低意味着分子接受电子的能力越强. HOMO能级EH反映了分子失去电子能力的强弱, HOMO能级越高意味着分子就越容易失去电子. 能隙Eg代表电子从占据轨道向未占据轨道发生跃迁的能力, Eg = EL – EH, 在一定程度上代表分子参与化学反应的能力[17,18], 化学活性随能隙减小而增大, 化学活性越大, 则分子越不稳定.本文选用上述同样的方法和基组, 计算了电场中CFC-11分子轨道能级, 如图5所示, 分子的最高占据轨道能级升高, 最低未占据轨道能级则是先增大, 到F = 0.02 a.u.后开始降低. 图6显示, 随着电场的变化, 能隙随EH和EL的变化出现先增大后减小. 当电场强度大于0.02 a.u.时, 其能隙急剧下降, 电场处于0 a.u.至–0.04 a.u.时, 能隙随电场数值的增大而减小, 占据轨道上的电子越容易被激发. 正向与反向电场强度增加, 对能隙的影响略有差异. 总之, 电场的增强加剧了分子不稳定性, 如C—F键发生断裂等现象. 此外, Eg的大小与紫外光谱有直接关联, Eg的减小可观察到紫外光谱的吸收向长波方向移动, 即产生红移.
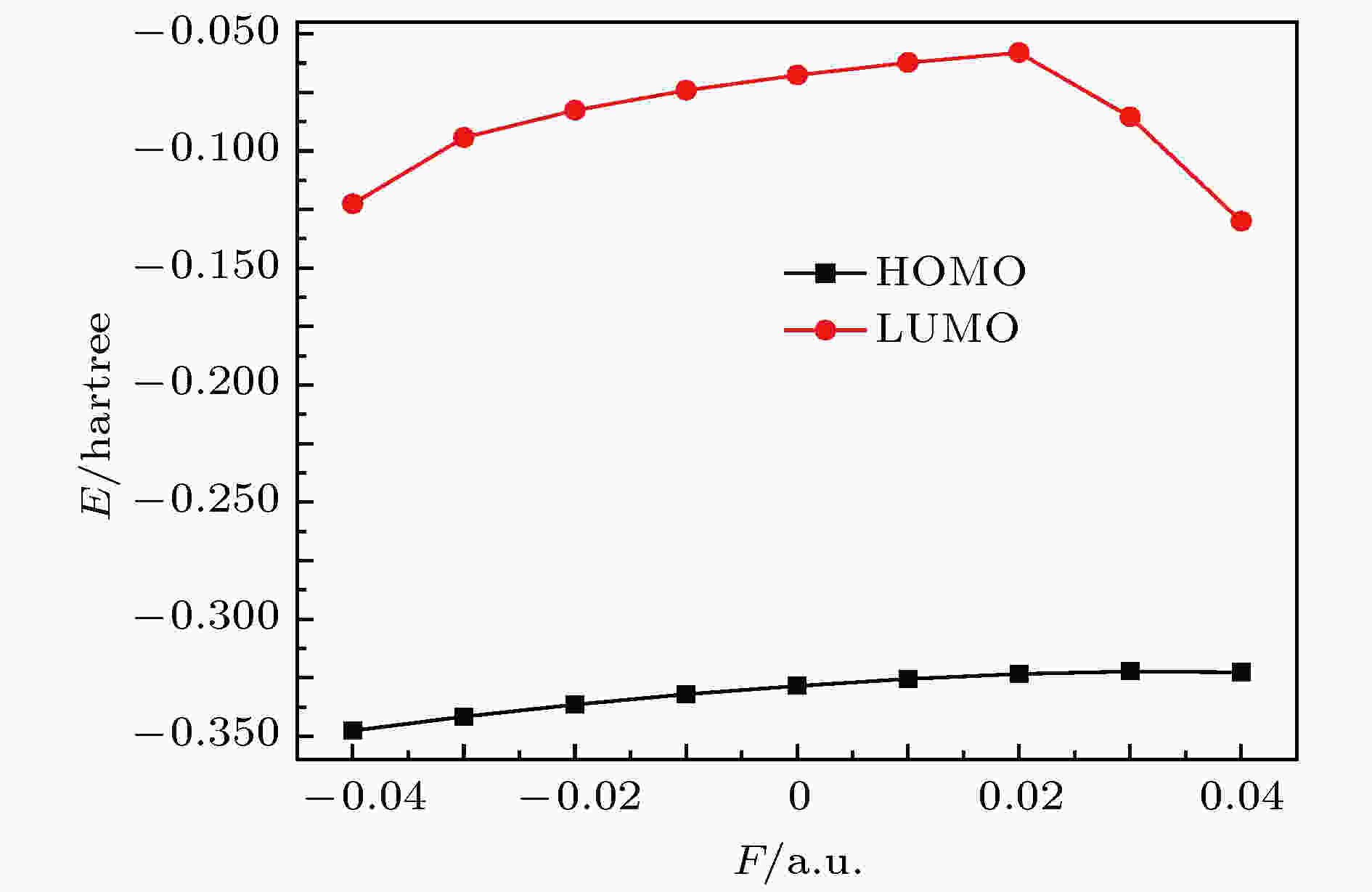 图 5 HOMO和LUMO能级随电场变化
图 5 HOMO和LUMO能级随电场变化Figure5. The HOMO and LUMO energy level variation with external electric field.
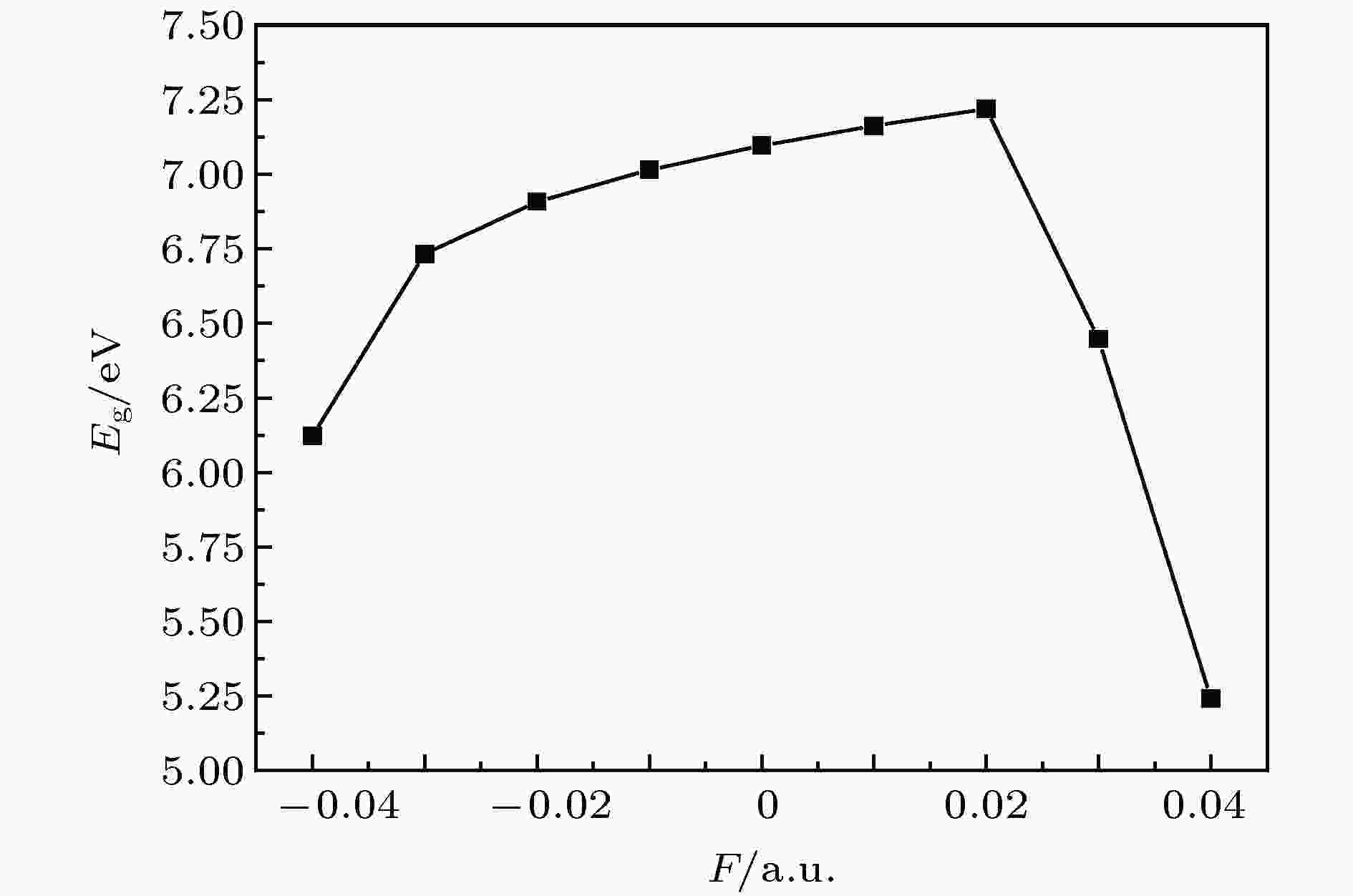 图 6 能隙随电场变化
图 6 能隙随电场变化Figure6. Energy gap variation with external electric field.
2
3.4.辐射场中CFC-11分子的红外与拉曼光谱特性
采取B3LYP/6-311++ g(3df, 3pd)方法和基组对CFC-11分子红外与拉曼光谱进行了计算. 无电场时(表2), 该分子的红外谱共有六种简正模. 如最强峰847 cm–1 C—Cl3的d-deform振动, 本文得到的二度简并值为802.3721, 802.4017 cm–1. 在次强峰位置于1085 cm–1 C—F的stretch振动, 本文计算值为1071.2887 cm–1等. 与实验对比可见, 计算得到的红外光谱值与实验值相吻合, 也进一步展示了所选方法的合理性.| Frequency | 本文 | 实验值[21] | 实验值[22] | 实验值[23] |
| f1/cm–1 | 1071.2887 | 1085 | 1085 | 1085 |
| f2/cm–1 | 526.5703 | 535 | — | 535 |
| f3/cm–1 | 347.5578 | 350 | — | 351 |
| f4/cm–1 | 802.3721, 802.4017 | 847 | 846 | 847 |
| f5/cm–1 | 394.9112, 394.9163 | 394 | — | 395 |
| f6/cm–1 | 242.9898, 242.9928 | 241 | — | 243 |
表2无电场时CFC-11分子的红外谱实验值与计算值
Table2.Experiment data and calculated data of infrared spectrum for CFC-11 molecule without external electric field.
红外光谱随电场的变化如图7所示. 电场对红外谱的影响较为明显, 如: 当电场从0 a.u.增大到0.04 a.u., 最强峰C—Cl3振动光谱随着电场增大向长波方向移动, 出现红移; 电场从0 a.u.减小到–0.04 a.u., 红外光谱则向短波方向移动, 出现蓝移. 而次强峰位置于C—F的振动则与之相反.
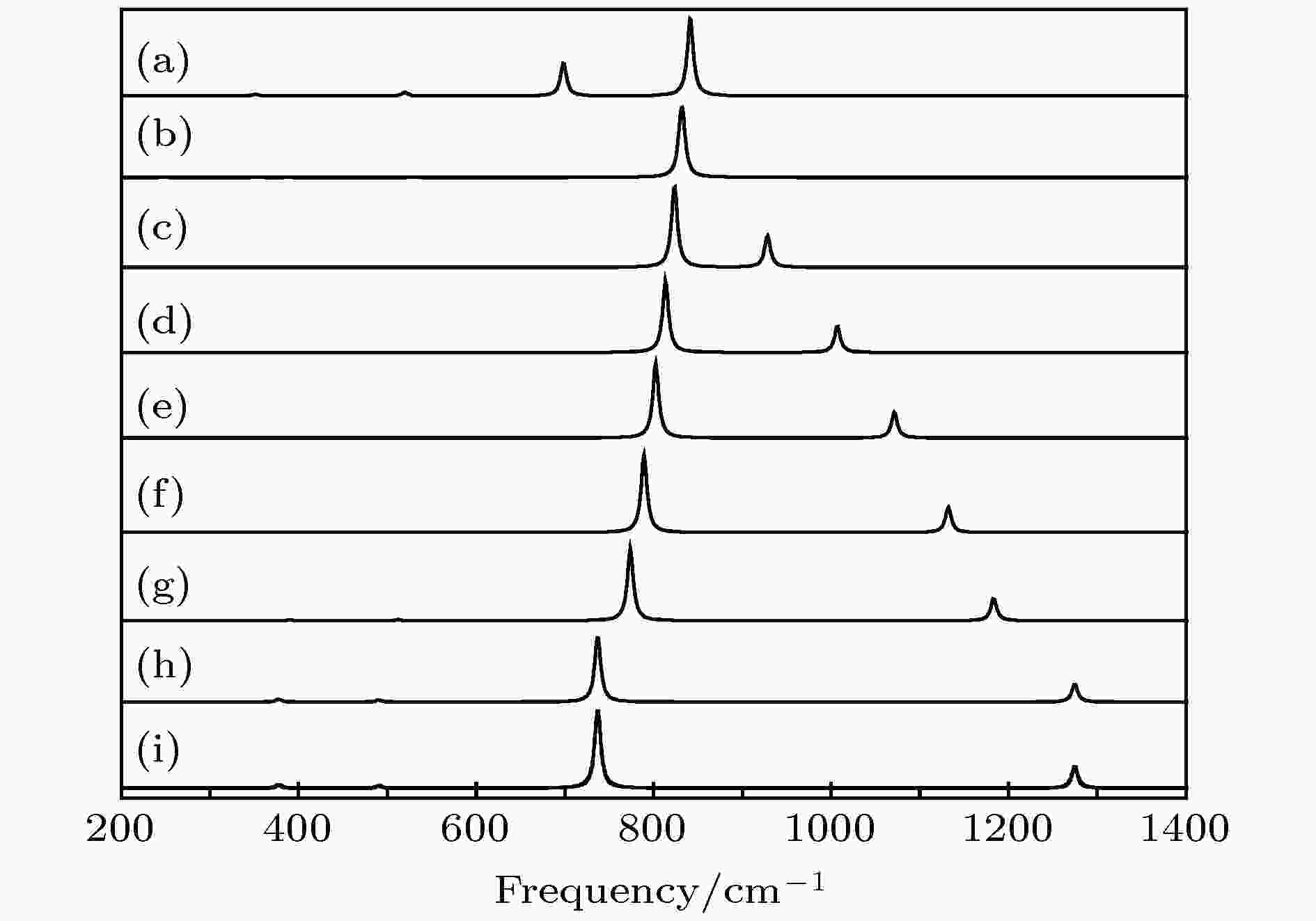 图 7 红外光谱随电场强度的变化 (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) a.u.; (f) 0.01 a.u.; (g) 0.02 a.u.; (h) 0.03 a.u.; (i) 0.04 a.u.
图 7 红外光谱随电场强度的变化 (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) a.u.; (f) 0.01 a.u.; (g) 0.02 a.u.; (h) 0.03 a.u.; (i) 0.04 a.u.Figure7. Variation of the infrared intensities with external electric field: (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) 0 a.u.; (f) 0.01 a.u.; (h) 0.02 a.u.; (g) 0.03 a.u.; (i) 0.04 a.u..
为了更清楚地看到电场对红外谱的影响, 图8是从图7中选取一条谱线的放大图, 其谱线位于242.99 cm–1 (见表2), 图8(a)是电场强度分别为0, –0.01, –0.02, –0.03, –0.04 a.u.的谱线特征, 图8(b)是电场强度分别为0, 0.01, 0.02, 0.03, 0.04 a.u.的谱线特征. 电场对红外光谱强度吸收是复杂的. 从图8(a)可知, 首先是CFC-11分子的红外谱强度发生改变, 无电场时的吸收强度不为零, 电场强度为–0.01和–0.02 a.u.的红外谱几乎消失, –0.03 a.u.的谱强度与0 a.u.时相近, 在0.04 a.u.强度增加非常明显. 其次, 谱线的位置受电场的影响, 谱线蓝移非常微弱. 由图8(b)可知, 电场对谱线吸收强度逐渐递增, 谱线的位置随电场强度增加出现红移. 图9同样也选取了图7中另一条位于802.4 cm–1的谱线, 图9(a)是电场强度分别为0, –0.01, –0.02, –0.03, –0.04 a.u.的谱线特征, 图9(b)是电场强度分别为0, 0.01, 0.02, 0.03, 0.04 a.u.的谱线特征. 对比图9(a)和图9(b)可知, 电场只是对谱线的位置进行了改变, 对其红外谱吸收强度的影响微弱. 综合图8(a)、图8(b)、图9(a)、图9(b)可得, 电场对不同谱线吸收谱强度的影响不同, 但对谱线位置出现红移或者蓝移的方向却是一致的.
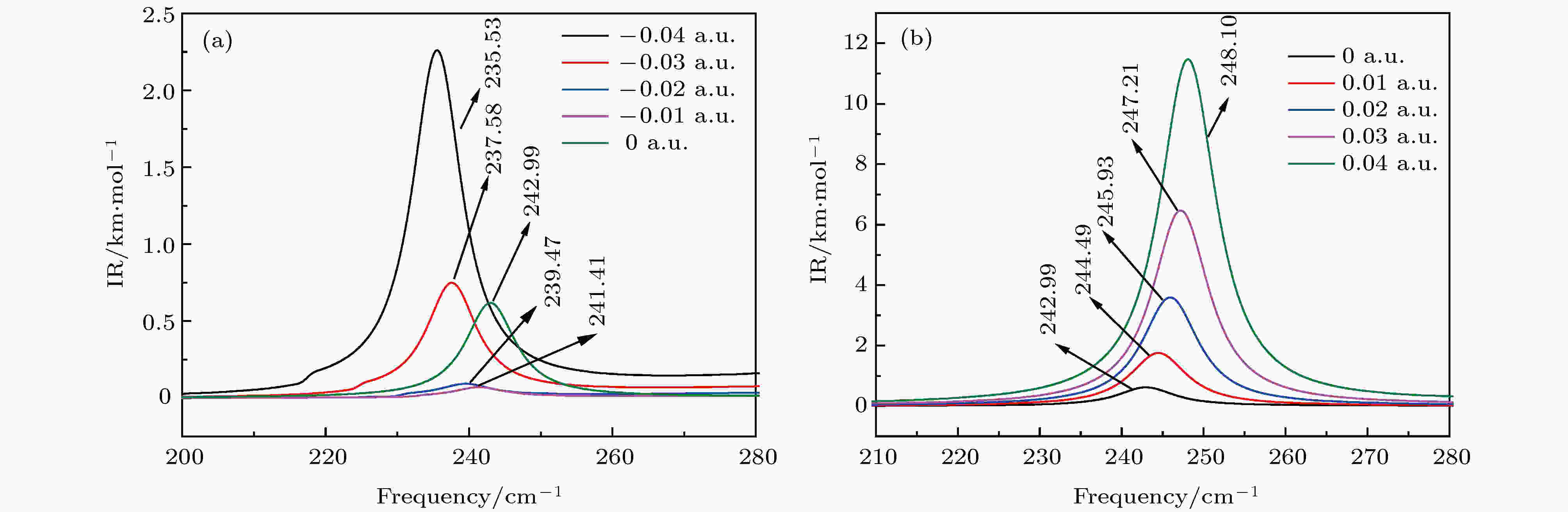 图 8 红外谱线242.99 cm–1随电场的变化 (a)反向电场; (b)正向电场
图 8 红外谱线242.99 cm–1随电场的变化 (a)反向电场; (b)正向电场Figure8. Variation of infrared spectrum of 242.99 cm–1 with external electric field: (a) Negative electric field; (b) positive electric field.
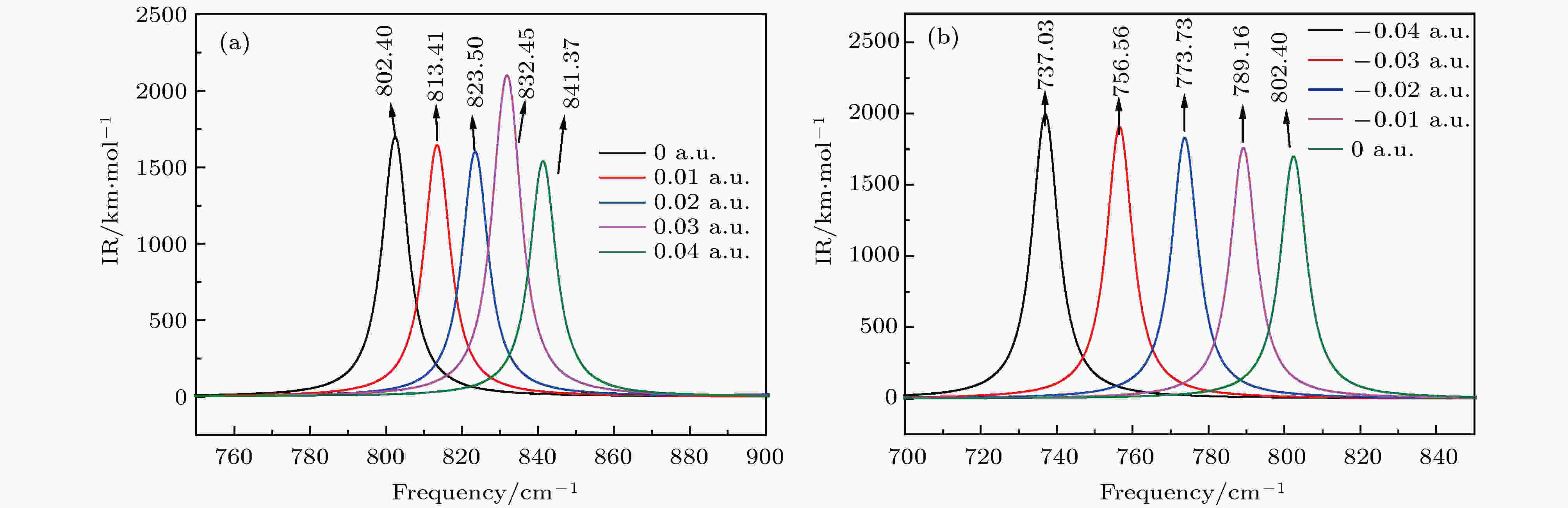 图 9 红外谱线802.40 cm–1随电场的变化 (a)反向电场; (b)正向电场
图 9 红外谱线802.40 cm–1随电场的变化 (a)反向电场; (b)正向电场Figure9. Variation of infrared spectrum of 802.40 cm–1 with external electric field: (a) Negative electric field; (b) positive electric field.
此外, 鉴于电场作用下谱线的移动以及对红外谱强度的影响, 在多种分子或多种基团混合中, 当谱线重叠或紧挨着而很难区分各基团或各分子谱带来的信息时, 电场可作为一种辅助手段对其谱线分离, 从而实现获取各种分子信息.
不同电场强度下的拉曼光谱绘制于图10中, 共6条拉曼光谱谱线, 可见电场可以改变拉曼光谱谱峰的位置和强度. 同上述红外光谱一样, 分别选取图10中的局部谱线, 即394.42和802.40 cm–1拉曼光谱谱线, 并且绘制于图11(a)、图11(b), 及图12(a)、图12(b)中, 其中图11(a)和图12(a)是拉曼光谱随反向电场的变化, 图11(b)和图12(b)则是随正向电场的变化.
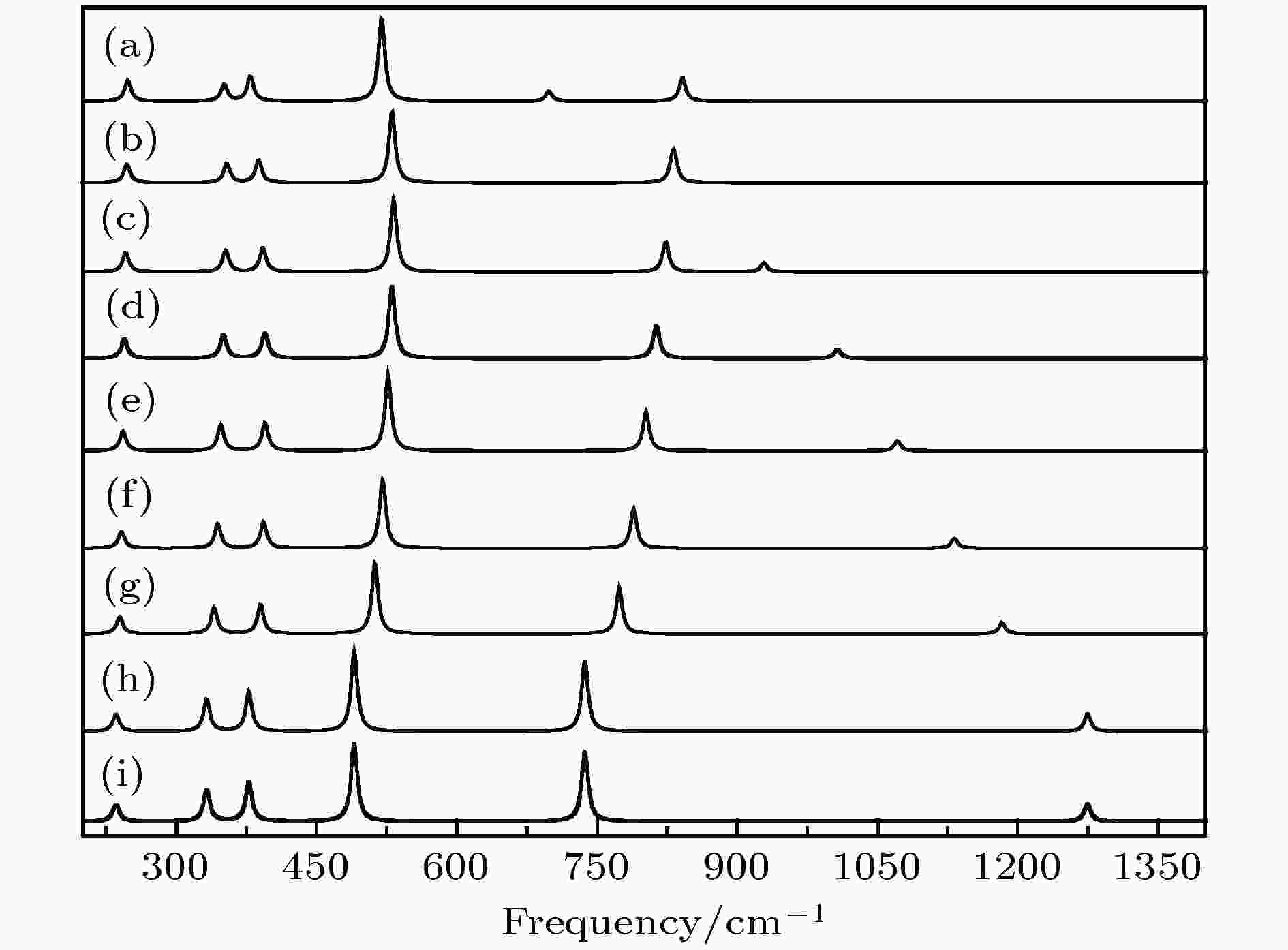 图 10 拉曼光谱随电场强度的变化 (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) 0 a.u.; (f) 0.01 a.u.; (g) 0.02 a.u.; (h) 0.03 a.u.; (i) 0.04 a.u.
图 10 拉曼光谱随电场强度的变化 (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) 0 a.u.; (f) 0.01 a.u.; (g) 0.02 a.u.; (h) 0.03 a.u.; (i) 0.04 a.u.Figure10. Variation of Raman spectrum with external electric field: (a) –0.04 a.u.; (b) –0.03 a.u.; (c) –0.02 a.u.; (d) –0.01 a.u.; (e) 0 a.u.; (f) 0.01 a.u.; (h) 0.02 a.u.; (g) 0.03 a.u.; (i) 0.04 a.u..
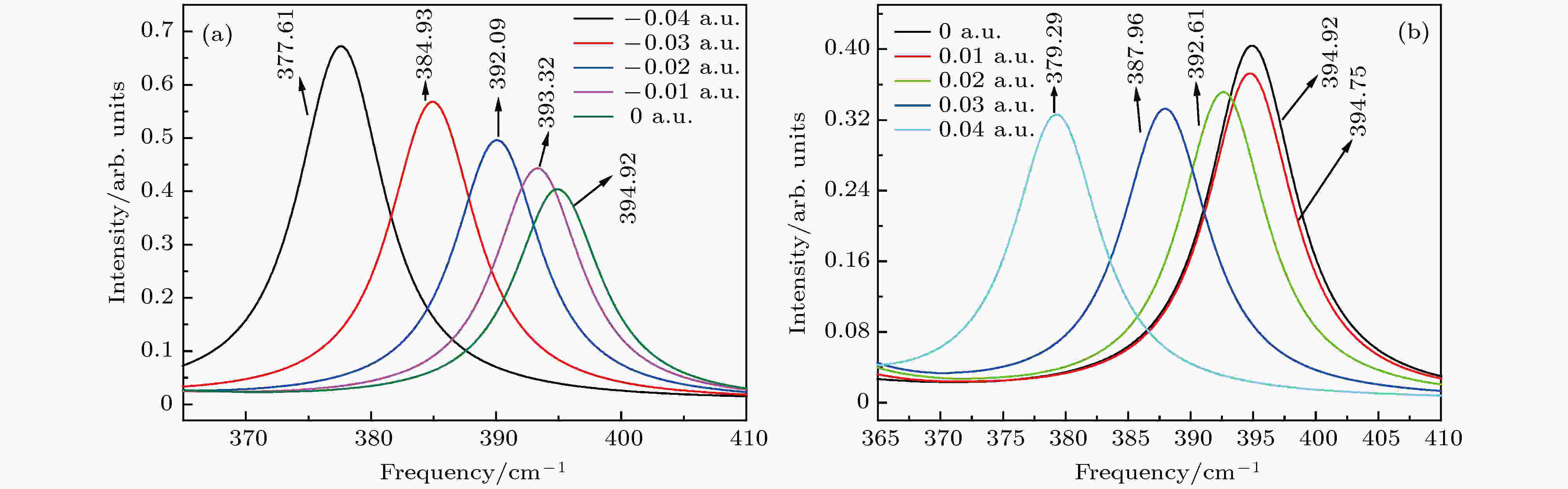 图 11 拉曼谱394.42 cm–1随电场的变化 (a)反向电场; (b)正向电场
图 11 拉曼谱394.42 cm–1随电场的变化 (a)反向电场; (b)正向电场Figure11. Variation of Raman spectrum of 394.42 cm–1 with external electric field: (a) Negative electric field; (b) positive electric field.
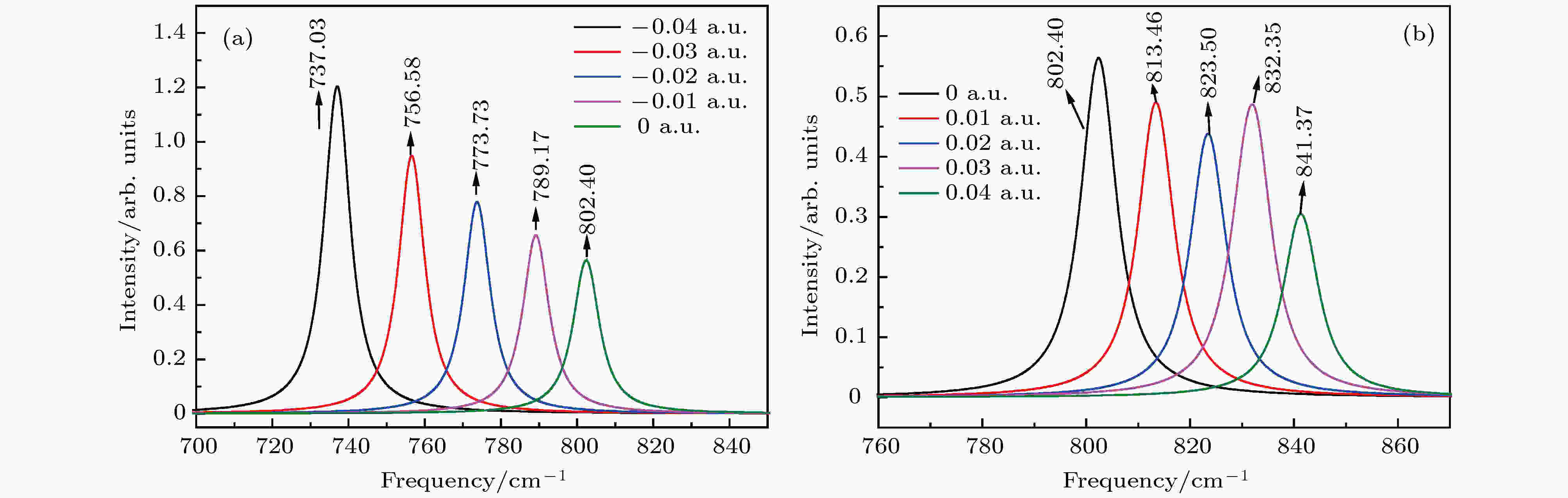 图 12 拉曼谱802.40 cm–1随电场的变化 (a)反向电场; (b)正向电场
图 12 拉曼谱802.40 cm–1随电场的变化 (a)反向电场; (b)正向电场Figure12. Variation of Raman spectrum of 802.40 cm–1 with external electric field: (a) Negative electric field; (b) positive electric field.
综合图11(a)、图11(b)、图12(a)和图12(b)可看出, 正向电场作用下的拉曼光谱向长波方向移动, 反向电场作用下拉曼光谱则向短波方向移动, 这与红外光谱随电场的变化一致. 拉曼光谱线394.42 cm–1强度在反向电场区随着电场的增大而增大, 在正向电场区随电场强度的增大而减小; 在802.40 cm–1拉曼光谱谱线中, 随着反向电场强度的增加拉曼光谱强度增加, 随着正向电场的增加, 拉曼光谱强度则有高有低.
综上, 外加电场可以对分子或基团红外谱和拉曼谱进行调控, 也可用于分子或基团谱线分离, 实现对分子或基团谱线信息的捕捉.
2
3.5.辐射场中分子C—F的解离特性
本文还计算了不同电场强度下CFC-11分子中的C—F键势能曲线. 依然选用B3LYP/6-311++ g(3df, 3pd)方法, 如图1, 沿着z方向分别加正向电场至0.04 a.u., 反向电场至–0.04 a.u., C—F键扫描范围从0.8 ?到5.8 ?, 步长设置为0.05 ?, 共101个数据点. 将扫描的势能点分别绘制于图13和图14中. 由图13(a)和图14可知, 处于势阱最低位置时, 无电场时的势阱值要高于有电场时的值. 这与图4结果一致. 从图13可以看出C—F键值大于1.7 ?时, 有电场时的势能曲线高于无电场时的曲线, 且势垒一直存在, 从图13(b)可看到电场为0.04 a.u. 的势能曲线与无电场时出现二次相交, 势能曲线整体上将出现一个稳定点的极小值和非稳定点极大值, 类似于“火山态”[19], 这表明在极小值与极大值之间的能垒随电场增大逐渐减小, 继续增大电场强度, 解离会逐渐变得容易. 图14中C—F键的势能曲线随电场强度增大, 能垒逐渐减小, C—F键的束缚能力逐渐减弱, 当电场增加到一定程度时, 能垒消失, 分子发生解离.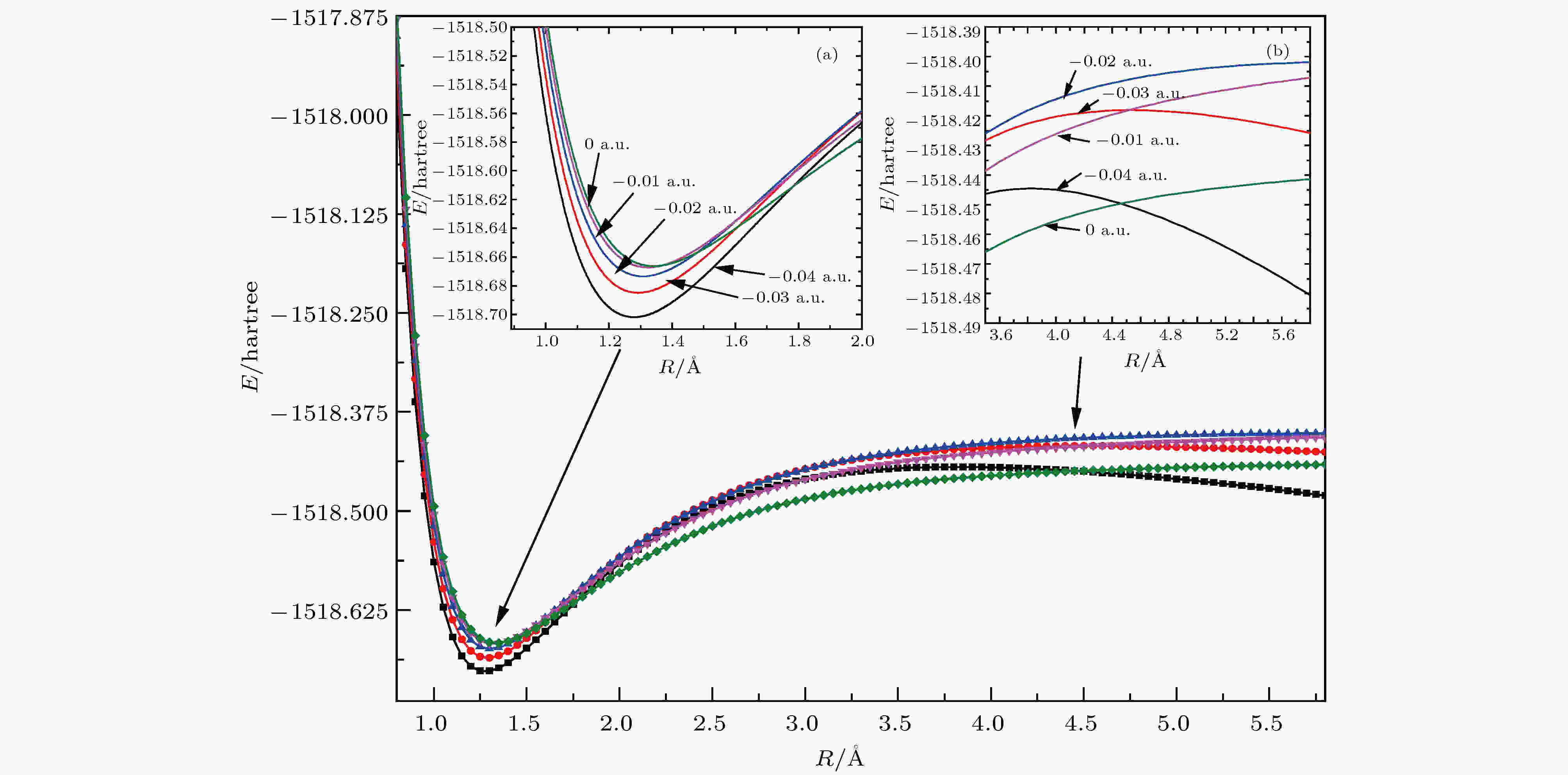 图 13 反向电场下C—F键势能曲线
图 13 反向电场下C—F键势能曲线Figure13. Potential energy curve variation with negative electric field.
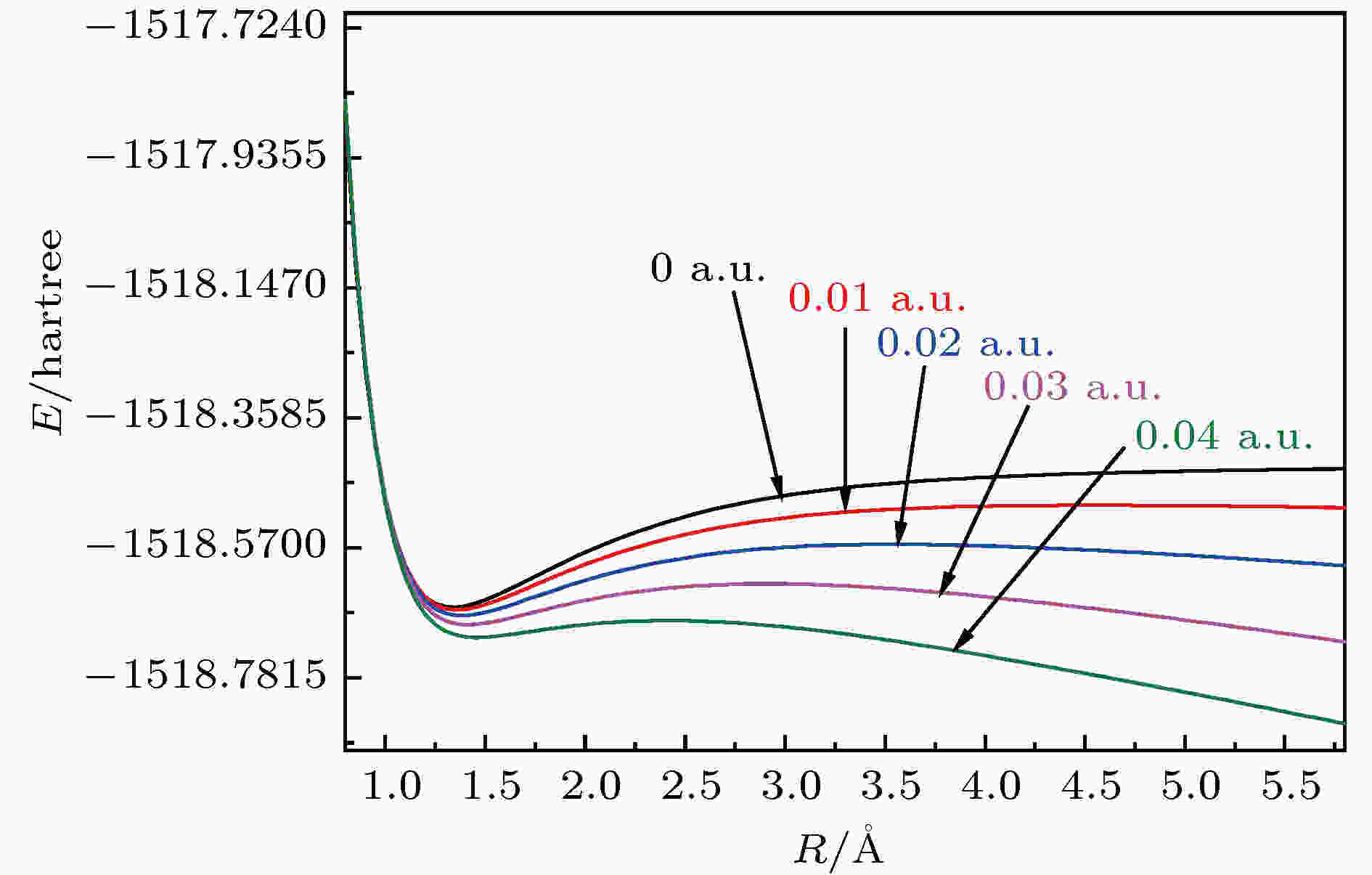 图 14 正向电场下C—F键势能曲线
图 14 正向电场下C—F键势能曲线Figure14. Potential energy curve variation with positive electric field.
图13和图14中C—F键在电场中的势能曲线差异明显, 这是因为电场中C—F键长的变化比C—Cl键的变化要明显. 正向电场下, F原子远离C原子, F原子周围的电子云与其他原子干涉越来越小, 能垒逐渐减弱, 解离越来越容易. 在反向电场中, F原子向C原子靠拢, 加大了C原子与其他原子的电子相互作用, 但由于电场的存在, 导致C—F键暂时更加“紧密”, 能垒增强, 即出现高于无电场时的能垒. 当C—F键逐渐增大, 这种“紧密”被打破, 势能曲线二次相交现象即出现.
综上, CFC-11分子中的C—F键在电场作用下将会发生断裂, 从而使得该分子发生降解, 该结果为降解该污染物提供了一种理论依据.
本文无电场时计算的红外谱与实验值相吻合. 电场对红外谱产生分子振动斯塔克效应, 红外与拉曼光谱随着电场变化出现红移或蓝移现象, 同时影响红外与拉曼光谱吸收强度. 电场可作为一种辅助手段对其谱线分离而获取各种分子信息.
不同强度下对CFC-11分子中的C—F键进行势能面扫描, 能垒逐渐反向电场增大而减小, C—F键的束缚能力逐渐减弱, 当电场增加到一定程度时, 能垒消失, 分子发生解离. 本文有望为实现CFC-11分子最终发生解离而降解提供一种可行有效的调控手段.
