 ,淮阴工学院生命科学与食品工程学院,江苏淮安 223003
,淮阴工学院生命科学与食品工程学院,江苏淮安 223003Identification, Systematic Evolution and Expression Analysis of HD-Zip Gene Family in Capsicum annuum
SHAO ChenBing, HUANG ZhiNan, BAI XueYing, WANG YunPeng, DUAN WeiKe ,College of Life Sciences and Food Engineering, Huaiyin Institute of Technology, Huai’an 223003, Jiangsu
,College of Life Sciences and Food Engineering, Huaiyin Institute of Technology, Huai’an 223003, Jiangsu通讯作者:
责任编辑: 赵伶俐
收稿日期:2019-07-30接受日期:2019-09-23网络出版日期:2020-03-01
| 基金资助: |
Received:2019-07-30Accepted:2019-09-23Online:2020-03-01
作者简介 About authors
邵晨冰,E-mail:1457599372@qq.com。

摘要
关键词:
Abstract
Keywords:
PDF (10281KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
邵晨冰, 黄志楠, 白雪滢, 王云鹏, 段伟科. 辣椒HD-Zip基因家族鉴定、系统进化及表达分析[J]. 中国农业科学, 2020, 53(5): 1004-1017 doi:10.3864/j.issn.0578-1752.2020.05.012
SHAO ChenBing, HUANG ZhiNan, BAI XueYing, WANG YunPeng, DUAN WeiKe.
0 引言
【研究意义】辣椒(Capsicum annuum),属茄科(Solanaceae)茄亚族(Solaninae Dunal)辣椒属一年生或多年生植物,是我国重要的蔬菜作物,近几年种植面积及产量均居世界首位(http://faostat.fao.org)。HD-Zip转录因子(homeodomain-leucine zipper,HD-Zip)是植物中特有的一类转录因子,参与调控植物光合作用、形态建成以及逆境胁迫应答等重要生长发育过程[1,2]。通过在辣椒基因组中系统鉴定HD-Zip基因家族成员,并对其染色体定位、基因结构、进化关系和表达特征进行分析,对进一步认识辣椒生长发育过程及培育改良辣椒品种具有重要意义。【前人研究进展】HD-Zip转录因子属于同源异形域(Homeodomain,HD)转录因子超家族,参与调控正常生长条件和环境胁迫后植物的生长发育[3]。该转录因子均由同源异型域及亮氨酸拉链(leucine zipper,LZ)结构域共同构成。HD和LZ结构域的存在共同决定了该类蛋白的转录因子功能[1]。根据基因序列的保守性及结构特点,该家族可被分为4个亚族,HD-Zip I—IV:HD-Zip I亚族只包含HD和LZ结构域;II亚族另包含一个N端保守区域(N-term);III亚族较复杂,包含除HD和LZ结构域之外的START、SAD和MEKHLA结构域;IV亚族与III亚族类似但没有C端的MEKHLA结构域[1]。HD-Zip基因家族不同亚族参与不同的代谢途径[1]。以模式植物拟南芥为例,HD-Zip I在非生物胁迫(ATHB1、ATHB5、ATHB6、ATHB7、ATHB12)[4],光信号转导(ATHB16)[5],叶片发育(ATHB1、ATHB3、ATHB16和ATHB20)[4]等方面发挥重要的作用;HD-Zip II主要在植物发育过程中参与环境改变应答机制,特别是光质改变应答调控(ATHB2、ATHB4、ATHB2)[6,7];HD-Zip III主要参与胚胎发育(PHB和PHV)[8],茎和花分生组织形成(ATHB15、ATHB8、REV)[9]和维管发育(REV、ATHB15)[10,11]等;HD-Zip IV则主要在植物毛状体的形成(HDG11、HDG12、GL2)[12],表皮细胞的发育(ATHB10、PDF2、AtML1)[13],叶片形态和生殖细胞发育(HDG1)[14],花色素苷积累(ANL2)[15]等过程起重要作用。HD-Zip的同一亚族在不同植物中具有相似的功能。但由于物种和环境的差异,特别是不同植物在进化过程中经历了不同选择、复制和保留事件,HD-Zip基因家族同源基因在不同物种中均有不同程度的分化。比如油椰子(Elaeis guineensis)中的EgHOX1(II亚族),该基因参与早期体胚的形成,并且影响了形成层发育中胚性能力的获得[16]。番茄中的13条HD-Zip IV基因在新叶和花朵中高度表达,对不同的植物激素和非生物胁迫具有应答作用[17]。【本研究切入点】目前,该家族基因已经在拟南芥[1]、葡萄[18]、玉米[19]等多个物种中被鉴定,并发现其发生不同程度的功能分化。辣椒的全基因组测序在两个品种‘CM334’及‘遵辣1号’中已完成[20,21],为研究相关基因的功能及关系奠定了坚实的基础。虽然该家族在‘CM334’基因组中进行了初步分析[22],但进化及表达数据分析较少,并未进行深入研究和比较分析。【拟解决的关键问题】本研究利用生物信息学手段鉴定辣椒HD-Zip基因家族,并系统分析其在基因组中的分布、基因结构、进化分化特征及在不同组织中的时空表达特异性,为阐明辣椒HD-Zip基因家族分化历程及生物学功能奠定基础。1 材料与方法
试验于2018—2019年在淮阴工学院园艺作物系统生物学实验室进行。1.1 辣椒HD-Zip基因家族成员的鉴定
本研究主要基于我国辣椒测序品种‘遵辣1号(Zunla-1)’进行系统分析,同时利用墨西哥地方品种‘CM334’进行比较分析。研究中使用的辣椒基因组数据分别从辣椒基因组网站(Pepper Genome Database2.0,http://peppersequence.genomics.cn/page/ species/index.jsp)及PGP(Pepper genome platform,http://peppergenome.snu.ac.kr/)下载获得。参照前人报道[1]及PlantTFDB(Plant Transcription Factor Database http://planttfdb.cbi.pku. edu.cn/)确定拟南芥HD-Zip基因家族成员。随后,将其作为诱饵利用本地BLAST工具在辣椒基因组中进行比对(参数为E<1e-10,Identity>40%),获得与拟南芥同源性高的HD-Zip序列信息,并利用Pfam(http://pfam.sanger. ac.uk/search)及SMART(http://smart.emblheidelberg. de/)进行验证分析,删除缺失结构域的序列,最终获得辣椒HD-Zip基因家族候选基因。
辣椒HD-Zip家族成员蛋白分子量和等电点利用在线工具EMBOSS Programs(https://www.ebi.ac.uk/ Tools/emboss/)进行分析鉴定。
1.2 辣椒HD-Zip基因家族系统进化树构建和分组确定
利用CLUSTALW将拟南芥及辣椒HD-Zip氨基酸序列进行多序列比对分析[23]。并通过邻接法(Neighbour-Joining,NJ)在MEGA 6.0中构建系统进化树,自展值(Bootstrap)设定为1 000。HD-Zip基因的核苷酸差异同样应用MEGA6.0进行计算[24]。1.3 辣椒HD-Zip家族成员结构和保守结构域分析
HD-Zip的外显子和内含子位置信息参考辣椒基因组注释信息GFF文件,之后应用本地perl语言提取位置信息转变为GSDS(Gene Structure Display Server;http://gsds.cbi.pku.edu.cn)可读bed文件。应用在线工具GSDS进行HD-Zip结构的绘制。应用MEME 4.9.0预测分析HD-Zip蛋白序列的结构域,搜寻motif值设置为16,结构域宽度设定为最小10、最大100,其他设定为默认参数。通过TBbool软件绘制出MEME结构[25]。HD及LZ结构域通过SMART(http://smart.embl-heidelberg.de)数据库分析确定。
1.4 辣椒HD-Zip基因家族染色体定位和基因复制类型分析
应用本地perl语言在辣椒基因组注释信息GFF文件中提取位置信息并构建辣椒染色体定位图。HD-Zip在辣椒基因组中的复制类型根据MCScanX下游程序duplicate_gene_classifier获得[26],并标注在染色体上。1.5 HD-Zip直系(Orthologous)和旁系(Paralogous)同源基因分析
辣椒、番茄和拟南芥HD-Zip的直系与旁系同源关系通过OrthoMCL(http://orthomcl.org/orthomcl/)软件进行鉴别,HD-Zip在3个基因组中的直系与旁系之间的关系图用Circos(http://circos.ca/)软件绘制。1.6 辣椒HD-Zip的组织表达差异分析和共表达网络构建
通过GEO数据库(https://www.ncbi.nlm.nih.gov/geo/)获得‘遵辣1号’材料不同时期的转录组(GSE45037)注释文件[21],运用R软件绘制辣椒HD-Zip基因家族的表达热图。辣椒HD-Zip在不同组织之间的表达关系皮尔森相关系数(Pearson’s correlation coefficient,PCC)通过本地perl语言进行计算,显著相关共表达基因对的网络显示利用Cytoscape 3.1进行构建。
2 结果
2.1 辣椒HD-Zip基因家族的成员分析和分组鉴定
利用生物信息学方法并经过后续的筛选验证,从辣椒‘遵辣1号’全基因组中共鉴定到42个HD-Zip家族成员,根据染色体顺序依次命名为CaHDZ01—CaHDZ42,其中基因CaHDZ42并没有锚定在染色体(表1)。Table 1
表1
表1辣椒HD-Zip基因家族信息
Table 1
| 基因名称 Gene name | 亚族 Group | 基因组登录号 Gene accession No. | 大小 Size (aa) | 长度 Length (bp) | 染色体位置 Chromosome location | 分子量 Molecular weight (kD) | 等电点 pI | 拟南芥同源蛋白 Arabidopsis homologous | E值 E-value |
|---|---|---|---|---|---|---|---|---|---|
| CaHDZ01 | I | Capana01g000046 | 211 | 636 | Chr01:803719..804778 | 24.44 | 4.83 | ATHB7 | 1.00E-31 |
| CaHDZ02 | II | Capana01g000658 | 282 | 849 | Chr01:12827760..12830218 | 31.94 | 7.26 | ATHB2 | 2.00E-102 |
| CaHDZ03 | IV | Capana01g001104 | 842 | 2529 | Chr01:30759598..30765550 | 93.61 | 4.98 | HDG5 | 0 |
| CaHDZ04 | IV | Capana01g001442 | 764 | 2295 | Chr01:45982654..45987435 | 83.76 | 6.31 | ANL2 | 0 |
| CaHDZ05 | II | Capana01g002526 | 392 | 1179 | Chr01:165755875..165758134 | 42.42 | 7.36 | HAT14 | 1.00E-64 |
| CaHDZ06 | II | Capana01g003482 | 300 | 903 | Chr01:227843358..227845842 | 33.34 | 6.76 | HAT3 | 9.00E-65 |
| CaHDZ07 | I | Capana02g000407 | 219 | 660 | Chr02:53806313..53809076 | 25.62 | 6.28 | ATHB40 | 2.00E-70 |
| CaHDZ08 | II | Capana02g000632 | 241 | 726 | Chr02:79582528..79585428 | 27.00 | 9.36 | HAT22 | 3.00E-73 |
| CaHDZ09 | I | Capana02g000916 | 273 | 822 | Chr02:102327531..102329744 | 31.10 | 5.87 | ATHB3 | 9.00E-51 |
| CaHDZ10 | III | Capana02g001374 | 830 | 2493 | Chr02:123107922..123114705 | 91.73 | 6.17 | ATHB14 | 0 |
| CaHDZ11 | IV | Capana02g002164 | 708 | 2127 | Chr02:141118184..141122121 | 77.85 | 5.97 | PDF2 | 0 |
| CaHDZ12 | I | Capana02g002657 | 215 | 648 | Chr02:148700184..148702221 | 25.03 | 5.26 | ATHB40 | 1.00E-64 |
| CaHDZ13 | II | Capana02g002922 | 272 | 819 | Chr02:152663803..152665091 | 30.28 | 8.15 | HAT22 | 4.00E-96 |
| CaHDZ14 | I | Capana02g003384 | 245 | 738 | Chr02:160009225..160010619 | 28.01 | 5.39 | ATHB13 | 3.00E-61 |
| CaHDZ15 | I | Capana02g003485 | 215 | 648 | Chr02:161300767..161302593 | 24.09 | 4.51 | ATHB1 | 2.00E-55 |
| CaHDZ16 | III | Capana03g000260 | 838 | 2517 | Chr03:3882950..3890673 | 92.06 | 6.46 | ATHB15 | 0 |
| CaHDZ17 | IV | Capana03g000292 | 772 | 2319 | Chr03:4166533..4174964 | 86.44 | 6.80 | GL2 | 0 |
| CaHDZ18 | I | Capana03g001081 | 322 | 969 | Chr03:18412063..18413771 | 37.09 | 4.78 | ATHB1 | 7.00E-42 |
| CaHDZ19 | IV | Capana03g001526 | 720 | 2163 | Chr03:28572926..28576191 | 79.49 | 6.64 | HDG11 | 0 |
| CaHDZ20 | I | Capana03g001926 | 220 | 663 | Chr03:39229362..39230232 | 25.76 | 6.11 | ATHB7 | 1.00E-39 |
| CaHDZ21 | IV | Capana03g002346 | 800 | 2403 | Chr03:61310140..61314456 | 86.93 | 6.27 | ANL2 | 0 |
| CaHDZ22 | I | Capana03g002675 | 178 | 537 | Chr03:99390829..99391365 | 20.60 | 8.16 | ATHB52 | 6.00E-29 |
| CaHDZ23 | I | Capana04g000966 | 294 | 885 | Chr04:23370253..23371908 | 33.69 | 4.77 | ATHB16 | 4.00E-41 |
| CaHDZ24 | I | Capana04g002305 | 211 | 636 | Chr04:195248401..195250017 | 25.13 | 6.98 | ATHB40 | 7.00E-55 |
| CaHDZ25 | I | Capana05g001458 | 222 | 669 | Chr05:129767576..129768389 | 25.69 | 4.92 | ATHB7 | 3.00E-34 |
| CaHDZ26 | I | Capana05g001741 | 284 | 855 | Chr05:172400277..172401713 | 32.24 | 4.26 | ATHB16 | 1.00E-51 |
| CaHDZ27 | IV | Capana06g000834 | 734 | 2205 | Chr06:13187448..13191074 | 80.88 | 6.50 | HDG11 | 0 |
| CaHDZ28 | II | Capana06g001620 | 286 | 861 | Chr06:41280020..41282406 | 32.52 | 8.17 | ATHB2 | 2.00E-93 |
| CaHDZ29 | IV | Capana07g001455 | 777 | 2334 | Chr07:184550371..184557526 | 85.90 | 5.52 | HDG2 | 0 |
| CaHDZ30 | I | Capana07g002156 | 177 | 534 | Chr07:215423716..215424249 | 20.70 | 5.84 | ATHB52 | 9.00E-25 |
| CaHDZ31 | III | Capana08g000475 | 553 | 1662 | Chr08:73848414..73853082 | 61.12 | 7.73 | ATHB8 | 0 |
| CaHDZ32 | I | Capana09g002322 | 245 | 738 | Chr09:236366842..236370358 | 28.43 | 8.01 | ATHB51 | 5.00E-56 |
| CaHDZ33 | IV | Capana10g000585 | 731 | 2196 | Chr10:26552568..26561787 | 80.57 | 5.67 | PDF2 | 0 |
| CaHDZ34 | II | Capana10g002189 | 333 | 1002 | Chr10:200359705..200363261 | 37.16 | 8.65 | HAT14 | 5.00E-69 |
| CaHDZ35 | III | Capana11g000079 | 841 | 2526 | Chr11:2280596..2286141 | 92.17 | 6.15 | IFL1 | 0 |
| CaHDZ36 | I | Capana11g001580 | 278 | 837 | Chr11:181752291..181754489 | 32.10 | 4.54 | ATHB1 | 4.00E-49 |
| CaHDZ37 | I | Capana11g001647 | 311 | 936 | Chr11:187454288..187456636 | 35.61 | 6.00 | ATHB13 | 2.00E-126 |
| CaHDZ38 | II | Capana11g002379 | 152 | 459 | Chr11:219730688..219733084 | 18.09 | 8.51 | ATHB17 | 6.00E-62 |
| CaHDZ39 | III | Capana12g001248 | 486 | 1461 | Chr12:64777481..64784271 | 53.89 | 8.48 | ATHB15 | 0 |
| CaHDZ40 | I | Capana12g002675 | 354 | 1065 | Chr12:225304884..225307563 | 39.57 | 4.20 | ATHB6 | 1.00E-68 |
| CaHDZ41 | IV | Capana12g002821 | 634 | 1905 | Chr12:228410133..228419272 | 71.59 | 6.36 | HDG8 | 2.00E-113 |
| CaHDZ42 | II | Capana00g004586 | 211 | 636 | Chr00:656715560..656716427 | 24.26 | 10.00 | HAT22 | 2.00E-46 |
新窗口打开|下载CSV
辣椒中HD-Zip家族基因长度介于459 bp(CaHDZ38)和2 529 bp(CaHDZ03)之间;分子量从最小18.09 kD(CaHDZ38)到最大93.61 kD(CaHDZ03)不等;等电点介于4.20(CaHDZ40)至9.36(CaHDZ08)之间。因此,HD-Zip基因家族的基因长度跨度很大,且与分子量具有相关性,而pI主要取决于氨基酸中酸性氨基酸和碱性氨基酸的数量比,大多数CaHDZ蛋白(70%)的pI小于7.0,证明其可能是一类酸性蛋白(表1)。
基因序列若高度同源,则可能具有相似的功能。在拟南芥HD-Zip与辣椒的HD-Zip基因家族成员对比结果中可知,大多数辣椒HD-Zip与拟南芥具有高度同源性(E-value=0,表1),为指导辣椒HD-Zip基因家族的生物学功能研究提供了参考。
为进一步了解辣椒HD-Zip基因家族和拟南芥之间的同源关系,构建了辣椒、拟南芥HD-Zip基因家族系统进化树(图1)。由图可知,与拟南芥一样,辣椒HD-Zip基因家族可分为4个亚族(为I、II、III和IV)。在辣椒基因组中这4个亚族分别含有18、9、5、10个HD-Zip,I、II、III亚族数目与拟南芥中类似,其中III亚族基因个数一致,证明这3个亚族HD-Zip并没有在辣椒基因组中大范围变化,而辣椒中IV组基因明显比在拟南芥中减少,可能是在辣椒全基因组复制过程中丢失较多(图1)。
图1
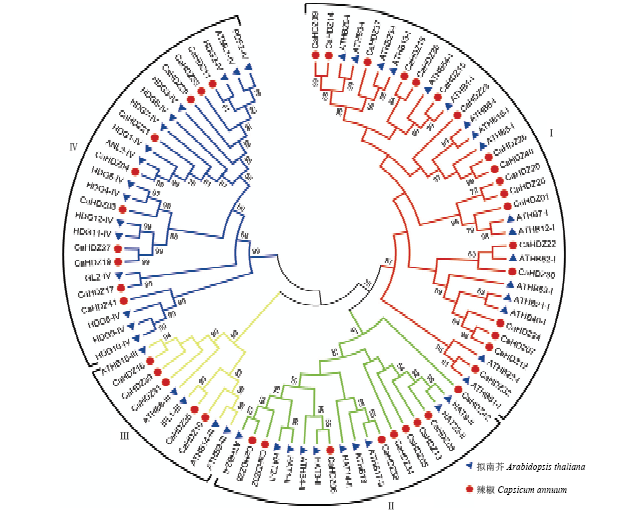 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图1辣椒、拟南芥HD-Zip基因家族系统进化树
Fig. 1The unrooted phylogenetic tree of HD-Zip gene family between pepper and Arabidopsis
2.2 辣椒HD-Zip基因家族的结构特征分析
从图2可以看出辣椒HD-Zip基因家族中4个亚族的基因结构有显著差别。整体看来,I、II亚族的基因编码序列较III和IV亚族结构简单,I亚族外显子数目最少,均为2—3个,II亚族为3—4个,而III、IV亚族成员外显子数目多在10个以上(图2-B)。大多数进化树节支点的基因具有类似的外显子结构,但从基因全长来看,相似的CDS长度却有不同的基因全长,说明内含子长度具有较大的差异性。图2
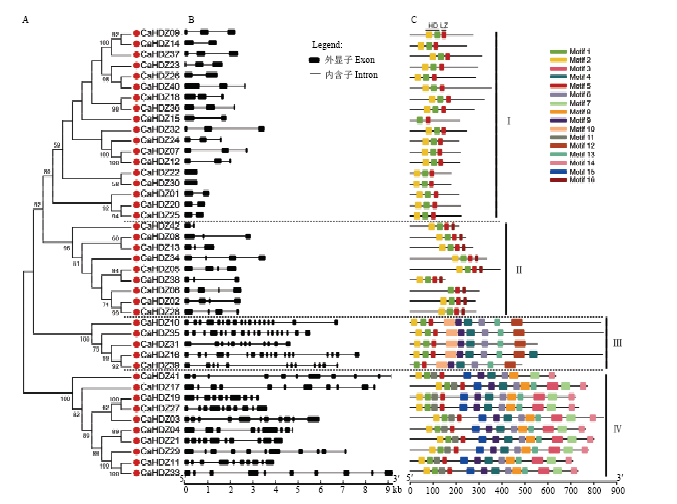 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2辣椒HD-Zip基因家族成员的结构特征
A:系统进化树;B:基因结构;C:蛋白结构域特征 A: Phylogenetic tree; B: Gene structure; C: Protein structure
Fig. 2An analytical view of HD-Zip family in pepper
同时,对辣椒HD-Zip基因家族进行了蛋白保守结构域分析,共鉴定获得16个保守基序(Motif),将这些Motif进行了注释。Motif 1和2对应HD,Motif 3对应LZ。结果表明,辣椒HD-Zip成员均含有HD和Zip结构域,但部分成员的HD结构域并不完整,如第I亚族中CaHDZ15和III亚族CaHDZ39缺失了部分HD结构域(Motif 2)。此外,IV亚族HD结构域中多了Motif 7(图2-C)。从4个亚族的结构来看,与前人一致,I亚族只包含HD和Zip两个结构域;II亚族除CaHDZ38外,motif多集中于序列后半段;III亚族和IV亚族含有另外的结构域,但它们之间并不完全保守(图2-C)。
2.3 辣椒HD-Zip基因家族的染色体定位分析
依据辣椒CaHDZ染色体位置信息,除CaHDZ42外,剩下41条基因不均匀地分布在12条染色体上(图3)。其中1号、2号、3号染色体上分布的基因较多,分别有6条、9条和7条。2号染色体上的基因大多分布在其下端,3号染色体的基因大多分布在其上端,8号和9号染色体上最少,均只分布有1条HD-Zip家族基因,其余染色体在2—4条。通过4个亚族基因在染色体上分布情况比较,发现I亚族基因主要集中在2号和3号染色体上,其余亚族成员不均等分布在染色体上。部分染色体仅有单个亚族的成员,比如4号、5号和9号仅有I亚族基因,8号染色体仅有III亚族基因,推测在辣椒三倍化快速扩增过程中并未均等的发生片段复制,或者复制后HD-Zip丢失较多。图3
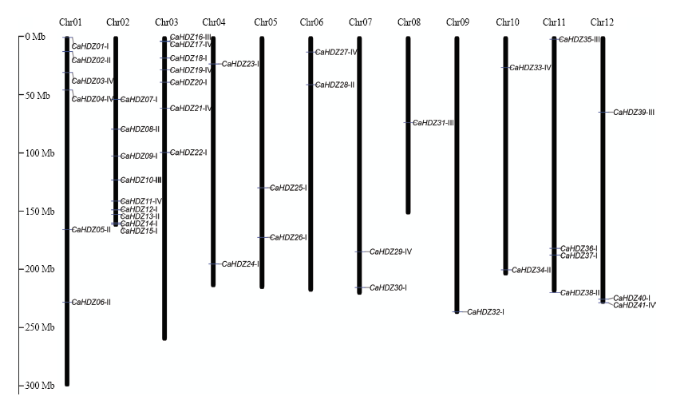 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图3HD-Zip在辣椒染色体上的位置
Fig. 3The chromosome location of the HD-Zip genes in pepper
此外,通过MCScanX及下游程序对所有基因进行共线性和复制基因分析,结果表明,CaHDZ01/ CaHDZ20、CaHDZ12/CaHDZ24、CaHDZ26/CaHDZ40、CaHDZ10/CaHDZ27都发生了片段复制。片段复制使得基因数目增多,特别是I亚组基因数目的增加。
2.4 辣椒、番茄和拟南芥HD-Zip直系、旁系同源基因的鉴定
在对辣椒、番茄和拟南芥3个物种内部直、旁系同源基因的对比研究中(图4),发现在3个物种中直系同源基因对都很多,这可能是由于HD-Zip序列极度保守和相似。在表1中,辣椒和拟南芥HD-Zip的比对结果也表明大部分基因对的E值都很小,甚至为0,证明这类基因极保守,特别是第III亚组基因。此外,通过比较3个物种中的直系同源基因对数目,发现直系同源基因对大体相同,但辣椒和番茄之间的稍多于其他组,表明辣椒与番茄两物种间的基因相似度高,有较高的保守性。这也与辣椒和番茄的亲缘关系相一致,一般亲缘关系越近,两物种间的同源基因对就越多。而旁系同源基因的鉴定结果则表明,拟南芥中要明显多于番茄和辣椒,辣椒中最少,说明辣椒基因组的倍增事件并没有导致HD-Zip的明显扩增,或者是基因组复制后基因丢失较多。图4
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图4拟南芥、番茄和辣椒的直系及旁系同源HD-Zip的分布
Fig. 4Circle plots of paralogous and orthologous HD-Zip pairs between Arabidopsis thaliana, Solanum lycopersicum and Capsicum annuum
2.5 HD-Zip基因家族进化特征分析
为进一步明确HD-Zip基因家族进化特征,分别选取无油樟(Amborella trichopoda)、水稻(Oryza sativa)[19]、玉米(Zea mays)[19]、番茄(Solanum lycopersicum)[17]、马铃薯(Solanum tuberosum)[27]、辣椒‘CM334’、辣椒‘Zunla-1’、毛果杨(Populus trichocarpa)[28]、葡萄(Vitis vinifera)[18]以及拟南芥[1]9个代表物种进行分析(表2、图5)。与孑遗植物无油樟相比,HD-Zip在其余8种植物中具有不同程度的倍增(表2),证明其在不同的进化过程中被不均等的复制保留下来。系统进化树分析表明,包含无油樟在内这9个物种的HD-Zip序列不均等的分布在4个亚族中,说明从被子植物开始,HD-Zip基因家族就稳定存在4个亚族。在这9个物种中,I亚族含有最多的数目,而III数目最少(图5-A),证明在被子植物全基因组复制过程中I亚族复制保留的基因最多,而III亚族基因没有发生复制或复制后丢失。这也侧面证明III亚族基因可能相对比较保守。Table 2
表2
表2HD-Zip在不同物种中数目情况统计
Table 2
| 物种 Species | 亚族 Group | 总和 Sum | |||
|---|---|---|---|---|---|
| I | II | III | IV | ||
| 无油樟Amborella trichopoda | 8 | 6 | 3 | 4 | 21 |
| 水稻Oryza sativa | 14 | 13 | 9 | 12 | 48 |
| 玉米Zea mays | 17 | 18 | 5 | 15 | 55 |
| 番茄Solanum lycopersicum | 24 | 11 | 6 | 17 | 58 |
| 马铃薯Solanum tuberosum | 15 | 11 | 7 | 10 | 43 |
| 辣椒Capsicum annuum cv. CM334 | 19 | 10 | 5 | 11 | 45 |
| 辣椒Capsicum annuum cv. Zunla-1 | 18 | 9 | 5 | 10 | 42 |
| 毛果杨Populus trichocarpa | 21 | 17 | 8 | 17 | 63 |
| 葡萄Vitis vinifera | 13 | 7 | 5 | 8 | 33 |
| 拟南芥Arabidopsis thaliana | 17 | 10 | 5 | 16 | 48 |
新窗口打开|下载CSV
图5
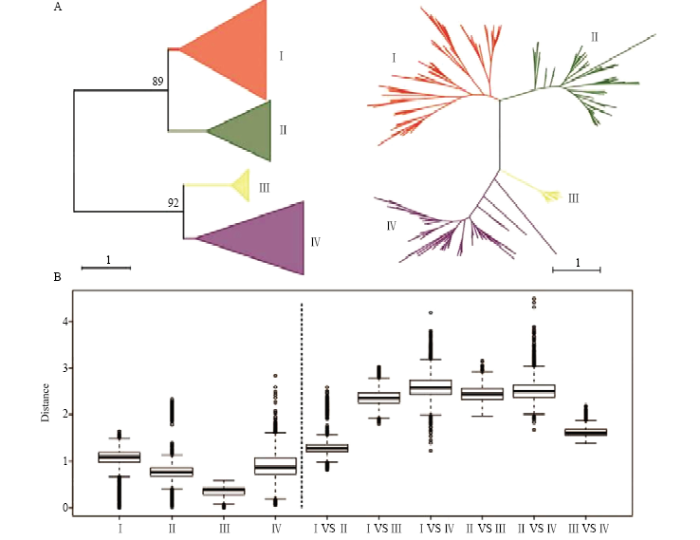 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图5HD-Zip基因家族4个亚族之间的关系
A:系统进化树;B:4个亚族核苷酸差异比较盒形图
Fig. 5Phylogenetic relationship of HD-Zip gene family and characteristic of the four groups
A: Phylogenetic trees; B: Boxplot of the nucleotides distance among four HD-Zip gene family groups
通过系统进化树来看,I和II亚族具有较近的亲缘关系,而III和IV亚族亲缘关系较近(图5-A)。为研究这4个亚族基因之间的亲缘关系,分别鉴定了它们之间的核苷酸差异。从图5-B中可以看出,III亚族基因内部的核苷酸差异最小,证明该亚族基因非常保守,与前期结果一致。I亚族基因的平均核苷酸差异最大,但与II和IV亚族并未有明显差异。II和IV亚族基因内部的核苷酸差异则更加分散,证明II和IV亚族基因发生了明显的分化。从不同亚族之间的差异来看,I和II亚族基因之间核苷酸差异最小,表明I和II亚族亲缘关系最近,其次是III和IV亚族。根据结果可以推测最先存在的HD-Zip基因家族可分为两组,其中一组分化成I和II亚族,而另一组则分化成为III和IV亚族。
2.6 辣椒HD-zip基因家族在不同组织中表达模式分析
对42个辣椒HD-Zip在根、茎、叶、花芽、花和果实不同发育时期的表达模式进行分析。结果显示,该家族基因的4个亚族具有不同程度的表达趋势,其中I亚族中的基因在辣椒不同组织中的表达量相对较高,且亚族内部呈现出不同的表达模式,近一半基因在辣椒不同组织及果实发育前期均具有较高的表达量,证明这部分基因对辣椒的生长发育,特别是果实成熟前期具有重要的作用(图6)。其中,CaHDZ22在茎中的表达程度最强,表明该基因可能对辣椒茎的生长有重要作用(图6)。较I亚族相比,II、III和IV亚族基因在不同组织中的表达量相对较低,但部分基因在特定组织中具有较大的表达量,例如CaHDZ13在根、茎、芽、叶、花和果实成熟前期具有较高的表达量,CaHDZ34在辣椒果实成熟后期具有较大的表达量,CaHDZ02和CaHDZ28在果实刚刚膨大时具有较高的表达量,CaHDZ04在果实成熟前期具有较大的表达量,证实这些基因在辣椒的特定时期均具有重要的作用(图6)。此外,CaHDZ09、CaHDZ42和CaHDZ41这3个基因在根、茎、芽、叶、花和果实成熟过程中均不表达。图6
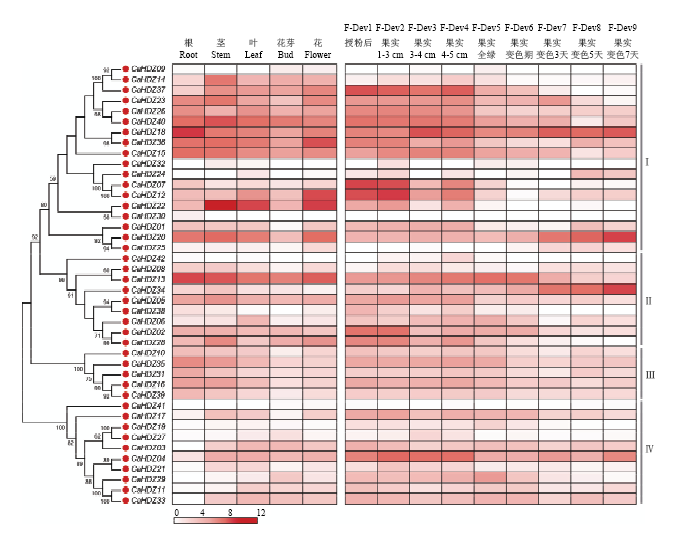 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图6辣椒HD-Zip在不同组织及果实发育过程中的表达分析
Fig. 6Expression profile analysis of pepper HD-Zip genes in different tissues and fruit development
此外,I亚族中大多数基因在根、茎、芽、叶和花中的表达程度相差不多。为了更好地了解辣椒HD-Zip及其同源基因之间的表达差异,通过筛选皮尔森相关系数(PCC,P<0.05)显著共表达基因对,构建了辣椒HD-Zip表达网络(图7)。该网络包含35个节点(基因)和87个边(调控关系),有33对基因表达趋势PCC大于0.8,6对大于0.9,CaHDZ14/ CaHDZ22及CaHDZ07/CaHDZ02之间的PCC达到0.96。虽然在不同组织中表达有强有弱,但具有明显共表达趋势。除了正向协同,另外有9对CaHDZ之间为负调控关系。以上结果表明HD-Zip在调控植物生长发育过程中起到了重要的协同作用,并且不同亚族之间也具有一定的协同性(图7)。
图7
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图7辣椒HD-Zip共表达网络
Fig. 7Co-expression network of HD-Zip genes in pepper
3 讨论
植物转录因子通过其特有结构域与DNA及其他蛋白或转录因子间的相互作用,激活或抑制基因的表达来调控植物正常的生理过程或应激反应[3]。HD-Zip蛋白是植物界所特有的一类转录因子,包含4个亚族,而不同亚族的结构域差异又决定了其功能的多样性[1]。随着分子生物学技术的发展,模式植物拟南芥中的HD-Zip家族成员功能均已被解析,证实不同亚族间确实存在多样性的功能[1,4,8,12]。但在进化过程中,随着不同物种经历的不同复制选择事件,同源基因发生不同程度的分化,常见的是产生次功能(Subfunctionalization)、产生新功能(Neofunctionalization)和丢失复制基因或功能冗余这3种类型[29]。HD-Zip基因家族目前已经在多个植物中被详细鉴定,包括拟南芥[1]、玉米[19]、葡萄[18]、毛果杨[28]等。研究结果表明该家族成员具有较高的系统发育相似性,但是在不同物种中表现出不同的时空表达模式,并具有明显的组织差异性表达,对植物生长发育的调控也存在功能分化和冗余的现象。此外,尽管感知同样的环境胁迫因子,但是不同成员在同样的环境胁迫下的调控方式并不相同[1,30]。辣椒基因组经历了快速三倍化扩增[20,21],给研究重要基因复制分化提供了很好的基础。本研究从我国自主选育的辣椒‘遵辣1号’基因组中鉴定获得42条HD-Zip,在‘CM334’中鉴定得到45条HD-Zip,经过FGENESH对基因序列进行手动矫正和重新注释,最终确定以‘遵辣1号’基因组为主要研究对象。42条HD-Zip中除了1条没有被锚定在染色体上,剩下41条不均等地分布在辣椒12条染色体上。通过共线性分析,发现片段复制是CaHDZ基因家族扩增的主要原因,这和马铃薯、拟南芥一致[1,27]。CaHDZ基因家族4个亚族成员的数目并不均等,I亚族最多且主要集中在2号染色体上,III亚族最少,这和拟南芥中的类似[1]。辣椒中IV亚族发生了丢失,但在拟南芥中,IV亚族保留的较多。同时,I亚族发生片段复制的基因数量最多,这可能是I亚族基因数目最多的原因。III亚族基因相对比较稳定,并未发生复制事件或复制后丢失。在所选的9个代表物种中,同样发现I亚族扩增最为明显。特别是在茄科植物中,I亚族基因数目占比达到40%以上。IV亚族基因在被子植物中也发生了比较明显的扩增,但在‘遵辣1号’中该亚族基因数目占比只有24%,发生了明显的丢失。III亚族在多个物种中均只有5条基因,相对比较保守。核苷酸差异分析结果表明III亚族基因内部的核苷酸差异确实最小,证明在物种进化过程中III亚族基因的选择压力比较小,因此基因也比较保守;而剩下3个亚族核苷酸差异较大,特别是I亚族,且差异比较分散。可以推测在进化过程中这3个亚族的基因,具有较大的选择压力,更容易进化出新的功能[29,31]。通过不同亚族之间的差异来看,I和II亚族亲缘关系最近,其次是III和IV亚族。由此推测I和II亚族、III和IV亚族可能分别从相同的祖先分化而来,或者IV亚族是从III亚族分化而来。
基因结构是研究基因功能和进化的重要依据,本研究详细分析了辣椒HD-Zip基因家族的结构特征和保守结构域。辣椒HD-Zip同一亚族的基因,其结构相似。从外显子数目来看,I亚族最少,III亚族最多,这和玉米[19]、毛果杨[28]等一致。III和IV亚族基因长度显著长于I和II组,证明其有更加复杂的结构特征,保守结构域分析也印证了这一点。I和II亚族基因的保守结构域基本只包含了特有的HD和Zip结构域,而III和IV保守基序更加复杂。III亚族中还包含START、SAD和MEKHLA结构域,而IV亚族则包含START和SAD结构域[1,8,12],这与前人研究一致[1,6,13]。此外,III和IV亚族中的START和SAD结构域在两组间并不完全保守,而在亚族内部很保守,可能在功能上也具有不同的表达模式。
辣椒HD-Zip存在明显的组织差异性表达,I亚族差异最为明显,而III亚族差异最小。这也证实了上面的推测,I亚族确实发生了明显的功能分化,在不同物种中可能参与更多的代谢与发育过程[4]。I亚族基因在黄瓜中可以响应多种环境信号[32],烟草NaHD20可以调控花的发育[33],蒺藜苜蓿中HB1在一定条件下可诱导其在初生根和侧根中表达[34]。在辣椒中,发现I亚族基因在茎中表达的基因最多,且表达量最大,特别是CaHZD22在茎中具有最高的表达,证明该类基因对辣椒茎的发育起到重要作用。此外,CaHZD18在根中表达量最大,CaHZD12和CaHZD22在花中表达量最大,CaHZD12和CaHZD07在果实成熟前期表达量最大,CaHZD18和CaHZD20在果实成熟后期有较大表达量,证明该亚族基因对辣椒的形态建成和果实发育具有重要的作用。虽然辣椒I亚族发生了明显的功能分化,但和拟南芥直系同源相比,仍具有一定的功能相似性,ATHB1、ATHB3、ATHB16和ATHB20[4-5,35-36]参与叶片生长发育过程,CaHZD15、14和40在叶片中具有较高的表达量,可能参与了叶发育过程。辣椒中III亚族基因变化趋势并不显著,说明在不同组织发育和果实发育过程中功能分化并不明显。通过和拟南芥中同源基因相比也具有一定的相似性,拟南芥该组基因主要在植物发育过程和维管发育中起作用[8],辣椒中该基因也在植物组织中特别是茎中具有高表达。另外,辣椒的II和IV亚族基因也发生了不同程度分化,虽然HD-Zip在辣椒中发生了明显的表达分歧,但其仍有一定的共表达趋势,证明其在调控植物生长发育过程中起到了重要的协同作用。此外,为维护植物的正常生长发育,同一家族基因会存在一些抑制性表达调控。
4 结论
本研究在辣椒中共鉴定到42条HD-Zip,根据进化关系和结构特征分为4个亚族,不同亚族的基因结构、蛋白保守结构域及表达模式不同;CaHZD不均等地分布在12条染色体上,并有多个基因发生了片段复制;在进化历程中,CaHZD保守性高,数目没有明显倍增,III亚族最为保守,I和II亚族、III和IV亚族亲缘关系更近;CaHZD具有明显的组织差异性表达,协同调控了辣椒的生长发育。参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[本文引用: 15]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 5]
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
[本文引用: 4]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 3]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 3]
[本文引用: 5]
[本文引用: 2]
[本文引用: 3]
URL [本文引用: 1]
URL [本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 3]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
