鲍根生1,2

 , 宋梅玲1,2, 王玉琴1,2, 李春杰3
, 宋梅玲1,2, 王玉琴1,2, 李春杰3 1. 青海大学畜牧兽医科学院, 青藏高原优良牧草种质资源研究重点实验室, 青海 西宁 810016;
2. 青海大学省部共建三江源生态与高原农牧业国家重点实验室, 青海 西宁 810003;
3. 兰州大学草地农业科技学院, 草地农业生态系统国家重点实验室, 甘肃 兰州 730020
收稿日期:2019-04-03;修回日期:2019-07-01;网络出版日期:2019-11-12
基金项目:国家自然科学基金(31660690,31700098);青海省“高端创新人才****”拔尖人才培养计划;青藏高原优良牧草种质资源研究重点实验室(2017-ZJ-Y12)
*通信作者:鲍根生, Tel/Fax:+86-971-8128271;E-mail:baogensheng2008@hotmail.com.
摘要:[目的] 甘肃马先蒿与感染内生真菌的禾草(紫花针茅和麦宾草)建立根寄生关系,有关内生真菌对根寄生危害禾草光合作用调控方面的研究较少。[方法] 本研究以紫花针茅和麦宾草带菌(E+)、不带菌(E-)植株为研究对象,研究甘肃马先蒿寄生和未寄生处理对紫花针茅和麦宾草E+、E-植株不同生长阶段光合特性影响的动态变化。[结果] 甘肃马先蒿寄生显著降低紫花针茅和麦宾草的净光合速率、蒸腾速率和气孔导度,而胞间二氧化碳浓度和水分利用率却显著增加,这与禾草是否感染内生真菌无关。甘肃马先蒿寄生后E+紫花针茅的净光合速率、气孔导度和蒸腾速率高于E-植株,而麦宾草E+植株的净光合速率、气孔导度和蒸腾速率却低于E-植株;同时,根寄生条件下E+紫花针茅的胞间二氧化碳浓度和水分利用率低于E-植株;而E-麦宾草植株的胞间二氧化碳浓度和水分利用率却低于E+植株。[结论] 内生真菌侵染影响甘肃马先蒿根寄生危害禾草的光合作用;甘肃马先蒿和内生真菌同时成为禾草营养消耗库时,内生真菌与禾草的共生关系处于一种互惠共生和相互拮抗的动态变化。
关键词:甘肃马先蒿紫花针茅冷季型禾草内生真菌根寄生植物光合作用互惠共生拮抗
Effects of Pedicularis kansuensis parasitism on the photosynthetic characteristics of host grass-Epichlo? symbionts
Gensheng Bao1,2

 , Meiling Song1,2, Yuqin Wang1,2, Chunjie Li3
, Meiling Song1,2, Yuqin Wang1,2, Chunjie Li3 1. Key Laboratory of Qinghai-Tibet Plateau Forage Germplasm Research, Academy of Animal and Veterinary Medicine, Qinghai University, Xining 810016, Qinghai Province, China;
2. State Key Laboratory of Plateau Ecology and Agriculture, Qinghai University, Xining 810003, Qinghai Province, China;
3. State Key Laboratory of Grassland Agro-ecosystems, College of Pastoral Agriculture Science and Technology, Lanzhou University, Lanzhou 730020, Gansu Province, China
Received: 3 April 2019; Revised: 1 July 2019; Published online: 12 November 2019
*Corresponding author: Bao Gensheng, Tel/Fax:+86-971-8128271;E-mail:baogensheng2008@hotmail.com.
Foundation item: Supported by the National Natural Science Foundation of China (31660690, 31700098), by the Program for Qinghai Province Thousand Talent Innovative Plan, and by the Key Laboratory of Superior Forage Germplasm in the Qinghai-Tibetan Plateau (2017-ZJ-Y12)
Abstract: [Objective] Pedidcularis kansuensis forms parasitic relationship with Epichlo?-infected host grasses through root haustoria connections. However, only few studies have paid attention to the effects of Epichlo? endophyte on host grass photosynthetic characteristics while the host grasses were parasitized by root hemiparasitic plants. [Methods] Thus, in this study, we evaluated effects of endophyte infection on net photosynthesis rate (Pn), transpiration rate (Tr), stomatal conductance (Gs), concentration of CO2 intercellular (Ci) and water use efficiency (WUE) of two host grasses (Stipa purpurea and Elymus tangutorum) in the presence (or absence) of P. kansuensis. [Results] Irrespective of endophyte status, Pn, Tr and Gs of host plants decreased in the presence of P. kansuensis; however, Ci and WUE of host plants increased in the presence of P. kansuensis. Pn, Tr and Gs of endophyte-infected (E+) S. purpurea were higher than endophyte-free (E-) counterpart, while Ci and WUE of E+ S. purpurea were lower than E- ones. By contrast, Pn, Tr and Gs of E+ E. tangutorum was lower than E- counterpart, while Ci and WUE of E+ E. tangutorum higher than E- ones. [Conclusion] Consequently, these results suggest that interactions between endophyte and host grasses are context-dependent, and the relationships between host grass and Epichlo? endophyte range from mutualism to parasitism when grasses become common hosts to root hemiparasitic plant and Epichlo? endophyte.
Keywords: Pedicularis kansuensisStipa purpureacool-seasonal grassEpichlo? endophyteroot hemiparasitephotosynthesismutualismantagonism
草地生态系统内各组成单元间的关系是一个持续变化的过程,影响草地群落结构和物种组成的关键限制因素主要有草食动物、病原真菌和与植物建立共生关系微生物及非生物因素[1]。目前,有关植物生理生态方面的研究主要聚焦于生物和非生物因子及多个因素叠加效应对植物种群适应性或植物群落结构组成和生态功能等方面的影响[2];有关3个或更多营养级间相互影响的研究较少。植物共生微生物通过增强宿主对非生物逆境耐受能力和降低有害生物的侵害频率,从而提高宿主与其他物种间的竞争能力,并最终增加种群数量和扩大分布范围。基于此,有关宿主与共生微生物间互利共生关系研究成为现阶段植物和微生物间互作研究的热点研究内容[3]。
禾草内生真菌是指在禾草体内度过整个或大部分生命周期,而禾草不表现外部症状的一类真菌。禾草生殖生长阶段,内生真菌侵染禾草种子的种皮和糊粉层,种子传播成为内生真菌由母系植株向子代传播的主要传播途径[4]。内生真菌与冷季型禾草经自然选择和长期协同进化过程建立了互利共生关系:一方面内生真菌提高禾草对非生物逆境的耐受力,例如在干旱或营养贫瘠条件下,内生真菌侵染显著增加禾草种子萌发和幼苗存活能力;同时,内生真菌降低草食家畜和病原微生物对禾草的采食和侵染,这主要与内生真菌合成易造成家畜中毒的生物碱有关[5-6]。另一方面,禾草为内生真菌提供生长和繁殖所需的全部营养物质,同时禾草种子也是内生真菌传播的主要媒介[7]。以往研究主要关注内生真菌提高禾草生长、内生真菌分类地位和生物碱合成途径等方面[8];然而,有关内生真菌如何调控禾草和其他植物间竞争及带菌禾草种群扩张等方面的研究较少[9]。
根寄生植物是被子植物中一类寄生于寄主根部,掠夺寄主体内水分、碳水化合物和营养物质的特殊植物类群,广泛分布于草地、森林、农田等各类生态系统[10]。根寄生植物利用特殊功能器官——吸器直接从寄主体内获取营养物质,加快自身生长和繁殖,从而抑制寄主生长[11]。由于全球气候变化、啮齿动物挖掘破坏和人类不合理活动等因素的综合作用,导致青藏高原地区高寒草地呈大面积退化态势[12]。甘肃马先蒿(Pedicularis kansuensis)是一种根部半寄生植植物,成为高寒草地重度退化阶段的主要本地入侵性杂草种类,在紫花针茅(Stipa purpurea)和麦宾草(Elymus tangutorum)为优势禾草的高寒草原大面积滋生且呈“斑块”状集群分布[13]。鲍根生等调查发现青海高原天然草地中紫花针茅和麦宾草感染内生真菌水平较高[14-15]。根寄生植物与寄主建立寄生关系后,主要抑制寄主的光合作用和水分利用率,造成寄主生物量积累降低,导致寄主处于营养胁迫的生物逆境[16]。与根寄生植物对禾草的寄生伤害相反,内生真菌提高宿主在生物和非生物逆境条件下禾草的光合作用能力,缓解或提高禾草对逆境的耐受能力[17]。如果禾草同时成为根寄生植物和内生真菌共同寄主时,内生真菌侵染能否通过调控禾草的光合能力对根寄生危害过程作出响应并增强禾草对根寄生胁迫的耐受能力呢?基于上述科学问题的假设,以感染(E+)、未感染(E-)紫花针茅和麦宾草为研究对象,通过比较甘肃马先蒿寄生的E+、E-紫花针茅和麦宾草植株在不同寄生阶段的光合参数变化,探讨根寄生植物寄生和内生真菌侵染对禾草光合特性的影响,明晰内生真菌侵染对禾草光合作用过程和产物的潜在调节作用,为有效利用内生真菌-禾草共生体这一特殊生物资源作为生物防控手段来控制根寄生杂草提供新思路。
1 材料和方法 1.1 试验地概况及供试种子来源
1.1.1 试验地概况: 试验地位于青海省海北藏族自治州海晏县托勒村(37°06′54.78″N,100°70′88.00″E),草地类型为草甸化草原。草地建群种为矮嵩草(Kobresia humilis),主要伴生禾草为紫花针茅、高原早熟禾(Poa alpigena)和麦宾草,土壤类型为栗钙土。由于放牧强度较强(4只藏羊/ha),造成矮嵩草和伴生禾草盖度降低,而甘肃马先蒿盖度高于20%,成为草地群落优势种[13]。
1.1.2 供试种子来源: 2012年10月在试验点按照单株采集方法,分别收集紫花针茅和麦宾草种子,并随机收集成熟甘肃马先蒿植株的种子。参照李春杰等(2004)方法,检测紫花针茅和麦宾草植株带菌率。具体步骤为:用浓度5%氢氧化钠溶液浸泡禾草种子24 h,剥离软化种子种皮并用苯胺蓝染液染色,光学显微镜20倍视野下检查内生真菌菌丝分布情况[18]。另外,挑选部分带菌种子分别用75%酒精和1%次氯酸钠进行表面消毒后,摆放到马铃薯葡萄糖琼脂(PDA)培养基上,22 ℃黑暗条件下培养数周。种子表面长出菌落后,用接菌针挑取少量菌丝进行纯培养。4周后观测菌落形态、分生孢子和分生孢子梗,从形态特征判断符合Epichlo?属内生真菌特征。另外,利用管家基因(tubβ、tefα、actin)扩增基因片段并构建系统发育树,最终将紫花针茅和麦宾草感染的内生真菌鉴定为Epichlo? inebrians和Epichlo? bromicola [14-15]。不带菌植物种子获取方法为:一半带菌植株种子用3%甲基托布津浸泡8 h,去离子水清洗种子表面残留杀菌剂溶液并在室温条件下晾干[19]。细砂和黄绵土持续8 h高温灭菌处理后,按1:1比例充分混匀后装入体积250 cm3花盆。4粒带菌(E+)、不带菌(E-)禾草种子分别播种于花盆中,播种深度为2 cm。将花盆随机摆放于兰州大学草地农业科技学院智能温室苗床,白天、夜晚温度分别设定为25 ℃和20 ℃及自然采光的种子发芽和幼苗培育环境。2013年5月中旬,将幼苗移栽到试验田。种子成熟后,分别收集自然带菌和杀菌剂处理不带菌植株种子,并按李春杰等(2004)方法重新检测E+和E-种子带菌率[18]。检测结果表明,E+种子内生真菌侵染率高达100%,而紫花针茅和麦宾草E-种子内生真菌侵染率分别为2%和4%。E+、E-和甘肃马先蒿种子存放在4 ℃冰箱内备用。
1.2 试验设计 将400粒紫花针茅和麦宾草E+、E-种子放置在光照培养箱内进行发芽试验,待种子发芽后,将4粒E+、E-发芽种子分别移栽到6 L花盆。花盆中装入灭菌的细砂和栗钙土混合物,混合比例为9:1。将花盆按随机摆放到温室苗床上,设定白天25 ℃和夜晚20 ℃及自然采光的幼苗培育环境。紫花针茅和麦宾草幼苗长至5 cm高度,在距离幼苗四周2.0-2.5 cm处移栽4粒已发芽的甘肃马先蒿种子。每天观察甘肃马先蒿生长状态,发现甘肃马先蒿幼苗快速生长,判定甘肃马先蒿与紫花针茅或麦宾草建立寄生关系[20]。每周用自来水浇灌花盆保持表层湿润,同时每周添加50 mL Hogland营养液,营养液配方参照宋梅玲等的方法[21]。本试验包括8个处理组合:(1) E+ × P表示1株带菌紫花针茅或麦宾草幼苗与1株甘肃马先蒿建立寄生关系;(2) E-× P表示1株不带菌紫花针茅或麦宾草幼苗与1株甘肃马先蒿建立寄生关系;(3) E+表示带菌紫花针茅或麦宾草幼苗;(4) E-表示不带菌紫花针茅或麦宾草幼苗。每个处理重复20次,总计160盆。
1.3 光合作用参数测定 采用LI-6400便携式光合仪在甘肃马先蒿寄生E+、E-紫花针茅和麦宾草植株第10、20、30、40、50、60天,9:00-11:00分别测定供试禾草叶片光合作用参数的动态变化,叶室选用标准簇状叶室。由于紫花针茅叶片为针状叶,随机挑选5片新鲜叶片通过扫描仪获得图片,按照叶面积计算程序求算总投影面积即为紫花针茅叶面积[22];而麦宾草叶片较宽只随机挑选1片叶片通过叶面积扫描仪计算麦宾草叶面积。光合作用测定指标主要为:净光合速率(Pn)、气孔导度(Gs)、蒸腾速率(Tr)和胞间二氧化碳浓度(Ci)。各测定指标的计算参考von Caemmerer和Farquhar的方法[23]。气体交换时叶室内测定条件为:内置LED红蓝光二极管提供光源,光照强度1000 μmol/(m2·s),叶室内CO2浓度和气流速度分别为360 μmol/mol和500 mol/s,叶片温度30 ℃。上述各项设定参数处于稳定状态时,测定并保存Pn、Gs、Tr和Ci。为消除叶片个体大小对光合作用指标测定产生的系统内部差异,紫花针茅选择5片叶片开展且长度相近的叶片,麦宾草选择1片生长健康且完全开展的叶片,每次挑选5盆用于测定光合作用指标。
1.4 统计分析 采用一般线性模型中重复测量方差分析甘肃马先蒿寄生处理、禾草感染内生真菌状态、不同寄生阶段(不同天数)及三者间互作效应对紫花针茅和麦宾草光合作用指标的影响。其中,禾草带菌状态和甘肃马先蒿寄生处理为固定变量,不同寄生时间为内部变量因子,Pn、Gs、Tr、Ci和WUE为因变量。采用独立样本T检验比较同一测定时间对照和寄生处理组内E+、E-植株之间光合作用指标差异。采用SPSS 11.0分析软件对数据进行分析。
2 结果和分析 2.1 甘肃马先蒿寄生对E+、E-紫花针茅和麦宾草净光合速率的影响 内生真菌带菌状态、甘肃马先蒿寄生处理和不同寄生时间对紫花针茅和麦宾草净光合速率有显著影响,甘肃马先蒿寄生处理和不同寄生时间之间出现明显的互作效应(表 1)。整个试验期内,紫花针茅、麦宾草净光合速率总体呈“降-升-降”变化;甘肃马先蒿寄生30 d紫花针茅净光合速率出现最低值(图 1-A),而麦宾草净光合速率出现最高值(图 1-B);甘肃马先蒿寄生第10、30、40、50天,E-植株净光合速率显著高于E+植株(图 1-B,P<0.01);而紫花针茅被寄生后第30、50、60天E+净光合速率却显著高于E-植株(图 1-A,P<0.05)。甘肃马先蒿未寄生状态下,紫花针茅和麦宾草净光合速率随生长时间增加呈先增加后降低变化,紫花针茅E+和E-间差异不显著(图 1-A,P>0.05),而麦宾草E+植株净光合速率显著高于E- (图 1-A,P<0.05)。
表 1. 内生真菌侵染状态(E)和甘肃马先蒿寄生处理(P)在不同寄生天数(D)对麦宾草和紫花针茅光合作用参数的重复度量方差分析结果 Table 1. Results of repeated measure ANOVA for the effects of endophyte infection status of host grasses (E), Pedicularis kansuensis parasitism (P) and different parasitized days (D) on photosynthetic parameters (including: net photosynthesis rate (Pn), transpiration rate (Tr), stomatal conductance (Gs), concentration of CO2 intercellular (Ci) and water use efficiency (WUE)) of Elymus tangutorum and Stipa purpurea
| Species | Treatments | d.f | Pn | Tr | Gs | Ci | WUE | |||||||||
| F | P | F | P | F | P | F | P | F | P | |||||||
| Elymus tangutorum | E | 1 | 30.29 | <0.01 | 9.43 | 0.02 | 25.80 | <0.01 | 12.05 | <0.01 | 5.22 | 0.05 | ||||
| P | 1 | 298.5 | <0.01 | 96.70 | <0.01 | 572.8 | <0.01 | 282.6 | <0.01 | 100.9 | <0.01 | |||||
| D | 5 | 52.07 | <0.01 | 538.1 | <0.01 | 31.06 | <0.01 | 54.86 | <0.01 | 178.9 | <0.01 | |||||
| E×P | 1 | 2.41 | 0.16 | 0.22 | 0.65 | 0.77 | 0.62 | 5.79 | 0.04 | 1.391 | 0.26 | |||||
| E×D | 5 | 1.62 | 0.18 | 3.69 | 0.12 | 0.96 | 0.34 | 1.33 | 0.40 | 4.65 | 0.08 | |||||
| P×D | 5 | 17.84 | <0.01 | 120.7 | <0.01 | 1.99 | 0.26 | 5.28 | 0.07 | 13.65 | 0.01 | |||||
| E×P×D | 5 | 0.42 | 0.83 | 9.40 | 0.03 | 0.24 | 0.92 | 0.84 | 0.58 | 3.24 | 0.14 | |||||
| Stipa purpurea | E | 1 | 46.33 | <0.01 | 11.69 | <0.01 | 254.4 | <0.01 | 23.36 | <0.01 | 9.09 | 0.02 | ||||
| P | 1 | 391.4 | <0.01 | 86.34 | <0.01 | 12.32 | <0.01 | 57.88 | <0.01 | 125.2 | <0.01 | |||||
| D | 5 | 134.2 | <0.01 | 45.02 | <0.01 | 73.54 | <0.01 | 79.12 | <0.01 | 6.38 | 0.05 | |||||
| E×P | 1 | 11.32 | 0.01 | 0.02 | 0.80 | 0.29 | 0.60 | 5.16 | 0.05 | 0.13 | 0.73 | |||||
| E×D | 5 | 3.92 | 0.11 | 60.40 | <0.01 | 7.72 | 0.04 | 0.27 | 0.91 | 0.53 | 0.75 | |||||
| P×D | 5 | 45.87 | <0.01 | 42.24 | <0.01 | 0.30 | 0.89 | 4.41 | 0.09 | 0.44 | 0.80 | |||||
| E×P×D | 5 | 3.51 | 0.12 | 2.93 | 0.16 | 1.81 | 0.29 | 7.57 | 0.04 | 0.97 | 0.53 | |||||
| The F value indicates the ratio of the variance of the group means to that of the pooled within group variance, the P value indicates the significant level. | ||||||||||||||||
表选项
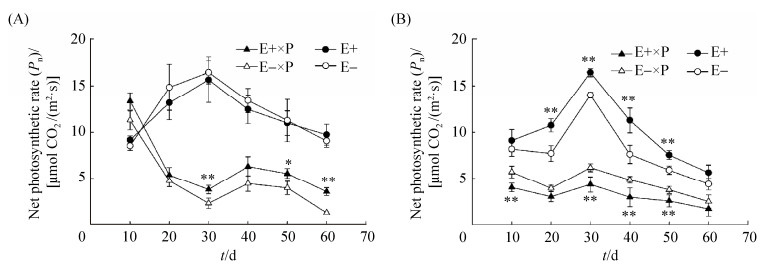 |
| 图 1 甘肃马先蒿寄生不同时间紫花针茅和麦宾草E+、E-植株净光合速率变化 Figure 1 Effects of Pedicularis kansuensis parasitism on Stipa purpurea (A) and Elymus tangutorum (B) net photosynthesis rate (Pn) between E+ and E- during different parasitized days. Asterisks (*, **) indicated mean significant difference (P < 0.05, P < 0.01) between E+ and E– plants under Pedicularis kansuensis parasitism or control. |
| 图选项 |
2.2 甘肃马先蒿寄生对紫花针茅和麦宾草E+、E-植株蒸腾速率的影响 内生真菌带菌状态、甘肃马先蒿寄生处理和不同寄生时间对紫花针茅和麦宾草E+、E-植株蒸腾速率有显著影响。其中,甘肃马先蒿寄生处理与不同寄生时间对麦宾草蒸腾速率有明显交互作用,而不同寄生时间分别与甘肃马先蒿寄生处理和内生真菌带菌状态对紫花针茅蒸腾速率也存在显著的交互作用(表 1)。甘肃马先蒿寄生显著降低紫花针茅和麦宾草的蒸腾速率,随寄生时间增加紫花针茅和麦宾草的蒸腾速率持续降低(图 2)。其中,甘肃马先蒿寄生紫花针茅20 d后,E+植株蒸腾速率显著高于E-植株(P<0.05;图 2-A);而甘肃马先蒿寄生后E-麦宾草蒸腾速率显著高于E+植株(P<0.05;图 2-B)。甘肃马先蒿未寄生状态下,紫花针茅和麦宾草E+植株蒸腾速率高于E-植株(图 2);同时,紫花针茅蒸腾速率呈先升后降变化(图 2-A),而麦宾草的蒸腾速率呈持续降低变化(图 2-B)。
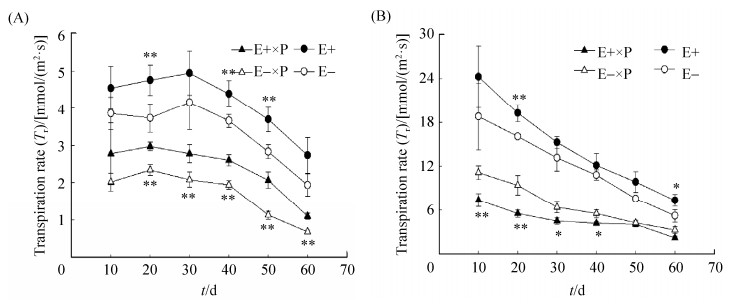 |
| 图 2 甘肃马先蒿寄生不同时间紫花针茅和麦宾草E+、E-植株蒸腾速率变化 Figure 2 Effects of Pedicularis kansuensis parasitism on Stipa purpurea (A) and Elymus tangutorum (B) transpiration rate (Tr) between E+ and E- during different parasitized days. Asterisks (*, **) indicated mean significant difference (P < 0.05, P < 0.01) between E+ and E- plants under Pedicularis kansuensis parasitism or control. |
| 图选项 |
2.3 甘肃马先蒿寄生对紫花针茅和麦宾草E+、E-植株气孔导度的影响 内生真菌带菌状态、甘肃马先蒿寄生处理和不同寄生时间对紫花针茅和麦宾草气孔导度有显著影响(表 1)。甘肃马先蒿寄生处理能显著降低紫花针茅和麦宾草气孔导度(图 3);整个试验期内,紫花针茅气孔导度呈“降-升-降”变化;同时,寄生30 d后,E+植株气孔导度显著高于E-植株(图 3-A)。甘肃马先蒿寄生麦宾草后,麦宾草气孔导度呈持续降低变化(图 3-B)。同时,E-麦宾草气孔导度高于E+植株。甘肃马先蒿未寄生状态下,紫花针茅和麦宾草气孔导度变化趋势与寄生条件下禾草变化相似,紫花针茅和麦宾草E+植株的气孔导度高于E-植株,但E+、E-间差异不显著(图 3)。
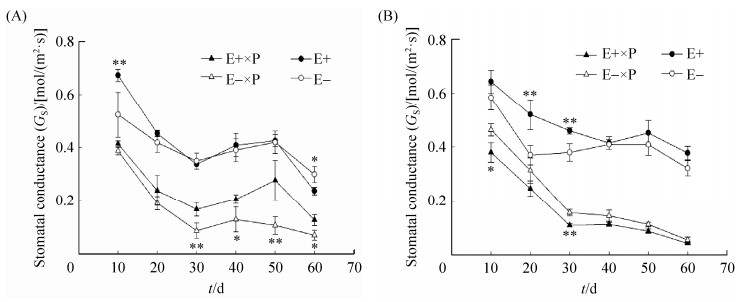 |
| 图 3 甘肃马先蒿寄生不同时间紫花针茅和麦宾草E+、E-植株气孔导度变化 Figure 3 Effects of Pedicularis kansuensis parasitism on Stipa purpurea (A) and Elymus tangutorum (B) stomatal conductance (Gs) between E+ and E- during different parasitized days. Asterisks (*, **) indicated mean significant difference (P < 0.05, P < 0.01) between E+ and E- plants under Pedicularis kansuensis parasitism or control. |
| 图选项 |
2.4 甘肃马先蒿寄生对紫花针茅和麦宾草E+、E-植株胞间二氧化碳浓度的影响 内生真菌带菌状态、甘肃马先蒿寄生处理和不同寄生时间对紫花针茅和麦宾草胞间二氧化碳浓度有显著影响;其中,内生真菌带菌状态和甘肃马先蒿寄生对麦宾草胞间二氧化碳浓度存在交互效应(表 1)。甘肃马先蒿寄生后,紫花针茅和麦宾草胞间二氧化碳浓度显著增加;整个试验期内,紫花针茅和麦宾草胞间二氧化碳浓度呈先上升后下降的变化趋势(图 4)。甘肃马先蒿寄生紫花针茅第30天胞间二氧化碳浓度出现最高值;同时,E-植株胞间二氧化碳浓度显著高于E+植株(图 4-A)。甘肃马先蒿寄生麦宾草20 d胞间二氧化碳浓度出现最高值;同时,E+植株胞间二氧化碳浓度显著高于E-植株(图 4-B)。自然生长条件下,紫花针茅和麦宾草体内胞间二氧化碳浓度变化也呈先增加后降低的变化趋势(图 4)。
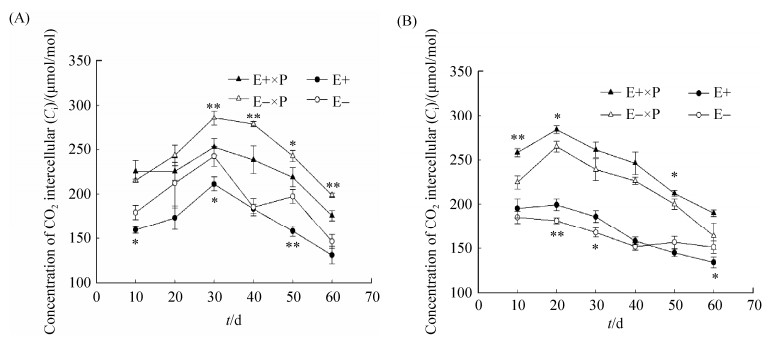 |
| 图 4 甘肃马先蒿寄生不同时间紫花针茅或麦宾草E+、E-植株胞间二氧化碳浓度变化 Figure 4 Effects of Pedicularis kansuensis parasitism on Stipa purpurea (A) and Elymus tangutorum (B) concentration of CO2 intercellular (Ci) between E+ and E- during different parasitized days. Asterisks (*, **) indicated mean significant difference (P < 0.05, P < 0.01) between E+ and E- plants under Pedicularis kansuensis parasitism or control. |
| 图选项 |
2.5 甘肃马先蒿寄生对紫花针茅和麦宾草E+、E-植株水分利用率的影响 甘肃马先蒿寄生处理对紫花针茅和麦宾草水分利用率有显著影响;其中,甘肃马先蒿寄生处理和不同寄生时间对麦宾草水分利用率有明显交互作用(表 1)。整个试验期内,紫花针茅和麦宾草的水分利用率持续下降(图 5)。甘肃马先蒿寄生紫花针茅后,E-植株水分利用率高于E+植株(图 5-A),而E+麦宾草水分利用率高于E-植株(图 5-B)。自然生长条件下,紫花针茅E+、E-植株间水分利用率无差异(图 5-A,P>0.05);而自然生长麦宾草E+植株水分利用率在第10、20、40和60天显著高于E-植株(图 5-B,P<0.05)。
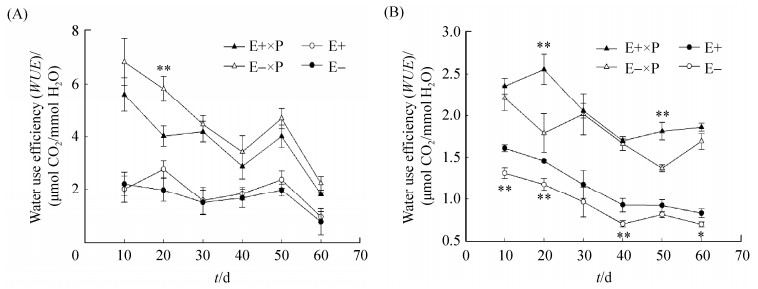 |
| 图 5 甘肃马先蒿寄生不同时间紫花针茅或麦宾草E+、E-植株水分利用率变化 Figure 5 Effects of Pedicularis kansuensis parasitism on Stipa purpurea (A) and Elymus tangutorum (B) water use efficiency (WUE) between E+ and E- during different parasitized days. Asterisks (*, **) indicated mean significant difference (P < 0.05, P < 0.01) between E+ and E- plants under Pedicularis kansuensis parasitism or control. |
| 图选项 |
3 结论和讨论 本研究发现紫花针茅和麦宾草被甘肃马先蒿寄生后,净光合速率、蒸腾速率、气孔导度显著低于未寄生植株,这与其他寄生植物与寄主建立寄生关系后光合作用受抑和生长速率降低的研究结果相似[16, 24-25],主要与根寄生植物抑制寄主植物地上茎叶生长、降低寄主对太阳光的捕获能力、导致寄主光合代谢能力下降有关[26]。Parker和Riches (1993)研究发现独脚金(Striga asiatica)寄生高粱(Sorghum bicolor)后,寄生危害主要体现在对高粱光合作用的抑制效应。独脚金寄生能显著影响寄主叶片的生长和降低寄主叶面积,从而抑制寄主的光合能力并最终影响寄主生物量积累[27]。与自然生长条件下紫花针茅和麦宾草相比,甘肃马先蒿寄生显著影响紫花针茅和麦宾草净光合速率,这可能与根寄生植物寄生禾草后能影响禾草叶片气孔闭合,这种现象已在独脚金寄生高粱的叶片显微结构观测中得到证实[27]。同时,Rodenburg等(2011)发现寄生植物不仅影响寄主光合代谢能力,而且抑制光系统Ⅱ中与寄主光合作用相关的化学物质活性[28]。另外,随着甘肃马先蒿寄生天数增加,紫花针茅和麦宾草净光合速率不断降低,这可能与寄主生长后期叶片形态、叶绿素含量及叶片老化程度等因素有关,上述因素直接影响植物对光照的敏感性。Shen等(2007)研究发现入侵植物加拿大一枝黄花(Solidago Canadensis)被平原菟丝子(Cuscuta campestris)寄生后,幼嫩叶片净光合速率显著低于成熟叶片。同时,平原菟丝子对加拿大一枝黄花净光合速率在寄生后期表现出更强的抑制效应[26];这种现象也与独脚金[29]、埃及列当(Orobanche aegyptiaca)和弯管列当(Orobanche cernua)[30]寄生寄主时得出的结论一致。然而,寄生植物对不同寄主光合作用的抑制效应存在明显差异。Jaschke等(1995)发现光饱和环境中独脚金寄生的豆科植物植株的净光合速率显著高于未寄生植株[31];而弯管列当对烟叶新生且完全展开叶片的光合作用过程未表现出抑制效应[32]。由此可见,寄主种类、寄生时期和生存环境等因素是影响寄生植物对寄主光合作用主要影响因素。
甘肃马先蒿寄生能降低紫花针茅和麦宾草的气孔导度,从而影响寄主茎叶气孔开张和关闭能力。这与独脚金寄生造成寄主气孔导度变化,进而影响高粱光合能力的作用机理相似[33]。气孔导度直接影响植物叶片从大气环境中吸收和转化二氧化碳能力;植物处于根寄生或茎寄生条件下,寄主叶片的气孔导度明显降低,而这一现象与植物遭受其他寄生生物侵害时得出的结论相一致[26, 34]。一些研究发现植物被植食性土壤线虫寄生后植物蒸腾速率明显下降,而这主要与植物体内内源激素——脱落酸含量增加有关[26]。本研究中我们尚未对紫花针茅和麦宾草体内脱落酸含量进行测定,故在以后研究中需进一步检测禾草体内内源激素含量,来验证甘肃马先蒿寄生导致禾草体内激素含量发生变化进而影响禾草气孔导度这一假设。
内生真菌与禾草间的共生关系是一种动态、不稳定的变化过程。近期一些研究结果证明侵染禾草Epichlo?属内生真菌是一种兼具互利共生和寄生危害双重特性的一类真菌,当禾草不能提供基本营养植物来满足体内内生真菌生长和繁殖等条件时,内生真菌从共生菌转化为活体寄生菌,从而加剧生物或非生物逆境对宿主的伤害,最终影响宿主植物的生长和发育进程[35]。本研究发现麦宾草被甘肃马先蒿寄生后,E-植株净光合速率、气孔导度和蒸腾速率显著高于E+植株(图 1-B,2-B,3-B),而E+植株的胞间二氧化碳浓度高于E-植株(图 4-B)。主要原因可能是:(1)甘肃马先蒿持续从寄主体内摄取禾草体内光合产物,导致禾草体内内生真菌从互利共生的有益共生菌转变为具有寄生危害的病原菌,进而影响禾草光合能力[35]。(2)内生真菌菌丝主要分布于禾草茎叶细胞间隙,导致植物叶片细胞形状发生变形[4]。与之相反,甘肃马先蒿寄生紫花针茅后,E+植株的净光合速率、蒸腾速率和气孔导度高于E-植株(图 1-A,2-A,3-A),而E-植株胞间二氧化碳浓度和却高于E+植株(图 4-A)。可见,内生真菌具有缓解或提高紫花针茅对甘肃马先蒿根寄生危害的防御能力,紫花针茅与内生真菌仍保持一种互利共生关系。这与紫花针茅分布在干旱、寒冷和贫瘠土壤的生存环境中,纤细的叶片和发达的根系结构能有效防止水分散失、获取更多营养物质和增强光合作用能力[36-37];而麦宾草宽大的叶片和稀疏的根系导致水分和营养物质易流失等形态特征有关。另外,紫花针茅、麦宾草感染不同种类Epichlo?属内生真菌(紫花针茅感染Epichlo?inebrians, 麦宾草感染Epichlo? bromicola),导致不同种类的内生真菌共生体对甘肃马先蒿根寄生危害具有不同的抵御能力。
本研究证明内生真菌侵染影响根寄生危害禾草的光合作用,虽然内生真菌对不同寄主(紫花针茅和麦宾草)光合作用出现相反的调控结果,证明内生真菌与宿主共生关系是一种介于互惠共生和相互拮抗的动态变化[8]。甘肃马先蒿寄生禾草后,甘肃马先蒿成为禾草的外部能量消耗库[16, 25, 34];同时,禾草体内内生真菌也是禾草体内的一个能量消耗库[38]。当禾草光合作用产物在甘肃马先蒿、内生真菌和禾草间共同分配时,造成根寄生植物、内生真菌和禾草间处于营养竞争状态。土壤养分贫瘠条件下,甘肃马先蒿寄生影响禾草与内生真菌间的共生关系,禾草能否保障内生真菌生长所需养分成为决定宿主和内生真菌间关系的主要限定因素。总而言之,内生真菌侵染显著增强紫花针茅对甘肃马先蒿根寄生危害的防御能力,进一步支持甘肃马先蒿大面积发生天然退化草地中带菌紫花针茅成为草地优势种的原因,为利用禾草内生真菌共生体作为生物防控资源来控制甘肃马先蒿提供新思路。
References
| [1] | Stachowicz JJ. Mutualism, facilitation, and the structure of ecological communities:positive interactions play a critical, but underappreciated, role in ecological communities by reducing physical or biotic stresses in existing habitats and by creating new habitats on which many species depend. Bioscience, 2001, 51(3): 235-246. DOI:10.1641/0006-3568(2001)051[0235:MFATSO]2.0.CO;2 |
| [2] | Clay K. Fungal endophytes of grasses:a defensive mutualism between plants and fungi. Ecology, 1988, 69(1): 10-16. DOI:10.2307/1943155 |
| [3] | Bonfante P, Genre A. Mechanisms underlying beneficial plant-fungus interactions in mycorrhizal symbiosis. Nature Communications, 2010, 1: 48. DOI:10.1038/ncomms1046 |
| [4] | Schardl CL, Leuchtmann A, Spiering MJ. Symbioses of grasses with seedborne fungal endophytes. Annual Review of Plant Biology, 2004, 55: 315-340. DOI:10.1146/annurev.arplant.55.031903.141735 |
| [5] | Malinowski DP, Belesky DP. Tall fescue aluminum tolerance is affected by Neotyphodium coenophialum endophyte. Journal of Plant Nutrition, 1999, 22(8): 1335-1349. DOI:10.1080/01904169909365716 |
| [6] | Wilkinson HH, Siegel MR, Blankenship JD, Mallory AC, Bush LP, Schardl CL. Contribution of fungal loline alkaloids to protection from aphids in a grass-endophyte mutualism. Molecular Plant-Microbe Interactions, 2000, 13(10): 1027-1033. DOI:10.1094/MPMI.2000.13.10.1027 |
| [7] | Scott B, Schardl C. Fungal symbionts of grasses:evolutionary insights and agricultural potential. Trends in Microbiology, 1993, 1(5): 196-200. DOI:10.1016/0966-842X(93)90091-5 |
| [8] | Saikkonen K, Faeth SH, Helander M, Sullivan T. Fungal endophytes:a continuum of interactions with host plants. Annual Review of Ecology and Systematics, 1998, 29: 319-343. DOI:10.1146/annurev.ecolsys.29.1.319 |
| [9] | Lehtonen P, Helander M, Wink M, Sporer F, Saikkonen K. Transfer of endophyte-origin defensive alkaloids from a grass to a hemiparasitic plant. Ecology Letters, 2005, 8(12): 1256-1263. DOI:10.1111/j.1461-0248.2005.00834.x |
| [10] | Phoenix GK, Press MC. Linking physiological traits to impacts on community structure and function:the role of root hemiparasitic Orobanchaceae (ex-Scrophulariaceae). Journal of Ecology, 2005, 93(1): 67-78. DOI:10.1111/j.1365-2745.2004.00950.x |
| [11] | Cameron DD, Seel WE. Functional anatomy of haustoria formed by Rhinanthus minor:linking evidence from histology and isotope tracing. New Phytologist, 2007, 174(2): 412-419. DOI:10.1111/j.1469-8137.2007.02013.x |
| [12] | Wen L, Dong SK, Li YY, Li XY, Shi JJ, Wang YL, Liu DM, Ma YS. Effect of degradation intensity on grassland ecosystem services in the alpine region of Qinghai-Tibetan Plateau, China. PLoS One, 2013, 8(3): e58432. DOI:10.1371/journal.pone.0058432 |
| [13] | Bao GS, Suetsugu K, Wang HS, Yao X, Liu L, Ou J, Li CJ. Effects of the hemiparasitic plant Pedicularis kansuensis on plant community structure in a degraded grassland. Ecological Research, 2015, 30(3): 507-515. DOI:10.1007/s11284-015-1248-4 |
| [14] | Bao GS, Li CJ. Isolation and identification of endophytes infecting Stipa purpurea, a dominant grass in meadows of the Qinghai-Tibet Plateau. Acta Prataculturae Sinica, 2016, 25(3): 32-42. (in Chinese) 鲍根生, 李春杰. 青藏高原高寒草地优势禾草——紫花针茅内生真菌分离和鉴定. 草业学报, 2016, 25(3): 32-42. |
| [15] | Song H, Nan ZB. Origin, divergence, and phylogeny of asexual Epichlo? endophyte in Elymus species from western China. PLoS One, 2015, 10(5): e0127096. DOI:10.1371/journal.pone.0127096 |
| [16] | Tě?itel J, Tě?itelová T, Fisher JP, Lep? J, Cameron DD. Integrating ecology and physiology of root-hemiparasitic interaction:interactive effects of abiotic resources shape the interplay between parasitism and autotrophy. New Phytologist, 2015, 205(1): 350-360. DOI:10.1111/nph.13006 |
| [17] | Rozp?dek P, W??owicz K, Nosek M, Wa?ny R, Tokarz K, Lembicz M, Miszalski Z, Turnau K. The fungal endophyte Epichlo? typhina improves photosynthesis efficiency of its host orchard grass (Dactylis glomerata). Planta, 2015, 242(4): 1025-1035. DOI:10.1007/s00425-015-2337-x |
| [18] | Li CJ, Nan ZB, Paul VH, Dapprich PD, Liu Y. A new Neotyphodium species symbiotic with drunken horse grass (Achnatherum inebrians) in China. Mycotaxon, 2004, 90(1): 141-147. |
| [19] | Yao X, Li XZ, Zhu XX, Li CJ. Effects of two fungicides on Neotyphodium seed-borne fungal endophyte of Festuca sinensis. Pratacultural Science, 2013, 30(10): 1517-1522. (in Chinese) 姚祥, 李秀璋, 朱小晓, 李春杰. 两种杀菌剂对中华羊茅种传内生真菌的影响. 草业科学, 2013, 30(10): 1517-1522. |
| [20] | Klaren CH, Janssen G. Physiological changes in the hemiparasite Rhinanthus serotinus before and after attachment. Physiologia Plantarum, 1978, 42(1): 151-155. |
| [21] | Song ML, Chai Q, Li XZ, Yao X, Li CJ, Christensen MJ, Nan ZB. An asexual Epichlo? endophyte modifies the nutrient stoichiometry of wild barley (Hordeum brevisubulatum) under salt stress. Plant and Soil, 2015, 387(1/2): 153-165. |
| [22] | Hu MY, Zhang L, Luo TX, Shen W. Variations in leaf functional traits of Stipa purpurea along a rainfall gradient in Xizang, China. Chinese Journal of Plant Ecology, 2012, 36(2): 136-143. (in Chinese) 胡梦瑶, 张林, 罗天祥, 沈维. 西藏紫花针茅叶功能性状沿降水梯度的变化. 植物生态学报, 2012, 36(2): 136-143. |
| [23] | von Caemmerer S, Farquhar GD. Some relationships between the biochemistry of photosynthesis and the gas exchange of leaves. Planta, 1981, 153(4): 376-387. DOI:10.1007/BF00384257 |
| [24] | Wicke S, Müller KF, de Pamphilis CW, Quandt D, Wickett NJ, Zhang Y, Renner SS, Schneeweiss GM. Mechanisms of functional and physical genome reduction in photosynthetic and nonphotosynthetic parasitic plants of the broomrape family. The Plant Cell, 2013, 25(10): 3711-3725. DOI:10.1105/tpc.113.113373 |
| [25] | Tě?itel J, Lep? J, Vráblová M, Cameron DD. The role of heterotrophic carbon acquisition by the hemiparasitic plant Rhinanthus alectorolophus in seedling establishment in natural communities:a physiological perspective. New Phytologist, 2011, 192(1): 188-199. DOI:10.1111/j.1469-8137.2011.03777.x |
| [26] | Shen H, Hong L, Ye WH, Cao HL, Wang ZM. The influence of the holoparasitic plant Cuscuta campestris on the growth and photosynthesis of its host Mikania micrantha. Journal of Experimental Botany, 2007, 58(11): 2929-2937. DOI:10.1093/jxb/erm168 |
| [27] | Parker C, Riches CR. Parasitic weeds of the world: biology and control. Wallingford: CAB International, 1993. |
| [28] | Rodenburg J, Meinke H, Johnson DE. Challenges for weed management in African rice systems in a changing climate. The Journal of Agricultural Science, 2011, 149(4): 427-435. DOI:10.1017/S0021859611000207 |
| [29] | Hibberd JM, Quick WP, Press MC, Scholes JD. The influence of the parasitic angiosperm Striga gesnerioides on the growth and photosynthesis of its host, Vigna unguiculata. Journal of Experimental Botany, 1996, 47(4): 507-512. DOI:10.1093/jxb/47.4.507 |
| [30] | Barker ER, Scholes JD, Press MC, Quick WP. Effects of the holoparasite Orobanche aegyptiaca on the growth and photosynthesis of its tomato host. Aspects of Applied Biology, 1995(42): 141-148. |
| [31] | Jeschke WD, Baumel P, Rath N. Partitioning of nutrients in the Cuscuta reflexa-Lupinus albus association. Aspects of Applied Biology, 1995(42): 71-79. |
| [32] | Hibberd JM, Quick WP, Press MC, Scholes JD. Can source-sink relations explain responses of tobacco to infection by the root holoparasitic angiosperm Orobanche cernua?. Plant, Cell & Environment, 1998, 21(3): 333-340. |
| [33] | Graves JD, Press MC, Stewart GR. A carbon balance model of the sorghum-Striga hermonthica host-parasite association. Plant, Cell & Environment, 1989, 12(1): 101-107. |
| [34] | Watling JR, Press MC. Infection with the parasitic angiosperm Striga hermonthica influences the response of the C3 cereal Oryza sativa to elevated CO2. Global Change Biology, 2000, 6(8): 919-930. DOI:10.1046/j.1365-2486.2000.00366.x |
| [35] | Saikkonen K, W?li P, Helander M, Faeth SH. Evolution of endophyte-plant symbioses. Trends in Plant Science, 2004, 9(6): 275-280. DOI:10.1016/j.tplants.2004.04.005 |
| [36] | Wang ZY, Hou J, Qu ZQ, Guo JY, Li JR. Root distribution of 430 plants in temperate grassland of northern China. Applied Ecology and Environmental Research, 2017, 15(3): 1625-1651. |
| [37] | Yang YQ, Li X, Kong XX, Ma L, Hu XY, Yang YP. Transcriptome analysis reveals diversified adaptation of Stipa purpurea along a drought gradient on the Tibetan Plateau. Functional & Integrative Genomics, 2015, 15(3): 295-307. |
| [38] | Christensen MJ, Bennett RJ, Schmid J. Growth of Epichlo?/Neotyphodium and p-endophytes in leaves of Lolium and Festuca grasses. Mycological Research, 2002, 106(1): 93-106. DOI:10.1017/S095375620100510X |
