 , 朱利军3, 徐慧1,2
, 朱利军3, 徐慧1,2
 , 王东升1,2
, 王东升1,21. 中国科学院生态环境研究中心 环境水质学国家重点实验室, 北京 100085;
2. 中国科学院大学, 北京 100049;
3. 清上(苏州)环境科技有限公司, 苏州 215004
收稿日期: 2020-11-05; 修回日期: 2021-01-21; 录用日期: 2021-01-21
基金项目: 国家科技重大专项(No.2017ZX07108-002);国家科技重大专项(No.2017ZX07501-002);国家自然科学基金面上项目(No.51778604);宁夏回族自治区重大项目(No.2019BFG02032)
作者简介: 李明霜(1996-), 女, E-mail: limingshuang11@163.com
通讯作者(责任作者): 徐慧, E-mail: huixu@rcees.ac.cn
摘要:为比较APAM和HCA对给水厂污泥调理的效果并探究其作用机制,测定了污泥调理前后的毛细吸水时间(CST)、污泥比阻(SRF)、溶解性有机污染物含量(DOC)、Zeta电位和絮体粒径的变化情况,并结合三维荧光谱图、液相-有机碳联用(LC-OCD)、热重差热法(TG-DTA)以及傅立叶红外(FTIR)的变化进行分析.结果表明,APAM和HCA的最佳投加量分别为0.05和0.10 g·L-1,与之对应的CST分别从71.0 s降到25.8 s和37.6 s,SRF从9.72×1012 m·kg-1降到4.18×1012 m·kg-1和5.70×1012 m·kg-1,APAM的调理效果占优.HCA仅可释放毛细水,而APAM可释放污泥的毛细水和表面吸附水.APAM通过氢键的吸附架桥形成大块絮体以改善污泥脱水性能,Zeta电位的升高和有机物的变化显示出电中和及去水化作用是HCA的主要调理机制.本研究结果可为给水厂污泥脱水有机药剂的选择提供数据基础.
关键词:APAMHCA水分分布氢键去水化作用
The performance and mechanism of sludge dewatering with APAM and HCA in drinking water plant
LI Mingshuang1,2
 , ZHU Lijun3, XU Hui1,2
, ZHU Lijun3, XU Hui1,2
 , WANG Dongsheng1,2
, WANG Dongsheng1,21. State Key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085;
2. University of Chinese Academy of Sciences, Beijing 100049;
3. Tingshang(Suzhou) Environmental S&T Co., LTD, Suzhou 215004
Received 5 November 2020; received in revised from 21 January 2021; accepted 21 January 2021
Abstract: The mechanism of sludge dewatering with APAM and HCA was explored by comparing its performance in a drinking water treatment plant, the capillary suction time (CST), specific resistance to filtration (SRF), dissolved organic carbon (DOC), Zeta potential and the floc size were measured, combined with the characterization with three-dimensional excitation-emission matrix (3D-EEM), liquid chromatography-organic carbon detection (LC-OCD), thermo gravimetric-differential thermal analyzer (TG-DTA) and Fourier transform infrared (FTIR). The results showed that the optimal dosages of APAM and HCA were 0.05 and 0.10 g·L-1, where CST decreased from 71.0 s to 25.8 s and 37.6 s, SRF decreased from 9.72×1012 m·kg-1 to 4.18×1012 and 5.70×1012 m·kg-1, respectively. Meanwhile, APAM could release capillary water and surface adsorbed water from sludge, whereas HCA could only release capillary water. APAM improved sludge dewatering performance by adsorption and bridging through hydrogen bond. The increase of Zeta potential and the change of organic matter reflected that charge neutralization and dehydration are the main mechanism of HCA. In summary, this study can provide a data base for sludge dewatering conditioners in drinking water treatment plants.
Keywords: APAMHCAmoisture distributionhydrogen bondingdehydration
1 引言(Introduction)随着居民用水需求的不断增长, 给水厂在产水量增加的同时也产生了大量的污泥(陶赟, 2018), 这部分污泥的脱水及资源化利用已成为当下研究的热点问题(Yao et al., 2020; Kulandaivelu et al., 2020).给水厂污泥含水率高, 污泥颗粒与表面的水化层形成稳定的胶体悬浮液, 难以自然沉降脱水, 因此需要对污泥调理使水分脱出(刘彤, 2018).目前, 我国给水厂污泥的处理方式主要是污泥浓缩后进入脱水机, 脱水后泥饼外运, 处置方式以卫生填埋为主(陈洋, 2017).
给水厂污泥进入脱水机前, 需投加药剂进行调理, 其中最常用的调理剂为无机高分子调理剂聚合氯化铝(PACl)和有机高分子调理剂聚丙烯酰胺(PAM), 前者价格低, 但投加量大, 且存在金属离子的二次污染问题;后者絮凝能力强、用量少, 但价格相对较高(Cao et al., 2021).Huang等(2014)认为PAM和蒙脱石联用通过电中和、吸附架桥使得污泥具有良好的脱水性能, 但无法影响污泥水分分布;Wang等(2017)认为PAM通过吸附架桥将污泥中的物理结合水转化为游离水, 略微降低了污泥饼水分的含量, 并在后来的研究(Wang et al., 2019)中指出, PAM和无机混凝剂联用, 混凝和絮凝协同作用使得污泥结合水含量进一步降低.此外, 具有高电荷密度的HCA也广泛用于污泥调理(Saveyn et al., 2008), Xiao等(2018)将HCA应用于预氧化污泥, 使较小的污泥颗粒团聚成较大的聚集体, 从而提高了污泥的脱水性能;Wang等(2019)得出, HCA与过硫酸铁和沸石联用三步脱水:过硫酸铁破坏有机物释放结合水, HCA重新絮凝, 沸石提供骨架, 极大改善了污泥的脱水性能.尽管两种药剂已得到广泛应用, 但其对污泥水分分布的影响仍不明确(Wang et al., 2017), 他们与给水污泥颗粒的作用过程仍需进一步探究.
本文比较了APAM和HCA对给水厂污泥的脱水性能的影响, 利用三维荧光和LC-OCD等观测调理前后有机物的变化情况, 通过分析调理前后的污泥絮体性质、污泥泥饼水分分布及配水实验的絮体红外谱图等探究其对给水厂污泥的调理机制.
2 材料与方法(Materials and methods)2.1 实验材料2.1.1 污泥来源本研究所用污泥取自某给水厂污泥浓缩池, 该水厂日产水量为9×104 t.污泥取回后静沉浓缩, 其基本性质见表 1.
表 1(Table 1)
| 表 1 污泥基本性质 Table 1 Basic properties of sludge | ||||||||||||||||||
表 1 污泥基本性质 Table 1 Basic properties of sludge
| ||||||||||||||||||
2.1.2 化学试剂APAM(分子量为1000×104~1200×104, 麦克林)、HCA(分子量为40×104~50×104, 阿拉丁)、高岭土(< 2.5 μm, 阿拉丁)、牛血清蛋白(96%, 阿拉丁)、腐殖酸(≥90%, 阿拉丁)、葡萄糖(98%, 阿拉丁).硝酸钠(NaNO3)、碳酸氢钠(NaHCO3)、六水合氯化铝(AlCl3·6H2O)均为分析纯, 购于中国国药化学试剂有限公司.
2.2 试验方法2.2.1 调理方法污泥调理实验在六联搅拌器上进行, 6个烧杯中分别倒入300 mL污泥, APAM的投加量依次为0.02、0.03、0.04、0.05、0.06、0.07 g·L-1, HCA投加量分别为0.04、0.06、0.08、0.10、0.12、0.14 g·L-1.搅拌器程序设定为:250 r·min-1快搅30 s, 加药后200 r·min-1搅拌1 min, 再以40 r·min-1慢搅10 min.
2.2.2 配水实验给水厂污泥成分复杂, 为了解APAM、HCA在污泥调理过程中的细微变化, 模拟污泥体系配制水体进行研究.配水成分如下:500 mL超纯水, 200 mg高岭土模拟污泥无机颗粒, 10 mg牛血清蛋白、葡萄糖、腐殖酸模拟给水污泥中的有机物, 5 mmol·L-1 NaNO3调节离子强度, 4 mmol·L-1 NaHCO3调节碱度.调理实验在六联搅拌器上进行, 搅拌程序同上, 先加入4 mg·L-1 AlCl3混凝生成微小絮体, 再分别加入APAM和HCA对其进行调理, APAM和HCA的投加量分别为4和8 mg·L-1.沉淀后取絮体做红外分析.
2.2.3 测定方法调理前后污泥性质的测定.CST取样后由CST测定仪(RTC-304B, 英国Triton公司)直接测定.SRF在压力为0.6 MPa下将一定量污泥倒入布氏漏斗中抽滤测定(Niu et al., 2013).Zeta电位用纳米粒度及Zeta电位分析仪(ZS90, 马尔文公司)测定.含水率和有机质使用电热恒温干燥箱(DHG-9146A, 北京天林恒泰科技有限公司)和箱式电阻炉(SX2-2 5-10TP, 上海一恒科学仪器有限公司)测定(熊巧, 2018).
絮体粒径的动态变化用马尔文激光粒度分析仪(Mastersizer 2000, 马尔文公司)测定.混凝程序:A段快搅阶段, 250 r·min-1快搅30 s, 加药后200 r·min-1搅拌1 min;B段慢搅阶段, 40 r·min-1慢搅10 min;C段破碎阶段, 250 r·min-1快搅1 min破碎絮体;D段恢复阶段, 40 r·min-1慢搅10 min使絮体再生成.根据各段的平均粒径可计算出絮体的恢复因子和强度因子(Su et al., 2017).
污泥上清液有机物的测定.用液相有机碳联用仪(LC-OCD)对不同分子量、不同化学性质的有机物分离定量.LC-OCD可将水中的有机物分为4类:MW>20000的生物聚合物、MW>1000的腐殖质、300 < MW < 500的腐殖质降解产物以及MW≤350的小分子中性物质和小分子酸(Chen et al., 2016).用荧光分光光度计(F-7000, 日立公司)测定三维荧光谱图, 采用150 W氙灯为激发光源, 激发波长(Ex)为200~400 nm, 发射波长(Em)为220~550 nm, 狭缝宽度为5 nm.DOC由总有机碳测定仪(岛津, 岛津公司)测定.
絮体的表征.用傅里叶变换显微红外光谱仪(Nicolet iN10MX, Thermo Fisher Scientific)检测配水实验产生的絮体官能团的变化.用场发射扫描电子显微镜(SU-8020, 日立公司)观察污泥絮体微观结构.
污泥水分结合能的测定.使用热重差热分析仪(TG-DTA, X70, 耐驰公司)测量污泥水分结合能变化.分析条件如下:起始温度为25 ℃, 终止温度为70 ℃, 保温时间为1 h, 升温速率为10 ℃·min-1, 气氛N2, 扫描速度为40 mL·min-1.TG-DTA是测量污泥水分结合能的一个常用方法, 它将污泥泥饼中结合水的结合能定义为释放这部分水所需要的能量.结合能Eb的公式如下(Dai et al., 2018):
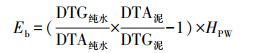 | (1) |
3 结果与讨论(Results and discussion)3.1 APAM和HCA调理对污泥脱水性能的影响污泥调理后的CST和SRF如图 1所示, 相比于HCA, APAM在较少投加量下即可得到更优的脱水效果.APAM的最佳投加量为0.05 g·L-1, 该投加量下CST从71.0 s减小到25.8 s, SRF从9.72×1012 m·kg-1降到4.18×1012 m·kg-1, 污泥脱水性能显著提高;此时APAM将污泥颗粒絮凝成肉眼可见的大块絮体并迅速下沉, 形成明显的固液界面.HCA的最佳投加量为0.10 g·L-1, 该投加量下CST降至最小值37.6 s, SRF为5.70×1012 m·kg-1, 这是因为HCA通过正电荷中和污泥颗粒的负电荷使其聚集沉降;继续投加HCA, 会使污泥颗粒电荷变正, 引起颗粒复稳(Wu et al., 2016), CST会有小幅上升.
图 1(Fig. 1)
 |
| 图 1 不同浓度APAM和HCA调理后的污泥的CST (a)和SRF (b) Fig. 1The CST(a) and SRF(b) of sludge conditioned with different concentrations of APAM and HCA |
3.2 APAM和HCA调理对污泥有机物的影响给水厂污泥主要成分为原水中的无机颗粒、有机物以及净水工艺中投加的混凝剂(Zhou et al., 2018), 其DOC浓度低, 所含的有机物主要是原水中的天然有机物(NOM)(穆丹琳, 2015).本研究通过测定调理前后给水厂污泥上清液中有机物的种类和含量, 分析APAM和HCA对污泥有机物的影响.
图 2为调理后上清液中有机物的DOC浓度变化情况.原泥上清液中有机物的DOC浓度为10.09 mg·L-1, 经APAM和HCA分别调理后, 上清液DOC浓度均有不同程度增加, 最佳投加量下DOC浓度分别为11.92和11.08 mg·L-1.原泥以及APAM和HCA最佳投加量调理后的三维荧光图谱如图 3所示, 原泥中主要呈现两个峰:Ex/Em 260~290/270~330、220~230/270~335, 分别为微生物代谢产物峰和蛋白质峰, 由图 3b、3c可知, 经APAM和HCA调理后, 蛋白质峰的荧光强度减弱, 但其他区域荧光强度增加, 说明两种调理剂均对蛋白质有少量去除作用, 但整体有机物浓度升高.
图 2(Fig. 2)
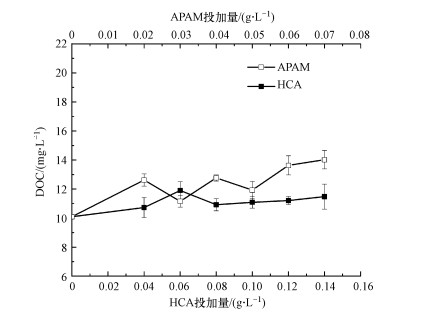 |
| 图 2 原泥和APAM、HCA调理后的污泥不同上清液的DOC值 Fig. 2DOC content of raw sludge and sludge conditioned with APAM、HCA |
图 3(Fig. 3)
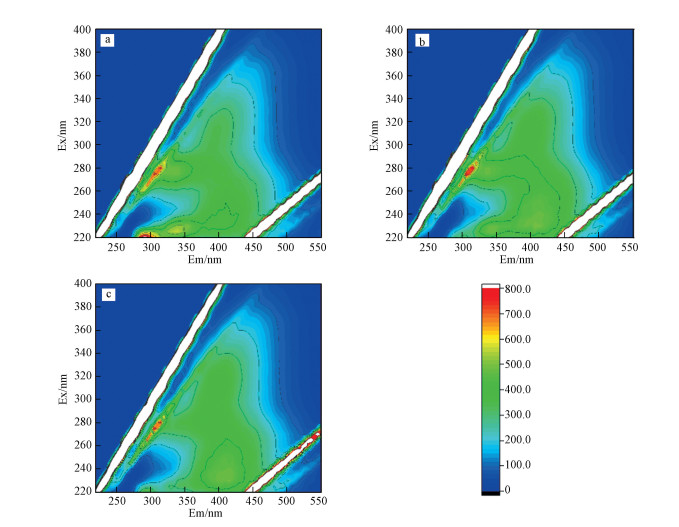 |
| 图 3 原泥(a)以及APAM (b)和HCA (c)最佳投加量调理后的三维荧光图谱 Fig. 33D-EEM spectra of raw sludge(a) and conditioned sludge using APAM(b)、HCA(c) |
图 4为经APAM和HCA最佳投加量调理前后的污泥上清液的LC-OCD图.原泥中的4类有机物出峰时间依次为15.3、22.3、26.6和38.5 min, 分别对应生物聚合物、腐殖酸类物质、腐殖酸降解产物、小分子酸和小分子中性物质;经APAM调理后, 前3个峰的强度无明显变化, 小分子中性物质和小分子酸类处的峰强度降低, 说明APAM对小分子物质具有一定的去除作用, 但去除量相对较少;经HCA调理后的污泥上清液中, 生物聚合物和小分子物质对应的峰强度明显降低, 且在55.0 min处形成一个新峰, 说明HCA的加入, 使得部分大分子生物聚合物被去除, 且有新的小分子物质产生.
图 4(Fig. 4)
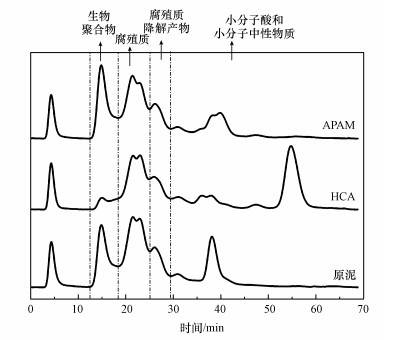 |
| 图 4 原泥以及APAM和HCA最佳投加量调理后的LC-OCD分析 Fig. 4LC-OCD spectra of raw sludge and conditioned sludge using APAM、HCA |
综合图 2~图 4可得, 投加APAM和HCA的污泥上清液总有机物的含量略有增加, 这是因为APAM和HCA均为高分子有机聚合物, 加入污泥后会在污泥上清液中有一定的残留.相比于APAM, HCA对生物大分子生物聚合物去除效果明显, 但也相对增加了小分子酸和小分子中性物质的含量.生物大分子聚合物包括蛋白质、多糖等, 这些亲水性物质包裹在污泥颗粒表面形成一层水化层, 与污泥脱水性能呈正相关(Li et al., 2007), HCA的加入去除了这部分水化层, 使污泥更易脱水.
3.3 APAM和HCA调理对污泥絮体性质的影响胶体的稳定性是影响污泥脱水效果的因素之一, 表面电荷可从一定程度上反映胶体的稳定性(Mikkelsen et al., 1996), 本文用Zeta电位表征胶体的稳定性.APAM和HCA不同投加量下污泥的Zeta电位变化情况如图 5所示. 原泥的Zeta电位为-9.06 mV, HCA带正电, 所以随着HCA投加量的增加, Zeta电位逐渐增高, 最佳投加量对应的Zeta电位为-6.25 mV, 继续投加HCA, 污泥电位由负转正, 此时颗粒复稳, 脱水性能变差, 与CST和SRF反映的结果一致;值得注意的是, 污泥的最佳脱水性能并非在等电点处取得, 故电中和并不能完全解释HCA的作用(Forster, 2002).APAM带负电, 其加入使得污泥胶体负电量不断增加, Zeta电位数值不断减小, 这说明APAM改善污泥脱水性能并不是电中和的作用.
图 5(Fig. 5)
 |
| 图 5 原泥和APAM、HCA调理后的zeta电位 Fig. 5Zeta potential of raw sludge and conditioned sludge using APAM and HCA |
污泥絮体粒径的大小也与污泥的脱水效果相关, 污泥絮体粒径的增大有助于水通道的形成, 使污泥水分释放(Zhu et al., 2018).图 6为APAM和HCA最佳投加量时, 絮体粒径随时间的变化情况.原泥粒径为42.0 μm, 快搅30 s后加入APAM和HCA, 继续快搅60 s, 此阶段絮体粒径变化不明显;90 s后进入慢搅阶段, 使用APAM调理的絮体粒径急剧增长, 最大可达743.0 μm, 稳定后的平均粒径为560.0 μm, 而使用HCA调理的污泥絮体虽稍有增长, 但稳定后平均粒径仅有81.5 μm, 远小于经APAM调理的污泥絮体粒径;690~750 s为破碎阶段, 使用APAM调理的污泥絮体粒径在破碎之初迅速减小, 下降幅度超过150 μm, 经HCA调理的污泥絮体粒径也出现下降特征, 但相对较小;750 s后为破碎后再生成阶段, 两种调理剂作用下的絮体粒径再次增大, APAM一组的平均粒径为444.5 μm, 小于破碎之前, 整体波动幅度较大, 而HCA一组的平均粒径为112.6 μm, 且总体呈平稳上升态势.由图 7扫描电镜图可以看出, 相对于原泥, 经APAM和HCA调理后的污泥絮体颗粒较为松散.综上, 相比于HCA, 使用APAM调理的污泥可迅速形成大块絮体, 从而产生更多的水通道, 有利于污泥水分的释放, 因此APAM脱水效果优于HCA;此外, 经计算可得APAM和HCA的强度因子分别为69.4%和68.5%, 恢复因子分别为32.5%和191.2%.强度因子越高, 絮体抗剪切能力越强;恢复因子越高, 絮体破坏后越容易重新团聚成絮体(Peter et al., 2005), 因此两种药剂形成的污泥絮体抗剪切能力相当, 而HCA形成的絮体受到破坏后更容易恢复.
图 6(Fig. 6)
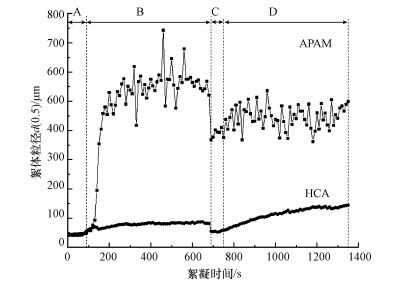 |
| 图 6 APAM、HCA最佳投加量时的絮体粒径变化 Fig. 6The floc size under the optimal dosage of APAM and HCA |
图 7(Fig. 7)
 |
| 图 7 原泥(a)和APAM (b)、HCA (c)最佳投加量时絮体的扫描电镜 Fig. 7SEM of raw sludge(a) and conditioned sludge under the optimal dosage of APAM(b) and HCA(c) |
3.4 APAM和HCA调理对污泥水分分布的影响污泥滤饼中所含水分的结合能定义为释放这部分水分所需要的能量(谢浩辉, 2011).图 8为原泥和纯水的TG-DTA曲线, 从图 8a中可以看出, 原泥的恒速蒸发区为18~26 ℃, 此区间内DTA/DTG的比值为0.1234, 同理, 纯水在上述区间内的DTG/DTA比值为8.1145, 进一步, 根据公式(1)可求得原泥水分结合能为3 kJ·kg-1.Foucat等(2014)认为, 释放水分的类型不同, 所需的结合能也不同, 并给出了释放自由水、毛细水、表面吸附水和结合水所需的最低结合能, 分别为0、5.5、167、278 kJ·kg-1, 因此可以通过测定污泥水分结合能来判断污泥含水类型.如原泥的水分结合能为3 kJ·kg-1, 小于释放毛细水的最低结合能, 因此原泥中不仅含有毛细水, 还有表面吸附水、结合水和少量的自由水;若结合能为200 kJ·kg-1, 则表明污泥泥饼中含有结合水和少量表面吸附水;若结合能大于278 kJ·kg-1, 则表明污泥滤饼中只剩下结合水.
图 8(Fig. 8)
 |
| 图 8 原泥(a)和纯水(b)的TG-DTA曲线 Fig. 8TG-DTA curves of raw sludge(a) and pure water(b) |
表 2给出了原泥和HCA和APAM投加后, 污泥结合能和水分类型的变化情况.由表 2可知, 随着APAM和HCA投加量的增加, 污泥泥饼的结合能逐渐升高, 而且相同投加量时, APAM一组的结合能增加更多.HCA的加入可以使原泥中的毛细结合水释放出来, 对应于最佳投加量0.10 g·L-1时, 污泥泥饼的结合能为111 kJ·kg-1, 此时泥饼中只含有表面吸附水、结合水以及少部分毛细水;随着APAM的不断投加, 表面吸附水也会逐渐释放, 最终只剩结合水和少部分表面吸附水.由此可见, HCA的加入可以释放大部分毛细水, 而APAM不仅可以释放毛细水, 还能将大部分表面吸附水释放出来, 因此APAM调理后的污泥脱水效果优于HCA.
表 2(Table 2)
| 表 2 APAM、HCA不同投加量下的污泥泥饼结合能和水分类型 Table 2 Eb of bound water and bound water type in sludge cake conditioned with different APAM and HCA dosage | ||||||||||||||||||||||||||||||||||||||||||||||||||
表 2 APAM、HCA不同投加量下的污泥泥饼结合能和水分类型 Table 2 Eb of bound water and bound water type in sludge cake conditioned with different APAM and HCA dosage
| ||||||||||||||||||||||||||||||||||||||||||||||||||
3.5 APAM和HCA的污泥调理机制关于高分子聚合物对给水厂污泥的调理作用, 目前主要有3种解释机理:电中和、吸附架桥以及去水化作用(Bolto et al., 2007). 电中和指中和胶体的表面电位, 使其脱稳聚沉;吸附架桥是指高分子有机物通过氢键或离子结合等方式将污泥胶体颗粒聚集成更大的颗粒;去水化作用指高分子聚合物与污泥胶体颗粒发生反应, 将亲水胶体转变为憎水胶体(Bolto et al., 2007).
图 9是未加调理剂和投加APAM、HCA的絮体红外光谱, 位于3455~3465、2287~2360、1639~1655、1384~1385 cm-1处的吸收峰分别对应N—H的伸缩振动、C ≡ C和C ≡ N的伸缩振动、C=O的伸缩振动、C—H的弯曲振动(Sheng et al., 2006; Wang et al., 2014).N—H和C=O所形成的氢键为均为红移氢键, 形成氢键或氢键作用增强, 红外吸收峰红移(Joseph et al., 2007; 周瑜, 2016).加入APAM和HCA后, 絮体的N—H峰分别向低波移动了10和5 cm-1, 说明二者N—H氢键作用均增强, 且前者强于后者;C=O峰分别红移13 cm-1和蓝移3 cm-1, 说明APAM体系中C=O氢键作用增强而HCA体系中C=O氢键作用减弱.
图 9(Fig. 9)
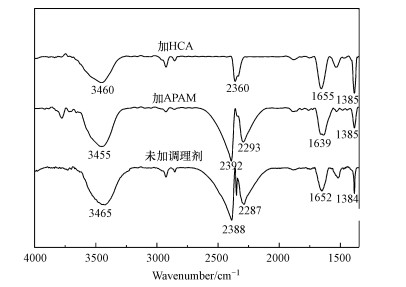 |
| 图 9 未加调理剂和加APAM、HCA的絮体红外光谱 Fig. 9FTIR of flocs conditioned with APAM、HCA and without flocculant |
图 10为APAM和HCA对给水厂污泥调理机制图.如前所述, 带正电的HCA中和了污泥颗粒的表面电位, 使污泥颗粒脱稳形成絮体;同时HCA可以降低大分子生物聚合物的含量并产生小分子新物质, 这说明其对污泥的调理过程有去水化作用的影响.APAM通过氢键吸附架桥显著增大了污泥颗粒的尺寸, 形成水通道, 使水分得到释放, 但并未对有机物产生显著影响.综上, HCA的调理机制主要为电中和及去水化作用, APAM的调理机制主要为氢键的吸附架桥作用.
图 10(Fig. 10)
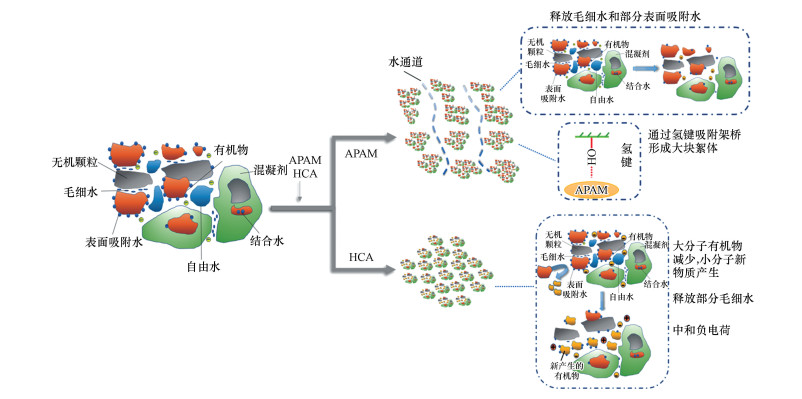 |
| 图 10 APAM、HCA污泥调理机制图 Fig. 10Mechanism of APAM、HCA sludge conditioning |
值得注意的是, 实际应用中多采用阳离子聚丙烯酰胺(CPAM)用于污泥调理, 调理后会残留少量单体丙烯酰胺, 可能损伤人体神经系统, HCA安全无毒(Boettcher et al., 2006).而本实验中采用的是阴离子聚丙烯酰胺(APAM), 其毒性相较于CPAM更小, 在合理设置投加量的情况下, 既能达到良好的脱水效果, 又不会对人体造成危害.APAM在较少的投加量下即可达到更优的调理效果, 因此更适用给水厂污泥的使用.
4 结论(Conclusions)1) 与HCA相比, APAM的脱水性能更佳, APAM和HCA的最佳投加量分别为0.05和0.10 g·L-1, 该投加量下对应的CST从71.0 s分别降到25.8和37.6 s, SRF从9.72×1012 m·kg-1分别降到4.18×1012 m·kg-1和5.70×1012 m·kg-1.
2) 相比于HCA仅能形成较小的絮体, APAM投加后, 污泥絮体粒径显著增大, 从而形成了更多的水通道, 有利于污泥水分的释放.
3) HCA的加入仅可释放大部分毛细水, 而APAM的加入不仅能够释放毛细水, 还可以将大部分表面吸附水释放出来.
4) APAM的调理机制主要为氢键的吸附架桥作用, HCA的调理机制主要为电中和及去水化作用.
参考文献
| Boettcher M I, Boettcher M I, Bolt H M, et al. 2006. Excretion of mercapturic acids of acrylamide and glycidamide in human urine after single oral administration of deuterium-labelled acrylamide[J]. Archives of Toxicology, 80(2): 55-61. DOI:10.1007/s00204-005-0011-y |
| Bolto B, Gregory J. 2007. Organic polyelectrolytes in water treatment[J]. Water Research, 41(11): 2301-2324. DOI:10.1016/j.watres.2007.03.012 |
| Cao B, Zhang T, Zhang W, et al. 2021. Enhanced technology based for sewage sludge deep dewatering: A critical review[J]. Water Research, 189: 116650. DOI:10.1016/j.watres.2020.116650 |
| Chen F, Peldszus S, Elhadidy A M, et al. 2016. Kinetics of natural organic matter (NOM) removal during drinking water biofiltration using different NOM characterization approaches[J]. Water Research, 104: 361-370. DOI:10.1016/j.watres.2016.08.028 |
| 陈洋. 2017. 给水厂污泥陶粒的制备及其在废水除磷中应用的研究[D]. 济南: 山东大学. 74 |
| Dai Q, Ma L, Ren N, et al. 2018. Investigation on extracellular polymeric substances, sludge flocs morphology, bound water release and dewatering performance of sewage sludge under pretreatment with modified phosphogypsum[J]. Water Research, 142: 337-346. DOI:10.1016/j.watres.2018.06.009 |
| Forster C F. 2002. The rheological and physico-chemical characteristics of sewage sludges[J]. Enzyme and Microbial Technology, 30(3): 340-345. DOI:10.1016/S0141-0229(01)00487-2 |
| Foucat L, Lahaye M M. 2014. A subzero H-1 NMR relaxation investigation of water dynamics in tomato pericarp[J]. Food Chemistry, 158: 278-282. DOI:10.1016/j.foodchem.2014.02.100 |
| Huang P, Ye L. 2014. Enhanced dewatering of waste sludge with polyacrylamide/montmorillonite composite and its conditioning mechanism[J]. Journal of Macromolecular Science Physics, 53(9): 1465-1476. DOI:10.1080/00222348.2013.879783 |
| Joseph J, Jemmis E D. 2007. Red-, blue-, or no-shift in hydrogen bonds: A unified explanation[J]. Journal of the American Chemical Society, 129(15): 4620-4632. DOI:10.1021/ja067545z |
| Kulandaivelu J, Choi P M, Shrestha S, et al. 2020. Assessing the removal of organic micropollutants from wastewater by discharging drinking water sludge to sewers[J]. Water Research, 181: 115945. DOI:10.1016/j.watres.2020.115945 |
| Li X Y, Yang S F. 2007. Influence of loosely bound extracellular polymeric substances (EPS) on the flocculation, sedimentation and dewaterability of activated sludge[J]. Water Research, 41(5): 1022-1030. DOI:10.1016/j.watres.2006.06.037 |
| 刘彤. 2018. 净水厂排泥水处理技术的试验研究[D]. 哈尔滨: 哈尔滨工业大学. 72 |
| Mikkelsen L H, Gotfredsen A K, Agerb?k M L, et al. 1996. Effects of colloidal stability on clarification and dewatering of activated sludge[J]. Water Science and Technology, 34(3/4): 449. |
| Niu M, Zhang W, Wang D, et al. 2013. Correlation of physicochemical properties and sludge dewaterability under chemical conditioning using inorganic coagulants[J]. Bioresource Technology, 144: 337-343. DOI:10.1016/j.biortech.2013.06.126 |
| Peter J, Bruce J, Simon A. 2005. Breakage, regrowth, and fractal mature of natural organic matter flocs[J]. Environmental Science & Technology: ES&T, 39(7): 2307-2314. |
| Saveyn H, Curvers D, Thas O, et al. 2008. Optimization of sewage sludge conditioning and pressure dewatering by statistical modelling[J]. Water Research, 42(4): 1061-1074. |
| Sheng G, Yu H, Wang C. 2006. FTIR-spectral analysis of two photosynthetic hydrogen-producing[corrected] strains and their extracellular polymeric substances[J]. Applied Microbiology and Biotechnology, 73(1): 204-210. DOI:10.1007/s00253-006-0442-2 |
| Su Z, Li X, Yang Y. 2017. Regrowth ability and coagulation behavior by second dose: Breakage during the initial flocculation phase[J]. Colloids and surfaces. A, Physicochemical and Engineering Aspects, 527: 109-114. |
| Wang H, Hu H, Wang H, et al. 2019. Combined use of inorganic coagulants and cationic polyacrylamide for enhancing dewaterability of sewage sludge[J]. Journal of Cleaner Production, 211: 387-395. DOI:10.1016/j.jclepro.2018.11.208 |
| Wang H, Wang H, Hu H, et al. 2017. Applying rheological analysis to understand the mechanism of polyacrylamide (PAM) conditioning for sewage sludge dewatering[J]. RSC Advances, 7(48): 3274-3282. |
| Wang J, Tan Y, Pan Y, et al. 2019. Altering extracellular biopolymers and water distribution of waste activated sludge by Fe(Ⅱ) persulfate oxidation with natural zeolite and polyelectrolyte as skeleton builders for positive feedbacks to dewaterability[J]. ACS sustainable Chemistry & Engineering, 7(19): 16549-16559. |
| Wang Z, Gao M, Wang S, et al. 2014. Effect of hexavalent chromium on extracellular polymeric substances of granular sludge from an aerobic granular sequencing batch reactor[J]. Chemical Engineering Journal, 251: 165-174. DOI:10.1016/j.cej.2014.04.078 |
| Wu H, Liu Z, Yang H, et al. 2016. Evaluation of chain architectures and charge properties of various starch-based flocculants for flocculation of humic acid from water[J]. Water Research, 96: 126-135. DOI:10.1016/j.watres.2016.03.055 |
| Xiao K, Pei K, Wang H, et al. 2018. Citric acid assisted Fenton-like process for enhanced dewaterability of waste activated sludge with in-situ generation of hydrogen peroxide[J]. Water Research, 140: 232-242. DOI:10.1016/j.watres.2018.04.051 |
| 谢浩辉. 2011. 污泥的结合水测量和热水解试验研究[D]. 杭州: 浙江大学. 83 |
| 熊巧. 2018. 活化过硫酸盐-生物质复合调理污泥脱水性能与机理研究[D]. 武汉: 武汉大学. 176 |
| Yao M, Chen T, Ran Z, et al. 2020. Integral evaluation of production safety and genotoxicity of recycling residual sludge for drinking water treatment plants[J]. Environmental Technology, 30(10): 1-41. |
| Zhou Z, Yang Y, Li X, et al. 2018. Optimized removal of natural organic matter by ultrasound-assisted coagulation of recycling drinking water treatment sludge[J]. Ultrasonics Sonochemistry, 48: 171-180. |
| Zhu C, Li F, Zhang P, et al. 2018. Combined sludge conditioning with NaCl-cationic polyacrylamide-rice husk powders to improve sludge dewaterability[J]. Powder Technology, 336: 191-198. |
| 周瑜. 2016. 二元缔合溶液体系的结构和分子间相互作用研究[D]. 北京: 清华大学. 113 |
