 , 梁嘉林1,2, 曾刘婷1, 关智杰1, 廖小健1, 周思宇1, 黄绍松1, 孙水裕1,3
, 梁嘉林1,2, 曾刘婷1, 关智杰1, 廖小健1, 周思宇1, 黄绍松1, 孙水裕1,3

1. 广东工业大学环境科学与工程学院, 广州 510006;
2. 香港浸会大学生物系生物资源与农业研究所, 香港 999077;
3. 广东环境保护工程职业学院, 佛山 528216
收稿日期: 2020-11-18; 修回日期: 2021-01-06; 录用日期: 2021-01-26
基金项目: 国家重点研发计划(No.2018YFD0800700);广东省科技计划项目(No.2017A030223007);广东省环保厅专项资金项目(2017);佛山市科技创新项目(No.2016AG100482);广东高校省级重点平台和重大科研项目(No.2017GKZDXM007)
作者简介: 杨贤(1995-), 男, E-mail: yonsion@foxmail.com
通讯作者(责任作者): 孙水裕, E-mail: sysun@gdut.edu.cn
摘要:城市污水厂二级处理出水中含有大量的溶解性有机物(Dissolved organic matters,DOM)会对生物和受纳水体构成潜在的危害,因此有必要对二级处理出水进行深度处理.本研究以农业废弃物茶叶渣为原料,通过对废弃茶叶改性和负磁制备一种磁性废茶生物炭(Fe-tea biochar,Fe-TB),用于活化过一硫酸盐(Peroxymonosulfate,PMS)氧化降解水中的腐殖酸(Humic acid,HA)和富里酸(Fulvic acid,FA).考察Fe-TB铁负载量、PMS浓度、Fe-TB投加量、初始pH、HA和FA的初始浓度对Fe-TB/PMS体系氧化降解HA和FA的影响.结果表明,在铁碳比为2/1(W/W)、PMS=0.2 g·L-1,2Fe-TB投加量分别为0.6 g·L-1(HA体系)和0.4 g·L-1(FA体系)、初始pH=7条件下,50 min时对初始浓度为20 mg·L-1的HA和FA的去除率分别达到95.3%和77.4%;经过4次重复循环使用,HA和FA的去除率均在59.0%以上,表明其良好的稳定性和重复使用性.淬灭实验及电子顺磁共振(EPR)分析结果证明2Fe-TB/PMS体系以单线态氧(1O2)为主要氧化活性物种降解HA和FA.实际二级处理出水中的DOM降解结果表明,2Fe-TB /PMS体系可以有效降解实际水体中的DOM,具有良好的应用前景.
关键词:磁性废茶生物炭过一硫酸盐(PMS)腐殖酸(HA)富里酸(FA)单线态氧(1O2)
Efficient degradation of humic acid and fulvic acid in water by magnetic waste tea biochar activated persulfate
YANG Xian1
 , LIANG Jialin1,2, ZENG Liuting1, GUAN Zhijie1, LIAO Xiaojian1, ZHOU Siyu1, HUANG Shaosong1, SUN Shuiyu1,3
, LIANG Jialin1,2, ZENG Liuting1, GUAN Zhijie1, LIAO Xiaojian1, ZHOU Siyu1, HUANG Shaosong1, SUN Shuiyu1,3

1. School of Environmental Science and Engineering, Guangdong University of Technology, Guangzhou 510006;
2. Institute of Bioresource and Agriculture, Department of Biology, Hong Kong Baptist University, Hong Kong SAR 999077;
3. Guangdong Polytechnic of Environmental Protection Engineering, Foshan 528216
Received 18 November 2020; received in revised from 6 January 2021; accepted 26 January 2021
Abstract: Abundant dissolved organic matters (DOM) in the secondary effluent from the wastewater treatment plants would cause potential harm to organisms and the receiving water. Therefore, it is deemed necessary to find out an advanced method for the secondary effluent treatment. In this study, a modified Fe-tea biochar (Fe-TB) was successfully prepared using the agricultural tea wastes. The Fe-TB was used to activate peroxymonosulfate (PMS) and their combination could oxidize the humic acid (HA) and fulvic acid (FA) in the wastewater. The effects of the iron loading of the Fe-TB, PMS concentrations, Fe-TB dosages, and initial pH as well as the concentrations of HA and FA on their degradation in Fe-TB/PMS process were investigated. Results showed that the removal efficiency of HA with the initial concentration of 20 mg·L-1 was 95.3%, while FA with the same concentration was 77.4% at 50 min under the conditions of 2/1 (W/W), 0.2 g·L-1 of PMS, Fe-TB dosage of 0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), respectively, and initial pH 7. After recycling 4 times, the removal efficiency of HA and FA were both over 59.0%, indicating that 2Fe-TB/PMS system has an excellent stability. The results of the quenching free radical experiments and electron paramagnetic resonance (EPR) showed that in the 2Fe-TB/PMS system, 1O2 as the main reactive oxygen species could efficiently degrade HA and FA. Furthermore, the 2Fe-TB/PMS system could effectively degrade DOM in the actual secondary effluent, which confirmed the efficiency of this system. Thus, the 2Fe-TB/PMS system has a promising application prospect.
Keywords: magnetic waste tea biocharperoxymonosulfatehumic acidfulvic acidsinglet oxygen
1 引言(Introduction)动植物残体经微生物分解转化, 在河流、湖泊等水环境中累积了大量的腐殖酸(Humic Acid, HA)和富里酸(Fulvic Acid, FA)等溶解性有机物(dissolved organic matters, DOM), 其最高浓度达到30 mg·L-1(地表水)(Wang et al., 2012;Zhou et al., 2019).值得注意的是, 近年来, 在污水处理厂二级处理出水中也检测出较高浓度的DOM, 其主要成分为残留的不可生物降解的有机物(HA和FA)(金鹏康等, 2015;Shi et al., 2020), 存在二次污染受纳水体的风险(Zhang et al., 2020).在水环境中, 腐殖质的浓度(高达500~1500 mg·L-1)会影响水体的色度;此外, 腐殖质还会与水体残留的农药或者金属离子形成络合物, 从而影响金属离子的迁移转化并增大其生物毒性(Tian et al., 2018).在饮用水氯化消毒过程中, 腐殖质会与含氯消毒剂反应生成具有“三致效应”的消毒副产品, 对人类健康造成威胁(Zhou et al., 2019).由此可知, 水环境中腐殖质的累积将会对生物和受纳水体构成严重威胁.因此, 找到一种高效去除水体中腐殖质的方法意义重大.
目前, 基于过硫酸盐(Persulfate, PS)的高级氧化技术(Advanced oxidation process, AOP)由于其处理效率高、氧化性能强、pH适应范围广等优点, 而被广泛应用于有机废水、污泥深度脱水、土壤地下水原位修复等领域(Liu et al., 2016).过硫酸盐分为过一硫酸盐(Peroxymonosulfate, PMS)和过二硫酸盐(Perdisulfate, PDS).与PDS相比, PMS由于其自身结构的不对称性, 更容易被活化产生强氧化性的硫酸根自由基(SO4-·)或单线态氧(1O2), 更具有应用前景(Yang et al., 2020).一般而言, PMS可通过光(Fu et al., 2019)、热(Hu et al., 2020)、碳基材料(Wang et al., 2019)和过渡金属(Ni et al., 2019)等活化产生大量活性氧(reactive oxygen species, ROS)从而达到高效去除有机污染物的效果(Wang et al., 2019).在这些活化的方法中, 碳基材料由于无需消耗能量被认为是一种有效活化PMS的催化剂.生物炭是以废弃生物质为原材料, 在限氧条件下, 经高温裂解得到的产物(Zhang et al., 2019), 且由于其制备简单、价格低廉和环境友好等优点而备受关注(Wu et al., 2019).我国作为世界最大的产茶大国, 在生产茶叶的过程中会伴生大量的茶渣、茶沫和枝梗等茶叶副产品(Lee et al., 2012).仅2018年在我国产生的茶叶副产品便达27万吨之多;经茶饮料行业的加工后, 也会产生90%以上的茶叶副产品, 造成大量的资源浪费(Cai et al., 2018).由于废茶具有较高的碳含量, 近年来被用于制备生物炭的前驱体, 有一定的潜在优势.Auta等(2011)和宋磊等(2014)制备出的废茶生物炭比表面积均大于850 m2·g-1, 该比表面积是农业废弃物生物炭(包括桉树叶生物炭、树叶生物炭和小麦秸秆)的4.5~20倍(郜礼阳等, 2018;崔志文等, 2020;Liu et al., 2021).因此, 废茶生物炭具有一定的应用潜力.
生物炭活化PMS虽然能有效降解持久性有机污染物, 然而生物炭难以回收再用、表面活性位点种类较少、含量较低等缺点限制其进一步推广(Hao et al., 2020;李小娟等, 2020).近年来, 生物炭负载磁性材料不仅可以弥补过渡金属离子活化过硫酸盐而导致体系存在大量金属离子的缺点, 而且有利于催化剂的回收再用(Li et al., 2020), 最终可以有效提高生物炭的催化活性.Rong等(2019)利用香蕉皮提取物制成负载铁基的磁性生物炭活化过硫酸盐产生OH·和SO4-·降解双酚A, 结果表明, 在20 min内将双酚A完全降解.与单独生物炭活化过硫酸盐相比, 磁性生物炭的速率常数几乎是单独生物炭的两倍, 而且反应时间节省一半.Fu等(2019)实验探究负载MnFe2O4的磁性生物炭活化PMS降解Orange Ⅱ的效果, 研究发现该反应体系可实现Orange Ⅱ的完全降解, 而且该磁性生物炭可通过磁场回收再用, 进一步降低催化剂成本, 具有良好的前景.然而, 目前采用磁性生物炭活化PMS对水体中的DOM进行深度处理的研究较少, 仍未知该处理过程的降解效果.
鉴于此, 本研究以废弃茶叶作为原料, 采用ZnCl2作为活化剂制备出改性废茶渣生物炭, 然后采用共沉淀法对生物炭进行铁基负载, 并活化PMS降解水体中HA和FA.本文主要深入探讨磁性生物炭活化PMS对HA和FA的降解及动力学分析, 探究磁性生物炭用量、PMS浓度、初始pH对磁性生物炭活化PMS降解HA和FA的影响, 以及在最优条件下, 探究磁性生物炭活化PMS对不同初始浓度HA和FA降解效率的影响, 并对磁性生物炭进行相应的表征, 分析其降解机理.最后采用实际水体作为研究对象, 进一步验证该体系的可行性, 为其在后续的工程实践中奠定基础.
2 材料与方法(Materials and methods)2.1 材料试剂本实验采用的废茶叶为铁观音茶叶末, 购自福建省泉州市某茶叶专业合作社;腐殖酸(HA)、过一硫酸盐(KHSO5·0.5KHSO4·0.5K2SO4, PMS)、六水氯化铁(FeCl3·6H2O)、七水硫酸亚铁(FeSO4·7H2O)、5, 5-二甲基-1吡咯氮-N-氧化物(DMPO)、4-氨基-2, 2, 6, 6四甲基哌啶(TEMP)均购自上海阿拉丁生化科技股份有限公司;黄腐酸(富里酸, FA)、氯化锌(ZnCl2)、氢氧化钠(NaOH)、糠醇(FFA)均购自上海麦克林生化科技有限公司;硫酸(H2SO4)购自广州化学试剂厂;甲醇(MeOH)购自广东光华科技股份有限公司;叔丁醇(TBA)购自天津市大茂化学试剂厂;叠氮化钠(NaN3)购自天津市福晨化学试剂厂;实验用水均为超纯水.
2.2 磁性生物炭的制备将废茶叶洗净于105 ℃烘干后, 取适量经粉碎的废茶叶末与ZnCl2以质量比1:1于烧杯中, 加入适量超纯水后静置一段时间, 烘干得到固体, 将所得固体置于管式炉中, 通入N2保护, 在500 ℃下保温1 h, 冷却取出.用(1+9)盐酸洗去残留ZnCl2后用超纯水洗涤至滤液为中性, 烘干后得到改性生物炭(TB).取适量TB加入到不同铁碳比(m/m)的Fe3+、Fe2+混合溶液中, 超声20 min使TB在溶液中分散均匀, 用NaOH调节pH至11, 搅拌2 h后陈化24 h, 用超纯水和乙醇反复洗涤数次至上清液为中性, 烘干得到磁性生物炭, 记为1Fe-TB(铁碳比为1/1)、2Fe-TB(铁碳比为2/1)、3Fe-TB(铁碳比为3/1)和4Fe-TB(铁碳比为4/1).
2.3 腐殖酸和富里酸模拟废水配制腐殖酸模拟废水:取1.000 g腐殖酸固体和4.000 g氢氧化钠固体于烧杯中, 加入超纯水搅拌, 使腐殖酸和氢氧化钠充分溶解后移入1000 mL容量瓶中, 并加超纯水定容至1000 mL, 置于冰箱冷藏保存.
富里酸模拟废水:取1.000 g富里酸固体溶于超纯水中, 将所得溶液移至容量瓶中并定容至1000 mL, 置于冰箱冷藏保存.实验过程中所需浓度的腐殖酸和富里酸溶液均根据母液稀释, 现配现用.
2.4 腐殖酸和富里酸降解实验取100 mL已知浓度的腐殖酸/富里酸溶液于250 mL锥形瓶中, 加入不同投加量的Fe-TB和PMS后置于180 r·min-1、30 ℃条件下的恒温摇床中振荡反应, 按预定时间取样3.5 mL, 加入0.5 mL淬灭剂后用0.45 μm微孔滤膜过滤, 采用UV254表征腐殖酸和富里酸的含量(郑可等, 2012), UV254采用紫外分光光度计(UV-2100, 北京瑞利)测定.
2.5 分析方法采用扫描电子显微镜(SEM, Zeiss Auriga, 美国赛默飞世尔)、振动样品磁强计(VSM, PPMS-9, 美国Quantum Design)、X射线粉末衍射仪(XRD, SmartLab, 日本理学)、傅里叶变换红外光谱仪(FT-IR, iS50R, 美国THEMOR-FILSHER)、全自动比表面及孔隙度分析仪(BET, ASAP2460, 美国麦克)对2Fe-TB进行表征;采用三维荧光光谱仪(3D-EEM, F-4600, 日本日立)分析水体中DOM的变化;采用总有机碳分析仪(TOC-LCPH, 日本岛津公司)测定反应前后TOC浓度变化;采用电子顺磁共振波谱仪(EPR, EMXplus-10/12, 德国Bruker)分析反应体系的活性物种;采用原子吸收分光光度计(ABS, TAS-990, 北京普析)测定反应体系铁溶出浓度.
3 结果与讨论(Results and discussion)3.1 2Fe-TB的表征3.1.1 扫描电镜和理化性质分析图 1和表 1分别为3种生物炭的SEM图及其元素分析和比表面积的结果.如图所示, 原始生物炭(图 1a)表面较为光滑, 具有少部分孔结构, 以大孔为主, 平均孔径为11.584 nm, 因其不发达的孔结构, 原始生物炭的比表面积仅有1.690 m2·g-1;经过ZnCl2改性后生物炭(图 1b)表面粗糙、蓬松, ZnCl2使废茶叶表面进一步芳化从而形成微孔结构(赵朔等, 2012), 因此改性生物炭的孔结构更为发达, 其比表面积显著增加至890.885 m2·g-1, 总孔容也从原始生物炭的0.0049 cm3·g-1增加至0.5043 cm3·g-1;而经过改性和负磁后, 2Fe-TB(图 1c)表面附着了大量小球状颗粒物, 说明磁性粒子成功负载到改性生物炭表面, 而2Fe-TB的比表面积为502.830 m2·g-1, 低于改性生物炭的比表面积, 原因是磁性粒子负载到改性生物炭的表面及部分孔隙中.与树叶生物炭或秸秆生物炭(比表面积低于190 m2·g-1)相比(郜礼阳等, 2018;崔志文等, 2020;Liu et al., 2021), 废茶生物炭显示出发达的孔径结构(Yagmur et al., 2012).此外, EDS元素分析结果表明, 2Fe-TB主要的组成元素为C、O、N和Fe(表 1), 这也证实改性生物炭负磁成功.
图 1(Fig. 1)
 |
| 图 1 3种生物炭的SEM图像 (a.原始生物炭, b.改性生物炭, c.磁性生物炭) Fig. 1SEM images of three kinds of biochar (a. Raw biochar, b. Modified biochar, c. 2Fe-TB) |
表 1(Table 1)
| 表 1 3种生物炭的元素分析和比表面积 Table 1 Elemental analysis and BET of three kinds of biochar | ||||||||||||||||||||||||||||||||||||||||
表 1 3种生物炭的元素分析和比表面积 Table 1 Elemental analysis and BET of three kinds of biochar
| ||||||||||||||||||||||||||||||||||||||||
3.1.2 2Fe-TB的磁学性能利用VSM分析2Fe-TB的磁学性能, 结果如图 2a所示.2Fe-TB的饱和磁感应强度为12.22 emμ·g-1, 说明2Fe-TB具有较好的磁性.2Fe-TB的磁滞回线经过原点, 且以原点为中心呈中心对称, 剩余磁感应强度和矫顽力接近于0, 说明2Fe-TB具有超顺磁性, 可通过外加磁场进行固液分离, 有利于后续回收利用.
图 2(Fig. 2)
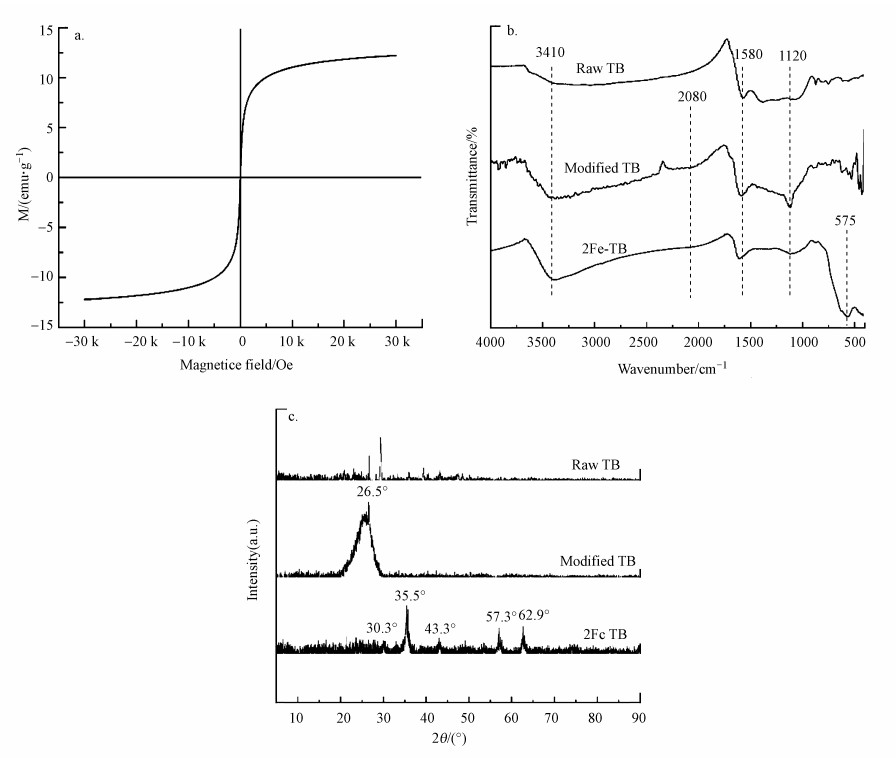 |
| 图 2 2Fe-TB的磁滞回线(a)、3种生物炭的FT-IR谱图(b)及XRD谱图(c) Fig. 2Magnetization curves of 2Fe-TB(a), FT-IR(b) and XRD(c) of three kinds of biochar |
3.1.3 红外光谱分析图 2b为3种生物炭的FT-IR谱图.结果显示, 经ZnCl2改性的生物炭和负载铁后的生物炭, 其表面的官能团明显比原始生物炭更丰富.3种生物炭在3410 cm-1左右的峰为羟基(─OH)的伸缩振动峰, 在1580 cm-1左右的峰为芳环C=C的伸缩振动峰, 在1120 cm-1左右的峰为C─O伸缩振动吸收峰(Song et al., 2020);经ZnCl2改性的生物炭和负载铁后的生物炭在2080 cm-1左右出现较弱的叁键和累积双键峰(R─C≡C─H), 而2Fe-TB在575 cm-1左右新增Fe─O的特征伸缩振动峰, 进一步说明2Fe-TB成功负磁(杜文琪等, 2018).
3.1.4 XRD分析通过XRD研究3种生物炭的晶体结构, 如图 2c所示, 原始生物炭和经ZnCl2改性生物炭在2θ=26.5°均出现有序碳层结构的特征峰, 对应生物炭中石墨结构的(002)平面(Hu et al., 2017), 且改性生物炭的衍射峰较原始生物炭宽, 呈小山丘状, 表明其结晶度降低, 是无定形碳结构, 有利于增加改性生物炭的比表面积(Oh et al., 2015), 与BET测试结果相符.2Fe-TB的XRD图谱说明, 其表面的晶体结构和衍射峰出现明显的变化, 在2θ=30.3°、35.5°、43.3°、57.3°和62.9°出现的特征衍射峰与磁铁矿(Fe3O4)的特征峰相一致(Yan et al., 2011), 分别对应磁铁矿晶体结构的(220)、(311)、(400)、(511)以及(440)平面, 说明2Fe-TB存在Fe3O4晶体结构, 与FT-IR的表征结果相一致.
3.2 Fe-TB/PMS体系降解水中HA和FA的可行性图 3显示不同体系下HA和FA的降解效率及动力学拟合.由图 3c、3d结果可知, 不同反应体系降解HA和FA的过程均符合伪一级动力学.图 3a、3b结果表明, 单独PMS存在时, 反应50 min后HA和FA的去除率仅有10.1%和14.7%, 说明PMS自发反应降解HA和FA的效率较低.经TB和2Fe-TB反应50 min后, HA的去除率分别达到44.2%和30.2%, 而FA的去除率分别达到22.5%和29.7%, 这说明TB和2Fe-TB均表现出一定的吸附性能.在2Fe-TB活化PMS的反应体系中, 反应50 min后, HA和FA的去除率分别为95.3%和77.4%, TB/PMS体系与Fe3O4/PMS体系去除率提升16.4%以上, 表明2Fe-TB活化PMS能有效降解HA和FA.比较各反应体系降解HA和FA, 经催化剂活化PMS降解HA和FA在反应前5 min均可达到较高的去除率, 然后反应速率有所减缓, 这一方面可能是催化剂的加入提供大量的活性位点活化PMS, 增加单位时间内产生的活性物种数量, 使HA和FA被快速降解;另一方面, 反应初始HA和FA浓度较高, 活性物种可快速与污染物结合进行氧化降解, 因此在前5 min反应速率较快, 而在5 min后, 反应体系内HA和FA的浓度大幅降低, 同时活性物种被大量消耗, 因此导致反应速率降低(Feng et al., 2015;Yang et al., 2018).此外, 通过对比不同反应体系降解HA和FA的伪一级动力学的标贯速率常数k值(表 2)可知:当仅使用PMS或仅使用TB或2Fe-TB时, 其对应的速率常数k值均处于较低的水平, 分别为0.0013~0.0055 min-1(HA)和0.0026~0.0046 min-1(FA), 在Fe3O4/PMS和TB/PMS体系中, k值均有不同程度的升高, 这进一步说明PMS经过活化后可以产生强氧化性自由基或非自由基, 进而提高反应效率.当2Fe-TB/PMS降解HA和FA时, k值分别升高至0.0269 min-1和0.0089 min-1, 表明2Fe-TB/PMS是一种可以高效降解HA和FA的方法.这归因于2Fe-TB表面的磁性粒子和生物炭表面的活性位点可以协同高效活化PMS, 从而产生大量强氧化性活性物种, 提高HA和FA的去除率(徐劼等, 2020).
图 3(Fig. 3)
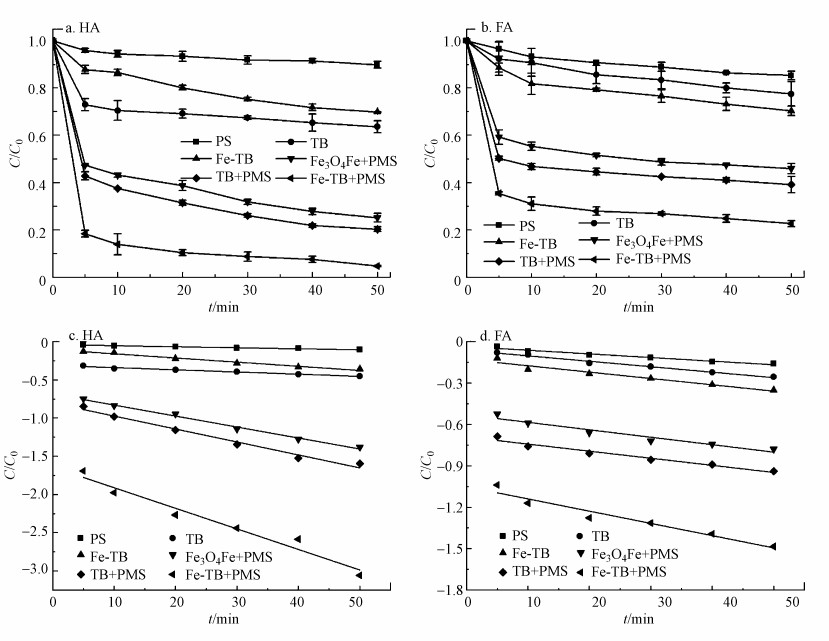 |
| 图 3 不同反应体系对HA和FA降解的影响及动力学拟合 (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), Fe3O4=0.6 g·L-1(HA)和0.4 g·L-1(FA), pH=7.0) Fig. 3Degradation kinetics of HA and FA in different systems (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), Fe3O4=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), pH=7.0) |
表 2(Table 2)
| 表 2 不同反应降解HA和FA的伪一级动力学速率常数 Table 2 The pseudo first-order kinetic rate constants of degradation of HA and FA in different systems | |||||||||||||||||||||||||||||||||||||||||
表 2 不同反应降解HA和FA的伪一级动力学速率常数 Table 2 The pseudo first-order kinetic rate constants of degradation of HA and FA in different systems
| |||||||||||||||||||||||||||||||||||||||||
3.3 铁负载量对HA和FA降解的影响由于不同的铁负载量对催化剂的催化性能有一定影响(Yuan et al., 2017), 因此有必要考察不同铁负载量对HA和FA降解的影响.如图 4所示, 在PMS存在的条件下, 当铁碳比从1/1增加到2/1(W: W)时, Fe-TB/PMS体系对HA和FA的去除率随之升高.在铁碳比为2/1时(即2Fe-TB)显示出最高的HA和FA的去除率, 分别高达95.3%和77.4%(50 min).然而当铁碳比从2/1增加到4/1时, HA和FA的去除率逐渐降低, 分别为74.6%和71.6%(50 min), 这是由于投加过量的铁使Fe3O4颗粒团聚导致生物炭活性位点失活和比表面积的降低, 进一步减少活性位点, 最终降低材料的催化活性(张倩等, 2019;Rong et al., 2019).由此可知, 2Fe-TB的催化特性最佳.根据上述分析并考虑经济因素, 本文以铁碳比为2/1作为Fe-TB的最佳铁负载量用于后续的研究.
图 4(Fig. 4)
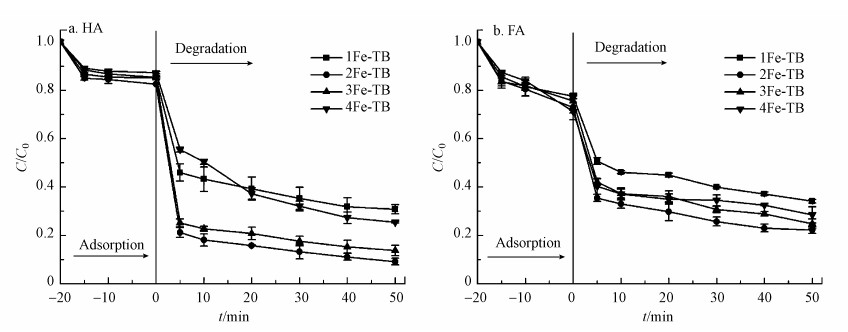 |
| 图 4 铁负载量对HA和FA降解的影响 (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, (1-4)Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), pH=7.0) Fig. 4Effect of Fe loading on HA and FA degradation (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, (1-4) Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), pH=7.0) |
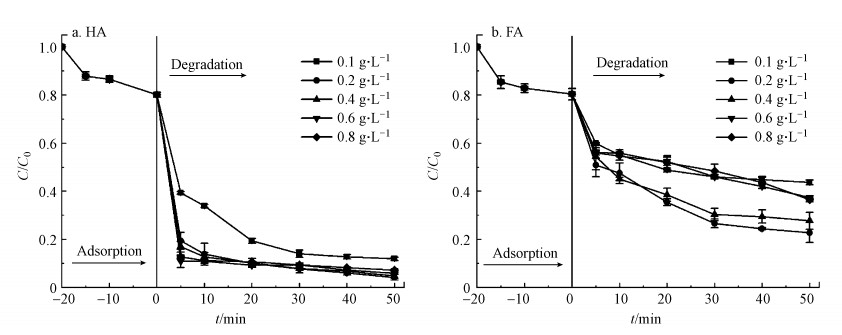
3.4 2Fe-TB活化PMS降解HA和FA的条件优化3.4.1 PMS浓度对HA和FA降解的影响不同PMS浓度对HA和FA降解的影响如图 5所示.随着PMS浓度的增加, HA和FA浓度均呈现先大幅降低后趋于平缓的趋势.当PMS的浓度从0.1 g·L-1增大到0.2 g·L-1, HA和FA的去除率分别从88.1%和56.3%提高到95.3%和77.4%, 这是因为随着PMS浓度的增大, 2Fe-TB表面的活性位点能充分与PMS反应, 产生更多强氧化性的活性物种, 最终实现HA和FA的高效降解(杨珂等, 2019).然而当PMS浓度逐步增加到0.8 g·L-1时, HA和FA的去除率随之降低.这主要是过多的PMS使其产生自淬灭反应, 过量的HSO5-和SO4-·会反应产生SO5-·(式(1)、(2))(Zhou et al., 2020;Liu et al., 2020), 从而降低降解效率.因此, 选择0.2 g·L-1的PMS浓度作为实验的最佳浓度.
 | (1) |
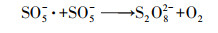 | (2) |
 |
| 图 5 PMS浓度对HA和FA降解的影响 (HA=20 mg·L-1, FA=20 mg·L-1, 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), pH=7.0) Fig. 5Effects of PMS concentration on HA and FA degradation (HA=20 mg·L-1, FA=20 mg·L-1, 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), pH=7.0) |
3.4.2 2Fe-TB投加量对HA和FA降解的影响图 6a、6b显示2Fe-TB投加量对HA和FA降解的影响.结果表明, HA的去除率随着催化剂投加量的增加而逐渐上升, 这是因为随着2Fe-TB投加量的增加, 能提供更多的活性位点供PMS反应, 进而产生更多活性物种(Khodadadi et al., 2020).而2Fe-TB的不同投加量对HA的吸附效果差异不大.当2Fe-TB的投加量从0.6 g·L-1增加到1.0 g·L-1时, HA的去除率仅从95.3%上升到99.1%, 由此可见, HA的去除率的提升幅度不大.考虑到药剂成本, 选择0.6 g·L-1为2Fe-TB活化PMS氧化降解HA的最优投加量.类似地, 在降解FA过程中, 当2Fe-TB的投加量从0.2 g·L-1增加到0.4 g·L-1, FA的去除率从66.1%上升至77.4%, 表明FA被大幅降解.这是由于2Fe-TB催化剂大量存在时, 能提供更多活性位点参与PMS的催化氧化过程, 进而增加反应体系中活性物种的数量(Wang et al., 2017), 最终提高FA的去除率;当2Fe-TB的投加量继续增大至1.0 g·L-1时, 2Fe-TB对FA的吸附量增大, 但在经过50 min的降解后, FA的去除率没有明显增幅, 这可能受限于PMS的浓度以及大量的2Fe-TB会在溶液中团聚从而减少活性位点, 导致降解效率降低.上述结果表明, 过多的2Fe-TB投加量并不能进一步提高HA和FA的去除率(Luo et al., 2020;李立等, 2020).所以选取0.6 g·L-1和0.4 g·L-1的2Fe-TB投加量分别作为降解HA和FA的最佳催化剂投加量.
3.4.3 初始pH对HA和FA降解的影响根据此前的研究, 催化剂表面的零电荷点会影响反应效率(董正玉等, 2018).实验使用0.1 mol·L-1 H2SO4和0.1 mol·L-1 NaOH调节初始pH, 考察不同初始pH对HA和FA降解的影响, 如图 6c、6d所示.当pH为3、5、7时, HA的去除率均在90%左右, FA的去除率均在76%左右, 说明在酸性及中性条件下有利于氧化反应的进行, 促进强氧化性活性物种的产生, 最终实现目标污染物的高效降解(王莹等, 2017);在pH为9和11时, HA和FA的去除率显著下降, 说明碱性条件下阻碍反应的进行.此外, 在不同初始pH的HA和FA中, 2Fe-TB的吸附性能也随着pH的升高而逐渐降低.通过zeta电位分析仪测试2Fe-TB在不同pH值的zeta电位, 如图 6e所示;而HA和FA的零电荷点分别约为1.6和3.0(Zhang et al., 2016), 即当pH分别大于1.6和3.0时, HA和FA带负电.在pH为3、5时, 2Fe-TB表面带正电, 增强其与带负电的HA和FA之间的静电相互作用, 提高2Fe-TB对HA和FA的吸附效率, 这也使得HA和FA的去除率得以维持较高的水平;pH为9和11时, 2Fe-TB表面带负电, 不仅使2Fe-TB与HA和FA产生静电排斥, 同时抑制2Fe-TB与HSO5-之间的静电作用, 导致活化PMS效率降低, 最终降低HA和FA的去除率.
图 6(Fig. 6)
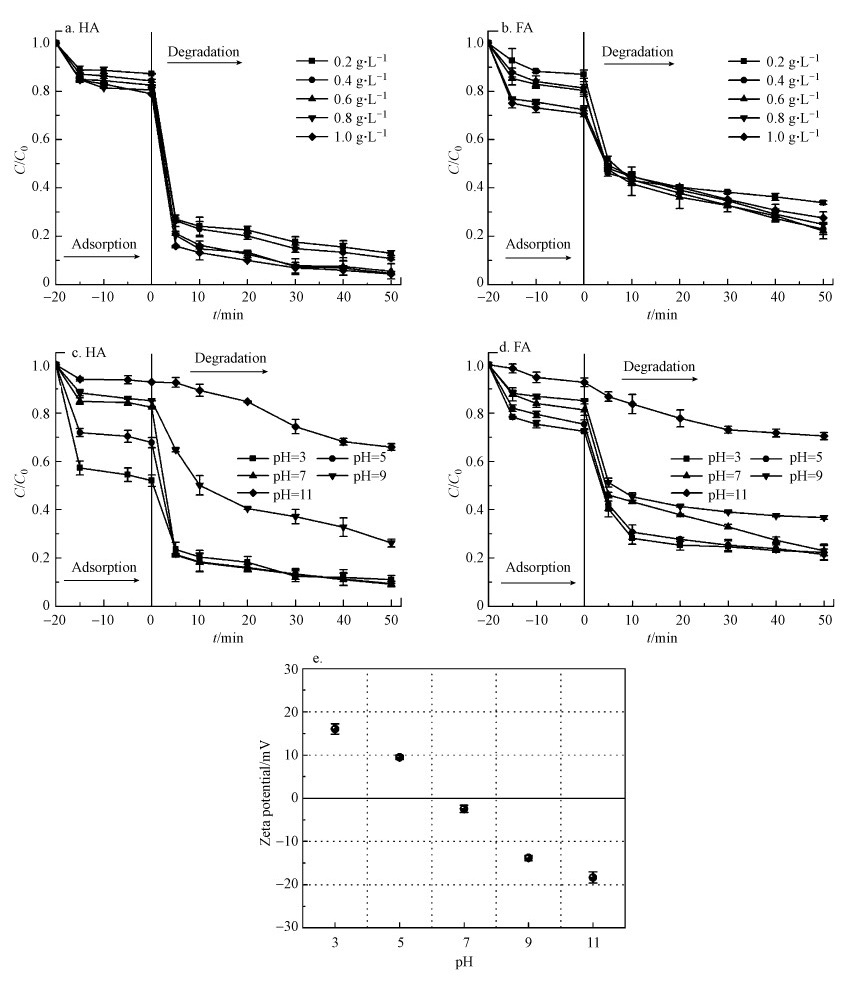 |
| 图 6 2Fe-TB投加量对HA(a)和FA(b)降解的影响 (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, pH=7.0);初始pH对HA(c)和FA(d)降解的影响(HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA))及2Fe-TB在不同pH的Zeta电位(e) Fig. 6Effects of 2Fe-TB dosages on HA (a) and FA(b) degradation (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, pH=7.0); Effect of initial pH on HA(c) and FA(d) degradation (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA)) and Zeta potential of 2Fe-TB at different pH(e) |
3.4.4 HA和FA初始浓度的影响图 7为2Fe-TB/PMS对不同初始浓度的HA和FA降解效果.随着初始浓度的增加, HA和FA的降解速率随之降低.可能的原因是①在高浓度反应体系中, 2Fe-TB和PMS的投加量不足, 导致产生的自由基(SO4-·、OH·)或非自由基(1O2)不足以完全降解高浓度的目标污染物;②随着污染物初始浓度的增加, 反应过程中产生的中间产物也相对增多, 这使得其与目标污染物竞争降解所需的活性物种, 从而降低去除率(张黎明等, 2016).
图 7(Fig. 7)
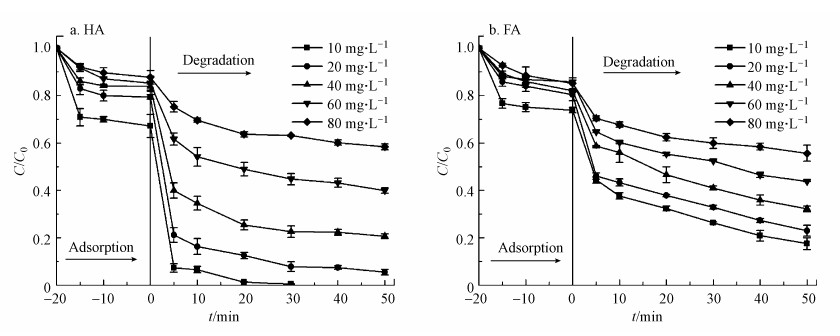 |
| 图 7 初始浓度对HA和FA降解的影响 (PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), pH=7.0) Fig. 7Effect of initial concentration on HA and FA degradation (PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), pH=7.0) |
3.5 反应机理探究3.5.1 三维荧光光谱和TOC分析三维荧光(3D-EEM)是一种用于分析水体DOM的组成结构的快捷灵敏的方法.根据Wang等(2010)的研究, 可以将3D-EEM图谱划分为6个区域, 表 3详细显示6个荧光区域的分布.同时采用荧光区域指数法(fluorescence regional integration, FRI)对有机物含量进行量化分析(黄锦佳等, 2020).图 8a~8d为经2Fe-TB/PMS反应前后水中HA和FA的三维荧光光谱变化情况.反应前HA和FA三维荧光图谱主要出现Ⅱ峰(富里酸)、Ⅳ峰(类芳香腐殖酸)和Ⅵ峰(聚羧酸类腐殖酸), 这与Tian等(2018)的研究相一致.经过50 min的反应后, HA和FA荧光图谱的荧光强度显著下降, 光谱形状也发生明显的变化, 最终相应的特征峰几乎消失且没有出现新的荧光物质, 进一步确认2Fe-TB/PMS能有效降解HA和FA.反应后HA和FA的TOC分别降至3.42 mg·L-1和4.66 mg·L-1, 去除率分别为60.8%和48.9%, 结果与UV254和三维荧光表征结果相一致, 部分剩余的TOC可能由于HA和FA在降解过程中未被完全矿化为CO2和H2O, 而转化为有机中间产物所导致的(聂明华等, 2018).
表 3(Table 3)
| 表 3 荧光光谱区域分布 Table 3 The distributions of fluorophore regions | |||||||||||||||||||||
表 3 荧光光谱区域分布 Table 3 The distributions of fluorophore regions
| |||||||||||||||||||||
图 8(Fig. 8)
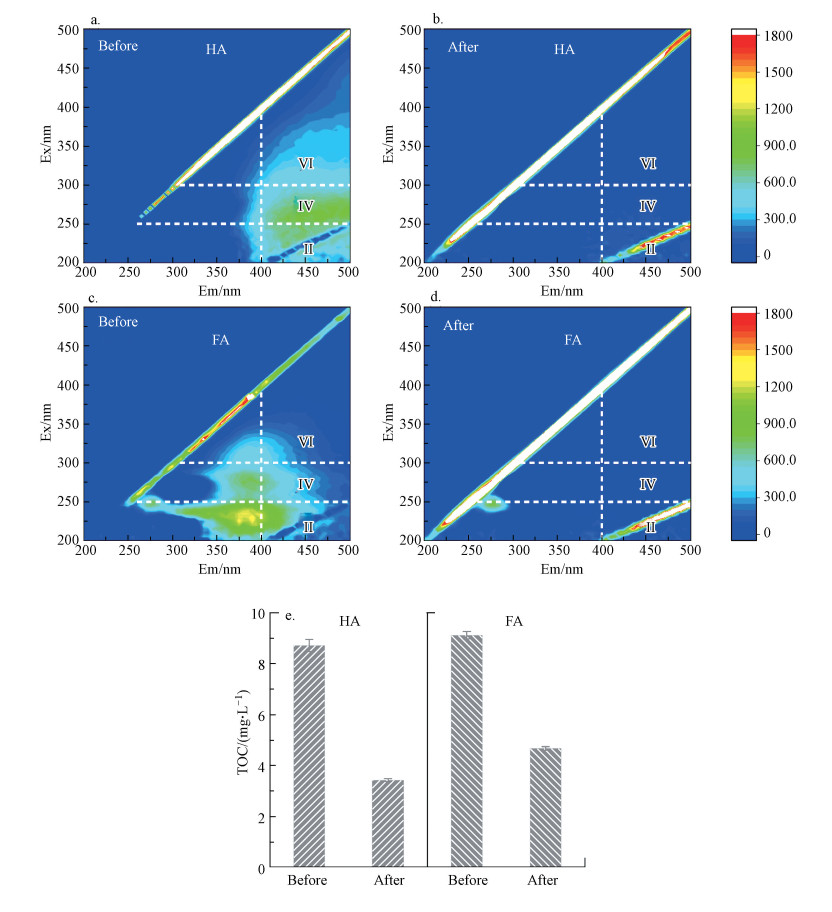 |
| 图 8 反应前后HA和FA的荧光光谱特征和TOC变化 Fig. 8The fluorescence spectra and TOC changes of HA and FA before and after the reaction |
表 4显示HA和FA反应前后体系中有机物的FRI结果, 量化反应前后体系中有机物的变化.在经过2Fe-TB/PMS反应后, HA和FA中的3种有机物的FRI值均有大幅度下降, 进一步说明体系中芳香族等大分子被有效降解, 该结果与前文经UV254测量的结果相一致.
表 4(Table 4)
| 表 4 EEM分析中有机物在HA和FA反应前后分布的FRI计算结果 Table 4 FRI results of organic matter distribution before and after HA and FA reactions in EEM analysis | ||||||||||||||||||||
表 4 EEM分析中有机物在HA和FA反应前后分布的FRI计算结果 Table 4 FRI results of organic matter distribution before and after HA and FA reactions in EEM analysis
| ||||||||||||||||||||
3.5.2 淬灭实验与EPR分析为探究2Fe-TB活化PMS降解HA和FA的机理, 在反应体系中加入自由基淬灭剂甲醇(MeOH)和叔丁醇(TBA), 甲醇用于淬灭SO4-·和OH·, 叔丁醇用于淬灭OH·(佘月城等, 2019), 以及单线态氧(1O2)的淬灭剂叠氮化钠(NaN3)和糠醇(FFA)进行自由基或非自由基鉴定(Yang et al., 2018;Meng et al., 2020), 实验结果和动力学拟合如图 9所示.在不加入淬灭剂的反应体系中, HA和FA的去除率分别为95.3%和77.4%, 其速率常数k分别为0.0269 min-1和0.0108 min-1(表 5), 在反应体系中加入MeOH和TBA后(n(PMS): n(MeOH / TBA)=1:5000), 对HA和FA去除率的影响不大, HA的去除率分别为94.7%和93.0%, FA的去除率分别为79.2%和67.4%, 与加入MeOH相比, 加入过量TBA后HA和FA的降解受到微弱的抑制, 这归因于TBA的粘度比MeOH高, 掩盖2Fe-TB表面的活性位点, 影响2Fe-TB催化效率(Fu et al., 2019).然而, 在反应体系中加入1 mmol NaN3和3.25 mmol FFA后, HA和FA的降解明显受到抑制, 50 min后HA和FA的去除率均低于30%, 反应速率常数k也大幅下降(均高于85%).由此可知, 在2Fe-TB/PMS的反应体系中, 加入过量的MeOH和TBA并不能抑制反应的进行, 说明SO4-·和OH·并不是降解HA和FA的关键活性自由基.而在反应体系中加入NaN3和FFA后, 明显抑制HA和FA的降解, 此时的去除率几乎与2Fe-TB吸附的效果相一致, 说明2Fe-TB/PMS降解HA和FA过程中起最重要作用的活性物种是1O2.此外Wei等(2016)研究表明, 碳材料中的酮基(C=O)也可活化过硫酸盐产生1O2, 是碳材料活化过硫酸盐的重要活性位点(式(3)~(6)).因此, 可以推断1O2是由2Fe-TB表面的磁性粒子和生物炭本身表面的酮基共同产生的, 是高效降解HA和FA的主要活性氧.
图 9(Fig. 9)
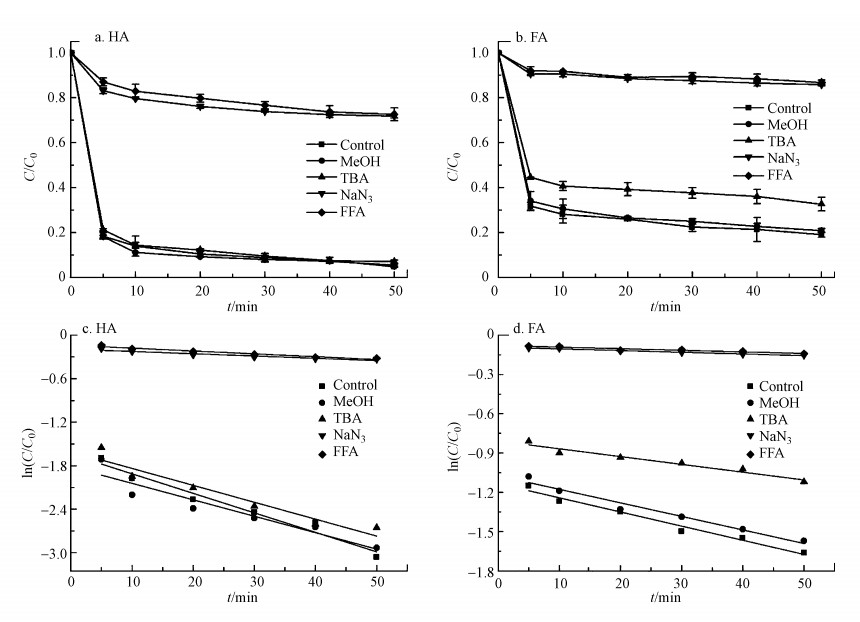 |
| 图 9 各类抑制剂对HA和FA降解的影响及动力学拟合 (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), MeOH=TBA=1.63 mol·L-1, FFA=0.0325 mol·L-1, NaN3=10 mmol·L-1, pH=7.0) Fig. 9Effects of various scavengers on HA and FA degradation and kinetic fitting (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), MeOH=TBA=1.63 mol·L-1, FFA=0.0325 mol·L-1, NaN3=10 mmol·L-1, pH=7.0) |
表 5(Table 5)
| 表 5 各类抑制剂对HA和FA降解的伪一级动力学速率常数 Table 5 The pseudo first-order kinetic rate constants of HA and FA degradation by various scavengers | |||||||||||||||||||||||||||||||||||||
表 5 各类抑制剂对HA和FA降解的伪一级动力学速率常数 Table 5 The pseudo first-order kinetic rate constants of HA and FA degradation by various scavengers
| |||||||||||||||||||||||||||||||||||||
为进一步验证活性物种是1O2, 实验以DMPO作为SO4-·、OH·和O2-·的捕获剂, TEMP作为1O2的捕获剂进行电子顺磁共振(EPR)分析(Gao et al., 2018), 结果如图 10所示, EPR检测到特征峰为1:1:1的1O2特征信号(Cheng et al., 2017)以及极弱的SO4-·和OH·的特征信号, 但未检测到O2-·的特征信号.综合淬灭实验及EPR分析, 可以确定1O2在2Fe-TB/PMS体系降解HA和FA起主导作用.
图 10(Fig. 10)
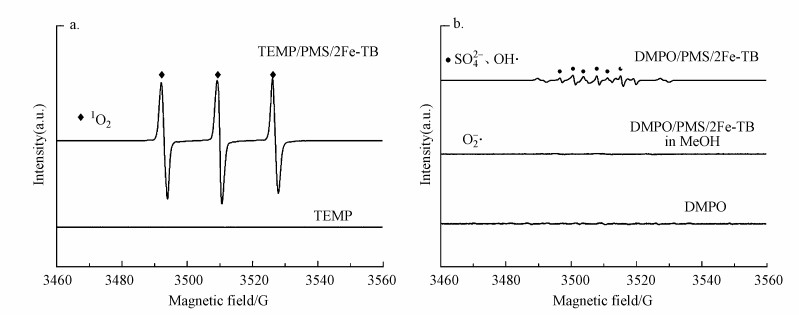 |
| 图 10 1O2电子顺磁共振图谱(a)及SO4-·、OH·、O2-·电子顺磁共振图谱(b) Fig. 10The EPR spectrum of 1O2(a) and the EPR spectrum of SO4-·、OH·、O2-·(b) |
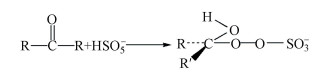
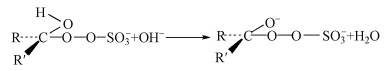
根据上述的研究结果, 提出2Fe-TB/PMS降解HA和FA可能的非自由基途径:首先, PMS被吸附到2Fe-TB表面, HSO5-与2Fe-TB表面的Fe2+和Fe3+生成SO4-·和SO5-·(式(7)、(8)), SO5-·进一步与H2O反应生成1O2(式(9)), 同时PMS的自分解也会产生一部分1O2(式(10)、(11)).体系产生的1O2能高效降解水体中的HA和FA, 最终使其转化为小分子有机物(Guo et al., 2018).
 | (3) |
 | (4) |
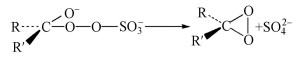 | (5) |
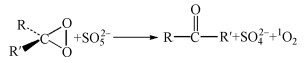 | (6) |
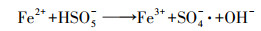 | (7) |
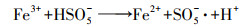 | (8) |
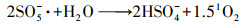 | (9) |
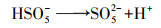 | (10) |
 | (11) |
图 11(Fig. 11)
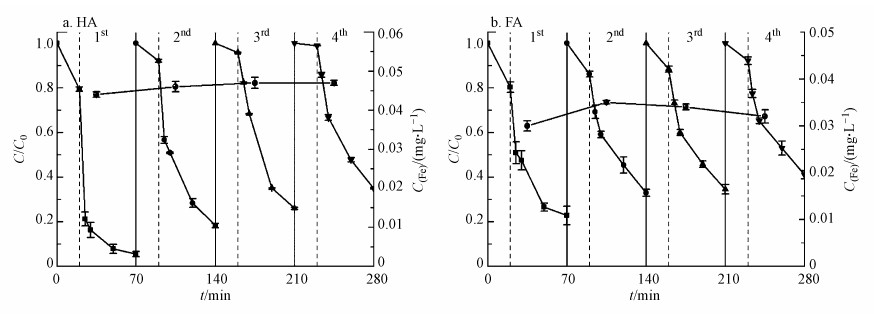 |
| 图 11 2Fe-TB的重复使用对HA和FA降解的影响和铁溶出浓度 (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1(HA)和0.4 g·L-1(FA), pH=7.0) Fig. 11Effects of reused 2Fe-TB on HA and FA degradation and iron dissolution concentration (HA=20 mg·L-1, FA=20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1 (HA) and 0.4 g·L-1 (FA), pH=7.0) |
3.7 2Fe-TB活化PMS处理实际废水DOM为验证2Fe-TB活化PMS处理实际污水厂二级处理出水中DOM的效果, 选取广州市番禺区某污水处理厂的出水, 该水厂日处理量为40万t, 处理工艺主要为A/A/O, 表 6为供试废水的基本性质.
表 6(Table 6)
| 表 6 供试废水的基本性质 Table 6 The properties of wastewater | ||||||||||||||||
表 6 供试废水的基本性质 Table 6 The properties of wastewater
| ||||||||||||||||
图 12a为废水反应前后的紫外图谱, 未经处理的废水在波长210~300 nm出现山丘状宽峰, 其对应的主要是水体存在的有机化合物、脂肪族化合物和芳香族化合物(孟昭瑞等, 2017).经2Fe-TB/PMS处理后, UV254下降38.9%, 证实水体中芳香族化合物被降解.通过经处理后水体的紫外图谱可以看出在波长228 nm出现微弱的特征峰, 这可能是芳香族化合物降解的中间产物, 大分子有机物转化为其他含氮有机物或者是脂肪烃(曹海华等, 2013).
图 12(Fig. 12)
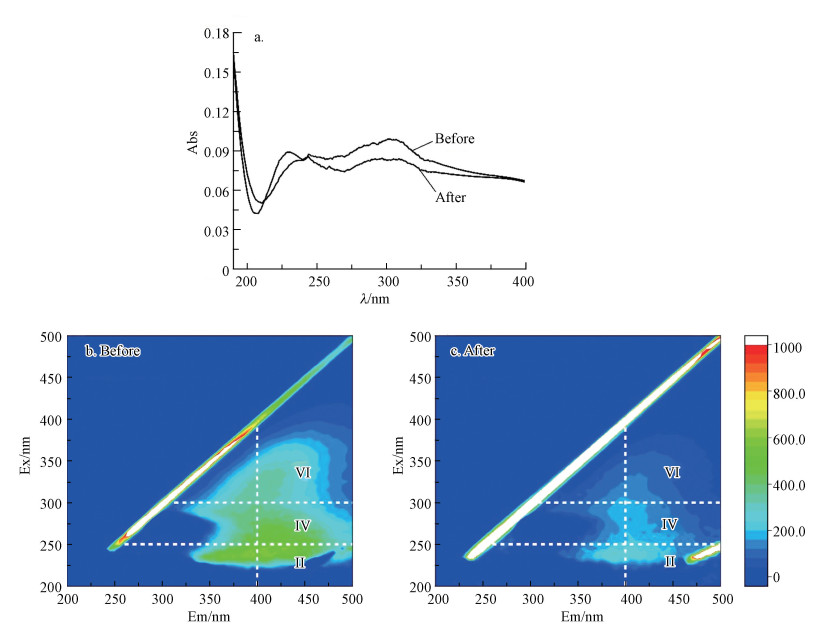 |
| 图 12 废水反应前后的紫外光谱(废水=100 mL, PMS=0.2 g·L-1, 2Fe-TB=0.4 g·L-1)(a)及废水反应前后的荧光光谱特征(b、c) Fig. 12The UV spectrum of wastewater before and after reaction (Wastewater=100 mL, PMS=0.2 g·L-1, 2Fe-TB=0.4 g·L-1) (a) and The fluorescence spectra of wastewater before and after the reaction(b、c) |
为进一步体现2Fe-TB活化PMS去除水中DOM的效果, 采用三维荧光光谱对反应前后水中有机物进行表征.通过对比反应前后三维荧光图谱(图 12b、12c), 反应后水体中各个特征峰的荧光物质均减少, 荧光强度均降低, 进一步证实2Fe-TB/PMS反应能有效降解水体中HA和FA, 但与前文模拟废水处理的效果存在一定的差距, 这可能是实际水体成分复杂, 存在其他无机阴离子等干扰因素, 导致体系非自由基数量减少(Li et al., 2020);或者是水体其他有机物与HA和FA竞争非自由基, 从而影响HA和FA的降解效果.
4 结论(Conclusions)1) 成功制备磁性废茶生物炭2Fe-TB, 其具有比表面积大、表面官能团丰富, 可以通过磁分离回收的特点.
2) 2Fe-TB/PMS体系可高效同时降解HA和FA.在HA和FA初始浓度为20 mg·L-1, PMS=0.2 g·L-1, 2Fe-TB=0.6 g·L-1 (HA)、0.4 g·L-1 (FA), pH=7的条件下, HA的去除率达到95.3%, FA的去除率达到77.4%, 该过程遵循伪一级动力学.而且循环4次使用后, HA和FA的去除率均可达59.0%以上, 显示2Fe-TB良好的重复使用性.
3) 淬灭实验与EPR分析证实2Fe-TB/PMS体系降解HA和FA机制以非自由基途径为主, 主要的活性物种为单线态氧(1O2).
4) 2Fe-TB/PMS体系可以有效处理实际污水厂二级处理出水中DOM, 具有一定的应用潜力.
参考文献
| Auta M, Hameed B. 2011. Preparation of waste tea activated carbon using potassium acetate as an activating agent for adsorption of Acid Blue 25 dye[J]. Chemical Engineering Journal, 171(2): 502-509. DOI:10.1016/j.cej.2011.04.017 |
| Cai H, Zou H, Liu J, et al. 2018. Thermal degradations and processes of waste tea and tea leaves via TG-FTIR: Combustion performances, kinetics, thermodynamics, products and optimization[J]. Bioresource Technology, 268: 715-725. DOI:10.1016/j.biortech.2018.08.068 |
| 曹海华. 2013. 紫外光谱在化合物结构分析中的应用[J]. 内蒙古石油化工, 39(8): 34-36. DOI:10.3969/j.issn.1006-7981.2013.08.013 |
| Cheng X, Guo H, Zhang Y, et al. 2017. Non-photochemical production of singlet oxygen via activation of persulfate by carbon nanotubes[J]. Water Research, 113: 80-88. DOI:10.1016/j.watres.2017.02.016 |
| 崔志文, 任艳芳, 王伟, 等. 2020. 碱和磁复合改性小麦秸秆生物炭对水体中镉的吸附特性及机制[J]. 环境科学, 41(7): 3315-3325. |
| 董正玉, 吴丽颖, 王霁, 等. 2018. 新型Fe3O4@α-MnO2活化过一硫酸盐降解水中偶氮染料[J]. 中国环境科学, 38(8): 3003-3010. DOI:10.3969/j.issn.1000-6923.2018.08.028 |
| 杜文琪, 曹玮, 周航, 等. 2018. 磁性生物炭对重金属污染废水处理条件优化及机理[J]. 环境科学学报, 38(2): 492-500. |
| Feng Y, Liu J, Wu D, et al. 2015. Efficient degradation of sulfamethazine with CuCo2O4 spinel nanocatalysts for peroxymonosulfate activation[J]. Chemical Engineering Journal, 280: 514-524. DOI:10.1016/j.cej.2015.05.121 |
| Fu H, Ma S, Zhao P, et al. 2019. Activation of peroxymonosulfate by graphitized hierarchical porous biochar and MnFe2O4 magnetic nanoarchitecture for organic pollutants degradation: Structure dependence and mechanism[J]. Chemical Engineering Journal, 360: 157-170. DOI:10.1016/j.cej.2018.11.207 |
| Fu Y, Li S, Shi Y, et al. 2019. Removal of artificial sweeteners using UV/persulfate: Radical-based degradation kinetic model in wastewater, pathways and toxicity[J]. Water Research, 167: 115102. DOI:10.1016/j.watres.2019.115102 |
| 郜礼阳, 邓金环, 唐国强, 等. 2018. 不同温度桉树叶生物炭对Cd2+的吸附特性及机制[J]. 中国环境科学, 38(3): 1001-1009. DOI:10.3969/j.issn.1000-6923.2018.03.025 |
| Gao Y, Zhu Y, Lyu L, et al. 2018. Electronic structure modulation of graphitic carbon nitride by oxygen doping for enhanced catalytic degradation of organic pollutants through peroxymonosulfate activation[J]. Environmental Science and Technology, 52(24): 14371-14380. DOI:10.1021/acs.est.8b05246 |
| Guo F, Wang K, Lu J, et al. 2018. Activation of peroxymonosulfate by magnetic carbon supported Prussian blue nanocomposite for the degradation of organic contaminants with singlet oxygen and superoxide radicals[J]. Chemosphere, 218: 1071-1081. |
| Hao H, Zhang Q, Qiu Y, et al. 2020. Insight into the degradation of Orange G by persulfate activated with biochar modified by iron and manganese oxides: Synergism between Fe and Mn[J]. Journal of Water Process Engineering, 37: 101470. DOI:10.1016/j.jwpe.2020.101470 |
| Hu C, Hou Y, Lin Y, et al. 2020. Investigation of iohexol degradation kinetics by using heat-activated persulfate[J]. Chemical Engineering Journal, 379: 122403. DOI:10.1016/j.cej.2019.122403 |
| Hu X, Xu J, Wu M, et al. 2017. Effects of biomass pre-pyrolysis and pyrolysis temperature on magnetic biochar properties[J]. Journal of Analytical and Applied Pyrolysis, 127: 196-202. DOI:10.1016/j.jaap.2017.08.006 |
| 黄锦佳, 梁嘉林, 杨贤, 等. 2020. 超声-生物沥浸-氧化钙联合超高压压滤系统实现市政污泥深度脱水及其泥饼的毒性评估[J]. 环境科学学报, 40(5): 1745-1759. |
| 金鹏康, 石彦丽, 任武昂. 2015. 城市污水处理过程中溶解性有机物转化特性[J]. 环境工程学报, 9(1): 1-6. |
| Khodadadi M, Al-Musawi T, Kamani H, et al. 2019. The practical utility of the synthesis FeNi3@SiO2@TiO2 magnetic nanoparticles as an efficient photocatalyst for the humic acid degradation[J]. Chemosphere, 239: 124723. |
| Lee H, Lee Y, Youn H, et al. 2012. Anti-influenza virus activity of green tea by-products in vitro and efficacy against influenza virus infection in chickens[J]. Poultry Science, 91(1): 66. DOI:10.3382/ps.2011-01645 |
| 李立, 吴丽颖, 董正玉, 等. 2020. 高晶度Mn-Fe LDH催化剂活化过一硫酸盐降解偶氮染料RBK5[J]. 环境科学, 41(6): 2736-2745. |
| Li X, Jia Y, Zhou M, et al. 2020. High-efficiency degradation of organic pollutants with Fe, N co-doped biochar catalysts via persulfate activation[J]. Journal of Hazardous Materials, 397: 122764. DOI:10.1016/j.jhazmat.2020.122764 |
| 李小娟, 叶兰妹, 廖凤珍, 等. 2020. 杂原子掺杂碳材料活化过硫酸盐技术的研究进展[J]. 化工进展: 1-17. |
| Li Y, Li J, Pan Y, et al. 2019. Peroxymonosulfate activation on FeCo2S4 modified g-C3N4 (FeCo2S4-CN): Mechanism of singlet oxygen evolution for nonradical efficient degradation of sulfamethoxazole[J]. Chemical Engineering Journal, 384: 123361. |
| Liu F, Li W, Wu D, et al. 2020. New insight into the mechanism of peroxymonosulfate activation by nanoscaled lead-based spinel for organic matters degradation: a singlet oxygen-dominated oxidation process[J]. Journal of Colloid and Interface Science, 572: 318-327. DOI:10.1016/j.jcis.2020.03.116 |
| Liu J, Ren S, Cao J, et al. 2021. Highly efficient removal of thallium in wastewater by MnFe2O4-biochar composite[J]. Journal of Hazardous Materials, 401: 123311. DOI:10.1016/j.jhazmat.2020.123311 |
| Liu J, Yang Q, Wang D, et al. 2016. Enhanced dewaterability of waste activated sludge by Fe(Ⅱ)-activated peroxymonosulfate oxidation[J]. Bioresource Technology, 206: 134-140. DOI:10.1016/j.biortech.2016.01.088 |
| Luo J, Bo S, Qin Y, et al. 2020. Transforming goat manure into surface-loaded cobalt/biochar as PMS activator for highly efficient ciprofloxacin degradation[J]. Chemical Engineering Journal, 395: 125063. DOI:10.1016/j.cej.2020.125063 |
| Meng H, Nie C, Li W, et al. 2020. Insight into the effect of lignocellulosic biomass source on the performance of biochar as persulfate activator for aqueous organic pollutants remediation: Epicarp and mesocarp of citrus peels as examples[J]. Journal of Hazardous Materials, 399: 123043. DOI:10.1016/j.jhazmat.2020.123043 |
| 孟昭瑞, 高宁. 2017. 有机化合物的紫外光谱分析[J]. 西部资源, (6): 179-182. DOI:10.3969/j.issn.1672-562X.2017.06.065 |
| Ni B, Yan X, Sun J, et al. 2019. Persulfate and zero valent iron combined conditioning as a sustainable technique for enhancing dewaterability of aerobically digested sludge[J]. Chemosphere, 232: 45-53. DOI:10.1016/j.chemosphere.2019.05.148 |
| 聂明华, 徐文丽, 张文静, 等. 2018. Fe2+和零价铁活化过一硫酸盐降解酸性橙7[J]. 环境科学学报, 38(10): 3997-4005. |
| Oh W, Lua S, Dong Z, et al. 2015. Performance of magnetic activated carbon composite as peroxymonosulfate activator and regenerable adsorbent via sulfate radical-mediated oxidation processes[J]. Journal of Hazardous Materials, 284: 1-9. DOI:10.1016/j.jhazmat.2014.10.042 |
| Rong X, Xie M, Kong L, et al. 2019. The magnetic biochar derived from banana peels as a persulfate activator for organic contaminants degradation[J]. Chemical Engineering Journal, 372: 294-303. DOI:10.1016/j.cej.2019.04.135 |
| 佘月城, 董正玉, 吴丽颖, 等. 2019. MnFe2O4活化过一硫酸盐降解废水中LAS[J]. 中国环境科学, 39(8): 3323-3331. |
| Shi Y, Li S, Wang L, et al. 2020. Characteristics of DOM in 14 AAO processes of municipal wastewater treatment plants[J]. Science of The Total Environment, 742: 140654. DOI:10.1016/j.scitotenv.2020.140654 |
| 宋磊, 张彬, 邓文. 2014. 废茶活性炭脱硫脱硝性能的应用研究[J]. 环境科学, 35(10): 3674-3682. |
| Song Y, Hu J, Liu J, et al. 2020. Catalytic effects of CaO, Al2O3, Fe2O3, and red mud on Pteris vittata combustion: Emission, kinetic and ash conversion patterns[J]. Journal of Cleaner Production, 252: 119646. DOI:10.1016/j.jclepro.2019.119646 |
| Tian X, Tian C, Nie Y, et al. 2018. Controlled synthesis of dandelion-like NiCo2O4 microspheres and their catalytic performance for peroxymonosulfate activation in humic acid degradation[J]. Chemical Engineering Journal, 331: 144-151. DOI:10.1016/j.cej.2017.08.115 |
| Wang B, Li Y, Wang L, et al. 2019. Metal-free activation of persulfates by corn stalk biochar for the degradation of antibiotic norfloxacin: Activation factors and degradation mechanism[J]. Chemosphere, 237: 124454. DOI:10.1016/j.chemosphere.2019.124454 |
| Wang C, Yang Q, Li Z, et al. 2019. A novel carbon-coated Fe-C/N composite as a highly active heterogeneous catalyst for the degradation of Acid Red 73 by persulfate[J]. Separation & Purification Technology, 213: 447-455. |
| Wang G, Chen S, Quan X, et al. 2017. Enhanced activation of peroxymonosulfate by nitrogen doped porous carbon for effective removal of organic pollutants[J]. Carbon, 115: 730-739. DOI:10.1016/j.carbon.2017.01.060 |
| Wang M, Liao L, Zhang X, et al. 2012. Adsorption of low concentration humic acid from water by palygorskite[J]. Applied Clay Science, 67-68: 164-168. DOI:10.1016/j.clay.2011.09.012 |
| 王莹, 魏成耀, 黄天寅, 等. 2017. 氮掺杂碳纳米管活化过一硫酸盐降解酸性橙AO7[J]. 中国环境科学, 37(7): 2583-2590. |
| Wang Z, Zhang T. 2010. Characterization of soluble microbial products (SMP) under stressful conditions[J]. Water Research, 44: 5499-5509. DOI:10.1016/j.watres.2010.06.067 |
| Wei M, Gao L, Li J, et al. 2016. Activation of peroxymonosulfate by graphitic carbon nitride loaded on activated carbon for organic pollutants degradation[J]. Journal of Hazardous Materials, 316: 60-68. DOI:10.1016/j.jhazmat.2016.05.031 |
| Wu P, Ata-Ul-Karim S, Singh B, et al. 2019. A scientometric review of biochar research in the past 20 years (1998-2018)[J]. Biochar, 1: 23-43. DOI:10.1007/s42773-019-00002-9 |
| 徐劼, 陈家斌, 卢建, 等. 2020. LaCo0.5Cu0.5O3型钙钛矿活化过一硫酸盐降解AO7[J]. 中国环境科学, 40(3): 1123-1131. |
| Yagmur E. 2012. Preparation of low cost activated carbons from various biomasses with microwave energy[J]. Journal of Porous Materials, 19(6): 995-1002. DOI:10.1007/s10934-011-9557-7 |
| Yan J, Lei M, Zhu L, et al. 2011. Degradation of sulfamonomethoxine with Fe3O4 magnetic nanoparticles as heterogeneous activator of persulfate[J]. Journal of Hazardous Materials, 186(2/3): 1398-1404. |
| Yang J, Lin Y, Peng H, et al. 2020. Novel magnetic rod-like Mn-Fe oxycarbide toward peroxymonosulfate activation for efficient oxidation of butyl paraben: Radical oxidation versus singlet oxygenation[J]. Applied Catalysis B: Environmental, 268. |
| 杨珂, 唐琪, 杨晓丹, 等. 2019. 铁酸铜非均相活化过硫酸盐降解罗丹明B[J]. 中国环境科学, 39(9): 3761-3769. |
| Yang S, Wu P, Liu J, et al. 2018. Efficient removal of bisphenol A by superoxide radical and singlet oxygen generated from peroxymonosulfate activated with Fe0-montmorillonite[J]. Chemical Engineering Journal, 350: 484-495. DOI:10.1016/j.cej.2018.04.175 |
| Yuan Y, Bolan N, Prévoteau A, et al. 2017. Applications of biochar in redox-mediated reactions[J]. Bioresource Technology, 246: 271-281. DOI:10.1016/j.biortech.2017.06.154 |
| Zhang J, Gong J, Zenga G, et al. 2016. Simultaneous removal of humic acid/fulvic acid and lead from landfill leachate using magnetic graphene oxide[J]. Applied Surface Science, 370: 335-350. DOI:10.1016/j.apsusc.2016.02.181 |
| Zhang L, Liu H, Peng Y, et al. 2020. Characteristics and significance of dissolved organic matter in river sediments of extremely water-deficient basins: A Beiyun River case study[J]. Journal of Cleaner Production, 277: 123063. DOI:10.1016/j.jclepro.2020.123063 |
| 张黎明, 陈家斌, 李文卫, 等. 2016. 碳纳米管活化过一硫酸盐降解金橙G过程及动力学[J]. 环境科学, 37(7): 2601-2609. |
| 张倩, 谢陈飞洋, 仇玥, 等. 2019. Fe/污泥基生物炭持久活化过硫酸盐降解酸性橙G[J]. 中国环境科学, 39(9): 3879-3886. |
| Zhang Z, Zhu Z, Shen B, et al. 2019. Insights into biochar and hydrochar production and applications: A review[J]. Energy, 171: 581-598. DOI:10.1016/j.energy.2019.01.035 |
| 赵朔, 裴勇. 2012. 氯化锌活化法制备笋壳基活性炭的工艺研究[J]. 材料导报, 26(4): 87-90. |
| 郑可, 周少奇, 杨梅梅. 2012. 臭氧降解高浓度腐殖酸动力学[J]. 环境科学, 33(3): 879-884. |
| Zhou X, Zhou S, Ma F, et al. 2019. Synergistic effects and kinetics of rGO-modified TiO2 nanocomposite on adsorption and photocatalytic degradation of humic acid[J]. Journal of Environmental Management, 235: 293-302. |
| Zhou Y, Zhang Y, Hu X. 2020. Enhanced activation of peroxymonosulfate using oxygen vacancy-enriched FeCo2O4x spinel for 2, 4-dichlorophenol removal: Singlet oxygen-dominated nonradical process[J]. Colloids and Surfaces A Physicochemical and Engineering Aspects, 597: 124568. DOI:10.1016/j.colsurfa.2020.124568 |
