全文HTML
--> --> -->蚕丝是一种古老的生物材料, 它的起源可以追溯到公元前3500年左右. 到公元前130年, 中国的丝绸面料和制造技术已经在全世界范围内传播开来. 蚕丝纤维自古以来就因其光泽的外观、良好的弹性和轻盈的重量而被广泛用于纺织工业, 使得横贯亚欧大陆的贸易路线被称为“丝绸之路”. 此外, 由于其机械韧性, 蚕丝纤维已被用作眼部和唇部手术的缝合线[14]. 从本质上讲, 天然丝是存在于一些节肢动物腺体中的纤维蛋白质, 例如蚕、蜘蛛、蝎子、螨虫和蜜蜂等. 目前, 商用的蚕丝主要来源于家蚕(bombyx mori)[15], 其具有高产量[16]、优异的拉伸强度(0.5—1.3 GPa)和韧性(6 × 104—16 × 104 J/kg)[17]、良好的生物相容性、可降解性以及易加工性[18]等重要特征. 这赋予了蚕丝蛋白在生物领域中的多种应用, 包括组织工程[16]、伤口愈合[19]和药物缓释[20]等. 2009年, 美国西北大学Kim等[3]首次将蚕丝材料引入柔性电子领域, 在具有水溶性和生物相容性的蚕丝膜上集成了单晶硅电子器件. 2010年, Kim等[21]利用蚕丝膜为柔性基底构建出全贴合的生物集成电子器件. 2011年, Hwang等[22]在PET基底上利用蚕丝薄膜作为栅极电介质, 开发出一种柔性并五苯有机场效应晶体管(flexible organic thin film transistors, OTFTs). 它具有23.2 cm2·V–1·s–1的高迁移率值和–3 V的低工作电压, 性能优于几种无机薄膜晶体管. 2012年, Hota等[23]开发出一种丝蛋白基的生物忆阻器. 图1详细展示了蚕丝基先进材料在柔性电子中的时间发展线.
 图 1 蚕丝基先进材料应用于柔性电子领域的时间发展线 生物可吸收电子[3](2009); 超共形电子[21](2010); 柔性OTFTs[22](2011); 瞬态电子[5](2012); 共形无线生物传感器[30](2012); 柔性太阳能电池[31](2014); 生物摩擦发电机[32](2015); 生物忆阻器[33](2015); 碳化丝织物(CSF)可穿戴应变传感器[34](2016); 蚕丝衍生的碳基电子皮肤[35](2017年); 皮肤可拉伸电极[36](2018); 基于生物可降解和可拉伸蛋白质的传感器[37](2019); 全纺织电子皮肤[38](2019); 可调温度的电子皮肤[39] (2020)
图 1 蚕丝基先进材料应用于柔性电子领域的时间发展线 生物可吸收电子[3](2009); 超共形电子[21](2010); 柔性OTFTs[22](2011); 瞬态电子[5](2012); 共形无线生物传感器[30](2012); 柔性太阳能电池[31](2014); 生物摩擦发电机[32](2015); 生物忆阻器[33](2015); 碳化丝织物(CSF)可穿戴应变传感器[34](2016); 蚕丝衍生的碳基电子皮肤[35](2017年); 皮肤可拉伸电极[36](2018); 基于生物可降解和可拉伸蛋白质的传感器[37](2019); 全纺织电子皮肤[38](2019); 可调温度的电子皮肤[39] (2020)Figure1. The timeline of the development of silk-based advanced materials for soft electronics: Bioresorbable electronics[3] (2009); ultraconformal bioelectronics[21](2010); flexible OTFTs[22] (2011); transient electronics[22](2012); conformal wireless biosensors[22](2012); flexible solar cells[31] (2014); bio-triboelectric generator[31] (2015); bio-memristor[33] (2015); carbonized silk fabric (CSF) wearable strain sensors[34] (2016); silk-derived carbon based E-skins[35] (2017); on-skin stretchable electrodes[36] (2018); biodegradable and stretchable protein-based sensor[37] (2019); all-textile electronic skin[38] (2019); electronic skin for human thermoregulation[39] (2020).
可穿戴传感器是柔性电子设备中最重要的部分之一, 在监测人体和机器人运动[24-26]、个人医疗保健[27,28]以及检测食品系统的整体卫生[29]等方面有广泛的应用潜力. 本文的目的是总结近年来蚕丝材料在可穿戴传感器领域的研究进展. 首先介绍蚕丝的层级结构和蚕丝基先进材料的形态、特征. 随后, 重点讨论和总结近年来蚕丝材料在可穿戴传感器上的应用, 包括机械(应变、压力)、电生理、温度和湿度传感器等. 最后, 给出对蚕丝材料在可穿戴传感领域的总结及展望.
2.1.蚕丝的层级结构
天然蚕丝纤维由两种类型的自组装蛋白组成: 丝素蛋白(silk fibroin, SF)和丝胶蛋白(silk sericin, SS)[40]. SF是蚕丝纤维的结构中心, 约占蚕丝重量的70%—80%, 而SS是毛虫分泌的水溶性蛋白质, 占蚕丝重量的25%—30%, 用于将SF粘合成茧[14,15]. SS在人体中会引起免疫反应, 所以一般将其溶解在煮沸的碱性溶液中去除. SF的主要结构由甘氨酸(Gly, G), 丙氨酸(Ala, A)和丝氨酸(Ser, S)以(-G-A-G-A-G-S-)n的序列组成[15,33]. SF具有非常高的分子量, 由结晶区的疏水重链(约390 kDa)和非结晶区的亲水轻链(约26 kDa)组成, 比例为1∶1, 两者通过二硫键结合在一起. 重链是高度规则的生物聚合物, 其由12个疏水结构域组成, 其中散布有11个亲水结构域. 疏水结构域含有重复序列的氨基酸(称为重复结构域), 而亲水结构域含有非重复序列的氨基酸(称为非重复结构域)[41-44]. 其中, 重复结构域(主要包含G, A, S)能够通过氢键作用将它们组合成β-片或α-螺旋. 在此基础上, β-片又通过范德瓦耳斯力/疏水相互作用构建出高度紧密且有组织的三维(3D)结构——β-微晶; 非重复结构域(主要包含谷氨酸、天冬氨酸、精氨酸和赖氨酸等)形成SF中的半无定形区域(无规则卷曲)[45]. 这些无定形链将β-微晶连接在一起, 形成纳米原纤维. 目前, 所有形态的蚕丝基材料(包括纤维、水凝胶、薄膜和支架等)在介观尺度下均由纳米原纤维网络构成. 所以, 单个纳米原纤维被定义为蚕丝的基本介观结构单元[46]. 显然, 纳米原纤维的强度和稳定性以及它们之间的相互作用对宏观机械性能有很大影响. 比如, 天然蚕丝纤维通过纳米原纤维之间强的物理接触形成, 而在SF水凝胶、薄膜和骨架中, 纳米原纤维的交互作用较弱. 图2详细展示了SF基材料的多级网络结构.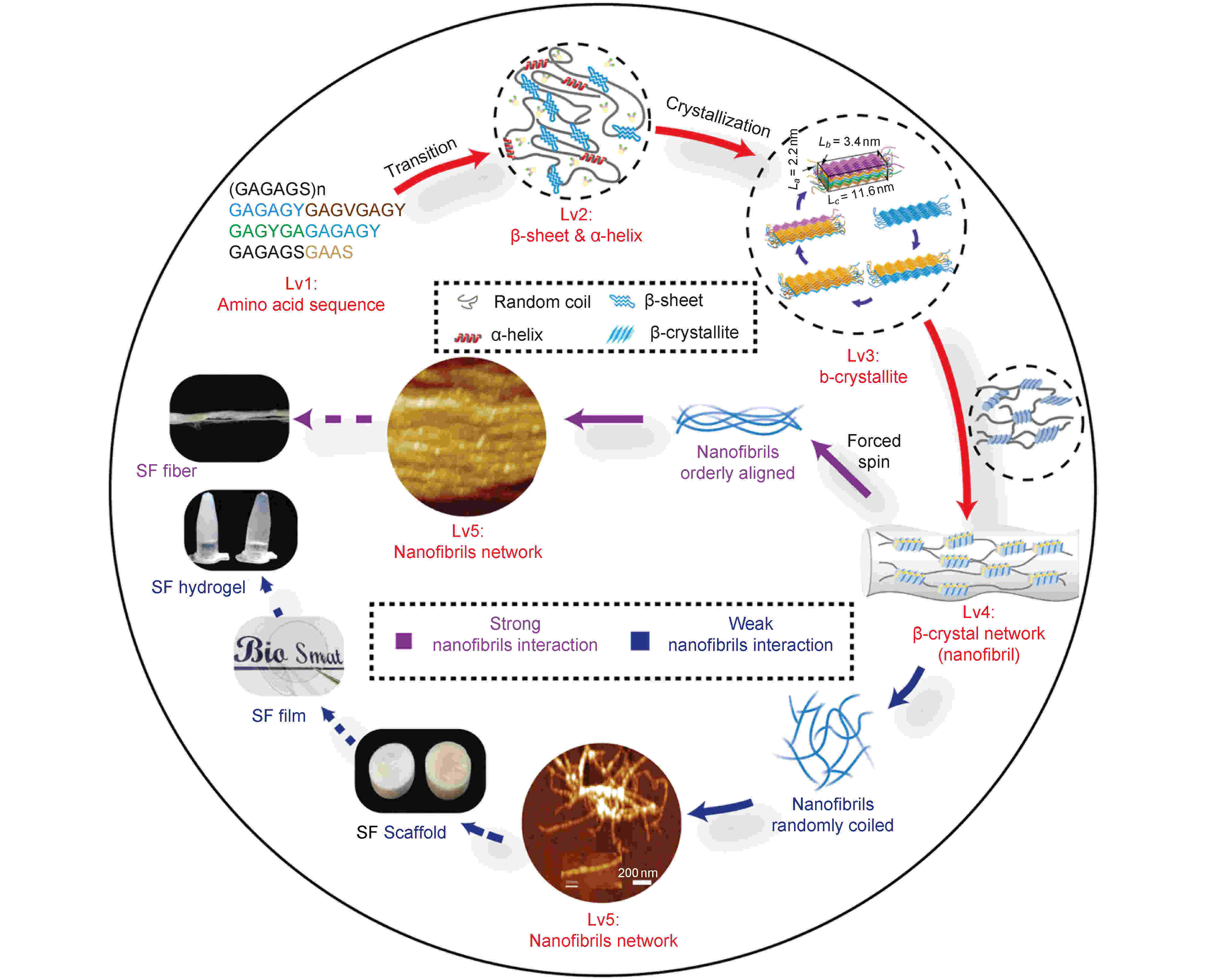 图 2 SF纤维和非纤维材料的层级网络结构示意图[46] Lv1: 氨基酸序列; Lv2: α-螺旋和β-折叠; Lv3: β-微晶; Lv4: β-晶体网络; Lv5: 纳米纤维网络
图 2 SF纤维和非纤维材料的层级网络结构示意图[46] Lv1: 氨基酸序列; Lv2: α-螺旋和β-折叠; Lv3: β-微晶; Lv4: β-晶体网络; Lv5: 纳米纤维网络Figure2. Schema of the hierarchical network structures of SF fibers and none-fiber silk materials[46]. Lv1: the amino acid sequence; Lv2: α-helix & β-sheet; Lv3: β-crystallites; Lv4: crystal network; Lv5: nanofibrils network.
2
2.2.蚕丝基先进材料
天然蚕丝纤维被广泛制成纱线和纺织品, 与聚合物纤维相比具有良好的生物相容性和机械韧性. 将无机或有机功能材料(例如碳基材料、金属纳米材料和导电聚合物)与丝纤维整合在一起, 可开发出导电纤维[34]或导电织物[38]. 例如, 氧化石墨烯(graphene oxide, GO)作为一种常见的功能性无机材料, 利用氧化还原反应将GO转化为还原GO (reduced GO, rGO)后, 可以通过分子间氢键和疏水相互作用与蚕丝纤维结合[47] (图3(a)), 构筑成导电的rGO涂层纤维. Liu等[48]利用浸涂方式构建了柔软且导电的rGO涂层丝织物, 进而将其开发成一种具有多层结构的可穿戴压力传感器, 可用于监测人体运动.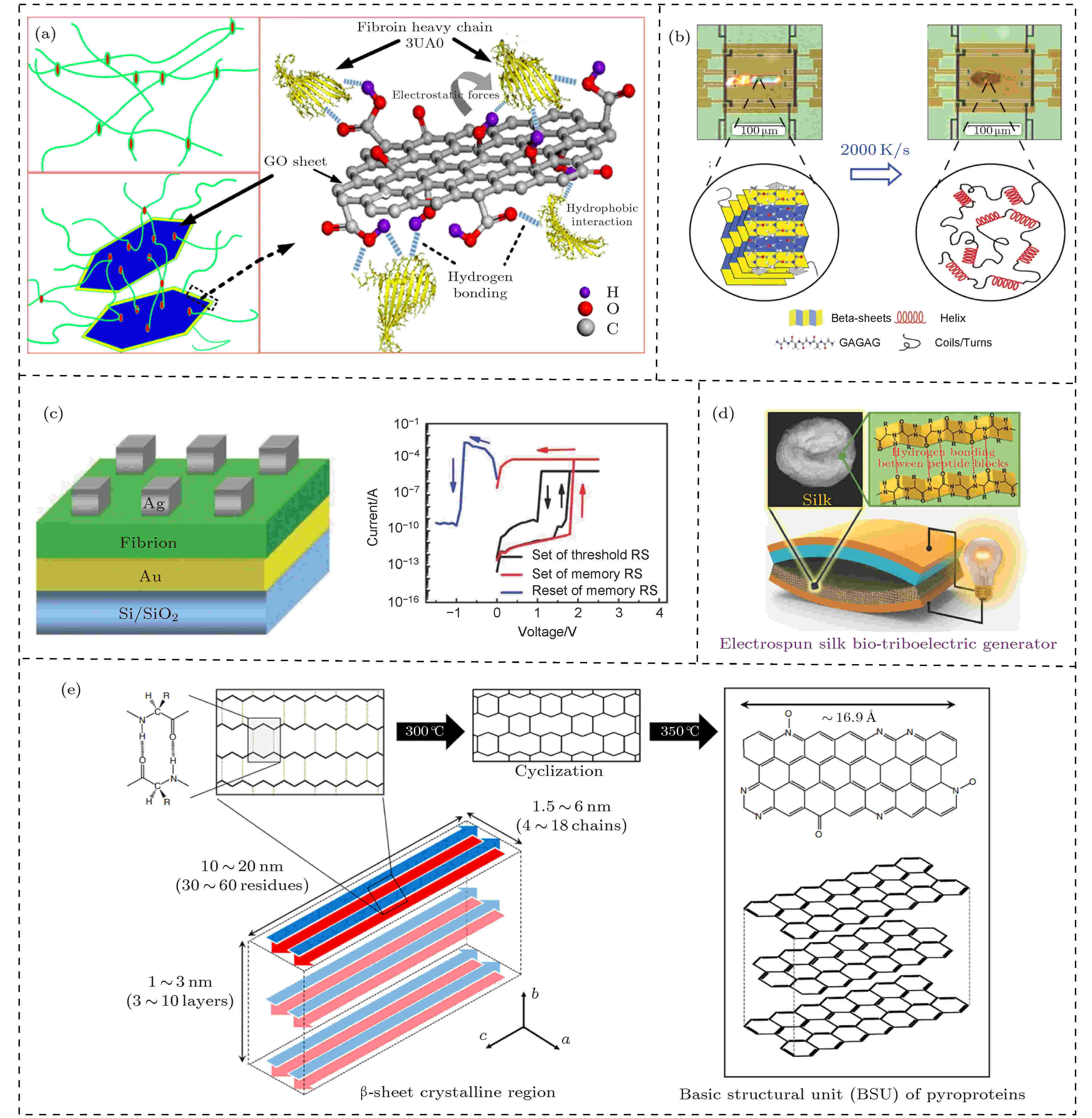 图 3 蚕丝基材料的介观功能化 (a) SF和GO之间的键合[47]; (b) 热处理下β片和无规则卷曲之间可调控的结构变化[17]; (c) 一种蚕丝基忆阻器[33]; (d) 用于生物摩擦发电机的蚕丝纳米纤维膜[32]; (e) β-折叠衍生的碳结构的基本示意图[64]
图 3 蚕丝基材料的介观功能化 (a) SF和GO之间的键合[47]; (b) 热处理下β片和无规则卷曲之间可调控的结构变化[17]; (c) 一种蚕丝基忆阻器[33]; (d) 用于生物摩擦发电机的蚕丝纳米纤维膜[32]; (e) β-折叠衍生的碳结构的基本示意图[64]Figure3. Mesoscopic functionalization of silk-based materials: (a) The chemical bonding between SF and GO[47]; (b) the revisable structure changes of β-sheets and random coils under high thermal treatment[17]; (c) a silk-based memristor[33]; (d) silk nanofiber membrane for bio-triboelectric generator[32]; (e) schematic of β-sheet-derived carbon basic structural units[64].
天然蚕丝纤维经过脱胶处理后得到再生SF(regenerated silk fibroin, RSF)溶液[49]. RSF具有生物相容性和可降解性, 在人体内不会引起炎症反应, 因此, 基于RSF的柔性电子设备能够用于可穿戴和植入式生物医学或医疗保健[22,50-52]. 同时, RSF的光学透明性和基于溶液的易加工性使其可制成各种形态, 比如薄膜、水凝胶和骨架等, 这一方面为柔性薄膜或透明电子器件的微/纳米加工提供便利[7,23,53]. 另一方面, 有助于其与功能材料在介观尺度下的结合, 改善本身的机械性能和导电性能. 比如, Pan等[54]通过引入碳纳米管(carbon nano tubes, CNT)增加RSF中的β-折叠结构来改善其机械性能和电导率. Lv等[55]在RSF水溶液中掺入凯夫拉纳米纤维后合成出一种RSF纤维膜, 其杨氏模量提高了2倍. 此外, RSF的介观可控性使得其能够改善本身的亲/疏水性能、酶/药释放速率和降解速率. 例如, Cebe等[17]发现, 在热处理的条件下, RSF的β-微晶可以翻转成无规则卷曲(图3(b)). 2014年, Huang等[56]指出提高RSF中β-微晶的含量能降低RSF的水溶性, 这完全可以通过控制水蒸气退火时间和退火温度来实现. Musameh等[57]利用RSF在膜中易于固定酶的特性, 制备出第三代生物传感器. RSF薄膜的降解速率的可控性促使新技术的出现, 比如以可编程的方式溶解植入式器件[22,58-60].
通过介观功能化, SF也能成为柔性电子器件中的有效组分. 首先, 丰富的氢键和疏水相互作用使其被开发成一种优异的介电材料(介电常数为6.1), 可以用作OTFTs和阻变存储器的介电层, 例如, 2015年, Wang等[33]利用RSF薄膜开发出一种具有双极阻变效应的存储器(图3(c)). 对于可擦写阻变效应, 开关比约107、保持时间大于 4500 s; 而在写一次读多次阻变效应上, 开关比为108、保持时间为104 s. 另外, 由于RSF优异的机械强度、电负性和生物相容性, Kim等[32]开发出一种弓形的生物摩擦发电机(bio-triboelectric generator, Bio-TEG)(图3(d)), 选取静电纺丝的蚕丝纤维膜作为摩擦层. 在5 MΩ的电阻率下, Bio-TEG的表面电荷密度和瞬时电功率分别高达1.86 μC·m–2和4.3 mW·m–2. 除了二维膜状的Bio-TEG外, 还可以设计RSF与其他功能成分组合, 将其加工成基于蚕丝织物的柔性摩擦纳米发电机[61]. 特别地, SF结构中含有大量官能团而使其成为一种有前途的生物可再生碳源[14]. 通过对蚕丝进行热处理后, 可以合成出具有可控孔径的氮掺杂“丝碳”[62,63]. Cho等[64]报道了SF的碳化机理, 当加热至350 ℃时, SF中的β-片层结构会转变为sp2杂化的碳六方结构. 而加热至2800 ℃后, 结晶层会进一步生长成高度有序的石墨结构(见图3(e)).
| 传感器类型 | 传感材料 | 基底材料 | 信号 | 应用 | 文献 |
| 应变 | 蚕丝纤维和Gr | Ecoflex | 电阻 | 关节运动 | [34] |
| 应变 | 碳化的丝织物 | Ecoflex | 电阻 | 人体运动 | [65] |
| 应变 | PSB | PSB | 电阻 | 手指运动 | [67] |
| 应变 | Ag NWs | RSF膜 | 电流 | 人体运动 | [68] |
| 压力 | CSFM | PDMS | 电流 | 脉搏运动 | [35] |
| 应变+压力 | Ag NFs和Ecoflex | RSF膜 | 电容 | 手臂运动 | [37] |
| 压力 | 蚕丝纤维和Ag NWs | Ecoflex | 电容 | 智能织物 | [69] |
| 压力 | rGO | 蚕丝织物 | 电阻 | 脉搏运动 | [48] |
| 压力 | Ag NWs | 蚕丝织物 | 电容 | 手臂运动 | [38] |
| 电生理 | Au | RSF膜 | 电阻 | 肌电图 | [36] |
| 电生理 | Ag/AgCl | RSF水凝胶 | 电压 | 心电图 | [72] |
| 电生理 | Ag NWs | RSF水凝胶 | 电压 | 心电图 | [73] |
| 温度+压力 | 碳化的丝纤维 | PET | 电阻 | 电子皮肤 | [74] |
| 温度 | 离子液体和丝纤维 | Ecoflex | 电阻 | 智能织物 | [69] |
| 温度+加热器 | Ag NFs + Pt | RSF膜 | 电阻 | 电子皮肤 | [39] |
| 湿度 | Gr | RSF膜 | 电阻 | 表皮电子 | [75] |
| 应变+湿度+温度 | IDE (Ag NWs) | RSF膜 | 电容 | 呼吸监测 | [81] |
表1蚕丝基可穿戴传感器的材料特性和功能总结
Table1.Summary of properties and functions of silk-based wearable sensors.
2
3.1.机械应变传感器
2016年, Zhang等[34]开发出一种皮芯结构的蚕丝纤维型应变传感器(图4(a)). 利用迈耶棒涂层的方式, 将石墨(graphene, Gr)涂覆在丝纤维表面形成导电纤维, 随后用Ecoflex(一种硅胶)将其封装成应变传感器. 在对蚕丝纤维进行拉伸时, 贴附在上面的Gr片产生裂纹, 导致纤维电导率的变化, 从而实现了应变传感的功能. 该传感器在0—15%的应变范围内, 灵敏度系数 (gauge factor, GF)值为14.5, 3000次循环测试后仍保持良好的稳定性. 将其贴附在皮肤上可以监测关节运动, 比如手指、手腕弯曲, 或者集成到多向应变传感器中监测人体运动的多轴应变. Wang等[65]开发了一种蚕丝织物应变传感器, 将编织好的蚕丝织物进行碳化处理[64], 随后用Ecoflex封装成柔性应变传感器(图4(b)). 当对其进行拉伸时, 内部被碳化的纤维接触减少甚至断裂, 对总电阻产生变化, 从而实现了应变传感. 它具有极高的拉伸极限(大于500%), 应变小于250%时, GF为9.6; 应变在250%— 500%之间时, GF为37.5; 即使对于0—1%的范围内的应变, GF仍可达到5.8, 几乎是金属传感材料GF(2.0)的3倍[66]. 另外该传感器还具有快速响应(小于70 ms)和高稳定性(100%应变下拉伸6000个周期). 由于其优异的灵活性、高灵敏度和广泛的工作范围, 这种碳化的蚕丝织物传感器可应用于监测全方位的人体活动, 包括剧烈运动, 如关节的弯曲和旋转、行进、慢跑和跳跃, 或者微妙的运动, 如脉搏、呼吸、情绪表达和发声. 2019年, Yang等[67]利用聚乙烯醇(polyvinyl alcohol, PVA)/ RSF/硼砂(PVA/RSF/borax, PSB)制成一种水凝胶应变传感器(图4(c)), 在PSB水凝胶中, PVA和硼砂分别具有高拉伸性和导电性, 而RSF可提高水凝胶的稳定性, 增加凝胶的水分摄入量以及保水性. 该PSB水凝胶具有可承受5000%的应变极限, 良好的保水性、自愈性以及可调节的导电性和胶粘性, 同时, 其作为传感平台可监测人体运动. Gogurla等[68]将银纳米线(Ag nanowires, Ag NWs)线植入RSF薄膜中制备了一种应变传感器, 其拥有较高灵敏度(GF = 30), 能稳定地监测手指和关节的弯曲, 同时利用RSF膜作为摩擦层, Ag NWs作为电极制备出一种单电极的Bio-TEG, 它能很好地贴合皮肤, 当手指触摸时, 皮肤与RSF膜发生电荷转移, 进而产生开路电压且功率密度为2 mW/m2. 此外将两者整合在一张RSF膜后, 器件兼具应变传感和能量收集(图4(d)). 这对于在人机界面上带来多功能的生物电子传感器具有借鉴意义.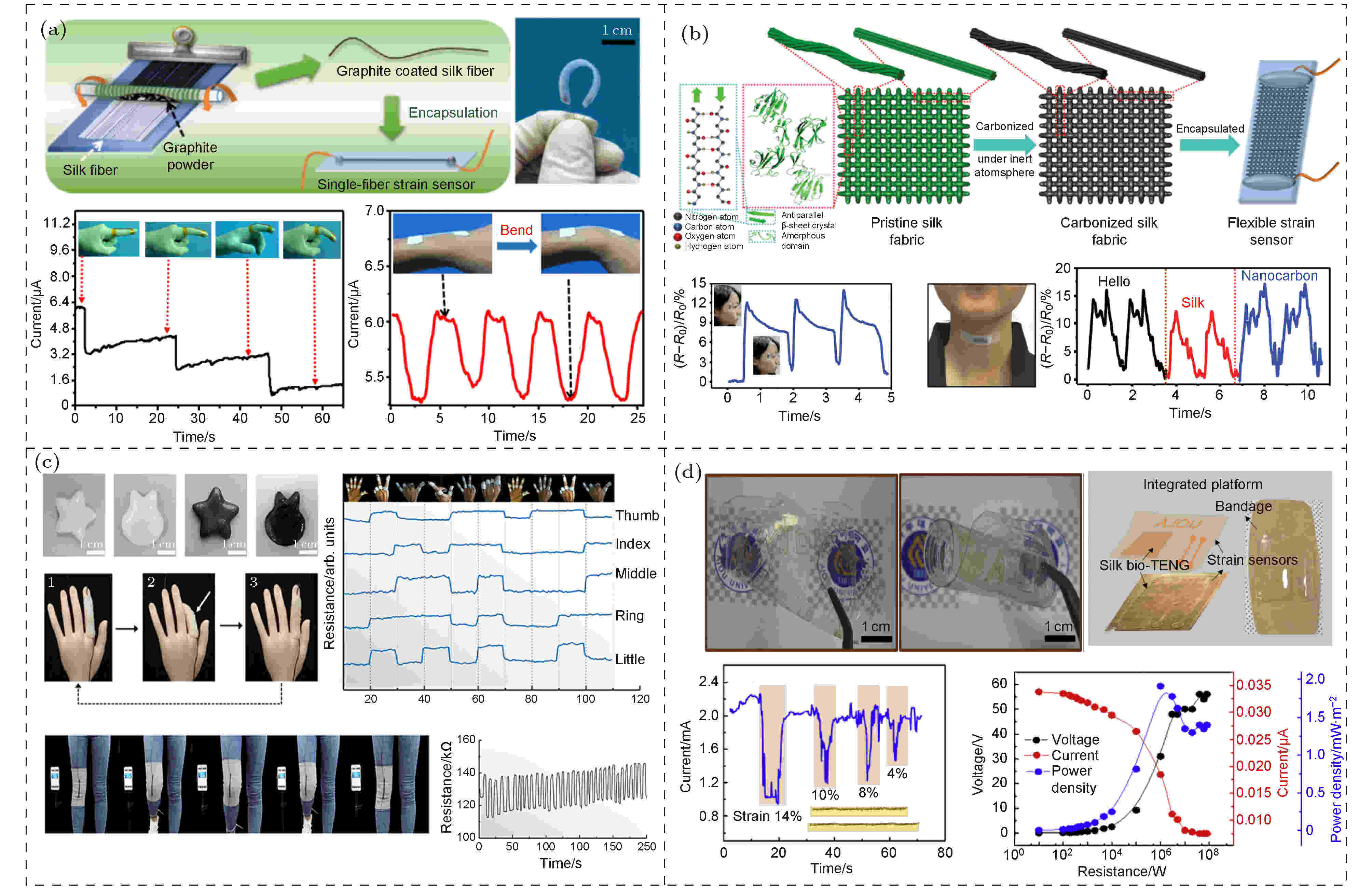 图 4 蚕丝基应变传感器的设计 (a)一种皮芯结构的石墨/蚕丝柔性应变传感器[34]; (b)一种基于碳化蚕丝织物的可穿戴应变传感器[65]; (c)一种用于监测人体运动的RSF基水凝胶[67]; (d)一种RSF基的单电极TENG和应变传感器整合平台[68]
图 4 蚕丝基应变传感器的设计 (a)一种皮芯结构的石墨/蚕丝柔性应变传感器[34]; (b)一种基于碳化蚕丝织物的可穿戴应变传感器[65]; (c)一种用于监测人体运动的RSF基水凝胶[67]; (d)一种RSF基的单电极TENG和应变传感器整合平台[68]Figure4. Design of silk-based strain sensor: (a) A graphite/silk flexible strain sensor with sheath-core structure[34]; (b) a wearable strain sensor based on carbonized silk fabric[65]; (c) an RSF-based hydrogel for monitoring human movement[67]; (d) an RSF-based single electrode TENG and strain sensor integrated platform[68].
2
3.2.机械压力传感器
2017年, 清华大学Qi等[35]利用静电纺丝技术将RSF溶液加工成纳米纤维薄膜, 随后对其进行碳化处理, 制得碳化的蚕丝纳米纤维膜(carbonized silk nanofiber membranes, CSNM)并将其作为传感器的活性材料. 使用聚二甲基硅氧烷(polydimethylsiloxane, PDMS)将其封装成透明的类皮肤电阻压力传感器. 当粘附在人体皮肤上可以检测和收集人体生理信号(脉搏、呼吸、静脉脉冲和声带振动)和物理信号, 并展示出高灵敏性(sensitivity, S), 在0.8—400.0 Pa下, S = 34.47 kPa–1, 在400—5000 Pa下, S = 1.16 Pa–1. 检测限最低为0.8 Pa, 响应时间小于16.7 ms, 在大于10000次循环下保持良好的稳定性. 此外, 可以通过改变静电纺丝时间来调节其灵敏度, 以满足各种应用的不同要求. 通过溶液法制备的RSF薄膜拥有良好的生物降解、生物相容以及亲肤性, 常常被视作皮肤和植入式电子设备的理想平台之一. 然而, RSF膜的固有脆性限制了其在柔性电子器件中的应用. 厦门大学Hou等[37]成功克服薄膜的脆性和水溶性, 开发了一种高度可拉伸、透明、柔韧、低弹性模量的RSF薄膜, 可以舒适地粘附在皮肤上, 不会产生排斥反应. 其次, 通过静电纺丝与转移技术将这种RSF薄膜与银纳米纤维(Ag nanofibers, Ag NFs)结合, 制备了一种柔性/可拉伸的Ag NFs/SF导电电极. 该电极具有可控的低表面电阻(10.5 Ω/sq)和高透光率(大于90%). 同时, 在拉伸大于 60%, 弯折次数超过 2200次后, 方阻保持不变. 基于此电极, 进一步制备出柔性电容式触觉传感器(图5(a)), 兼具压力和应变传感. 它不仅具有广泛的压力和应变的监测范围(从35 Pa—700 kPa), 还具有良好的透气/透水性和生物相容性, 因此可贴在皮肤上长期使用. 在监测人体活动上, 将传感器贴附在喉咙上可实时监测气管和食道的振动. 另外, 该传感器还能监测手臂的大幅度运动. 经过7200次循环稳定性测试后, 信号仍保持稳定. 结合其生物降解性和皮肤舒适性, 基于Ag NFs/SF的贴肤传感器将在体外甚至体内的健康监测设备中有广泛的应用前景. 2019年, Wu等[69]开发出一种蚕丝包裹的纤维型压力传感器(图5(b)). 其中每个传感单位由两根Ecoflex封装的导电纱线垂直贴合在一起组成, 而导电纱线首先需要将蚕丝纤维包裹在聚对苯二甲酸乙二醇酯(polyethylene terephthalate, PET)或聚氨酯(polyurethane, PU)纱线上, 随后再将Ag NWs涂覆在蚕丝纤维上或者纤维之间的空隙中. 在此, 蚕丝和Ag NWs的混合体为电极, Ecoflex为介电弹性体. 该传感器拥有高的灵敏度(0—4 kPa内, S = 0.136 kPa–1), 低的响应时间(0.25 s), 良好的稳定性(大于5000次循环). Wu等[38]制备了一种基于蚕丝纤维的全织物无线压力传感器(图5(c)), 通过在蚕丝织物表面上转移Ag NFs获得高导电织物(方阻为0.33 Ω/sq), 夹在两个织物电极之间的3D透气织物用作介电层. 该传感器具有0.283 kPa–1的灵敏度和良好的稳定性(大于20000个循环). 可用于监测人体运动(手指和关节等). 同时, 将其贴附在衣服上通过光纤感应线圈能进行无线实时压力检测, 谐振频率偏移灵敏度为6.8 MHz/kPa. 为此, 全织物传感器在电子皮肤智能织物领域将有广阔的应用前景.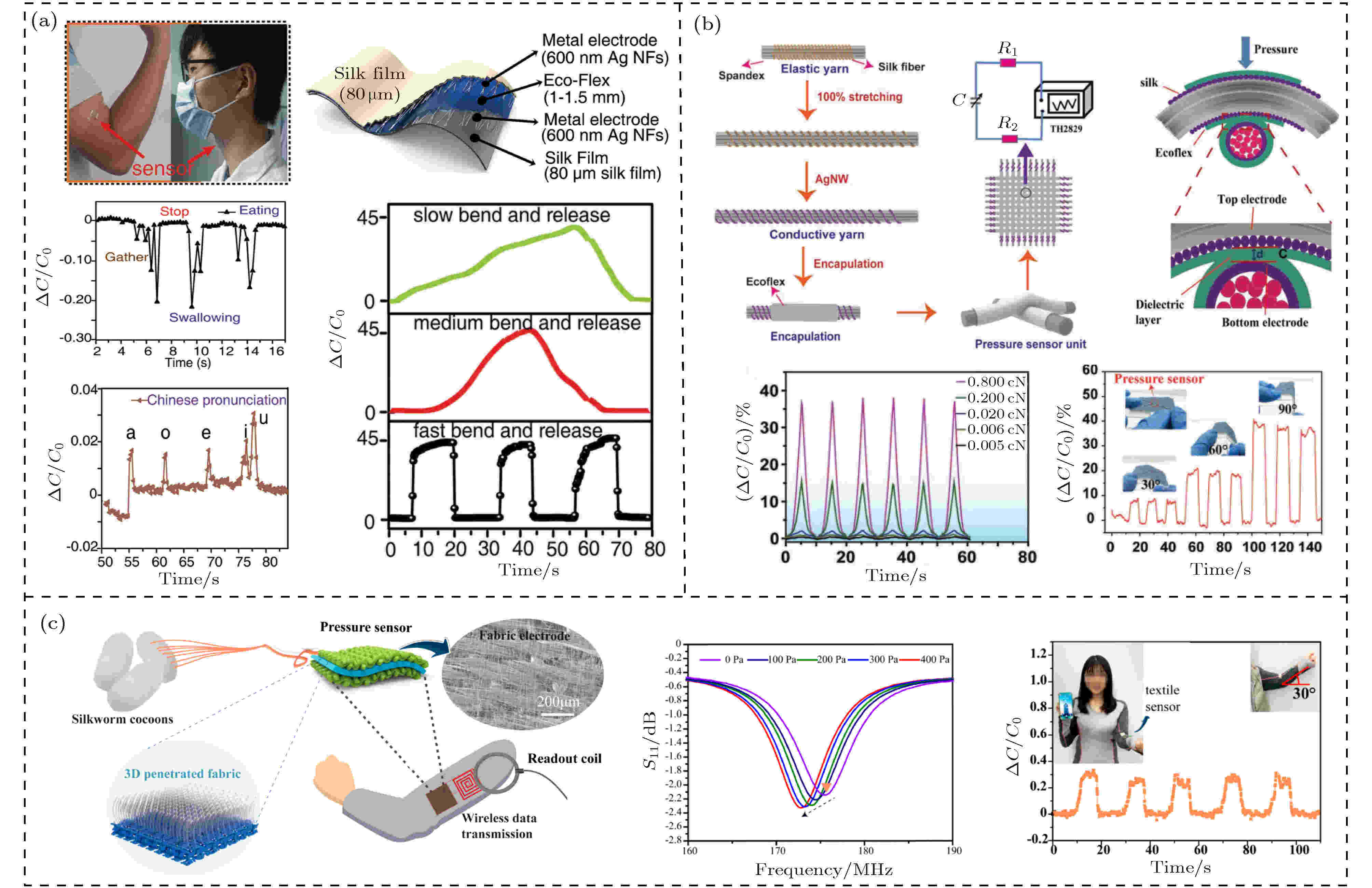 图 5 蚕丝基压力传感器的设计 (a)一种RSF基的生物相容和可降解压力传感器[37]; (b)一种蚕丝包裹的纤维基压力传感器[69]; (c)一种基于蚕丝织物的无线压力传感器[38]
图 5 蚕丝基压力传感器的设计 (a)一种RSF基的生物相容和可降解压力传感器[37]; (b)一种蚕丝包裹的纤维基压力传感器[69]; (c)一种基于蚕丝织物的无线压力传感器[38]Figure5. Design of silk-based pressure sensor: (a) An RSF-based biocompatible and degradable pressure sensor[37]; (b) a silk fiber wrapped fibrous pressure sensors[69]; (c) an wireless pressure sensor based on silk fabric[38].
2
3.3.电生理传感器
电生理传感器可检测人体心血管、神经和肌肉活动期间的生物电势变化[70]. 这些传感器的核心问题是设计薄的、共形的以及生物相容的表皮电极, 以减少皮肤与电极的接触阻抗. 因此, 为了获得可靠的电生理信号, 考虑柔软电极与皮肤之间的界面至关重要. 2018年, Chen等[36]在RSF膜中引入Ca2+, 并通过控制环境湿度, 得到塑化的RSF膜, 与人体皮肤有较高的贴合度. 增塑后的RSF膜杨氏模量从5—12 GPa减小为0.4—2.0 MPa, 拉伸率从20%增大到400%. 在此基础上, 将金(Au)沉积在RSF薄膜上制得电极. Au电极在塑化期间形成褶皱结构[71], 同时保持了电极的高导电性和可拉伸性. 由此组成的电生理传感器与皮肤产生共形接触, 实现低界面阻抗, 从而获得高质量的肌电图(electromyogram, EMG)信号 (图6(a)). 2018年, Seo等[72]报道了一种用于监测心电图(electrocardiogram, ECG)的Ca2+改性RSF水凝胶. 随着掺入Ca2+浓度升高, RSF水凝胶展现出强的粘弹性并实现了离子型导电, 电导率由0.005提高到5.99 mS/cm. 当RSF胶粘剂置于Ag/AgCl金属电极和生物界面之间时, 测得1.5 kΩ的低阻抗且2 h后阻抗没有变化. 如图6(b)所示, 由于金属电极和皮肤之间的弱接触和高阻抗, 可观察到基线的波动、高的噪声水平及较低的信号幅度. 相反, 含RSF的ECG电极测量的电生理信号清晰, 噪声水平低且基线波动可忽略. 由于商用水凝胶的剥离强度(0.2 N/m)较低, 这种电极在弯曲和松弛时, 会与皮肤发生脱落现象, 从而导致测量ECG信号波动. 而使用RSF的电极测量的信号即使在重复弯曲下也不会变形, 且在手臂上保持稳定, 不会在多次运动循环中脱落. 因此, RSF不仅可用作胶粘剂, 还可用作导电凝胶, 以精确测量实时的ECG信号. 与之类似地, Jo等[73]克服商用Ag/AgCl湿电极不能长期贴合皮肤的缺点, 开发出一种RSF基ECG传感器. 如图6(c)所示, 在PET基底上旋涂一层Ag NWs薄膜, 再利用RSF水凝胶将薄层与金属帽联锁在一起, 最后去除PET得到可监测ECG的电极. 虽然RSF/Ag NWs电极的ECG信号略微嘈杂, 但基线没有漂移表明电极很好地附着在皮肤上. 共形接触电极即使附着在出汗的皮肤上也能记录ECG信号, 产生清晰可见的P, Q, R, S和T波. 这些结果展示了RSF/Ag NWs电极作为ECG传感器的显著优势, 可用于人们的长期健康监测.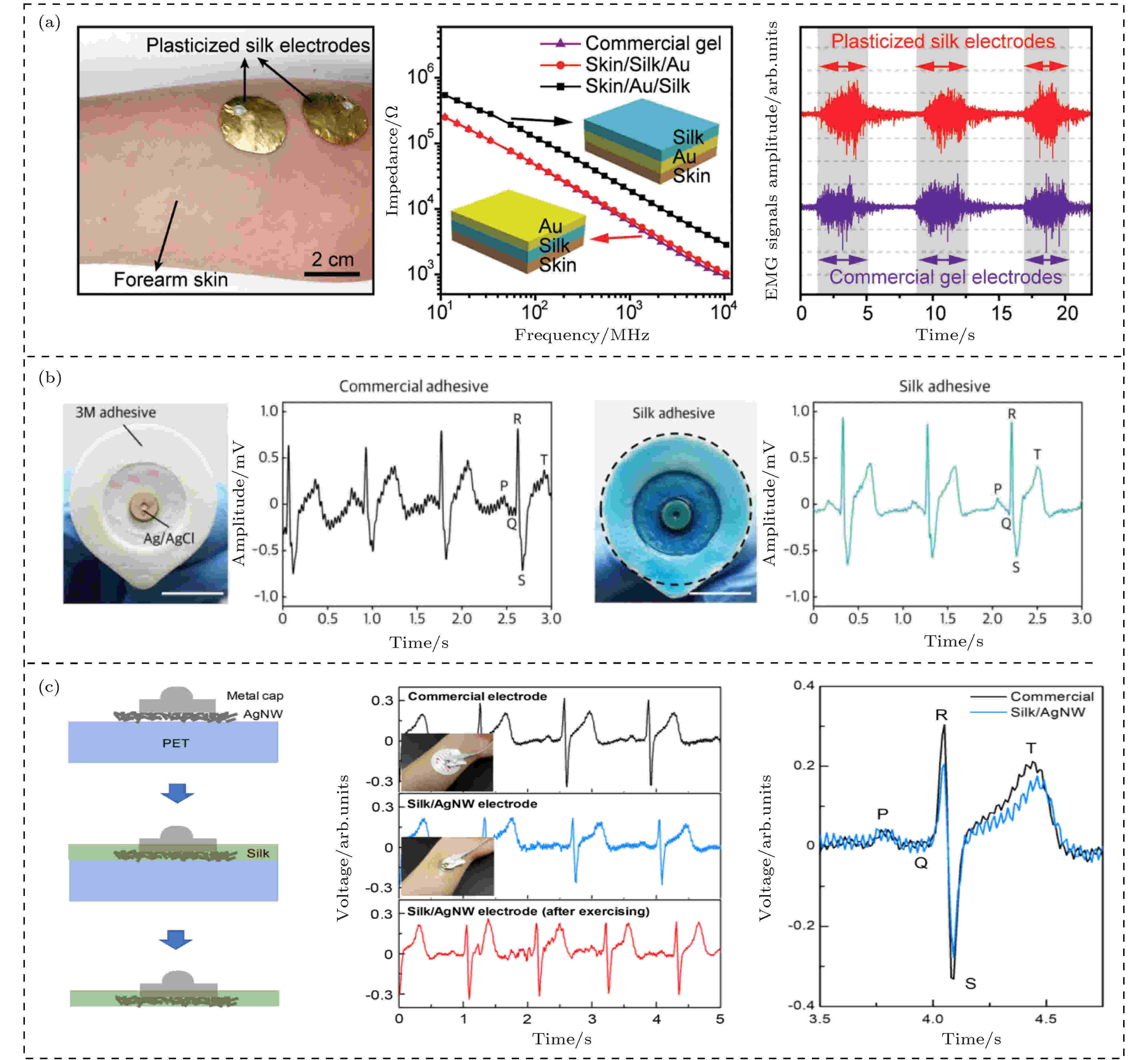 图 6 RSF基电生理传感器的设计 (a)一种用于EMG监测的RSF塑化电极[36]; (b)一种Ca2+改性的RSF胶粘剂[72]; (c)一种用于ECG监测的可穿戴Ag NW/RSF电极[73]
图 6 RSF基电生理传感器的设计 (a)一种用于EMG监测的RSF塑化电极[36]; (b)一种Ca2+改性的RSF胶粘剂[72]; (c)一种用于ECG监测的可穿戴Ag NW/RSF电极[73]Figure6. Design of RSF-based electrophysiological sensors: (a) An RSF plasticized electrode for EMG monitoring[36]; (b) a Ca2+ modified RSF adhesive[72]; (c) a wearable Ag NW/RSF electrode for ECG monitoring[73].
2
3.4.温度和湿度传感器
除了机械传感器和电生理传感器, 许多其他类型的蚕丝基可穿戴传感器被用作监测温度、湿气等. 2017年, Wang等[74]利用静电纺丝技术将蚕丝纤维沉积到铜箔上, 随后对其进行碳化处理, 再将其转移到PET基底上制得蚕丝衍生的双模传感器, 可同时监测温度和压力(图7(a)). 当温度升高时, 其电阻下降, 灵敏度约为0.81%/℃, 响应时间少于2 s. 此外该传感器显示出良好的柔韧性, 在弯折和正常的状态下对外部温度的改变有相同的响应. 厦门大学Wu等[69]通过对比Gr, CNT, Ag NWs和TF2N(一种离子液体)发现CNT+TF2N组合的温敏性能最好, 达到1.23%/℃. 将蚕丝纤维包裹在纱线上并涂覆CNT+TF2N, 最后利用Ecoflex将其封装成纤维传感器进而制备出电子织物(图7(b)). 蚕丝纤维作为中间介质增加了纱线的柔韧性、耐磨性及导热性. 该传感器在30—65 ℃范围内具有良好的灵敏度(|ΔR|R/R0/ΔT = 1.23%/℃). 在10 V的固定电压下, 器件的电流从30 ℃的17.30 μA增加到100 ℃的44.93 μA, 显示出负温度系数行为. 30—45 ℃的响应时间为16.5 s, 400个循环期内性能保持稳定. 这表明了传感器具有良好的稳定性和循环性. 此外, 蚕丝包裹结构增加了纤维的柔韧性, 从而该传感器可以承受较大的弯曲而不改变其导电性能. 在弯曲角度0°—360°下, 传感器的电阻变化小于1%. 此外, 其还具有感测水温和防水性能, 适用于制造手套和衣服等纺织品. 厦门大学Huang等[39]设计了一种三明治夹层的RSF基加热控温器件(图7(d)), 通过在RSF复合膜两面分别构筑高机械柔性的金属纳米丝来实现加热与测温. 在加热方面, 将银的纳米纤维丝与此RSF复合膜结合, 得到柔性可穿戴的蛋白基加热器, 该加热器能量密度达到152.2 W–1·cm2, 在75%拉伸下, 其发热温度变化小于10%. 除了稳定的焦耳加热性能, 该加热器利用热致变色原理, 作为电子皮肤, 能在特定环境下对人体进行伪装. 在控温方面, 铂(Pt)纳米网络与RSF复合膜结合得到测温元件. 如图7(d)所示, 用模板法分隔成的5 × 5的阵列型感温元件, 并结合喷墨打印法制备电路. 研究表明, 这种阵列型测温器能较精确地获得加热器发热的温度分布图和每个单元的温度值, 实现了皮肤加热与控温. 同时, 该RSF基柔性温度传感器具有生物相容性与降解性, 消除了因合成材料引起大量电子垃圾的顾虑, 且能较好地实现规模化控温加热功能. 在蚕丝基湿度传感器的研究中, Wang等[75]报道了一种基于Gr/RSF/Ca2+的自愈合、多功能电子纹身. 这种高度灵活的电子纹身通过将Gr/RSF/Ca2+悬浮液打印或直接书写在RSF薄膜上制得(图7(c)). RSF/Ca2+薄膜提供了可拉伸性和生物相容性, 可以长时间贴肤使用, 而分布在基质中的Gr形成导电路径, 用于响应环境变化. 由于其对多种刺激的灵敏性, 被开发为兼具应变、湿度和温度的多功能传感器. 当相对湿度从11.3%增加到85.1%时, 相对电阻变化(R/R0)从0.2%增加到2.3%. 这表明 Gr/ RSF/Ca2+薄膜能够监测较大范围的湿度变化. 且其在重复的湿度感应测试中有良好的稳定性, 响应和恢复时间(定义为达到稳定值的90%所需的时间)分别为3和6 s. 这与大多数报道的湿度传感器[76-78]相当. 其湿度传感的原理与Gr/RSF/Ca2+基质与水分子的相互作用有关. 因为RSF基质中的Ca2+离子可以从环境中捕获水, 一个Ca2+离子可以结合6—8个水分子[79]. 因此, 相对湿度越大, 越多的水分子被Ca2+捕获, 从而导致基质膨胀和Gr导电路径的减少[80]. 这个过程是可逆的, 当相对湿度恢复到其初始值时, 传感器电阻又恢复到原点状态. 2020年, Luo等[81]开发了一种基于Ag NWs 叉指电极(interdigitated electrodes, IDEs)的RSF薄膜传感器, 用于可穿戴式呼吸监测. 其通过刮涂、氧化和刻蚀等工艺将IDE与RSF集成在一起. 经处理后的RSF薄膜显示出对水蒸气渗透及人类呼吸的出色响应, 能准确区分人的呼吸频率, 有效辨别正常、深呼吸及快呼吸, 响应速度快(4 Hz). 该湿度传感器在弯曲测试中表现出良好的机械稳定性, 并且能直接与商业电容测试模块集成在一起, 这表明其在未来能以环保、便携式和低成本的方式应用于呼吸监测.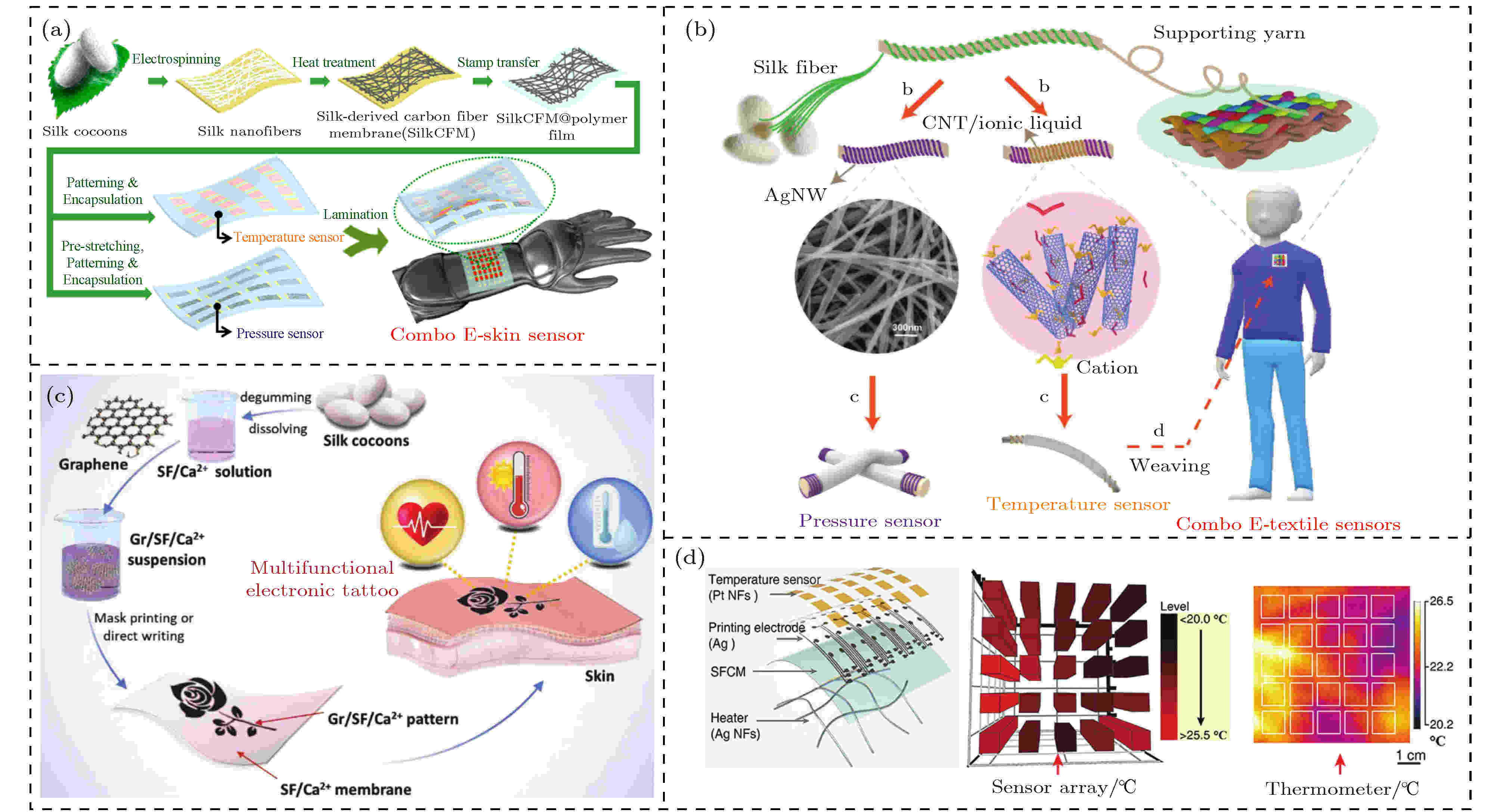 图 7 蚕丝基温度和湿度传感器的设计 (a)一种蚕丝衍生的可穿戴温度和压力传感器[74]; (b)一种可监测温度和压力蚕丝基电子织物[69]; (c)一种基于RSF的可自愈的多功能电子纹身[75]; (d)一种可控温的RSF基耐热电子皮肤[39]
图 7 蚕丝基温度和湿度传感器的设计 (a)一种蚕丝衍生的可穿戴温度和压力传感器[74]; (b)一种可监测温度和压力蚕丝基电子织物[69]; (c)一种基于RSF的可自愈的多功能电子纹身[75]; (d)一种可控温的RSF基耐热电子皮肤[39]Figure7. Design of silk-based temperature and humidity sensor: (a) A silk-derived wearable temperature and pressure sensor[74]; (b) a silk-based electronic fabric for temperature and pressure sensing[69]; (c) a self-healable multifunctional electronic tattoos based on RSF[75]; (d) an RSF-based heat-resistant electronic skin for thermoregulation[39].
尽管已经获得了各种性能良好的蚕丝基物理传感器, 但离产业化仍有很长距离. 例如, 许多研究集中在检测单个信号并提高其感测性能上, 而尚未实现无噪声干扰的同时多模态检测[82]. 传感器与电源、通信和数据处理单元的集成是另一个巨大的挑战. 目前, 传感信号是通过传感器和数据采集系统的刚性接线接收的, 这些信号未达到实时健康监控中便携性和舒适性的要求. 然而, 考虑到蚕丝基可穿戴传感器仅在最近几年才出现, 因此可以期待具有高灵敏度、灵活性、生物相容性、耐用性和便携性的新型传感器出现.
