全文HTML
--> --> -->众所周知, 材料特定的性能必对应特定的结构. 因此, 从结构根源出发, 寻找成分背后的结构载体, 即寻找最小结构单元, 从原子或分子层面认识成分规律、建立适用的成分设计方法, 是优化成分设计、提升材料性能的有效途径.
对于玻璃而言, 成分非常复杂, 比如手机的盖板玻璃至少含有十几种氧化物, 由于缺少准确描述玻璃成分结构的方法, 导致无法认清成分背后的结构载体, 无法建立成分、结构和性能之间的关联, 因此长期以来, 不得不依靠大量的实验探索来改善玻璃性能. 而本文基于团簇加连接原子模型构造的类分子结构单元, 将有助于我们认识玻璃成分的结构根源, 有望解决氧化物玻璃的成分设计难题.
1)化学成分: H:O = 2:1;
2)满足八电子规则的稳定电子结构: 价电子数e/u = 8, 电荷平衡H+1×2+O–2=0如图1所示;
3)特定的原子空间构型: H—O—H, 氧氢键键角为105°;
4)分子的原子密度等于由该分子组成的物质密度;
5)分子内的化学键强

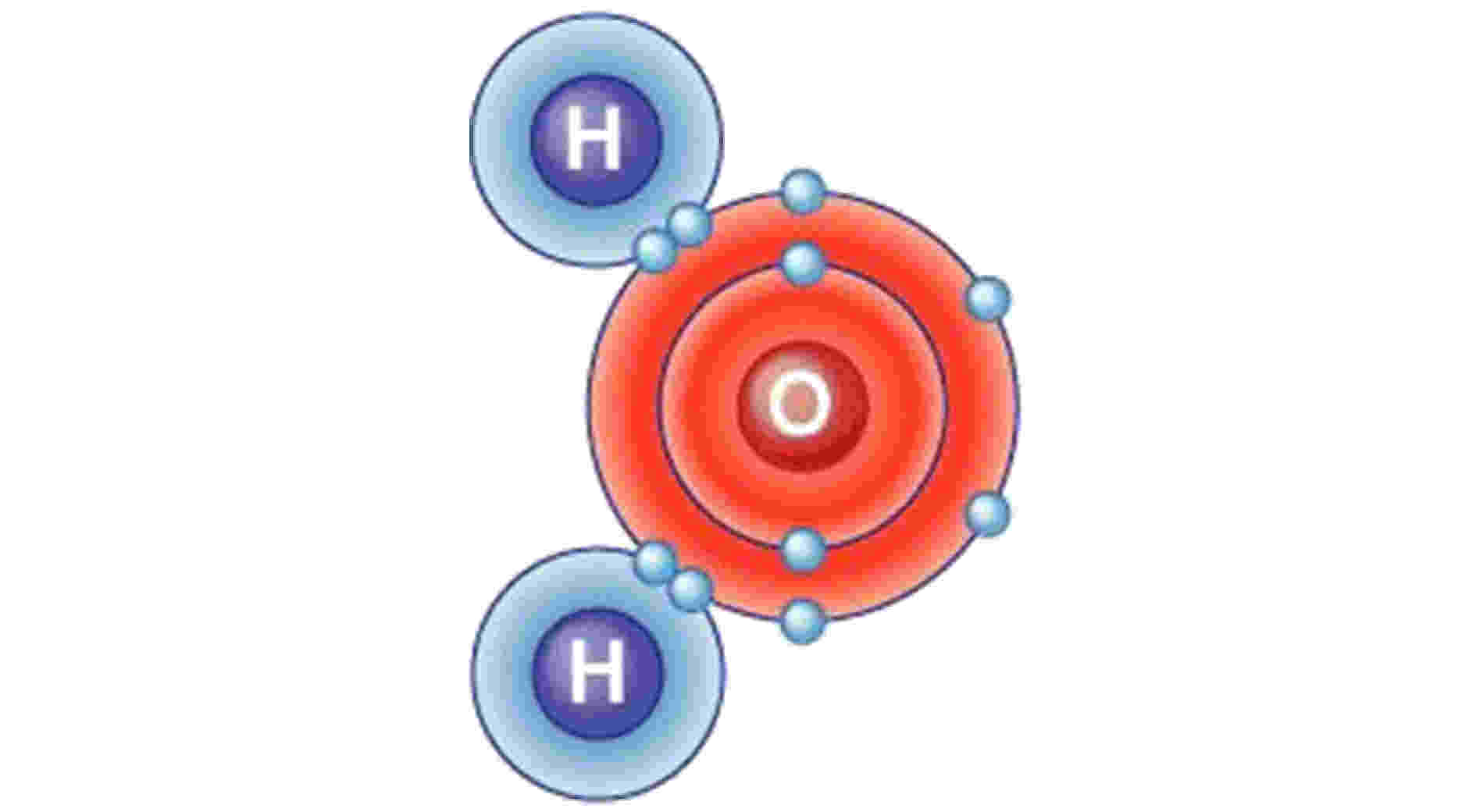 图 1 水分子的电子结构[2]
图 1 水分子的电子结构[2]Figure1. Electron structure of water molecule[2].
上述分子特征保证了物质化学性质落在分子层面上. 其中最后一个特征可以使我们认为分子是一个独立的结构单元.
但是, 很多化合物并不存在H2O这类独立的结构单元, 例如二氧化硅(图2), Si原子与4个O原子相连, 形成一个以Si为中心, O为最近邻的四面体[Si-O4], 中心的4价Si为4个Si—O键中的每个键贡献1个电子, 使得每个O获得1个电子后, 周围有7个电子, 这与8个电子的稳定电子构型相比, 缺少1个价电子. 于是, 4个O原子立即与下一个壳层中的Si原子相连, 以便在这些O原子中满足八电子规则, 而这些Si原子又需要进一步连接O原子······也就是说, 没有明确的界线来定义像H2O分子那样独立的结构单元. 可见, 无机化合物(例如SiO2)的化学式仅表示元素的组成种类和化学价信息, 但并未给出类似于分子的结构单元, 而团簇加连接原子模型恰恰可以解决这个难题.
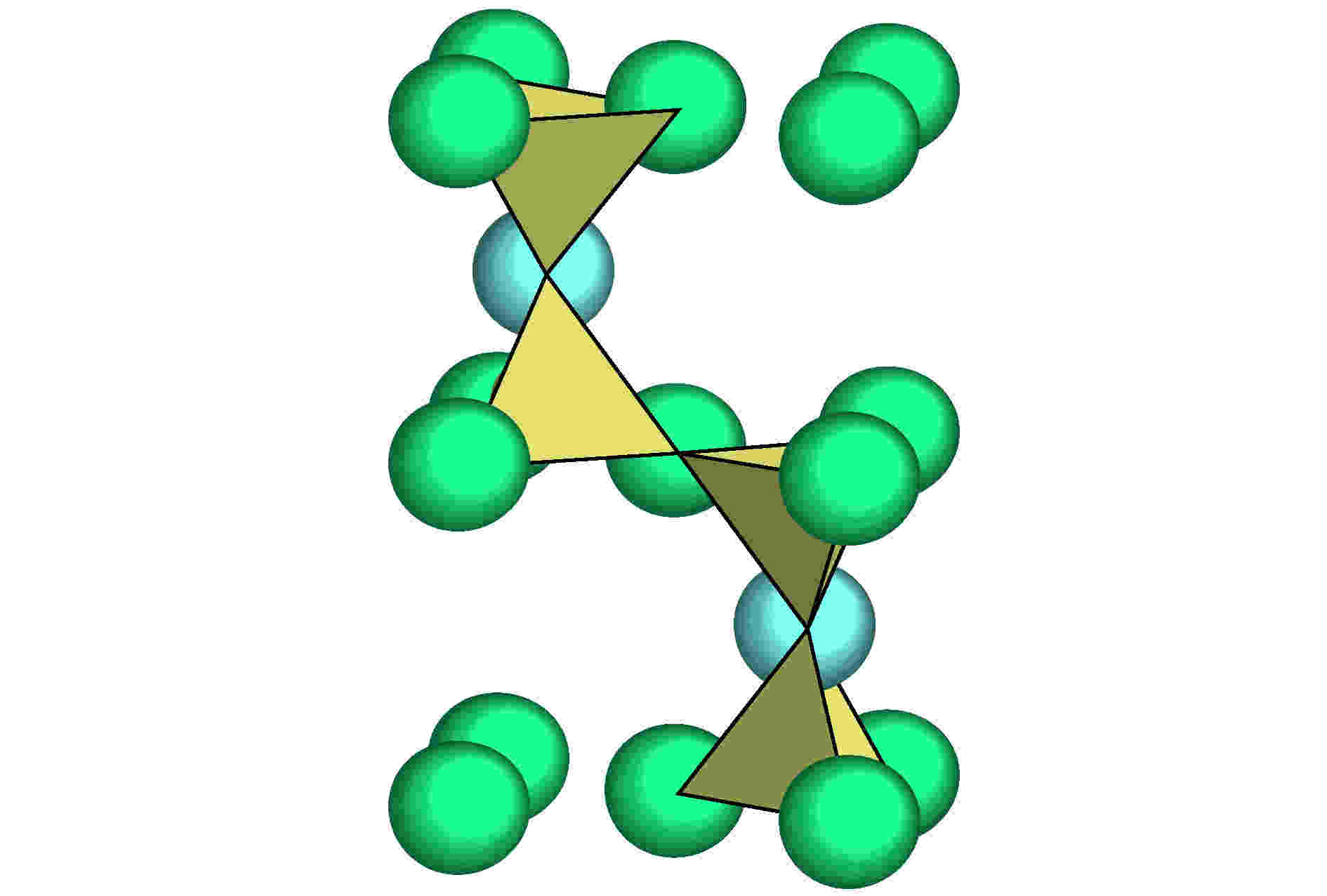 图 2 基于[Si-O4]四面体的鳞石英β-SiO2晶体结构[3]
图 2 基于[Si-O4]四面体的鳞石英β-SiO2晶体结构[3]Figure2. Crystal structure of β-SiO2 using tetrahedral cluster [Si-O4][3].
基于氧化硅的玻璃, 是一种非晶态的无序固体, 其结构长程无序, 但是呈现接近于稳定的晶态结构的近程序特征, 氧化硅玻璃的近程序基本保持了[Si-O4]四面体的原子排列(图3)[4-7]. 我们知道, 无论是在晶态还是非晶态结构中, 近邻原子间都存在强烈的交互作用, 这种交互作用导致了近程序的产生, 可以用第一近邻配位多面体(本文简称为团簇)来描述这种近程有序. 课题组在第一近邻配位多面体团簇概念的基础上, 提出了用于描述局域结构有序性的团簇加连接原子模型[8-10], 在该模型中, 任何一个相结构都可看做由团簇(即最近邻的配位多面体)和团簇之外的少量连接原子构成, 如图4所示[11], 可以用团簇式: [团簇](连接原子) x表示, 其中x表示连接原子个数.
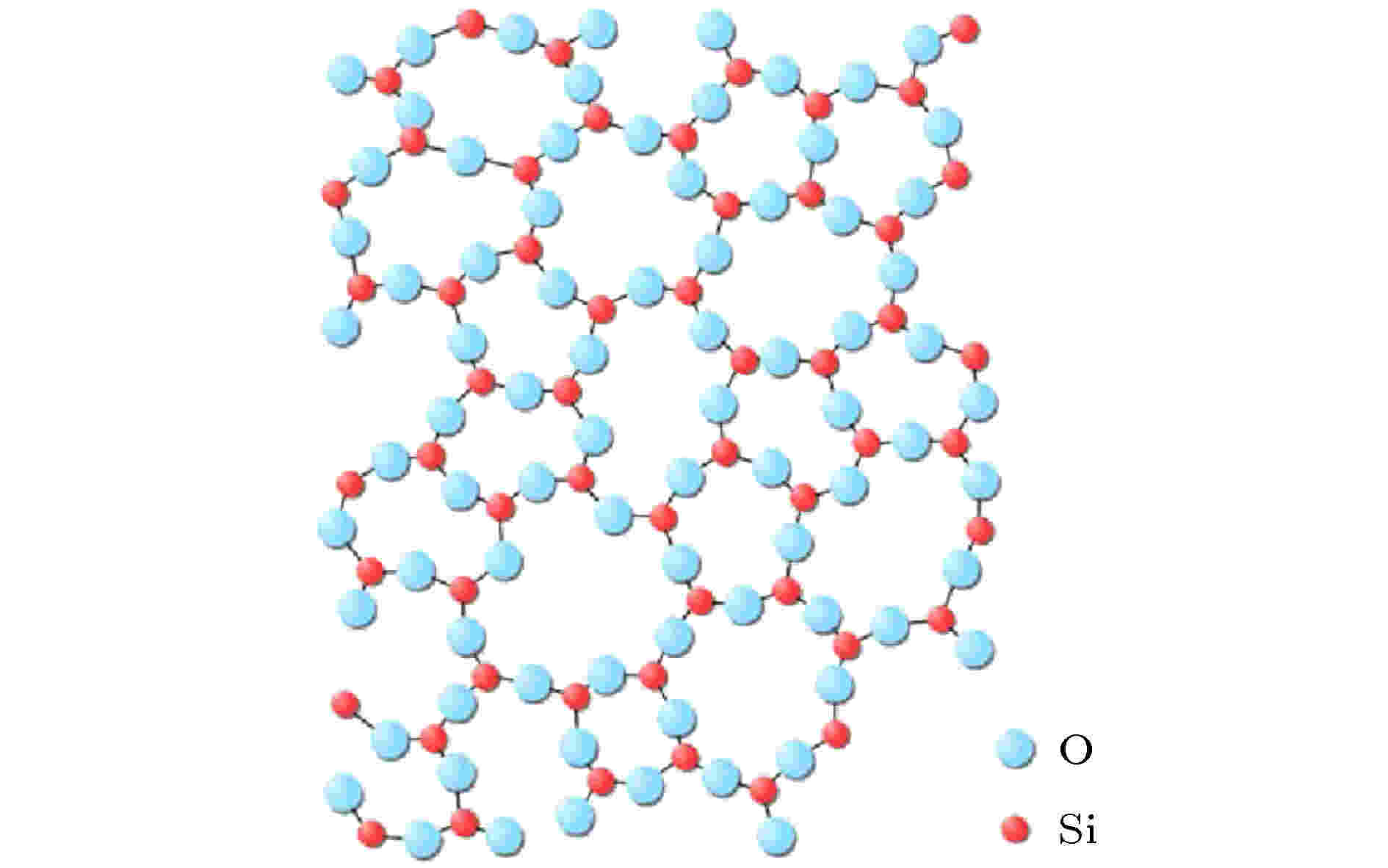 图 3 氧化硅玻璃的结构示意图, 显示了长程无序和近程有序(硅氧四面体)特征[4]
图 3 氧化硅玻璃的结构示意图, 显示了长程无序和近程有序(硅氧四面体)特征[4]Figure3. The amorphous structure of glassy silica (SiO2) in two dimensions[4]
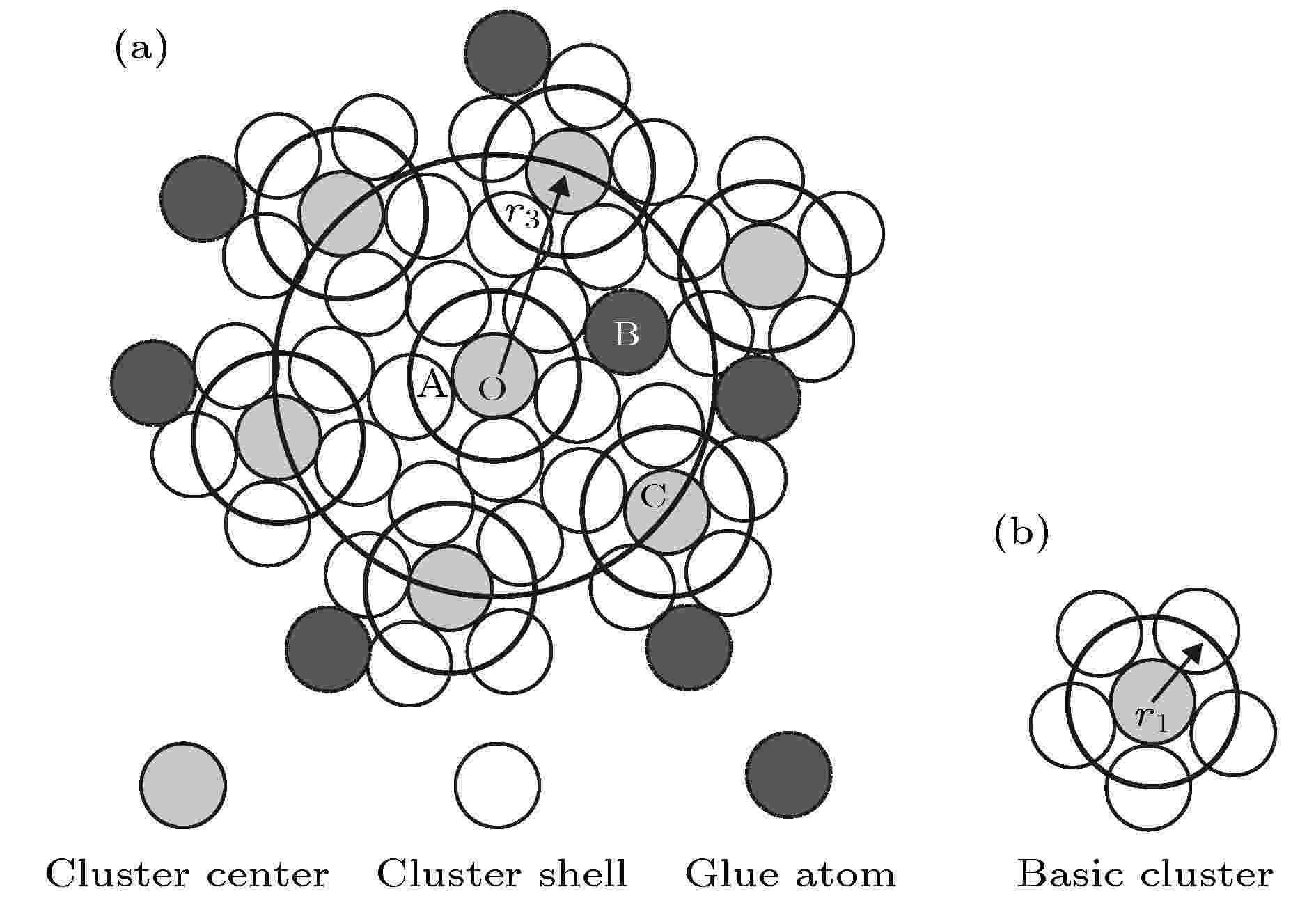 图 4 (a) 团簇加连接原子模型[11]; (b) 团簇的间距为r3
图 4 (a) 团簇加连接原子模型[11]; (b) 团簇的间距为r3Figure4. (a) Cluster-plus-glue-atom model[11]; (b) the inter-cluster distance is r3.
团簇是反映相结构最近邻局域结构有序性的配位多面体, 这里的最近邻有别于一般意义上的最近邻, 一般意义上最近邻指的是离中心原子最近的壳层原子, 而这里的最近邻可能包括多个子壳层. 团簇内部原子具有相对较强的原子键合作用, 因此团簇结构比较稳定, 而团簇之间的连接则相对较弱[12]. 在一个给定的相结构中, 往往存在多个局域团簇, 一般只有一个(亦有例外)能进入到描述稳定非晶结构的成分式中, 我们称之为“主团簇”[13]. 主团簇被认为是键合最强的局域结构, 由于其稳定性强, 这部分通常在相变后会保留下来, 即具有遗传性. 从几何结构上看, 主团簇的原子密堆度趋向于理想密堆, 并具有高度的团簇分离度(由于晶体中的周期性约束, 团簇之间往往相互重叠), 这两个性质通常作为主团簇的判据[13-15]. 而连接原子位于团簇之外次近邻的位置, 因此, 该模型实际上描述了最主要的化学局域结构和拓扑结构, 这种团簇式提供了相结构的局部近程有序特征的平均图像.
团簇加连接原子模型反映着第一近邻和次近邻的化学近程序特征, 能够像“分子”一样描述有序和无序的非分子型材料的结构特征, 即第一近邻团簇加上若干位于次近邻的连接原子构成了“类分子”结构单元[14,16], 它是满足八电子规则[17]的最小结构单元, 类似于“分子”那样兼具成分、原子构型、电子平衡和密度等信息, 只是不存在分子间的弱相互作用力. 化合物的类分子结构单元统一表示式为: [主团簇](连接原子)x, 其中e/u = 8n.
建立类分子结构单元的第一个要点是确定主团簇, 前文指出筛选主团簇的两个规则——原子密堆度和团簇分离度. 原子密堆意味着主团簇应是所有团簇中原子最密集的, 由中心原子与第一近邻原子壳层原子的平均原子半径比值R*来衡量[18]. 团簇分离度实际上强调了团簇的连接性质在结构中的重要性, 即一个优选出来的团簇不会与同类的相邻团簇共享很多原子, 而是保持相对较高的孤立度. 为了选择孤立度高的主团簇, 通常根据最大的相成分式进行判断.
建立类分子结构单元的第二个要点是连接原子的种类与个数的选择. 要考虑两方面: 一是要保证类分子结构单元与分子一样, 内部电子结构具有稳定性. 参考分子中的八电子规则, 本文要求主团簇加连接原子构成的类分子结构单元, 价电子数为8n个. 另一方面, 要实现8n个电子, 存在多种选取连接原子的方法, 因此, 要参考实际结构中次近邻位置出现的原子种类, 同时要保证构建的结构单元最小.
下面以β-SiO2为例, 叙述类分子结构单元的构建过程:
1)分析化合物结构, 获得所有第一近邻配位多面体团簇.通过皮尔森手册可知β-SiO2(空间群194, 表1[19])的数据信息. 以β-SiO2相的3个非等效占位为中心可确立3个团簇, 其中O1, O2为心的团簇均为[O-Si2], 配位数为CN2; 以Si为心的团簇是配位数为CN4的四面体[Si-O4](图5(a)).
| O2Si | Structure type O2Si | Pearson symbol hP12 | Space group P63/mmc | No.194 | ||
| a = 0.5052(9) nm | c = 0.827(2) nm | γ = 120° | ||||
| O1 | 2c | $ {\bar 6}m2$ | x = 1/3 | y = 2/3 | z = 1/4 | occ. = 1 |
| Si | 4f | 3m. | x = 1/3 | y = 2/3 | z = 0.0620 | occ. = 1 |
| O2 | 6g | .2/m | x = 1/2 | y = 0 | z = 0 | occ. = 1 |
表1鳞石英(Tridymite)β-SiO2的晶体结构数据表[19]
Table1.Crystal structure data of Tridymite β-SiO2[19].
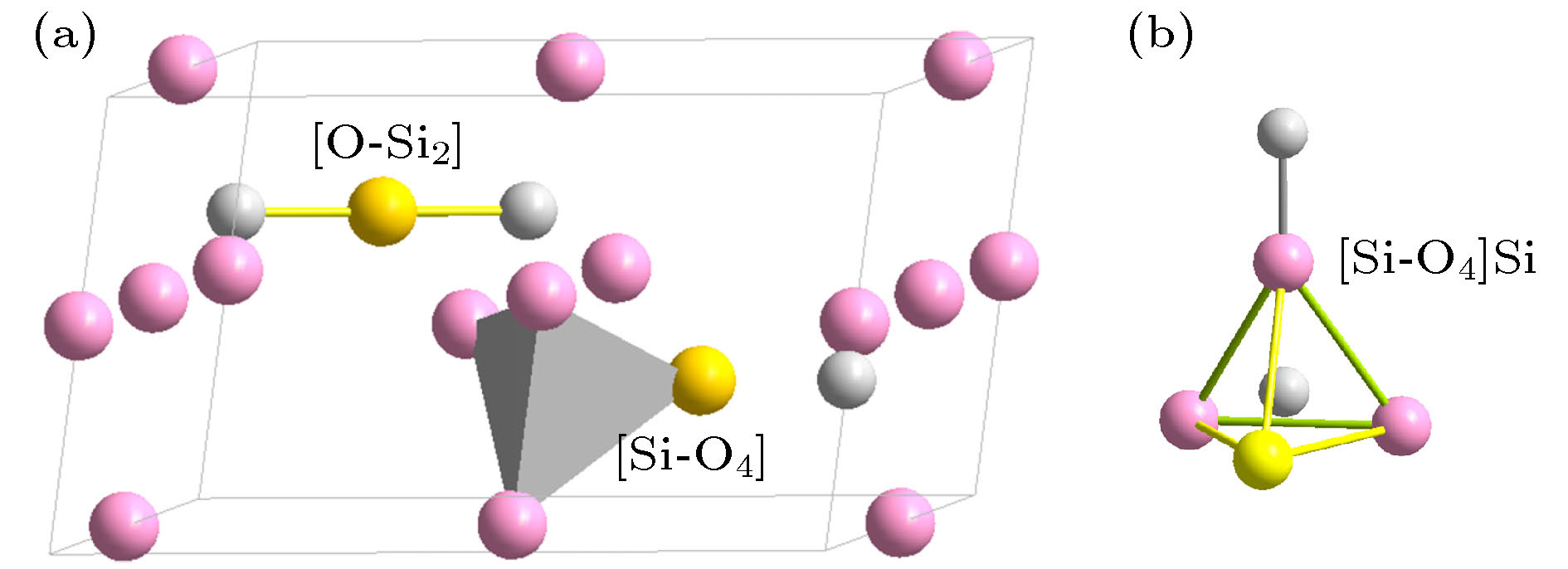 图 5 (a) β-SiO2(SiO2结构, 空间群194)的主团簇[Si-O4]和[O-Si2], 大原子为O, 小原子为Si; (b)类分子结构单元[Si-O4]Si
图 5 (a) β-SiO2(SiO2结构, 空间群194)的主团簇[Si-O4]和[O-Si2], 大原子为O, 小原子为Si; (b)类分子结构单元[Si-O4]SiFigure5. (a)Principal cluster [Si-O4] and [O-Si2] in β-SiO2 structure (space group 194). Large and small spheres are O and Si atoms, respectively; (b) molecule-like structural unit[Si-O4]Si.
2)按照原子个数的比例, 构建反映团簇共享关系的有效团簇.在周期结构中, 团簇之间往往有重叠, 为了获得有效团簇, 需要分析团簇之间的搭接方式, 这个过程比较复杂. 实际上, 无论团簇之间满足何种共享关系, 最后的有效团簇均满足晶体结构给出的原子个数比例. 根据表1, 在1个β-SiO2晶胞内的3个非等效占位上, 原子个数分别为2(O1), 4(Si), 6(O2), 即3种位置的原子个数比为O1∶Si∶O2 = 2∶4∶6 = 1∶2∶3. 由于有效团簇满足晶体结构给出的原子个数比, 因此, 以O1为心的有效团簇保持不变, 仍为[O-Si2](两种原子个数比为O1∶Si = 1∶2); 而以Si为心的团簇[Si-O4]则变成[Si-O1/2O3/2], 其中壳层上有O1和O2两种O原子, Si与其个数比分别为1∶1/2和1∶3/2; 以O2为心的团簇[O-Si2]则变成[O-Si2/3], 此时两种原子个数比为O2∶Si = 3∶2.
3)将有效团簇匹配以合适的连接原子, 使其满足相成分比例. 根据最大相成分式对应的团簇即为主团簇, 我们按照表1所给的相成分比例O1∶Si∶O2 = 2∶4∶6 = 1∶2∶3, 将前面获得的3种有效团簇[O-Si2](O1为心), [Si-O1/2O3/2](Si为心), [O-Si2/3](O2为心), 匹配以连接原子, 得到对应的相成分式[O-Si2]O3, [Si-O1/2O3/2], [O-Si2/3]O1/3. 可以看到, 以O1为心构建的相成分式[O-Si2]O3最大, 故[O-Si2]应为主团簇. 但根据密堆性判据R*推断, 团簇中心应为小原子. 由于Si-O键具有双重的共价和离子键属性, 大约各占一半, 如果取共价半径(O为0.068 nm, Si为0.117 nm), 则[O-Si2]仍为主团簇; 如果取离子半径(O为0.14 nm, Si为0.041 nm), 则[O-Si2]不满密堆要求, 而是以小离子Si为心的团簇[Si-O4]为密堆团簇, 因此本文将两个团簇均处理为主团簇.
根据建立类分子结构单元的第二个要点, 将主团簇[O-Si2]和[Si-O4]匹配以合适的连接原子, 得到类分子结构单元[O-Si2]O3, [Si-O4]Si(图5(b)), 可见[O-Si2]O3 = [Si-O4]Si = Si2O4, 即主团簇可以不唯一, 但最终构建的类分子结构单元必唯一.
[O-Si2]O3和[Si-O4]Si的类分子特征总结如下:
1) 具有相的化学成分比例Si∶O = 1∶2;
2) 内部电荷平衡(2个Si4+与4个O2–), 外层电子总数为e/u = 32个(e/u指1个结构单元所具有的价电子个数), 满足八电子规则;
3) 结构单元和相的原子密度相等;
4) 特定的局域构型, 覆盖第一近邻及次近邻连接原子;
5) 原子间化学键在空间连续分布, 而无弱的分子键的间隔.
可见, 除了最后一点外, 本文利用团簇加连接原子模型定义的结构单元均满足分子的特征, 故称之为“类分子结构单元”, 表示为类分子式: [主团簇](连接原子)x, 它是满足八电子规则的最小结构单元. 虽然实际中类分子结构单元之间并无弱分子键间隔, 但整个二氧化硅物质可以等效于最小结构单元Si2O4的堆垛.
| Classification | Oxide (space group) | Cationic structural unit (e/u) | Anion structural unit (e/u) |
| Network formation | β-SiO2 (P63/mmc) | [Si-O4]Si = 2{SiO2} (32) | [O-Si2]O3= 2{SiO2} (32) |
| B2O3 (P31) | [B-O3]B = {B2O3} (24) | [O-B2]O2 = {B2O3} (24) | |
| B2O3 (Cmc21) | [B-O4]B3O2 = 2{B2O3} (48) | [O-B2]O2 = {B2O3} (24) | |
| [O-B3]O5B1 = 2{B2O3} (48) | |||
| GeO2 (P41212) | [Ge-O4]Ge = 2{GeO2} (32) | [O-Ge2]O3 = 2{GeO2} (32) | |
| P2O5 (Pnma) | [P-O4]P1O1 = {P2O5} (40) | [O-P2]O4 = {P2O5} (40) | |
| [O-P1]P1O4 = {P2O5} (40) | |||
| Network outside body | (Li, Na, K)2O (anti-fluorite$ Fm{\bar 3}m$) | [(Li, Na, K)-O4](Li, Na, K)7 = 4{(Li, Na, K)O2} (32) | [O-(Li, Na, K)8]O3 = 4{(Li, Na, K)O2} (32) |
| (Mg, Ca, Ba)O (Halite, $ Fm{\bar 3}m$) | [(Mg, Ca, Ba)-O6](Mg, Ca, Ba)5 = 6{(Mg, Ca, Ba)O} (48) | [O-(Mg, Ca, Ba)6]O5 = 4{(Mg, Ca, Ba)O} (48) | |
| ZrO2 (rutile, P42/mnm) | [Zr-O6]Zr2 = 3{ZrO2} (48) | [O-Zr3]O5 = 3{ZrO2} (48) | |
| Network intermediate | (Be, Zn)O (sphalerite, P43m) | [(Be, Zn)-O4](Be, Zn)3 = 4{(Be, Zn)O} (32) | [O-(Be, Zn)4]O3 = 4{(Be, Zn)O} (32) |
| (Be, Zn)O (Wurtzite, P63mc) | [Zn-O4]Zn3 = 4{ZnO} (32) | [O-Zn4]O3 = 4{ZnO} (32) | |
| (Be, Zn)O (Halite, $ Fm{\bar 3}m$) | [Zn-O6]Zn5 = 6{ZnO} (48) | [O-Zn6]O5 = 6{ZnO} (48) | |
| α-Al2O3 ($ R{\bar 3}c$) | [Al-O6]Al3 = 2{Al2O3} (48) | [O-Al4]O5 = 2{Al2O3} (48) | |
| γ-Al2O3 (Spinel, $ Fd{\bar 3}m$) | [Al-O4]O2Al3 = 2{Al2O3} (48) | [O-Al4]O5 = 2{Al2O3} (48) | |
| [Al-O6]Al3 = 2{Al2O3} (48) | |||
| Ga2O3 (α-Al2O3, $ R{\bar 3}c$) | [Ga-O6]Ga3 = 2{Ga2O3} (48) | [O-Ga4]O5 = 2{Ga2O3} (48) | |
| Ga2O3 (Spinel, $ Fd{\bar 3}m$) | [Ga-O4]O2Ga3 = 2{Ga2O3} (48) | [O-Ga4]O5 = 2{Ga2O3} (48) | |
| [Ga-O6]Ga3 = 2{Ga2O3} (48) | |||
| Fe2O3 (α-Al2O3, $ R{\bar 3}c$) | [Fe-O6]Fe3 = 2{Fe2O3} (48) | [O-Fe4]O5 = 2{Fe2O3} (48) | |
| Fe3O4 (Spinel, $ Fd{\bar 3}m$) | [Fe-O4]Fe2 = {Fe3O4} (32) | [O-Fe4]O7Fe2 = 2{Fe3O4} (64) | |
| [Fe-O6]Fe5O2 = 2{Fe3O4} (64) | |||
| TiO2 (Rutile, P42/mnm) | [Ti-O6]Ti2 = 3{TiO2} (48) | [O-Ti3]O5 = 3{TiO2} (48) | |
| TiO2 (Anatase, I41/amd) | [Ti-O6]Ti2 = 3{TiO2} (48) | [O-Ti3]O5 = 3{TiO2} (48) | |
| TiO2 (Brookite, Pbca) | [Ti-O6]Ti2 = 3{TiO2} (48) | [O-Ti3]O5 = 3{TiO2} (48) | |
| TiO2 (P21/m) | [Ti-O4]Ti = 2{TiO2} (32) | [O-Ti2]O3 = 2{TiO2} (32) | |
| [Ti-O3]TiO = 2{TiO2} (32) | [O-Ti]O3Ti = 2{TiO2} (32) |
表2硅酸盐玻璃相关氧化物的类分子结构单元, 分为中心为阳离子和阴离子O两种; 依托于主团簇的类分子结构单元用黑体标出
Table2.Molecule-like structural units of glass-relevant oxides. Molecule-like structural unit, based on principal clusters, are bolded.
2
3.1.网络形成体
在玻璃体系中, 能够单独形成玻璃网络体结构的氧化物有SiO2, B2O3, GeO2, P2O5[20,21]. 它们的配位数一般为3或4, 所形成的配位多面体为三角形或四面体. 在玻璃的网络形成体的结构单元中, 彼此之间以顶角相连, 是极性共价键, 具有离子和共价键特性, 共价键占大多数, 键能一般为338.6—497.4 kJ/mol. 前文已描述β-SiO2(图5(a))的类分子结构单元, 现讨论另一种网络形成体中常见的氧化物B2O3(如图6(a)和图6(b)), 此外还给出其他氧化物GeO2(如图6(c)), P2O5(如图6(d))的团簇结构.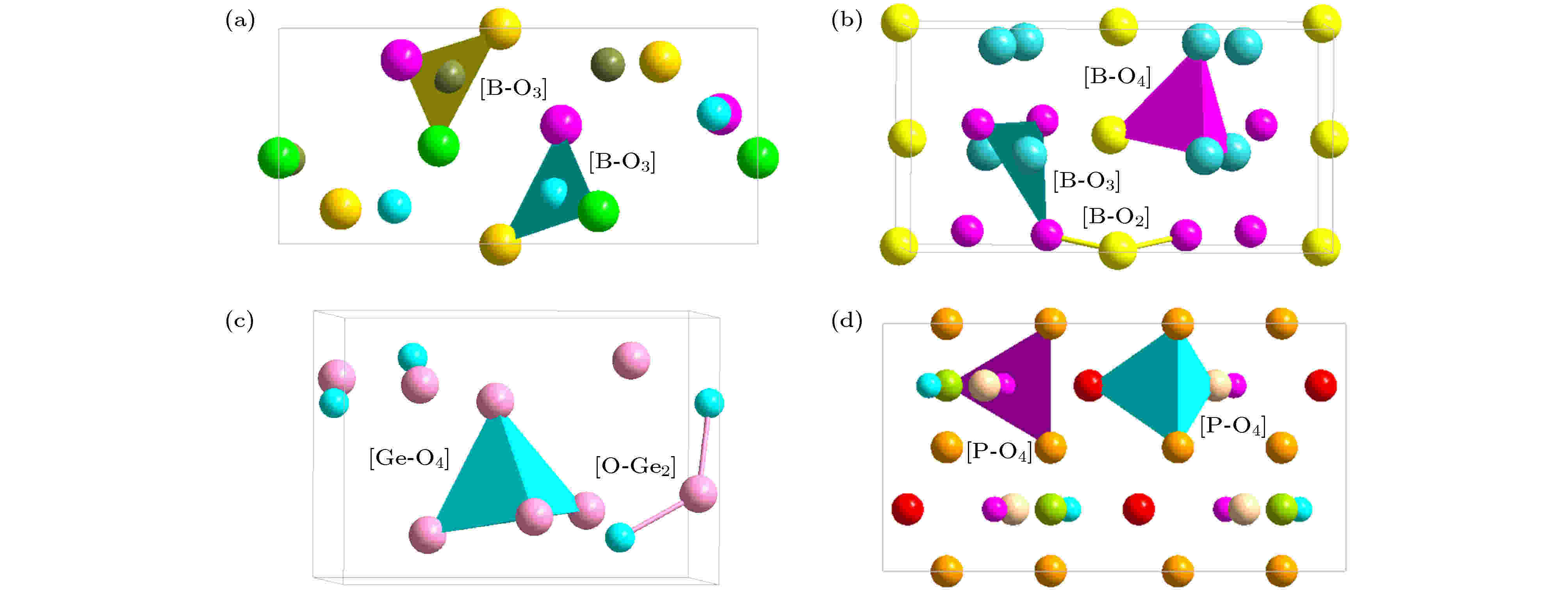 图 6 氧化物的单胞结构, 大原子为O: (a) B2O3(P31); (b) B2O3(Cmc21); (c) GeO2(P41212); (d) P2O5(Pnma)
图 6 氧化物的单胞结构, 大原子为O: (a) B2O3(P31); (b) B2O3(Cmc21); (c) GeO2(P41212); (d) P2O5(Pnma)Figure6. The cell structure of oxides, and large atoms are O: (a) B2O3(P31); (b) B2O3(Cmc21); (c) GeO2(P41212); (d) P2O5(Pnma).
B2O3中B3+有夺取游离氧形成硼氧四面体的趋势, 使结构趋向紧密, 故硼又能提高玻璃的低温黏度.下面所讨论的是常温常压下的B2O3晶体结构[20,21].
首先讨论空间群为P31的B2O3结构, B2O3单胞中有5个非等效占位为B1, B2, O1, O2, O3, 以B为心的团簇为[B-O3], 以O为心的团簇为[O-B2]. B和O的离子半径分别是0.023 nm和0.14 nm, 因此[B-O3]比[O-B2]密堆, 为主团簇(图6(a)). 由于[B-O3]的e/u为3 + 3 × 6 = 21, 不满足八电子规则, 需要1个B作为连接原子, 即类分子式是以阳离子为心的[B-O3]B, e/u = 24, 该式与常用的化学式B2O3恰好相同. 而以阴离子O为心的团簇[O-B2], 其构建的结构单元为[O-B2]O2, 形式上与前者相同.
另一个B2O3(B2O3结构), 空间群Cmc21以单胞中有3个非等效占位O1, B, O2为心确定的团簇分别为: [O-B2], [B-O4], [O-B3](图6(b)). 依据3种团簇构建的相成分式(按照原子个数比O1∶B∶O2 = 4∶8∶8 = 1∶2∶2)分别为[O-B2]O2, [B-O4/8]O, [O-B3/3]O1/2. 由此可见前者为主团簇, 构建的类分子结构单元为[O-B2]O2(e/u = 24), 恰巧与相成分式相同, 也与通常使用的化学式相同. 另外两个结构单元[B-O4]B3O2和[O-B3]O5B1均为类分子结构单元的两倍.
2
3.2.网络外体
此类氧化物处于网络之外, 不能形成玻璃, 但能改变玻璃的性质. Li2O, Na2O, K2O为玻璃中常用的碱金属氧化物, 玻璃结构中K+和Na+主要起断网的作用, Li+主要起“积聚”作用, 即能使硅氧四面体[Si-O4]聚集, 使玻璃结构趋于紧密[20,21].Li2O, Na2O, K2O都为反萤石结构, 以Li2O为代表, 空间群为

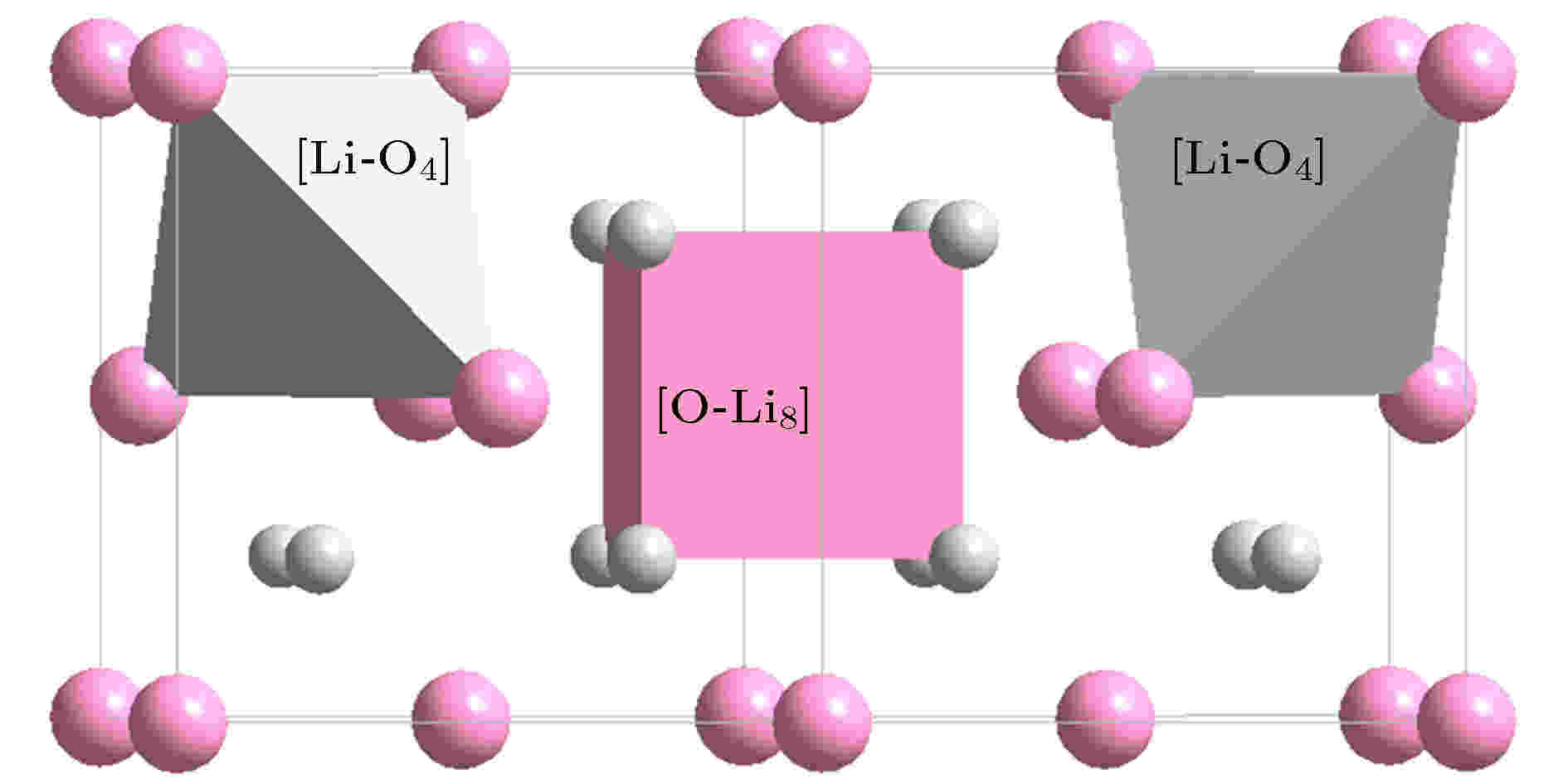 图 7 反萤石结构Li2O的团簇[Li-O4]与[O-Li8], 后者为主团簇. 大原子为O, 小原子为Li
图 7 反萤石结构Li2O的团簇[Li-O4]与[O-Li8], 后者为主团簇. 大原子为O, 小原子为LiFigure7. Clusters in anti-fluorite Li2O, [Li-O4] and [O-Li8] (principal cluster). Large spheres represent O and small spheres represent Li.
类似于碱金属, 碱土金属CaO, MgO, BaO也不能形成玻璃, 而是充当网络外体的角色, 只能以八面体填充基础四面体网络的间隙. 这几种碱土金属均为为NaCl结构, 以CaO为代表(图8).
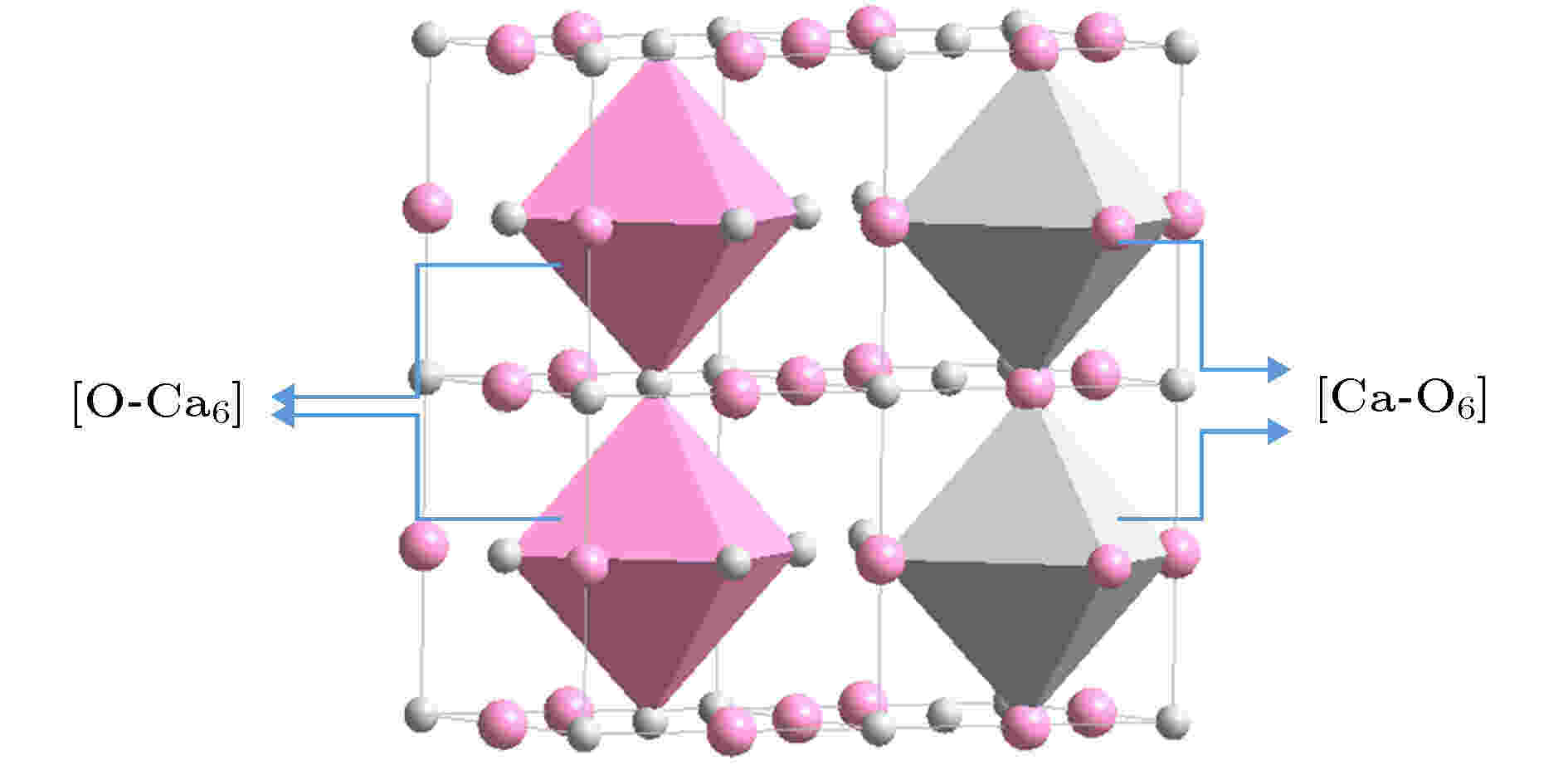 图 8 NaCl结构CaO的团簇[Ca-O6]与[O-Ca6], 前者为主团簇. 大原子为O, 小原子为Ca
图 8 NaCl结构CaO的团簇[Ca-O6]与[O-Ca6], 前者为主团簇. 大原子为O, 小原子为CaFigure8. Clusters in NaCl structure of Li2O, [Ca-O6] (principal cluster)and [O-Ca6]. Large spheres represent O and small spheres represent Li.
2
3.3.网络中间体
不能单独形成玻璃, 其作用介于网络形成体和网络外体之间. 在阳离子配位数为3和4时, 起网络形成体(补网)作用. 常见的氧化物有Al2O3, Ga2O3, Fe2O3, TiO2, BeO, ZnO等[20,21].3
3.3.1.Al2O3, Ga2O3, Fe2O3
Al2O3, Ga2O3, Fe2O3这3种氧化物具有相同的结构, 以Al2O3为例说明. 在Al2O3中, Al3+有较高的配位数6, 使氧倾向于紧密排列, 故有利于调整成为有规则排列的晶体, Al2O3有十几种晶型, 常见的有α和γ.α-Al2O3空间群为

 图 9 α-Al2O3中的团簇: 四面体[O-Al4]与八面体[Al-O6](主团簇), 小原子为Al
图 9 α-Al2O3中的团簇: 四面体[O-Al4]与八面体[Al-O6](主团簇), 小原子为AlFigure9. Clusters in α-Al2O3 unit cell, including [O-Al4] and [Al-O6] (principal cluster). Small spheres represent Al.
γ-Al2O3为Al2MgO4(尖晶石结构), 空间群为Fdm, No.227, 点阵常数a = 0.79471 nm. 对于尖晶石Al2MgO4, 单胞中有3个非等效占位: Mg, Al, O, 以它们为心的团簇有 [O-MgAl3], [Mg-O4], [Al-O6], 其中[Mg-O4]是主团簇, 类分子结构单元是阳离子Mg为心的[Mg-O4]Al2, 其中e/u = 32, 这恰巧与通常使用的化学式Al2MgO4相同. 类似地, 可以构建以Al和O为心的结构单元, 分别为[Al-O6]Al3Mg2O2和[O-MgAl3]O7AlMg. 对于氧化铝, Al占据Mg位置, 因此同时形成四面体和八面体团簇, 主团簇因此为[Al-O4] (图10), 此时相的成分式为Al3O4. 由于Al2MgO4的类分子结构单元是[Mg-O4]Al2, 满足八电子规则(e/u = 32). 据此, γ-Al3O4的类分子结构单元应该为[Al-O4]Al2, 注意到, 这个成分式Al3O4与名义成分Al2O3不一致, 而且e/u = 33, 非8的整数倍, 因此必须调整化学成分到名义相成分(是Al2O3的整数倍), 故类分子结构单元只能是[Al-O4]O2Al3, e/u = 48, 这与α型的[Al-O6]Al3在形式上一致. 再次说明, 同素异构体的类分子结构单元一般是一致的, 这里两个结构的变化只涉及到6配位的O(α型)转变为4配位(γ型), 而多余的两个O移到连接位置.
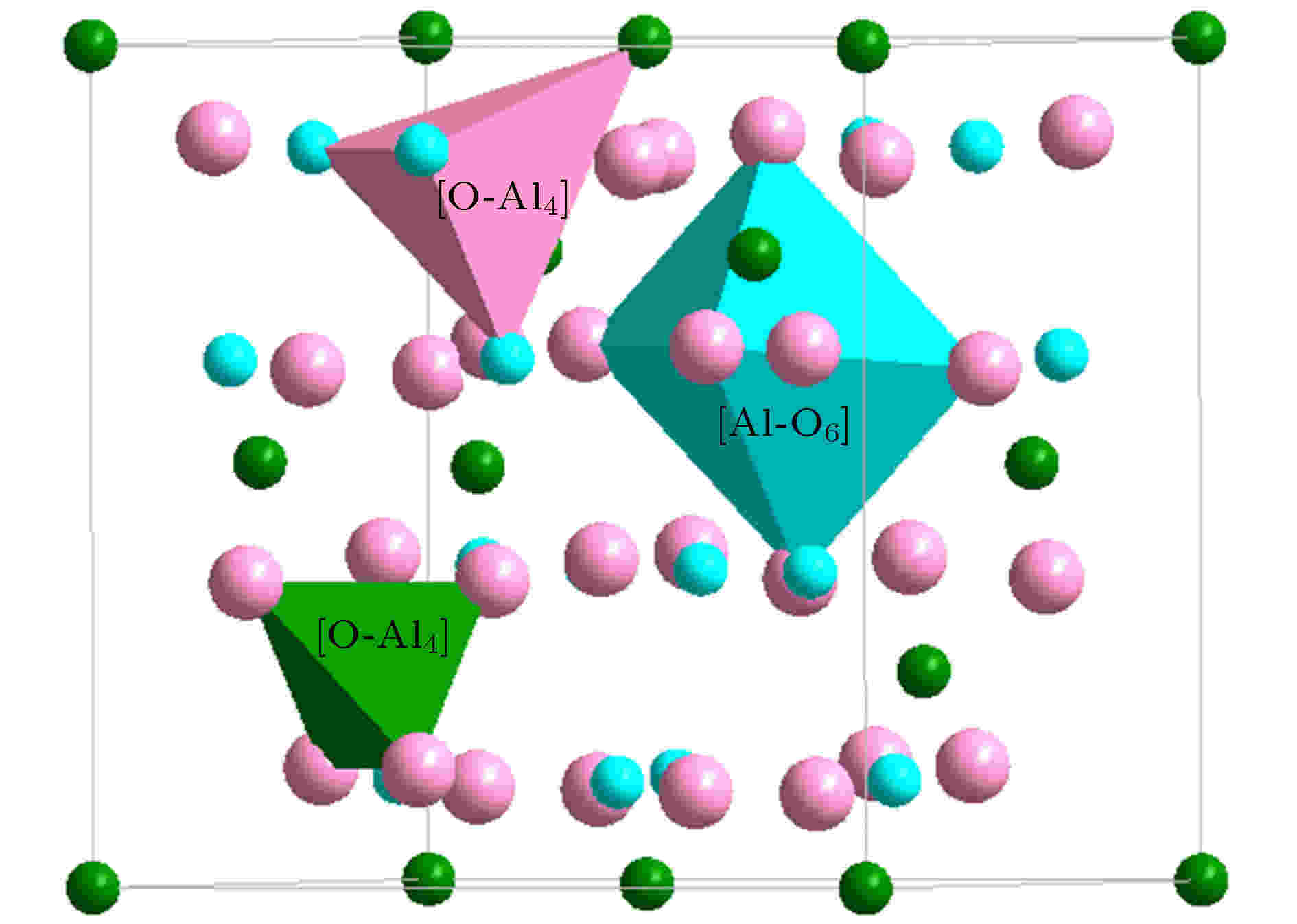 图 10 γ-Al2O3(Al2MgO4尖晶石结构)中的团簇, 含有两种四面体[O-Al4]和[Al-O4](主团簇)与一种八面体[Al-O6], 小原子为Al
图 10 γ-Al2O3(Al2MgO4尖晶石结构)中的团簇, 含有两种四面体[O-Al4]和[Al-O4](主团簇)与一种八面体[Al-O6], 小原子为AlFigure10. Clusters in γ-Al2O3 (Al2MgO4 structure), including [O-Al4], [Al-O4] (principal cluster), and [Al-O6]. Small spheres represent Al.
同时存在四面体和八面体的事实说明, Al在硅酸盐玻璃中, 虽然易于形成八面体而作为网络外体存在, 但是在一定情况下(类似于B, 在存在碱或者碱土元素时), 亦能生成四面体而直接参与网络构建.
3
3.3.2.BeO, ZnO
ZnO的结晶态有3种晶体结构[22]: 闪锌矿相(立方ZnS结构)、岩盐相(NaCl结构)、纤锌矿相(六方ZnS结构). ZnO在玻璃中一般以[Zn-O6]作为网络外体氧化物存在, 但在某些情况下也可以形成[Zn-O4]进入玻璃网络结构, 比如作为晶核剂时[23,24]. BeO与ZnO一样有闪锌矿相、岩盐相、纤锌矿相这3种相结构[25,26], 其稳定结构、在玻璃中的存在情况均与ZnO一致.闪锌矿相ZnO空间群为

 图 11 ZnO的单胞结构, 小原子为Zn (a) ZnO (
图 11 ZnO的单胞结构, 小原子为Zn (a) ZnO (
Figure11. The cell structure of ZnO, and small spheres represent Ti: (a) ZnO (

常温常压下, ZnO最稳定的构型是六方纤锌矿结构[21], 即六方ZnS结构, 空间群P63mc, 点阵常数a = 0.32494 nm, c = 0.5203814 nm. ZnO(ZnS相)晶胞中有两个非等效占位Zn和O, 以它们为心的团簇是四面体的[Zn-O4]和[O-Zn4] (图11(b)), 其中[Zn-O4]为主团簇, 构建的类分子式为[Zn-O4]Zn3, e/u = 32, 该式是通用化学式的4倍.以阴离子O为心得到的结构单元形式及连接原子个数均与其完全相同, 为[O-Zn4]O3.
ZnO(NaCl结构, 空间群

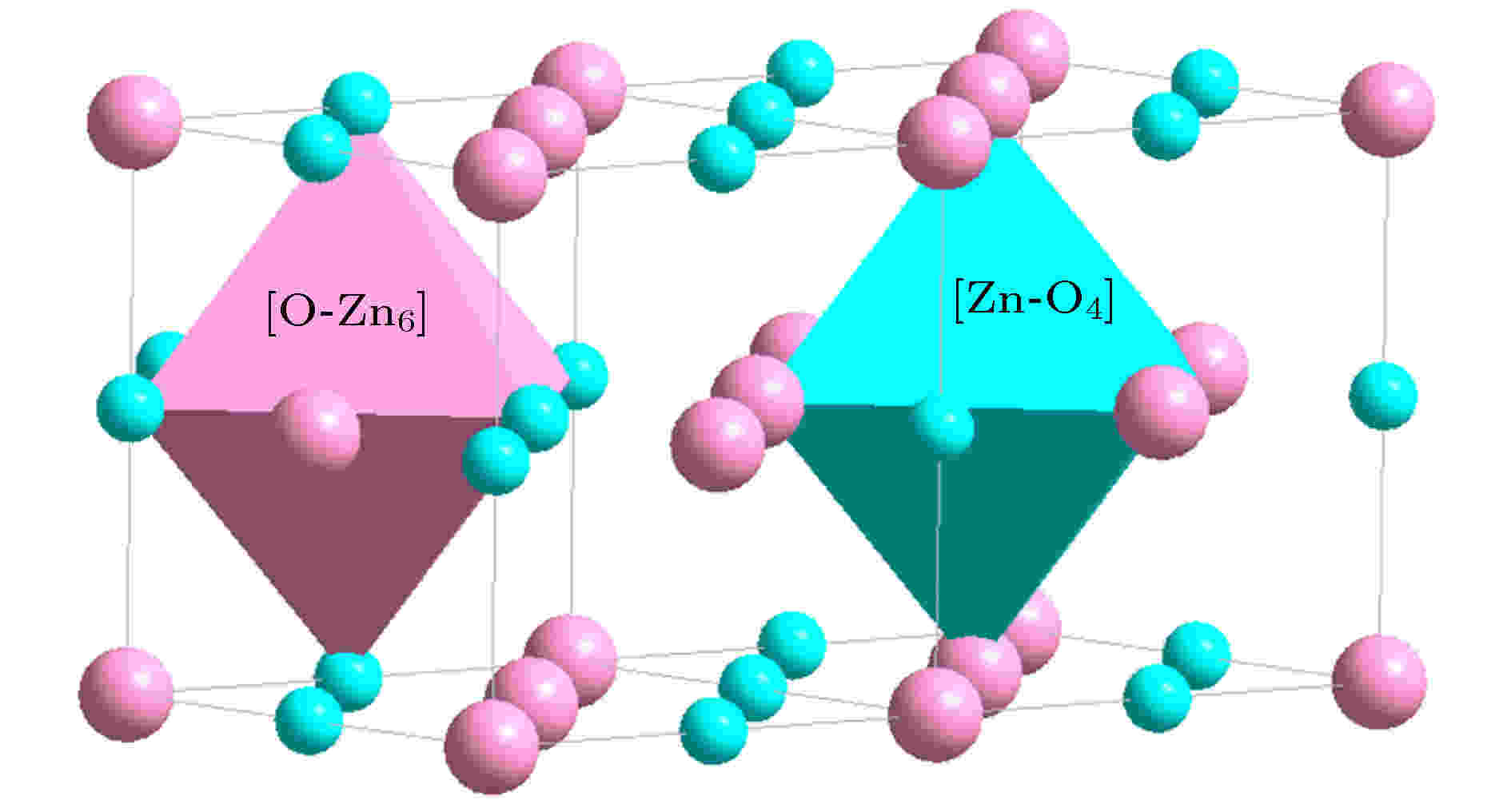 图 12 ZnO(NaCl结构)中的八面体团簇[Zn-O6]与[O-Zn6], 前者为主团簇. 小原子为Zn
图 12 ZnO(NaCl结构)中的八面体团簇[Zn-O6]与[O-Zn6], 前者为主团簇. 小原子为ZnFigure12. Octahedral clusters [Zn-O6] (principal cluster) and [O-Zn6] in ZnO (NaCl structure). Small spheres represent Zn.
可见, 化合物BeO和ZnO同时能形成四面体和八面体, 因此能够同时进入四面体网络和以八面体填充间隙, 属于中间体.
3
3.3.3.TiO2
TiO2晶体主要以3种形式存在自然界中, 分别是金红石、锐钛矿及板钛矿, 其中金红石型相结构是TiO2中最常见的晶体形式, 也是热力学最稳定的晶体形式. 金红石相结构的TiO2(P42/mnm, No.136, 图13(a)), 八面体[Ti-O6]为主团簇, 相应的类分子式为[Ti-O6]Ti2, e/u = 48, 该式是通用化学式的3倍. 而以O为心的结构单元表述为[O-Ti3]O5, e/u = 48, 形式和连接原子个数与前者均相同.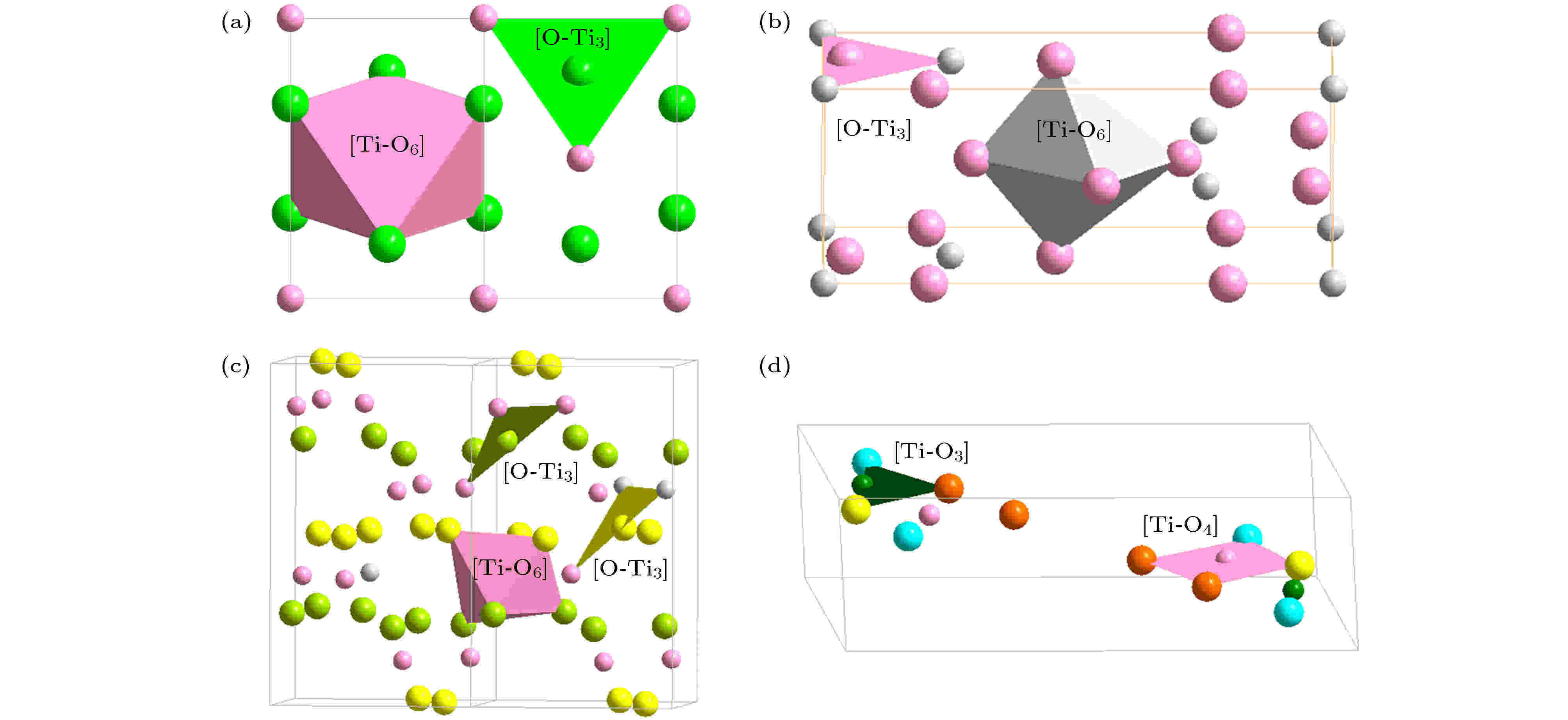 图 13 TiO2的单胞结构, 小原子为Ti (a) TiO2(P42/mnm); (b) TiO2(I41/amd); (c) TiO2( Pbca); (d) TiO2 (P21/m)
图 13 TiO2的单胞结构, 小原子为Ti (a) TiO2(P42/mnm); (b) TiO2(I41/amd); (c) TiO2( Pbca); (d) TiO2 (P21/m)Figure13. The cell structure of TiO2, and small spheres represent are Ti: (a) TiO2(P42/mnm); (b) TiO2(I41/amd); (c) TiO2( Pbca); (d) TiO2 (P21/m)
锐钛矿相的空间群为I41/amd, No.141, 点阵常数a = 0.37851 nm, c = 0.95146 nm. 有两个非等效位点: Ti, O为心的团簇分别为 [Ti-O6], [O-Ti3] (图13(b)). 与金红石相的一样, 八面体[Ti-O6]为此相的主团簇, 类分子结构单元为[Ti-O6]Ti2, e/u = 48, 该式是通用化学式的3倍.
板钛矿相空间群为Pbca, No.61, 点阵常数a = 0.9166 nm, b = 0.5436, c = 0.5135 nm. 有3个非等效位点: O1, O2, Ti. 以Ti为心的团簇为 [Ti-O6], 以O1和O2为心的团簇均为[O-Ti3] (图13(c)). 和前面两种结构一样, [Ti-O6]为此相的主团簇, 类分子结构单元为[Ti-O6]Ti2, e/u = 48, 该式是通用化学式的3倍. 以O1和O2为心的相团簇式为[O-Ti3]O5, e/u = 48.
TiO2还有一种异构体(表2), 空间群为P21/m, No.11, 点阵常数a = 1.2178710 nm, b = 0.374122, c = 0.652495 nm. 有6个非等效位点: O1, O2, O3, O4, Ti1, Ti2. 以Ti1和Ti2为心的团簇分别为四边形[Ti-O4]和三角形[Ti-O3] (图13(d)), 完全独立, 但由密堆性可知应选[Ti-O4]为主团簇. 其相应的相成分式[Ti-O4]Ti和[Ti-O3]TiO, 即所构建的类分子结构单元为[Ti-O4]Ti和[Ti-O3]TiO, e/u = 32, 该式是通用化学式的2倍. 以O1, O2, O3为心的团簇均为[O-Ti2], 构建的结构单元为[O-Ti2]O3, 以O4为心的团簇为[O-Ti1]O3Ti.
TiO2结构以[Ti-O6]八面体团簇为主要特征, 因此一般置于网络之外, 填充四面体网络的间隙; 但是, 正如空间群P21/m, No.11的结构所示, 该结构也能呈现[Ti-O4]四边形和类似于B2O3的三角形网络, 从而参与硅酸盐的基础四面体网络的构建, 因此属于中间体.
玻璃中氧化物类分子结构单元概念的提出, 将为后续玻璃成分设计的研究工作打下基础. 实际的玻璃中包含多种氧化物组元, 研究其结构模型不仅涉及氧化物本身, 更需要建立各种结构单元的连接方式, 我们将在下一步的工作中逐步确定.
