0 引言
【研究意义】 中国是甜瓜生产大国,近年来种植面积的不断扩大,甜瓜细菌性叶斑病有发展蔓延的趋势[1-3]。有研究报道,在某些特定产区,甜瓜细菌性叶斑病的发病率在30%以上,严重时达到100%,致使甜瓜大幅减产[4-5]。建立快速、灵敏、便捷的甜瓜细菌性叶斑病菌检测体系用以检测甜瓜种子,能够有效防止甜瓜细菌性叶斑病的发生和传播。【前人研究进展】SZEMES等[6]运用Padlock探针结合Microarray技术对10种重要的植物病原菌进行了检测并对这种技术成功地进行了优化,结果表明这是一种灵敏度、特异性很好,效率很高的高通量检测技术;田艳丽等对水稻白叶枯病菌(Xanthomomas oryzae pv. oryzae)、瓜类细菌性果斑病菌(Acidovorax citrulli)等病原菌设计了Padlock探针,并且成功地将其运用于实际样品检测,其中在瓜类细菌性果斑病菌上设计Padlock探针能将其成功与燕麦褐条病菌(Acidovorax avenae)区分开,并且这两种病原菌所选的特异性序列只有一个碱基的差异[7-8];王辉等[9]运用斑点杂交技术鉴定了4种支原体即人型支原体(MH)、生殖支原体(MG)、解脲脲原体(UU)和微小脲原体(UP),能够同时进行多种病原菌的检测,提高了临床检测的效率;黄冠军[10]建立了柑橘溃疡病菌(Xanthomonas axonopodis pv. citri)锁式探针检测技术,此方法特异性很强、灵敏度很高、重复性高;王念武等[11]建立了番茄溃疡病菌(Clavibacter michiganensis subsp. michiganensis)基于锁式探针技术的实时荧光PCR快速检测方法,并用该方法对来自日本、韩国等的45份样本进行了分析检测。此检测方法高于常规PCR两个数量级,成功地从45份样品中检测到5份样品带有番茄溃疡病菌;陈艳鸿等[12]建立了锁式探针结合正向斑点杂交技术对地毯草黄单胞菌大豆致病变种(Xanthomonas axonopodis pv. glycines)检测体系,建立的体系能够对大豆细菌性斑疹病菌特异性识别,检测灵敏度达到100 fg·μL-1;李志锋等[13]对菜豆晕疫病菌(Pseudomonas savastanoi pv. phaseolicola)建立了锁式探针体系,与传统PCR相比灵敏度高出了10倍;王婷[14]以番茄上危害较大的番茄细菌性溃疡病菌(Clavibacter michiganensis subsp. michiganensis)、番茄细菌性斑点病菌(Pseudomonas syringae pv. tomato)和番茄青枯病菌(Ralstonia solanacearum)为研究对象,分别建立了基于锁式探针的反向斑点杂交技术体系,检测体系能够特异性的识别目标菌株,实现对靶标序列的特异性检测;蔡俊等[15]建立的基于小麦矮腥黑穗病菌(Tilletia controversa)超分支滚环扩增检测体系,能够专一地检测出小麦矮腥黑穗病菌,完全将其与近缘种分开,同样灵敏度高于常规PCR 10倍。【本研究切入点】目前主要用普通PCR对甜瓜细菌性叶斑病进行检测,而普通PCR容易出现假阳性等问题,锁式探针能够避免常规的PCR等检测方法易受检测样品中杂质干扰以及假阳性的现象。迄今为止,尚未见锁式探针技术检测甜瓜细菌性叶斑病的相关报道。【拟解决的关键问题】以甜瓜细菌性叶斑病菌为研究对象,寻找特异性核苷酸片段,设计Padlock探针。建立甜瓜细菌性叶斑病菌Padlock探针结合斑点杂交的高通量检测体系,为甜瓜细菌性叶斑病快速检测提供技术支持。1 材料与方法
试验于2012年7月至2014年4月在南京农业大学完成。1.1 试验材料与仪器
共选用51株参试菌株,包括26株丁香假单胞杆菌流泪病致病变种甜瓜菌株、12株丁香假单胞杆菌流泪病致病变种黄瓜菌株及13株其他参试菌株(表1)。Table 1
表1
表1供试菌株
Table 1Bacterial strains used in this study
| 编号 Number | 菌株 Strain | 宿主 Host | 来源 Source |
|---|---|---|---|
| 丁香假单胞杆菌流泪病致病变种甜瓜菌株 P. syringae pv. lachrymans strains from muskmelon | |||
| 1 | 361 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 2 | 362 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 3 | 363 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 4 | 364 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 5 | 371 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 6 | 372 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 7 | 373 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 8 | 374 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 9 | 381 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 10 | 382 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 11 | 383 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 12 | 384 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 13 | 401 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 14 | 402 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 15 | 403 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 16 | 404 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 17 | 451 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 18 | 491 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 续表1 Continued table 1 | |||
| 编号 Number | 菌株 Strain | 宿主 Host | 来源 Source |
| 19 | 492 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 20 | 493 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 21 | 501 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 22 | 502 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 23 | 503 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 24 | 504 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 25 | njl16 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 26 | njl18 | 甜瓜 Muskmelon | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 丁香假单胞杆菌流泪病致病变种黄瓜菌株 P. syringae pv. lachrymans strains from cucumber | |||
| 27 | NCPPB277 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 28 | NCPPB467 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 29 | NCPB540 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 30 | NCPPB541 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 31 | NCPPB542 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 32 | NCPPB543 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 33 | NCPPB1425 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 34 | NCPPB1428 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 35 | NCPPB1096 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 36 | NCPPB1097 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 37 | Jiifen1 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 38 | Jiifen2 | 黄瓜 Cucumber | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 39 | 麦叶褐斑病菌 Pseudomonas syringae pv. atropurpurea NCPPB1328 | 未知 Unknown | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 40 | 桃树细菌性溃疡病菌 P. syringae pv. persicae NCPPB2254 | 桃 Peach | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 41 | 丁香假单胞菌斑点致病变种 P. syringae pv. maculicola ATCC51320 | 未知 Unknown | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 42 | 大豆细菌性斑点病菌 P. syringae pv. glycinea ATCC8727 | 未知 Unknown | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
| 43 | 烟草野火病菌 P. syringae pv. tabaci ATCC11527 | 未知 Unknown | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 44 | 丁香假单胞菌 P. syringae NCPPB4276 | 未知 Unknown | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 45 | 豌豆细菌性枯萎病菌 P. syringae pv. pisi ATCC11043 | 豌豆 Pea | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 46 | 番茄细菌性斑点病菌 P. syringae pv. tomato DC3000 | 番茄 Tomato | 中国检验检疫科学研究院 China Academy of Inspection and Quarantine |
| 47 | 瓜类细菌性果斑病菌 Acidovorax citrulli ATCC29625 | 哈密瓜 Cantaloupe | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
| 48 | 甜菜细菌疫病假单胞菌 P. syringae pv. aptata | 未知 Unknown | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
| 49 | 丁香假单胞菌丁香致病变种 P. syringae pv. syringae | 未知 Unknown | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
| 50 | 铜绿假单胞菌 Pseudomonas vifidiflava | 未知 Unknown | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
| 51 | 荧光假单胞菌 Pseudomonas fluorescens | 未知 Unknown | 南京农业大学,胡白石 Hu BaiShi, Nanjing Agricultural University |
新窗口打开
清JS-780全自动凝胶成像分析系统(上海培清科技有限公司);Eppendorf Mastercycler pro384梯度PCR扩增仪(德国艾本德股份公司);VP HL-2000紫外交联仪(美国思伯明科学器材有限公司);Y-8C双稳定时电泳仪(北京六一仪器厂)。10×UDG缓冲液、Taq DNA连接酶购自New England Biolabs(英国);dNTP、MgCl2、核酸外切酶Ⅲ、核酸外切酶Ⅰ、10×Taq聚合酶Buffer、Taq聚合酶购自大连宝生物公司;细菌基因组DNA制备试剂盒购自爱思进生物技术有限公司(杭州);Nylon-N+尼龙膜购自Amersham(英国);地高辛标记检测试剂盒购自罗氏公司(德国)。
1.2 靶标基因选取及锁式探针设计
将GAPDH作为靶标基因,用Bioedit软件将所有参试菌株的GAPDH基因序列比对,选取甜瓜细菌性叶斑病基因序列的特异部分为Padlock探针T2端,靠近T2端的作为T1端。然后将设计的Padlock探针与GenBank登录的所有细菌序列比较以确保Padlock探针的特异性。甜瓜细菌性叶斑病菌探针由生工生物技术公司(上海)合成(表2)。Table 2
表2
表2试验所用锁式探针序列
Table 2Padlock probes sequence used in this study
| 名称 Name | 序列 Sequence (5′-3′) |
|---|---|
| PLP | GATCAATGGAATGCTCATTTCTAAGCTCTCGACCGTTAGCAGCATGACCGAGATGTACCGCTATCGTTGCACTGCCGTCATTAGCGTTCAAGCACTGATCGTCAA |
| cZipcode | ACGCTAATGACGGCAGTGCA |
新窗口打开
1.3 核酸提取
所有参试菌株活化后,用Axygen的细菌基因组DNA制备试剂盒(爱思进生物技术(杭州)有限公司)分别提取参试菌株的DNA,操作参照产品说明书。1.4 锁式探针连接、酶切和扩增反应
锁式探针连接反应:1 μL Padlock探针(2 μmol·L-1),1 μL 10×Taq DNA连接酶Buffer,0.4 μL Taq DNA连接酶(40 U·μL-1),6.6 μL灭菌去离子水,2 μL待测模板DNA。反应程序:预变性96℃ 7 min;96℃变性30 s,68℃连接40 s,67℃退火4 min,共30个循环;最后96℃灭活5 min。锁式探针酶切反应:连接反应后的产物管中加入0.5 U Exonuclease I,0.5 U Exonuclease III(TaKaRa Biotechnology Dalian China),1 μL 10×Exonuclease I Buffer [500 mmol·L-1 Tris-HCl(pH 8.0),50 mmol·L-1 MgCl2, 10 mmol·L-1 DTT]和11 μL 10×Exonuclease III Buffer [670 mmol·L-1 Tris-HCl(pH 8.0),67 mmol·L-1 MgCl2, 10 mmol·L-1 DTT]。反应程序:37℃反应1 h,然后将反应后的产物95℃灭活30 min。
锁式探针扩增反应:1.5 µL MgCl2(25 mmol·L-1),2.0 μL dNTP(2.5 mmol·L-1 each),2.5 µL 10×Taq聚合酶Buffer,0.2 μL Taq DNA聚合酶,2.5 μL Uracil- DNA Glycosylase,1 µL 10×Uracil-DNA Glycosylase Buffer,通用引物各2 μL(2 µmol·L-1),加入2 μL酶切产物作为扩增反应模板,无菌水补足到25 μL。通用引物序列:P1-f19(5′-CGAGATGTACCGCTA TCGT-3′)、P2-r20(5′-TCATGCTGCTAACGGTCG AG-3′)。
1.5 锁式探针与斑点杂交结合的高通量检测技术
(1)探针制备取zipcode反向互补序列20 μL,加入Roche DIG杂交试剂盒中的1号4 μL,充分混匀,放置于37℃温育22—24 h。70℃水浴中终止反应10 min,保存于-20℃冰箱;(2)点样中和及紫外交联将PCR产物于沸水浴中10 min中后迅速放置于冰盒中,取2 μL点于尼龙膜上。在干净的玻璃上放置一张比膜稍大的滤纸并用中和液浸湿,将点样后的尼龙膜置于上面静置4 min。然后放于自然空气干燥30 min,置于紫外交联仪上交联5 min。将固定好的杂交膜置于10×SSC溶液中浸润平衡5 min;(3)将10 mL预杂交液倒入杂交管中,按55℃杂交温度预热15 min。将浸润平衡好的尼龙膜放入预热的杂交管中,55℃预杂交1 h;(4)取出杂交膜置于另一杂交管中,加入5 mL含有探针的新鲜杂交液,55℃杂交过夜;(5)用100 mL洗脱液A于68℃杂交炉中洗涤30 min,然后用洗脱液B于68℃杂交炉中洗膜两次,每次15 min。然后用Washing Buffer(50 mL马来酸加入150 µL吐温-20)于室温下轻摇洗脱5 min;(6)将尼龙膜转置于1×Blocking Buffer静置30 min,接着放于Antibody solution中静置40 min,Washing Buffer每次洗脱15 min,洗脱2次,尼龙膜置于30 mL Detection Buffer中平衡5 min,最后置于15 mL现配的Color substrate中避光显色1—8 h。尼龙膜出现明显清晰的条带后,用无菌水浸泡10 min终止反应。1.6 锁式探针特异性检测
根据上述试验过程,用锁式探针对51株参试菌株(表1)进行检测,探针的特异性通过PCR扩增结果(反应体系和反应程序同1.4)和斑点杂交结果(反应体系和反应程序同1.5)来判定。1.7 锁式探针灵敏度检测
甜瓜细菌性叶斑病的DNA依次稀释为1 ng·μL-1、100 pg·μL-1、10 pg·μL-1、1 pg·μL-1、100 fg·μL-1、10 fg·μL-1和1 fg·μL-1 7个梯度,运用锁式探针将7个梯度分别作为模板扩增(反应体系和反应程序同1.4)及斑点杂交(反应体系和反应程序同1.5),根据扩增和斑点杂交结果判定探针的灵敏度。1.8 人工模拟种子带菌检测
取约200颗健康的甜瓜种子浸泡于甜瓜细菌性叶斑病菌悬液中4 h,将种子自然风干,风干后的带菌甜瓜种子和健康甜瓜种子按0/1 000、1/1 000、10/1 000、50/1 000和100/1 000混合。浸泡于200 mL无菌水中,振荡4 h后抽取浸提液,提取DNA作为目标模板进行斑点杂交。1.9 市售种子检测
对市售的205份甜瓜种子进行检测。分别将待测种子加入一定量的无菌水浸泡4 h,将浸出液取出离心后提取DNA,然后用对应的探针对提取的DNA进行检测。2 结果
2.1 锁式探针特异性测定
用设计的锁式探针对51株参试菌株进行试 验。26株目标菌株反应结果为阳性,均扩增到一条105 bp的特异性目的条带。而剩余25株参试菌株及空白对照均无扩增产物产生(图1)。说明此研究设计的锁式探针对甜瓜细菌性叶斑病有较好的特异性。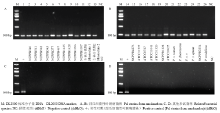 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图1锁式探针特异性
-->Fig. 1Specificity amplification of Padlock probe
-->
2.2 锁式探针灵敏度测定
将DNA浓度为1 ng·μL-1左右的目的菌株按10倍梯度稀释,依次稀释为1 ng·μL-1、100 pg·μL-1、10 pg·μL-1、1 pg·μL-1、100 fg·μL-1、10 fg·μL-1和1 fg·μL-1作为模板,共7个梯度。由图2可以看出,连接体系中加入1 pg目的DNA基因组,都能扩增出105 bp的目的片段。探针的检测灵敏度为1 pg·μL-1。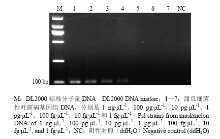 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图2锁式探针灵敏度
-->Fig. 2Sensitivity of Padlock probe
-->
2.3 锁式探针结合斑点杂交特异性检测
取4 μL锁式探针扩增产物(2.1部分)点在尼龙膜上进行斑点杂交测定。26株甜瓜细菌性叶斑病病菌杂交后出现了显色反应,而非目的菌株杂交后无颜色反应(图3)。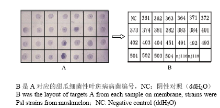 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图3锁式探针结合斑点杂交特异性
-->Fig. 3The specificity of dot-blot hybridization combined with Padlock probe
-->
2.4 锁式探针结合斑点杂交灵敏度检测
将4 μL锁式探针扩增产物(上述2.2)点在尼龙膜上进行斑点杂交测定。同样灵敏度也能达到1 pg·μL-1(图4)。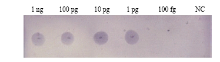 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图4锁式探针结合斑点杂交灵敏度
-->Fig. 4Sensitivity of dot-blot hybridization combined with Padlock probe
-->
2.5 锁式探针结合斑点杂进行人工模拟种子带菌检测
模拟种子带菌检测率达到0.1%(1/1 000)(图5),能将1粒带菌种子从1 000粒健康的种子检测出来。 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图5锁式探针结合斑点杂进行人工模拟种子带菌检测
-->Fig. 5Detection of artificially infested seeds by dot-blot hybridization combined with Padlock probe
-->
2.6 锁式探针结合斑点杂交对市售疑似带有甜瓜细菌性叶斑病的甜瓜种子检测
运用锁式探针结合斑点杂交对市售疑似带有甜瓜细菌性叶斑病的甜瓜种子检测,从205份市售甜瓜种子中检测到7份甜瓜种子带菌。由图6中可以看出1、12、55、58、104、110和111号种子带有甜瓜细菌性叶斑病。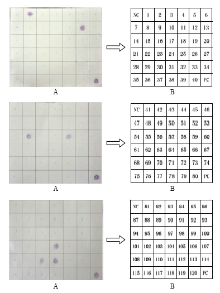 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图6锁式探针结合斑点杂交对市售甜瓜种子的检测
-->Fig. 6Detection of commercially available sweet melon seeds by dot-blot hybridization combined with Padlock probe
-->
3 讨论
甜瓜细菌性叶斑病的检测方法有多种,主要有免疫检测技术和常规分子生物学检测方法,但是这些检测方法均存在不足之处。凝集试验拥有能够定性、操作简便、检测周期短等特点,但灵敏度不高。目前植物细菌性病害诊断应用较广免疫学方法是酶标抗体技术-酶联免疫吸附法(ELISA)。ELISA能用于定性分析检测和定量分析检测[16],由于ELISA自身反应过程较为复杂,使得ELISA灵敏度和特异性较低,容易出现假阳性和假阴性[17]。流动注射免疫检测和胶体金标记免疫层析检测法是两种新型的免疫检测技术[18],也都存在一定的缺陷,流动注射免疫检测不能实现大批量的样品分析[19],胶体金标记免疫层析检测法稳定性和灵敏度不高[20]。基因芯片技术能够实现一次分析检测大量样品和高通量的特点,但其重复性有待提高[21-22]。巢式PCR是运用两对引物进行扩增容易引起交叉污染[23]。多重PCR具有检测费用低和操作简单等特点,但其要求多对引物同时加入同一PCR体系中,引物的竞争性扩增和引物间的配对影响,从而影响其扩增效果[24]。荧光定量PCR具有定量准确、安全快速和准确灵敏等优点,但它能与非特异性的双链DNA结合造成假阳性结果[25]。锁式探针是一条长的寡聚核苷酸链,长度为100 bp左右[26],探针两端(磷酸化的5′端和羟基化的3′端)能与目的片段进行特异性结合[27]。探针两端称为T1端和T2端,锁式探针两端有很强的特异性,能够检测单碱基突变[28-29]。锁式探针设计的前期是找到一条特异性的序列,得到特异性序列后并不能简单的得到一条特异性探针。特异性探针的设计是一个大量筛选和反复验证的过程,T1端和T2端的位置、长度、GC含量等都要经过反复考量,多次试验后才有可能得到一条特异性强和灵敏度高的Padlock探针。
将锁式探针结合斑点杂交技术能够实现甜瓜细菌性叶斑病菌高通量检测。此方法避免了常规的PCR等检测方法易受检测样品中杂质干扰、以及假阳性的现象。
4 结论
以甘油醛-3-磷酸脱氢酶(glyceraldehyde-3- phosphate dehydrogenase,GAPDH)基因为靶标基因,设计了能特异性识别甜瓜细菌性叶斑病的锁式探针,并且将锁式探针与斑点杂交技术相结合建立了甜瓜细菌性叶斑病的高通量检测体系,将反应过程进行了优化,该体系灵敏度达到1 pg·μL-1。该方法适用于甜瓜细菌性叶斑病菌的检测,对防止该病的蔓延传播有实际应用价值。The authors have declared that no competing interests exist.
