 ,中国农业科学院郑州果树研究所/国家瓜果改良中心,郑州 450009
,中国农业科学院郑州果树研究所/国家瓜果改良中心,郑州 450009Chemical Compositions and Gene Mapping of Wax Powder on Watermelon Fruit Epidermis
GONG ChengSheng, ZHAO ShengJie, LU XuQiang, HE Nan, ZHU HongJu, DOU JunLing, YUAN PingLi, LI BingBing, LIU WenGe ,Zhengzhou Fruit Research Institute, Chinese Academy of Agricultural Sciences/National Cucurbits and Fruits Improvement Center, Zhengzhou 450009
,Zhengzhou Fruit Research Institute, Chinese Academy of Agricultural Sciences/National Cucurbits and Fruits Improvement Center, Zhengzhou 450009通讯作者:
收稿日期:2018-10-28接受日期:2018-02-17网络出版日期:2019-05-01
| 基金资助: |
Received:2018-10-28Accepted:2018-02-17Online:2019-05-01
作者简介 About authors
龚成胜,E-mail:

摘要
关键词:
Abstract
Keywords:
PDF (4734KB)元数据多维度评价相关文章导出EndNote|Ris|Bibtex收藏本文
本文引用格式
龚成胜, 赵胜杰, 路绪强, 何楠, 朱红菊, 豆峻岭, 袁平丽, 李兵兵, 刘文革. 西瓜果实表皮蜡粉的化学成分与基因定位[J]. 中国农业科学, 2019, 52(9): 1587-1600 doi:10.3864/j.issn.0578-1752.2019.09.010
GONG ChengSheng, ZHAO ShengJie, LU XuQiang, HE Nan, ZHU HongJu, DOU JunLing, YUAN PingLi, LI BingBing, LIU WenGe.
0 引言
【研究意义】西瓜(Citrullus lanatus)属于葫芦科西瓜属,是重要的瓜果类作物,在世界范围内广泛种植。我国是世界上最大的西瓜生产和消费大国,西瓜在我国果蔬生产和周年供应中占据重要地位,据统计,2016年我国西瓜播种面积已增至1.89×106 hm2,总产量达7 940万t[1,2]。植物蜡粉又称蜡质、蜡被,它是存于植物组织表面的疏水性晶体结构物质,在农作物生长发育过程中,表皮蜡质能够有效地保护植株,进而提高农作物的质量、产量和抗性。附着于西瓜果实表皮白色粉末状物质即为蜡粉,目前,用于生产销售的西瓜主栽培品种果实表皮大多有蜡粉附着,然而尚没有对西瓜蜡粉性状的系统研究。对西瓜果实表皮蜡粉的研究有助于阐明性状的抗性机制,同时可以为新品种选育和遗传机理研究奠定理论基础,因此本研究的开展具有重要意义。【前人研究进展】蜡粉一般为灰绿、灰白霜状,广泛分布于玉米、葡萄、甘蓝、黄瓜、西瓜等多种植物中,它存在于不同植物叶、茎、嫩枝、果实等不同组织部位,而目前对它的研究多集中在叶片上,植物果实表皮蜡粉的研究相对较少。研究发现,蜡粉在植物生长发育过程中起到重要的保护作用,它能够减少水分蒸发和外部水分进入植物组织、减缓高温胁迫[3,4]、减少紫外线损伤[5],同时还具有抵抗部分病虫侵害的作用[6]。蜡粉的形态和化学成分变异丰富,常见的蜡粉形态结构有柱状、棒状、树枝状和板状[7]等;蜡粉的主要组成成分为特长链脂肪酸及其衍生物,可能还存在一些萜类等成分。在蜡粉组分合成时,脂肪酸延伸酶复合体(FAE)催化特长链脂肪酸(VLCFAs)C16、C18的形成,然后通过醇合成途径合成初级醇和烷基酯,或者通过烷烃合成途径合成烷烃、次级醇、酮和醛[8,9]等物质。目前,关于植物蜡粉的遗传规律已有较多的报道,刘东明等[10]以叶片无蜡粉亮绿油菜LD10和叶片有蜡粉甘蓝21-3为双亲构建六世代群体,遗传分析表明蜡粉为单基因控制显性性状;张曦等[11]以大白菜花茎有蜡粉的材料‘08A161’为母本,无蜡粉的材料‘08A235-2’为父本构建了六世代群体,遗传分析表明花茎蜡粉为核基因控制,有蜡粉对无蜡粉表现为完全显性。近年来,植物蜡粉合成的相关基因被不断的挖掘,如拟南芥中的FAE1编码的蛋白特异催化C20、C22脂肪酸的合成[12],CER10编码的烯酰CoA还原酶(ECR)是合成长链脂肪酸所必需[13],CER4编码的脂酰CoA还原酶(FAR)负责催化表皮初级醇的合成[14],CER3则被认为和醛类物质合成有关[15]。相关蜡质生成的基因也在玉米、水稻等多种作物中被克隆。【本研究切入点】迄今,对植物蜡粉的生理生化作用以及遗传机制研究不断深入,但西瓜果实表皮蜡粉结构、化学成分还不清楚,对性状的遗传分析和基因定位工作也未见报道。【拟解决的关键问题】本试验以无蜡粉的西瓜自交系‘FH’和有致密蜡粉层附着的西瓜自交系‘美佳选黑’为双亲构建六世代群体,通过双亲果实表皮结构观察、蜡粉化学成分测定、群体遗传分析以及基因定位工作的开展,为新品种选育提供理论支撑,同时为今后进一步进行精细定位和分子标记辅助育种奠定工作基础。1 材料与方法
1.1 试验材料
试验选用‘美佳选黑’和‘FH’为供试材料,这两份材料均为中国农业科学院郑州果树研究所多倍体西瓜育种课题组选育的高代自交系。‘美佳选黑’果实椭圆形,果实底色墨绿,表皮光滑,无蜡粉层附着(图1-A);‘FH’果实高圆型,果实底色墨绿,表皮有灰白色蜡粉层附着(图1-B)。将‘美佳选黑’和‘FH’分别作为母本P1和父本P2,通过人工授粉杂交的方式获得F1群体,F1自交获得F2群体,F1与P1、P2杂交分别获得BC1P2、BC1P2群体。供试材料于2018年种植于中国农业科学院新乡综合实验基地大棚,育苗移栽,行间距1.5 m,株间距0.8 m,地膜覆盖,单蔓整枝,第二雌花自交授粉留瓜,西瓜雌、雄花于开花前1 d下午进行套帽,在次日10:00前进行人工授粉,田间施肥、灌溉等栽培管理措施一致。图1
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图1成熟西瓜果实表皮形态比较
A:无蜡粉西瓜品种‘美佳选黑’;B:有蜡粉西瓜品种‘FH’
Fig. 1The morphology comparison of ripe watermelon fruit epidermis
A: In glossy watermelon inbred line ‘Meijiaxuanhei’; B: In waxy watermelon inbred line ‘FH’
1.2 试验方法
1.2.1 西瓜果实表皮蜡粉的结构观察 供试材料‘美佳选黑’和‘FH’果实生长至成熟期时,用单面美工刀片分别在两份材料外果皮中部相同位置处取大小为1 cm×0.5 cm×0.3 cm的长方体样品,注意不要触碰果皮,以保证蜡粉的完整性,每个样本设置3次重复。然后通过以下5个步骤处理样品。第一步:化学固定。所取样品立即用pH 7.2的2.5%戊二醛进行固定。第二步:清洗。磷酸缓冲盐溶液(PBS)清洗3次,每次清洗15 min。第三步:脱水。依次用质量分数为50%、75%、85%、95%、100%、100%的乙醇溶液各清洗20 min。第四步:干燥。在临界点干燥器中用液体作为置换剂置换中间介质,进行临界干燥。第五步:喷金。将干燥的样品用导电性好的粘合剂粘在金属样品台上,随后放在真空蒸发器中喷镀一层50—300 ?厚的金属膜。处理好的样品在扫描电子显微镜下利用二次电子成像原理实现对表皮结构的观察。试验使用英国Quorum K850进行CO2临界点干燥,使用FEI Quanta 250扫描电子显微镜进行结构观察。样品制备和扫描电镜观察由河大科技公司协助完成。1.2.2 西瓜果实表皮蜡粉成分的提取与检测 供试材料‘FH’果实成熟时,用单面美工刀片刮取果实表皮附着的白色蜡粉,注意避免刮到果皮。电子天平精确称量0.01 g蜡粉于2 mL密封玻璃瓶,然后加入1 mL三氯甲烷提取蜡质成分,待提取液蒸干后,加入50 μg正二十四烷作为内标,加入100 μL N,O-双(三甲基硅烷基)三氟乙酰胺作为衍生试剂,橡皮塞盖好玻璃瓶后用封口膜进行密封,接着将样品放于65℃水浴中衍生1 h,衍生完成后用氮吹仪吹去衍生试剂,再加入1 mL三氯甲烷进行溶解,随后用0.22 μm有机系滤头进行过滤,得到待测液。取1 μL待测液进行GC-MS分析,3次重复。以不同时间点的峰面积为指标,定量各化学成分,各物质的离子峰面积与有效提取物总离子峰面积的比值作为该物质的相对含量占比。
应用美国Agilent公司生产的7890A-5975C顶空G1888气质联用仪进行蜡粉成分分析。参数设置如下,色谱柱:DB5-MS,30 m×0.25 mm×0.25 μm毛细管柱,脉冲不分流进样,压强为270 kPa,保持0.7 min。衬管型号:19251-6050,进样量为1 μL,进样口温度设置为300℃。炉温箱的起始温度为50℃,并以40℃?min-1的速度升温至200℃,保持1 min,然后以3℃?min-1的速度升温至300℃,并保持15 min。检测温度为300℃,四级杆温度为150℃,离子源温度 230℃,模式设置为全扫模式,扫描范围50—550 amu。试验在郑州果树研究所果品质量检测中心实验室完成。检测方法参考罗倩等[16]。
1.2.3 西瓜果实表皮蜡粉性状的鉴定与统计 本试验将西瓜果实表皮蜡粉性状表型定义为有和无,果实成熟时通过目测法进行鉴定。亲本及后代群体P1、P2、F1、F2、BC1P1、BC1P2的种植株数分别为50、50、50、714、279、50。使用SAS 9.2软件进行显著性分析。
1.2.4 基因池的建立与重测序 试验采用集团分离分析法,即BSA法,对西瓜果实表皮蜡粉性状进行基因定位。在F2分离群体中,选取果实表皮有蜡粉和无蜡粉的西瓜各30株,分别取幼嫩叶片并保存在液氮中,用植物基因组DNA提取试剂盒分别提取样品DNA,然后将极端性状单株的DNA等量混合构建2个混池(R03、R04),加上两个双亲池(R01、R02),共构建4个DNA池。构建的基因池送至北京百迈客生物有限公司进行建库和测序,试验选用Illumina HiSeq测序仪进行测序,试验的流程按照Illumina公司提供的标准protocol执行。DNA提取试剂盒购自洛阳爱森生物科技有限公司。
1.2.5 关联分析与候选基因挖掘 重测序数据经质控及过滤后,使用bwa软件与西瓜参考基因组‘97103’[17]进行比对。接着使用GATK等软件对检测得到的高质量SNP、InDel进行变异检测,然后通过ED、SNP-index对SNP进行关联分析,通过ED、InDel-index对InDel进行关联分析,综合关联分析结果获得可能控制该性状的候选区间。进一步通过KEGG、COG 、GO等数据库完成候选区间的深度基因注释,并通过突变位点分析挖掘候选基因,最终获得可能控制西瓜果实表皮蜡粉生成的候选基因。
2 结果
2.1 西瓜果实表皮蜡粉的形态特征与结构
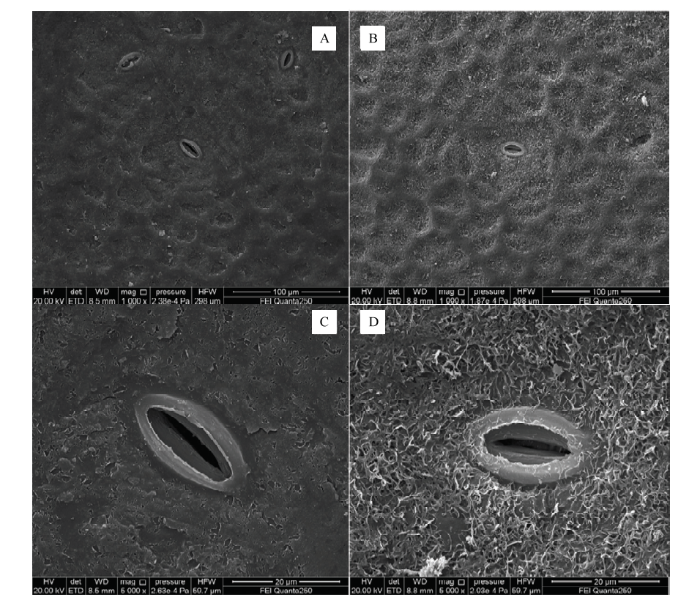
通过肉眼观察,在供试材料中,无蜡粉西瓜‘美佳选黑’果实表皮光滑,无蜡粉层附着(图1-A)。而有蜡粉西瓜‘FH’果实表皮附着一层致密的灰白色霜状物质,即为西瓜果实表皮蜡粉(图1-B),同时,田间材料观察发现,无蜡粉西瓜比有蜡粉材料更容易产生日灼伤。扫描电子显微镜下观察发现,西瓜果实表皮凹凸不平,气孔不均匀分布在表皮上,‘美佳选黑’果实表皮在果皮凹陷处光滑(图2-A,图2-C),未观察到绒毛状晶体结构;而‘FH’果实表皮凹陷及气孔附近观察到丰富的灰白色蜡粉晶体,呈板状结构,长度约5 μm(图2-B,图2-D)。
图2
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图2扫描电镜下西瓜果实表皮蜡粉结构
A:‘美佳选黑’果实表皮(1000×);B:‘FH’果实表皮(1000×);C:‘美佳选黑’果实表皮(5000×);D:‘FH’果实表皮(5000×)
Fig. 2Wax powder structure of watermelon fruit epidermis under scanning electron microscope
A: ‘Meijiaxuanhei’fruit epidermis (1000×); B: ‘FH’ fruit epidermis (1000×); C: ‘Meijiaxuanhei’ fruit epidermis (5000×); D: ‘FH’ fruit epidermis (5000×)
2.2 西瓜果实表皮蜡粉的化学成分
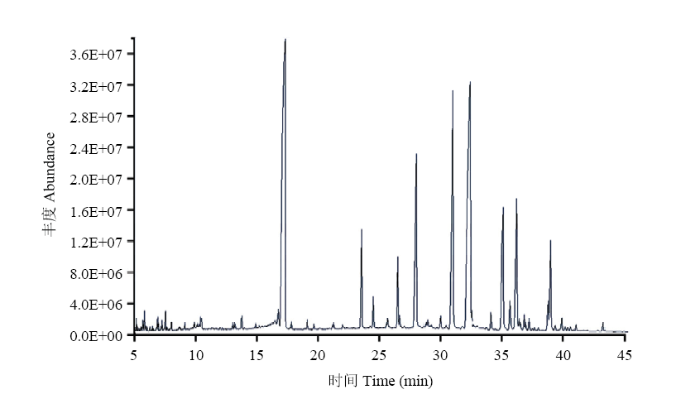
GC-MS实现了对西瓜果实表皮蜡粉各组分的有效分离(图3),共分离鉴定出24种已知化学结构的化学物质(表1),包括烃类物质10种,醇类5种,酯类5种,酸类2种,酚类1种,醛类1种。其中,烃类物质相对含量占比高达77.72%,烷烃的碳原子变化范围为C17—C36,主要包括C17、C26、C27、C28、C29、C32、C33、C34、C36的正链烷烃,正三十四烷相对含量占比最高,为40.76%;醇类相对含量占比为12.60%,包括3个初级醇和2个次级醇,其中1,30-三十烷二醇占比最高,为11.55%;酯类、酸类、酚类和醛类的相对含量占比依次为12.60%、0.43%、0.53%、0.80%、3.99%。检测结果表明,西瓜表皮蜡粉主要由脂肪族化合物烃类、醇、酯、脂肪酸和醛组成,其中烷烃的相对含量占比最高。图3
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图3西瓜果实表皮蜡粉的GC-MS总离子流分析
Fig. 3Total ion chromatograph of GC-MS for compounds in epicuticular wax of watermelon fruit
Table 1
表1
表1西瓜果实表皮蜡粉的组成成分与相对含量
Table 1
| 化合物类别 Categories | 化合物名称 Compounds | 保留时间 Retention time (min) | 相对含量 Relative content (%) |
|---|---|---|---|
| 正二十四烷* Tetracosane* | 17.20 | ||
| 烃类 Hydrocarbons | 2,6,10-三甲基十四烷 Tetradecane,2,6,10-trimethyl- | 4.92 | 0.05 |
| 3-乙基-5-(2-乙基丁基)十八烷 Octadecane, 3-ethyl-5-(2-ethylbutyl)- | 19.00 | 0.01 | |
| 正二十八烷 Octacosane | 23.45 | 5.89 | |
| 正二十九烷 Nonacosane | 27.92 | 16.24 | |
| 17-三十五烯 17-Pentatriacontene | 28.58 | 0.60 | |
| 正二十七烷 Heptacosane | 29.90 | 1.14 | |
| 正三十四烷 Tetratriacontane | 32.31 | 40.76 | |
| 正三十二烷 Dotriacontane | 34.02 | 1.07 | |
| 正三十三烷 Tritriacontane | 36.12 | 10.67 | |
| 正三十六烷 Hexatriacontane | 39.79 | 0.93 | |
| 酯类 Esters | (E)-3,7-二甲基-2,6-辛二烯醇3-甲基丁酸酯 Geranyl isovalerate | 5.28 | 0.10 |
| 顺式-9-十八碳烯酸-2-苯基-1,3-二氧杂环己烷-4-甲基酯 9-Octadecenoic acid, (2-phenyl-1,3-dioxolan-4-yl)methyl ester, cis- | 7.58 | 0.09 | |
| 俞酸甘油酯 Docosanoic acid, 1,2,3-propanetriyl ester | 35.83 | 0.11 | |
| 胆酸乙酯 Ethyl iso-allocholate | 12.21 | 0.05 | |
| 十八烯酸-3(十八烷氧基)丙酯 Oleic acid, 3-(octadecyloxy)propyl ester | 40.79 | 0.07 | |
| 醇类 Alcohols | 1-三十七烷醇 1-Heptatriacotanol | 9.64 | 0.15 |
| E,E,Z-1,3,12-十九烯-4,14-二醇 E,E,Z-1,3,12-Nonadecatriene-4,14-diol | 13.04 | 0.21 | |
| 1,30-三十烷二醇 1,30-Triacontanediol | 34.99 | 11.55 | |
| 1-三十五醇 1-Pentatriacontanol | 36.86 | 0.48 | |
| 乙酰氧基-7,8-环氧羊毛甾烷-11-醇 7,8-Epoxylanostan-11-ol, 3-acetoxy- | 37.58 | 0.21 | |
| 酸类 Acids | 顺式-1-二十碳烯酸 cis-13-Eicosenoic acid | 6.83 | 0.33 |
| 五氟丙酸八碳五烯酸Octatriacontyl pentafluoropropionate | 40.29 | 0.20 | |
| 酚类Phenols | 2,4-二叔丁基苯酚Phenol,2,4-bis(1,1-dimethylethy)- | 5.701 | 0.80 |
| 醛类Aldehyde | 十八醛 Octadecanal | 26.42 | 3.99 |
新窗口打开|下载CSV
2.3 西瓜果实表皮蜡粉性状的遗传分析
田间性状表型鉴定统计显示(表2),在F1群体中,成熟西瓜果实表面均有致密蜡粉层;在F2群体中,性状出现分离。其中,529株西瓜表皮有蜡粉,185株西瓜表皮无蜡粉,分离比例经过卡方检验基本符合3﹕1的孟德尔分离比例(χ2=0.32<χ20.05=3.841);BC1P1群体中有蜡粉和无蜡粉西瓜株数分别为150株129株,分离比符合1﹕1的理论比(χ2=1.58<χ20.05=3.841),BC1P2西瓜单株果实表皮均附着蜡粉。遗传规律分析表明,西瓜果实表皮蜡粉性状的有或无是质量性状,其遗传受一对显性基因控制,有蜡粉对无蜡粉为显性。Table 2
表2
表2六世代群体植株分离情况统计
Table 2
| 世代 Generations | 植株总数 Number of total plants | 有蜡粉株数 Number of plants with wax | 无蜡粉株数 Number of wax-free plants | 有﹕无 Ratios | P值 P value | 卡方值 χ2 values |
|---|---|---|---|---|---|---|
| P1 | 50 | - | 50 | |||
| P2 | 50 | 50 | - | |||
| F1 | 50 | 50 | - | |||
| F2 | 714 | 529 | 185 | 2.86:1 | 0.57 | 0.32 |
| BC1P1 | 279 | 150 | 129 | 1.16:1 | 0.21 | 1.58 |
| BC1P2 | 50 | 50 | - |
新窗口打开|下载CSV
2.4 西瓜果实表皮蜡粉性状的基因定位
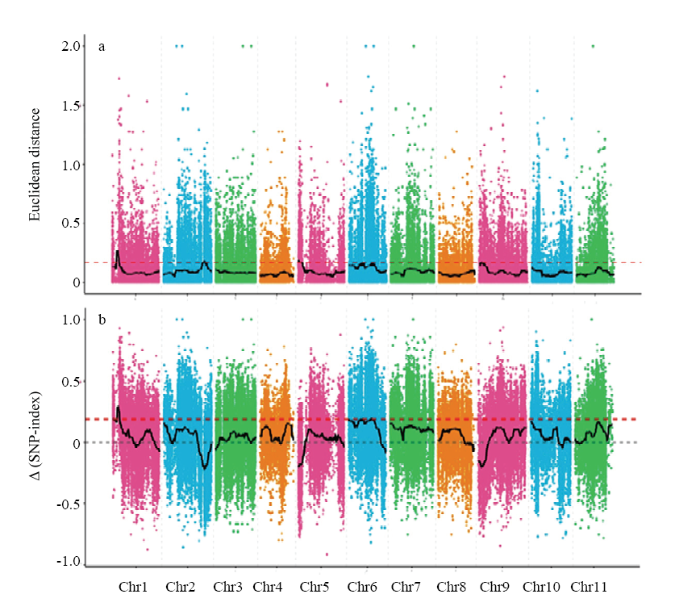
2.4.1 Illumina HiSeq测序结果 对构建的4个基因池进行全基因组重测序,共获得56.02 Gb的数据量,过滤后得到55.47 Gb的数据,Q30达到80%,4个样品的平均测序深度为39.06×。样品同参考基因组的平均比对效率为99.08%,平均覆盖深度为30.50×,基因组覆盖度99.57%,保证了至少一个碱基的覆盖。测序结果表明,样品数据量充足,测序质量合格,成功完成测序和建库工作,可用于后续的变异检测及性状的基因定位。2.4.2 SNP关联分析 SNP变异检测共获得了144 533个高质量SNP,这些SNP采用欧式距离(euclidean distance,ED)和SNP-index两种方法进行关联分析。ED算法通过寻找混池间存在显著差异标记,来对目标性状相关联的区域进行评估。ED值计算参见HILL等[18]研究,本项目取原始ED的2次方作为关联值,然后采用DISTANCE方法对ED值进行拟合,取全部位点拟合值的median+3SD作为分析的关联阈值。根据计算得ED分析关联阈值为0.17,结合关联阈值判定,共获得8个关联区域(图4-a),长度大小为5.95 Mb,分别在:Chr1(2.97—4.98 Mb),Chr2(28.88—30.07 Mb),Chr5(0—2.37 Mb),Chr9(1.49—1.50 Mb、1.53—1.58 Mb、1.74—1.74 Mb、1.76—1.98 Mb、2.04—2.14 Mb)。图4
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图4基于SNP的ED和Δ(SNP-index)关联分析图
Fig. 4ED and delta (SNP-index) correlation analysis chart based on SNP
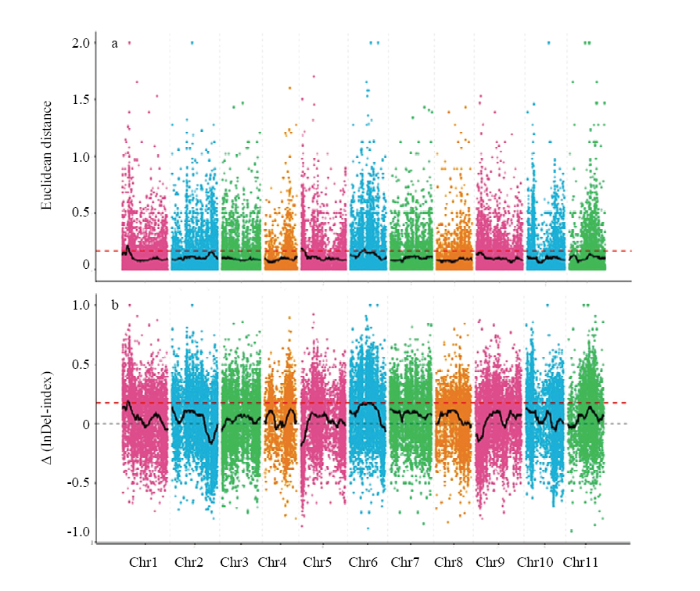
SNP-index通过寻找混池间基因型频率的显著差异Δ(SNP-index)进行标记关联分析,目标性状与标记SNP关联度越强,Δ(SNP-index)的值越接近于1。采用SNP-index方法关联分析时,利用拟合后Δ(SNP-index)的99百分位数计算关联阈值,计算得到关联阈值为0.19。依据参考阈值,共获得9个关联区域(图4-b),总长度大小为3.19 Mb,这9个关联区域在参考基因组上的位置为:Chr1(0—0.63 Mb、2.37—2.40 Mb、2.95—4.99 Mb),Chr6(10.27—10.34 Mb、10.36—10.36 Mb、16.54—16.89 Mb、17.01—17.02 Mb、17.04—17.07 Mb、17.10—17.11 Mb)。两种关联分析方法的关联区域在1号染色体2.97—4.98 Mb处存在交集,区间大小为2.01 Mb,包含172个基因。2.4.3 InDel关联分析 InDel变异检测获得高质量InDel位点50 258个,使用ED和InDel-index两种关联分析方法对这些InDel进行关联分析,分析方法与SNP分析所用的方法相同。ED关联分析计算得关联阈值为0.19。根据关联阈值进行判定,共获得了5个关联区域(图5-a),总长度大小为6.69 Mb,对应参考基因组上位置分别为:Chr1(3.00—5.02 Mb,Chr5(0—2.39 Mb),Chr6(10.14—10.16 Mb、10.18—11.15 Mb、8.87—10.07 Mb)。InDel-index方法分析时计算得到关联阈值为0.17,共得到6个区域(图5-b),总长度大小为3.25 Mb,关联区域分别位于:Chr1(3.16—4.48 Mb),Chr6(10.21—10.41 Mb、10.43—11.15 Mb、13.54—13.64 Mb、13.66—14.11 Mb、15.13—15.23 Mb)。
图5
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图5基于InDel的ED和Δ(InDel-index)关联分析
Fig. 5ED and delta (InDel-index) correlation analysis based on InDel
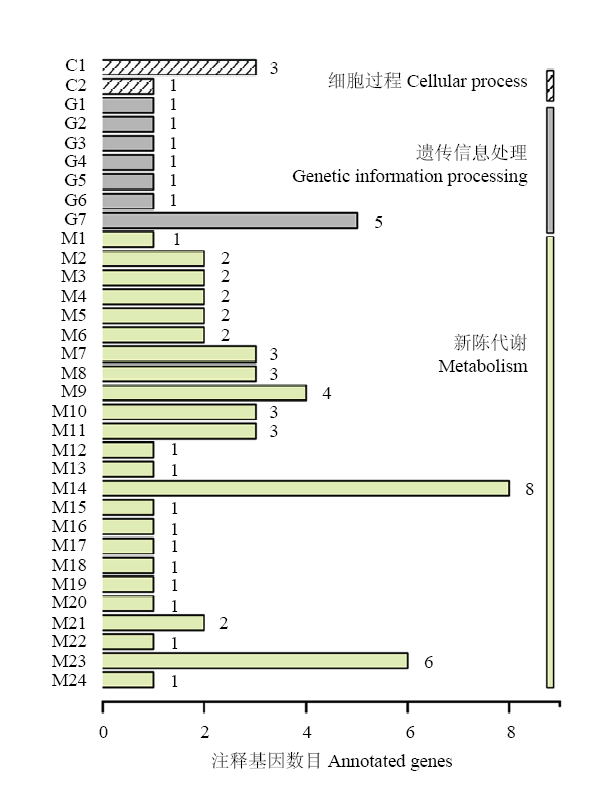
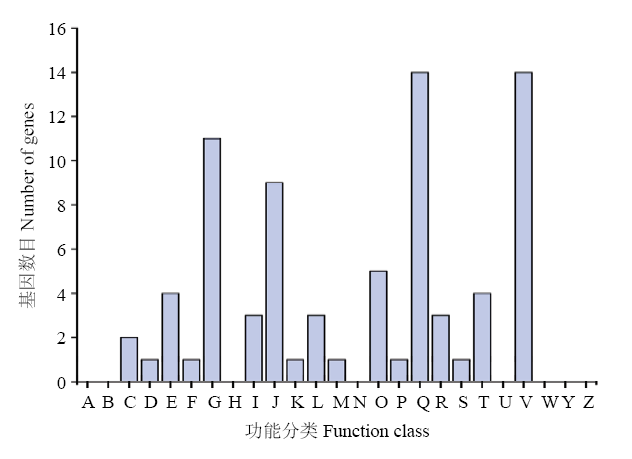
两种方法取交集共得到2.6 Mb关联区域,分别位于1号染色体起始位置3.16—4.84 Mb,6号染色体10.21—10.41 Mb和10.43—11.15 Mb处,关联区域包含182个基因。将SNP和InDel关联分析结果取交集得到1号染色体3.16—4.84 Mb共1.68 Mb的关联区域,该区域共144个基因。4种关联分析方法在该区域均有较高的峰值,说明在关联区域中可能存在西瓜果实表皮蜡粉生成相关的基因。2.4.4 候选区域的基因功能注释 为进一步对关联区域的基因进行挖掘,快速筛选获得与性状相关的基因,本试验利用BLAST软件对候选区间的编码基因进行KEGG和COG、GO等多个数据库的深度注释。KEGG数据库通过对基因间作用通路对基因的功能进行解读,注释结果显示(图6),富集到注释基因种类最多的依次为淀粉与蔗糖代谢、嘌呤代谢、核糖体、半乳糖代谢等。COG数据库能够对基因产物进行直系同源分类,注释结果显示(图7),富集较多注释基因的为防御机制、次生代谢产物的生物合成,转运和分解代谢、碳水化合物运输与代谢、翻译,核糖体结构与生物发生等。在候选区间中,多个数据库比对共注释到138个基因(表3)。在被注释到的基因中(表4),非同义突变基因10个,移码突变基因1个,这些突变的产生很可能与目标性状的表达差异有关。
图6
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图6候选区域内基因的KEGG功能分类
C1:内吞作用;C2:自噬的调节;G1:基底切除修复;G2:DNA复制;G3:同源重组;G4:错配修复;G5:核苷酸切除修复;G6:氨酰-tRNA生物合成;G7:核糖体;M1:半胱氨酸和蛋氨酸代谢;M2:甘氨酸、丝氨酸、苏氨酸代谢;M3:苯丙氨酸代谢;M4:酪氨酸代谢;M5:异喹啉生物碱生物合成;M6:对苯二甲酸、哌啶和吡啶生物碱的生物合成;M7:氨基糖和核苷酸糖代谢;M8:果糖和甘露糖代谢;M9:半乳糖代谢;M10:糖酵解/糖异生;M11:戊糖磷酸途径;M12:丙酸盐代谢;M13:丙酮酸代谢;M14:淀粉和蔗糖代谢;M15:氧化磷酸化;M16:氨基酸的生物合成;M17:碳代谢;M18:脂肪酸代谢;M19:脂肪酸生物合成;M20:甘油磷酸代谢;M21:β-丙氨酸代谢;M22:二萜生物合成;M23:嘌呤代谢;M24:嘧啶代谢
Fig. 6KEGG functional classification of genes in candidate regions
C1: Endocytosis; C2: Regulation of autophagy; G1: Base excision repair; G2: DNA replication; G3: Homologous recombination; G4: Mismatch repair; G5: Nucleotide excision repair; G6: Aminoacyl-tRNA biosynthesis; G7: Ribosome; M1: Cysteine and methionine metabolism; M2: Glycine, serine and threonine metabolism; M3: Phenylalanine metabolism; M4: Tyrosine metabolism; M5: Isoquinoline alkaloid biosynthesis; M6: Tropane, piperidine and pyridine alkaloid biosynthesis; M7: Amino sugar and nucleotide sugar metabolism; M8: Fructose and mannose metabolism; M9: Galactose metabolism; M10: Glycolysis / Gluconeogenesis; M11: Pentose phosphate pathway; M12: Propanoate metabolism; M13: Pyruvate metabolism; M14: Starch and sucrose metabolism; M15: Oxidative phosphorylation; M16: Biosynthesis of amino acids; M17: Carbon metabolism; M18: Fatty acid metabolism; M19: Fatty acid biosynthesis; M20: Glycerophospholipid metabolism; M21: beta-Alanine metabolism; M22: Diterpenoid biosynthesis; M23: Purine metabolism; M24: Pyrimidine metabolism
图7
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图7候选区域内基因的COG功能分类
A:RNA加工与修饰;B:染色质结构与变化;C:能量产生与转化;D:细胞周期调控与分裂,染色体重排;E:氨基酸运输与代谢;F:核苷酸运输与代谢;G:碳水化合物运输与代谢;H:辅酶运输与代谢;I:脂类运输与代谢;J:翻译,核糖体结构与生物合成;K:转录;L:复制、重组与修复;M:胞壁/膜生物发生;N:细胞运动;O:蛋白质翻译后修饰与转运,分子伴侣;P:无机离子运输与代谢;Q:次生产物合成,运输及代谢;R:一般功能基因;S:功能未知;T:信号传导机制;U:胞内分泌与膜泡运输;V:防御机制;W:细胞外结构;Y:核酸结构;Z:细胞骨架
Fig. 7COG functional classification of genes in candidate regions
A: RNA processing and modification; B: Chromatin structure and dynamics; C: Energy production and conversion; D: Cell cycle control, cell division, chromosome partitioning; E: Amino acid transport and metabolism; F: Nucleotide transport and metabolism; G: Carbohydrate transport and metabolism; H: Coenzyme transport and metabolism; I: Lipid transport and metabolism; J: Translation, ribosomal motility; K: Transcription; L: Replication, recombination and repair; M: Cell wall/memberance/envelope biogenesis; N: Cell motility; O: Posttranslational modification, protein turnover, chaperones; P: Inorganic ion transport and metabolism; Q: Secondary metabolites biosynthesis, transport and catabolixm; R: General function prediction only; S: Function unknown; T: Signal transduction mechanisms; U: Intracellular trafficking, secretion, and vesicular transport; V: Defense mechanisms; W: Extracellular structures; Y: Nuclear structure; Z: Cytoskeleton
Table 3
表3
表3候选区域内基因功能注释结果统计
Table 3
| 功能注释数据库Annotated_databases | 有注释信息基因数 Annotated information gene number | 存在非同义突变的基因数Number of genes with nonsynonymous mutations | 存在移码突变的基因数 Number of genes with frameshift mutation |
|---|---|---|---|
| GO | 42 | 6 | 0 |
| KEGG | 46 | 4 | 0 |
| COG | 63 | 8 | 1 |
| NR | 137 | 10 | 1 |
| NT | 133 | 10 | 1 |
| trEMBL | 136 | 10 | 1 |
| SwissProt | 118 | 10 | 1 |
| Total | 138 | 10 | 1 |
新窗口打开|下载CSV
Table 4
表4
表4候选区域内非同义突变基因和移码突变基因功能注释
Table 4
| 突变类型 Mutation type | 基因 Gene Id | 基因注释 Gene annotation |
|---|---|---|
| 非同义突变 Non synonymous mutation | Cla011514 | 细胞色素P450 Cytochrome P450 |
| Cla011577 | 乳酸/苹果酸脱氢酶 Lactate/malate dehydrogenase, | |
| Cla011542 | 铜胺氧化酶,酶结构域 Copper amine oxidase, enzyme domain | |
| Cla011561 | 3-Oxoacyl-[酰基载体蛋白(ACP)]合成酶Ⅲ 3-Oxoacyl-[acyl-carrier-protein (ACP)] synthase III | |
| Cla002342 | 含IPRO结构域(S)的IPRO1128细胞色素P450 Contains Inerpro domain(s) IPR001128 Cytochrome P450 | |
| Cla002367 | 烯酰基-(酰基载体蛋白)还原酶 Enoyl-(Acyl carrier protein) reductase | |
| Cla002326 | 木聚糖酶抑制剂N端 Xylanase inhibitor N-terminal | |
| Cla002353 | ABC转运体 ABC transporter | |
| Cla002337 | 细胞色素P450 Cytochrome P450 | |
| Cla011554 | 无顶端分生组织(NAM)蛋白 No apical meristem (NAM) protein | |
| 移码突变 Frameshift mutation | Cla002327 | rRNA/tRNA 2′-O-甲基转移酶类纤维蛋白样蛋白 rRNA/tRNA 2'-O-methyltransferase fibrillarin-like protein |
新窗口打开|下载CSV
2.4.5 候选基因的预测 结合参考基因组和数据库的基因注释发现,Cla002367基因注释的信息为烯酰ACP-还原酶(ECR),该基因编码的酶在特长链脂肪酸(VLCFAs)生物合成过程中起重要催化作用;Cla011514、Cla002337和Cla002342基因注释结果为细胞色素P450(CYP),研究表明,部分P450家族基因的编码蛋白能够通过催化烷基的羟化、烃基的氧化等生物学反应影响脂肪族化合物的生成;Cla002353基因注释信息为ABC转运体,蜡质组分从质膜转移到质外体的过程中,需要在ABC转运体作用下进行。因此,推测这5个非同义突变基因可能与西瓜果实表皮蜡粉的生成有关。
进一步根据DNA池的重测序数据及参考基因组信息,对5个潜在候选基因的SNP变异情况进行分析。结果显示,5个潜在候选基因由于编码区碱基序列的变异,导致氨基酸序列发生改变:Cla002367基因在4 208 461位置碱基处G突变成A,导致无蜡粉亲本蛋白序列第161位氨基酸发生改变(图8);Cla011514、Cla002337和Cla002342基因分别在3 302 452、4 550 489和4 513 862位置处发生C→T、G→A、T→C单碱基的突变并引物氨基酸的改变(图8);在无蜡粉亲本中,Cla002353在4 383 332位置处碱基由C突变成T,从而导致蛋白质翻译的提前终止,并在第708位置发生氨基酸终止编码(图8)。因此,推测以上5个基因为西瓜果实表皮蜡粉性状的候选基因。
图8
 新窗口打开|下载原图ZIP|生成PPT
新窗口打开|下载原图ZIP|生成PPT图8‘美佳选黑’(R01)和‘FH’(R02)候选基因蛋白质差异序列比较
虚线区域和箭头代表氨基酸序列发生变异的位置
Fig. 8Sequence polymorphisms of the protein sequence of candidate genes between ‘Mwijiaxuanhei’ and ‘FH’
The dotted area and arrows represented protein polymorphisms of candidate genes
3 讨论
3.1 植物蜡质具有保护作用
植物表皮蜡质具有重要保护作用,对表皮蜡质结构的研究有助于理解蜡质与环境的互作机制。蜡质的结构变异丰富,BARTHLOTT等[7]利用扫描电子显微镜对13 000多种植物表皮蜡质进行了观察,将蜡质的结构分成柱状、板状、管状等23类。根据其对不同植物表皮蜡质结构的分类描述,发现西瓜品种‘FH’果实表皮蜡粉符合板状结构的特征,蜡质晶体紧密地排列在一起,形成果实表皮灰白色霜状蜡粉层,而无蜡粉西瓜品种‘美佳选黑’表皮光滑,无蜡粉层附着。致密的蜡粉层对植物的保护作用不断被研究,如周会玲等[19]对‘巨峰’‘红地球’‘秋红’‘秋黑’葡萄果实结构和超微结构进行了观察,发现蜡质层厚、分布均匀且致密的品种耐储藏性更强;李宏建等[20]通过多功能荧光显微镜对不同苹果品种果实表皮细胞大小、蜡质层等指标进行测定,发现排列紧凑、蜡质厚的品种失水率较低。紧密排列的蜡粉层附着于西瓜表皮,相当于给西瓜果实穿上了一层“外衣”,从而减轻不良环境对果实造成的损害。3.2 蜡粉主要由脂肪族化合物组成
于海宁等[21]研究发现,脂肪族化合物是植物表皮蜡质最常见的化学成分,包括长链脂肪酸、醛、醇等物质,碳链长度一般为C18—C36,这与本研究的结果相符合。对蜡质化学成分进行研究也有助于了解组成成分的合成通路。本研究利用GC-MS分析发现西瓜果实蜡粉由脂肪族化合物烷烃(10种)、醇(5种)、酯(5种)、脂肪酸(2种)和醛(1种)组成,其中C17—C36正链烷烃的相对含量在蜡粉提取化合物中占比非常高,为77.72%。虽然蜡粉的化学成分种类相似,但不同植物化学物质含量有所差异,如与西瓜果实表皮蜡粉中烷烃占据绝对优势不同,王金秋等[9]研究发现3个品种柑橘果实表皮蜡质成分均以醛(41%—50%)为主,烷烃或酸次之,伯醇最少;BAUER等[22]对3个茄子果实表皮蜡粉成分进行测定,发现蜡粉成分主要为烷烃和醛类物质,占比77.00%。目前,蜡粉化学成分合成途径已经清楚,VLCFAs在质体中合成后,通过醇合成途径合成初级醇和烷基酯,或者经过烷烃合成途径合成烷烃、次级醇、酮和醛等物质。西瓜果实表皮蜡粉的24种化学成分涉及以上两条代谢途径,说明在西瓜中,果实表皮蜡粉同样是通过前体物质形成VLCFAs,然后通过两条合成途径生成各化学成分,无蜡粉西瓜果实表皮未形成致密蜡粉层,可能与蜡粉化学成分合成途径受阻有关。3.3 基因定位与候选基因分析
本试验建立了六世代群体,并对性状鉴定结果进行遗传分析,结果表明西瓜表皮蜡粉是由单基因控制的质量性状,有蜡粉为显性性状。目前还没有有关蜡粉遗传规律的研究报道,本研究结果丰富了西瓜表皮蜡粉的研究内容,同时对育种工作具有一定的指导作用。近年来,由于测序技术的快速发展,基于全基因组测序的BSA-seq技术也得到了相应的发展,并在玉米[23]、白菜[24]、桃[25]、油菜[26]、西瓜[27]等多种作物中大量应用,并定位到一大批与重要农艺性状相关的候选基因,该方法适合对单基因控制的质量性状或数量性状的主效基因进行定位,因此,采用BSA技术对西瓜果实表皮蜡粉进行基因定位合理可行。本研究采用4种关联算法对BSA-seq检测到的高质量SNP和InDel进行关联分析,将4种关联分析的结果取交集后得到1号染色体3.16—4.84 Mb,共1.68 Mb的区域内。但由于BSA无法精准获得目标性状的调控基因,所以本试验对关联区域的基因进行进一步的基因注释分析,以挖掘候选基因。候选区域138个有注释信息的基因中存在10个非同义突变的基因和1个移码突变基因。进一步对这11个基因进行分析发现,Cla002367为ECR类基因,它所编码的蛋白属于脂肪酸延伸酶复合物(FAE)的组成成分,乙酰辅酶A在FAE催化下经过缩合、还原、脱水、再还原四步反应后延伸酰基链生成VLCFAs,四步反应依次经过β-酮脂酰辅酶A合酶(KCS)、β-酮脂酰辅酶A还原酶(KCR)、β-羟酰辅酶A脱水酶(HCD)、烯酰辅酶A还原酶(ECR)催化完成。其中,再还原步骤是在ECR的催化作用下反应完成。KOHLWEIN等[28]首次从一个酵母突变体tsc13中分离了得到TSC13,该基因负责编码ECR,其编码蛋白能够与酵母KCS-Elo2p和Elo3p共同作用催化VLCFAs的合成;在拟南芥中,对cer10突变体和酵母突变体的互补研究说明CER10编码一个功能性的ECR[13,29],CER10的突变导致VLCFAs合成受阻;赵利[30]等从构建的木奈cDNA文库中得到一个ECR基因PsECR,对该基因在叶片不同生长发育过程中的动态分析表明,该基因很可能参与叶片蜡质合成的调控。在拟南芥ecr2突变体中,表皮蜡粉碳链长度最多达到C28,说明ECR2在C28延长过程中发挥着重要的作用[31]。Cla011514、Cla002337、Cla002342这3个基因注释信息为细胞色素P450家族基因。P450作为一类很大的可自身氧化的亚铁红素蛋白家族,主要参与的反应有烷基的羟化、烯基的环氧化、烃基的氧化等 [32]。如P450 BM3是脂肪酸羟基化酶,对碳链长C12—C40正链烷烃以及脂肪酸具有很高的催化活性,同时还可以催化一些杂环化合物[33,34];P450 2B4结构适应性强,催化完成C-H键的羟基化[35,36],在脱羰基等反应中也发挥着重要作用。西瓜果实表皮蜡粉成分主要为烃类、醇类和酯类的脂肪族有机化合物,所以猜测候选区域内存在的3个细胞色素P450家族基因的编码蛋白可能参与西瓜蜡粉组成成分的合成。Cla002353与ABC转运体相关,蜡质分子在运输的过程中,通过ABC转运体从质膜转移到细胞外基质,虽然目前转运机制还没完全被揭示,但ABC转运体在蜡质运输过程中发挥的重要作用毋庸置疑,如在拟南芥中,CER5和WBC11是转运蛋白编码基因,基因缺失的突变体中表皮蜡质含量减少[37,38]。综上所述,可以推测以上5个基因可能和西瓜蜡粉生成与转运有关。
本研究对西瓜表皮蜡粉性状进行初步定位并对候选基因进行预测,为完善蜡粉合成基因的定位工作打下基础,可以进一步的开发与目标性状紧密连锁的分子标记,并在子代分离群体中筛选重组单株,进而缩小候选区域,实现精细定位。
4 结论
西瓜果实表皮蜡粉为板状结构,主要是由脂肪族化合物组成,且烷烃成分的相对含量占比最高。遗传分析表明西瓜蜡粉是由单基因控制的质量性状,有蜡粉对无蜡粉为显性。利用BSA获得1号染色体1.68 Mb的关联区域,并预测该区域中Cla002367、Cla011514、Cla002337、Cla002342、Cla002353共5个非同义突变基因为调控西瓜果实表皮蜡粉性状的候选基因。参考文献 原文顺序
文献年度倒序
文中引用次数倒序
被引期刊影响因子
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
DOI:10.1016/S1161-0301(01)00094-6URL [本文引用: 1]
[本文引用: 1]
[本文引用: 1]
DOI:10.1111/boj.1998.126.issue-3URL [本文引用: 2]
DOI:10.16420/j.issn.0513-353x.2015-0048Magsci [本文引用: 1]

为了探索甘蓝蜡粉缺失突变体的特征特性和实际应用价值,对不同类型的5份甘蓝蜡粉缺失突变体进行了研究。叶表超微结构观察及蜡粉成分分析发现:突变体叶表面蜡粉严重缺失,其蜡粉量仅约为野生型的30%;野生型叶表蜡粉晶体结构主要为柱状和线状,而突变体主要为颗粒状和短棒状;野生型叶表蜡粉成分主要为烷烃、脂肪酸、醇、醛和酮,而突变体主要缺失成分为烷烃和酮,推测突变体蜡粉合成途径中的烷烃合成途径受阻,从而表现为蜡粉缺失。突变体的叶绿素浸出率和叶片失水率均显著高于其野生型,说明其叶片角质层透性增加。植株生长曲线的测定结果显示:突变体1和突变体3与其野生型相比生长相对滞后,生长势稍弱,而突变体2的生长与其野生型无显著差异。农艺性状及杂种优势的调查结果表明:蜡粉缺失甘蓝叶色亮绿,商品性好,特别是突变体2,不仅球形美观且其蜡粉缺失性状为显性遗传;用纯合显性的突变体2的自交系与普通材料配制的杂交组合具有球色亮绿、杂种优势明显的优点,实际应用价值较大。
DOI:10.16420/j.issn.0513-353x.2015-0048Magsci [本文引用: 1]

为了探索甘蓝蜡粉缺失突变体的特征特性和实际应用价值,对不同类型的5份甘蓝蜡粉缺失突变体进行了研究。叶表超微结构观察及蜡粉成分分析发现:突变体叶表面蜡粉严重缺失,其蜡粉量仅约为野生型的30%;野生型叶表蜡粉晶体结构主要为柱状和线状,而突变体主要为颗粒状和短棒状;野生型叶表蜡粉成分主要为烷烃、脂肪酸、醇、醛和酮,而突变体主要缺失成分为烷烃和酮,推测突变体蜡粉合成途径中的烷烃合成途径受阻,从而表现为蜡粉缺失。突变体的叶绿素浸出率和叶片失水率均显著高于其野生型,说明其叶片角质层透性增加。植株生长曲线的测定结果显示:突变体1和突变体3与其野生型相比生长相对滞后,生长势稍弱,而突变体2的生长与其野生型无显著差异。农艺性状及杂种优势的调查结果表明:蜡粉缺失甘蓝叶色亮绿,商品性好,特别是突变体2,不仅球形美观且其蜡粉缺失性状为显性遗传;用纯合显性的突变体2的自交系与普通材料配制的杂交组合具有球色亮绿、杂种优势明显的优点,实际应用价值较大。
[本文引用: 2]
[本文引用: 2]
[本文引用: 1]
.
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 2]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
Magsci [本文引用: 1]

<FONT face=Verdana>通过对‘巨峰’、‘红地球’、‘秋红’、‘秋黑’葡萄果实解剖结构和超微结构的比较, 探讨<BR>葡萄果实品种间耐贮性差异的生理学原因。结果表明: 葡萄的耐贮性与果皮和果肉的组织结构有密切关系。<BR>耐贮性好的品种其角质层及表皮组织均比较厚, 表皮细胞排列整齐而致密, 且与亚表皮细胞的结合紧密,<BR>其果肉组织排列也比较紧密, 且果肉细胞大小均匀。不同葡萄品种之间, 表面蜡质超微结构相差很大, 蜡<BR>质层较厚、蜡质分布均匀而致密的品种对SO<SUB>2</SUB> 抗性较强; 相反, 蜡质层薄、蜡质排列疏松、蜡层之间空隙<BR>较大的品种对SO<SUB>2</SUB> 较为敏感。</FONT>
Magsci [本文引用: 1]

<FONT face=Verdana>通过对‘巨峰’、‘红地球’、‘秋红’、‘秋黑’葡萄果实解剖结构和超微结构的比较, 探讨<BR>葡萄果实品种间耐贮性差异的生理学原因。结果表明: 葡萄的耐贮性与果皮和果肉的组织结构有密切关系。<BR>耐贮性好的品种其角质层及表皮组织均比较厚, 表皮细胞排列整齐而致密, 且与亚表皮细胞的结合紧密,<BR>其果肉组织排列也比较紧密, 且果肉细胞大小均匀。不同葡萄品种之间, 表面蜡质超微结构相差很大, 蜡<BR>质层较厚、蜡质分布均匀而致密的品种对SO<SUB>2</SUB> 抗性较强; 相反, 蜡质层薄、蜡质排列疏松、蜡层之间空隙<BR>较大的品种对SO<SUB>2</SUB> 较为敏感。</FONT>
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
DOI:10.16420/j.issn.0513-353x.2016-0240Magsci [本文引用: 1]

<p><span >大白菜</span><span lang="EN-US">[</span><em ><span lang="EN-US">Brassica rapa</span></em><span >(</span><span lang="EN-US">Lour.</span><span >)</span><span lang="EN-US">ssp. <em >pekinensis</em></span><span lang="EN-US">]</span><span >紫心纯系‘</span><span lang="EN-US">14S839</span><span >’</span><span >和橙色纯系‘</span><span lang="EN-US">14S162</span><span >’</span><span >为亲本,构建</span><span lang="EN-US">F<sub>2</sub></span><span >群体,对大白菜紫色基因(</span><em ><span lang="EN-US">BrPur</span></em><span >)进行遗传连锁分析。性状分离调查结果显示,在</span><span lang="EN-US">F<sub>2</sub></span><span >群体中紫心与非紫心单株符合</span><span lang="EN-US">3</span><strong ><span >︰</span></strong><span lang="EN-US">1</span><span >分离比例,说明大白菜紫心性状的有、无符合单基因显性遗传模式,紫心性状是一种显性性状。采用改良的</span><span lang="EN-US">BSA</span><span >方法对紫色基因</span><em ><span lang="EN-US">BrPur</span></em><span >进行定位,经过对白菜全基因组</span><span lang="EN-US">297</span><span >个</span><span lang="EN-US">SSR</span><span >标记的筛选,得到了</span><em ><span lang="EN-US">BrPur</span></em><span >的两个侧翼标记</span><span lang="EN-US">A710</span><span >和</span><span lang="EN-US">A714</span><span >,同时结合白菜基因组信息,将</span><em ><span lang="EN-US">BrPur</span></em><span >定位于大白菜</span><span lang="EN-US">A07</span><span >连锁群上。结合前人关于花青素代谢相关基因的研究报道,通过分析</span><em ><span lang="EN-US">Br4CL3</span></em><span lang="EN-US"></span><span >和</span><span lang="EN-US">Bra004214</span><span >的序列、</span><span >开发新的标记,得到了两个特异共显性标记</span><span lang="EN-US">CL-12</span><span >和</span><span lang="EN-US">B214-87</span><span >。利用</span><span lang="EN-US">F<sub>2</sub></span><span >群体扩增验证筛选到的所有标记,结果表明,<a name="OLE_LINK184">经</a></span><span ><span lang="EN-US">Join Map 4.0</span><span >作图得到的遗传连锁图</span></span><span >与非紫色交换单株“基因型矩阵”显示的结果完全一致,标记</span><span lang="EN-US">CL-12</span><span >和</span><span lang="EN-US">B214-87</span><span >位于</span><em ><span lang="EN-US">BrPur</span></em><span >两侧,遗传距离分别是</span><st1:chmetcnv w:st="on" unitname="cm" sourcevalue="3.1" hasspace="True" negative="False" numbertype="1" tcsc="0"><span lang="EN-US">3.1 cM</span></st1:chmetcnv><span >和</span><st1:chmetcnv w:st="on" unitname="cm" sourcevalue="3.5" hasspace="True" negative="False" numbertype="1" tcsc="0"><span lang="EN-US">3.5 cM</span></st1:chmetcnv><span >。</span></p>
DOI:10.16420/j.issn.0513-353x.2016-0240Magsci [本文引用: 1]

<p><span >大白菜</span><span lang="EN-US">[</span><em ><span lang="EN-US">Brassica rapa</span></em><span >(</span><span lang="EN-US">Lour.</span><span >)</span><span lang="EN-US">ssp. <em >pekinensis</em></span><span lang="EN-US">]</span><span >紫心纯系‘</span><span lang="EN-US">14S839</span><span >’</span><span >和橙色纯系‘</span><span lang="EN-US">14S162</span><span >’</span><span >为亲本,构建</span><span lang="EN-US">F<sub>2</sub></span><span >群体,对大白菜紫色基因(</span><em ><span lang="EN-US">BrPur</span></em><span >)进行遗传连锁分析。性状分离调查结果显示,在</span><span lang="EN-US">F<sub>2</sub></span><span >群体中紫心与非紫心单株符合</span><span lang="EN-US">3</span><strong ><span >︰</span></strong><span lang="EN-US">1</span><span >分离比例,说明大白菜紫心性状的有、无符合单基因显性遗传模式,紫心性状是一种显性性状。采用改良的</span><span lang="EN-US">BSA</span><span >方法对紫色基因</span><em ><span lang="EN-US">BrPur</span></em><span >进行定位,经过对白菜全基因组</span><span lang="EN-US">297</span><span >个</span><span lang="EN-US">SSR</span><span >标记的筛选,得到了</span><em ><span lang="EN-US">BrPur</span></em><span >的两个侧翼标记</span><span lang="EN-US">A710</span><span >和</span><span lang="EN-US">A714</span><span >,同时结合白菜基因组信息,将</span><em ><span lang="EN-US">BrPur</span></em><span >定位于大白菜</span><span lang="EN-US">A07</span><span >连锁群上。结合前人关于花青素代谢相关基因的研究报道,通过分析</span><em ><span lang="EN-US">Br4CL3</span></em><span lang="EN-US"></span><span >和</span><span lang="EN-US">Bra004214</span><span >的序列、</span><span >开发新的标记,得到了两个特异共显性标记</span><span lang="EN-US">CL-12</span><span >和</span><span lang="EN-US">B214-87</span><span >。利用</span><span lang="EN-US">F<sub>2</sub></span><span >群体扩增验证筛选到的所有标记,结果表明,<a name="OLE_LINK184">经</a></span><span ><span lang="EN-US">Join Map 4.0</span><span >作图得到的遗传连锁图</span></span><span >与非紫色交换单株“基因型矩阵”显示的结果完全一致,标记</span><span lang="EN-US">CL-12</span><span >和</span><span lang="EN-US">B214-87</span><span >位于</span><em ><span lang="EN-US">BrPur</span></em><span >两侧,遗传距离分别是</span><st1:chmetcnv w:st="on" unitname="cm" sourcevalue="3.1" hasspace="True" negative="False" numbertype="1" tcsc="0"><span lang="EN-US">3.1 cM</span></st1:chmetcnv><span >和</span><st1:chmetcnv w:st="on" unitname="cm" sourcevalue="3.5" hasspace="True" negative="False" numbertype="1" tcsc="0"><span lang="EN-US">3.5 cM</span></st1:chmetcnv><span >。</span></p>
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
DOI:10.1096/fasebj.10.2.8641552URL [本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
[本文引用: 1]
