
 , 张兰河
, 张兰河 东北大学 资源与土木工程学院, 辽宁 沈阳 110819
收稿日期:2021-02-18
基金项目:国家自然科学基金资助项目(51678119)。
作者简介:徐小惠(1986-),女,吉林白山人,东北大学博士研究生;
魏德洲(1956-),男,河南南阳人,东北大学教授,博士生导师。
摘要:为了快速、高效地提取活性污泥的胞外聚合物(extracellular polymeric substances, EPS), 采用4种方法提取紧密结合型EPS(tightly bound EPS, TB-EPS), 对比不同提取方法的优缺点, 考察TB-EPS对Mn2+吸附性能的影响, 研究了TB-EPS的吸附机理.结果表明: 加热法提取的TB-EPS效率高, 方法简单, 操作方便, 不破坏细胞结构.加热法提取的TB-EPS用于吸附重金属Mn2+, 其最大吸附率为53.8 %, 吸附过程符合二级反应动力学特征和Langmuir吸附等温方程, 该吸附以化学吸附为主.在TB-EPS中色氨酸和酪氨酸的疏水作用是主要的吸附机理.
关键词:活性污泥胞外聚合物(EPS)提取方法吸附Mn2+
Extraction and Adsorption Properties of Extracellular Polymeric Substance
XU Xiao-hui, WEI De-zhou

 , ZHANG Lan-he
, ZHANG Lan-he School of Resources & Civil Engineering, Northeastern University, Shenyang 110819, China
Corresponding author: WEI De-zhou, E-mail: dzwei@mail.neu.edu.cn.
Abstract: In order to quickly and efficiently extract extracellular polymeric substances(EPS)from activated sludge, four methods were used to extract tightly bound EPS(TB-EPS). The advantages and disadvantages of different extraction methods were compared, the effect of TB-EPS on the adsorption performance of Mn2+was investigated, and the adsorption mechanism of TB-EPS was studied. The results show that the heating method is simple and efficient with no damage to cell structure.When adsorbing heavy metal Mn2+, the maximum adsorption rate of TB-EPS extracted by heating method is 53.8 %. The adsorption process conforms to the second-order reaction kinetic characteristics and the Langmuir adsorption isotherm equation, which is mainly the chemical adsorption. The main adsorption mechanism of TB-EPS is the interaction of hydrophobic tryptophan and tyrosin.
Key words: activated sludgeextracellular polymeric substances(EPS)extraction methodadsorptionMn2+
胞外聚合物(EPS)是细胞新陈代谢分泌的一种高分子聚合物, 位于微生物细胞膜外部, 是生物膜的重要组成部分, 具有保护和维持生物膜的作用[1].EPS的成分以蛋白质(protein, PN)和多糖(polysaccharide, PS)为主, 约占70 % ~80 %, 其余为核酸、脂类和其他物质.EPS可以分为溶解态EPS(soluble EPS, S-EPS)和结合型EPS, 其中结合型EPS包括: 疏松结合型EPS(loosely bound EPS, LB-EPS)和紧密结合型EPS(tightly bound EPS, TB-EPS)[2-3].EPS与细胞结合紧密, 附着于细胞壁上, 可保护污泥絮凝体中的微生物不受外界环境变化的影响[4], 只有采用特定的方法才能将其提取出来.其中, 提取TB-EPS容易引起细胞损伤导致细胞破碎, 因此, 选择合适的提取方法对TB-EPS具有重要意义.目前, TB-EPS提取方法主要有物理法: 加热法、超声波法、离心法和阳离子树脂交换法(cation exchange resin, CER).化学法: 乙二胺四乙酸法(ethylene diamine tetraacetic acid, EDTA)、NaOH法和甲醛+NaOH法[5-9].物理法是机械法, 提取率低; 采用化学法提取TB-EPS产量高, 但会产生试剂和细胞裂解的污染.例如, 碱提取法加入NaOH使EPS中多糖和蛋白质的羧基失去其质子, 去质子化导致EPS分子间产生强烈的斥力并使其水溶性增强[10].采用EDTA法提取EPS, 会使细胞高度裂解, 干扰蛋白质的测定[11].目前, 提取TB-EPS尚无标准方法, 不同文献中所涉及不同物质提取EPS的方法得到的结论不尽相同.因此, 确定一种高效、不破坏细胞壁且适用于活性污泥的TB-EPS提取方法尤为重要.
TB-EPS含有大量的羟基、氨基、磷酸基等活性基团, 可以通过络合和静电作用吸附重金属离子, 为微生物提供良好的保护层[12].目前, TB-EPS吸附重金属的研究受到人们的关注.Wei等[13]研究了污泥胞外聚合物对Cu2+, Zn2+, Cd2+的吸附行为, 表明蛋白质对3种金属离子的吸附能力较高, 其次是腐殖酸, 多糖的吸附能力最低.此外, 国内外****发现不同污泥的EPS对金属离子的吸附作用和吸附机理不同.Wei等[14]研究了好氧颗粒污泥的EPS对Zn(Ⅱ)的吸附, 研究表明, 蛋白质更容易与Zn(Ⅱ)结合, 其吸附符合拟二级动力学模型, 吸附等温线符合Freundlich方程.Wei[15]等研究了活性污泥、厌氧颗粒污泥和厌氧絮凝污泥中EPS对Cu2+, Zn2+的吸附, 其中厌氧颗粒污泥的吸附力更强, Cu2+比Zn2+更容易被吸附.Wei等[16]研究了活性污泥和好氧颗粒污泥中EPS对Zn(Ⅱ)的生物吸附, 结果表明其吸附均符合拟二级动力学方程和Freundlich等温线, 但活性污泥的EPS与Zn(Ⅱ)的结合能力更强.Mn2+在细胞的生命活动中起重要作用, 可以作为金属蛋白存在, 锰的危害不受关注, 随冶金、炼钢和化工行业的发展, 含锰废水的产量也不断增加, 水中高浓度锰的存在会影响儿童智力发育, 产生注意力缺陷障碍[17].因此, 含锰废水的治理对人类健康和环境安全具有重要意义.研究了锰离子对EPS的结构和含量的影响, 采用活性污泥法处理含锰废水时, TB-EPS对锰离子的吸附行为的研究未见报道, 其吸附机理尚不清楚.
采用4种方法对A2O反应器中污泥TB-EPS的提取效果进行对比, 考察TB-EPS对Mn2+的吸附性能, 利用FTIR和3D-EEM分析TB-EPS组成的变化, 探讨其吸附动力学和吸附机理.
1 材料与方法1.1 实验污泥来源实验所用的污泥来源于稳定运行的A2O工艺二沉池, 实验取泥阶段反应器运行稳定, 化学需氧量(chemical oxygen demand, COD)去除率达到90 % 以上, 总氮(total nitrogen, TN)和总磷(total phosphorus, TP)去除率达到75 % 以上, 混合液体悬浮物(mixed liquid suspended solids, MLSS)约为12 000 mg · L-1.
1.2 污泥EPS提取方法污泥分层提取S-EPS, LB-EPS和TB-EPS, 具体方法如下: 取30 mL污泥离心10 min(4 ℃, 4 000 r · min-1), 上清液通过0.45 μm滤膜过滤, 滤液为S-EPS[18]; 剩余底泥利用质量分数为0.9 % NaCl补充至30 mL, 离心15 min(4 ℃, 8 000 r · min-1), 上清液通过0.45 μm滤膜过滤, 提取LB-EPS; 底泥再利用质量分数为0.9 % NaCl溶液补充至30 mL后, 利用超声法、加热法、甲醛+NaOH法和离心法分别处理污泥, 具体操作[19]流程如下.
1) 超声法: 将剩余底泥重新悬浮后用超声波发生器在130 W下超声10 min;
2) 加热法: 将剩余底泥重新悬浮后在60 ℃下水浴加热30 min;
3) 甲醛+NaOH法: 向重新悬浮后的底泥中加入适量的36.5 % 甲醛溶液, 并在4 ℃下震荡1 h后, 再加入1 mol /L的NaOH溶液震荡3 h;
4) 离心法: 将剩余底泥重新悬浮后在4 000 r/min, 4 ℃下离心20 min.
经过上述不同方法处理后, 所有样品在12 000 r · min-1, 4 ℃下离心15 min, 收集其上清液即为不同提取方法所得的TB-EPS.S-EPS, LB-EPS, TB-EPS溶液通过0.45 μm的滤膜过滤后进行组分分析.
1.3 Mn2+吸附实验pH=6时, 以一定量冷冻干燥后的TB-EPS粉末为吸附剂, 取25 mL一定质量浓度的Mn2+溶液至烧杯中, 在室温下用磁力搅拌(150 r/min)一定时间后, 取上清液, 经0.45 μm的滤膜过滤后, 用原子吸收分光光度计测定残留Mn2+(ρt).去除率Y(%)和吸附量q(mg/g)计算如下.
单位吸附量的计算式为
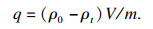 |
去除率的计算式为
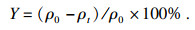 |
采用RF-6000型荧光分光光度计对TB-EPS进行三维荧光光谱测定.
将提取的TB-EPS进行冷冻干燥, 成为粉末状固体, 用KBr压片法对样品进行处理, 利用傅里叶变换红外光谱仪(Fourier transform infrared spectrometer, FTIR)(德国布鲁克公司, Tensor 27)测定处理后的样品.
2 结果与讨论2.1 TB-EPS的提取方法对比2.1.1 不同提取方法对TB-EPS含量的影响采用超声法、加热法、甲醛+NaOH法及离心法提取TB-EPS时, TB-EPS总量及各组分质量浓度的变化如表 1所示.
表 1(Table 1)
| 表 1 不同提取方法提取TB-EPS总量及各组分含量变化(质量浓度) Table 1 Total amount of TB-EPS and the content change of each component using different extraction methods ? | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
由表 1可知, 采用加热法和甲醛+NaOH法提取活性污泥EPS的质量浓度最高, 超声法次之, 离心法最差.超声法提取TB-EPS的质量浓度仅高于离心法, 为171.85 mg/L.离心法提取EPS的DNA质量浓度最低, 仅为0.5 mg/L.超声波法利用超声波(剪切力、空穴效应等)使污泥絮体分散, EPS脱离细胞表面释放到水中, 细胞裂解释放细胞内物质, 从而影响EPS中碳水化合物、蛋白质、腐殖酸和DNA的含量.超声作用时间短, 污泥受到的剪切力较弱, 导致EPS剥离不彻底; 超声作用时间延长, 大量微气泡会突然破裂产生强大的水力剪切力, 从而破坏了EPS的基质结构, 甚至使细胞壁和细胞膜破裂[20].
离心法利用离心力将EPS与进入水相的微生物表面的聚合物剥离, 与其他提取方法相比, TB-EPS的质量浓度最低, 为160.41 mg/L; 在TB-EPS各组分中, 活性污泥提取的主要成分均为蛋白质, 占总TB-EPS的72.89 %.该提取方法操作简单, 不会使细胞破裂, 无试剂污染, 但提取效率较低, 可作为EPS提取方法的对照方法.
甲醛+NaOH法对活性污泥提取的TB-EPS中蛋白质的质量浓度最高, 为105.77 mg/L, 但其DNA含量占总TB-EPS的8.02 %.甲醛+NaOH法利用甲醛与细胞膜上的蛋白质和核酸的氨基、羟基、羰基与巯基反应, 将其固定在细胞上, 防止细胞裂解; 加入NaOH使污泥pH升高, 中和EPS表面的酸性基团, 排斥带负电EPS, 促进絮凝物的扩散, 使得EPS在水中的溶解度增加, 有效提高EPS提取效率[21-22].采用甲醛+NaOH法耗时较长, EPS质量浓度高, 主要是由于采用甲醛+NaOH法提取EPS时, DNA含量高于其他提取方法, 而EPS中主要成分是多糖和蛋白质.化学法提取EPS会受到化学试剂的污染, 有可能影响EPS成分的测定[11].
加热法提取的TB-EPS的生化组成均高于其他物理方法, 加热法与甲醛+NaOH法提取的蛋白质的质量浓度相近, 加热法提取EPS中的多糖和腐殖酸的质量浓度均高于其他提取方法.DNA含量高于其他物理提取方法, DNA含量占总TB-EPS的0.62 %.EPS中DNA含量高, 表明提取过程中细胞破裂导致细胞内物质污染[23].EPS中的蛋白质和多糖等分子在提取过程中可以水解, 同时加热法有利于将牢固结合的EPS提取到絮凝物中, 从而提高EPS提取量[11].温度过高会影响EPS的性质, 故采用加热法提取EPS, 温度不宜过高.加热法操作简单、用时短、提取率高, 对细胞的破坏程度小, 对提取活性污泥TB-EPS是一种较优的方法.
2.1.2 不同方法提取TB-EPS三维荧光光谱3D-EEM可以快速检测EPS的组成成分.不同提取方法的TB-EPS的3D-EMM如图 1所示.图 1出现4个明显的荧光峰[24]: 色氨酸类荧光峰A的λex为260~280 nm, λem为315~330 nm; 酪氨酸类荧光峰B的λex为220~235 nm, λem为315~330 nm; 腐殖酸类荧光峰C的λex为340~370 nm, λem为410~440 nm; 富里酸类荧光峰D的λex为260~280 nm, λem为420~450 nm.由此可知, 提取的EPS主要包括色氨酸、酪氨酸类蛋白质和腐殖酸, 因此, EPS可以通过络合、离子交换、静电吸引、表面微沉淀等作用去除水中重金属[25-26].由图 1可知, 采用超声法、甲醛+NaOH法和离心法提取EPS均有峰A、峰B和峰C; 加热法提取EPS产生峰D, 有富里酸类物质存在, 富里酸中含有大量酚羟基、羰基等基团能与金属离子发生相互作用.采用加热法提取EPS的3D-EEM的荧光强度高于甲醛+NaOH法提取EPS, 采用超声法提取EPS的荧光强度次之, 离心法提取EPS的荧光强度最弱, 其中加热法的荧光强度远大于其他方法, 这与本研究中EPS组分质量浓度的变化基本一致.研究表明,活性污泥EPS质量浓度高是金属离子具有良好吸附性能的主要原因.
图 1(Fig. 1)
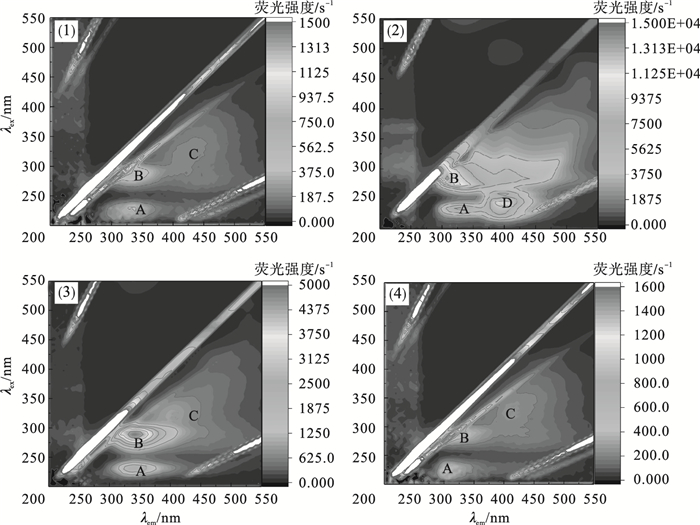 | 图 1 不同提取方法TB-EPS三维荧光光谱Fig.1 Three-dimensional fluorescence spectra of TB-EPS with different extraction methods (1)—超声法; (2)—加热法; (3)—甲醛+NaOH法; (4)—离心法. |
2.1.3 不同方法提取的TB-EPS红外光谱采用4种方法提取活性污泥TB-EPS的红外光谱谱图, 如图 2所示.由图可知, 4种方法均在3 250~3 500 cm-1处存在一个较宽的吸收峰, 由O—H和N—H伸缩振动导致, 该基团类型为缔合的羟基和氨基, 其中氨基为蛋白质的主要基团[27].在1 640 cm-1处存在一个较明显的吸收峰, 由C=O伸缩振动导致, 该峰属于蛋白质中肽键的酰胺Ⅰ, 处于蛋白质二级结构中的β折叠[28].在1 424 cm-1存在一个由—COO—基团的C=O对称拉伸产生的吸收峰, 属于酰胺Ⅱ.在1 100 cm-1处存在一个由C—O—C伸缩振动产生的峰, 该基团属于多糖结构.900~600 cm-1为指纹区域, 表明存在硫、磷不饱和键[29].采用物理法提取TB-EPS的红外光谱与Comte等[11]的研究结果基本相似.在甲醛+NaOH方法中无指纹区域, 但在2 930 cm-1左右处出现CH2不对称伸缩振动吸收峰, 该峰与碳水化合物、蛋白质、脂质和腐殖酸的脂肪链有关[22].
图 2(Fig. 2)
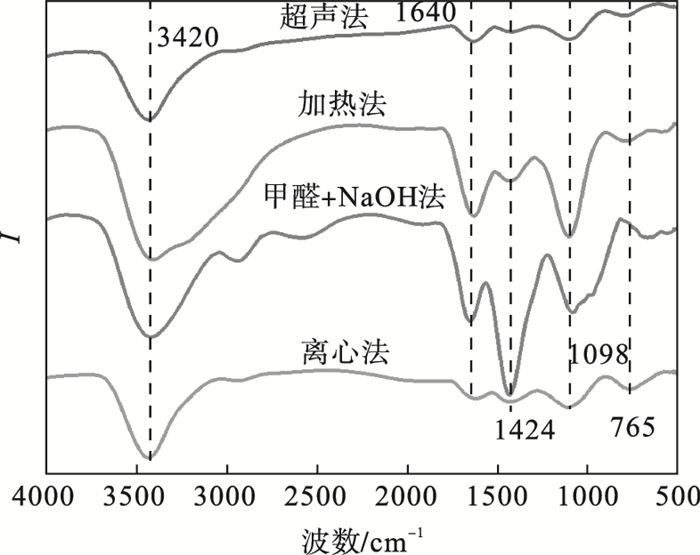 | 图 2 不同提取方法TB-EPS红外光谱Fig.2 TB-EPS infrared spectroscopy with different extraction methods |
根据TB-EPS的质量浓度、三维荧光光谱和红外光谱定性分析, 采用加热法提取TB-EPS.
2.2 吸附锰离子的TB-EPS组成变化2.2.1 红外光谱分析采用加热法, 对提取的TB-EPS进行吸附锰离子, 其吸附前后的FT-IR光谱如图 3所示.由图 3可知, TB-EPS吸附锰离子前后的谱峰相近, 主要基团组成相似.Mn2+的加入并未使吸收峰的位置发生明显改变, 说明EPS的主要成分为PN和PS, 其中以羟基、氨基、羧基和酰胺基团为主[30-31].TB-EPS与Mn2+结合后, 1 425 cm-1处的吸收峰完全消失, 说明酰胺Ⅱ基团在重金属吸附过程中发挥了作用[32].
图 3(Fig. 3)
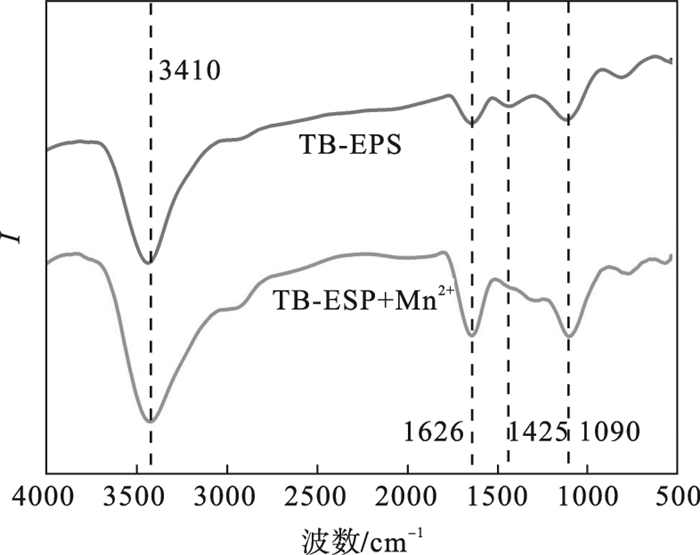 | 图 3 EPS吸附Mn2+前后的FT-IRFig.3 FT-IR of EPS before and after Mn2+ adsorption |
2.2.2 三维荧光光谱分析TB-EPS吸附Mn2+后的三维荧光光谱如图 4所示.当TB-EPS吸附Mn2+后, 色氨酸、酪氨酸蛋白、腐殖酸、富里酸的荧光强度减弱, 表现出不同程度的猝灭.色氨酸和酪氨酸是具有强疏水性侧链的疏水性氨基酸, 主要在TB-EPS上提供疏水性吸附位点.疏水作用使TB-EPS与Mn2+紧密结合, 荧光强度的猝灭可能归因于新化合物的形成.一旦重金属离子进入蛋白质内部疏水区, TB-EPS中的肽链就会伸展, 更多的色氨酸和酪氨酸暴露在水溶液中, 它们容易结合并占据更多的吸附位点[33].研究表明, TB-EPS中的主要成分为蛋白质和多糖, 其质量比约为1.7, 蛋白质在吸附过程中起重要作用.由于TB-EPS中含有大量的蛋白质且具有较强的结合力, 所以TB-EPS的疏水作用可能在吸附过程中起主导作用.
图 4(Fig. 4)
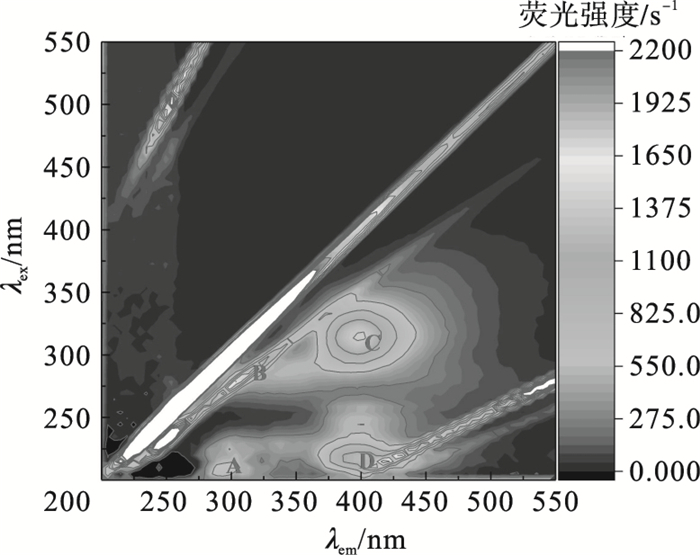 | 图 4 TB-EPS吸附Mn2+后的3D-EEM谱图Fig.4 3D-EEM spectrum of TB-EPS after Mn2+ adsorbtion |
2.2.3 Zeta电位分析EPS通过静电吸附作用与重金属结合, 改变EPS的表面电荷[34].TB-EPS吸附Mn2+后Zeta电位的变化如图 5所示.可知, 随着Mn2+质量浓度增加, Zeta电位增加, TB-EPS表面电荷相应减少, 说明TB-EPS通过静电作用与Mn2+相结合.吸附前后Zeta电位的变化不大, Zeta电位从-20.94 mV增高到-12.34 mV, 但TB-EPS对Mn2+有较高的吸附力.结合3D-EEM谱图可知, 在吸附过程中存在静电吸附和疏水作用, 但更倾向于TB-EPS的疏水作用.
图 5(Fig. 5)
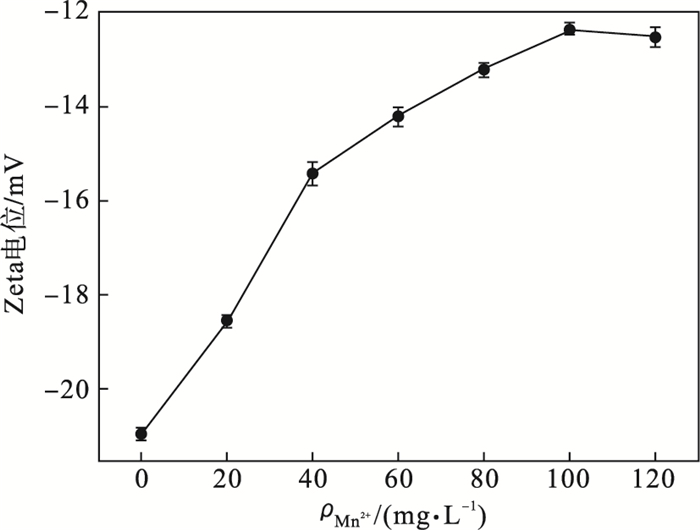 | 图 5 TB-EPS吸附Mn2+后的Zeta电位Fig.5 Zeta potential of TB-EPS before and after Mn2+ adsorption |
2.3 TB-EPS吸附锰离子的机理适当增加吸附时间有利于吸附剂的扩散及吸附剂与目标污染物的碰撞接触.当TB-EPS投加量为0.4 g/L, Mn2+初始质量浓度为100 mg/L时, 考察吸附时间对Mn2+去除率的影响, 结果如图 6a所示, 表明不同吸附时间下EPS对Mn2+的吸附能力.TB-EPS对Mn2+的吸附过程包含快速吸附阶段(0~5 min)和慢速吸附阶段(5~40 min), 40 min后吸附基本达到平衡, Mn2+去除率为53.8 %.将实验数据进行一级动力学和二级动力学模拟[35], 结果如表 2所示.
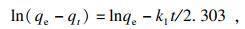 | (1) |
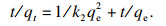 | (2) |
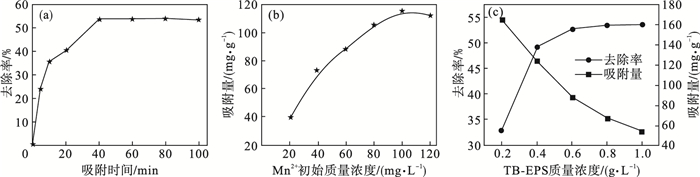 | 图 6 TB-EPS对锰离子的吸附效果Fig.6 Adsorption effect of TB-EPS on Mn2+ (a)—吸附时间; (b)—Mn2+初始质量浓度; (c)—TB-EPS质量浓度. |
表 2(Table 2)
| 表 2 吸附动力学拟合参数 Table 2 Fitting parameters of adsorption kinetics | ||||||||||||||||||||
式中: qe和qt分别为平衡时及t时刻吸附剂吸附的重金属离子的量, mg/g; k1为一级吸附速率常数, min-1; ln(qe-qt)和t的线性拟合决定速率常数k1; k2为二级吸附速率常数, g · mg-1 · min-1; t/qt和t线性拟合决定速率常数k2.
由表 2可知, 吸附时间对TB-EPS吸附Mn2+的影响符合二级动力学方程.在TB-EPS中PN的质量浓度高于PS的质量浓度, 这表明在TB-EPS中蛋白质对重金属的吸附速度较多糖快.
在TB-EPS的投加量为0.4 g/L, 吸附时间40 min时, 考察Mn2+初始质量浓度对其吸附量的影响, 结果如图 6b所示.当Mn2+的质量浓度为20 mg/L时, TB-EPS对Mn2+的吸附量只有39.50 mg/g; 当Mn2+的初始质量浓度达到100 mg/L时, 其吸附量升高到115.50 mg/g.当Mn2+初始浓度较低时, Mn2+数量少于TB-EPS表面的吸附位点, 吸附量小.随着重金属离子质量浓度的增加, 重金属离子与TB-EPS表面吸附位点的碰撞几率必然上升, 从而增加了Mn2+的吸附量.随Mn2+初始质量浓度的继续增高, TB-EPS对其吸附量的增加呈减小趋势, 最终会达到吸附平衡状态[36].
在Mn2+初始质量浓度为100 mg/L, 吸附时间40 min时, 考察TB-EPS投加量对Mn2+去除效果的影响, 结果如图 6c所示.由图 6c可知, 随着TB-EPS用量的增加Mn2+的去除率增大, 吸附量变小.随着吸附剂用量的增加, 其高分子链状结构吸附位点被包埋,未发挥吸附作用[37]; TB-EPS中的静电作用和反应基团的相互干扰也会导致TB-EPS的吸附量降低, 可能是因为吸附剂表面结合位点的强弱不同, 使吸附剂之间对金属离子发生竞争吸附, 从而导致单位吸附量降低.
采用Langmuir和Freundlich等温式对TB-EPS吸附Mn2+的过程进行拟合, 等温模型参数如表 3所示.
表 3(Table 3)
| 表 3 等温吸附模型的拟合参数 Table 3 Fitting parameters of isothermal adsorption model | ||||||||||||||||||||
Langmuir等温式为
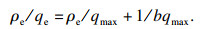 | (3) |
Freundlich等温式为
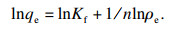 | (4) |
由表 3可知, Langmuir方程能较好地描述TB-EPS对Mn2+的吸附, 说明TB-EPS吸附Mn2+属于单分子层吸附.所有吸附位点对Mn2+的影响是相同的, 这也间接地说明化学作用在吸附过程中起主导作用.
3 结论1) 采用加热法提取TB-EPS的质量浓度最高, TB-EPS含有大量的蛋白质、多糖、富里酸类物质, 均对重金属类物质有较高的吸附作用.
2) TB-EPS对Mn2+吸附符合Langmuir等温方程和二级反应动力学, 说明TB-EPS对Mn2+是典型单分子层吸附; 主要吸附类型为化学吸附, 其吸附机理主要是TB-EPS的疏水作用.
3) TB-EPS吸附Mn2+的官能团主要是氨基、多聚糖、羟基、羧基和酰胺基团等.
参考文献
| [1] | 赵青, 卞伟, 李军, 等. DO/NH4+-N实现短程硝化过程中生物膜特性[J]. 环境科学, 2018, 39(3): 1278-1285. (Zhao Qing, Bian Wei, Li Jun, et al. Characteristics of biofilm during the transition process of complete nitrification and partial nitrification[J]. Environmental Science, 2018, 39(3): 1278-1285.) |
| [2] | Pellicer-Nacher C, Domingo-Felez C, Mutlua G, et al. Critical assessment of extracellular polymeric substances extraction methods from mixed culture biomass[J]. Water Research, 2013, 47(15): 5564-5574. DOI:10.1016/j.watres.2013.06.026 |
| [3] | Yu G H, He P J, Shao L M, et al. Stratification structure of sludge flocs with implications to dewater ability[J]. Environmental Science & Technology, 2008, 42(21): 7944-7949. |
| [4] | Liu Y, Li J, Qiu X F, et al. Bactericidal activity of nitrogen-doped metal oxide nanocatalysts and the influence of bacterial extracellular polymeric substances(EPS)[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2007, 190(1): 94-100. DOI:10.1016/j.jphotochem.2007.03.017 |
| [5] | King R O, Forster C F. Effects of sonication on activated-sludge[J]. Enzyme and Microbial Technology, 1990, 12: 109. DOI:10.1016/0141-0229(90)90082-2 |
| [6] | Frolund B, Palmgren R, Keiding K, et al. Extraction of extracellular polymers from activated sludge using a cation exchange resin[J]. Water Research, 1996, 30: 1749-1758. DOI:10.1016/0043-1354(95)00323-1 |
| [7] | Karapanagiotis N K, Rudd T, Sterritt R M, et al. Extraction and characterization of extracellular polymers in digested sewage-sludge[J]. Journal of Chemical Technology and Biotechnology, 2007, 44(2): 107-120. DOI:10.1002/jctb.280440203 |
| [8] | Morgan J W, Forster C F, Evison L. A comparative study of the nature of biopolymers extracted from anaerobic and activated sludges[J]. Water Research, 1990, 24: 743-750. DOI:10.1016/0043-1354(90)90030-A |
| [9] | Liu H, Fang H H P. Extraction of extracellular polymeric substances(EPS)of sludges[J]. Journal of Biotechnology, 2002, 95: 249-256. DOI:10.1016/S0168-1656(02)00025-1 |
| [10] | Klai N, Ram S K, Sellamuthu B, et al. Critical review of EPS production, synthesis and composition for sludge flocculation[J]. Journal of Environmental Sciences, 2018, 66: 225-245. DOI:10.1016/j.jes.2017.05.020 |
| [11] | Comte S, Guibaud G, Baudu M. Relation between extraction protocols of the activated sludge extracellular polymeric substances(EPS)and EPS complexation properties[J]. Enzyme Microbial Technology, 2006, 38: 237-245. DOI:10.1016/j.enzmictec.2005.06.016 |
| [12] | 林伟雄, 顾海奇, 郑诗琳, 等. 不同提取方法对活性污泥胞外聚合物吸附废水中Cd(Ⅱ)效能的影响[J]. 环境工程学报, 2020, 14(3): 829-834. (Lin Wei-xiong, Gu Hai-qi, Zheng Shi-lin, et al. Effect of different extracellular polymer extraction methods from activated sludge on its adsorption capacity of Cd(Ⅱ)in wastewater[J]. Chinese Journal of Environmental Engineering, 2020, 14(3): 829-834.) |
| [13] | Wei L L, Li J J, Xue M, et al. Adsorption behaviors of Cu2+, Zn2+ and Cd2+ onto proteins, humic acid, and polysaccharides extracted from sludge EPS: sorption properties and mechanisms[J]. Bioresource Technology, 2019, 291: 1-9. |
| [14] | Wei D, Li M, Wang X, et al. Extracellular polymeric substances for Zn(Ⅱ)binding during its sorption process onto aerobic granular sludge[J]. Journal of Hazardous Materials, 2016, 301: 407-415. DOI:10.1016/j.jhazmat.2015.09.018 |
| [15] | Wei L L, Yang L, Daniel R N, et al. Adsorption of Cu2+ and Zn2+ by extracellular polymeric substances(EPS)in different sludges: effect of EPS fractional polarity on binding mechanism[J]. Journal of Hazardous Materials, 2017, 321(5): 473-483. |
| [16] | Wei L, An X, Wang S, et al. Effect of hydraulic retention time on deterioration/restarting of sludge anaerobic digestion: extracellular polymeric substances and microbial response[J]. Bioresource Technology, 2017, 244: 261-269. DOI:10.1016/j.biortech.2017.07.110 |
| [17] | Joseph E, Mai X Y, Jiang Y J, et al. Oxidation of manganese(Ⅱ)with ferrate: stoichiometry, kinetics, products and impact of organic carbon[J]. Chemosphere, 2016, 159: 457-464. DOI:10.1016/j.chemosphere.2016.06.014 |
| [18] | 张海丰, 于海欢, 问志勇, 等. 铁离子分布规律及其对MBR微生物代谢产物的影响[J]. 硅酸盐通报, 2016, 35(3): 784-788. (Zhang Hai-feng, Yu Hai-huan, Wen Zhi-yong, et al. Distributions of Fe3+ and its influence on microbial products in membrane bioreactor[J]. Bulletin of the Chinese Ceramic Society, 2016, 35(3): 784-788.) |
| [19] | 周俊, 周立祥, 黄焕忠. 污泥胞外聚合物的提取方法及其对污泥脱水性能的影响[J]. 环境科学, 2013, 34(7): 2752-2757. (Zhou Jun, Zhou Li-xiang, Huang Huan-zhong. Optimization of extracellular polymeric substance extraction method and its role in the dewaterability of sludge[J]. Environmental Science, 2013, 34(7): 2752-2757.) |
| [20] | Han X M, Wang Z W, Zhu C W, et al. Effect of ultrasonic power density on extracting loosely bound and tightly bound extracellular polymeric substances[J]. Desalination, 2013, 329: 35-40. DOI:10.1016/j.desal.2013.09.002 |
| [21] | Sutherland B W, Toews J, Kast J. Utility of formaldehyde cross linking and mass spectrometry in the study of protein-protein interactions[J]. Journal of the American Society for Mass Spectrometry, 2008, 43: 699-715. DOI:10.1002/jms.1415 |
| [22] | Dabzac P, Bordas F, Hullebusch E V, et al. Extraction of extracellular polymeric substances(EPS)from anaerobic granular sludges: comparison of chemical and physical extraction protocols[J]. Applied Microbiology & Biotechnology, 2010, 85(5): 1589-1599. |
| [23] | Zhang X G, Bishop P L, Kinkle B K. Comparison of extraction methods for quantifying extracellular polymers in biofilms[J]. Water Science Technology, 1999, 39: 211-218. |
| [24] | Zhang L H, Zhao Q N, Zhang M S, et al. Mg2+ distribution in activated sludge and its effects on the nitrifying activity and the characteristics of extracellular polymeric substances and sludge flocs[J]. Process Biochemistry, 2020, 88: 120-128. DOI:10.1016/j.procbio.2019.10.002 |
| [25] | Liu W, Zhang J S, Jin Y J, et al. Adsorption of Pb(Ⅱ), Cd(Ⅱ)and Zn(Ⅱ)by extracellular polymeric substances extracted from aerobic granular sludge: efficiency of protein[J]. Journal of Environmental Chemical Engineering, 2015, 3(2): 1223-1232. DOI:10.1016/j.jece.2015.04.009 |
| [26] | 张兰河, 徐英, 陈子成, 等. Fe3+和Na+共存对缺氧污泥脱氮除磷效率和胞内外聚合物的影响[J]. 农业工程学报, 2020, 36(8): 197-204. (Zhang Lan-he, Xu Ying, Chen Zi-cheng, et al. Effects of coexisting Fe3+and Na+on nitrogen and phosphorus removal intracellular polymeric substances and extracellular polymeric substances of anoxic sludge[J]. Transactions of the Chinese Society of Agricultural Engineering, 2020, 36(8): 197-204.) |
| [27] | Zhao B Q, Chen N, Feng C P, et al. Adsorption for phosphate by crosslinked/non-crosslinke-chitosan-Fe(Ⅲ)complex sorbents: characteristic and mechanism[J]. Chemical Engineering Journal, 2018, 353: 361-372. DOI:10.1016/j.cej.2018.07.092 |
| [28] | Zhu L, Qi H Y, Lyu M, et al. Component analysis of extracellular polymeric substances(EPS)during aerobic sludge granulation using FTIR and 3D-EEM technologies[J]. Bioresource Technology, 2012, 124: 455-459. DOI:10.1016/j.biortech.2012.08.059 |
| [29] | 王琰, 钱飞跃, 王建芳, 等. 亚硝化颗粒污泥中EPS提取方法与组成特性的比较研究[J]. 环境科学学报, 2015, 35(11): 3515-3521. (Wang Yan, Qian Fei-yue, Wang Jian-fang, et al. Comparative study on extraction methods and composition of extracellular polymeric substances(EPS)in granular nitrosation sludge[J]. Acta Scientiae Circumstantiae, 2015, 35(11): 3515-3521.) |
| [30] | 张明爽. Fe3+对A2O工艺脱氮除磷的影响及其迁移转化规律的研究[D]. 吉林: 东北电力大学, 2020: 26-27. (Zhang Ming-shuang. The Influence study of Fe3+on nitrogen and phosphorus removal and its migration and transformation law by A2O process[D]. Jilin: Northeast Electric Power University, 2020: 26-27. ) |
| [31] | 郑晶. Al3+对A2O工艺生物脱氮和污泥性质的影响[D]. 吉林: 东北电力大学, 2020: 27-28. (Zheng Jing. Effects of Al3+on biological denitrification and sludge properties using A2O process[D]. Jilin: Northeast Electric Power University, 2020: 27-28. ) |
| [32] | 康得军, 谢丹瑜, 匡帅, 等. 活性污泥胞外聚合物对Pb2+和Cu2+的吸附机理[J]. 中国给水排水, 2016, 32(21): 28-33. (Kang De-jun, Xie Dan-yu, Kuang Shuai, et al. Adsorption mechanism of extracellular polymeric substances in activated sludge on Pb2+and Cu2+[J]. China Water & Waste Water, 2016, 32(21): 28-33.) |
| [33] | Pi S S, Li A, Cui D, et al. Biosorption behavior and mechanism of sulfonamide antibiotics in aqueous solution on extracellular polymeric substances extracted from Klebsiella sp.J1[J]. Bioresource Technology, 2019, 272: 346-350. DOI:10.1016/j.biortech.2018.10.054 |
| [34] | Alvarez-Puebla R A, Garrido J J. Effect of pH on the aggregation of a gray humic acid in colloidal and solid states[J]. Chemosphere, 2005, 59: 659-667. DOI:10.1016/j.chemosphere.2004.10.021 |
| [35] | Niu C M, Wu W H, Wang Z, et al. Adsorption of heavy metal ions from aqueous solution by cross linked carboxymethyl konjac glucomannan[J]. Journal of Hazardous Materials, 2007, 141: 209-214. |
| [36] | 鲁敏, 关晓辉, 魏德洲, 等. 氨基磺酸铵-细菌纤维素对Pb2+的吸附性能及机理[J]. 东北大学学报(自然科学版), 2011, 32(7): 1036-1040. (Lu Min, Guan Xiao-hui, Wei De-zhou, et al. Adsorption property and mechanism of ammonium sulfamate-bacterial cellulose to Pb2+[J]. Journal of Northeastern University(Natural Science), 2011, 32(7): 1036-1040.) |
| [37] | 郑燕. 含重金属废水、低浊度废水净化剂的制备及应用研究[D]. 上海: 上海交通大学, 2008: 96-97. (Zheng Yan. Production of purifying agent and its use in treatment of heavy metal and supension wastewater[D]. Shanghai: Shanghai Jiao Tong University, 2008: 96-97. ) |
