全文HTML
--> --> -->由于铝和钛的氧化热力学条件十分接近, 在高温条件下, TiAl基合金表面主要形成由TiO2和α-Al2O3混合的氧化膜, 而不是连续致密的纯α-Al2O3氧化膜. 疏松多孔的TiO2不能阻挡外部的氧原子往基质内部扩散, 从而导致氧化持续进行. 当含有大量TiO2的氧化膜与基质间的应力达到临界值时, 氧化膜极易剥落[6,7]. 因此, 在高温条件下, 促进α-Al2O3、抑制TiO2生成是改善TiAl基合金高温抗氧化性能的有效手段之一. 添加合金元素是解决该类合金氧化问题的一条有效途径[8—10].
实验方面, 朱绍祥等[11]研究了Ta对Ti-60A钛合金(一种近α型高温钛合金)抗氧化性能的影响. 结果表明, Ta可促使合金表层氧化物更致密、增加氧化膜与基质的黏附性. Izumi等[12]发现在TiAl合金中添加2%Ta(at%)可明显提高其抗氧化性能. 刘杰等[13]研究了合金元素Nb, W和Y对TiAl合金高温氧化行为的影响. 结果显示, 添加Nb, W和Y使得TiAl合金的全片层组织的片层团变小, 从而导致氧化物颗粒尺寸更小、氧化膜更致密. 杨忠波等[14,15]发现Nb掺杂主要是通过细化氧化物晶粒来改善合金抗氧化性的. Zhao等[16]发现添加Nb后氧化膜的生长速度变缓, 在氧化100 h后仍未发生氧化膜剥落现象. Zhao等[17]研究了Y含量对高Nb-TiAl合金循环抗氧化行为的影响. 结果表明, 适量的Y可以细化晶粒, 从而提高氧化膜与基质的黏附性; 而过量的Y会导致Y2O3偏聚在晶界处, 这会为氧离子提供扩散通道, 从而加速合金的内氧化. 周玉俊等[18]研究了Y对Ti-48Al-2Nb-2Cr合金高温抗氧化性能的影响, 发现Y元素可以改变氧化膜的结构, 细化氧化膜颗粒, 促使其生成连续致密的Al2O3层. 王艳晶等[19]研究了微量Y和Hf对高铌TiAl基合金高温抗氧化性的影响, 发现掺杂0.1Y(mol%)使合金抗氧化性增强, 但Hf和Y双掺杂导致合金内氧化严重. 因此, 双掺杂效应并不是简单的各个元素单掺杂效应的叠加. 董利民等[20]研究了Si对TiAl合金抗氧化性能的影响. 结果显示, Si的加入可以细化表层TiO2的颗粒, 且Si含量越高, 细化作用越明显. 肖伟豪等[21]发现Si对抗氧化性的贡献可归结于Si可降低Ti原子的活性、阻碍Ti原子向外扩散. 理论方面, 文献[22]研究表明, Nb和Si双掺杂γ-TiAl略微减弱了Ti-Al间和Al-Al间的相互作用, 明显增强了Ti-Ti间的相互作用, 从而提高Al原子的活性、降低Ti原子的活性, 有利于α-Al2O3的生成. 吴红丽等[23]进行了Nb元素影响TiAl金属间化合物键合特征的第一性原理计算, 发现Nb掺杂减弱了Ti-O间的相互作用、增大了TiO2的生成势垒, 而增强了Al-O间的相互作用, 减小了Al2O3的生成势垒, 有益于生成氧化膜并提高其致密性.
目前, 对TiAl基合金抗氧化性的研究报道主要集中在实验方面, 而理论研究方面报道相对较少, 许多微观机制问题尚有待深入探讨. 已有报道的研究成果揭示, Si掺杂或Y掺杂对提升γ-TiAl基合金高温抗氧化性能均有重要作用, 但关于Si和Y双掺杂对γ-TiAl基合金结构和性质的影响, 尤其是从微观视角进行理论探索工作尚未见报道. 本文以此类体系为研究对象, 从基于密度泛函理论的第一性原理方法出发, 研究Si和Y双掺杂γ-TiAl基合金体系的结构稳定性和抗氧化性, 旨在为改善该类合金材料的抗氧化性能提供理论依据, 进而为TiAl基合金研发和工程化提供基础数据.
2.1.结构模型
为便于叙述, 用Sp0表示纯γ-TiAl体系, 用Sd表示Si和Y双掺杂γ-TiAl体系; 下角标O、□Ti和□Al分别表示含有O原子、Ti空位和Al空位的γ-TiAl体系.3
2.1.1.纯γ-TiAl及其含氧或空位体系的结构模型
γ-TiAl为L10型面心四方结构, 如图1(a)所示, 空间群为P4/mmm, 晶格参量为a0 = b0 = 0.398 nm, c0 = 0.404 nm, α = β = γ = 90°[24]. 其最小单元结构如图1(b)所示, 对应的晶格参量为a = b = 0.283 nm, c = 0.407 nm, α = β = γ = 90°. 本文以最小结构单元为基础, 构建了2×2×2 的γ-TiAl超胞结构模型, 其中包含8个Ti原子和8个Al原子, 如图1(c)所示. 此即为体系Ti8Al8, 记为Sp0. 图 1 γ-TiAl晶胞结构模型 (a) L10型面心四方结构单元; (b)最小结构单元; (c) Sp0(Ti8Al8)结构单元
图 1 γ-TiAl晶胞结构模型 (a) L10型面心四方结构单元; (b)最小结构单元; (c) Sp0(Ti8Al8)结构单元Figure1. Structure models of γ-TiAl: (a) The L10 face-center tetragonal unit cell; (b) the least tetragonal unit cell; (c) the unit of Sp0(Ti8Al8).
仅考虑一个O原子进入Ti8Al8晶格, 形成体系Ti8Al8O, 记为Sp0-O. 由于O原子半径(rO= 0.066 nm)较小, 其在晶胞中主要占据间隙位置, 且更容易占据八面体间隙[25]. 考虑到Ti8Al8晶胞具有高度对称性, 可选择出四种典型的八面体间隙, 如图2所示. 其中, 图2(a)和图2(b)为2个Ti原子和4个Al原子形成的八面体间隙; 图2(c)和图2(d)为4个Ti原子和2个Al原子形成的八面体间隙. 因此, 对应这四种八面体间隙, 纯γ-TiAl含氧体系Ti8Al8O共有四种基本构型Sp0-Oa, Sp0-Ob, Sp0-Oc和Sp0-Od. 据此, 可计算研究含氧体系Ti8Al8O的结构与性质.
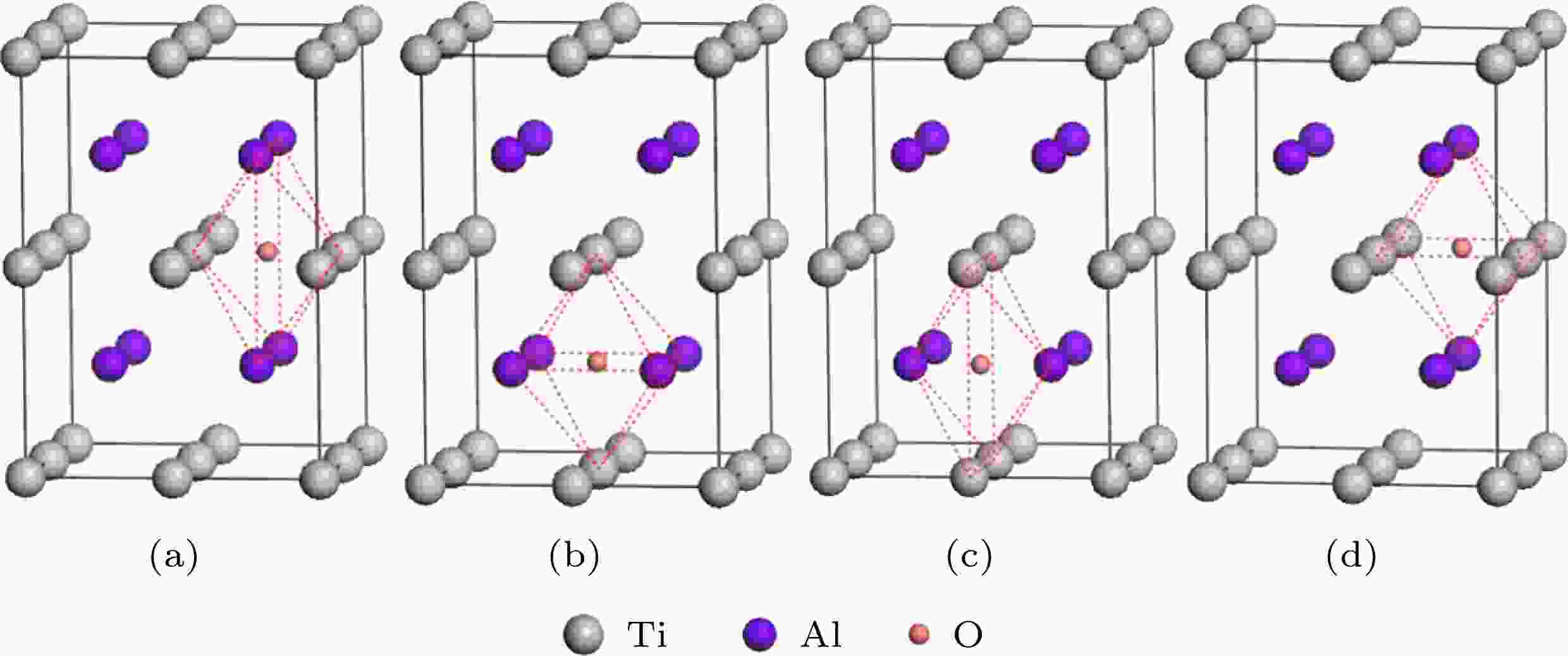 图 2 包含O原子的γ-TiAl晶胞结构模型 (a) Sp0-Oa; (b) Sp0-Ob; (c) Sp0-Oc; (d) Sp0-Od
图 2 包含O原子的γ-TiAl晶胞结构模型 (a) Sp0-Oa; (b) Sp0-Ob; (c) Sp0-Oc; (d) Sp0-OdFigure2. Structure models of γ-TiAl including O (Ti8Al8O): (a) Sp0-Oa; (b) Sp0-Ob; (c) Sp0-Oc; (d) Sp0-Od
同样, 仅考虑含有一个空位(用□标记)的情况. 对纯γ-TiAl含Ti空位体系Ti7□Al8, 记为Sp0-□Ti; 含Al空位体系Ti8Al7□, 记为Sp0-□Al. 典型构型如图3所示.
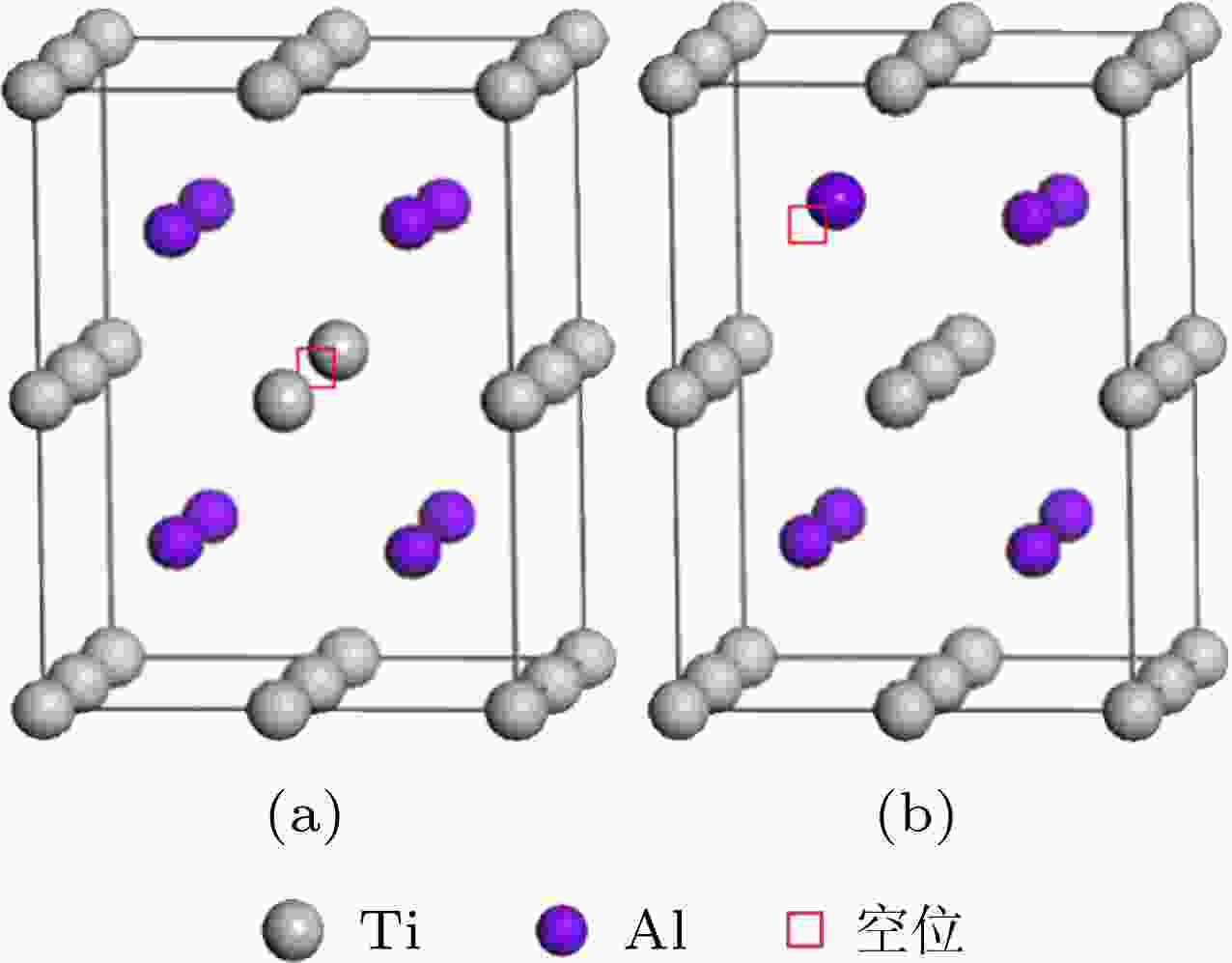 图 3 包含Ti空位或Al空位的γ-TiAl典型结构模型 (a) Sp0-□Ti (Ti7□Al8); (b) Sp0-□Al (Ti8Al7□)
图 3 包含Ti空位或Al空位的γ-TiAl典型结构模型 (a) Sp0-□Ti (Ti7□Al8); (b) Sp0-□Al (Ti8Al7□)Figure3. Typical structure models of γ-TiAl including Ti or Al vacancy: (a) Sp0-□Ti (Ti7□Al8); (b) Sp0-□Al (Ti8Al7□)
3
2.1.2.Si和Y替位双掺杂γ-TiAl及其含氧或空位体系的结构模型
对Si和Y双掺杂γ-TiAl体系, 用下角标1, 2, 3和4分别标记: Si和Y均替位Ti体系, Y替位Ti且Si替位Al体系, Si替位Ti且Y替位Al体系, Si和Y均替位Al体系. 用x标记各个体系的不同构型, 上述四种双掺杂γ-TiAl体系分别对应10, 1, 1, 1个不同的构型, 双掺杂γ-TiAl含氧体系分别对应10, 3, 3, 3个不同的构型, 双掺杂γ-TiAl含Ti空位体系分别对应48, 5, 5, 6个不同的构型, 双掺杂γ-TiAl含Al空位体系分别对应10, 5, 5, 3个不同的构型. 图4给出了Si和Y双掺杂γ-TiAl体系的4个典型构型, 包括Sd1x(Ti6SiYAl8), Sd2(Ti7YAl7Si), Sd3(Ti7SiAl7Y)和Sd4(Ti8Al6SiY).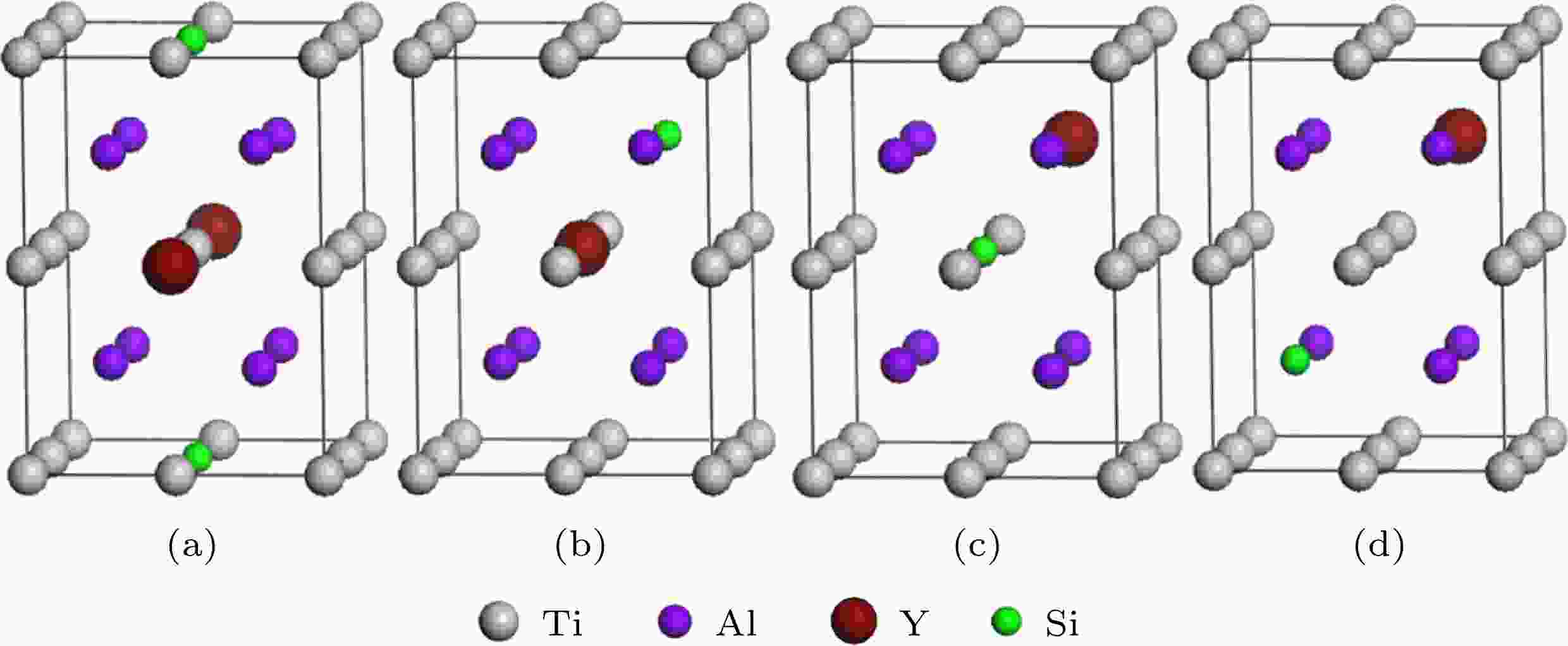 图 4 Si和Y替位双掺杂γ-TiAl体系的典型结构模型 (a) Sd1x (Ti6SiYAl8); (b) Sd2 (Ti7YAl7Si); (c) Sd3 (Ti7SiAl7Y); (d) Sd4(Ti8Al6SiY)
图 4 Si和Y替位双掺杂γ-TiAl体系的典型结构模型 (a) Sd1x (Ti6SiYAl8); (b) Sd2 (Ti7YAl7Si); (c) Sd3 (Ti7SiAl7Y); (d) Sd4(Ti8Al6SiY)Figure4. Typical structure models of Si and Y co-doping γ-TiAl: (a) Sd1x (Ti6SiYAl8); (b) Sd2 (Ti7YAl7Si); (c)Sd3 (Ti7SiAl7Y); (d) Sd4(Ti8Al6SiY)
Si和Y双掺杂γ-TiAl含氧体系包括Sd1x-Od (Ti6SiYAl8O), Sd2x-Od(Ti7YAl7SiO), Sd3x-Od (Ti7SiAl7YO)和Sd4x-Od(Ti8Al6SiYO)等, 典型构型如图5所示.
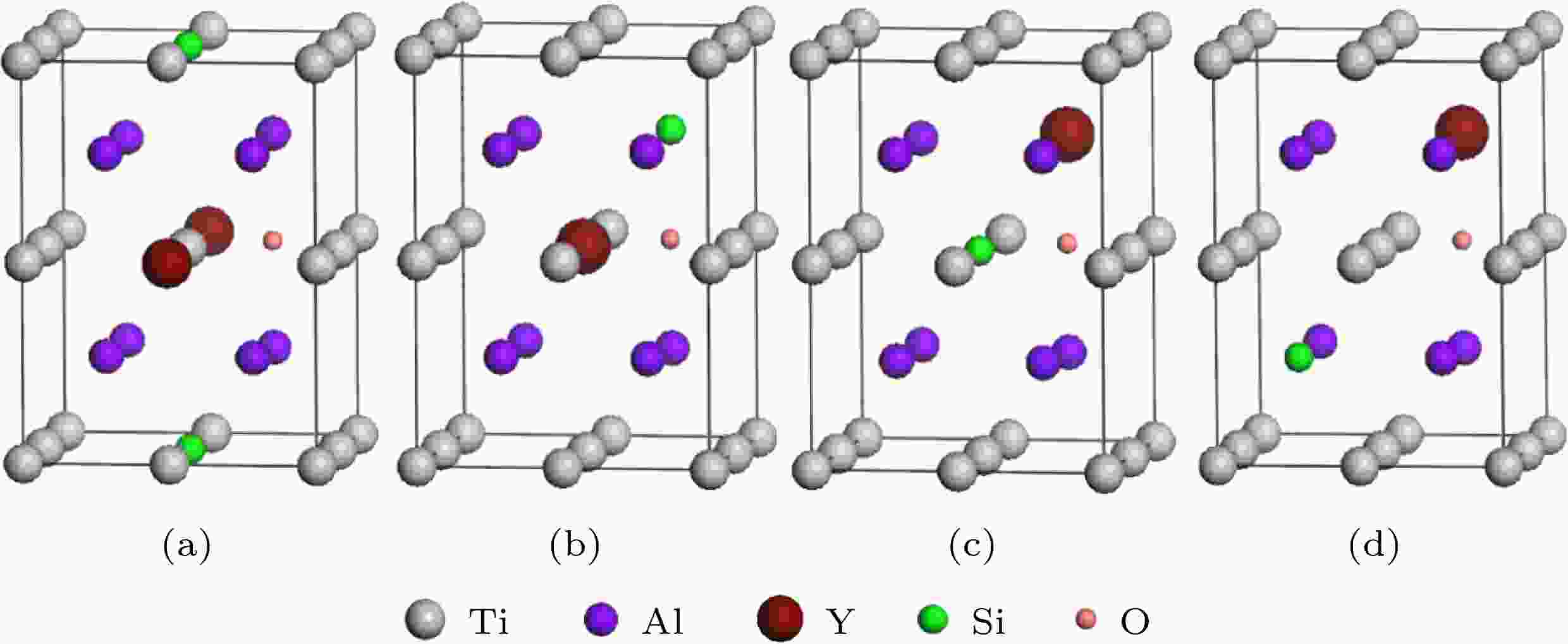 图 5 Si和Y替位双掺杂γ-TiAl含氧体系的典型结构模型 (a) Sd1x-Od (Ti6SiYAl8O); (b) Sd2x-Od (Ti7YAl7SiO); (c) Sd3x-Od (Ti7SiAl7YO); (d) Sd4x-Od(Ti8Al6SiYO)
图 5 Si和Y替位双掺杂γ-TiAl含氧体系的典型结构模型 (a) Sd1x-Od (Ti6SiYAl8O); (b) Sd2x-Od (Ti7YAl7SiO); (c) Sd3x-Od (Ti7SiAl7YO); (d) Sd4x-Od(Ti8Al6SiYO)Figure5. Typical structure models of Si and Y co-doping γ-TiAl including O: (a) Sd1x-Od (Ti6SiYAl8O); (b) Sd2x-Od (Ti7YAl7SiO); (c) Sd3x-Od (Ti7SiAl7YO); (d) Sd4x-Od(Ti8Al6SiYO)
Si和Y双掺杂γ-TiAl含Ti空位体系包括Sd1x-□Ti(Ti5SiY□Al8), Sd2x-□Ti(Ti6Y□Al7Si), Sd3x-□Ti(Ti6Si□Al7Y), Sd4x-□Ti(Ti7□Al6SiY); Si和Y替位双掺杂γ-TiAl含Al空位体系包括Sd1x-□Al(Ti6SiYAl7□), Sd2x-□Al(Ti7YAl6Si□), Sd3x-□Al(Ti7SiAl6Y□), Sd4x-□Al(Ti8Al5SiY□)等, 其典型结构模型如图6所示.
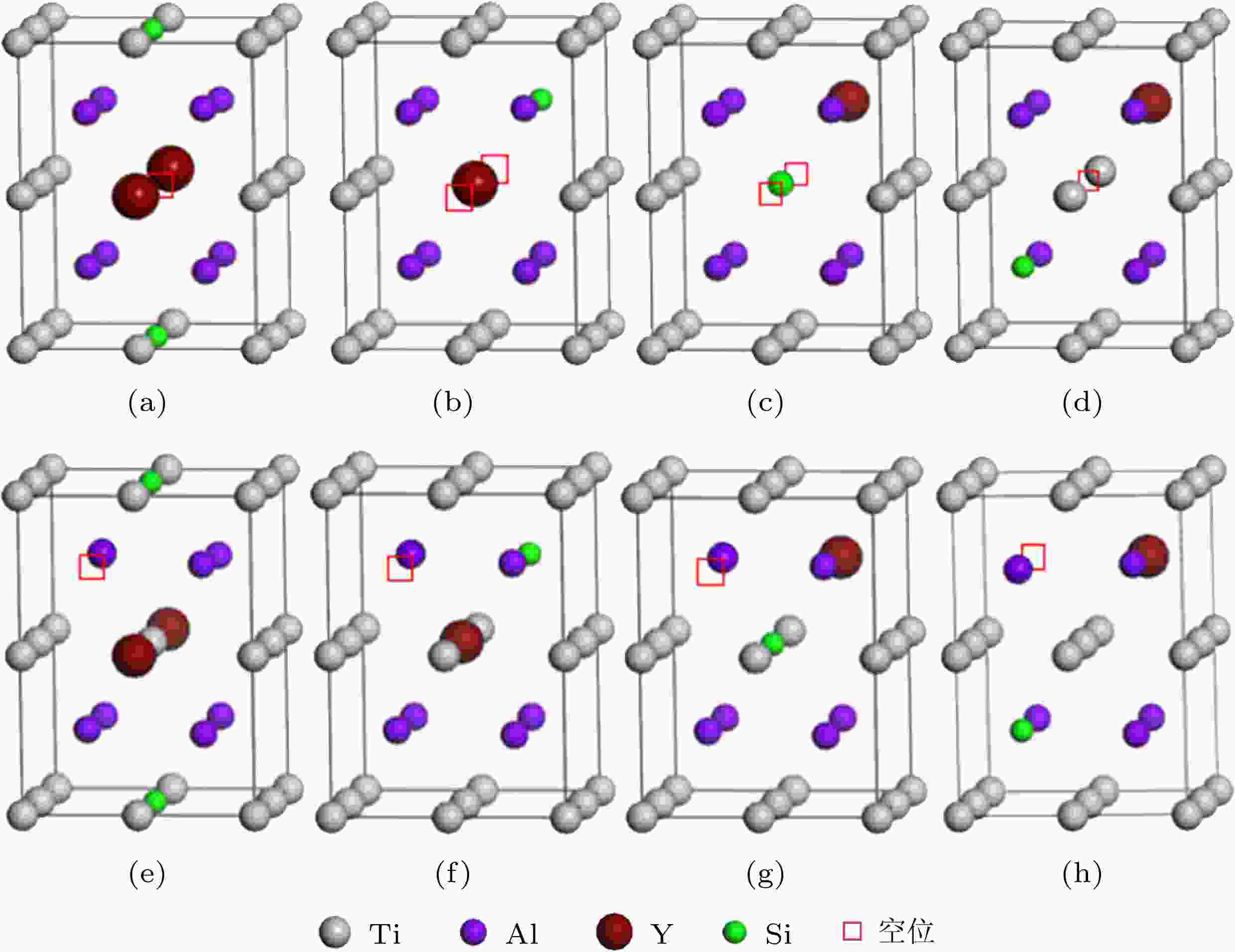 图 6 Si和Y替位双掺杂γ-TiAl含空位体系的典型结构模型 (a) Sd1x-□Ti (Ti5SiY□Al8); (b) Sd2x-□Ti (Ti6Y□Al7Si); (c) Sd3x-□Ti(Ti6Si□Al7Y); (d) Sd4x-□Ti(Ti7□Al6SiY); (e) Sd1x-□Al (Ti6SiYAl7□); (f) Sd2x-□Al (Ti7YAl6Si□); (g) Sd3x-□Al(Ti7SiAl6Y□); (h) Sd4x-□Al(Ti8Al5SiY□)
图 6 Si和Y替位双掺杂γ-TiAl含空位体系的典型结构模型 (a) Sd1x-□Ti (Ti5SiY□Al8); (b) Sd2x-□Ti (Ti6Y□Al7Si); (c) Sd3x-□Ti(Ti6Si□Al7Y); (d) Sd4x-□Ti(Ti7□Al6SiY); (e) Sd1x-□Al (Ti6SiYAl7□); (f) Sd2x-□Al (Ti7YAl6Si□); (g) Sd3x-□Al(Ti7SiAl6Y□); (h) Sd4x-□Al(Ti8Al5SiY□)Figure6. Typical structure models of Si and Y co-doping γ-TiAl including vacancy: (a)Sd1x-□Ti (Ti5SiY□Al8); (b) Sd2x-□Ti (Ti6Y□Al7Si); (c) Sd3x-□Ti(Ti6Si□Al7Y); (d) Sd4x-□Ti(Ti7□Al6SiY); (e) Sd1x-□Al (Ti6SiYAl7□); (f) Sd2x-□Al (Ti7YAl6Si□); (g) Sd3x-□Al(Ti7SiAl6Y□); (h) Sd4x-□Al(Ti8Al5SiY□)
依据上述结构模型, 对各个体系的构型进行结构弛豫和性质的计算研究.
2
2.2.计算研究方案
采用基于密度泛函理论的第一性原理方法, 并结合物理与化学理论方法进行研究. 用超软赝势描述离子实与价电子之间的相互作用势. 使用高性能计算机集群, 用Materials Studio 6.0软件包中的Visualizer模块[26]完成模型构建, 用CASTEP(Cambridge serial total energy package)模块[27]进行结构与性能的计算与分析.首先设计几种计算方案, 采用拟牛顿算法, 对Sp0(Ti8Al8)体系进行几何结构优化, 直至达到收敛标准. 将优化得到的几何结构参量与已经报道的实验研究结果进行对比, 据此选取合适的计算方案. 其中平面波截断能设置为330 eV, 布里渊区k点设置为4 × 4 × 2, 采用Pulay密度混合法进行自洽计算. 迭代计算的收敛标准为: 原子的能量增量2.0 × 10–5 eV/atom; 原子作用力误差0.05 eV/nm; 位移偏差0.0002 nm; 应力偏差0.1 GPa.
采用同种计算研究方案, 对纯γ-TiAl含氧体系、含空位体系, 各个Si和Y替位双掺杂γ-TiAl体系及其含氧体系、含空位体系的几何结构进行优化, 直至达到收敛标准; 计算各个平衡体系的总能量, 弹性常数, 间隙O原子的形成能, Ti空位和Al空位的形成能等, 对各个体系的稳定性和抗氧化性进行分析讨论.
2
3.1.Si和Y替位双掺杂体系的形成能与能量稳定性
材料的能量稳定性可以用平均形成能表征[28]. 对于任意多原子体系, 原子平均形成能可以表示为| 体系 | 能量性质 | |
| Et /eV | E f/eV | |
| Sp0 | –13283.2619 | –0.3579 |
| Sd17 | –10375.5782 | –0.2448 |
| Sd19 | –10375.3125 | –0.2282 |
| Sd2 | –11923.1797 | –0.3078 |
| Sd3 | –11921.0891 | –0.1771 |
| Sd4 | –13468.5526 | –0.2315 |
表1纯γ-TiAl体系与Si和Y替位双掺杂γ-TiAl体系的能量性质
Table1.Energy properties of pure γ-TiAl and Si and Y co-doping γ-TiAl systems.
由表1可知, Si和Y替位双掺杂前后体系的原子平均形成能均为负值, 理论预报它们均具有良好的能量稳定性, 可以实验制备并稳定存在. 各个Si和Y替位双掺杂体系的平均形成能较掺杂前均升高, 即能量稳定性降低.
通过对比可知,



2
3.2.Si和Y替位双掺杂体系的弹性常数与力学稳定性
材料的弹性常数是标志其力学性质的基础数据, 而材料的力学稳定性也可由Born-Huang判据[29], 依据弹性常数的相互关系进行判定.对于四方晶系, 其弹性常数有6个独立变量, 即C11, C12, C13, C33, C44和C66. 四方晶系的力学稳定性判据为:
| 体系 | C11/GPa | C12/GPa | C13/GPa | C33/GPa | C44/GPa | C66/GPa |
| Sp0 | 232.2438 | 39.8470 | 69.3592 | 196.4413 | 112.3486 | 44.8147 |
| Sd11 | 130.8671 | 75.6434 | 87.7505 | 134.2535 | 70.0558 | 46.6357 |
| Sd13 | 136.8296 | 75.1812 | 86.9261 | 134.1158 | 64.9601 | 49.0225 |
| Sd14 | 180.5075 | 43.1529 | 81.6884 | 138.5193 | 73.0642 | 19.7364 |
| Sd15 | 136.6952 | 74.6364 | 84.6822 | 128.5797 | 67.3934 | 47.4253 |
| Sd16 | 160.1225 | 90.0601 | 87.6092 | 137.2518 | 106.8941 | 43.0277 |
| Sd19 | 130.8850 | 74.3862 | 78.7846 | 125.4646 | 68.9906 | 56.7747 |
| Sd110 | 132.4566 | 95.9060 | -40.8881 | 351.4524 | 24.8135 | 42.5965 |
| Sd4 | 174.4526 | 59.4503 | 76.4982 | 151.9303 | 82.9168 | 12.5223 |
表2纯γ-TiAl体系与Si和Y替位双掺杂γ-TiAl体系中四方晶系的弹性常数
Table2.Elastic constants of tetragonal systems in pure γ-TiAl and Si and Y co-doping γ-TiAl systems.
对于正交晶系, 其弹性常数有9个独立变量, 即C11, C12, C13, C22, C23, C33, C44, C55和C66. 正交晶系的力学稳定性判据为:
| 体系 | C11/GPa | C12/GPa | C13/GPa | C15/GPa | C22/GPa | C23/GPa | C25/GPa |
| Sd17 | 174.0489 | 51.0128 | 78.8477 | – | 178.6799 | 73.6936 | – |
| Sd2 | 177.5408 | 69.1504 | 69.7969 | –3.6774 | 172.7134 | 65.2400 | –1.6610 |
| Sd3 | 158.9597 | 58.6004 | 72.7099 | –10.1161 | 160.3606 | 73.2300 | –0.1101 |
| 体系 | C33/GPa | C35/GPa | C44/GPa | C46/GPa | C55/GPa | C66/GPa | |
| Sd17 | 117.2748 | – | 59.8220 | – | 64.1452 | 10.4758 | |
| Sd2 | 170.8100 | –1.4732 | 77.8416 | –1.2719 | 78.4798 | 38.6156 | |
| Sd3 | 139.6061 | –1.4377 | 67.2411 | 0.7657 | 67.6317 | 26.4129 |
表3Si和Y替位双掺杂γ-TiAl体系Sd17, Sd2和Sd3的弹性常数
Table3.Elastic constants of Si and Y co-doping γ-TiAl systems Sd17, Sd2 and Sd3.
对于单斜晶系, 其弹性常数有13个独立变量, 即C11, C12, C13, C15, C22, C23, C25, C33, C35, C44, C46, C55和C66. 单斜晶系的力学稳定性判据为:
2
3.3.Si和Y替位双掺杂体系的形成能对抗氧化性的影响
γ-TiAl基合金材料表面氧化膜的主要成分是TiO2和α-Al2O3, 其中TiO2质地疏松且易于剥落, 它的存在不利于抑制O原子往基质内部扩散; α-Al2O3连续致密且能够与基质紧密结合, 它能够有效抑制O原子往基质内部扩散. 因此, 改善γ-TiAl基合金材料的抗氧化性, 主要思路就是有效促进α-Al2O3、抑制TiO2的生成. 影响γ-TiAl基合金材料表面区域发生氧化的主要因素包括O原子向基质内部的扩散和Ti原子、Al原子向基质表面的扩散. 氧原子半径较小往往是通过间隙通道在基质内部运动的, 而金属原子的扩散则主要是通过空位机制实现的. 研究Si和Y替位双掺杂γ-TiAl体系的抗氧化性, 首先就需要研究其含氧体系、含空位体系的结构和性质.3
3.3.1.间隙O原子的形成能对抗氧化性的影响
1)纯和双掺杂γ-TiAl体系中间隙O原子的位置对能量性质的影响在TiAl合金高温氧化的过程中, 材料表面积累的O原子(离子)会通过间隙通道, 不断扩散到基质内部, 从而发生进一步氧化.
为了探索间隙O原子在γ-TiAl体系中间隙位置的差异性, 本文计算了四种构型的纯γ-TiAl含氧体系的总能量和原子平均形成能, 如表4所列, 其中a, b, c和d分别代表O原子的间隙位置.
| 体系 | 能量性质 | |
| Et /eV | E f /eV | |
| Sp0 | –13283.2619 | –0.3579 |
| Sp0-Oa | –13718.1429 | –0.0716 |
| Sp0-Ob | –13720.0413 | –0.1832 |
| Sp0-Oc | –13720.6086 | –0.2166 |
| Sp0-Od | –13720.9863 | –0.2388 |
表4纯γ-TiAl体系及其含氧体系的能量性质
Table4.Energy properties of pure γ-TiAl and the systems including O.
由表4可知, 纯γ-TiAl体系Sp0的能量稳定性最好. 加入间隙O原子后, 纯γ-TiAl含氧体系的原子平均形成能均升高、能量稳定性降低. 当O原子位于八面体间隙a时, 该含氧体系的原子平均形成能最高; 位于八面体间隙d时, 该含氧体系的原子平均形成能最低. 这说明O原子在晶体内扩散过程中会优先占据间隙位置d, 或者说对于纯γ-TiAl体系Sp0, O原子有最大概率在八面体间隙位置d与基质结合.
为了更定量化, 对于Si和Y替位双掺杂γ-TiAl含氧体系, 定义间隙O原子的形成能为[25]
间隙O原子在含氧体系中的形成能越高, 其进入γ-TiAl基质中扩散的难度就越大[25]. 相应地, 不含氧的基质材料的抗氧化性越好. 因此, O原子在含氧体系中的扩散能力与相应的基质材料的抗氧化能力是负相关的. 对于体系Sp0-Oa, O原子的形成能E f(Oa)= 4.5099 eV; 而对体系Sp0-Od, E f(Od)=1.6665 eV. 即E f(Oa)明显大于E f(Od). 这表明, 间隙O原子在Sp0-Oa中扩散的难度比在Sp0-Od中大. 即在四个纯γ-TiAl含氧体系中, O原子位于八面体间隙a时, Sp0的抗氧化性能最好, O原子位于八面体间隙d时, Sp0的抗氧化性能最差.
我们以体系Sd11和Sd41为例, 比较了O原子在含氧体系中的形成能与间隙位置的关系. 计算结果表明, 体系Sd11-Od和Sd41-Od中, O原子的形成能分别为1.8160和0.3252 eV; 而在体系Sd11-Oa和Sd41-Oa中, O原子形成能分别为1.7961和0.3259 eV, 形成能差值分别为–0.0199和0.0007 eV. 而在体系Sp0中, O原子的形成能差值则高达2.8434 eV. 这表明, O原子在γ-TiAl晶胞中的间隙位置对体系Sp0的能量性质影响较大; 而对体系Sd11和Sd41的能量性质影响很小, 几乎可以忽略. 因此, 在后续有关含氧体系的计算分析中, 主要考虑将O原子置于纯γ-TiAl体系、Si和Y替位双掺杂γ-TiAl体系的八面体间隙d处. 在此基础上, 计算研究各种含氧体系的结构和能量性质, 并且与纯γ-TiAl及其含氧体系的相应性质进行对比, 重点是间隙O原子的形成能.
2) Si和Y替位双掺杂γ-TiAl含O体系的能量性质
表5列出了Si和Y替位双掺杂γ-TiAl含氧体系中O原子的形成能.
| 体系 | 能量性质 | ||
| Et(SdO)/eV | Et (Sd)/eV | E f(O)/eV | |
| Sp0-Od | –13720.9863 | –13283.2619 | 1.6665 |
| Sd11-Od | –10812.9929 | –10375.4180 | 1.8160 |
| Sd13-Od | –10813.0355 | –10375.3811 | 1.7365 |
| Sd14-Od | –10813.1059 | –10375.4175 | 1.7025 |
| Sd15-Od | –10813.0129 | –10375.3988 | 1.7768 |
| Sd16-Od | –10813.0989 | –10375.3983 | 1.6903 |
| Sd17-Od | –10813.1600 | –10375.5782 | 1.8091 |
| Sd19-Od | –10813.0084 | –10375.3125 | 1.6950 |
| Sd110-Od | –10813.0341 | –10375.3121 | 1.6689 |
| Sd21-Od | –12361.2419 | –11923.1797 | 1.3287 |
| Sd22-Od | –12361.1930 | –11923.1797 | 1.3776 |
| Sd23-Od | –12361.2834 | –11923.1797 | 1.2872 |
| Sd31-Od | –12359.6285 | –11921.0891 | 0.8515 |
| Sd32-Od | –12360.0430 | –11921.0891 | 0.4370 |
| Sd33-Od | –12359.9518 | –11921.0891 | 0.5282 |
| Sd41-Od | –13907.6183 | –13468.5526 | 0.3252 |
| Sd42-Od | –13906.9550 | –13468.5526 | 0.9885 |
| Sd43-Od | –13906.7798 | –13468.5526 | 1.1637 |
表5Si和Y替位双掺杂γ-TiAl含氧体系中间隙O原子的形成能
Table5.Formation energies of interstitial O atoms in Si and Y co-doping γ-TiAl systems.
为直观起见, 将表5中各个间隙O原子的形成能绘于图7中. 由表5和图7可知, 与Sp0-Od相比, 体系Sd1x-Od中O原子的形成能均升高, 也就是O原子进入基质材料扩散的难度增大. 即Si原子和Y原子同时替位Ti原子形成的四元体系可以在一定程度上抑制间隙O原子在其中的扩散. 在体系Sd2x-Od, Sd3x-Od和Sd4x-Od中, 间隙O原子的形成能均降低. 这也就意味着, 体系Sd2, Sd3和Sd4的构型及性质不利于改善材料的抗氧化性能.
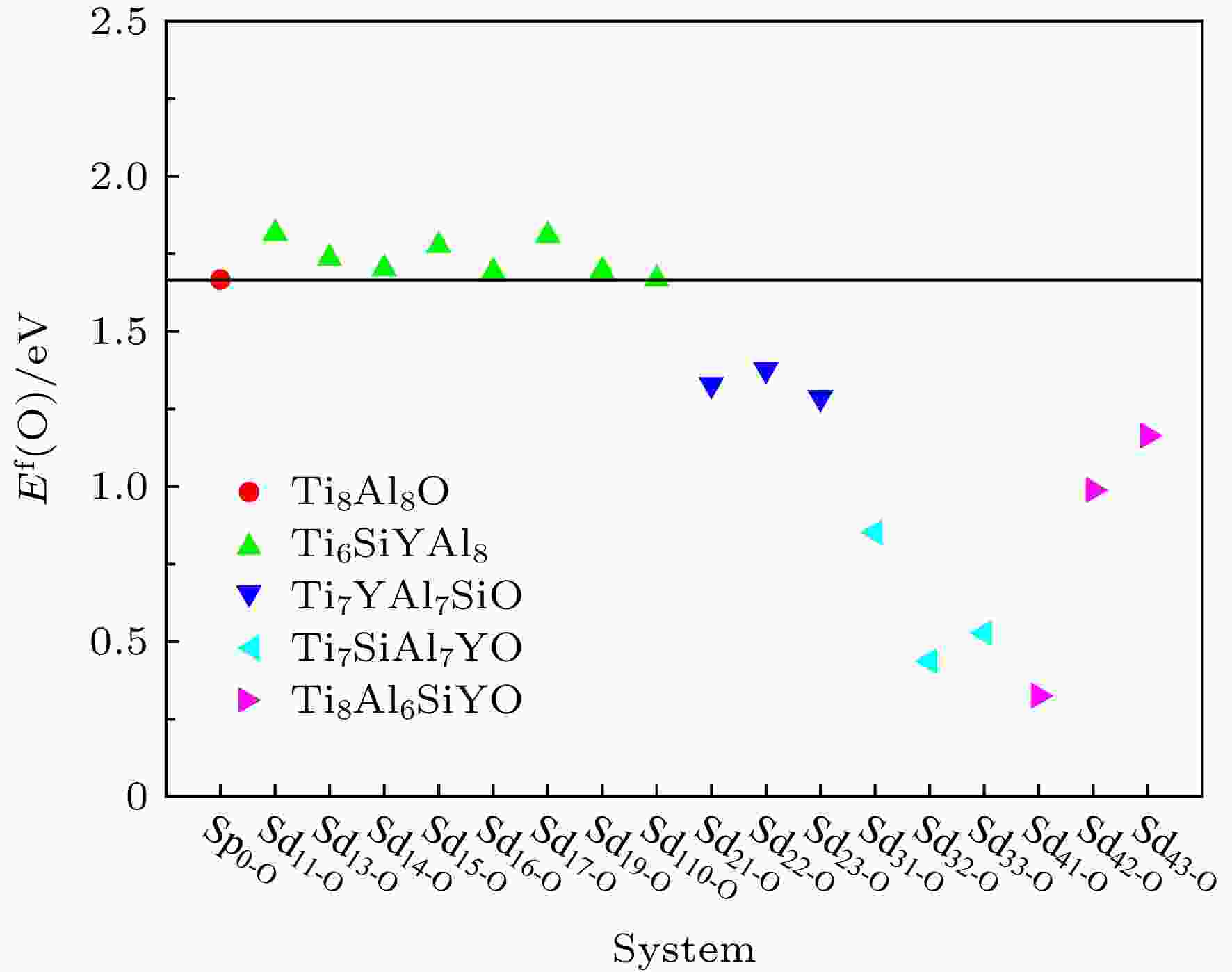 图 7 Si和Y替位双掺杂γ-TiAl含氧体系中间隙O原子的形成能
图 7 Si和Y替位双掺杂γ-TiAl含氧体系中间隙O原子的形成能Figure7. Formation energies of interstitial O atoms in the Si and Y co-doping γ-TiAl systems.
3
3.3.2.Ti空位和Al空位的形成能对抗氧化性的影响
空位是与内氧化问题密切相关的另一类重要缺陷. 在高温合金氧化过程中, 材料内部的金属原子会通过空位的移动(或者说是扩散)不断扩散到基质表面, 从而与O原子结合, 发生进一步氧化. 在γ-TiAl基合金中主要存在Ti空位和Al空位. Ti空位形成能越高, Ti原子通过空位机制扩散到材料表面与O原子生成TiO2的难度越大, 这就不利于TiO2的生成. Al空位形成能越低, Al原子扩散到材料表面与O原子生成α-Al2O3的难度越小, 这有利于α-Al2O3的生成, 从而增大α-Al2O3在氧化膜中所占的比重, 增加氧化膜的致密度、连续性, 进而改善材料的抗氧化性能. Ti(或Al)空位的形成能可表示为[25]| 体系 | Et (Sd)/eV | Et (Sd□Al)/eV | Et (Sd□Ti)/eV | E f (□Al)/eV | E f (□Ti)/eV |
| Sp0-□ | –13283.2619 | –13224.0362 | –11678.3061 | 2.6764 | 1.8132 |
| Sd11-□ | –10375.4180 | –10317.9824 | –8770.2288 | 0.8863 | 2.0466 |
| Sd13-□ | –10375.3811 | –10317.9645 | –8770.1941 | 0.8673 | 2.0444 |
| Sd14-□ | –10375.4175 | –10317.9637 | –8770.2884 | 0.9045 | 1.9865 |
| Sd15-□ | –10375.3988 | –10317.9620 | –8770.2113 | 0.8875 | 2.0449 |
| Sd16-□ | –10375.3983 | –10317.9032 | –8770.2649 | 0.9098 | 1.9908 |
| Sd17-□ | –10375.5782 | –10317.4973 | –8770.0900 | 1.5316 | 2.3456 |
| Sd19-□ | –10375.3125 | –10318.4246 | –8770.2557 | 0.3386 | 1.9143 |
| Sd110-□ | –10375.3121 | –10318.0212 | –8770.2609 | 0.7416 | 1.9086 |
| Sd2-□ | –11923.1797 | –11865.3646 | –10317.9810 | 1.2658 | 2.0561 |
| Sd3-□ | –11921.0891 | –11865.3095 | –10317.6100 | –0.7697 | 0.3365 |
| Sd4-□ | –13468.5526 | –13409.4369 | –11865.3562 | 2.5664 | 0.0538 |
表6Si和Y双掺杂γ-TiAl含空位体系中Ti空位和Al空位的形成能
Table6.Formation energies of Ti and Al vacancies in Si and Y co-doping γ-TiAl systems.
为了便于直观分析, 将表6中各个Ti空位和Al空位的形成能绘于图8中. 由表6和图8可知, 对于纯γ-TiAl体系, E f(□Al) > E f(□Ti), 即Ti空位比Al空位更容易进入基质材料进行扩散. 也就表明, 在材料表面, TiO2比α-Al2O3更容易生成. 与体系Sp0-□相比, Si和Y双掺杂后形成的所有体系中Al空位的形成能均降低. 这表明, Al空位进入Si和Y替位双掺杂γ-TiAl体系中扩散的难度明显减小, 这有利于生成α-Al2O3.
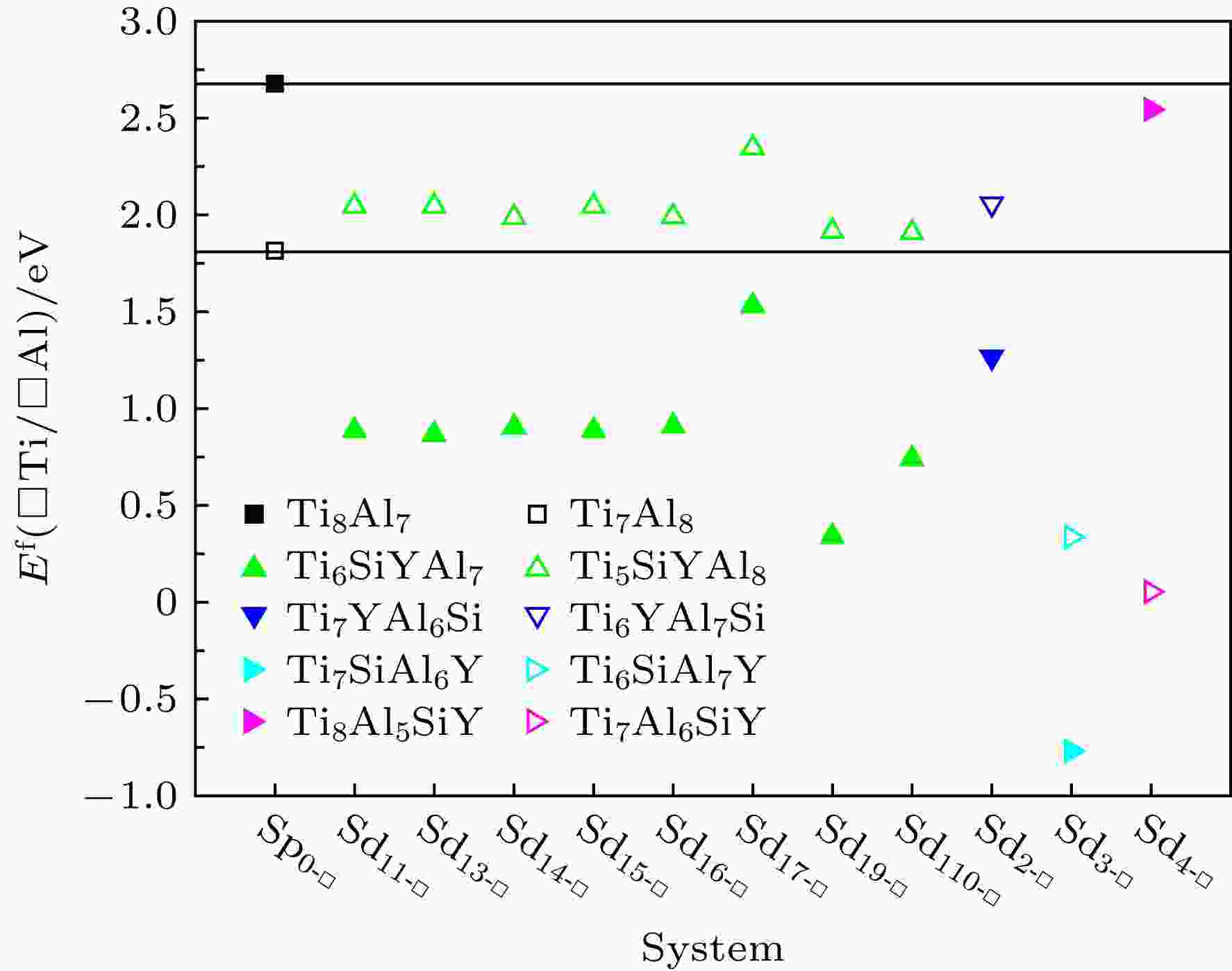 图 8 Si和Y双掺杂γ-TiAl含空位体系中Ti空位和Al空位的形成能
图 8 Si和Y双掺杂γ-TiAl含空位体系中Ti空位和Al空位的形成能Figure8. Formation energies of Ti and Al vacancies in Si and Y co-doping γ-TiAl systems.
与体系Sp0-□相比, 体系Sd1x-□和Sd2x-□中Ti空位的形成能均升高. 这表明, Ti空位进入Si和Y替位双掺杂γ-TiAl体系中扩散的难度增大, TiO2的生成受到抑制. 并且, 体系Sd1x-□, Sd2-□和Sd3-□中Ti空位的形成能均高于Al空位的形成能, 即在这类基质材料中Al空位易于扩散. 也就是说Al原子更易于通过空位机制移动扩散到材料表面、与O原子结合. 这样, 在材料表面生成α-Al2O3比生成TiO2更容易. 这表明, 体系Sd1x, Sd2和Sd3的构型及性质是有助于改善材料的抗氧化性的. 这与Nb掺杂γ-TiAl体系中替位Ti的情况相似[25]. 体系Sd4-□中Al空位的形成能为2.5664 eV, 与体系Sp0-□中Al空位的形成能极为接近; 而其中Ti空位的形成能仅为0.0538 eV, 远低于体系Sp0-□中Ti空位的形成能1.8132 eV. 这显示, 体系Sd4-□的构型及其性质对于提高抗氧化性是极为不利的. 为改善γ-TiAl基合金的抗氧化性能, 应尽量控制避免体系Sd4构型的生成.
综上所述, 可将间隙O原子的形成能升高、Al空位的形成能明显降低和Ti空位的形成能明显升高作为判定材料抗氧化性得以改善的三个判据. 即要改善γ-TiAl基合金的抗氧化性能, 必须保证材料满足第一个判据, 且满足第二个判据或第三个判据. 综合分析可以看出, 满足力学稳定性条件的Sd1x系列的各个构型均同时满足这三个判据; 体系Sd2同时满足后两个判据; 体系Sd3只满足第二个判据; 体系Sd4不满足任何一个判据. 总体来说, 预测Si和Y替位双掺杂能够改善γ-TiAl体系的抗氧化性. 这可与Si掺杂TiAl合金和Y掺杂TiAl合金得到的实验结果进行综合比较. 董利民等[20]实验研究发现Si的加入使TiAl合金表层形成细小致密的氧化物. 他们认为, 连续致密的Al2O3使氧元素向内扩散速率降低, 从而降低了合金氧化的速率. 肖伟豪等[21]报道, 在TiAl中掺杂10%的Si后, 其表面可生成连续致密的Al2O3保护膜, 且Si与Ti的良好亲和力使其可以有效降低Ti离子活度、阻碍Ti离子向外扩散. Zhao等[17]通过实验证实适量浓度的Y可以抑制TiO2、促进Al2O3生成, 从而提高合金的抗氧化性. 周玉俊等[18]指出Y的添加促进了氧化层中形成极具保护性的致密Al2O3层, 它抑制了氧向基体内扩散以及Ti离子外扩散生成TiO2. 根据本文的理论结果也可对双掺杂效应并非简单的各个合金元素单掺杂效应的叠加给出合理解释. 为了使Si和Y替位双掺杂改善γ-TiAl基合金抗氧化性能的效应更为显著, 需要调控制备条件, 使合金元素Si和Y同时替位Ti, 从而有较大比例的Sd1x系列(Ti6SiYAl8)构型生成.
1)各个双掺杂γ-TiAl体系都具有良好的能量稳定性, 理论预报它们可以实验制备并稳定存在;
2)除体系Sd12和Sd18(Ti6SiYAl8)外, 各个双掺杂γ-TiAl体系的弹性常数均满足力学稳定性条件;
3)对于满足力学稳定性条件的Si和Y替位双掺杂γ-TiAl体系, 综合间隙O原子、Ti空位和Al空位形成能的分析结果, 理论预报: Si和Y均替位Ti生成的体系Ti6SiYAl8, 对改善γ-TiAl基合金的抗氧化性最为有利; Y替位Ti且Si替位Al生成的体系Ti7YAl7Si、Si替位Ti且Y替位Al生成的体系Ti7SiAl7Y, 对改善γ-TiAl基合金的抗氧化性具有不确定性影响; Si和Y均替位Al生成的体系Ti8Al6SiY, 不利于改善γ-TiAl基合金的抗氧化性. 在实验中应调控制备条件, 使Si和Y同时替位Ti, 以生成较大占比的Sd1x系列(Ti6SiYAl8)构型, 使合金材料总体上抑制Ti原子向外扩散和间隙O原子向内部扩散; 有利于Al原子向外的扩散, 从而促进合金表面易于生成致密的α-Al2O3占主导成分的氧化膜.
