0 引言
【研究意义】猕猴桃果实耐贮性及其贮藏品质都与采后生理变化密切相关,特别是采后果实的乙烯代谢和呼吸作用。这是由于乙烯促进了果实的成熟、衰老,而呼吸作用则为果实采后正常生理代谢提供了能量及中间产物[1]。乙烯是植物体内的重要激素,参与植物生长发育和衰老的整个过程,包括果实的后熟软化[2]。在植物体内乙烯的合成途径为蛋氨酸(Met)→S-腺苷蛋氨酸(SAM)→1-氨基环丙烷-1-羧酸(ACC)→乙烯,SAM合成酶催化蛋氨酸合成SAM,ACC合成酶(ACS)催化SAM生成ACC,ACC在ACC氧化酶(ACO)作用下最终生成乙烯[3]。猕猴桃属于典型的呼吸跃变型果实,对乙烯极为敏感,采后极易软化;如何抑制乙烯合成、降低果实呼吸速率是猕猴桃贮藏保鲜的核心所在。膨大剂俗称“膨大素”、“大果灵”,化学名称为细胞激动素。常用膨大剂的有效成分为氯吡脲(CPPU),可以促进细胞分裂、分化、扩大和细胞形成[4],从而具有促进果实膨大的作用。膨大剂被广泛应用于柿子、甜瓜、苦瓜、猕猴桃、葡萄、番茄、苹果、梨、西瓜等果蔬中[5]。猕猴桃生产中为了增加单果重和亩产量,在幼果膨大期普遍使用较高浓度CPPU处理,但这会显著增加采后果实的呼吸速率和乙烯释放量,加快果实后熟和软化,缩短贮藏时间,为猕猴桃采后贮藏保鲜带来了极大地负面效应。O3在杀菌、消毒过程中只产生无毒无害的氧化物,并最终被还原为氧气,不存在二次污染,2001年被美国FDA列为可直接和食品接触的添加剂。O3因具有杀菌、抑制和消除乙烯、减缓果实的呼吸作用而在果蔬贮藏保鲜中逐渐得到应用[6];O3还能调节果蔬新陈代谢,延长果实的贮藏期,减少果实软化速度,抑制菌丝的生长等[7,8,9,10]。【前人研究进展】何靖柳等[11]对红阳猕猴桃进行不同保鲜处理,研究其贮藏期生理及品质变化的影响,结果表明,O3处理后贮藏至120 d的猕猴桃,其呼吸强度、硬度、腐烂率、可溶性固形物等指标均优于其他处理。李子龙等[12]对猕猴桃进行臭氧处理,探究臭氧对其酶活性的影响,试验结果表明O3浓度为6 g·L-1可以抑制猕猴桃果汁PPO酶的活性,可以防止褐变。HAN等[13]对桑果进行O3处理,发现臭氧能有效降低其呼吸速率和乙烯释放量和多酚氧化酶。【本研究切入点】虽然已经有较多的猕猴桃贮藏的研究报道,但是并未见O3处理对猕猴桃乙烯代谢途径的相关研究。【拟解决的关键问题】本文以生长期使用CPPU的猕猴桃为试材,探究O3处理能否有效减轻因使用20 mg·L-1 CPPU对猕猴桃果实乙烯代谢带来的负面影响,为O3保鲜技术及其在猕猴桃贮藏保鲜上的应用提供科学依据。1 材料与方法
1.1 材料与试剂
猕猴桃秦美品种采自陕西省杨凌示范区(管理良好的果园)。在猕猴桃盛花期后28 d,用20 mg·L-1 CPPU进行蘸果处理,对照用清水蘸果处理(CPPU对照组CK);当果实生长至可溶性固形物含量达到6.0%—6.5%时采收。剔除有机械损伤、病斑及畸形果实,预冷24 h后入库。氯吡脲(CPPU),四川省兰月科技有限公司;HgCl2,山东西亚化学股份有限公司;NaClO,广州华大化学试剂有限公司;PVP,上海蓝季科技发展有限公司;NaHCO3,广东光华科技股份有限公司;FeSO4,西陇化工股份有限公司;ACC、交联聚乙烯吡咯烷酮(PVPP)、二硫苏糖醇(DTT)、SAM、Tris、抗坏血酸钠、蛋氨酸均为北京索莱宝科技有限公司。
1.2 仪器与设备
GC-14C气相色谱,日本岛津;LC-20A高效液相色谱,日本岛津;HC-3018R高速冷冻离心机,安徽中科中佳科学仪器有限公司;有毒有害气体检测报警仪,深圳市瑞凯雷科技有限公司;O3发生器,青岛欣美净化设备有限公司。1.3 方法
1.3.1 处理分组 将预冷后的猕猴桃装于网眼塑料筐中,分别放置于4个小型试验冷库中(每个冷库容积23 m3),每库20箱,每箱15 kg,库内温度(0±1)℃,RH 90%—95%。对使用20 mg·L-1 CPPU处理的猕猴桃进行O3处理,将额定产量为20 g·h-1的O3发生器产生的O3通入冷库中,使3个冷库浓度分别达到10、40、70 mg·m-3(分别为O3处理1、处理2、处理3,记为T1、T2、T3;用O3检测仪对O3浓度进行检测);未使用CPPU也未使用O3的为CPPU对照组CK,使用CPPU但未使用O3处理的为臭氧处理对照组CK1;每15 d 处理1次,每次处理2 h;随机取样,乙烯含量和呼吸强度每15 d测定1次,Met、SAM、ACC、MACC含量以及SAM合成酶(SAMS)、ACS、ACO活性30 d测定1次,试验设3次重复。1.3.2 测定指标
(1)蛋氨酸含量的测定参照KÜHNREICH等[14]的方法略有改动。
称取6.0 g猕猴桃研磨,于12 000×g离心15 min,将上清液定容到10 mL容量瓶中,经0.22 μm滤膜过滤后进行HPLC检测。
高效液相色谱条件:采用C18柱,流动相为V(12.5 mmol·L-1磷酸):V(乙腈)=97:3,柱温30℃,流速1 mL·min-1,检测波长210 nm,进样量10 μL。
(2)SAM含量的测定参照杨宇辉[15]略有改动。
称取2.0 g猕猴桃研磨,于10 000×g离心15 min,将上清液倒掉,在残渣中加入2.0 mL 1.5 mol·L-1的HClO4,常温下震荡90 min,于4℃过夜,12 000×g离心10 min,经0.22 μm滤膜过滤后进行HPLC检测。
高效液相色谱条件:采用C18柱,流动相为V(0.01 mmol·L-1甲酸铵):V(甲醇)=97:3,柱温30℃,流速1 mL·min-1,检测波长254 nm,进样量10 μL。
(3)ACC含量的测定参考曹建康等[16]的方法。
称取5.0 g猕猴桃研磨,转入试管中并加入10 mL 95%乙醇溶液,煮沸浸提20 min,冷却后于10 000×g离心15 min,收集上清液,再向残渣中加入10 mL 80%乙醇,于70℃浸提30 min,离心收集上清液,合并两次上清液,用旋转蒸发仪浸提蒸发至干,向蒸发残留物中加入2.0 mL蒸馏水振荡溶解,即为ACC制备液。
取1.0 mL ACC制备液,置于容积为20 mL的样品瓶中,加入40 μL 25mmol·L-1 HgCl2溶液,用橡胶塞密封样品瓶,冰浴10 min使温度平衡。再通过注射器加入0.2 mL经冰浴预冷的5% NaClO-饱和NaOH混合液(NaClO:NaOH=2:1,体积比)迅速振荡5 s后,放回冰浴平衡5 min,顶空取1 mL气体,用气相色谱法测定乙烯生成量。
(4)1-(丙二酰氨基)环丙烷-1-羧酸(MACC)含量的测定。
取1.0 mL ACC制备液,加入0.2 mL 12 mol·L-1盐酸,于沸水浴中加热3 h。冷却后加入1.2 mL 2 mol·L-1 NaOH溶液中和,然后按照测定ACC的方法测定,即得总的ACC含量,MACC含量为总的ACC含量减去游离ACC含量。
(5)SAM合成酶活性的测定参照姚高峰等[17]方法略有改动。
称取10 g猕猴桃研磨,于12 000×g离心15 min,将上清液倒掉,在残渣中加入10 mL Tris-HCl缓冲液,按冰浴30 s震荡1 min交替进行8次,于12 000×g离心10 min,即为酶液。在室温下反应1 h,加入1.5 mL 20% HClO4,4℃放置0.5 h以上终止反应,12 000×g离心10 min,经0.22 μm滤膜过滤后进行HPLC检测。
高效液相色谱条件:采用C18柱,流动相为V (0.01 mmol·L-1甲酸铵):V(甲醇)=97:3,柱温30℃,流速l mL·min-1,检测波长254 nm,进样量20 μL。
(6)ACS活性的测定。
取5 g猕猴桃加入5.0 mL含有1 mmol·L-1 EDTA、1 mmol·L-1 PMSF、4 mmol·L-1 DTT、3% PVPP和10 μmol·L-1磷酸吡哆醛的提取缓冲液进行研磨,于12 000×g离心30 min,上清液即为酶提取液。
将1 mL酶提取液和1.5 mL反应缓冲液加入到20 mL样品瓶中,用橡皮塞密封样品瓶后,在30℃水浴中保温1 h。然后注射加入0.1 mL 25 mmol·L-1 HgCl2溶液以终止反应,并置于冰浴10 min平衡温度,再用注射器加入0.2 mL经冰浴预冷的5% NaClO-饱和NaOH混合液(NaClO:NaOH=2:1,体积比)迅速震荡5 s后,放回冰浴平衡5 min,顶空取1 mL气体测定乙烯释放量。
(7)ACO活性的测定。
称取5 g猕猴桃,加入5.0 mL含有10%甘油、5% PVP、5.0 mmol·L-1 DTT、30 mmol·L-1抗坏血酸钠和0.1 mmol·L-1 FeSO4提取缓冲液,于12 000×g离心30 min,上清液即为酶提取液。
将2.0 mL酶提取液和2 mL反应缓冲液(加入30 mmol·L-1 NaHCO3)加入到20 mL样品瓶中,用橡皮塞密封样品瓶后,在30℃摇床震荡2 h。然后顶空取1 mL气体测定乙烯释放量。
(8)乙烯释放量的测定。
取1 kg果实放置在1.6 L的密封干燥器内1 h,抽顶空气体,通过气相色谱(GC-14C型气相色谱仪)进行测定。气相条件:FID检测器,柱温90℃,进样口温度160℃,GDX-102不锈钢填充柱,载气:N2(50 MPa),燃气:H2(75 MPa),助燃气:空气(50 MPa);对照及处理果实各设3组重复。
(9)硬度测定采用TAXT PLUS/50物性测定仪。
在TPA模式下,随机取4个果实进行测定,在猕猴桃果实赤道部位均匀取3点,削去果实表皮,沿果实赤道上120°等距离测定3次,重复3次。
1.4 数据处理方法
采用Origin8.0软件进行作图分析,SPSS 20软件对数据进行显著差异性检验,P<0.05被认为具有显著性差异。2 结果
2.1 O3处理对猕猴桃果实乙烯代谢途径中主要物质含量变化的影响
2.1.1 O3处理对猕猴桃果实Met含量的影响 Met是植物体内合成乙烯的前体物质。从图1-a中可以看出,在贮藏前期Met含量较高,随着贮藏时间的延长,Met含量呈下降趋势。在贮藏开始时CK的Met含量低于CK1,在贮藏过程中,CK的Met下降趋势小于CK1。在贮藏60 d后,Met含量下降减缓,60 d时CK1和各O3处理组(10、40、70 mg·m-3)的Met含量分别为1.36、2.62、4.41和2.60 mg·(100 g)-1,40 mg·m-3 O3处理的Met含量是CK1的3.24倍;且在整个贮藏期,40 mg·m-3 O3处理组Met均高于其他处理和CK1。 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图1O3 对使用20 mg·L-1 CPPU秦美猕猴桃Met(a)、SAM(b)含量的影响
-->Fig. 1Effects of O3 on the Met (a) and SAM (b) content of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
2.1.2 O3处理对猕猴桃果实SAM含量的影响 SAM是由Met转化生成的,随着Met含量的减少,SAM含量也随之减少(图1-b)。CK下降趋势低于CK1。贮藏60 d时CK1和40 mg·m-3 O3处理组的SAM含量分别为15.48 mg·(100 g)-1和20.73 mg·(100 g)-1,具有显著性差异(P<0.05),且在整个贮藏期内40 mg·m-3 O3处理SAM含量均高于其他处理和CK,和对Met的影响一致,10、70 mg·m-3 O3处理效果较差,差异不显著(P>0.05)。
2.1.3 O3处理对猕猴桃果实ACC和MACC含量的影响 ACC是乙烯合成的直接前体物质,经过ACC氧化酶生成乙烯,这是乙烯合成途径中的限速步骤。图2-a中,随着贮藏时间的延长,ACC呈先上升后下降的趋势,在60 d时出现高峰。ACC含量增加是由SAM转化而来,在60 d之后SAM保持不变,而ACC向乙烯转化,故呈下降趋势。CK较CK1的ACC含量低,CPPU加快了ACC含量的增加,从而促进内源乙烯的释放;CK1与各O3处理组相比,O3能有效减少果实中ACC含量的增加,从而抑制乙烯释放量的增加。60 d时CK1和各O3处理(10、40、70 mg·m-3)的ACC含量分别为0.068、0.059、0.038和0.055 nmol·g-1,40、70 mg·m-3 O3处理与CK1具有显著性差异(P<0.05)。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图2O3 对使用20 mg·L-1 CPPU秦美猕猴桃ACC(a)、MACC(b)含量的影响
-->Fig. 2Effects of O3 on the ACC (a) and MACC (b) content of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
在ACC代谢途径中,除向乙烯转化外,ACC还可以转化生成MACC(图2-b),在贮藏过程中MACC含量呈上升趋势。
不同浓度O3处理效果不同,10 mg·m-3 O3处理由于浓度太低,没有达到预期效果;40 mg·m-3 O3处理效果较好;70 mg·m-3 O3处理因浓度过高,O3的强氧化活性可能损伤了细胞结构,造成ACC和MACC含量均高于40 mg·m-3 O3处理。
2.2 O3处理对猕猴桃果实乙烯相关酶活性的影响
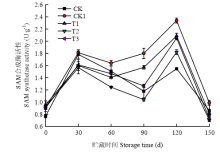
SAM合成酶是催化Met生成SAM的关键酶,ACS、ACO是乙烯合成途径中的关键酶和限速酶。抑制SAM合成酶、ACS和ACO酶的活性,均可以抑制乙烯的生成,延缓果实后熟软化。2.2.1 O3处理对猕猴桃果实SAM合成酶活性的影响 SAM合成酶催化Met生成SAM。图3显示,SAM合成酶在贮藏过程中呈先上升后下降的趋势,在贮藏30 d和120 d时分别达到高峰。在整个贮藏期,40 mg·m-3 O3处理均低于其他处理和CK1,40 mg·m-3 O3处理与CK1有显著性差异(P<0.05),10、70 mg·m-3 O3处理之间差异不显著(P>0.05)。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图3O3对使用20 mg·L-1 CPPU秦美猕猴桃SAM合成酶活性的影响
-->Fig. 3Effect of O3 on the SAM synthetase activity of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
2.2.2 O3处理对猕猴桃果实ACS活性的影响 ACS是催化SAM生成ACC的关键酶。图4-a中,贮藏前期ACS活性呈上升趋势,在60 d时达到高峰,之后下降,这与ACC含量的变化趋势一致(图2-a)。在贮藏过程中CK的ACS活性低于CK1。60 d时CK1和各O3处理组(10、40、70 mg·m-3)的ACS活性分别为0.084、0.069、0.054和0.080 nmol·(g·h)-1;且在整个贮藏期,40 mg·m-3 O3处理ACS活性均低于其他处理和CK1,40 mg·m-3 O3处理与CK1具有显著性差异(P<0.05),10、70 mg·m-3 O3处理之间差异不显著(P>0.05)。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图4O3对使用20 mg·L-1 CPPU秦美猕猴桃ACS(a)、ACO(b)的影响
-->Fig. 4Effects of O3 on the ACS (a) and ACO (b) activity of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
2.2.3 O3处理对猕猴桃果实ACO活性的影响 ACO以抗坏血酸和氧作为辅基,Fe2+和CO2作为辅助因子,将ACC氧化成乙烯。图4-b显示,ACO活性随着贮藏时间的延长呈先上升后下降趋势,在60 d 时出现高峰。同样,在贮藏过程中CK的ACO活性低于CK1,CK1和各O3处理组(10、40、70 mg·m-3)ACO活性的峰值分别为0.062、0.046、0.029和0.051 nmol·(g·h)-1,处理组和CK1之间存在显著性差异(P<0.05),40 mg·m-3 O3处理对ACO活性的抑制效果较适宜,10、70 mg·m-3 O3处理之间差异不显著(P>0.05)。
2.3 O3处理对猕猴桃果实乙烯释放量、呼吸速率的影响
猕猴桃是典型的呼吸跃变型水果,乙烯能催化果实软化,加速果实衰老,乙烯释放量越高,果实软化越快。O3处理对果实乙烯释放量的影响如图5-a所示,CK乙烯释放量低于CK1,CPPU增加了猕猴桃乙烯的释放,从而影响贮藏时间。CK1和O3处理组(10、40、70 mg·m-3)果实的乙烯释放量均在45 d时达到高峰,其值分别为18.42、15.99、9.86、11.69 μL·kg-1·h-1,且乙烯高峰出现时间晚于呼吸高峰,乙烯释放量的变化同ACC含量变化一致(图2-a)。40 mg·m-3 O3处理组果实的乙烯释放量在整个贮藏期始终最低,是较适宜的处理浓度。 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图5O3对使用20 mg·L-1 CPPU秦美猕猴桃乙烯释放量(a)、呼吸强度(b)的影响
-->Fig. 5Effect of O3 on the ethylene production rate (a), respiration intensity (b) of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
如图5-b所示,O3处理和CK1的呼吸速率呈先上升后下降趋势,O3处理呼吸高峰出现在贮藏时间30 d,而CK1则在15 d出现呼吸高峰(CK的呼吸峰值要低于CK1),且呼吸峰值要高于O3处理组,CK1和O3处理组(10、40、70 mg·m-3)的呼吸峰值分别为18.77、16.15、12.24、15.48 mg·kg-1·h-1,O3不仅能降低呼吸峰值还能延迟呼吸峰出现的时间。随着贮藏时间的延长,O3处理果实呼吸强度始终低于CK1(P<0.05)。40 mg·m-3 O3处理效果适宜,贮藏期内果实呼吸强度最低;10 mg·m-3和70 mg·m-3 O3处理对果实呼吸作用的抑制效果均较差。
2.4 O3处理对猕猴桃果实硬度的影响
果实硬度是影响贮藏效果的关键因素,随着贮藏时间的延长,硬度呈逐渐下降趋势(图6)。CK贮藏前期高于CK1,随着贮藏时间的延长,40 mg·m-3 O3处理的硬度高于CK;O3处理果实的硬度高于CK1,贮藏时间为30 d时,各处理硬度分别下降了15.95%、7.61%、6.00%和10.17%。贮藏30—75 d时硬度呈现快速下降趋势,之后的贮藏期内硬度下降较为缓慢。在贮藏中期,40 mg·m-3 O3处理的硬度显著高于CK1(P<0.05),10、70 mg·m-3 O3处理效果较差。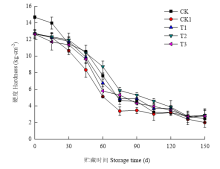 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图6O3对使用20 mg·L-1 CPPU秦美猕猴桃硬度的影响
-->Fig. 6Effect of O3 on the hardness of Qinmei kiwifruit treated with 20 mg·L-1 CPPU
-->
3 讨论
乙烯与果实生长发育及其成熟衰老过程有着密切关系,对影响果实生命周期的变化起着很大作用。在采后的果蔬产品中,内源乙烯启动了体内一系列与衰老有关酶的活性,从而导致采后旺盛的新陈代谢,使果实迅速衰老变质[18]。在贮藏过程中经常采用保鲜剂来抑制乙烯代谢,环丙烯类物质1-OCP能有效抑制番茄的呼吸速率和乙烯释放量,但对贮藏过程中ACC含量影响较小,并在贮藏后期对果实带来了一定的伤害[19];TASSONI等[20]研究发现1-MCP抑制了乙烯的生成和ACS的表达,推迟了番茄的成熟,但对ACO影响不大。而O3与其他保鲜剂相比具有无污染、无残留等优点,是一种新型的绿色保鲜剂,并能很好的抑制呼吸速率、乙烯释放量等。果农为了增加猕猴桃产量,采前使用CPPU处理,虽然增加了果实的单果重,但对猕猴桃贮藏带来了消极影响。宋小青等[21]研究发现CPPU处理有效促进了秦美猕猴桃果实乙烯的释放,造成果实软化加快,减少了猕猴桃的贮藏时间。而O3能使果蔬新陈代谢的有毒有害产物被氧化,从而达到延长贮藏期的效果。本试验研究发现采用适宜浓度O3处理能有效抑制使用了20 mg·L-1 CPPU的秦美猕猴桃果实中内源乙烯的代谢。
猕猴桃的乙烯代谢是由Met经SAM合成酶催化生成SAM,再经过ACS催化生成ACC,最终经ACO催化生成乙烯。Met是乙烯代谢的前体物质,在贮藏中呈下降趋势,在贮藏后期,Met含量又有上升的趋势,这可能是甲硫基核糖向Met转化速率快于Met向乙烯转化速率[3]。SAM同Met含量变化趋势一致(图1-a)。这可能是因为在贮藏后期乙烯释放量减少,呼吸速率下降,消耗的Met和SAM减少。SAM合成酶催化Met向SAM转化,随着SAM合成酶活性的增加,SAM含量呈下降趋势(图1-b),这可能是因为Met(底物)含量不足,致使生成物SAM同底物Met含量变化趋势一致,但由于酶活性的增加,SAM含量相较于Met含量下降速率减缓。
HOFFMAN等[22]指出,ACC除了能转变成乙烯外,还能与丙二酸发生酰化形成MACC,并认为这是植物体内避免ACC积累的一种“去毒”调节。本试验中,我们发现O3处理抑制了ACC含量的积累,增加了ACC向MACC途径的转化,从而减少了乙烯的释放,延长了使用高浓度CPPU处理猕猴桃的贮藏时间。ACS是以磷酸吡哆醛为辅基的酶[23],O3处理能显著抑制ACS活性,这与MINAS[24]的研究结果相同,这可能是因为O3启动了ACS1基因的表达,从而抑制了ACS活性。ACO是乙烯合成途径中的最后一个酶,直接催化ACC合成乙烯,据KENTJ[25]研究发现,ACO可能也是乙烯生物合成途径中的一个限速酶,它在转录水平上调控着乙烯的生成速率。本文研究发现O3处理显著降低了ACO活性,这与MINAS[24]的研究结果相同,这可能是O3处理抑制了ACO1基因的表达,从而抑制了乙烯的生成。郭芹等[26]对番木瓜进行研究发现乙烯高峰出现在第6天,而ACC和ACS活性的高峰则在贮藏后第8天出现,表明ACS的活性加速ACC含量的积累,这与本试验研究结果相同。
猕猴桃是典型的呼吸跃变型果实,具有明显的乙烯释放高峰,O3处理能显著降低乙烯峰值,减少乙烯释放量,并降低果实呼吸速率,这与王玉萍等[27]的研究结果一致。O3处理不能推迟猕猴桃乙烯高峰出现的时间,但显著降低了乙烯高峰值,这是因为O3一方面能通过氧化消除库内的乙烯等有害气体,另一方面能抑制乙烯合成途径中相关酶的活性,从而减少乙烯释放量[28]。试验中还发现并非O3浓度越高越好,适宜的O3处理能有效减缓乙烯代谢,O3浓度过低起不到抑制的效果,而浓度过高产生大量氧气,使果蔬在一个富氧环境中,对乙烯代谢具有一定的促进作用。
4 结论
本研究表明O3处理能有效抑制使用了20 mg·L-1 CPPU的秦美猕猴桃果实的呼吸速率;O3处理也能显著降低果实中的乙烯代谢,延缓果实的后熟和衰老,抑制了果实硬度的下降。因此,在实际贮藏中可以采用40 mg·m-3 O3处理来改善因使用膨大剂而导致猕猴桃保鲜期大幅缩短的现象。(责任编辑 杨鑫浩)
The authors have declared that no competing interests exist.
