0 引言
【研究意义】小麦(Triticum aestivum L.)是世界上最早栽培的农作物之一,也是总产量仅次于玉米的第二大粮食作物。由禾谷镰刀菌(Fusarium graminearum)引起的小麦赤霉病(Fusarium head blight,FHB)是一种世界性病害,严重影响了小麦产量和品质,而且感染麦粒中禾谷镰刀菌的次生代谢产物,严重威胁人类的健康[1]。中国是小麦赤霉病受害面积最大的国家,近年来更有不断扩大受害面积的趋势,除长江中下游及东北三江平原外,在豫、鲁、陕等地也有发展,在全国每年受害面积约700万hm2,占小麦种植面积的四分之一,每年因赤霉病损失产量约200万—300万吨[2]。随着小麦育种中少数亲本的反复使用和耕作制度的变化,栽培小麦种内遗传变异急剧减少,继续在栽培小麦种内挖掘新的优良种质效果有限,使得小麦高产优质抗病育种进展不尽人意。为了拓宽小麦的遗传变异类型,提高小麦的育种效率,通过远缘杂交从小麦近缘野生种中引入有益基因,并利用这些有益基因培育小麦新品种,已成为人们的共识和小麦新品种选育的重要途径。【前人研究进展】小麦的野生近缘物种是小麦宝贵的基因资源库。二倍体长穗偃麦草(Thinopyrum elongatum (Host) A. Löve,2n=2x=14,EE),具有抗盐、抗旱、大穗、多花、优质、繁殖能力和适应性强、抗病虫害等许多优良性状[3-5]。利用RFLP等标记确定长穗偃麦草的E组7条染色体分别与小麦染色体A、B、D组7个部分同源群具有部分同源关系,表明长穗偃麦草E基因组与小麦A、B、D基因组的遗传分化程度相对较小[6]。因此,在普通小麦遗传改良中可以方便地利用长穗偃麦草的遗传基础。通过对小麦-长穗偃麦草全套附加系赤霉病接种鉴定发现,1E染色体上存在赤霉病抗性基因[7],硬粒小麦-长穗偃麦草1E染色体附加系的研究中也认为1E染色体上存在赤霉病抗性基因[8];除此之外,研究表明在7E染色体也具有赤霉病抗性基因,并将该抗性基因定位在7E长臂上[9-11]。培育小麦附加系、代换系和易位系是利用外源种质改良小麦的一条重要途径,其中,易位系以其导入外源染色体小片段仅含优良目标基因的优点,它比附加系及代换系在作物育种中的意义更重大。易位系可以直接作为品种在生产上推广利用,例如小麦-黑麦1BL/1RS易位系携有多种小麦叶部病害的抗性基因,同时具有广泛的适应性和高产的遗传效应,被广泛应用于世界各国栽培小麦的品种改良中[12-13]。目前,主要是通过远缘杂交材料经辐射[14-17]、ph1b[18-19]、组织培养[20]、杀配子染色体[21]等途径使染色体发生断裂后发生错误重接而培育易位系。通过众多科学家多年研究获得小麦与多个近缘种的易位系,如小麦与簇毛麦[22]、小麦与大赖草[23]、小麦与黑麦[24]、小麦与中间偃麦草[25-26]以及小麦与百萨偃麦草[27]等物种间染色体易位系。其中,电离辐射容易诱导染色体断裂重接而产生各种染色体结构变异,是易位系培育的常用方法[28]。在获得的小麦-长穗偃麦草易位系中,偃麦草染色体是来源于十倍体长穗偃麦草(Th. ponticurn, 2n = 70)的一对部分同源染色体7ell和7el2,与7E染色体具有部分同源性[29]。赤霉病抗性研究表明7el1的代换系和易位系均没有抗性,而臂间易位(7DS·7el2L)具有抗性[30]。利用ph1b突变体与7DS·7el2L臂间易位杂交,将其中的抗赤霉病基因(Fhb7)定位于7el2的长臂上,并获得聚合了Fhb1与Fhb7 2个抗赤霉病基因的育种材料[31]。【本研究切入点】综上所述,小麦与多个近缘种产生的易位系中多数是以中国春小麦为背景,在抗赤霉病育种中作为亲本的可利用性不高。二倍体长穗偃麦草也具有赤霉病抗性,研究表明其抗性基因位于1E和7E染色体[7-11],但未见在主栽小麦背景培育7E染色体易位系的成功报道。【拟解决的关键问题】本研究利用60Co辐射处理小麦-长穗偃麦草7E代换系DS7E(7B)与扬麦16杂交的F2种子,在辐射后代的繁殖过程中,首先进行表现型筛选,选择赤霉病抗性相对较强又具有长穗偃麦草相关特征的单株种植,继续进行赤霉病抗性和农艺性状选择,在此基础上利用长穗偃麦草7E染色体特异标记对获选单株进行PCR检测,最后通过基因组荧光原位杂交(genomic in situ hybridization,GISH)进行小麦-长穗偃麦草抗赤霉病易位系确认。利用赤霉病抗性鉴定、分子标记筛选和GISH确认3种方法相结合培育小麦-长穗偃麦草抗赤霉病易位系的途径,选择目标明确,选择效率高,培育周期短,为小麦异源易位系的培育提供了有效途径。所获小麦-长穗偃麦草7E抗赤霉病易位系为小麦品种改良和小片段易位系的研究提供了新种质或基础材料。1 材料与方法
1.1 植物材料
所用材料包括长穗偃麦草(Th. elongatum,2n=2x=14)、中国春-长穗偃麦草7E附加系(DA7E)、7E长臂附加系(DA7EL)、7E短臂附加系(DA7ES),中国春-长穗偃麦草7E代换系(DS7E(7B))、扬麦16(Y16)、中国春(CS)、苏麦3号(SU3)和安农8455(AN8455)。扬麦16、苏麦3号和安农8455引自江苏里下河地区农业科学研究所,其他材料由加拿大农业部Ottawa研究中心的Dr.FEDAK研究员提供。1.2 长穗偃麦草特异标记筛选
提取供试材料的基因组DNA[32],通过PCR进行分子标记筛选。用于染色体或染色体臂鉴定的分子标记为笔者前期开发的长穗偃麦草特异标记[33-35]。PCR反应体系为模板DNA(100 ng·μL-1)1 μL、上游引物和下游引物各1 μL(10 µmol·L-1)、10×PCR缓冲液2.5 μL、2.5 mmol·L-1的dNTP 2 μL、5 U·μL-1的Taq酶0.3 μL,ddH2O定容至25 μL。PCR反应过程为94℃ 5 min;94℃ 45 s,根据不同引物在50— 60℃退火1 min,72℃ 90 s,35个循环,72℃ 10 min。扩增产物利用1%琼脂糖凝胶电泳进行检测。1.3 易位系培育途径
利用扬麦16与DS7E(7B)杂交,60Co辐射(辐射剂量为30 000 rad)F2种子,收获成活M1植株自交种子为M2群体。从M2开始进行农艺性状、赤霉病抗性和染色体特异分子标记的筛选,各世代的中选植株均单株收获进行繁殖,最后对含有7E染色体特异标记扩增的M4抗性材料进行基因组原位杂交,获得小麦-长穗偃麦草7E抗赤霉病易位系(图1)。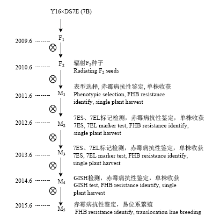 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图1辐射法培育小麦-长穗偃麦草抗赤霉病易位系
-->Fig. 1Development of wheat -Th. elongatum translocation lines with FBH resistance by radiation
-->
1.4 赤霉病抗性鉴定
对辐射后的各世代均进行赤霉病抗性选择,选择的M1单株赤霉病抗性表现不同,但具有长穗偃麦草的特征,M2以后的单株选择要求既具有7E染色体特异分子标记扩增,而赤霉病抗性表现又要好。M1赤霉病抗性以自然发病率(病穗率)进行筛选,从M2开始采用单花滴注法进行赤霉病的抗性鉴定,接种21 d后调查发病情况。发病结果调查以单株为单位,汇总各单株结果平均后作为整行的抗性表现。发病率以病小穗数除以总小穗数的病小穗率表示。1.5 基因组原位杂交
细胞学制片方法参考GILL等[36]的方法并稍加改进。将经前处理和固定后的根尖洗涤后在2%的醋酸洋红中浸泡24 h以上,制片时切下根尖分生组织于载玻片上,滴加45%的醋酸进行压片,选择染色体分散好的制片,-70℃冷冻后揭开盖玻片,系列酒精脱水处理保存备用。按照ZHANG等[37]的方法进行基因组原位杂交,以二倍体长穗偃麦草基因组DNA通过缺口平移法进行地高辛标记作为探针,中国春基因组DNA为封阻,具体比例为探针总浓度:封阻总浓度=1﹕50,在安装有CCD相机的Olympus荧光显微镜下观察杂交信号并拍照。2 结果
2.1 长穗偃麦草特异分子标记的筛选
利用扬州大学陈建民教授实验室开发的标记[33-35]对中国春-长穗偃麦草7E附加系(DA7E)、7E长臂附加系(DA7EL)、7E短臂附加系(DA7ES)、二倍体长穗偃麦草(2X)以及中国春(CS)、扬麦16(Y16)进行PCR特异性扩增,进一步对7E染色体、7ES、7EL染色体臂的标记进行选择。共选择7E染色体标记4个(7E染色体标记对7EL、7ES同样扩增),7EL标记11个,7ES标记6个,标记名称及序列见表1。Table 1
表1
表1小麦-长穗偃麦草7E染色体易位系鉴定所用分子标记
Table 1Molecular marker for identifying wheat- Th. elongatum 7E chromosome translocation lines
| 标记名称 New name of marker | 标记原名称 Old name of marker | 引物序列Primer sequence(5′-3′) | 扩增染色体 Amplified Chr. | |
|---|---|---|---|---|
| 正向 Forward | 反向 Reverse | |||
| 7E1 | SM1-7E_1 | CGACGAAACAGGGTAACT | CGAGGACAGTTCAGTGCT | 7E |
| 7E2 | SM1-7E_2 | CAAGTGCGGACGACGGAC | CGAGGACAGTTCAGTGCTGAC | 7E |
| 7E3 | P7E_No.32 | CTGAGCTGCGTCGGTA | CCAGAAATTGCTAAAATCTT | 7E |
| 7E4 | P7E_No.36 | TGTTTCTTAGTTGTTTTGTT | GCCTTGACCACCATAC | 7E |
| 7EL1 | P7E_No.1 | ATCAATCCCTCCACAAAGTC | GCCTTTTTTTTCTAATGTGC | 7EL |
| 7EL2 | P7E_No.7 | ATTTTGTCCCTATGCT | ATGCCTTCCTGATTTA | 7EL |
| 7EL3 | P7E_No.11 | TAGAATAGCTTTTAGGAATA | GTGAGCATTCTTAGCATTAC | 7EL |
| 7EL4 | P7E_No.20 | CTTTCCATAGTAGGTCCAGT | CGAACTTTGTTTGAAATATG | 7EL |
| 7EL5 | P7E_No.24 | CAAAATGAAAAGATAAAACT | AGATTCAAAATTTTAGTTAT | 7EL |
| 7EL6 | P7E_No.31 | CTACCCTTACCACCTCG | CCACTGGATGCTGTTTAT | 7EL |
| 7EL7 | P7E_No.37 | GGTAAGCTTGAAATACATGA | TCCAAGTGATATTGTAGTCG | 7EL |
| 7EL8 | P7E_No.49 | ATACTTGAGGTGATTTCGGT | GGTGCAAAGTTTTTACAATG | 7EL |
| 7EL9 | P7E_No.52 | ACAAGTCCATTCATTACAAC | TACTACTTTTGTGACAGCAG | 7EL |
| 7EL10 | P7E_No.53 | GTCAAGAGTTGGCTTTATTC | ATTTGCTAATTCTCGTCATA | 7EL |
| 7EL11 | P7E_No.56 | TTACACTAACCCATGGTGTT | GCAGAGAATGAAGCAAAATC | 7EL |
| 7ES1 | P7E_No.2 | AGCAAATAAAACGACAGT | GGTTTTCACCAATTACAG | 7ES |
| 7ES2 | P7E_No.13 | CACTTGTGCATATTCGAGAG | CCATTTTCCAATATATACAA | 7ES |
| 7ES3 | P7E_No.14 | GAAATGGCAAGTACCTAA | CAAGTAGAAGTTCAGCAA | 7ES |
| 7ES4 | P7E_No.39 | TTTATAAGTTGATGAGGGGG | AAGGCTTTACCGAAAATCAT | 7ES |
| 7ES5 | P7E_No.71 | GTCTTGCCTGTCCTCG | ATTTTCAAAGTTCTCACAAG | 7ES |
| 7ES6 | P7E_No.84 | CGAAGGGTCTTTGATT | GCAAACATCTGACAAGG | 7ES |
新窗口打开
2.2 基于特异分子标记选择目标单株
在M1选择了具有长穗偃麦草特征、株型比较好、赤霉病发病率不同的13个单株。利用7E染色体和7E染色体长臂及短臂标记对13个株行中M2单株进行PCR检测,部分结果如图2所示。第1株行出现2株7E扩增,未见臂的扩增。第2株行出现5株7E扩增,出现3株7ES扩增。第3株行出现3株7E扩增,出现3株7EL扩增。根据PCR检测和表现型结果,分别选择其中可能含有长穗偃麦草7EL片段7株和长穗偃麦草7ES片段14株,次年株行种植M3。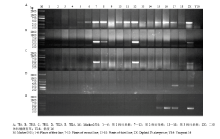 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图2M2单株分子标记检测结果
-->Fig. 2The PCR detection results of molecular markers for M2 plants
-->
利用7E染色体和7EL、7ES特异标记对21株M2衍生的222个M3植株的DNA进行检测,依据2个以上标记扩增和表现型的标准,共获得含有长穗偃麦草7EL片段13株,含有长穗偃麦草7ES片段3株(图3和图4)。不难看出,尽管上代选择具有7ES片段的单株比较多,但一代自交繁殖后,继续选择得到的短臂单株变少了。当7E染色体与小麦染色体发生易位后,向后代的传递比较稳定,而单独存在的染色体臂向后代的传递可能比较容易丢失。
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图3M3单株7EL分子标记检测
-->Fig. 3The PCR results of 7EL-specific molecular markers for M3 plants
-->
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图4M3单株7ES分子标记检测
-->Fig. 4The PCR results of 7ES-specific molecular markers for M3 plants
-->
2.3 扩增分子标记单株的赤霉病抗性鉴定
对获得标记扩增的M2、M3单株利用单花滴注法进行赤霉病抗性鉴定,选择具有赤霉病抗性和分子标记扩增的单株进行繁殖,对M4单株同样进行赤霉病抗性鉴定。由表2可见,最后获得的材料可追溯到M1代2个单株,赤霉病发病率明显不同。这两个单株在衍生后代过程中,一般上代具有特异标记扩增并赤霉病抗性好的单株,下代的赤霉病抗性表现也好并具有特异标记扩增,赤霉病抗性和特异标记具有共分离特征。标记筛选区别了7EL和7ES染色体组成的单株,这些单株也表现了赤霉病抗性的差别,连续3年的接种鉴定表明,具7EL植株组成的株行赤霉病抗性每年均好于中国春、扬麦16和安农8455,与苏麦3号相当,而且也好于具7ES植株组成的株行,意味着7EL具有抗赤霉病的基因。Table 2
表2
表2小麦-长穗偃麦草易位系系谱及不同世代的标记检测和赤霉病抗性鉴定
Table 2The pedigree, marker detection and FBH resistance identification for translocation lines in different generations
| M1 (2012) | M2( 2013) | M3 (2014) | M4(2015) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 材料名称 Name | 发病率 Morbidity rate (%) | 行号-株号Line num.- plant num. | 标记及数目 Marker and number | 发病率 Morbidity rate (%) | 行号-株号Line num.- plant num. | 标记及数目 Marker and number | 发病率 Morbidity rate (%) | 株系 Plant lines | 发病率 Morbidity rate (%) | ||||
| 7E | 7EL | 7ES | 7E | 7EL | 7ES | ||||||||
| A1150-2 | 29.17 | K12104-2 | 2 | 1 | 11.79 | Z13067-5 Z13067-7 | 1 4 | 9 6 | 14.14 | TW-7EL1 | 7.57 | ||
| Z13067-7 | 4 | 6 | |||||||||||
| K12104-4 | 2 | 1 | Z13068-2 | 2 | 3 | 6.74 | TW-7EL2 | 3.66 | |||||
| Z13068-3 | 4 | 9 | |||||||||||
| Z13068-4 | 4 | 8 | |||||||||||
| Z13068-6 | 4 | 8 | |||||||||||
| Z13068-8 | 4 | 9 | |||||||||||
| Z13068-9 | 1 | 3 | |||||||||||
| K12104-5 | 2 | 2 | Z13069-11 | 2 | 5 | 4.96 | TW-7EL3 | 1.43 | |||||
| A1152-1 | 100.0 | K12106-1 | 2 | 3 | 13.66 | Z13073-1 | 3 | 4 | 13.93 | W-DA7ES | 12.8 | ||
| Z13073-7 | 3 | 4 | |||||||||||
| Z13073-8 | 3 | 3 | |||||||||||
| CS | 80.32 | 17.31 | 26.13 | 11.51 | |||||||||
| Y16 | 15.38 | 23.67 | 20.22 | ||||||||||
| AN8455 | 86.16 | 55.67 | 59.1 | 28.74 | |||||||||
| SU 3 | 21.95 | 13.98 | 5.21 | 4.76 | |||||||||
新窗口打开
2012年发病率以病穗率表示,2013—2015年发病率以病小穗率表示
Morbidity rate expressed as FHB infected spike (%) in 2012 and as FHB infected spikelets (%) during 2013-2015
2.4 基因组原位杂交(GISH)检测和易位系的特征
对于M2、M3中连续2年均有分子标记扩增和赤霉病抗性较高单株衍生的后代(M4),可认为带有长穗偃麦草7E染色体。这些特异标记扩增的单株中,7E染色体有3种存在方式,完整的7E染色体、小麦染色体与7E的易位染色体以及7EL或7ES的附加染色体臂。利用经7EL特异分子标记检测过的12株M3代的后代进行GISH,共9株的后代具有小麦-长穗偃麦草易位染色体,体细胞染色体2n=42。这些植株来源于3个M2单株,分别命名为TW-7EL1、TW-7EL2和TW-7EL3(T:易位;W:小麦;7EL:长穗偃麦草7E染色体长臂;数字:易位系序号)。TW-7EL1和TW-7EL2易位系均为整臂易位(图5-A)。而TW-7EL3易位系中即存在整臂易位也存在小片段易位染色体,还在分离中。选择经7ES分子标记验证过的2株M3后代进行GISH,结果显示附加2条长穗偃麦草染色体短臂,是来自1个M2单株后代,命名为W-AD7ES1,体细胞染色体2n=44(图5-B),未见完整的7E染色体。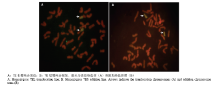 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图5小麦-长穗偃麦草7E染色体易位系的GISH结果
-->Fig. 5GISH result of wheat-Th.elongatum 7E chromosome translocation lines
-->
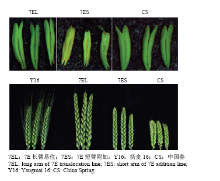
对GISH检测的小麦-长穗偃麦草纯合易位系和附加系进行农艺性状的考察(表3)。小麦-长穗偃麦草7EL易位系株高与中国春类似,而长穗偃麦草7ES附加系株高与Y16接近。易位系和附加系间的穗长、花药成熟情况也呈现明显的差别。由图6可以看出,7EL易位系的穗长较7ES附加系长,且小穗之间间距较大。穗型类似于中国春,7ES附加系的部分花药短小且干瘪,没有花粉,呈不育的状态,而7EL易位系的花药硕大饱满,与中国春类似。
Table 3
表3
表37EL易位系和7ES附加系的主要农艺性状
Table 3The main agronomic traits of 7EL translocation lines and 7ES addition line
| 材料 Materials | 株高 Plant hight (cm) | 单株穗数 Spike number per plant | 单穗小穗数 Spikelet number per spike | 结实小穗率 Spikelet number with seeds (%) | 穗粒数 Kernels per spike | 千粒重 TKW(g) |
|---|---|---|---|---|---|---|
| TW-7EL1 | 104.6 | 17.7 | 20.6 | 83.1 | 39.4 | 41.2 |
| TW-7EL2 | 121.4 | 23.4 | 21.1 | 85.6 | 51.7 | 37.4 |
| W-DA7ES | 81.0 | 21.0 | 23.2 | 88.2 | 24.3 | 28.9 |
新窗口打开
 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图6小麦-长穗偃麦草7EL易位系及7ES附加系的花药和穗子
-->Fig. 6The spikes and anthers of 7EL translocation lines and 7ES addition line
-->
3 讨论
3.1 赤霉病抗性基因所在染色体臂
长穗偃麦草是小麦属的近缘野生种,是小麦远缘杂交育种的重要亲本材料,一直被认为是小麦遗传改良重要的外源基因库。目前研究表明其染色体上携带对赤霉病具有很好抗性的基因。刘登才等[7]利用染色体附加系为材料研究发现,其赤霉病抗性主要归功于1E染色体的作用,同时3E、4E和6E染色体可能有作用微弱的基因存在。通过研究还发现赤霉病的抗性基因位于长穗偃麦草的7E染色体上,并定位于7E长臂上[9-11],但有人通过单花滴注法接种7E的2个端体附加系,则将抗赤霉病的基因定位在7E短臂上[38-39]。通过2年标记选择,本研究获得稳定的带有长穗偃麦草7E染色体的材料,分别来自不同的M2单株,GISH结果明显分为小麦-长穗偃麦草7EL易位系和7ES附加系。对这些材料连续3年的禾谷镰刀菌接种进行赤霉病抗性筛选,结果表明,长穗偃麦草7EL易位系的赤霉病抗性相对于长穗偃麦草7ES附加系要好,也比亲本的抗性好,这与以往的研究结果一致[9-11],支持抗赤霉病基因位于长穗偃麦草7E染色体长臂上。
3.2 小片段易位系的获得
利用电离辐射是诱导染色体异源易位的一种有效方法[15]。辐射后染色体的断裂是随机的,既有本身染色体也有外源染色体,本研究的辐射后代中未见完整的7E染色体充分证实了这一点。通过辐射培育易位系的频率很高,BIE等[16]通过电离辐射普通小麦-簇毛麦双二倍体的花粉,然后将这些花粉授于中国春小麦,从61份M1材料中检测到普通小麦——簇毛麦间易位染色体98条,易位出现频率高达72.1%。根据本研究所获易位系的系谱分析,小麦-长穗偃麦草7EL易位系和7ES附加系就是来自2株M1,通过这2株M1后代的分子标记检测和抗性鉴定而最后获得。通过GISH检验,发现获得的都是染色体的整臂易位系和附加系,并未出现小片段易位。利用种子进行辐射,电离辐射的主要效应是诱导染色体一次断裂,而且染色体断裂也最容易发生在着丝粒区域或着丝粒附近,因而产生的易位主要是整臂易位和较大的末端易位,中间插入易位的频率很低[15,22-23,40-41]。另一种原因是辐射的剂量不够大,导致染色体臂断裂的频率不高;第三点可能是辐射的放射源种类问题,利用快中子对小麦-黑麦双二倍体与普通小麦品种绵阳11杂交种子进行辐射,获得小麦-黑麦外源小片段易位、外源大片段易位和罗伯逊易位,随着辐射剂量的增加,小片段易位的频率也增加[24]。所以,想要获得小片段的易位系,可以对获得的整臂易位系通过辐射成熟中花粉进行授粉,使外源染色体二次断裂和重接,从其杂交后代中进行选择 [17]。
本研究采用60Co辐射种子,将田间赤霉病抗性鉴定、分子标记筛选和基因组原位杂交验证3种方法相结合,培育小麦-长穗偃麦草抗赤易位系。该培育方法有较多优点,目标染色体明确,标记选择效率高,培育周期短,为小麦异源易位系的创建提供了有效途径。在易位系培育的标记检测过程中,先用7E染色体特异标记对所有单株进行检测,再对阳性单株进行长穗偃麦草7EL、7ES特异标记检测。理论上染色体特异引物检测出的植株,有3种情况:标记所在的片段是长臂、标记所在的片段是短臂,或者是长、短臂都有。在分子标记的检测中,理论上染色体标记检测的植株总数和7EL、7ES标记分别检测的总数应该相等,而实际上7EL、7ES标记分别检测的植株总数每代总是小于染色体标记检测的总数。有时染色体标记能检测的单株,7EL或7ES标记却无法检测到。究其原因,在开发分子标记的时候,用的是正常附加系、代换系和亲本的DNA,标记在染色体上的物理位置不清楚。而经过辐射诱变处理的小麦植株中,染色体因断裂-重接而发生缺失、倒位、易位等一系列结构畸变,在DNA水平上则表现为DNA片段的重排而产生碱基序列变异,而且这种变化会持续几秒甚至若干年,有的染色体损伤可以修复,而有的损伤可能进一步加重[42-44]。PCR能扩增的片段相对于整条染色体来说只是一段很微小的DNA,电离辐射的次级效应将使这个很小的区段在易位系和附加系培育过程中可能发生持续的变异而产生遗传多样性,加上标记扩增的区段不同,导致某些区段用染色体标记能检测,而利用染色体臂标记分别检测却未能检测[45]。本研究是利用分子标记检测和赤霉病抗性鉴定相结合的方法对后代进行选择,最后获得的是整臂易位系,一些小片段的易位在选择过程中因没有扩增分子标记而被淘汰。开发更多的染色体特异标记并确定它们在染色体上的位置,对辐射后代小片段易位系的选择具有重要作用。
3.3 小麦-长穗偃麦草7EL易位系的应用
小麦异源易位系是小麦遗传改良中最有用的资源,尤其是小片段的易位系可以直接作为亲本与小麦杂交,丰富小麦基因库,在小麦育种中发挥重要的作用。本研究所获小麦-长穗偃麦草7EL易位系,属于Robertsonian易位,是小麦与其他近缘种培育的易位系中常见类型[12-13,27,46-50],是向小麦导入外源遗传物质的一种优良遗传中间材料和染色体研究材料,一直是小麦遗传育种研究者青睐的特殊种质。抗赤霉病基因(Fhb7)定位于7el2L上,并聚合了Fhb1与Fhb7 2个抗赤霉病基因[31]就是利用7DS·7el2L臂间易位材料。利用所获得的整臂易位系,继续辐射,可获得大量的结构变异体,如获得7E染色体不同长度片段的缺失变异体,就可以进行分子标记在7E染色体上物理定位,也可以获得小麦-长穗偃麦草7E小片段易位系和与其连锁的分子标记,在此基础上进一步筛选抗赤霉病的小片段易位系。也可作为亲本参与抗赤霉病小麦的培育,在杂交后代中,农艺性状的选择可按常规进行,而赤霉病抗性早代可借助分子标记辅助选择,保留农艺性状良好并具有长穗偃麦草7EL标记的单株进行繁殖,在高世代后再进行赤霉病抗性鉴定,可以节省早代赤霉病抗性鉴定,培育具有长穗偃麦草抗赤霉病基因的小麦高产品种。4 结论
利用60Co(30 000 rad)辐射扬麦16与小麦-长穗偃麦草代换系DS7E(7B)杂交的F2种子,通过染色体特异分子标记筛选和基因组原位杂交验证,从衍生的M4代中获得长穗偃麦草7E长臂易位系和短臂附加系,连续3年的赤霉病抗性鉴定表明7EL易位系的赤霉病抗性明显高于7ES附加系,表明赤霉病抗性基因位于7EL。通过赤霉病抗性鉴定、染色体特异分子标记筛选和GISH证实相结合从辐射后代中培育小麦-近缘种染色体易位系,易位片段鉴定快速和准确,培育周期短。(责任编辑 李莉)
The authors have declared that no competing interests exist.
