

1. 中国科学院分子植物科学卓越创新中心/植物生理生态研究所 植物分子遗传国家重点实验室,上海 200032;
2. 河南大学 生命科学学院,河南 开封 457000
收稿日期:2019-07-24;接收日期:2019-10-09
基金项目:科技部重点研发计划(No. 2016YFD0100704)资助
作者简介:晁代印??中国科学院分子植物科学卓越创新中心研究员,课题组组长,博士生导师,中组部“青年****”、国家自然科学基金委“优秀青年基金”获得者,中国植物生理学会植物修复委员会副主任。主要研究方向为植物离子组的遗传基础,研究植物在矿质元素吸收积累和对土壤环境适应能力等方面的分子机制及其适应机制的自然变异基础,在Science、Nature系列、Genes & Development、PLoS Biology以及Plant Cell等国际著名期刊上发表学术论文35篇,目前被他引2 500余次,H-index为20.
摘要:随着近代工业的发展,土壤重金属污染问题日益严重。重金属即使在极低浓度下仍然可以对人畜造成健康上的威胁,因此迫切需要有效的修复方法对土壤进行修复。生物修复,特别是植物修复目前已经成为重金属污染修复的重要手段之一,了解相关植物的重金属解毒和积累分子机制是提高修复效率、解决重金属污染问题的基础。文中以土壤修复方式为起点,结合植物吸收积累重金属以及解毒的相关分子机制研究,探讨了植物修复的发展现状以及趋势。
关键词:重金属土壤污染超积累植物植物修复
Phytoremediation of heavy metal contamination and related molecular mechanisms in plants
Pengyun Wang1,2, Daiyin Chao1


1. National Key Laboratory of Plant Molecular Genetics, CAS Center for Excellence in Molecular Plant Sciences, Shanghai Institute of Plant Physiology and Ecology, Chinese Academy of Sciences, Shanghai 200032, China;
2. School of Life Sciencse, Henan University, Kaifeng 457000, Henan, China
Received: July 24, 2019; Accepted: October 9, 2019
Supported by: The Ministry of Science and Technology Key R&D Program (No. 2016YFD0100704)
Corresponding author: Daiyin Chao. Tel/Fax: +86-21-54924158; E-mail: dychao@sibs.ac.cn.
Abstract: With the development of modern industry, heavy metal pollution of soil becomes more and more serious. Heavy metals can cause serious health problems to humans and animals even at very low concentrations. Thus, it is urgent to remediate the contaminated soils by effective methods. Different remediation strategies have been reported to remove heavy metals from contaminated soil, among which phytoremediation is the most important one. Understanding the mechanisms underlying heavy metal accumulation and detoxification in plants is one of the key points for phytoremediation. In this review, we try to summarize the progresses and trends on phytoremediation and related molecular mechanisms, and discuss the prospects for the future research.
Keywords: heavy metalsoil contaminationhyperaccumulatorphytoremediation
土壤是生态环境的重要组成部分,是人类赖以生存的重要资源。随着现代工业化的快速发展,生活及工业废水的排放、农业肥料的大量使用、生活垃圾的随意堆积等都会导致大量不同的污染物进入土壤中,其中重金属元素的积累是土壤污染中的突出问题。重金属通常是指原子序数大于20、元素密度大于5 g/cm3的元素,包括锌、铜、铁、镉、砷等[1]。土壤重金属污染不易被发现而且容易造成严重后果,过量的重金属会直接危害植物和土壤微生物的生长发育,进而通过食物链影响人类自身健康。如何修复重金属污染土壤,维持良好的土壤环境质量成为当前非常重要的研究课题之一。
1 重金属对生态环境的危害1.1 重金属重金属是一类金属的总称,在现有的90多种天然存在的金属中,有53种被归为重金属元素。其中有一些重金属如铜、锌、钼、铁等在低浓度下是植物生长所必需的元素,但当它们的浓度超过一定范围后也会损害植物和其他生物的生存,这些元素属于广义的重金属范畴,而更多的其他重金属(包括一些类重金属),如铅、汞、镉、砷(类重金属)等元素,在很低的浓度时就会引起动植物的毒害作用,可以认为是狭义的重金属,这些元素是本文讨论的重点[1]。
1.2 重金属污染对生物的毒害作用土壤重金属的污染造成的影响是长久性的,土壤质量严重下降的同时还会影响食品的生产及质量。植物通过吸附、络合等作用吸收土壤中的重金属离子,这些过程会受到土壤pH和土壤结构等因素的影响。虽然不同重金属的毒理各有不同,但是在重金属污染地区生长的植物由于体内重金属氧化还原作用产生的活性氧等,生理代谢水平都会发生相应的改变。有研究表明,重金属积累会抑制植物生长,导致叶片黄化、发育受阻、生物产量降低等现象[2-4]。同样,长期受到重金属毒害的人类会产生各种不良病症,例如癌症、心血管问题、肾脏中毒、肝脏中毒等[5-8]。因此了解重金属在植物中的作用机制,控制重金属污染土壤所造成的影响是非常重要的。
2 重金属污染土壤修复类型土壤重金属离子浓度增加后,随着时间的推移通过生物富集机制进行传递,进而对整个生态系统产生毒性。现在的重金属污染土壤修复方法主要分为两种:物理和化学修复、生物修复。
2.1 物理和化学修复物理和化学修复主要利用物理原理和特定的化学试剂清除土壤中的重金属。化学试剂经过与重金属发生氧化还原、吸附、络合等反应,降低其生物有效性进而减轻毒害作用。修复方式主要包含以下4种。第一,直接对被污染的土壤进行更换。第二,利用重金属离子带电荷的特性,在土壤中插入电极使其在电极处集中富集从而分离重金属,又名电动修复。研究发现,电动修复能够高效地富集重金属从而减少土壤中重金属的含量[9-10]。第三,土壤淋洗可以利用螯合、溶解等作用分离去除重金属离子[11]。第四,土壤固化/稳定化,主要是通过吸附、沉淀等作用钝化重金属,从而降低重金属在土壤中的毒性[12-13]。物理和化学修复方法简单,但由于代价高或者不能彻底去除土壤中的重金属,应用上具有一定的局限性。
2.2 生物修复生物修复是指利用生态系统自身富集有害物质或者改变有害物质的能力去除土壤中污染物的方法,在重金属污染物的生物修复方面主要有微生物修复技术以及植物修复技术两种方式。生物修复技术费用低、不容易产生二次污染并且可以改善土壤肥力,适合进行大面积的推广。
2.2.1 微生物修复微生物是重金属污染土壤环境修复的重要成员,具有积累重金属或者改变重金属化学状态的天然微生物或经过遗传工程改造的微生物都可以修复污染的土壤环境。重金属离子进入微生物体内后,通过微生物体内的新陈代谢储存于细胞内的不同部位,最终完成对受污染土壤的修复过程。微生物主要是通过溶解、吸附沉淀和转化三种方式结合并去除土壤中的重金属离子[14]。溶解是指微生物分泌一些有机酸或酶等物质活化重金属;吸附沉淀是指通过细胞表面或分泌的代谢产物吸附、沉淀重金属;转化主要是指利用自身的氧化还原、甲基化等作用改变重金属的价态,降低重金属的毒性。在细菌中,革兰氏阳性菌细胞壁的肽聚糖层、革兰氏阴性菌细胞壁的脂蛋白以及磷脂都可以结合重金属,修复受污染的土壤环境,是良好的重金属污染修复剂[15-16]。真菌吸收重金属离子后也可以通过转换金属离子价态等方式解除重金属对自身造成的危害[15]。此外,联合使用多种菌株,通过不同菌株的协同作用,使得微生物修复技术成为更为有效的重金属污染修复方法[17]。常见的商用微生物有黄色考克氏菌Kocuria flava、芽孢八叠球菌属细菌Sporosarcina ginsengisoli以及变色曲霉菌Aspergillus versicolor等[18]。
2.2.2 植物修复自然或人工培育的特殊植物可以通过根系吸收土壤中的重金属污染物,达到改良土壤的目的。植物修复技术主要有植物提取、植物固定以及植物挥发技术。植物提取主要是将重金属元素从土壤中转移至超积累植物地上部,降低土壤中重金属的含量[19]。植物固定是指利用植物根系通过络合、吸附等作用固定土壤中的重金属,阻止其在环境中的扩散[18]。植物挥发在重金属修复方面的应用主要是针对可挥发的重金属汞,植物根系吸收后转移至地上部后挥发进入空气中从而减轻危害。这种植物挥发有效性还没有得到广泛的证实,因此该提法目前仍然存在争议[20]。一些特殊的超积累植物可以在维持自身生长的情况下特异性地富集某种重金属离子,其地上部含量可以超过该重金属在其他普通植物体内积累量的百倍甚至千倍以上,从而达到将土壤中的重金属元素高效地转移至植物体内,减少重金属污染的效果[21]。超积累植物通常根系发达,具备对土壤重金属高吸附能力和转移至地上部的能力。过量的重金属离子可以积累在液泡中,这使得超积累植物在较高的重金属浓度下也能够存活[22]。
3 植物积累重金属及其解毒的分子机制超积累植物在积累重金属和解毒方面既具有其特殊性,又与普通植物具有一定的共性,因此了解超积累植物和非超积累的重金属富集植物积累重金属以及解除重金属毒性的机制,对于植物修复重金属污染土壤的研究都具有重要的意义。现有研究表明,植物主要通过螯合作用、细胞壁沉淀作用、区隔化作用、抗氧化系统解除重金属的危害[3]。下面从重金属转运蛋白、重金属的代谢以及螯合作用3个方面的进展开展介绍。
3.1 植物重金属转运蛋白研究植物对重金属元素稳态的维持是一个严密的调控过程,在当前研究中已经发现多种参与重金属响应的相关基因。这些重金属转运蛋白的细胞、组织定位各有不同,分别发挥不同的作用(图 1)。
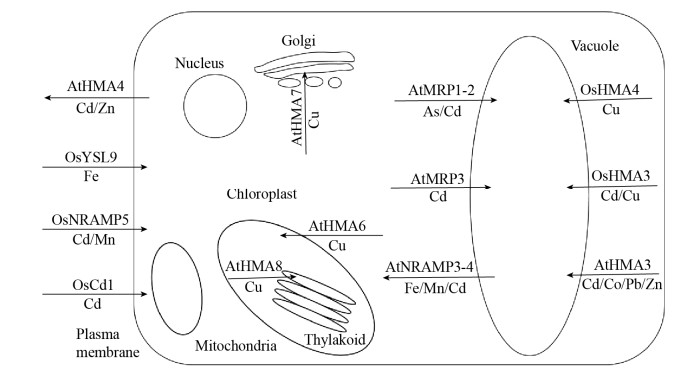 |
| 图 1 植物中重金属运输相关蛋白的功能和亚细胞定位 Fig. 1 The functions and subcellular localization of heavy metal transporters in plants. |
| 图选项 |
3.1.1 重金属ATP酶(HMA)蛋白家族重金属ATP酶(Heavy-metal ATPases,HMA)是P-type ATPases转运蛋白家族的一个亚家族,广泛存在于各种生物中,主要利用水解ATP产生的能量驱动一些重金属离子的跨膜转运,包括Ag+、Zn2+、Cd2+、Cu2+、Ni2+等金属离子[23] (图 1)。目前在拟南芥Arabidopsis thaliana中发现了8个HMA家族成员,其中AtHMA3位于液泡膜,过表达植株对镉的耐受性显著提高,同时AtHMA3也是控制拟南芥叶片镉含量变化的关键基因[24] (图 1)。AtHMA4定位于质膜,在根、茎、叶的维管组织中都有表达,负责镉和锌从地下部到地上部的运输,并且与AtHMA3类似,其遗传变异也是拟南芥叶片锌含量变化的重要原因[25] (图 1)。超积累植物Arabidopsis halleri叶片中锌和镉的浓度高达2.2%和0.28%,而研究表明这种超积累很大程度上可以归因于HMA4基因拷贝数的扩增以及顺式调控序列的改变,且这种遗传上的变异可能是A. halleri适应高镉高锌环境的遗传基础及其物种形成的第一步[26]。AtHMA8和AtHMA6都位于叶绿体上参与叶绿体中铜的转运过程[27] (图 1)。AtHMA7是一种铜转运蛋白,参与种子萌发过程[28-29] (图 1)。在水稻Oryza sativa中共有9个HMA家族成员,其中OsHMA3和OsHMA5分别参与镉、铜从地下部转运至地上部的长距离转运过程,过表达OsHMA3增加了水稻对镉的耐受性,其籽粒中镉的含量下降了94%–98%,具有很好的应用价值[30-32] (图 1)。OsHMA4定位在液泡膜上,将细胞内多余的铜隔离至液泡中,该基因功能丧失会导致水稻体内更多的铜转运至地上部,水稻籽粒中铜的含量明显增加[33] (图 1)。除此之外,HMA家族成员也是超积累植物的关键解毒蛋白。以镉超积累植物伴矿景天Sedum plumbizincicola为例,SpHMA1基因的表达量比其同源基因在非超积累植物东南景天Sedum alfredii高200倍以上,主要参与细胞内叶绿体对镉的外排解毒过程[34]。SpHMA3负责将细胞质内的镉区隔化进入液泡中,减少其在胞质中的积累,其突变体植株地上部新生组织生长受到了明显抑制[35]。上述基因都在维持伴矿景天在含镉土壤环境中的正常生长发育中发挥了重要作用。
3.1.2 ABC转运蛋白家族ABC (ATP-binding cassette transporter)转运蛋白家族是一类膜整合蛋白,利用水解ATP的能量对多种生物分子进行跨膜转运,是植物体内最大的蛋白家族之一[36]。拟南芥内ABC转运蛋白家族与重金属转运相关的主要是多效抗药性亚家族(Pleiotropic drug resistance,PDR)和广谱抗药性相关蛋白家族(Multidrug resistance-associated protein,MRP),以下几个是拟南芥内研究比较清楚的转运蛋白。AtMRP1、AtMRP2属于液泡膜定位的转运蛋白,可以与植物螯合肽(PCs)结合形成复合物,参与拟南芥对砷、镉、汞等重金属离子的解毒作用,其双突突变体对不同浓度的镉和汞都具有很高的敏感性[37-40] (图 1)。AtMRP3也可以运输Cd-PCs复合物,过表达该基因的转基因植株对镉的抗性明显增强[41] (图 1)。
3.1.3 自然抵抗相关巨噬细胞(NRAMP)蛋白家族NRAMP是生物体内一类大的转运蛋白家族,转运Mn2+、Zn2+、Cd2+等多种离子至细胞质中[42]。目前在拟南芥中共发现了6个NRAMP家族成员,其中AtNRAMP1定位于质膜,参与拟南芥根部对锰的吸收,而AtNRAMP2可以保护细胞免受因为锰氧化还原产生的活性氧的毒害作用,过表达AtNRAMP2促进植株在低锰环境下的生长[43-44]。AtNRAMP3和AtNRAMP4都定位于液泡膜上,转运足够的铁和锰参与种子的萌发和光合作用[45] (图 1)。在水稻中,OsNRAMP1除了介导水稻根部对镉和锰的吸收外,还可以增加植株对镉和砷的抗性[46]。OsNRAMP5定位于细胞质膜上,负责水稻根部对外界环境中Mn2+、Cd2+、Fe2+金属离子的吸收,其突变体籽粒中镉的含量大幅降低,该基因在低镉水稻品种的培育中具有良好的实际应用前景[47-50] (图 1)。
3.1.4 黄色条纹转运蛋白(YSL)家族黄色条纹转运蛋白(Yellow stripe-like transporter,YSL)的主要功能是转运金属与金属螯合物的复合物,包括尼克烟酰胺(NA)、PCs、2′-脱氧麦根酸(DMA)、谷胱甘肽(GSH)等物质。BjYSL7是一种质膜转运蛋白,参与芥菜Brassica juncea体内Cd和Ni从地下部到地上部的长距离运输,其过表达植株对镉和镍的耐受性明显提高[51]。SnYSL3定位于质膜,在过量镉处理条件下表达量明显上调,在龙葵Solanum nigrum应对镉胁迫中发挥着重要作用[52]。拟南芥基因AtYSL4和AtYSL6分别定位于液泡膜和叶绿体被膜上,两者通过调控铁在叶绿体中的释放和积累参与铁在叶绿体中的稳态[53]。OsYSL9是定位于质膜的Fe(Ⅱ)-NA和Fe(Ⅲ)-DMA的转运蛋白,负责种子发育过程中铁的运输[54] (图 1)。OsYSL13是定位于质膜的转运蛋白,参与水稻体内铁的分配过程[55]。OsYSL16可以转运Cu-NA以及Fe-DMA复合物,分配铁和铜到不同的水稻器官中[56-59]。
3.2 植物新型砷酸盐还原酶的克隆和功能研究砷酸盐与磷酸盐在化学性质上高度相似,因此生命体在摄入磷酸盐时会同时将砷酸盐摄入体内,从而造成损害。在细菌和酵母中,砷酸盐还原酶可以将砷酸盐还原为亚砷酸盐,从而将砷与磷区分开来,并可以将还原成三价砷的亚砷酸盐排至体外降低对细胞的损伤。在细菌中,编码砷酸盐还原酶的基因为ArsC,而酵母中则为ACR2[60-61]。虽然有研究者通过同源克隆分离到拟南芥和水稻的ACR2的同源基因,并在体外证明其具有砷酸盐还原酶的功能,但是却一直缺乏体内证据。更重要的是有研究者发现,当植物ACR2基因完全突变后并没有砷积累或解毒的表型,表明ACR2在植物体内可能并不具有砷酸盐还原酶的功能[62]。而我们课题组通过全基因组关联分析研究,在拟南芥中克隆了控制其叶片砷含量变化的关键基因HAC1 (High Arsenic Content 1),进一步研究揭示该基因编码植物砷酸盐还原酶[63]。深入研究表明,HAC1主要在拟南芥根部外皮层和根毛细胞中表达,因此可以将刚吸收入根部细胞中的砷酸盐迅速还原成亚砷酸盐并排出体外,从而极大地降低拟南芥地上部砷的含量[63]。另有独立的研究通过不同拟南芥生态型砷耐受性的自然变异克隆了HAC1的等位基因,并将其命名为ATQ1,同样证实了其编码蛋白的砷酸盐还原酶功能[64]。
水稻中,HAC1的同源基因OsHAC1;1与OsHAC1;2在根表皮细胞和中柱中表达较强,其超表达植株中对As(Ⅴ)的耐受性提高,并且地上部砷的含量也明显降低[65]。OsHAC4主要在根中表达,亚细胞定位与OsHAC1;1和OsHAC1;2类似,可以降低砷酸还原酶缺失突变体△arsC对As(Ⅴ)的敏感性,Oshac4突变体中砷含量明显提高[66]。除此之外,在对砷超积累植物蜈蚣草Pteris vittata的研究中发现了PvGSTF1同样具有砷酸盐还原酶的功能,并与另外两个蛋白PvGAPC1和PvOCT4协同调控了一个与细菌耐砷类似的砷积累和解毒机制[67]。
3.3 植物新型镉螯合肽及转运蛋白的研究镉进入植物体内后可以通过结合常见的PCs、MTs、GSH等螯合物进行转运,这些螯合物的含量直接影响镉的含量[68]。植物防御素广泛存在于植物中,主要参与植物抗菌作用,同时还与植物对重金属的耐受性有关。拟南芥基因PDF1s (Plant Defensin Type 1)参与锌在植物体内的运输过程[69-70]。拟南芥防御素蛋白AtPDF2.5定位于细胞壁,主要表达于根木质部维管束中,促进细胞质中积累的镉的外流。异源表达AtPDF2.5在水稻中可以增加植株对镉的耐受性,其突变体pdf2.5降低了对镉的解毒能力[71]。水稻防御素类蛋白OsCAL1定位于细胞壁上,可以螯合细胞质中的镉外排至细胞外。它主要在水稻的根、节中、叶鞘中表达,与镉结合后经木质部进行长距离运输转运至地上部,在水稻叶片中积累镉但不增加籽粒中镉的含量,是重要的修复性作物参考之一[72]。除此之外,利用全基因组关联分析技术研究发现了一个参与镉转运的主要协助转运蛋白超家族(Major facilitator superfamily,MFS)成员OsCd1,它主要在根外皮层、中柱细胞以及内皮层中表达,定位在细胞质膜上,其突变体oscd1对镉的吸收效率以及在籽粒中镉的含量都显著下降。OsCd1基因发生突变是造成籼稻和粳稻籽粒中镉差异的主要原因,OsCd1v449主要存在于粳稻中,将其转入籼稻后,含有OsCd1v449的水稻近等基因系籽粒中镉的含量明显降低,适合应用于新型低镉水稻品种的培育[73] (图 1)。
4 展望工业高速发展的同时,土壤环境问题也日益显著,如何更好地保护和修复土壤环境对于我国的可持续发展至关重要。生物修复为解决土壤环境污染问题提供了一个良好的解决方案。但是目前发现的超积累植物和合适的微生物种类较少,实用修复价值不高,能够解决的重金属环境污染能力有限。土壤环境保护可以从以下几个方向进行:1)减少人类生活、工业生产对于土壤环境的破坏,实行切实可行的保护土壤环境政策。2)根据实际情况选择多种合适的土壤修复技术,进行复合型修复以提高重金属污染土壤修复效率。3)选取周期短、吸收效率高、回收效率高等更优秀的超积累植物,更好地发挥植物修复技术在重金属污染中的作用。4)利用转基因技术,培育可以超积累重金属的微生物和植物。土壤环境与人类的生存息息相关,但是目前关于重金属污染土壤修复的研究能够转化到实际应用的并不多,如何更好地恢复受污染的土壤环境仍有很长的路要走。
参考文献
| [1] | Schutzendubel A, Polle A. Plant responses to abiotic stresses: heavy metal-induced oxidative stress and protection by mycorrhization. J Exp Bot, 2002, 53(372): 1351-1365. |
| [2] | Rizwan M, Ali S, Ibrahim M, et al. Mechanisms of silicon-mediated alleviation of drought and salt stress in plants: a review. Environ Sci Pollut Res Int, 2015, 22(20): 15416-15431. DOI:10.1007/s11356-015-5305-x |
| [3] | Shahid M, Dumat C, Khalid S, et al. Foliar heavy metal uptake, toxicity and detoxification in plants: A comparison of foliar and root metal uptake. J Hazard Mater, 2017, 325: 36-58. DOI:10.1016/j.jhazmat.2016.11.063 |
| [4] | Shi TR, Ma J, Wu X, et al. Inventories of heavy metal inputs and outputs to and from agricultural soils: a review. Ecotoxicol Environ Saf, 2018, 164: 118-124. DOI:10.1016/j.ecoenv.2018.08.016 |
| [5] | Praveena SM, Omar NA. Heavy metal exposure from cooked rice grain ingestion and its potential health risks to humans from total and bioavailable forms analysis. Food Chem, 2017, 235: 203-211. DOI:10.1016/j.foodchem.2017.05.049 |
| [6] | Jafari A, Kamarehie B, Ghaderpoori M, et al. The concentration data of heavy metals in Iranian grown and imported rice and human health hazard assessment. Data in Brief, 2018, 16: 453-459. DOI:10.1016/j.dib.2017.11.057 |
| [7] | Ma YK, Egodawatta P, McGree J, et al. Human health risk assessment of heavy metals in urban stormwater. Sci Total Environ, 2016, 557-558: 764-772. DOI:10.1016/j.scitotenv.2016.03.067 |
| [8] | Tepanosyan G, Sahakyan L, Belyaeva O, et al. Continuous impact of mining activities on soil heavy metals levels and human health. Sci Total Environ, 2018, 639: 900-909. DOI:10.1016/j.scitotenv.2018.05.211 |
| [9] | Wei XN, Guo SH, Wu B, et al. Effects of reducing agent and approaching anodes on chromium removal in electrokinetic soil remediation. Front Environ Sci Eng, 2016, 10(2): 253-261. DOI:10.1007/s11783-015-0791-0 |
| [10] | Peng Z, Jin CJ, Sun ZF, et al. Assessment of acid enhancement schemes for electrokinetic remediation of Cd/Pb contaminated soil. Water, Air, Soil Pollut, 2016, 227(6): 217. DOI:10.1007/s11270-016-2879-y |
| [11] | Saeedi M, Li LY, Grace JR. Simultaneous removal of polycyclic aromatic hydrocarbons and heavy metals from natural soil by combined non-ionic surfactants and EDTA as extracting reagents: laboratory column tests. J Environ Manage, 2019, 248: 109258. DOI:10.1016/j.jenvman.2019.07.029 |
| [12] | Yu K, Xu J, Jiang XH, et al. Stabilization of heavy metals in soil using two organo-bentonites. Chemosphere, 2017, 184: 884-891. DOI:10.1016/j.chemosphere.2017.06.040 |
| [13] | Bolan N, Kunhikrishnan A, Thangarajan R, et al. Remediation of heavy metal(loid)s contaminated soils—to mobilize or to immobilize?. J Hazard Mater, 2014, 266: 141-166. DOI:10.1016/j.jhazmat.2013.12.018 |
| [14] | Jan AT, Azam M, Ali A, et al. Prospects for exploiting bacteria for bioremediation of metal pollution. Crit Rev Env Sci Technol, 2014, 44(5): 519-560. DOI:10.1080/10643389.2012.728811 |
| [15] | Ayangbenro AS, Babalola OO. A new strategy for heavy metal polluted environments: a review of microbial biosorbents. Int J Environ Res Public Health, 2017, 14(1): 94. DOI:10.3390/ijerph14010094 |
| [16] | Srivastava S, Agrawal SB, Mondal MK. A review on progress of heavy metal removal using adsorbents of microbial and plant origin. Environ Sci Pollut Res Int, 2015, 22(20): 15386-15415. DOI:10.1007/s11356-015-5278-9 |
| [17] | Kang CH, Kwon YJ, So JS. Bioremediation of heavy metals by using bacterial mixtures. Ecol Eng, 2016, 89: 64-69. DOI:10.1016/j.ecoleng.2016.01.023 |
| [18] | Ojuederie OB, Babalola OO. Microbial and plant-assisted bioremediation of heavy metal polluted environments: a review. Int J Environ Res Public Health, 2017, 14(12): 1504. DOI:10.3390/ijerph14121504 |
| [19] | Jutsz AM, Gnida A. Mechanisms of stress avoidance and tolerance by plants used in phytoremediation of heavy metals. Arch Environ Prot, 2015, 41(4): 104-114. DOI:10.1515/aep-2015-0045 |
| [20] | Wang JX, Feng XB, Anderson CWN, et al. Remediation of mercury contaminated sites-a review. J Hazard Mater, 2012, 221-222: 1-18. DOI:10.1016/j.jhazmat.2012.04.035 |
| [21] | Muszyńska E, Hanus-Fajerska E. Why are heavy metal hyperaccumulating plants so amazing?. Biotechnologia, 2015, 96(4): 265-271. |
| [22] | Sharma SS, Dietz KJ, Mimura T. Vacuolar compartmentalization as indispensable component of heavy metal detoxification in plants. Plant Cell Environ, 2016, 39(5): 1112-1126. DOI:10.1111/pce.12706 |
| [23] | Rosenzweig AC, Argüello JM. Chapter five-toward a molecular understanding of metal transport by P1B-Type ATPases. Curr Top Membr, 2012, 69: 113-136. DOI:10.1016/B978-0-12-394390-3.00005-7 |
| [24] | Chao DY, Silva A, Baxter I, et al. Genome-wide association studies identify heavy metal ATPase3 as the primary determinant of natural variation in leaf cadmium in Arabidopsis thaliana. PLoS Genet, 2012, 8(9): e1002923. DOI:10.1371/journal.pgen.1002923 |
| [25] | Chen ZR, Kuang L, Gao YQ, et al. AtHMA4 drives natural variation in leaf Zn concentration of Arabidopsis thaliana. Front Plant Sci, 2018, 9: 270. DOI:10.3389/fpls.2018.00270 |
| [26] | Hanikenne M, Talke IN, Haydon MJ, et al. Evolution of metal hyperaccumulation required cis-regulatory changes and triplication of HMA4. Nature, 2008, 453(7193): 391-395. DOI:10.1038/nature06877 |
| [27] | Sautron E, Mayerhofer H, Giustini C, et al. HMA6 and HMA8 are two chloroplast Cu+-ATPases with different enzymatic properties. Biosci Rep, 2015, 35(3): e00201. DOI:10.1042/BSR20150065 |
| [28] | Li WB, Lacey RF, Ye YJ, et al. Triplin, a small molecule, reveals copper ion transport in ethylene signaling from ATX1 to RAN1. PLoS Genet, 2017, 13(4): e1006703. DOI:10.1371/journal.pgen.1006703 |
| [29] | Liu PW, Qi M, Wang YQ, et al. Arabidopsis RAN1 mediates seed development through its parental ratio by affecting the onset of endosperm cellularization. Mol Plant, 2014, 7(8): 1316-1328. DOI:10.1093/mp/ssu041 |
| [30] | Deng FL, Yamaji N, Xia JX, et al. A member of the heavy metal P-type ATPase OsHMA5 is involved in xylem loading of copper in rice. Plant Physiol, 2013, 163(3): 1353-1362. DOI:10.1104/pp.113.226225 |
| [31] | Sasaki A, Yamaji N, Ma JF. Overexpression of OsHMA3 enhances Cd tolerance and expression of Zn transporter genes in rice. J Exp Bot, 2014, 65(20): 6013-6021. DOI:10.1093/jxb/eru340 |
| [32] | Lu CN, Zhang LX, Tang Z, et al. Producing cadmium-free Indica rice by overexpressing OsHMA3. Environ Int, 2019, 126: 619-626. DOI:10.1016/j.envint.2019.03.004 |
| [33] | Huang XY, Deng FL, Yamaji N, et al. A heavy metal P-type ATPase OsHMA4 prevents copper accumulation in rice grain. Nat Commun, 2016, 7: 12138. DOI:10.1038/ncomms12138 |
| [34] | Zhao HX, Wang LS, Zhao FJ, et al. SpHMA1 is a chloroplast cadmium exporter protecting photochemical reactions in the Cd hyperaccumulator Sedum plumbizincicola. Plant Cell Environ, 2019, 42(4): 1112-1124. DOI:10.1111/pce.13456 |
| [35] | Liu H, Zhao HX, Wu LH, et al. Heavy metal ATPase 3 (HMA3) confers cadmium hypertolerance on the cadmium/zinc hyperaccumulator Sedum plumbizincicola. New Phytol, 2017, 215(2): 687-698. DOI:10.1111/nph.14622 |
| [36] | Hwang JU, Song WY, Hong D, et al. Plant ABC transporters enable many unique aspects of a terrestrial plant's lifestyle. Mol Plant, 2016, 9(3): 338-355. DOI:10.1016/j.molp.2016.02.003 |
| [37] | Raichaudhuri A. Arabidopsis thaliana MRP1 (AtABCC1) nucleotide binding domain contributes to arsenic stress tolerance with serine triad phosphorylation. Plant Physiol Biochem, 2016, 108: 109-120. DOI:10.1016/j.plaphy.2016.07.005 |
| [38] | Raichaudhuri A, Peng MS, Naponelli V, et al. Plant vacuolar ATP-binding cassette transporters that translocate folates and antifolates in vitro and contribute to antifolate tolerance in vivo. J Biol Chem, 2009, 284(13): 8449-8460. DOI:10.1074/jbc.M808632200 |
| [39] | Burla B, Pfrunder S, Nagy R, et al. Vacuolar transport of abscisic acid glucosyl ester is mediated by ATP-binding cassette and proton-antiport mechanisms in Arabidopsis. Plant Physiol, 2013, 163(3): 1446-1458. DOI:10.1104/pp.113.222547 |
| [40] | Park J, Song WY, Ko D, et al. The phytochelatin transporters AtABCC1 and AtABCC2 mediate tolerance to cadmium and mercury. Plant J, 2012, 69(2): 278-288. DOI:10.1111/j.1365-313X.2011.04789.x |
| [41] | Brunetti P, Zanella L, De Paolis A, et al. Cadmium-inducible expression of the ABC-type transporter AtABCC3 increases phytochelatin- mediated cadmium tolerance in Arabidopsis. J Exp Bot, 2015, 66(13): 3815-3829. DOI:10.1093/jxb/erv185 |
| [42] | Nevo Y, Nelson N. The NRAMP family of metal-ion transporters. Biochim Biophys Acta, 2006, 1763(7): 609-620. DOI:10.1016/j.bbamcr.2006.05.007 |
| [43] | Alejandro S, Cailliatte R, Alcon C, et al. Intracellular distribution of manganese by the trans-golgi network transporter NRAMP2 is critical for photosynthesis and cellular redox homeostasis. Plant Cell, 2017, 29(12): 3068-3084. DOI:10.1105/tpc.17.00578 |
| [44] | Gao HL, Xie WX, Yang CH, et al. NRAMP2, a trans-Golgi network-localized manganese transporter, is required for Arabidopsis root growth under manganese deficiency. New Phytol, 2018, 217(1): 179-193. DOI:10.1111/nph.14783 |
| [45] | Bastow EL, Garcia de la Torre VS, Maclean AE, et al. Vacuolar iron stores gated by NRAMP3 and NRAMP4 are the primary source of iron in germinating seeds. Plant Physiol, 2018, 177(3): 1267-1276. DOI:10.1104/pp.18.00478 |
| [46] | Tiwari M, Sharma D, Dwivedi S, et al. Expression in Arabidopsis and cellular localization reveal involvement of rice NRAMP, OsNRAMP1, in arsenic transport and tolerance. Plant Cell Environ, 2014, 37(1): 140-152. DOI:10.1111/pce.12138 |
| [47] | Tang L, Mao BG, Li YK, et al. Knockout of OsNramp5 using the CRISPR/Cas9 system produces low Cd-accumulating indica rice without compromising yield. Sci Rep, 2017, 7(1): 14438. DOI:10.1038/s41598-017-14832-9 |
| [48] | Sasaki A, Yamaji N, Yokosho K, et al. Nramp5 is a major transporter responsible for manganese and cadmium uptake in rice. Plant Cell, 2012, 24(5): 2155-2167. DOI:10.1105/tpc.112.096925 |
| [49] | Ishikawa S, Ishimaru Y, Igura M, et al. Ion-beam irradiation, gene identification, and marker-assisted breeding in the development of low-cadmium rice. Proc Natl Acad Sci USA, 2012, 109(47): 19166-19171. DOI:10.1073/pnas.1211132109 |
| [50] | Yang M, Zhang YY, Zhang LJ, et al. OsNRAMP5 contributes to manganese translocation and distribution in rice shoots. J Exp Bot, 2014, 65(17): 4849-4861. DOI:10.1093/jxb/eru259 |
| [51] | Wang JW, Li Y, Zhang YX, et al. Molecular cloning and characterization of a Brassica juncea yellow stripe-like gene, BjYSL7, whose overexpression increases heavy metal tolerance of tobacco. Plant Cell Rep, 2013, 32(5): 651-662. DOI:10.1007/s00299-013-1398-1 |
| [52] | Feng SS, Tan JJ, Zhang YX, et al. Isolation and characterization of a novel cadmium-regulated Yellow Stripe-Like transporter (SnYSL3) in Solanum nigrum. Plant Cell Rep, 2017, 36(2): 281-296. DOI:10.1007/s00299-016-2079-7 |
| [53] | Divol F, Couch D, Conéjéro G, et al. The Arabidopsis YELLOW STRIPE LIKE4 and 6 transporters control iron release from the chloroplast. Plant Cell, 2013, 25(3): 1040-1055. DOI:10.1105/tpc.112.107672 |
| [54] | Senoura T, Sakashita E, Kobayashi T, et al. The iron-chelate transporter OsYSL9 plays a role in iron distribution in developing rice grains. Plant Mol Biol, 2017, 95(4/5): 375-387. |
| [55] | Zhang C, Shinwari KI, Luo L, et al. OsYSL13 is involved in iron distribution in rice. Int J Mol Sci, 2018, 19(11): 3537. DOI:10.3390/ijms19113537 |
| [56] | Kakei Y, Ishimaru Y, Kobayashi T, et al. OsYSL16 plays a role in the allocation of iron. Plant Mol Biol, 2012, 79(6): 583-594. DOI:10.1007/s11103-012-9930-1 |
| [57] | Lee S, Ryoo N, Jeon JS, et al. Activation of rice Yellow Stripe1-Like 16 (OsYSL16) enhances iron efficiency. Mol Cells, 2012, 33(2): 117-126. DOI:10.1007/s10059-012-2165-9 |
| [58] | Zheng LQ, Yamaji N, Yokosho K, et al. YSL16 is a phloem-localized transporter of the copper- nicotianamine complex that is responsible for copper distribution in rice. Plant Cell, 2012, 24(9): 3767-3782. DOI:10.1105/tpc.112.103820 |
| [59] | Zhang C, Lu WH, Yang Y, et al. OsYSL16 is required for preferential Cu distribution to floral organs in rice. Plant Cell Physiol, 2018, 59(10): 2039-2051. DOI:10.1093/pcp/pcy124 |
| [60] | Rosen BP. Biochemistry of arsenic detoxification. FEBS Letters, 2002, 529(1): 86-92. DOI:10.1016/S0014-5793(02)03186-1 |
| [61] | Mukhopadhyay R, Rosen BP. Arsenate reductases in prokaryotes and eukaryotes. Environ Health Perspect, 2002, 110(S5): 745-748. |
| [62] | Liu WJ L, Schat H, Bliek M, et al. Knocking out ACR2 does not affect arsenic redox status in Arabidopsis thaliana: implications for as detoxification and accumulation in plants. PLoS ONE, 2012, 7(8): e42408. DOI:10.1371/journal.pone.0042408 |
| [63] | Chao DY, Chen Y, Chen JG, et al. Genome-wide association mapping identifies a new arsenate reductase enzyme critical for limiting arsenic accumulation in plants. PLoS Biol, 2014, 12(12): e1002009. DOI:10.1371/journal.pbio.1002009 |
| [64] | Sánchez-Bermejo E, Castrillo G, del Llano B, et al. Natural variation in arsenate tolerance identifies an arsenate reductase in Arabidopsis thaliana. Nat Commun, 2014, 5: 4617. DOI:10.1038/ncomms5617 |
| [65] | Shi SL, Wang T, Chen ZR, et al. OsHAC1;1 and OsHAC1;2 function as arsenate reductases and regulate arsenic accumulation. Plant Physiol, 2016, 172(3): 1708-1719. DOI:10.1104/pp.16.01332 |
| [66] | Xu JM, Shi SL, Wang L, et al. OsHAC4 is critical for arsenate tolerance and regulates arsenic accumulation in rice. New Phytol, 2017, 215(3): 1090-1101. DOI:10.1111/nph.14572 |
| [67] | Cai C, Lanman NA, Withers KA, et al. Three genes define a bacterial-like arsenic tolerance mechanism in the arsenic hyperaccumulating fern Pteris vittata. Curr Biol, 2019, 29(10): 1625-1633. DOI:10.1016/j.cub.2019.04.029 |
| [68] | Verbruggen N, Hermans C, Schat H. Mechanisms to cope with arsenic or cadmium excess in plants. Curr Opin Plant Biol, 2009, 12(3): 364-372. DOI:10.1016/j.pbi.2009.05.001 |
| [69] | Nguyen NNT, Ranwez V, Vile D, et al. Evolutionary tinkering of the expression of PDF1s suggests their joint effect on zinc tolerance and the response to pathogen attack. Front Plant Sci, 2014, 5: 70. |
| [70] | Shahzad Z, Ranwez V, Fizames C, et al. Plant Defensin type 1 (PDF1): protein promiscuity and expression variation within the Arabidopsis genus shed light on zinc tolerance acquisition in Arabidopsis halleri. New Phytol, 2013, 200(3): 820-833. DOI:10.1111/nph.12396 |
| [71] | Luo JS, Yang Y, Gu TY, et al. The Arabidopsis defensin gene AtPDF2.5 mediates cadmium tolerance and accumulation. Plant Cell Environ, 2019, 42(9): 2681-2695. DOI:10.1111/pce.13592 |
| [72] | Luo JS, Huang J, Zeng DL, et al. A defensin-like protein drives cadmium efflux and allocation in rice. Nat Commun, 2018, 9(1): 645. DOI:10.1038/s41467-018-03088-0 |
| [73] | Yan HL, Xu WX, Xie JY, et al. Variation of a major facilitator superfamily gene contributes to differential cadmium accumulation between rice subspecies. Nat Commun, 2019, 10(1): 2562. DOI:10.1038/s41467-019-10544-y |
