

中山大学 生命科学学院 有害生物控制与资源利用国家重点实验室,广东 广州 510006
基金项目:国家转基因生物新品种培育重大专项 (No. 2016ZX08006003-006),广东省自然科学基金 (No. 2016A030313310) 资助
摘要: 为探索哺乳动物非经典分泌信号肽在毕赤酵母表达系统中引导重组蛋白分泌的作用,本研究将一段来源于小鼠同源异型框蛋白 (En2) 的分泌信号序列 (SS) 融合至EGFP蛋白的N端,在毕赤酵母中表达。实验结果显示SS信号肽能通过一种不同于经典的内质网-高尔基体分泌通路的方式将EGFP蛋白分泌至细胞膜表面,与α交配因子前导肽相比,显著降低了细胞的内质网压力。本研究提示哺乳动物非经典分泌信号肽可作为递送重组蛋白至酵母膜表面的一项工具。
关键词: 内质网压力 非经典分泌 毕赤酵母 qPCR
Delivery of recombinant enhanced green fluorescent protein to Pichia pastoris cell wall directed by a mammalian nonclassical secretion signal peptide
Qin Yufeng, Chen Yaosheng, Liu Zhiguo, Zhang Ying, Liu Hailong, He Zuyong


State Key Laboratory of Biocontrol, School of Life Sciences, Sun Yat-Sen University, Guangzhou 510006, Guangdong, China
Received: January 6, 2016; Accepted: March 9, 2016
Supported by: National Transgenic Major Program (No. 2016ZX08006003-006), Natural Science Foundation of Guangdong Province (No. 2016A030313310)
Corresponding authors:Zuyong He. Tel/Fax: +86-20-39332940; E-mail: zuyonghe@foxmail.com
Abstract: A mammalian nonclassical secretion sequence derived from mouse Engrailed2 homeoprotein (En2) was used to direct the secretion of the enhanced green fluorescent protein from Pichia pastoris. This signal peptide conferred the transport of enhanced green fluorescent protein into periplasm through an endoplasmic reticulum-golgi independent pathway, without inducing severe unfolded protein response as compared with Saccharomyces cerevisae α-factor preprosequence. This study implies that this mammalian nonclassical signal peptide could be developed as a useful tool for delivering cargoes to the cell surface of yeast.
Key words: ER stress nonclassical secretion Pichia pastoris qPCR
嗜甲醇毕赤酵母表达系统作为一种广泛应用的高效蛋白表达系统,已被证明适用于多种外源重组蛋白的表达[1-3]。毕赤酵母能直接将外源重组蛋白分泌至培养基中,而且只分泌少量的内源性蛋白,非常有利于后续的外源重组蛋白的纯化。此外,一些胞内过表达的特殊外源蛋白的分泌能降低其对宿主细胞的毒害作用[4-5]。目标蛋白的分泌依赖于分泌信号肽,在毕赤酵母系统中,酿酒酵母交配因子α前导肽是被使用最为广泛的一种分泌信号肽[6]。该信号肽由19个氨基酸的前端信号序列连接后面包含3个潜在的N端糖基化位点和1个二元的Kex2内肽酶切位点在内的66个氨基酸序列而组成的[2, 7]。越来越多的研究表明[8],α前导肽引导的过表达外源重组蛋白的分泌会引起细胞内质网压力,尤其是在表达多拷贝外源基因的时候,这种现象更为明显。Zhu等[9]报道在表达猪胰岛素前体时,当整合到酵母基因组的表达载体拷贝数大于12时,蛋白表达量明显降低,这种现象被认为是由于内质网压力引起的未折叠蛋白应答效应增强[10]。
大多数的真核细胞蛋白通过经典的内质网-高尔基体分泌途径进行分泌,但是也有一些胞质和核蛋白因缺少内质网定位信号而通过非经典的分泌途径分泌到细胞表面[11-12]。Engrailed 同源异型框蛋白就是其中一种核蛋白[13],该蛋白上一段短肽 (AQELSLNESQ) 已被证明具有介导该蛋白通过非经典途径进行分泌的功能 (以下称SS信号肽)[14-15]。在我们前期的研究中,与经典分泌信号肽牛β酪蛋白信号肽相比较,SS信号肽能显著提高重组蛋白在CHO细胞中的分泌表达水平[16]。本研究通过构建SS信号肽融合EGFP蛋白酵母表达载体,以α前导肽作为对照,研究SS信号肽在毕赤酵母中引导外源重组蛋白分泌的效率和对内质网压力的影响。
1 材料与方法1.1 材料1.1.1 菌株与质粒大肠杆菌 (DH5α)、毕赤酵母表达菌株X33均为本实验室保存。pEGFP-N1及酵母表达载体pPICZA和pPICZαA均为本实验室保存。T-A克隆所用的载体为TaKaRa公司的pMD18-T Simple Vector。
1.1.2 试剂高保真LA酶、定量PCR试剂SYBR Premix Ex Taq qPCR均购自TaKaRa公司。核酸检测用SYBR Green I、核酸电泳上样缓冲液购自广州东盛生物公司。质粒小提中量试剂盒和凝胶回收试剂盒购自天根生化科技公司。T4 DNA连接酶,Xba Ⅰ、EcoR Ⅰ、Kpn Ⅰ、Sac Ⅰ等限制性内切酶购自NEB公司。Yeast DNA Kit和Yeast RNA Kit均购自OMEGA公司。酵母提取物 (Yeast extract)、胰蛋白胨 (Trypton) 购自OXOID公司。YNB购自广州翔博生物科技有限公司。蛋白胨 (Peptone) 购自Sigma公司。蛋白预染Marker购自Fermentas公司。PVDF膜购自Bio-Rad公司。抗6×His标签的鼠多克隆抗体购自美国Abcam公司。HRP标记的羊抗鼠IgG二抗购自广州优宁维公司。含有HRP底物ECL发光检测试剂盒购自Thermo公司。
1.1.3 仪器垂直电泳仪和电泳槽、转膜仪、电转化仪均购自Bio-Rad公司。多功能酶标仪为美国Bio-Tek公司。流式细胞分析仪为美国BD公司。激光共聚焦显微镜购自德国Leica。
1.2 方法1.2.1 EGFP基因的克隆设计带有EcoRⅠ、Xba Ⅰ两个酶切位点的引物,将EGFP序列从pEGFP-N1质粒上扩增。源于家鼠Engrailed2蛋白的SS信号肽序列从NCBI序列文库中下载,带有SS信号肽的EGFP基因序列通过设计的SS-EGFP引物经PCR扩增获得,相关引物序列见表 1。PCR扩增反应条件为:94 ℃ 5 min,94 ℃ 30 s,58 ℃ 40 s,72 ℃ 2 min,38个循环;最后72 ℃ 延伸10 min。反应产物连接T载体,并转化DH5α感受态细胞,挑取阳性克隆并提出质粒,获得α-EGFP-T和SS-EGFP-T质粒。
表 1 EGFP序列扩增的引物序列Table 1 Primers used for EGFP amplification
| Primer name | Primer sequence (5′-3′) |
| α-EGFP forward | GAATTC GTGAGCAAGGGCGAGGA |
| α-EGFP reverse | TCTAGA GCCTTGTACAGCTCGTCCA |
| SS-EGFP forward | GAATTCATGGCACAGGAGCTCAGCCTGAACGAGTCTCAGGTGAGCAAGGGCGAGGA |
| SS-EGFP reverse | GGTACCCTTGTACAGCTCGTCCATGC |
| The underlined sequences correspond to the EcoR Ⅰrestriction site in α-EGFP forward,the Xba Ⅰ site in α-EGFP reverse,and SS sequences in SS-EGFP forward,the Kpn Ⅰsite in SS-EGFP reverse. | |
表选项
1.2.2 酵母表达载体的构建和转化通过对重组α-EGFP-T质粒和pPICZαA质粒进行EcoR Ⅰ和Xba Ⅰ的双酶切反应,胶回收α-EGFP片段和相同酶切的pPICZαA质粒,按照一定比例连接,转化感受态细胞,筛选阳性克隆,最终质粒提取获得pPICZαA-EGFP表达载体。同理,通过EcoR Ⅰ和Kpn Ⅰ的双酶切反应,获得SS-EGFP片段和相同酶切的pPICZA质粒,经过连接转化反应以及质粒提取获得PICZA-SS-EGFP表达载体。载体构建图谱见 图 1,通过测序确定构建载体的准确性。
 |
| 图 1 pPICZA-SS-EGFP酵母表达质粒 (A) 和 pPICZαA-EGFP (B) 酵母表达质粒示意图 Figure 1 A schematic diagram of pPICZA-SS-EGFP (A) and pPICZαA-EGFP (B) expression vectors. |
| 图选项 |
用SacⅠ对5?20 μg表达载体进行线性化,之后2 000 V和4.9 ms电转化至毕赤酵母X33感受态细胞,并将200 μL菌体悬液涂布于含有Zeocin抗生素的YPDS平板上,将平板置于30 ℃培养,3?10 d左右,直至单个菌落出现。挑取阳性克隆于液体YPD中扩增,分别用Yeast DNA Kit试剂盒提取酵母基因组,用表 1中引物进行阳性克隆PCR鉴定。用Yeast RNA Kit提取阳性克隆酵母菌RNA,置于-80 ℃冰箱中保存。
1.2.3 阳性克隆酵母的诱导表达挑取SS-EGFP与α-EGFP阳性转化菌株各3个,分别置于装有25 mL BMGY培养基的 100 mL摇瓶中,于28-30 ℃、275 r/min培养至OD600=2?6。室温下2 000×g离心5 min,收集菌体,用BMMY重悬菌体至OD600=1.0左右,并置于1 L的摇瓶中,用四层纱布封口,放置于28-30 ℃、275 r/min的摇床上继续生长。每24 h向培养基中添加过滤过的100%甲醇至终浓度为1%。每隔24 h取一次菌液样品,取样量为 1 mL,置于1.5 mL EP管中,并置于-80 ℃保存。取样时间点为:24、48、72、96和120 h,每次取样取3批,以用于后期的流式分析、Western blotting等检测。
1.2.4 蛋白提取将收集的不同时间点的菌液1 500×g离心 5 min,分别收集上清并保存作为胞外蛋白样品。酵母菌则用PBS漂洗3次,1 500×g离心5 min,弃上清,用含有0.1 mol/L K3PO4 和1 mol/L山梨醇的酵母等渗缓冲液悬浮细胞,加入 2.5 mg/mL 的破壁酶溶液至终浓度1 mg/mL,37 ℃孵育1 h裂解细胞壁,700×g离心1 min,分别收集不同时间点的上清和球形原生质体,收集到的上清将用于细胞壁蛋白的检测。收集到的球形原生质体,用酵母蛋白提取试剂盒提取获得细胞内蛋白。
1.2.5 蛋白检测通过SDS-PAGE蛋白电泳及考马斯亮蓝染液检测不同时间点上清重组EGFP蛋白分泌情况。将收集的不同时间点的上清、细胞壁和细胞内蛋白SDS-PAGE蛋白电泳凝胶在蛋白电转移缓冲液中浸泡5 min,15 V恒压电转移50 min至PDVF膜,用3% BSA封闭过夜,稀释比为 1∶1 000的6×His一抗孵育2 h,TBST漂洗 3次,稀释比为1∶3 000的HRP二抗孵育1 h,TBST漂洗3次后ECL显色和拍照。
另外,收集到的5个时间点的培养基蛋白各吸取100 μL样品加入96孔色酶标板中,用多功能酶标仪 (Bio-Tek公司) 在485 nm/528 nm (激发光/发射光) 处检测。收集到的酵母细胞则用流式分析仪进行分析,荧光显微镜和激光共聚焦显微镜等观察。
1.2.6 内质网压力相关因子表达量的定量分析将前面提取的酵母RNA通过反转录试剂盒反转录获得cDNA,以MET2基因为内参基因对内质网压力Marker基因KAR2和PDI基因进行qPCR检测。用罗氏LightCycler 480 qPCR仪上进行实时定量信号检测,用Roche LightCycler 480分析软件分析SS-EGFP和α-EGFP酵母转化子的内质网功能相关因子的表达差异。相关引物序列见表 2。
表 2 定量PCR引物序列Table 2 Primers used for qPCR detection
| Primer name | Primer sequence (5′-3′) |
| MET2 forward | CGTTCTCGCAACTCTTTCGAA |
| MET2 reverse | CAATGGCATCAGTTATGACGGAAG |
| KAR2 forward | CACTTGGGTGGTGAGGACTT |
| KAR2 reverse | GGCCTTTTCGACCTCTCTCT |
| PDI forward | GCCGTTAAATTCGGTAAGCA |
| PDI reverse | TCAGCTCGGTCACATCTTTG |
表选项
2 结果与分析2.1 载体表达构建PCR反应从pEGFP-N1载体上扩增出EcoRⅠ- SS-EGFP-KpnⅠ片段和EcoRⅠ-EGFP-XbaⅠ片段,并与T载体连接。通过双酶切反应回收的SS-EGFP片段并直接连接到pPICZA载体上的AOX Ⅰ启动子后面,构成毕赤酵母X33的载体pPICZA-SS-EGFP,图 1A。而T载体上的EcoRⅠ- EGFP-XbaⅠ片段则连接到pPICZαA载体的α信号肽后面,构成pPICZαA-EGFP载体 (图 1B)。测序结果表示,所构建的这两个载体序列正确无误。
2.2 阳性转化子鉴定将pPICZαA-EGFP和pPICZA-SS-EGFP表达质粒分别电转化毕赤酵母X33菌株,待单克隆转化子长起来后,分别挑取SS-EGFP和α-EGFP单克隆菌落,提取基因组。通过对基因组AOXⅠ基因的PCR来鉴定阳性转化子 (图 2)。
 |
| 图 2 酵母阳性转化子基因组PCR鉴定 Figure 2 The phenotype identification of transformants using PCR. 1-2: wild yeast control; 3: transform pPICZαA; 4: transform pPICZA; M: DNA marker; 5-11: transform pPICZA-SS-EGFP expression vector; 12-17: transform pPICZαA-EGFP expression vector. |
| 图选项 |
2.3 胞外蛋白检测通过SDS-PAGE (图 3A)、Western blotting (图 3B) 和荧光值检测 (图 3C) 等方法分别对3个α-EGFP转化子和3个SS-EGFP转化子诱导表达的培养基分泌蛋白进行检测。结果显示,α-EGFP转化子培养基中含有大量重组EGFP蛋白,且重组EGFP蛋白分泌量随诱导表达时间增长而不断累积。而SS-EGFP转化子培养基中检测不到重组EGFP蛋白 (图 3)。说明α信号肽引导重组外源蛋白大量分泌至胞外,而SS信号肽则不能引导外源蛋白分泌至胞外。
 |
| 图 3 通过SDS-PAGE (A)、Western blotting (B) 和荧光值 (C) 等方法对分泌至胞外的EGFP蛋白进行分析 Figure 3 Detection of the recombinant EGFP in culture medium. SDS-PAGE (A) and Western blotting (B) analysis of the secretion of recombinant EGFP into the culture medium on the third day after methanol induction,under the direction of the α-factor preprosequence (α-EGFP transformants) or the secretion sequence of mouse Engrailed2 homeoprotein (SS-EGFP transformants). A time course measuring of EGFP fluorescence intensity (C) in supernatant ether from α-EGFP transformants or SS-EGFP transformants. Tansformants with empty vectors pPICZA and pPICZαA were expressed as negative controls. The value is presented as x±s (n=3). |
| 图选项 |
2.4 细胞壁蛋白检测通过破壁酶对酵母细胞壁进行酶解获得细胞壁蛋白。分别对两种转化子各3个阳性单克隆诱导表达96 h和120 h的酵母细胞壁酶解产物进行Western blotting检测,结果发现SS-EGFP转化子的细胞壁上都检测到重组EGFP蛋白的存在,而α-EGFP转化子细胞壁上没有检测到重组蛋白 (图 4)。说明SS信号肽能引导重组EGFP蛋白穿过酵母细胞膜到达细胞壁上,但未穿过细胞壁。
 |
| 图 4 Western blotting检测96 h (A) 和120 h (B) 细胞壁上重组EGFP蛋白含量 Figure 4 Western blotting analysis of the EGFP from yeast cell wall extraction 96 h (A) or 120 h (B) after methanol induction. α-EGFP and SS-EGFP stand for transformants with the α-factor preprosequence and the secretion sequence of mouse Engrailed2 homeoprotein directed EGFP respectively. For each type of transformants,three strains were randomly selected for analysis. Transformants with empty vector pPICZA was expressed as negative control,and a commercial recombinant GFP was loaded as positive control. |
| 图选项 |
2.5 细胞内蛋白检测对去掉细胞壁的酵母细胞中提取的细胞内蛋白进行Western blotting 检测表明,α-EGFP转化株的细胞内外源蛋白含量很少,而SS-EGFP转化株酵母细胞中,由于重组EGFP蛋白不能分泌到细胞外而大量累积在细胞内 (图 5A)。对5个时间点酵母细胞流式分析的结果与Western blot结果一致 (图 5B、5C)。
2.6 显微观察图 6A和6B显示了在荧光显微镜下直接观察两种转化株菌液的结果,进一步证明了α-EGFP转化株重组EGFP被大量分泌到培养基中,导致其培养基荧光高于SS-EGFP转化株,但是酵母细胞个体荧光亮度低于SS-EGFP转化株细胞。
 |
| 图 5 Western blotting (A) 检测和流式分析 (B、C) 细胞内重组EGFP蛋白含量 Figure 5 Western blotting (A) analysis and flow cytometry (B,C) analysis of the intracellular EGFP expression level of α-EGFP and SS-EGFP transformants. Culture medium of α-EGFP transformants was used as positive control in the western blotting analysis. The value in flow cytometry analysis is presented as x±s (n=3). |
| 图选项 |
激光共聚焦显微镜为能清晰观察两种转化子酵母细胞内的荧光分布,对两种转化子细胞采用不同的电压强度进行观察。发现在α-EGFP转化子细胞中的荧光集中分布在大的荧光斑点中(图 6C),这种现象与裂殖酵母中观察到的现象一致[17]。但是SS-EGFP转化株细胞中(图 6D),荧光均匀分布在细胞质和细胞膜周边,而非集中在细胞核周边,说明SS信号肽能在酵母细胞中通过非高尔基体-内质网依赖的蛋白分泌途径引导外源蛋白分泌。
 |
| 图 6 荧光显微镜 (A、B) 和激光共聚焦显微镜 (C、D) 观察 Figure 6 Fluorescence microscope observation of the culture of α-EGFP transformants (A) and SS-EGFP transformants (B),and subcellular localization of EGFP in α-EGFP transformants (C) and SS-EGFP transformants (D) using confocal laser scanning microscopy. Scale bar=100 μm in (A) and (B) and Scale bar=5 μm in (C) and (D). |
| 图选项 |
2.7 内质网压力相关基因表达检测未折叠蛋白应答是由于外源蛋白表达过多而大量累积在内质网上,产生内质网压力而引起的蛋白错误折叠,最终降低蛋白表达的现 象[8-9]。KAR2基因编码蛋白折叠相关的重要分子伴侣,PDI基因编码二硫化物异构酶,二者被认为是内质网压力Maker基因。我们前期的实验表明在酵母基因组中整合一至多个α-EGFP表达质粒,都可以使内质网压力显著提高[18]。图 7比较了在酵母基因组整合α-EGFP表达载体和SS-EGFP表达载体后引起的内质网压力Marker基因表达变化。结果表明整合SS-EGFP转化子引起的内质网压力显著低于α-EGFP转化子。同时进一步说明SS信号肽介导外源蛋白通过非高尔基体-内质网途径进行分泌,因而产生较低的内质网压力。
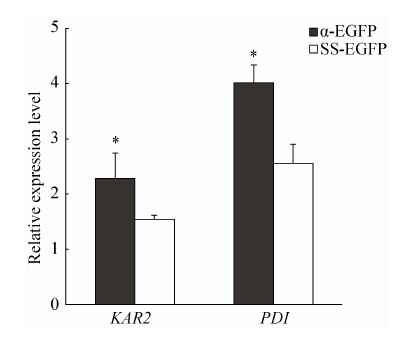 |
| 图 7 定量PCR分析内质网压力相关基因表达 Figure 7 Quantification of the expression levels of UPR-related gene Pdi and Kar2 in α-EGFP transformants and SS-EGFP transformants. The expression levels of tested genes were normalized relative to the internal reference gene MET2. Each qPCR analysis was repeated in triplicate. The value is presented as the x±s (n=3). P<0.05 was used as the level of significance. |
| 图选项 |
3 讨论在之前的研究中,SS信号肽通过非高尔基体-内质网分泌途径介导外源蛋白分泌至哺乳动物细胞表面,与经典的N端分泌信号肽不同,SS信号肽不会被内质网上的蛋白酶所切割[16]。本研究中,SS信号肽介导分泌的细胞内重组EGFP蛋白稍微大于商品化的EGFP蛋白 (图 4和图 5),可能是由于SS信号肽融合在重组蛋白N端导致的。SS信号肽能在酵母细胞过表达外源蛋白时产生较少的内质网压力 (图 7),但是不能引导外源蛋白穿过酵母细胞壁到达培养基中 (图 3)。
据报道SS信号肽能通过胞外体来源的运输小泡将外源蛋白转运至哺乳动物细胞外[13, 19]。这种现象与在网柄菌属酵母中非经典分泌的Acb1蛋白相似,Acb1先与自噬体相作用,再融合不断循环再生的胞内体,最后与细胞膜融合并释放到细胞外[19]。与哺乳动物细胞不同,在酵母细胞中,外源蛋白的分泌不仅需要穿过细胞膜还要穿过细胞壁[20-21]。研究认为,外源蛋白通过经典或非经典分泌途径运输到细胞膜上后,细胞膜通过出芽形成运输小泡,这些小泡具有水解细胞壁的酶组分以便形成通道穿过细胞壁[22-24]。在α-EGFP转化子中EGFP蛋白大量地分泌到了细胞外 (图 3)。但是在α-EGFP转化子酵母细胞壁酶解产物中并未检测到重组EGFP蛋白 (图 4),而SS-EGFP转化子细胞壁中不仅能检测到重组EGFP蛋白,且重组EGFP蛋白会随着诱导表达时间增加而得到累积 (图 6)。表明α-EGFP转化子酵母细胞中重组EGFP的运输小泡能十分高效地将EGFP蛋白转运至胞外,不会明显地在细胞周质外残留,相反SS-EGFP转化子细胞中的运输小泡被细胞壁阻挡而不能释放到细胞外 (图 3和图 4)。可能的机制是SS-EGFP转化子细胞形成的运输小泡缺失水解酵母细胞壁的酶的组分,也可能是与酵母细胞外表面的某些膜蛋白相似,因缺失经典分泌信号肽,SS-EGFP融合蛋白运输到细胞质外周后仍然松散地结合在细胞壁上[25]。详细的机制尚未明确。
总结全文,哺乳动物非经典分泌信号肽可介导外源蛋白分泌到毕赤酵母细胞外周隙中,但不能分泌到培养基中,同时产生较低的内质网压力。暗示了此信号肽可作为一项用于研究穿过酵母细胞壁必需组分的工具,且可作为递送重组蛋白至酵母外源蛋白分泌机制膜表面的一种工具。
参考文献
| [1] | Daly R, Hearn MTW. Expression of heterologous proteins in Pichia pastoris: a useful experimental tool in protein engineering and production.J Mol Recognit,2005, 18(2): 119–138.DOI: 10.1002/(ISSN)1099-1352 |
| [2] | Damasceno LM, Huang CJ, Batt CA. Protein secretion in Pichia pastoris and advances in protein production.Appl Microbiol Biotechnol,2012, 93(1): 31–39.DOI: 10.1007/s00253-011-3654-z |
| [3] | Macauley-Patrick S, Fazenda ML, McNeil B, et al. Heterologous protein production using the Pichia pastoris expression system.Yeast,2005, 22(4): 249–270.DOI: 10.1002/(ISSN)1097-0061 |
| [4] | Cereghino JL, Cregg JM. Heterologous protein expression in the methylotrophic yeast Pichia pastoris.FEMS Microbiol Rev,2000, 24(1): 45–66.DOI: 10.1111/j.1574-6976.2000.tb00532.x |
| [5] | Gasser B, Prielhofer R, Marx H, et al. Pichia pastoris: protein production host and model organism for biomedical research.Future Microbiol,2013, 8(2): 191–208.DOI: 10.2217/fmb.12.133 |
| [6] | Lin-Cereghino GP, Stark CM, Kim D, et al. The effect of α-mating factor secretion signal mutations on recombinant protein expression in Pichia pastoris.Gene,2013, 519(2): 311–317.DOI: 10.1016/j.gene.2013.01.062 |
| [7] | Mori A, Hara S, Sugahara T, et al. Signal peptide optimization tool for the secretion of recombinant protein from Saccharomyces cerevisiae.J Biosci Bio,2015, 120(5): 518–525.DOI: 10.1016/j.jbiosc.2015.03.003 |
| [8] | Puxbaum V, Mattanovich D, Gasser B. Quo vadis? The challenges of recombinant protein folding and secretion in Pichia pastoris.Appl Microbiol Biotechnol,2015, 99(7): 2925–2938.DOI: 10.1007/s00253-015-6470-z |
| [9] | Zhu T, Guo M, Tang Z, et al. Efficient generation of multi-copy strains for optimizing secretory expression of porcine insulin precursor in yeast Pichia pastoris.J Appl Microbiol,2009, 107(3): 954–963.DOI: 10.1111/jam.2009.107.issue-3 |
| [10] | Zhu TC, Guo MJ, Zhuang YP, et al. Understanding the effect of foreign gene dosage on the physiology of Pichia pastoris by transcriptional analysis of key genes.Appl Microbiol Biotechnol,2011, 89(4): 1127–1135.DOI: 10.1007/s00253-010-2944-1 |
| [11] | Nickel W, Rabouille C. Mechanisms of regulated unconventional protein secretion.Nat Rev Mol Cell Biol,2009, 10(2): 148–155.DOI: 10.1038/nrm2617 |
| [12] | Ding Y, Wang J, Wang JQ, et al. Unconventional protein secretion.Trends Plant Sci,, 17(10): 606–615.DOI: 10.1016/j.tplants.2012.06.004 |
| [13] | Prochiantz A, Joliot A. Can transcription factors function as cell-cell signalling molecules?.Nat Rev Mol Cell Biol,2003, 4(10): 814–819.DOI: 10.1038/nrm1227 |
| [14] | Maizel A, Bensaude O, Prochiantz A, et al. A short region of its homeodomain is necessary for engrailed nuclear export and secretion.Development,1999, 126(14): 3183–3190. |
| [15] | Joliot A, Trembleau A, Raposo G, et al. Association of Engrailed homeoproteins with vesicles presenting caveolae-like properties.Development,1997, 124(10): 1865–1875. |
| [16] | He ZY, Sun XZ, Mei G, et al. Nonclassical secretion of human catalase on the surface of CHO cells is more efficient than classical secretion.Cell Biol Int,2008, 32(4): 367–373.DOI: 10.1016/j.cellbi.2007.12.003 |
| [17] | Kjrulff S, Jensen MR. Comparison of different signal peptides for secretion of heterologous proteins in fission yeast.Biochem Biophys Res Commun,2005, 336(3): 974–982.DOI: 10.1016/j.bbrc.2005.08.195 |
| [18] | Liu HL, Qin YF, Huang YK, et al. Direct evaluation of the effect of gene dosage on secretion of protein from yeast pichia pastoris by expressing EGFP.J Microbiol Biotechnol,2014, 24(2): 144–151.DOI: 10.4014/jmb.1308.08010 |
| [19] | Duran JM, Anjard C, Stefan C, et al. Unconventional secretion of Acb1 is mediated by autophagosomes.J Cell Biol,2010, 188(4): 527–536.DOI: 10.1083/jcb.200911154 |
| [20] | Ahmad M, Hirz M, Pichler H, et al. Protein expression in Pichia pastoris: recent achievements and perspectives for heterologous protein production.Appl Microbiol Biotechnol,2014, 98(12): 5301–5317.DOI: 10.1007/s00253-014-5732-5 |
| [21] | Landes N, Maccani A, Leitner C, et al. Cross-species comparison of recombinant protein secretion in CHO cells and Pichia pastoris.New Biotechnol,2014, 31(S): S4. |
| [22] | Oliveira DL, Nakayasu ES, Joffe LS, et al. Biogenesis of extracellular vesicles in yeast: many questions with few answers.Commun Integr Biol,2010, 3(6): 533–535.DOI: 10.4161/cib.3.6.12756 |
| [23] | Roongsawang N, Puseenam A, Kitikhun S, et al. A novel potential signal peptide sequence and overexpression of ER-resident chaperones enhance heterologous protein secretion in thermotolerant methylotrophic yeast Ogataea thermomethanolica.Appl Biochem Biotechnol,2015: 1–15. |
| [24] | Hapala I, Gria? P, Nosek J, et al. Yeast membranes and cell wall: from basics to applications.Curr Genet,2013, 59(4): 167–169.DOI: 10.1007/s00294-013-0408-8 |
| [25] | Nombela C, Gil C, Chaffin WL. Non-conventional protein secretionin yeast.Trends Microbiol,2006, 14(1): 15–21.DOI: 10.1016/j.tim.2005.11.009 |
