 , 向平
, 向平
 , 姜文超, 张智, 莫静宇
, 姜文超, 张智, 莫静宇重庆大学三峡库区生态环境教育部重点实验室, 重庆 400045
收稿日期: 2020-12-02; 修回日期: 2021-01-16; 录用日期: 2021-01-16
基金项目: 重庆市建设科技项目(城科字2020第5-2)
作者简介: 李梦颖(1995-), 女, E-mail: 695689827@qq.com
通讯作者(责任作者): 向平, E-mail: xiangping74@cqu.edu.cn
摘要:采用水热法和共沉淀法将MnFe2O4负载在水热炭(HTC)表面制备磁性MnFe2O4@HTC复合催化剂.采用SEM、XRD、BET、FTIR、XPS对催化剂进行表征,通过考察MnFe2O4/HTC负载比、过硫酸钠(PS)投加量、初始pH和不同化学体系对除藻效果的影响,探究无供氧条件下MnFe2O4@HTC活化PS体系除藻的效能.基于自由基屏蔽实验和XPS分析对MnFe2O4@HTC活化PS体系反应机制进行研究验证.结果表明,当初始藻浓度为1.4×109个·L-1(OD680=0.14),催化剂投加量为0.2 g·L-1,PS投加量为0.4 g·L-1,pH为6时,降解30 min,该体系除藻率可达到99%.在该体系中,MnFe2O4@HTC材料可将藻细胞吸附在材料表面,通过Mn、Fe的价态循环和HTC的协同效应反应催化PS产生空穴、1O2、·O2-、SO4-·和·OH多种氧化物质,使藻细胞破裂死亡.
关键词:铁酸盐水热炭铜绿微囊藻过硫酸盐
Performance and mechanism of MnFe2O4@HTC activated persulfate system for algae removal
LI Mengying
 , XIANG Ping
, XIANG Ping
 , JIANG Wenchao, ZHANG Zhi, MO Jingyu
, JIANG Wenchao, ZHANG Zhi, MO JingyuKey Laboratory of the Three Gorges Reservoir Region's Eco-Environment, Ministry of Education, Chongqing University, Chongqing 400045
Received 2 December 2020; received in revised from 16 January 2021; accepted 16 January 2021
Abstract: A magnetic MnFe2O4@HTC composite catalyst was prepared by loading MnFe2O4 on the surface of the hydrothermal carbon (HTC) with hydrothermal-coprecipitation method. Through the Characterization by SEM, XRD, BET, FTIR and XPS, the effects of MnFe2O4/HTC load ratio, sodium persulfate (PS) dosage, initial pH and different chemical systems on algae removal performance of the catalyst were investigated, and the effects of MnFe2O4@HTC activated PS system on algae removal without oxygen were investigated. The reaction mechanism of MnFe2O4@HTC activated PS system was verified based on free radical quencing experiments and XPS analysis. The results indicated that when the initial algae concentration was 1.4×109 cell·L-1 (OD680=0.14), the catalyst dosage was 0.2 g·L-1, the PS dosage was 0.4 g·L-1, and the pH was 6, the algae removal rate reached 99% after 30 minutes of reaction. In this system, MnFe2O4@HTC could adsorb algal cells on its surface, catalyze PS to produce holes, 1O2, ·O2-, SO4-· and ·OH by the valence cycle of Mn and Fe as well as the synergistic reaction of HTC, and then made algal cells to burst and die.
Keywords: MnFe2O4hydrothermal carbonmicrocystis aeruginosapersulfate
1 引言(Introduction)水体富营养化导致藻类爆发威胁了水生态环境健康和饮用水安全(程昊等, 2020).传统除藻工艺以物理捕捞法和化学氧化法为主, 存在效果差、成本高、技术复杂等问题.近年来, 活化过硫酸盐(PS)高级氧化技术, 因其氧化还原电位高、pH适用范围广、低能耗、易储存运输等优点受到广泛关注(Matzek et al., 2016).尤其是以尖晶石型铁酸盐作为催化剂, 通过活化PS产生氧化基团, 能够对包括有毒和不可生物降解化合物在内的大部分有机物产生较强的降解能力(荣幸, 2019).其中, 铁酸锰(MnFe2O4)因其稳定的催化性能, 廉价的生产原料和简便的制备方法显现出优异的性能(Galindo et al., 2014).
然而铁酸盐在水体中存在易团聚, 催化效率低等问题.为解决此类问题, 生物质作为一种性质稳定的可再生能源材料是常见的良好载体.水热炭(HTC)是将生物质进行水热炭化处理所得到的一种均质、疏水、能量密集、包含微米或纳米尺寸炭球的多孔结构固体(俞盈等, 2018).不同于传统的高温煅烧热化学处理法, 水热炭化法可在反应温度较低且无需脱水预处理的条件下, 直接处理含水生物质原料, 生成具有更高的热值和能量密度的炭球, 以实现生物质的高效转化和资源利用.
炭质材料不仅作为MnFe2O4的载体能够提升材料的性能, 还能和金属元素实现协同催化.Du等(2020)用炭热改性MnFe2O4材料, 使MnFe2O4对PS的激活显著增强, 反应30 min去除了99.0%的酸性橙7.Li等(2017)将MnFe2O4负载在污泥衍生的活性炭(SAC)上作为更高效的非均相催化剂, 活化PS降解偶氮染料橙G, 在MnFe2O4和SAC的协同作用下30 min得到了95%以上的脱色率.
本文采用水热法和共沉淀法制得复合型MnFe2O4@HTC催化剂, 并用于催化PS处理高浓度含藻水, 通过扫描电镜、BET比表面积测定仪、X射线光电子能谱光谱仪等对MnFe2O4@HTC材料性能进行了研究, 并考察了不同条件下MnFe2O4@HTC活化PS去除水中铜绿微囊藻的效果, 提出了可能的催化反应机理.
2 材料与方法(Materials and methods)2.1 MnFe2O4@HTC复合材料的制备2.1.1 水热炭的制备采用水热法制备HTC(Hu et al., 2017): 称取7.0 g葡萄糖溶于70 mL超纯水中, 置于100 mL聚四氟乙烯高压反应釜中180 ℃加热10 h, 用蒸馏水洗涤数次, 放置于真空干燥箱中60 ℃烘干, 过100目筛备用.
2.1.2 MnFe2O4@HTC复合材料的制备采用共沉淀法制备MnFe2O4@HTC复合材料(黄芳龙, 2019): 称取一定质量的FeCl3·6H2O和MnCl2·4H2O(Fe、Mn的物质的量的比为2∶1)以及一定质量的HTC于40 mL超纯水中, 搅拌30 min.FeCl3·6H2O、MnCl2·4H2O与HTC投加量如表 1所示, 并编号为Mn-Fe1~4@HTC.将混合溶液置于100 mL三颈烧瓶中, 80 ℃水浴加热并机械搅拌均匀后缓慢滴入30 mL 30%氨水, 反应1 h, 过滤.采用水和乙醇对过滤所得固体物质交替清洗3次(水和乙醇各清洗3次), 将反应物放入真空干燥箱内60 ℃, 烘干12 h, 取出研磨, 获得粉末状MnFe2O4@HTC复合材料.
表 1(Table 1)
| 表 1 FeCl3·6H2O、MnCl2·4H2O与HTC投加量 Table 1 Dosages of FeCl3·6H2O, MnCl2·4H2O and HTC | |||||||||||||||||||||||||||
表 1 FeCl3·6H2O、MnCl2·4H2O与HTC投加量 Table 1 Dosages of FeCl3·6H2O, MnCl2·4H2O and HTC
| |||||||||||||||||||||||||||
2.2 MnFe2O4@HTC材料表征MnFe2O4@HTC的形貌通过扫描电镜(SEM, SU8220, 日本日立公司)观察, 在SEM上链接能谱仪(EDS, APOLLO X, 美国EDAX公司)分析其元素构成.元素的相对含量通过ICP-OES(美国瓦里安710-es)测定.材料的比表面积及孔径分析通过比表面积及孔隙度分析仪(BET, ASAP2020, 美国麦克仪器公司)用氮气吸附法测定.采用美国NICOLET 380型红外光谱仪并通过KBr压片法, 在波长4000~400 cm-1范围扫描测定材料的化学键种类(FTIR测定).材料反应前后元素的价态通过X射线光电子能谱(XPS, 美国赛默飞公司)在EscaLab250Xi光谱仪测定.
2.3 藻细胞降解实验实验以铜绿微囊藻(FACHB-315)为研究对象, 购于武汉中科院水生生物所, 实验装置系统由反应器(100 mL烧杯)、机械搅拌器等组成.使用0.1 mol·L-1 HCl和0.1 mol·L-1 NaOH调节初始pH=6, 初始藻细胞密度为1.4×109个·L-1 (OD680=0.14), PS投加量为0.4 g·L-1, 催化剂投加量为0.2 g·L-1, 降解时间为30 min.使用300 r·min-1转速的机械搅拌器对实验藻液进行搅拌, 使藻液和催化剂在降解过程中均匀混合.
2.4 分析及计算方法通过光学显微镜(BA310)采用血球计数法测定藻细胞生物量(钱奎梅等, 2015), 通过紫外分光光度计(photolab? 7600 UV-VIS)采用紫外分光光度法测定光密度(Rajasekhar et al., 2012).藻胆蛋白含量采用分光光度法(OD620)(薛志欣等, 2008)测定.藻液经0.22 μm PES过滤后采用紫外分光光度法(蒋绍阶等, 2002)测定其UV254.藻去除率(Separation Efficiency, SE)按式(1)计算.
 | (1) |
3 结果与讨论(Results and discussion)3.1 MnFe2O4@HTC催化剂的表征采用SEM对HTC单体及复合材料的形貌进行观察.如图 1a~1b所示, HTC单体为表面清晰光滑的不定型聚集球体, 且连通性好.负载MnFe2O4后的形貌结构如图 1c~1d所示, 可以观察到HTC表面粗糙, 有颗粒聚集.制备过程中高强度机械搅拌使MnFe2O4微粒保持了良好的分散性, 并具有一定的机械强度.将能谱仪连接在扫描电镜上分析其化学元素, 结果如图 2a所示, 能谱分析表明该复合材料主要由Mn、Fe、O和C组成, Mn、Fe的原子比大致为2∶1, 表明MnFe2O4单体成功负载在HTC表面.
图 1(Fig. 1)
 |
| 图 1 扫描电镜图 (a.HTC (×40 k), b. HTC (×160 k), c.MnFe2O4@HTC (×80 k), d. MnFe2O4@HTC (×160 k)) Fig. 1SEM images of HTC (×40 k) (a), HTC (×160 k) (b), MnFe2O4@HTC (×80 k) (c) and MnFe2O4@HTC (×160 k) (d) |
图 2(Fig. 2)
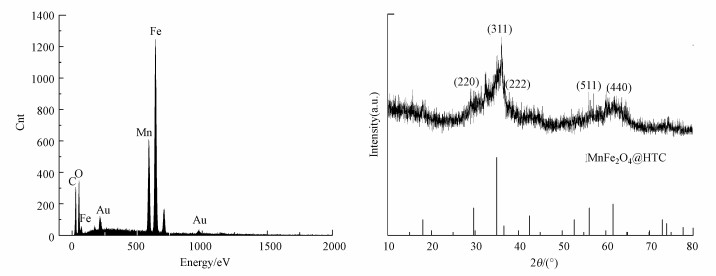 |
| 图 2 MnFe2O4@HTC材料的能谱分析图(a)及XRD谱图(b) Fig. 2Energy dispersive spectrum(a) and XRD pattern(b) of MnFe2O4@HTC material |
XRD图谱如图 2b所示, 样品在2θ为34.98°、56.20°、61.65°处有明显的衍射峰, 特征衍射峰的位置和尖晶石相MnFe2O4的标准图谱(JCPDS No. 10-0319)相一致.复合材料中部分弱峰消失, 可能是因为无定型炭的加入导致了MnFe2O4择优取向, 或是MnFe2O4含量太少无法被检测到.
采用BET对复合材料和HTC单体的比表面积分析见图 3a.根据IUPAC的分类标准, 复合材料的吸脱附等温线为Ⅳ曲线和H3滞后环.此现象说明该复合材料是中孔占主导, 孔隙分布随机, 并且孔隙之间相通;H3滞后环表明材料存在片状粒子堆积而形成的狭缝孔.BET表征结果表明, MnFe2O4@HTC复合材料的比表面积为448 m2·g-1, 平均孔径为7.7 nm;而HTC单体的BET表面积为10.7 m2·g-1, 平均孔径为50.2 nm.复合材料的比表面积由于金属微粒在HTC单体上的聚集而增大, 进而增大了材料与污染物之间的接触面积.
图 3(Fig. 3)
 |
| 图 3 MnFe2O4@HTC材料BET分析图(a)及MnFe2O4@HTC材料和HTC单体的FTIR表征图(b) Fig. 3BET diagram of MnFe2O4@HTC (a) and FTIR diagram of MnFe2O4@HTC and HTC monomer(b) |
复合材料和HTC单体的FTIR图谱结果如图 3b所示, 复合材料的Mn─O和Fe─O键吸收带分别出现在459和580 cm-1附近.这两个峰的出现表明尖晶石结构中处于八面体和四面体位点的金属-氧键的形成, 从而也说明了MnFe2O4纳米颗粒成功地附着在HTC的表面.3400 cm-1附近是O─H伸缩振动, 2930 cm-1附近是甲基C─H伸缩化合物, 2860 cm-1附近是亚甲基C─H伸缩化合物.CC键导致在1640 cm-1附近出现明显的吸收带, 表明HTC中C含量高, 且有一定的芳构化现象.在1450~1400 cm-1附近的其他的峰则是由于CO羰基的拉伸作用导致的, 其主要贡献则可能是HTC表面存在的羧基.1300~1000 cm-1为乙醇、苯酚和羟基中C─O键发生振动峰.水热炭化能够较大程度保留炭材料的原有官能团, 这可能有利于污染物的去除(Spataru et al., 2016).引入Mn、Fe后, C─O拉伸导致在1300~1000 cm-1出现的吸收带的峰出现下降, 这可能是由于复合材料表面形成了金属─O─C键所致(Zubir et al., 2014).复合材料表面多种功能的官能团能够提供大量有效的活性位点, 在多相催化中将发挥重要作用.
3.2 MnFe2O4/HTC负载比对除藻效果的影响MnFe2O4在HTC上的负载量会影响除藻效果.制备材料时HTC和Mn、Fe投加量如表 1所示, Fe、Mn负载量通过ICP测定如表 2所示, 4种催化剂在相同条件下的除藻率如图 4所示.图 4结果表明, 4组催化剂30 min的藻去除效果都在80%以上, HTC在复合材料中占比越高, 复合材料的初始反应速率越快, 这可能是由于反应初期材料的吸附作用.4组催化剂反应对微藻的总去除率随着HTC占比的增加而先增后减, 在Mn-Fe3@HTC时出现峰值.这可能是因为当HTC含量较少时, MnFe2O4颗粒负载的位点数量不足, 完全包覆在HTC表面, 使HTC表面的活性位点无法与PS接触并与MnFe2O4进行协同催化;而HTC含量过高时, MnFe2O4纳米颗粒的质量比重下降, 过低的Mn、Fe降低了PS生成SO4-·和·OH的效率, 因而除藻效率下降, 这与Zhao等(2017)的研究相似.因此Mn-Fe3@HTC材料质量比可以达到最佳藻去除效率, 且保证了材料的磁性, 后续实验均采用Mn-Fe3@HTC复合材料作为催化剂.
表 2(Table 2)
| 表 2 Fe、Mn元素相对负载量 Table 2 Relative loads of Fe and Mn elements | |||||||||||||||||||||||||||||||||||||||||
表 2 Fe、Mn元素相对负载量 Table 2 Relative loads of Fe and Mn elements
| |||||||||||||||||||||||||||||||||||||||||
图 4(Fig. 4)
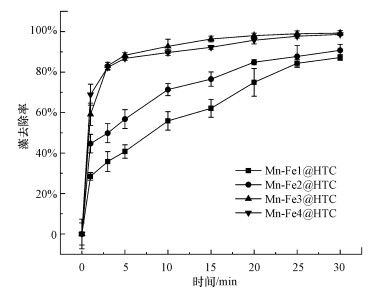 |
| 图 4 MnFe2O4/ HTC负载比对除藻效果的影响 Fig. 4Effects of MnFe2O4/ HTC load ratio on algal removal |
3.3 PS投加量对除藻效果的影响在过硫酸盐氧化的类芬顿体系中, PS用量是一个对污染物去除效率具有影响的重要因素(Ma et al., 2019; 佘月城, 等, 2019).图 5为不同PS投加量下微藻的去除效果.随着PS投加量的增大, 30 min藻去除率呈现先增加后降低的总体趋势, 这与赵莹等(2017)的研究结果相似.当PS用量仅为0.1 g·L-1时, 反应30 min藻去除率仅为71.25%, 这可能是因为藻液中PS浓度较低, 不足以在催化剂的作用下产生足量的有效氧化基团降解目标污染物.随着PS投加量的增加, 藻的去除效果提高, 在PS投加量为0.4 g·L-1 (1.68 mmol·L-1)时降解效果达到最佳, 基本实现完全从溶液中分离.当增加PS用量到0.5 g·L-1时, 藻去除效果略有下降, 说明此时PS处于过量状态, 反应中产生的SO4-·和·OH等自由基被过量的S2O82-竞争消耗, 从而降低了藻的去除率和PS的利用率(式(2)~(3)).
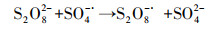 | (2) |
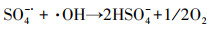 | (3) |
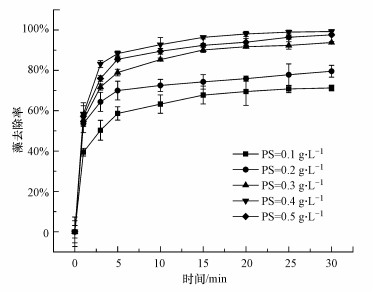 |
| 图 5 PS投加量对MnFe2O4@HTC /PS体系除藻效果的影响 Fig. 5Effects of PS dosage on the algal removal of MnFe2O4@HTC/PS system |
3.4 初始pH对除藻效果的影响为探究初始pH对Mn-Fe3@HTC/PS体系催化效果的影响, 在本实验中, pH值在3~10范围内设置了5组变量, 不同初始pH值对铜绿微囊藻去除效果如图 6所示.由图可知, 5组pH值条件下的藻去除率均高于90%, 且当pH值为3时在最短的时间内获得了更高的去除效率.
图 6(Fig. 6)
 |
| 图 6 初始pH对MnFe2O4@HTC /PS体系除藻效果的影响 Fig. 6Effects of initial pH on the algal removal of MnFe2O4@HTC/PS system |
传统均相类Fenton系统的显著缺点是要求溶液pH值在3左右, 在接近中性的pH值下, 大多数金属氧化物的表面类Fenton体系被钝化使反应效果变差.过低的pH不仅会增加运行成本, 还会造成铁泥的二次污染和催化剂的损失.而在活化PS的类芬顿体系中, pH的适用范围明显增加.由于藻类爆发会消耗水体中的CO2, 而使水体环境pH为6.5~7.5的偏碱性范围, 因此本体系更适用于高藻水原水处理.
3.5 不同体系对除藻效果的影响图 7a为单体和复合材料在无PS条件下对铜绿微囊藻的去除效果比较曲线.单体HTC和MnFe2O4对微藻的去除效果较差, 30 min吸附平衡时的藻吸附率分别为13.79%和14.57%.而Mn-Fe3@HTC微藻的吸附效果明显增加, 5 min左右达到吸附平衡, 30 min吸附率约为58%.一方面是因为藻细胞内容物,如蛋白质、氨基糖和其他有机酸等溶出粘附在完整细胞和破裂细胞表面(Huang et al., 2009);而复合材料官能团含量丰富且比表面积大,藻细胞及其表面的细胞内容物在与复合材料表面产生的静电作用、范德华力、氢键等作用下吸附在材料表面(向平等, 2020),当细胞表面物质被氧化后,引发藻细胞的脱落或死亡.另一方面铁锰元素负载在HTC材料表面, 使其与溶液的接触面积增加, 强化了微量铁锰在溶液中溶解而产生的絮凝效果(Zhou et al., 2020).
图 7(Fig. 7)
 |
| 图 7 不同催化剂对藻的吸附效果(a)及不同体系除藻效果(b) Fig. 7Adsorption performance of different catalysts on algae(a) and the algal removal efficiencies under different systems(b) |
图 7b为不同体系下催化剂活化PS降解铜绿微囊藻效果曲线.在初始藻浓度1.4×109个·L-1 (OD680=0.14), PS投加量为0.4 g·L-1, 催化剂投加量为0.2 g·L-1, 初始pH=6的条件下, 反应前5 min内催化剂催化PS的除藻速率非常快, 随着反应的进行降解曲线逐渐趋于平稳, 直至30 min时, 降解反应基本完成.含藻水中只加入PS时, 降解30 min后藻去除率为13.49%;同时投加PS和HTC后的藻去除率为17.16%, 说明HTC并不能催化PS产生氧化性自由基, 降解微藻.MnFe2O4催化PS体系30 min除藻率为50.62%, 且藻浓度在反应过程中呈持续降低趋势, 说明MnFe2O4单体可能会活化PS持续产生自由基, 但由于MnFe2O4存在团聚效应而导致藻去除率低.在Mn-Fe3@HTC/PS体系内, 短时间的藻浓度大幅降低, 其去除率相比MnFe2O4/PS体系提高了48.5%, 这可能是因为负载MnFe2O4后改变了HTC原有的表面结构, 使其表面活性位点增多, 与PS接触几率增加, 从而提高了藻去除效果.
3.6 UV254和OD620变化UV254能间接反映溶液中有机物含量, 因此该值的变化能够反映溶液中胞外有机物的变化, 判断该体系对于胞外有机物的去除效果.根据图 8a可知, 随着反应时间的延长, UV254呈现先增加后稳定的状态, 且整体吸光度都较小.鉴于藻液由超纯水配置, 溶液中无有机物添加, 因此有机物应来自于藻细胞内容物, 这说明藻细胞受到氧化而破损, 造成胞内有机物流出.可以看出反应初始时藻细胞迅速被大量破坏释放胞内有机物, 体系处理有机物的速率低于破坏藻细胞的速度, UV254突增.随着藻细胞的减少, 有机物释放速度变缓, 溶液中有机物持续被材料吸附和氧化, UV254增长速率变缓, 直至趋于稳定.由此可以看出该体系具有处理有机物的能力.
图 8(Fig. 8)
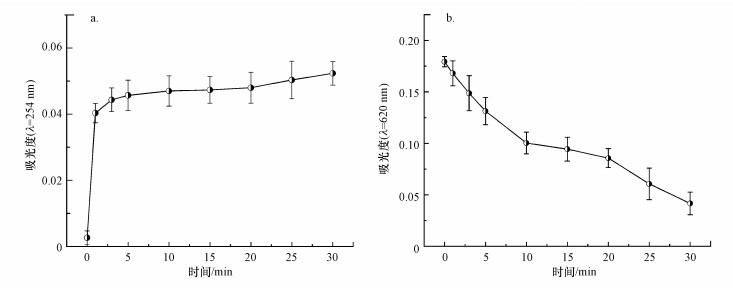 |
| 图 8 反应过程中UV254的变化(a)及OD620的变化(b) Fig. 8Changes of UV254(a) and OD620 (b)in the reaction |
藻胆蛋白是藻胆体中的捕光色素蛋白, 能有效促进光合作用, 在波长620 nm处有特征吸收峰, 因此通过研究溶液中OD620的变化可间接判断体系对藻细胞光合作用系统的影响.通过图 8b可知, 随着反应时间的增加, OD620的值不断减小, 藻胆蛋白含量不断减小, 说明该体系能有效破坏藻细胞光合作用系统.
3.7 MnFe2O4@HTC催化PS反应机理对于活化过硫酸盐的高级氧化除藻机理, 主要分为以SO4-·和·OH为主要作用的自由基氧化机理, 和以单线态氧(1O2)和氧化空穴为主要作用基团的非自由基理论.为验证MnFe2O4@HTC/ PS除藻体系的反应机理, 基于两种原理进行氧化基团淬灭实验.
图 9为最优工况下MnFe2O4@HTC催化PS降解铜绿微囊藻体系中可能的自由基团淬灭实验曲线.单线态氧(1O2)是一种活化PS产生的非自由基反应性物质.Cheng等(2017)研究发现1O2在PS活化中起关键作用, 因此选择糠醇(FFA)淬灭1O2, 以判断系统中是否有1O2的生成(k (1O2)=1.2×108 L·mol-1·s-1).由图 7可知, 投加FFA后的藻去除率为69.23%, 与对照和添加TBA的系统相比, 藻去除率下降了10.91%.结果表明了1O2在PS中的出现.另外, 通过添加乙二胺四乙酸二钠(EDTA-2Na)可以反映是否存在空穴氧化(Velo-Gala et al., 2017; Wu et al., 2018), 因此, 将用于捕获空穴以抑制氧化的EDTA-2Na引入MnFe2O4@HTC/ PS系统.EDTA-2Na的添加显著抑制了铜绿微囊藻的降解, 当EDTA-2Na的浓度增加到2 mmol·L-1时, 在30 min铜绿微囊藻的去除率仅为44.0%, 降低幅度大于其他氧化基团, 说明空穴氧化在整个氧化体系中占比最大, 主导了微藻的降解.这可能是由于金属离子的价态循环促进了HTC活性位点的电子跃迁, 在存在污染物的情况下, 界面电子转移反应激活:Fe(Ⅲ)和Mn(Ⅲ)在HTC的富电子位点上俘获电子, 从而抑制电子和空穴的重组, 微藻在相应的电子缺陷位点附近被氧化(Heidarpour et al., 2020; Wang et al., 2020).然而仍需要进一步对MnFe2O4@HTC/ PS体系的研究来确定空穴的产生原因.
图 9(Fig. 9)
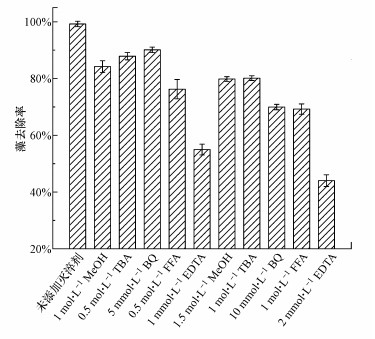 |
| 图 9 自由基抑制实验 Fig. 9Free radical inhibition experiments |
采用甲醇(MeOH)和叔丁醇(TBA)进行自由基屏蔽实验.MeOH是有效的SO4-·和·OH灭淬剂, 其反应速率常数分别为kSO4-·=2.5×107 L·mol-1·s-1和k·OH=9.7×108 L·mol-1·s-1;TBA与SO4-·和·OH的反应速率常数分别为kSO4-· =8.0×105 L·mol-1·s-1和k·OH =6.0×108 L·mol-1·s-1, 当反应液中同时含有两者自由基时, TBA会优先淬灭·OH, 保留SO4-·(Buxton et al., 1988).当体系中加入1 mol·L-1 TBA时, 30 min时的藻去除率从99.09%降到80.15%, 说明在体系中存在·OH被TBA捕获, 从而影响降解效果;当体系中加入1.5 mol·L-1 MeOH时, 约有79.83%的铜绿微囊藻被降解, 对比加入TBA的体系中藻去除率, 可说明体系中SO4-·含量少于·OH, 这可能是因为在pH=6条件下, 溶液中SO4-·被氢氧根离子清除并生成·OH(Ben Hammouda et al., 2017)(式(4)).采用对苯醌(BQ)屏蔽超氧自由基(·O2-),其30 min除藻率也出现了明显的降低,说明体系中产生了·O2-,且·O2-在除藻过程中的贡献率大于·OH和SO-· 4.·O2-可能来源于PS在生成·OH时和高价态金属的相互作用。另外,·O2-的出现,可能是导致1O2在该体系中大量生成的原因,有研究表明·O2-是1O2的前驱体,由·O2-的直接氧化或两个超氧阴离子自由基的重组产生(Zhou et al., 2021) (式5).
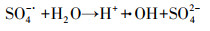 | (4) |
 | (5) |
图 10(Fig. 10)
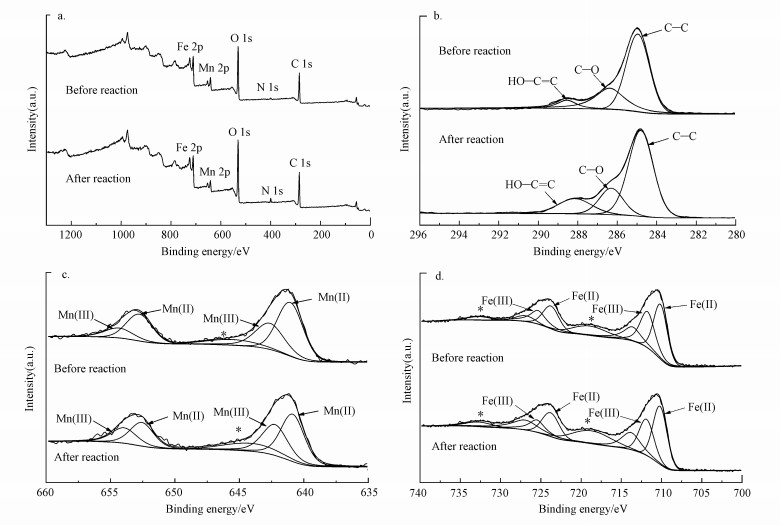 |
| 图 10 Mn-Fe3@HTC反应前后的全谱XPS图谱(a)、C 1s (b)、Fe 2p (c)和Mn 2p (d)高分辨XPS图谱 Fig. 10Full spectrum XPS spectra (a), C 1s (b), Fe 2p (C) and Mn 2p (d) before and after the reaction of Mn-Fe3@HTC |
根据XPS分析推测MnFe2O4@HTC活化PS的氧化反应.如图 10c所示, 641.04 eV和652.79 eV两个主峰分别对应于Mn 2p3/2和Mn 2p1/2, 卫星峰值646.03 eV对应了Mn(Ⅱ)信号.与PS反应后, 646.03 eV附近的卫星峰减弱, 表明催化剂表面的Mn(Ⅱ)在反应后部分转化为Mn(Ⅲ).MnFe2O4表面上Mn(Ⅱ)可以与PS反应生成Mn(Ⅲ)和SO4-·, 所生成的Mn(Ⅲ)可以连续与PS反应生成Mn(Ⅳ), 见式(6)~(7).
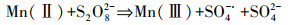 | (6) |
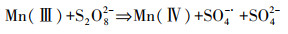 | (7) |
 | (9) |
 | (10) |
 | (11) |
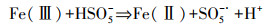 | (12) |
以上结果表明, 多种协同作用参与了微藻的降解, 如图 11所示.复合材料能够将藻细胞吸附到材料表面, 通过电子供体基团如羟基和羧基加速Fe(Ⅲ)、Fe(Ⅱ)和Mn(Ⅲ)、Mn(Ⅱ)、Mn((Ⅳ)之间的价态循环转化, 通过还原S2O82-, 产生空穴、1O2、SO4-·、·OH等多种氧化物质, 以实现藻的分离与氧化破裂.
图 11(Fig. 11)
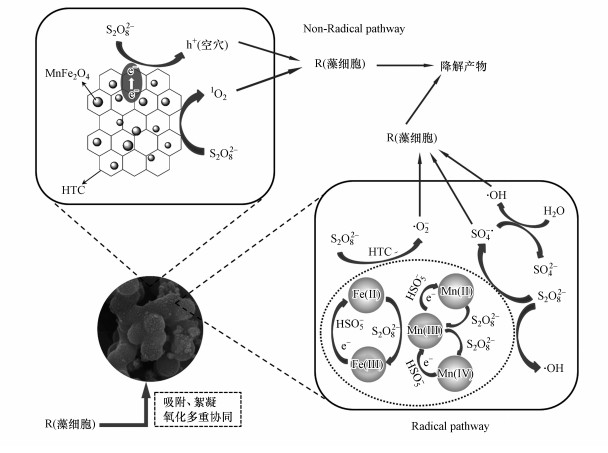 |
| 图 11 MnFe2O4@HTC/ PS体系除藻机理图 Fig. 11Diagram of algae removal mechanism of the MnFe2O4@HTC/PS system |
4 结论(Conclusions)1) 通过水热法和共沉淀法将锰铁氧化物负载HTC表面而制得了MnFe2O4@HTC复合材料, 该材料表面粗糙, 比表面积为448 m2·g-1, 平均孔径为7.7 nm.存在元素C、Mn、Fe、O, 其中Mn和Fe的含量比例大致为1∶2, 表明MnFe2O4成功负载在HTC表面.
2) 在藻初始浓度为1.4×109~1.5×109个·L-1, 催化剂投加量为0.2 g·L-1, 负载比为Mn-Fe3@HTC, PS投加量为0.4 g·L-1, pH=6时除藻效果最佳.pH变化对系统的影响不大, 在3~10的范围内都能达到90%以上的除藻率.Mn-Fe3@HTC/PS体系较单体MnFe2O4/PS体系除藻效能明显增加, 克服了MnFe2O4在溶液中易团聚的缺点.另外, 该体系能够使藻细胞破裂, 并破坏藻细胞光合作用系统, 具有处理有机物的能力.
3) 通过自由基屏蔽和XPS分析对反应机理进行了探究.MnFe2O4@HTC材料对藻细胞有良好的吸附性, 通过Fe(Ⅲ)、Fe(Ⅱ)和Mn(Ⅲ)、Mn(Ⅱ)、Mn((Ⅳ)之间的价态循环转化和HTC的协同作用反应催化PS产生以空穴为主导, 1O2、·O2-、SO4-·和·OH多种氧化物质协同作用的除藻机理.
参考文献
| Ben Hammouda S, Zhao F P, Safaei Z, et al. 2017. Degradation and mineralization of phenol in aqueous medium by heterogeneous monopersulfate activation on nanostructured cobalt based-perovskite catalysts AcoO3 (A=La, Ba, Sr and Ce): Characterization, kinetics and mechanism study[J]. Applied Catalysis B-Environmental, 215: 60-73. DOI:10.1016/j.apcatb.2017.05.051 |
| Buxton G V, Greenstock C L, Helman W P, et al. 1988. Critical-review of rate congtants for reactions of hydrated electrons, hydrogen-atoms and hydroxyl radicals (·OH/·O-) in aqueous-solution[J]. Journal of Physical and Chemical Reference Data, 17(2): 513-886. DOI:10.1063/1.555805 |
| 程昊, 张海平. 2020. 缺磷及高光照条件下紊动对铜绿微囊藻生长的影响[J]. 中国环境科学, 40: 816-823. DOI:10.3969/j.issn.1000-6923.2020.02.042 |
| Cheng X, Guo H G, Zhang Y L, et al. 2017. Non-photochemical production of singlet oxygen via activation of persulfate by carbon nanotubes[J]. Water Research, 113: 80-88. DOI:10.1016/j.watres.2017.02.016 |
| Du J Y, Xu W S, Liu J, et al. 2020. Efficient degradation of Acid Orange 7 by persulfate activated with a novel developed carbon-based MnFe2O4 composite catalyst[J]. Journal of Chemical Technology and Biotechnology, 95(4): 1135-1145. |
| Galindo R, Menendez N, Crespo P, et al. 2014. Comparison of different methodologies for obtaining nickel nanoferrites[J]. Journal of Magnetism and Magnetic Materials, 361: 118-125. DOI:10.1016/j.jmmm.2014.02.091 |
| Heidarpour H, Padervand M, Soltanieh M, et al. 2020. Enhanced decolorization of rhodamine B solution through simultaneous photocatalysis and persulfate activation over Fe/C3N4 photocatalyst[J]. Chemical Engineering Research & Design, 153: 709-720. |
| Hu Z F, Shen Z R, Yu J C. 2017. Converting carbohydrates to carbon-based photocatalysts for environmental treatment[J]. Environmental Science & Technology, 51(12): 7076-7083. |
| 黄芳龙. 2019. MnFe2O4/生物炭复合材料多相光芬顿降解水溶液中四环素的研究[D]. 长沙: 湖南大学 |
| Huang J, Graham N, Templeton M R, et al. 2009. A comparison of the role of two blue-green algae in THM and HAA formation[J]. Water Research, 43(12): 3009-3018. DOI:10.1016/j.watres.2009.04.029 |
| Li Y, Yang Z Q, Zhang H G, et al. 2017. Fabrication of sewage sludge-derived magnetic nanocomposites as heterogeneous catalyst for persulfate activation of Orange G degradation[J]. Colloids and Surfaces a-Physicochemical and Engineering Aspects, 529: 856-863. |
| 蒋绍阶, 刘宗源. 2002. UV254作为水处理中有机物控制指标的意义重庆建筑大学学报[J]. 重庆建筑大学学报, 24: 61-65. |
| Ma Q L, Zhang H X, Zhang X Y, et al. 2019. Synthesis of magnetic CuO/MnFe2O4 nanocompisite and its high activity for degradation of levofloxacin by activation of persulfate[J]. Chemical Engineering Journal, 360: 848-860. DOI:10.1016/j.cej.2018.12.036 |
| Matzek L W, Carter K E. 2016. Activated persulfate for organic chemical degradation: A review[J]. Chemosphere, 151: 178-188. DOI:10.1016/j.chemosphere.2016.02.055 |
| 钱奎梅, 刘霞, 陈宇炜. 2015. 淡水浮游植物计数与定量方法[J]. 湖泊科学, 27: 767-775. DOI:10.18307/2015.0502 |
| Rajasekhar P, Fan L H, Nguyen T, et al. 2012. Impact of sonication at 20 kHz on Microcystis aeruginosa, Anabaena circinalis and Chlorella sp[J]. Water Research, 46(5): 1473-1481. DOI:10.1016/j.watres.2011.11.017 |
| 荣幸. 2019. 磁性生物炭活化过硫酸盐降解水中有机污染物的研究[D]. 济南: 山东大学 |
| 向平, 江雨竹, 姜文超, 等. 2020. 载铁ACF/Ni阴极电化学体系除藻效能与机制[J]. 中国环境科学, 40(11): 5010-5019. DOI:10.3969/j.issn.1000-6923.2020.11.043 |
| 佘月城, 董正玉, 吴丽颖, 等. 2019. MnFe2O4活化过一硫酸盐降解废水中LAS[J]. 中国环境科学, 39: 3323-3331. DOI:10.3969/j.issn.1000-6923.2019.08.025 |
| Spataru A, Jain R, Chung J W, et al. 2016. Enhanced adsorption of orthophosphate and copper onto hydrochar derived from sewage sludge by KOH activation[J]. Rsc Advances, 6(104): 101827-101834. DOI:10.1039/C6RA22327C |
| Velo-Gala I, Lopez-Penalver J J, Sanchez-Polo M, et al. 2017. Role of activated carbon surface chemistry in its photocatalytic activity and the generation of oxidant radicals under UV or solar radiation[J]. Applied Catalysis B-Environmental, 207: 412-423. DOI:10.1016/j.apcatb.2017.02.028 |
| Wu Y, Guo J, Han Y J, et al. 2018. Insights into the mechanism of persulfate activated by rice straw biochar for the degradation of aniline[J]. Chemosphere, 200: 373-379. DOI:10.1016/j.chemosphere.2018.02.110 |
| 薛志欣, 杨桂朋, 马晓梅, 等. 2008. 分光光度法测定藻胆蛋白含量的研究[J]. 鲁东大学学报(自然科学版), (3): 250-253. |
| 俞盈, 韩兰芳, 姜晓满. 2018. 水热炭的制备、结构特征和应用[J]. 环境化学, 37: 1232-1244. |
| Zhao Y, Li Q, Ren H, et al. 2017. Activation of persulfate by magnetic MnFe2O4-bentonite for catalytic degradation of 2, 4-dichlorophenol in aqueous solutions[J]. Chemical Research in Chinese Universities, 33(3): 415-421. DOI:10.1007/s40242-017-6485-3 |
| 赵莹, 任月明, 张慧玉, 等. 2017. GO/CoFe2O4催化过硫酸盐降解邻苯二甲酸二丁酯效能[J]. 哈尔滨工业大学学报, 49: 31-36. |
| Zhou X Q, Jawad A, Luo M Y, et al. 2021. Regulating activation pathway of Cu/persulfate through the incorporation of unreducible metal oxides: Pivotal role of surface oxygen vacancies[J]. Applied Catalysis B-Environmental, 286(119914): 1-12. |
| Zhou Y, Xiao B, Liu S Q, et al. 2016. Photo-Fenton degradation of ammonia via a manganese-iron double-active component catalyst of graphene-manganese ferrite under visible light[J]. Chemical Engineering Journal, 283: 266-275. |
| Zou J, Yu J, Tang L, et al. 2020. Analysis of reaction pathways and catalytic sites on metal-free porous biochar for persulfate activation process[J]. Chemosphere, 261: 127747-127747. |
| Zubir N A, Yacou C, Motuzas J, et al. 2014. Structural and functional investigation of graphene oxide-Fe3O4 nanocomposites for the heterogeneous Fenton-like reaction[J]. Scientific Reports, 4: 1-8. |
