 , 蔺莉莉, 张梦雪, 顾莹莹
, 蔺莉莉, 张梦雪, 顾莹莹
 , 赵朝成, 张秀霞, 刘其友, 张云波
, 赵朝成, 张秀霞, 刘其友, 张云波中国石油大学(华东)环境与安全工程系, 青岛 266580
收稿日期: 2018-11-27; 修回日期: 2019-01-12; 录用日期: 2019-01-12
基金项目: 国家自然科学基金(No.41201303);山东省自然科学基金(No.ZR2017QEE016);中央高校基本科研业务费专项基金(No.17CX02075);中国石油大学(华东)研究生创新工程基金(No.YCX2018048)
作者简介: 杨政伟(1993-), 男, E-mail:yyangzhw@163.com
通讯作者(责任作者): 顾莹莹, E-mail:yingyinggu@upc.edu.cn
摘要: 氢气是一种理想的清洁能源.太阳能驱动的微生物光电化学池(Microbial photoelectrochemical cell,MPEC)因可同时实现废物处理与自发产氢而受到人们的关注.本文以剩余污泥为底物,构建了一种由无定型硫化钼改性硅纳米线(MoS3/SiNWs)光阴极和生物阳极组成的MPEC系统,研究了3组MPEC在不同的酸性阴极液pH和外加电压条件下的产氢及污泥减量效果.研究结果表明,MPEC在阴极液pH为1和3的条件下均能在无外加电压下自发产氢;pH=1的MPEC-1实验中平均产氢速率为(0.66±0.02)mL·h-1,约是pH=3的MPEC-2实验平均产氢速率的1.5倍,但阴极过酸的条件限制了其实际应用;pH为3、外加0.2 V电压的MPEC-3与MPEC-2相比,产氢周期由15 h增加到40 h,平均产氢速率由(0.44±0.05)mL·h-1提高到(0.52±0.04)mL·h-1,污泥TCOD、SCOD、TSS、VSS的降解率分别可达53.96%、70.18%、38.21%和61.76%.可见本文构建的MPEC系统是一种有前景的利用太阳能进行废物处理和资源化的新技术.
关键词:太阳能MoS3/SiNWs光阴极生物阳极产氢剩余污泥
Visible light-driven microbial photoelectrochemical cell for sludge reduction and hydrogen generation
YANG Zhengwei
 , LIN Lili, ZHANG Mengxue, GU Yingying
, LIN Lili, ZHANG Mengxue, GU Yingying
 , ZHAO Chaocheng, ZHANG Xiuxia, LIU Qiyou, ZHANG Yunbo
, ZHAO Chaocheng, ZHANG Xiuxia, LIU Qiyou, ZHANG Yunbo Department of Environmental and Safety Engineering, China University of Petroleum(East China), Qingdao 266580
Received 27 November 2018; received in revised from 12 January 2019; accepted 12 January 2019
Abstract: Hydrogen is an ideal clean energy resource. Microbial photoelectrochemical cell (MPEC) which can realize simultaneous wastes treatment and hydrogen generation has attracted great attention in recent years. In this study, we constructed a MPEC system consisting of a molybdenum sulfide modified silicon nanowire (MoS3/SiNWs) photocathode and a biocatalytic anode. Residual sludge was used as the substrate. Three experiments were carried out to study the effects of acidic catholyte pH and external voltage on hydrogen production and sludge reduction. The results show that MPEC system could generate hydrogen spontaneously at pH 1 &3 without external voltage. under pH 1 in MPEC-1, the average hydrogen production rate was (0.66±0.02) mL·h-1, which was approximately 1.5 times of that under pH 3 in MPEC-2. However, the extreme acidic conditions of catholyte limited its application. Compared with MPEC-2, by adding an additional voltage of 0.2 V at pH=3, the hydrogen production period prolonged from 15 h to 40 h, and the average hydrogen production rate increased from (0.44±0.05) mL·h-1 to (0.52±0.04) mL·h-1 in MPEC-3.The degradation efficiencies of TCOD, SCOD, TSS and VSS of the residual sludge reached 53.96%, 70.18%, 38.21% and 61.76%, respectively. It can be concluded that the MPEC system constructed in this study is a promising new technology for waste treatment and resource utilization.
Keywords: solar energyMoS3/SiNWs photocathodebioanodehydrogen productionresidual sludge
1 引言(Introduction)能源短缺和环境污染是目前人类生存所面临的两个严峻问题.氢气因其高燃值、无污染、热转化效率高等特点被认为是最理想的清洁能源(周汝雁等, 2006), 因此氢能源的利用和制备已经成为未来能源利用的关键所在.同时, 剩余污泥作为生活污水处理的副产物, 其成分复杂, 不仅含有有害的重金属、病菌等物质, 而且还含有大量的有机物质和氮、磷、钾等(Liu et al., 2001; Hlavsová et al., 2014).如果处理和处置剩余污泥的过程不当, 不仅会使资源造成大量的浪费, 还会使环境造成二次污染(王亚炜等, 2013).
微生物电解池(Microbial electrolysis cell, MEC)是一种利用产电微生物将化学能直接转化为氢气的新技术.富集在阳极的产电微生物利用废水或污泥中的有机物和一些还原性小分子无机物为底物, 依靠自身的催化代谢作用将底物降解并释放质子和电子, 电子通过外部导线与内部流动至阴极的质子结合生成氢气(刘文宗, 2011; 刘充等, 2015; Lu et al., 2017; 杨政伟等, 2017), 具有废物处理和同步产氢的优点, 是一种绿色环保无污染的技术.然而MEC阴极上产氢的氧化还原电位比阳极反应的低, 反应不能自发进行.为了克服此能量壁垒, 需外加一个理论值为0.13 V左右的电压(Cheng et al., 2007).而在实际反应中, 由于阴极过电位的存在, 需要更高的外加电压(约为0.3~0.8 V)才能使析氢反应顺利进行(Rozendal et al., 2006; Tartakovsky et al., 2009; Franks et al., 2010; Wang et al., 2013).
太阳能驱动的微生物光电化学池(MPEC)是一种将微生物电解池和光催化相结合的技术.光照射光阴极生成光生电子和空穴, 生物阳极利用自身的催化代谢作用降解底物并释放质子和电子, 电子通过外部导线流向光阴极, 与光生空穴结合, 抑制光生电子-空穴的复合, 而光生电子与H+结合生成氢气(图 1).人们研究了多种半导体材料作为MPEC光阴极在紫外光或可见光照射下的产氢情况.如TiO2光阴极在紫外光照射下与MEC耦合在零偏压、中性条件下可实现产氢(Chen et al., 2013; Wang, et al., 2013).但紫外光仅占太阳能光谱能量的不到5%, 不适用于太阳能制氢.Qian等(2010)首构建了由微生物阳极和p型Cu2O纳米线光电阴极的MPEC, 研究了在20 mW·cm-2的白光照射下在零偏压、中性条件下的协同效应, 成功地证明了MPEC可以产生200 μA的电流, 但没有观察到氢气的产生.Jeon等(2018)采用MoS2负载的p型Cu2O作为光阴极搭建了乙酸盐为底物的光辅助MEC系统, 研究了在外加偏压、中性条件下的产氢性能.结果表明在0.8 V外加偏压时, 该系统可达到225%的能量效率和(2.72±0.31) m3·m-3·d-1的产氢速率.目前Cu2O光阴极多需要施加外加偏压实现持续产氢, 并且易发生光腐蚀.Lu等(2017)采用GaInP2-TiO2-MoSx光阴极组装了以废水为底物、中性环境的单室MPEC系统, 在零偏压的情况下持续24 h产生0.4 mA·cm-2的稳定性电流并产氢.但In价格昂贵, 限制了其实际应用, 同时单室MPEC难以避免实际废水对光阴极造成污染.
图 1(Fig. 1)
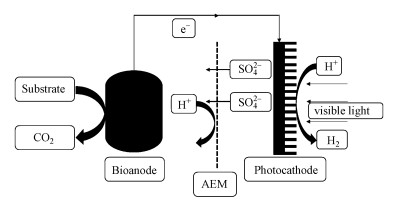 |
| 图 1 微生物光电化学池(MPEC)原理图 Fig. 1Schematic diagram of MPEC |
半导体硅因其具有合适的可见光产氢带隙、价格低廉, 是一种具有广泛应用前景的MPEC光阴极材料.Zang等(2014)构建了一种以乙酸盐为底物、由MoS3修饰的p型硅纳米线(SiNWs)光电阴极和生物阳极组成的MPEC系统, 实现了以4 h为周期的稳定产氢.然而由于系统阴极液为pH=1的极酸性条件, 易导致离子交换膜受到损坏而无法实现持续产氢.本文拟研究不同阴极液pH值和外加电压条件下, 以MoS3/SiNWs为光阴极的双室MPEC体系利用剩余污泥产氢的可行性, 为利用太阳能驱动的微生物电化学系统实现废物减量化与资源化提供理论依据.
2 材料与方法(Materials and methods)2.1 MoS3/SiNWs光阴极制备实验室使用的硅片为硼掺杂p(100)单晶硅片(表面积9 cm2, 厚0.7 mm, 0.005~0.5 Ω·cm-1, 浙江立晶光电有限公司), 硅片先分别用丙酮、乙醇超声清洗15 min, 再放入H2SO4:H2O2(体积比3:1)混合溶液中超声清洗15 min, 进一步去除表面有机物并形成氧化层, 接着用5%HF超声清洗硅片2 min把上一步骤形成的氧化层去除.将清洗后的单晶硅片放入60 mL 0.02 mol·L-1 AgNO3和4.2 mol·L-1 HF的混合溶液中, 在50 ℃下保温刻蚀60 min, 将其放入稀硝酸中处理1 h以去除表面的银颗粒.最后在沉积MoS3前用5% HF清洗2 min以去除表面氧化层(Hou et al., 2011).
如图 2所示, 使用电化学工作站(CHI660E, 上海辰华仪器有限公司), 采用循环伏安电法将MoS3沉积到硅纳米片电极上.电沉积法使用三电极体系, 以Pt丝作为辅助电极, Ag/AgCl为参比电极, 硅片为工作电极, 电解液为2 mmol·L-1 (NH4)2(MoS4)和0.1 mol·L-1 NaClO4混合溶液.扫描范围为-1.0~0.1 V, 扫描速度为50 mV·s-1, 扫描60圈, 将沉积完成的硅片用去离子水反复冲洗几次后用氮气吹干备用.
图 2(Fig. 2)
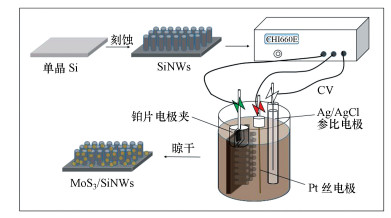 |
| 图 2 MoS3/SiNWs电极制备示意图 Fig. 2Schematic of MoS3/SiNWs electrode |
2.2 污泥来源与预处理本实验所用的污泥来自于山东省青岛市某污水处理厂回流污泥.污泥静置1周后进行碱预处理:向污泥中加入1 mol·L-1 NaOH溶液至pH=11, 搅拌1 h后用1 mol·L-1 HCl溶液中和至pH=7.污泥使用之前, 加入一定量的磷酸盐缓冲溶液(PBS), 并用高纯氮气(99.999%)曝气20 min以除去污泥中的氧气, 提供微生物生长的厌氧环境.预处理后的污泥参数如表 1所示.
表 1(Table 1)
| 表 1 预处理后剩余污泥的理化性质 Table 1 Physicochemical properties of the residual sludge after pretreatment | ||||||||||||||||||
表 1 预处理后剩余污泥的理化性质 Table 1 Physicochemical properties of the residual sludge after pretreatment
| ||||||||||||||||||
2.3 反应器的构建与运行本实验所用的MPEC生物阳极由双室MFC方式启动.在MFC中, 阳极和阴极分别为碳纤维刷和负载Pt/C粉(0.5 mg·cm-2)的防水碳布, 通过钛线经由510 Ω电阻相连.阴极液为pH=7.0的50 mmol·L-1 PBS.启动过程中通过数据采集仪(TP1608-Z, 深圳拓普瑞电子有限公司)实时监测510 Ω电阻两端的电压.
当MFC达到约350 mV稳定电压时视为完成启动.采用改变外部电阻法进行MFC的极化曲线和功率密度曲线测定, 并采用日立S4800型扫描电子显微镜(SEM)观察阳极表面微生物形貌.将富集完成的生物阳极取出放入双室MPEC装置中(图 3).阳极室和阴极室(两室体积均为216 mL)由阴离子膜(AMI-7001, 杭州绿合环保科技有限公司)隔开, 阳极和阴极分别为碳纤维刷和MoS3/SiNWs, 两电极之间串联一个51 Ω的电阻, 阴极室电解液为H2SO4+0.5 mol·L-1 K2SO4溶液(pH=1或3).通过数据采集仪实时监测电阻两端电压, 阴极室密封并用气袋收集阴极产生的气体, 使用气相色谱测定氢气含量.用300 W氙灯(PLS-SXE-300UV, 北京伯菲莱有限公司)加420 nm滤光片模拟可见光, 实验时分别在光照/不光照条件下进行.共进行了3组实验, 实验参数如表 2所示.
图 3(Fig. 3)
 |
| 图 3 MPEC装置 Fig. 3MPEC device |
表 2(Table 2)
| 表 2 MPEC实验的运行条件 Table 2 Operational conditions of MPEC experiments | ||||||||||||||||
表 2 MPEC实验的运行条件 Table 2 Operational conditions of MPEC experiments
| ||||||||||||||||
2.4 测定方法2.4.1 MoS3/SiNWs表征采用日立S4800型扫描电子显微镜(SEM)观察SiNWs和MoS3/SiNWs表面形貌, 加速电压为30 kV.采用热电ESCALab-250Xi型X射线光电子能谱仪(XPS)对MoS3/SiNWs的表面元素组成进行测定.采用日本理学MSAL-XD2型X射线衍射仪(XRD)对SiNWs和MoS3/SiNWs的晶型和结构进行测定, 辐射源为Cu Kα射线, 衍射角2θ为5°~75°.用电化学工作站(CHI660E, 上海辰华仪器有限公司)线性扫描伏安法(LSV)对MoS3/SiNWs光阴极进行电化学表征.以Pt丝作为辅助电极, Ag/AgCl为参比电极, MoS3/SiNWs为工作电极, H2SO4+0.5 mol·L-1 K2SO4溶液(pH=1或3)为光电化学测试的电解液, 300 W氙灯加上420 nm滤光片作为模拟可见光源对光阴极进行LSV扫描.扫描范围分别为-0.2~0.2 V(pH=1)、-0.5~0.2 V(pH=3), 扫描速率为50 mV·s-1.光电流对可见光的暂态电流响应也使用LSV表征, 扫描范围同上, 扫描速率为20 mV·s-1.
2.4.2 污泥指标测定污泥的pH值用pH计(PHS-3C, 上海仪电科学仪器股份有限公司)进行测量.污泥中总固体悬浮物(TSS)和可挥发性固体悬浮物(VSS)、可溶性化学需氧量(SCOD)和总化学需氧量(TCOD)分别按照国标GB11901-89和国标HJ828—2017测定.
2.4.3 氢气测定通过气体收集袋实时收集MPEC产出氢气, 使用配备有热导检测器和以氩气作为载气的1.5 m不锈钢柱的气相色谱仪(型号Agilen7890A, 安捷仑)每2 h测一次产氢.
3 结果与讨论(Results and discussion)3.1 MoS3/SiNWs光阴极表征MoS3/SiNWs光阴极的SEM图见图 4.通过XPS进一步分析MoS3/SiNWs表面的元素组成.图 5a为MoS3/SiNWs的XPS谱图, 图中给出了S、Mo元素的特征谱图.图 5b和5c分别为MoS3/SiNWs电极Mo 3d和S 2s区及S 2p区的XPS谱图.Mo 3d轨道的结合能为232. 6 eV, Mo元素的离子价态为+4价.Mo 3d信号显示Mo 3d3和3d5的特征双峰的结合能分别为232.6 eV和229.4 eV, 这与已有的报道中MoS3中Mo的结合能相同.在Mo 3d信号低的一侧, 有S 2s的XPS信号, 结合能为225. 8 eV.图 5c中XPS谱图中, 有S 2p的两个特征峰, 结合能分别为167.8 eV和162.4 eV, 表明S2-和S22-配体的存在(Merki et al., 2011; Xie et al., 2014).在162.4 eV的峰值可能是S2-, 另一个具有较高的结合能可能是S22-.通过对MoS3/SiNWs的XPS分析, 可以证明MoS3成功的负载到了硅纳米片上.图 5d为SiNWs和MoS3/SiNWs的XRD表征图, 从图中可以看出沉积MoS3前后SiNWs在2θ约为69°有一个超强特征峰, 这是典型的p-Si(100)晶面特征峰, 内插图中为两个较小的非p-Si(100)特征峰, 沉积后未出现其他特征峰, 而XPS分析确定了MoS3已经成功的负载到了硅纳米片上, 这说明SiNWs上的MoS3是以无定型的结构存在.
图 4(Fig. 4)
 |
| 图 4 MoS3 /SiNWs光阴极SEM图 Fig. 4SEM image of the MoS3 /SiNWs photocathode |
图 5(Fig. 5)
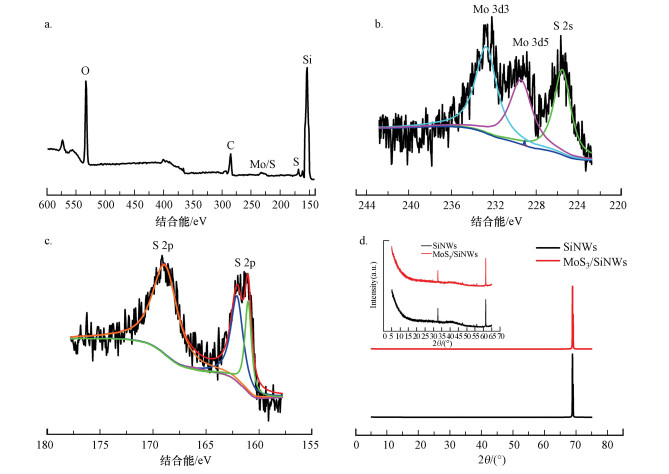 |
| 图 5 MoS3 /SiNWs的XPS图(a.全谱图; b. Mo 3d和S 2s区谱图; c. S 2p区谱图)及MoS3 /SiNWs的XRD图(d) Fig. 5XPS spectra of the MoS3/ SiNWs(a. full spectrum; b. Mo 3d and S 2s region; c. S 2p region) and XRD spectrogram of MoS3 /SiNWs(d) |
3.2 MoS3/SiNWs光阴极电化学性能图 6a比较了pH=1条件下SiNWs和MoS3/SiNWs的光响应线性扫描曲线及不同pH(pH=1、3和4)下MoS3/SiNWs的光响应线性扫描曲线. MoS3是一种非常高效的利用水产氢的非贵金属催化剂(Xie et al., 2014).从图中可以看出, 将MoS3沉积到SiNWs后, MoS3/SiNWs相较于SiNWs对光的响应更加优异, 在-0.18 V(vs Ag/AgCl)左右时, MoS3/SiNWs的光响应电流为-1.12 mA·cm-2; 而SiNWs在-0.18 V(vs Ag/AgCl)左右时, 光响应电流仅为-0.2 mA·cm-2左右.这说明MoS3对SiNWs大大增加了SiNWs的光响应.另一方面, 随着电解液pH值升高, MoS3/SiNWs光阴极的光电流呈明显降低趋势.MoS3/SiNWs在pH=1的情况下, 光响应效果优异, 在-0.18 V(vs Ag/AgCl)左右时, MoS3/SiNWs的光电流可达到-1.12 mA·cm-2; 而在pH=3时, 相同偏压下光电流仅为-0.03 mA·cm-2.当pH=4时, 产生-1.12 mA·cm-2光电流所施加的偏压比pH=1时增加了约0.4 V.这说明MoS3/SiNWs光阴极的光响应随着pH值升高明显降低.为了更清晰地反映出光电极的光响应特性, 采用手动斩光的方式进行线性扫描测试.从图 6b、6c和6d中可以更清晰地看出, 无论是SiNWs还是不同pH值条件下的MoS3/SiNWs电极在手动斩光下, 产生了显著的电流差异, 且随着扫描电压的负移呈现出的差异越来越明显.
图 6(Fig. 6)
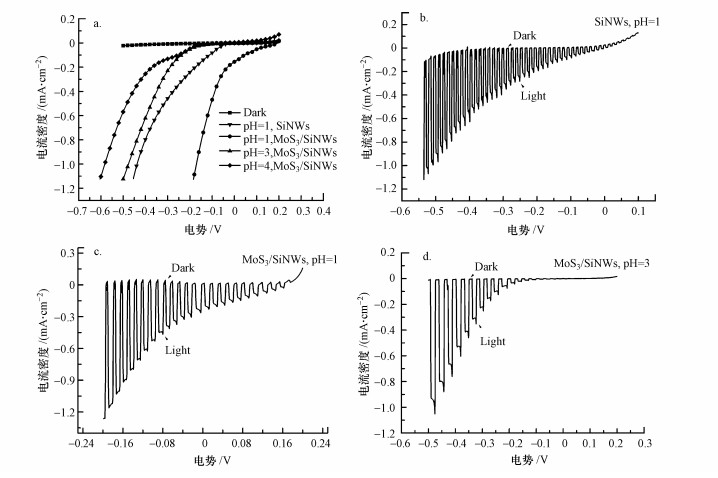 |
| 图 6 SiNWs和MoS3/SiNWs光响应线性扫描曲线对比图 (a.pH=1、3 & 4, MoS3/SiNWs和SiNWs(pH=1)的光响应线性扫描曲线图, b.pH=1, SiNWs的光瞬态电流响应线性扫描曲线图, c.pH=1, MoS3/SiNWs的光瞬态电流响应线性扫描曲线图, d. pH=3. MoS3/SiNWs的光瞬态电流响应线性扫描曲线图) Fig. 6Photoresponse linear sweep voltammograms (LSV) of SiNWs & MoS3/SiNWs (a.Photoresponse LSV of MoS3/SiNWs at pH=1、3 & 4 and SiNWs at pH=1, b. LSV transient current responses of SiNWs at pH=1, c.LSV transient current responses of MoS3/SiNWs at pH=1, d. LSV transient current responses of MoS3/SiNWs at pH=3) |
3.3 MFC启动性能通过双室MFC进行生物阳极的富集培养, 510 Ω外接电阻的电压从零开始逐渐增大, 经过约160 h的启动周期, 最高输出电压稳定在350 mV左右.采用改变外电阻法, 得到图 7a中的MFC极化曲线和功率密度曲线.从图中可以看出启动完成后的MFC最大功率密度可达到632 mW·cm-2.通过极化曲线直线部分的斜率, 可粗略计算出MFC内阻为200 Ω, 此时MFC记录电压为320 mV, 电流密度约为1.78 mA·cm-2.从图 7b的SEM图中, 可以看到有产电微生物已经成功富集在了碳纤维刷上.
图 7(Fig. 7)
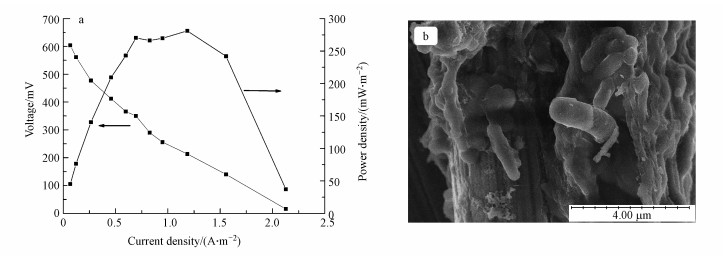 |
| 图 7 MFC的极化曲线和功率密度曲线(a)及MFC生物阳极的扫描电镜图(b) Fig. 7MFC polarization and power density curves(a) and SEM of MFC bioanode(b) |
3.4 MPEC系统电流密度从图 8可以看出, 3组MPEC实验在无可见光照条件下均没有监测到明显电流.这是因为MPEC在无光照时, 光阴极无法发生电子跃迁生成光生电子和空穴, 而由于析氢过电位的存在, 生物阳极降解污泥产生的电子无法流动到光阴极与质子结合生成氢气.而在有可见光照射时, 3个MPEC体系均有持续的电流.这表明MoS3/SiNWs光催化阴极在光照条件下可以克服系统的热力学壁垒, 构成了原电池系统.生物阳极降解底物产生的电子随着外部导线流向阴极, 抑制了MoS3/SiNWs电极在光照下产生的光生电子-空穴对复合.在可见光照条件下, MPEC-1(pH=1)的初始电流密度可高达0.49 mA·cm-2, 是相同条件下MPEC-2(pH=3)的初始电流(0.18 mA·cm-2)的2.72倍.可见pH值降低有利于提高MPEC的光阴极电位及开路电压, 可大大提高系统的电流密度.本研究同时构建了阴极电解液pH=4的MPEC系统, 发现电流始终为零, 即系统无法实现自发污泥降解和产氢.在MPEC-3中, 在生物阳极与光阴极之间施加了0.2 V的偏压, 系统的电流密度由0.18 mA·cm-2提高到了0.21 mA·cm-2.这说明外加电压可以有效增大MPEC系统阳极与阴极之间的电势差, 从而提高输出电流.对比3组实验的电流密度, 可见阴极电解液的pH值以及外加偏压均为影响MPEC的电流密度和系统性能的重要因素.
图 8(Fig. 8)
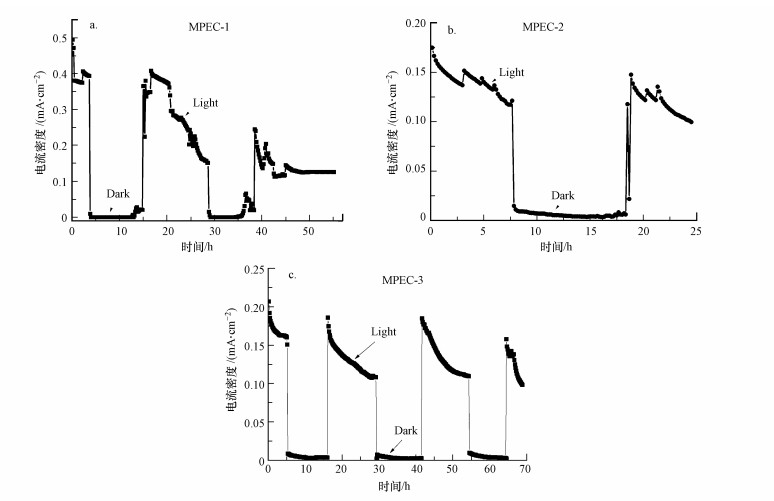 |
| 图 8 MPEC系统电流密度曲线 (a.MPEC-1, b.MPEC-2, c. MPEC-3) Fig. 8Current density curve of MPEC system (a. MPEC-1, b. MPEC-2, c. MPEC-3) |
在MPEC系统运行期间, 3组MPEC电流密度均随光照时间呈现持续下降趋势.其中MPEC-1实验中电流密度下降最为迅速, 由初始的0.49 mA·cm-2经过35 h的光照后下降到约0.11 mA·cm-2.而在MPEC-2 & 3实验中, 电流密度分别由初始的0.18 mA·cm-2和0.21 mA·cm-2经过15 h和40 h的光照降到0.10 mA·cm-2左右.当电流密度下降到0.10 mA·cm-2左右时阴极停止产氢, 此时实验停止.BPEC-1实验电流密度快速下降的原因可能是阴离子交换膜无法阻挡pH=1阴极液中的高浓度质子, 使得阳极液的pH快速降低(实验结束后测得阳极液的pH由初始的7.0降到2.3), 严重抑制了阳极产电微生物的活性, 从而导致电流密度的急剧降低.而在阴极液pH=3的MPEC-2 & 3实验中, 实验结束时阳极液的pH值仅从7.0分别降低到6.87和6.76.造成这两组实验电流密度降低的可能原因有3个:①MPEC系统在可见光的持续照射下, 由于阴离子交换膜被污染造成装置内阻逐渐增大(实验后靠近污泥阳极室一侧的膜表面有黑色污渍, 会堵塞离子通道); ②阳极室污泥COD被阳极微生物降解消耗, 底物浓度逐渐降低; ③MoS3/SiNWs光阴极电位在持续光照下因发生光腐蚀呈下降趋势, 实验结束时MPEC-1、MPEC-2和MPEC-3 3组实验的阴极电位分别从初始的-0.125、-0.267和-0.258 V(vs Ag/AgCl)降低到-0.295、-0.305和-0.309 V(vs Ag/AgCl).通过对MPEC-3实验后的MoS3/SiNWs光阴极进行LSV分析, 发现其光响应变差, 在-0.18 V(vs Ag/AgCl)偏压时, 光电流由反应前的-0.03 mA·cm-2降低到-0.008 mA·cm-2.MPEC-3的电流密度降低最缓慢, 说明外加0.2 V电压可以将生物阳极的电位维持在合适的范围, 从而有效阻止电流的下降.
3.5 MPEC产氢和污泥减量在本文设计的MPEC系统中, 在阴极液pH=1或3时, 光阴极均可在可见光的照射下实现自发产氢.通过对比图 8与图 9a, 可见MPEC体系的产氢量与电流密度随时间的变化趋势基本一致.MPEC-1的初始产氢速率最高, 产氢周期约为35 h左右; MPEC-2实验的产氢速率最低, 且产氢周期最短, 仅为15 h; 而MPEC-3实验的产氢速率比MPEC-2明显提高, 且产氢周期延长到40 h左右.在光照的前16~20 h期间, 3组实验的产氢量随时间的降低速率相近, 这说明在实验前期, 造成电流密度下降的原因主要是系统内阻的增大.在MPEC-1实验中, 产氢量在持续光照20 h后迅速降低, 这可能是因为阳极室pH值的急剧下降抑制了产电微生物对污泥的降解和电子的传递.而MPEC-2 & 3实验中阴离子交换膜可有效阻止阴极溶液中质子的通过, 阳极微生物未受到急剧冲击, 仅由于系统内阻增大导致电流密度降低, 从而使得阳极电位升高, 造成产氢性能逐渐降低.
图 9(Fig. 9)
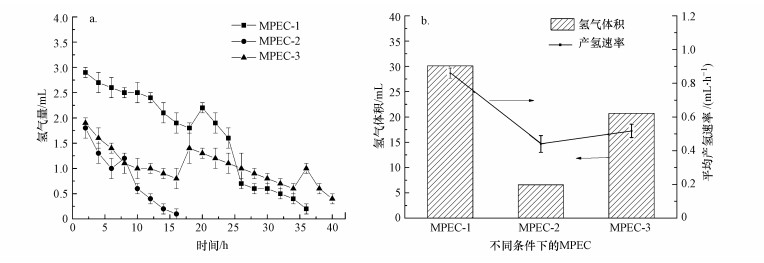 |
| 图 9 3组MPEC实验的产氢 (a.产氢量随时间变化, b.累积产氢量和平均产氢速率) Fig. 9Hydrogen generation in three MPEC experiemts (a.hydrogen volume with time, b. cumulative hydrogen volume and average hydrogen generation rate) |
图 9b给出了3组实验整个产氢周期的累积产氢量和平均产氢速率.3组MPEC实验的累积产氢量分别为30.1、6.6、20.7 mL, 平均产氢速率分别为(0.66±0.02)、(0.44±0.05)、(0.52±0.04) mL·h-1, 对比数据可知, MPEC-1的累积产氢量为MPEC-2的4.6倍, 平均产氢速率是其1.5倍.这是因为在相同的可见光照条件下, MoS3/SiNWs光阴极在pH=1的酸性条件下光响应较为优异, MPEC在不同pH条件下的电流密度也证明了这一观点.MPEC-3实验的累积产氢量和平均产氢速率与MPEC-1相近, 分别为MPEC-2的3.14倍和1.18倍.产氢周期也由一开始的15 h提高到40 h.
实验结束后, 分别对MPEC-2 & 3实验阳极室剩余污泥的TCOD、SCOD、TSS、VSS进行了测定.如图 10所示, MPEC-3中污泥的TCOD和SCOD的降解率分别高达53.96%和70.18%, 相比于MPEC-2的TCOD和SCOD去除率(13.97%和25.32%)分别提高了2.86和1.77倍.同时, 污泥的TSS和VSS也在较短的运行时间内得到较好的去除.MPEC-3中污泥的TSS和VSS的降解率分别为38.21%和61.76%, 相比于MPEC-2的TSS和VSS去除率(19.29%和32.67%)分别提高了0.98和0.89倍.这是因为在pH为3的MPEC体系中, 施加0.2 V额外电压不仅增加了系统的电流密度, 同时延长了产氢周期.这必然导致更多的剩余污泥被阳极微生物降解, 有利于污泥减量.
图 10(Fig. 10)
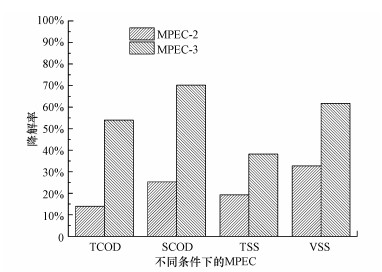 |
| 图 10 MPEC-2 & 3实验的污泥降解性能 Fig. 10Sludge degradation inexperiments MPEC-2 & 3 |
为了研究外加电压对MPEC性能的影响, 对施加0 V和0.2 V电压条件下的MPEC-2和MPEC-3系统的库仑效率、法拉第效率、H2转化效率和能量转化效率进行了比较, 结果如表 3所示.两组MPEC系统的库仑效率和H2转换效率均较低, 分别为1.57%、1.74%和1.62%、1.64%.在Lu等(2017)的研究中, 以人工废水为底物, GaInP2-TiO2-MoSx和GaInP2-PtRu分别作为光阴极的单室MPEC系统也获得了较低的库仑效率(分别为9%和4%).本研究中库仑效率和氢气转换效率均较低的原因可能是:①本研究采用的是双室装置, 相对于单室系统内阻较高; ②剩余污泥直接在阳极室被非产电微生物降解.外加0.2 V电压的MPEC-3系统的库仑效率和法拉第效率相比与MPEC-2未有明显提高.这不同于Lu等(2017)的研究结果, 可能是由于施加的电压较低, 并且污泥中存在大量的污泥发酵细菌.另一方面, 两组MPEC系统的法拉第效率分别可达到94%和96%, 这说明传递到外电路的电子被MoS3/SiNWs光阴极在光照下产生的光生空穴结合, 而绝大部分光生电子将阴极液中的H+还原为氢气.MPEC-3系统的能量回收效率为26.40%, 而无外加电压的MPEC-2系统可在无外界能量输入的条件下自发产氢, 具有较大的能量优势.
表 3(Table 3)
| 表 3 MPEC系统的库仑效率、法拉第效率、H2转换效率和能量效率 Table 3 Coulombic efficiency, faradaic efficiency, hydrogen conversion efficiency and energy recovery efficiency in MPEC systems | |||||||||||||||
表 3 MPEC系统的库仑效率、法拉第效率、H2转换效率和能量效率 Table 3 Coulombic efficiency, faradaic efficiency, hydrogen conversion efficiency and energy recovery efficiency in MPEC systems
| |||||||||||||||
4 结论(Conclusions)1) 3组MPEC在运行期间, 电流密度均呈下降趋势.在阴极液pH=1的MPEC-1中, 系统的初始电流密度可达0.49 mA·cm-2, 远高于阴极液pH=3的MPEC-2系统的初始电流密度(0.18 mA·cm-2); 施加0.2 V外加电压会提高系统的初始电流密度并减缓电流密度的下降.
2) MPEC系统的产氢量随时间的变化与电流密度的变化趋势大致相同, MPEC-1产氢速率最快.但由于阴极液质子的向阳极室扩散导致生物阳极性能下降, 产氢量急剧下降.MPEC-2系统中, 虽可实现自发产氢, 但产氢周期和累积产氢量仅分别为15 h和6.6 mL.通过施加0.2 V电压, MPEC-3的产氢周期和产氢量分别可提高到40 h和20.7 mL.
3) 施加0.2 V额外电压可通过增大电流密度和产氢周期显著提高MPEC的污泥降解性能.MPEC-3实验中污泥的TCOD、SCOD、TSS和VSS的降解率分别比MPEC-2实验提高了2.86、1.77、0.98和0.89倍.
本文构建的可见光驱动的MPEC系统可实现同步污泥减量和自发产氢, 在废物减量与资源化方向有较好的应用前景.今后可研究寻找在近中性条件下有持续优异性能的光催化阴极来提高MPEC的性能, 或通过改变MPEC构型设计(如三室构型)来解决酸性阴极液对阳极微生物的冲击破坏, 推动该系统的实际应用.
参考文献
| Chen Q Y, Liu J S, Liu Y, et al. 2013. Hydrogen production on TiO2 nanorod arrays cathode coupling with bio-anode with additional electricity generation[J]. Journal of Power Science, 238: 345–349.DOI:10.1016/j.jpowsour.2013.04.066 |
| Cheng S, Logan B E. 2007. Sustainable and efficient biohydrogen production via electrohydrogenesis[J]. Proceedings of the National Academy of Sciences, 104(47): 18871–18873.DOI:10.1073/pnas.0706379104 |
| Franks A E, Nevin K P. 2010. Microbial fuel cells, a current review[J]. Energies, 3(5): 899–919.DOI:10.3390/en3050899 |
| Hlavsová A, Corsaro A, Raclavská H, et al. 2014. The effects of varying CaO content and rehydration treatment on the composition, yield, and evolution of gaseous products from the pyrolysis of sewage sludge[J]. Journal of Analytical and Applied Pyrolysis, 108: 160–169.DOI:10.1016/j.jaap.2014.05.004 |
| Hou Y, Abrams B L, Vesborg P C K, et al. 2011. Bioinspired molecular co-catalysts bonded to a silicon photocathode for solar hydrogen evolution[J]. Nature Materials, 10(6): 434–438.DOI:10.1038/nmat3008 |
| Jeon Y, Kim J H, Koo K, et al. 2018. A photo-assisted microbial electrolysis cell for the exclusive biohydrogen production using a MoS2 -coated p-type copper oxide[J]. Journal of Power Sources, 373: 79–84.DOI:10.1016/j.jpowsour.2017.11.003 |
| Liu Y, Tay J. 2001. Strategy for minimization of excess sludge production from the activated sludge process[Z]. England: Elsevier Inc, 19: 97-107 |
| 刘充, 刘文宗, 王爱杰. 2015. 微生物电解池阳极生物膜功能菌群构建及群落特征分析[J]. 微生物学通报, 2015, 42(5): 845–852. |
| 刘文宗. 2011.有机废水微生物电解产氢研究及电极微生物功能解析[D].哈尔滨: 哈尔滨工业大学http://d.wanfangdata.com.cn/Thesis/D263882 |
| Lu L, Williams N B, Turner J A, et al. 2017. Microbial photoelectrosynthesis for self-sustaining hydrogen generation[J]. Environmental Science & Technology, 51(22): 13494–13501. |
| 路璐. 2012.生物质微生物电解池强化产氢及阳极群落结构环境响应[D].哈尔滨: 哈尔滨工业大学http://cdmd.cnki.com.cn/Article/CDMD-10213-1013035368.htm |
| Merki D, Fierro S, Vrubel H, et al. 2011. Amorphous molybdenum sulfide films as catalysts for electrochemical hydrogen production in water[J]. Chemical Science, 2(7): 1262–1267.DOI:10.1039/C1SC00117E |
| Qian F, Wang G, Li Y. 2010. Solar-Driven microbial photoelectrochemical cells with a nanowire photocathode[J]. Nano Letters, 10(11): 4686–4691.DOI:10.1021/nl102977n |
| Rozendal R, Hamelers H, Euverink G, et al. 2006. Principle and perspectives of hydrogen production through biocatalyzed electrolysis[J]. International Journal of Hydrogen Energy, 31(12): 1632–1640.DOI:10.1016/j.ijhydene.2005.12.006 |
| Tartakovsky B, Manuel M, Wang H, et al. 2009. High rate membrane-less microbial electrolysis cell for continuous hydrogen production[J]. International Journal of Hydrogen Energy, 34(2): 672–677.DOI:10.1016/j.ijhydene.2008.11.003 |
| Wang H, Qian F, Wang G M, et al. 2013. Self-biased solar-microbial device for sustainable hydrogen generation[J]. ACS Nano, 7(10): 8728–8735.DOI:10.1021/nn403082m |
| Wang H, Ren Z J. 2013. A comprehensive review of microbial electrochemical systems as a platform technology[J]. Biotechnology Advances, 31(8): 1796–1807.DOI:10.1016/j.biotechadv.2013.10.001 |
| 王亚炜, 肖庆聪, 阎鸿, 等. 2013. 基于微波预处理的源头污泥减量研究[J]. 中国给水排水, 2013, 29(15): 19–23.DOI:10.3969/j.issn.1000-4602.2013.15.005 |
| Xie C, Nie B, Zeng L, et al. 2014. Core-shell heterojunction of silicon nanowire arrays and carbon quantum dots for photovoltaic devices and self-driven photodetectors[J]. ACS Nano, 8(4): 4015–4022.DOI:10.1021/nn501001j |
| 杨政伟, 顾莹莹, 赵朝成, 等. 2017. 土壤微生物燃料电池的研究进展及展望[J]. 化工学报, 2017, 68(11): 3995–4004. |
| Zang G, Sheng G, Shi C, et al. 2014. A bio-photoelectrochemical cell with a MoS3-modified silicon nanowire photocathode for hydrogen and electricity production[J]. Energy & Environmental Science, 7(9): 3033–3039. |
