2.中国科学院大学,北京 100049
1.State Key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
2.University of Chinese Academy of Sciences, Beijing 100049, China
土壤/沉积物中重金属的污染问题越来越引起重视,而重金属在环境中的生态风险与其生物可利用性和生物有效性密切相关。在总结国内外研究的基础上,明确了重金属生物有效性和生物可利用性的定义;概述了用于研究土壤/沉积物中重金属生物有效性的生物模型(小鼠、猪、兔子等);总结了用于研究土壤/沉积物中重金属生物可利用性的几种体外方法,包括模拟人类肠胃消化(PBET、SBRC、UBM等)和底栖生物消化;分析了土壤/沉积物中重金属生物有效性和生物可利用性的关键影响因素(土壤/沉积物理化性质和分析方法)。提出了未来土壤/沉积物中重金属生物有效性和生物可利用性的研究方向,以期为重金属生态风险的评价和控制提供参考。
Heavy metal pollution of soil/sediment has attracted increasing attention, and heavy metal risk in the environment is closely related to their bioavailability and bioaccessibility. Based on the previous work, this paper clarified the definition of heavy metal bioavailability and bioaccessibility, summarized several animal models (mice, pigs, rabbits, etc.) for assessing heavy metal bioavailability and in vitro digestion models of simulating human stomach (PBET, SBRC, UBM, etc.) or benthon digestion for assessing heavy metal bioaccessibility in soil/sediment, analyzed the key factors (physico-chemical properties of soil/sediment and analysis methods) affecting their bioavailability and bioaccessibility. This study also pointed out the suggestion for future research directions, aiming at providing support for risk assessment and control of heavy metals in soil/sediment.
.
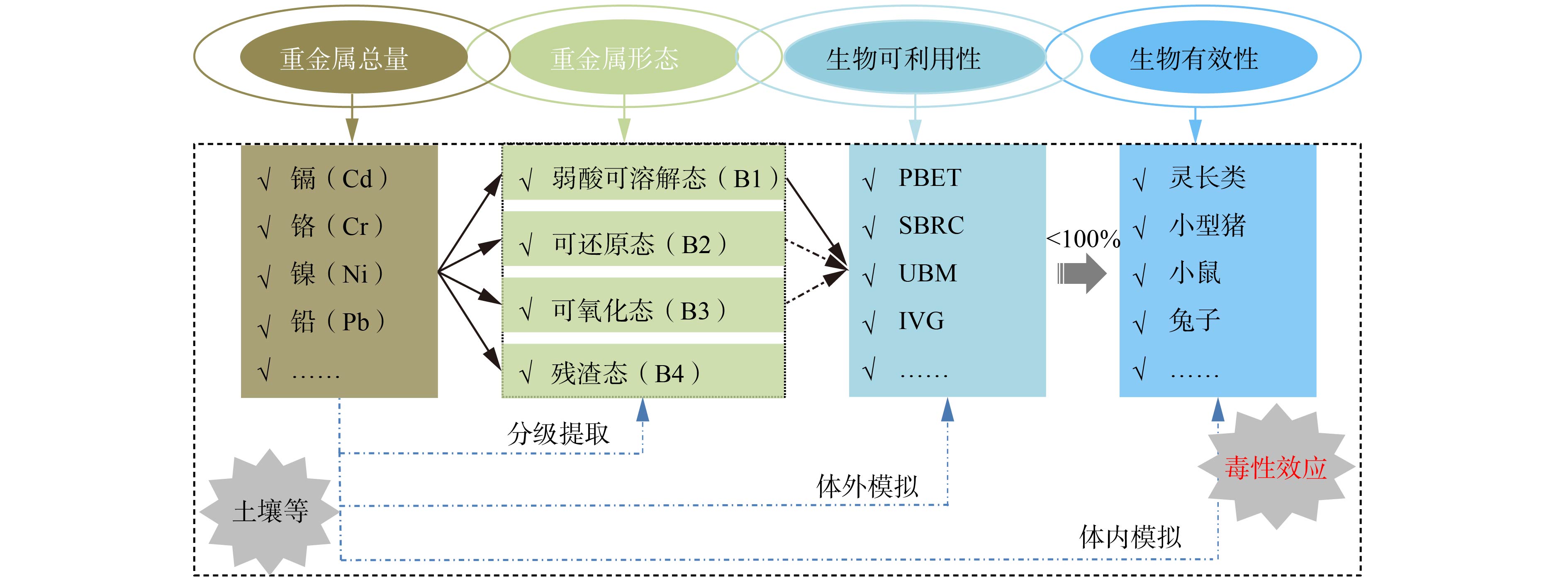
Relationship between heavy metal bioaccessibility and bioavailability
In vitro gastrointestinal simulation models for the determination of heavy metal bioaccessibility in soil
| [1] | 蔡美芳, 李开明, 谢丹平, 等. 我国耕地土壤重金属污染现状与防治对策研究[J]. 环境科学与技术, 2014, 37(2): 223-230. |
| [2] | 俞慎, 历红波. 沉积物再悬浮-重金属释放机制研究进展[J]. 生态环境学报, 2010, 19(7): 1724-1731. doi: 10.3969/j.issn.1674-5906.2010.07.038 |
| [3] | ZAHRA A, HASHMI M Z, MALIK R N, et al. Enrichment and geo-accumulation of heavy metals and risk assessment of sediments of the Kurang Nallah-Feeding tributary of the Rawal Lake Reservoir, Pakistan[J]. Science of the Total Environment, 2014, 470: 925-933. |
| [4] | SOFUOGLU S C, SOFUOGLU A. An exposure-risk assessment for potentially toxic elements in rice and bulgur[J]. Environmental Geochemistry and Health, 2018, 40(3): 987-998. doi: 10.1007/s10653-017-9954-1 |
| [5] | WATANABE T, WANG P Y, LIU A P, et al. Dietary intake of cadmium and lead by kindergarten children in several cities and villages in china[J]. Biomedical Research on Trace Elements, 2017, 28(1): 18-27. |
| [6] | JUHASZ A L, WEBER J, SMITH E, et al. Assessment of four commonly employed in vitro arsenic bioaccessibility assays for predicting in vivo relative arsenic bioavailability in contaminated soils[J]. Environmental Science & Technology, 2009, 43(24): 9487-9494. |
| [7] | 李士伟. 污染土壤中典型重金属的人体生物有效性研究[D]. 南京: 南京大学, 2017. |
| [8] | DAVIS A, RUBY M V, BERGSTROM P D. Bioavailability of arsenic and lead in soils from the Butte, Montana, mining district[J]. Environmental Science & Technology, 1992, 26(3): 461-468. |
| [9] | XIA Q. Assessing exposure risk of arsenic, cadmium and lead (or mixed with PAHs) in soils using in-vitro methods[D]. Queensland: The University of Queensland, 2016. |
| [10] | XIA Q, PENG C, LAMB D, et al. Effects of arsenic and cadmium on bioaccessibility of lead in spiked soils assessed by unified BARGE method[J]. Chemosphere, 2016, 154: 343-349. doi: 10.1016/j.chemosphere.2016.03.133 |
| [11] | JUHASZ A L, SMITH E, WEBER J, et al. Effect of soil ageing on in vivo arsenic bioavailability in two dissimilar soils[J]. Chemosphere, 2008, 71(11): 2180-2186. doi: 10.1016/j.chemosphere.2007.12.022 |
| [12] | LI S W, SUN H J, LI H B, et al. Assessment of cadmium bioaccessibility to predict its bioavailability in contaminated soils[J]. Environment International, 2016, 94: 600-606. doi: 10.1016/j.envint.2016.06.022 |
| [13] | LOPEZ G R, LEVINTON J S. Ecology of deposit-feeding animals in marine sediments[J]. The Quarterly Review of Biology, 1987, 62(3): 235-260. doi: 10.1086/415511 |
| [14] | 汪飞, 黄小平. 海洋沉积物中重金属对底栖无脊椎动物的生物有效性[J]. 生态学杂志, 2012, 31(1): 207-214. |
| [15] | ZHANG C, YU Z G, ZENG G M, et al. Effects of sediment geochemical properties on heavy metal bioavailability[J]. Environment International, 2014, 73: 270-281. doi: 10.1016/j.envint.2014.08.010 |
| [16] | NASR S M, KHAIRY M A, OKBAH M A, et al. AVS-SEM relationships and potential bioavailability of trace metals in sediments from the Southeastern Mediterranean Sea, Egypt[J]. Chemistry and Ecology, 2014, 30(1): 15-28. doi: 10.1080/02757540.2013.831080 |
| [17] | MEYLAN S, BEHRA R, SIGG L. Accumulation of copper and zinc in periphyton in response to dynamic variations of metal speciation in freshwater[J]. Environmental Science & Technology, 2003, 37: 5204-5212. doi: 10.1021/es034566+ |
| [18] | TANG W Z, XIA Q, SHAN B Q, et al. Relationship of bioaccessibility and fractionation of cadmium in long-term spiked soils for health risk assessment based on four in vitro gastrointestinal simulation models[J]. Science of the Total Environment, 2018, 631-632: 1582-1589. doi: 10.1016/j.scitotenv.2018.03.154 |
| [19] | RUBY M V, DAVIS A, LINK T E, et al. Development of an in vitro screening test to evaluate the in vivo bioaccessibility of ingested mine-waste lead[J]. Environmental Science & Technology, 1993, 27(13): 2870-2877. |
| [20] | RODRIGUEZ R R, BASTA N T. An in vitro gastrointestinal method to estimate bioavailable arsenic in contaminated soils and solid media[J]. Environmental Science & Technology, 1999, 33(4): 642-649. |
| [21] | JUHASZ A L, WEBER J, SMITH E, et al. Evaluation of SBRC-gastric and SBRC-intestinal methods for the prediction of in vivo relative lead bioavailability in contaminated soils[J]. Environmental Science & Technology, 2009, 43(12): 4503-4509. |
| [22] | WRAGG J, CAVE M, BASTA N, et al. An inter-laboratory trial of the unified BARGE bioaccessibility method for arsenic, cadmium and lead in soil[J]. Science of the Total Environment, 2011, 409(19): 4016-4030. |
| [23] | MAYER L M, CHEN Z, FINDLAY R H, et al. Bioavailability of sedimentary contaminants subject to deposit-feeder digestion[J]. Environmental Science & Technology, 1996, 30(8): 2641-2645. |
| [24] | National Research Council. Bioavailability of Contaminants in Soils and Sediments: Processes, Tools and Applications[M]. Washington: The National Academies Press, 2003. |
| [25] | NG J C, JUHASZ A, SMITH E, et al. Assessing the bioavailability and bioaccessibility of metals and metalloids[J]. Environmental Science and Pollution Research, 2015, 22(12): 8802-8825. doi: 10.1007/s11356-013-1820-9 |
| [26] | LI J, LI K, CAVE M, et al. Lead bioaccessibility in 12 contaminated soils from China: Correlation to lead relative bioavailability and lead in different fractions[J]. Journal of Hazardous Materials, 2015, 295: 55-62. doi: 10.1016/j.jhazmat.2015.03.061 |
| [27] | JUHASZ A L, SMITH E, WEBER J, et al. Comparison of in vivo and in vitro methodologies for the assessment of arsenic bioavailability in contaminated soils[J]. Chemosphere, 2007, 69(6): 961-966. doi: 10.1016/j.chemosphere.2007.05.018 |
| [28] | SCHRODER J L, BASTA N T, SI J T, et al. In vitro gastrointestinal method to estimate relative bioavailable cadmium in contaminated soil[J]. Environmental Science & Technology, 2003, 37(7): 1365-1370. |
| [29] | RUBY M V, SCHOOF R, BRATTIN W, et al. Advances in evaluating the oral bioavailability of inorganics in soil for use in human health risk assessment[J]. Environmental Science & Technology, 1999, 33(21): 3697-3705. |
| [30] | GRISCOM S B, FISHER N S, LUOMA S N. Kinetic modeling of Ag, Cd and Co bioaccumulation in the clam Macoma balthica: Quantifying dietary and dissolved sources[J]. Marine Ecology Progress Series, 2002, 240: 127-141. doi: 10.3354/meps240127 |
| [31] | LUOMA S N, JOHNS C, FISHER N S, et al. Determination of selenium bioavailability to a benthic particulate and solute pathways[J]. Environmental Science & Technology, 1992, 26(3): 485-491. |
| [32] | GAGNON C, FISHER N S. The bioavailability of sediment-bound Cd, Co, and Ag to the mussel Mytilus edulis[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1997, 54(1): 147-156. doi: 10.1139/f96-256 |
| [33] | WANG W X, FISHER N S. Modeling the influence of body size on trace element accumulation in the mussel Mytilus edulis[J]. Marine Ecology Progress Series, 1997, 161: 103-115. doi: 10.3354/meps161103 |
| [34] | GRISCOM S B, FISHER N S, LUOMA S N. Geochemical influences on assimilation of sediment-bound metals in clams and mussels[J]. Environmental Science & Technology, 2000, 34(1): 91-99. |
| [35] | FAN W, WANG W X. Sediment geochemical controls on Cd, Cr, and Zn assmilation by the clam Ruditapes philippinarum[J]. Environmental Toxicology Chemistry, 2001, 20(10): 2309-2317. doi: 10.1002/etc.v20:10 |
| [36] | RUBY M V, DAVIS A, SCHOOF R, et al. Estimation of lead and arsenic bioavailability using a physiologically based extraction test[J]. Environmental Science & Technology, 1996, 30(2): 422-430. |
| [37] | RAURET G, LOPEZ-SANCHEZ J F, SAHUQUILLO A, et al. Application of a modified BCR sequential extraction (three-step) procedure for the determination of extractable trace metal contents in a sewage sludge amended soil reference material (CRM 483), complemented by a threeyear stability study of acetic acid and EDTA extractable metal content[J]. Journal of Environmental Monitoring, 2000, 2(3): 228-233. doi: 10.1039/b001496f |
| [38] | 杨洁, 瞿攀, 王金生, 等. 土壤中重金属的生物有效性分析方法及其影响因素综述[J]. 环境污染与防治, 2017, 39(2): 217-223. |
| [39] | BRADHAM K D, SCHECKEL K G, NELSON C M, et al. Relative bioavailability and bioaccessibility and speciation of arsenic in contaminated soils[J]. Environmental Health Perspectives, 2011, 119(11): 1629-1634. doi: 10.1289/ehp.1003352 |
| [40] | REES M, SANSOM L, ROFE A, et al. Principles and application of an in vivo swine assay for the determination of arsenic bioavailability in contaminated matrices[J]. Environmental Geochemistry and Health, 2009, 31: 167-177. doi: 10.1007/s10653-008-9237-y |
| [41] | PATTERSON J K, LEI X G, MILLER D D. The pig as an experimental model for elucidating the mechanisms governing dietary influence on mineral absorption[J]. Experimental Biology and Medicine, 2008, 233(6): 651-664. doi: 10.3181/0709-MR-262 |
| [42] | MOCHIZUKI S, MAKITA T. Differences in intestinal length between specific-pathogen-free (SPF) and conventional swine[J]. Journal of Veterinary Medical Science, 1998, 60(5): 545-548. doi: 10.1292/jvms.60.545 |
| [43] | MARSCHNER B, WELGE P, HACK A, et al. Comparison of soil Pb in vitro bioaccessibility and in vivo bioavailability with Pb pools from a sequential soil extraction[J]. Environmental Science & Technology, 2006, 40(8): 2812-2818. |
| [44] | GAGNON C, FISHER N S. Bioavailability of sediment-bound methyl and inorganic mercury to a marine bivalve[J]. Environmental Science & Technology, 1997, 31(4): 993-998. |
| [45] | AMIRBAHMAN A, MASSEY D I, LOTUFO G, et al. Assessment of mercury bioavailability to benthic macroinvertebrates using diffusive gradients in thin films (DGT)[J]. Environmental Science-Processes & Impacts, 2013, 15(11): 2104-2114. |
| [46] | LEE B G, GRISCOM S B, LEE J S, et al. Influences of dietary uptake and reactive sulfides on metal bioavailability from aquatic sediments[J]. Science, 2000, 287(5451): 282-284. doi: 10.1126/science.287.5451.282 |
| [47] | KELLEY M E, BRAUNING S E, SCHOOF R A, et al. Assessing Oral Bioavailability of Metals in Soil[M]. Columbus, OH: Battelle Press, 2002. |
| [48] | DEVESA-REY R, PARADELO R, DIAZ-FIERROS F, et al. Fractionation and bioavailability of arsenic in the bed sediments of the Anllóns River (NW Spain)[J]. Water, Air and Soil Pollution, 2008, 195(1/2/3/4): 189-199. |
| [49] | UNDA-CALVO J, MARTINEZ-SANTOS M, RUIZ-ROMERA E. Chemical and physiological metal bioaccessibility assessment in surface bottom sediments from the Deba River urban catchment: Harmonization of PBET, TCLP and BCR sequential extraction methods[J]. Ecotoxicology and Environmental Safety, 2017, 138: 260-270. doi: 10.1016/j.ecoenv.2016.12.029 |
| [50] | LI S W, LI J, LI H B, et al. Arsenic bioaccessibility in contaminated soils: Coupling in vitro assays with sequential and HNO3 extraction[J]. Journal of Hazardous Materials, 2015, 295: 145-152. doi: 10.1016/j.jhazmat.2015.04.011 |
| [51] | ROUSSEL H, WATERLOT C, PELFRENE A, et al. Cd, Pb and Zn oral bioaccessibility of urban soils contaminated in the past by atmospheric emissions from two lead and zinc smelters[J]. Archives of Environmental Contamination and Toxicology, 2010, 58(4): 945-954. doi: 10.1007/s00244-009-9425-5 |
| [52] | SCHRODER J L, BASTA N T, CASTEEL S W, et al. Validation of the in vitro gastrointestinal (IVG) method to estimate relative bioavailable lead in contaminated soils[J]. Journal of Environmental Quality, 2004, 33(2): 513-521. doi: 10.2134/jeq2004.5130 |
| [53] | WESTON D P, MARUYA K A. Predicting bioavailability and bioaccumulation with in vitro digestive fluid extraction[J]. Environmental Toxicology and Chemistry, 2002, 21(5): 962-971. doi: 10.1002/etc.v21:5 |
| [54] | BAUMANN Z, KOLLER A, FISHER N S. Factors influencing the assimilation of arsenic in a deposit-feeding polychaete[J]. Comparative Biochemistry and Physiology C: Toxicology & Pharmacology, 2012, 156(1): 42-50. |
| [55] | VAHTER M, NORIN H. Metabolism of 74As-labeled trivalent and pentavalent inorganic arsenic in mice[J]. Environmental Research, 1980, 21(2): 446-457. doi: 10.1016/0013-9351(80)90049-3 |
| [56] | ODANAKA Y, MATANO O, GOTO S. Biomethylation of inorganic arsenic by the rat and some laboratory animals[J]. Bulletin of Environmental Contamination and Toxicology, 1980, 24(3): 452-459. |
| [57] | KENYON E M, HUGHES M F, LEVANDER O A. Influence of dietary selenium on the disposition of arsenate in the female B6C3F1 mouse[J]. Journal of Toxicology and Environmental Health, 1997, 51(3): 279-299. |
| [58] | XIA Q, PENG C, LAMB D, et al. Bioaccessibility of arsenic and cadmium assessed for in vitro bioaccessibility in spiked soils and their interaction during the unified BARGE method (UBM) extraction[J]. Chemosphere, 2016, 147: 444-450. doi: 10.1016/j.chemosphere.2015.12.091 |
| [59] | TANG X Y, ZHU Y G, CUI Y S, et al. The effect of ageing on the bioaccessibility and fractionation of cadmium in some typical soils of China[J]. Environment International, 2006, 32(5): 682-689. doi: 10.1016/j.envint.2006.03.003 |
| [60] | DI TORO D M, MCGRATH J A, HANSEN D J, et al. Predicting sediment metal toxicity using a sediment biotic ligand model: Methodology and initial application[J]. Environmental Toxicology and Chemistry, 2005, 24(10): 2410-2427. doi: 10.1897/04-413R.1 |
| [61] | DE JONGE M, EYCKMANS M, BLUST R, et al. Are accumulated sulfide-bound metals metabolically available in the benthic oligochaete Tubifex tubifex?[J]. Environmental Science & Technology, 2011, 45(7): 3131-3137. |
| [62] | CAMPANA O, SIMPSON S L, SPADARO D A, et al. Sub-lethal effects of copper to benthic invertebrates explained by sediment properties and dietary exposure[J]. Environmental Science & Technology, 2012, 46(12): 6835-6842. |
| [63] | HERNANDEZ-CRESPO C, MARTIN M, FERRIS M, et al. Measurement of acid volatile sulphide and simultaneously extracted metals in sediment from Lake Albufera (Valencia, Spain)[J]. Soil & Sediment Contamination, 2012, 21(2): 176-191. |
| [64] | CHEN F R, YANG Y Q, ZHANG D R, et al. Metals associated with reduced sulfur in sediments from different deposition environments in the Pearl River estuary, China[J]. Environmental Geochemistry and Health, 2006, 28(3): 265-272. doi: 10.1007/s10653-006-9042-4 |
| [65] | FANG T, LI X D, ZHANG G. Acid volatile sulfide and simultaneously extracted metals in the sediment cores of the Pearl River Estuary, South China[J]. Ecotoxicology and Environmental Safety, 2005, 61(3): 420-431. doi: 10.1016/j.ecoenv.2004.10.004 |
| [66] | LOURINO-CABANA B, LESVEN L, CHARRIAU A, et al. Potential risks of metal toxicity in contaminated sediments of Deule river in Northern France[J]. Journal of Hazardous Materials, 2011, 186(2/3): 2129-2137. |
| [67] | ZHUANG W, GAO X L. Assessment of heavy metal impact on sediment quality of the Xiaoqinghe estuary in the coastal Laizhou Bay, Bohai Sea: Inconsistency between two commonly used criteria[J]. Marine Pollution Bulletin, 2014, 83(1): 352-357. doi: 10.1016/j.marpolbul.2014.03.039 |
| [68] | BESSER J M, BRUMBAUGH W G, KEMBLE N E, et al. Effects of sediment characteristics on the toxicity of chromium(III) and chromium(VI) to the amphipod, Hyalella azteca[J]. Environmental Science & Technology, 2004, 38(23): 6210-6216. |
| [69] | NIZOLI E C, LUIZ-SILVA W. Seasonal AVS-SEM relationship in sediments and potential bioavailability of metals in industrialized estuary, southeastern Brazil[J]. Environmental Geochemistry and Health, 2012, 34(2): 263-272. doi: 10.1007/s10653-011-9430-2 |
| [70] | SIMPSON S L, WARD D, STROM D, et al. Oxidation of acid-volatile sulfide in surface sediments increases the release and toxicity of copper to the benthic amphipod Melita plumulosa[J]. Chemosphere, 2012, 88(8): 953-961. doi: 10.1016/j.chemosphere.2012.03.026 |
| [71] | HONG S W, KIM H S, CHUNG T H. Alteration of sediment organic matter in sediment microbial fuel cells[J]. Environmental Pollution, 2010, 158(1): 185-191. doi: 10.1016/j.envpol.2009.07.022 |
| [72] | WOOD P J, ARMITAGE P D. Biological effects of fine sediment in the lotic environment[J]. Environmental Management, 1997, 21(2): 203-217. doi: 10.1007/s002679900019 |
| [73] | 易文利, 王圣瑞, 金相灿, 等. 长江中下游浅水湖沉积物中有机质及其组分的赋存特征[J]. 西北农林科技大学学报(自然科学版), 2008, 7(5): 141-148. doi: 10.3321/j.issn:1671-9387.2008.05.026 |
| [74] | BESSER J M, BRUMBAUGH W G, MAY T W, et al. Effects of organic amendments on the toxicity and bioavailability of cadmium and copper in spiked formulated sediments[J]. Environmental Toxicology and Chemistry, 2003, 22(4): 805-815. doi: 10.1002/etc.v22:4 |
| [75] | STROM D, SIMPSON S L, BATLEY G E, et al. The influence of sediment particle size and organic carbon on toxicity of copper to benthic invertebrates in oxic/suboxic surface sediments[J]. Environmental Toxicology and Chemistry, 2011, 30(7): 1599-1610. doi: 10.1002/etc.v30.7 |
| [76] | SADEGHI S H R, HARCHEGANI M K, YOUNESI H A. Suspended sediment concentration and particle size distribution, and their relationship with heavy metal content[J]. Journal of Earth System Science, 2012, 121(1): 63-71. doi: 10.1007/s12040-012-0143-4 |
| [77] | ZHAO H T, LI X Y, WANG X M, et al. Grain size distribution of road-deposited sediment and its contribution to heavy metal pollution in urban runoff in Beijing, China[J]. Journal of Hazardous Materials, 2010, 183(1/2/3): 203-210. |
| [78] | CAMPANA O, BLASCO J, SIMPSON S L. Demonstrating the appropriateness of developing sediment quality guidelines based on sediment geochemical properties[J]. Environmental Science & Technology, 2013, 47(13): 7483-7489. |
| [79] | JYVASJARVI J, BOROS G, JONES R I, et al. The importance of sedimenting organic matter, relative to oxygen and temperature, in structuring lake profundal macroinvertebrate assemblages[J]. Hydrobiologia, 2013, 709(1): 55-72. doi: 10.1007/s10750-012-1434-0 |
| [80] | DE JONGE M, TEUCHIES J, MEIRE P, et al. The impact of increased oxygen conditions on metal-contaminated sediments part II: Effects on metal accumulation and toxicity in aquatic invertebrates[J]. Water Research, 2012, 46(10): 3387-3397. doi: 10.1016/j.watres.2012.03.035 |
| [81] | KALANTZI I, BLACK K D, PERGANTIS S A, et al. Metals and other elements in tissues of wild fish from fish farms and comparison with farmed species in sites with oxic and anoxic sediments[J]. Food Chemistry, 2013, 141(2): 680-694. doi: 10.1016/j.foodchem.2013.04.049 |
| [82] | KELDERMAN P, OSMAN A A. Effect of redox potential on heavy metal binding forms in polluted canal sediments in Delft (The Netherlands)[J]. Water Research, 2007, 41(18): 4251-4261. doi: 10.1016/j.watres.2007.05.058 |
| [83] | PENG J F, SONG Y H, YUAN P, et al. The remediation of heavy metals contaminated sediment[J]. Journal of Hazardous Materials, 2009, 161(2/3): 633-640. |
| [84] | ZOUMIS T, SCHMIDT A, GRIGOROVA L, et al. Contaminants in sediments: Remobilisation and demobilisation[J]. Science of the Total Environment, 2001, 266(1/2/3): 195-202. |
| [85] | SPEELMANS M, LOCK K, VANTHUYNE D R J, et al. Hydrological regime and salinity alter the bioavailability of Cu and Zn in wetlands[J]. Environmental Pollution, 2010, 158(5): 1870-1875. doi: 10.1016/j.envpol.2009.10.040 |
| [86] | LEE J S, LEE B G, LUOMA S N, et al. Influence of acid volatile sulfides and metal concentrations on metal partitioning in contaminated sediments[J]. Environmental Science & Technology, 2000, 34: 4511-4516. |
| [87] | TAN Q G, KE C H, WANG W X. Rapid assessments of metal bioavailability in marine sediments using coelomic fluid of sipunculan worms[J]. Environmental Science & Technology, 2013, 47(13): 7499-7505. |
| [88] | PALLER M H, KNOX A S. Amendments for the in situ remediation of contaminated sediments: Evaluation of potential environmental impacts[J]. Science of the Total Environment, 2010, 408(20): 4894-4900. doi: 10.1016/j.scitotenv.2010.06.055 |
| [89] | LEE B G, LEE J S, LUOMA S N, et al. Influence of acid volatile sulfide and metal concentrations on metal bioavailability to marine invertebrates in contaminated sediments[J]. Environmental Science & Technology, 2000, 34(21): 4517-4523. |
| [90] | SIMPSON S L, KING C K. Exposure-pathway models explain causality in whole-sediment toxicity tests[J]. Environmental Science & Technology, 2005, 39(3): 837-843. |
| [91] | SIMPSON S L, YVERNEAU H, CREMAZY A, et al. DGT-Induced copper flux predicts bioaccumulation and toxicity to bivalves in sediments with varying properties[J]. Environmental Science & Technology, 2012, 46(16): 9038-9046. |
| [92] | SIMPSON S L, BATLEY G E. Predicting metal toxicity in sediments: A critique of current approaches[J]. Integrated Environmental Assessment and Management, 2007, 3(1): 18-31. doi: 10.1002/ieam.5630030103 |
| [93] | STOCKDALE A, DAVISON W, ZHANG H. Formation of iron sulfide at faecal pellets and other microniches within suboxic surface sediment[J]. Geochimica Et Cosmochimica Acta, 2010, 74(9): 2665-2676. doi: 10.1016/j.gca.2010.02.005 |
 下载:
下载:  点击查看大图
点击查看大图