全文HTML
--> --> -->过渡金属二元化合物(MX2)在光电器件、电化学、生物传感器等方面有着明显的优势. 其中MoS2作为典型的材料, 随层数的不同, 带隙可在1.29—1.9 eV之间调节[9], 其在柔性、吸光性等方面优于其他半导体材料, 广泛应用于多个领域. 本研究组就此开展了一系列的实验研究, Li等[10,11]制备了大面积单层MoS2、不同形貌的MoS2微纳结构及其复合材料, 着重研究了其光学性质随结构与温度的变化、高压和变温拉曼光谱及复合材料的光限幅性质, 为MoS2在光电领域的实际应用提供了研究基础; Zhai等[12-13]制备了不同形貌的MoS2及其纳米复合材料, 并对MoS2材料的光学性质随层数和温度的变化规律、Au/MoS2复合结构的SERS特性、Au/MoS2复合材料的电化学生物传感特性及光化学传感特性等进行了研究; Shan等[14-15]制备了高质量的少层MoS2纳米材料及MoS2/WS2异质结, 对其形貌、结构及光电特性进行研究, 并成功制备基于不同层数的MoS2薄膜及其异质结的背栅场效应晶体管(FET), 首次利用此FET对极低浓度葡萄糖溶液实现了超灵敏检测, 以上研究为纳米材料在光电器件及生物传感器领域的应用提供了理论和实验基础. 本研究组多年研究发现, MoS2具有优异的吸附能力及荧光淬灭作用[16], 因而可应用于SERS研究, 但由于MoS2材料SERS基底以化学增强作用为主, 所以增强效果仅在两个数量级左右, 严重制约了单一MoS2基底的实际应用. 具有粗糙表面的金属纳米材料具备良好的SERS性能[17,18], 但单一金属SERS基底吸附能力较弱且易团聚氧化, 从而影响其增强效果. 将MoS2与金属复合材料作为SERS基底, 可弥补二者不足, 从电磁增强、化学增强两方面提升SERS性能. 目前对于SERS相关综述研究虽然很多, 但对MoS2及其金属复合SERS基底的发展及应用的研究概述鲜见报道.
本文将通过介绍金属、MoS2、MoS2/金属复合SERS基底, 对此类材料发展现状及应用研究加以阐述.
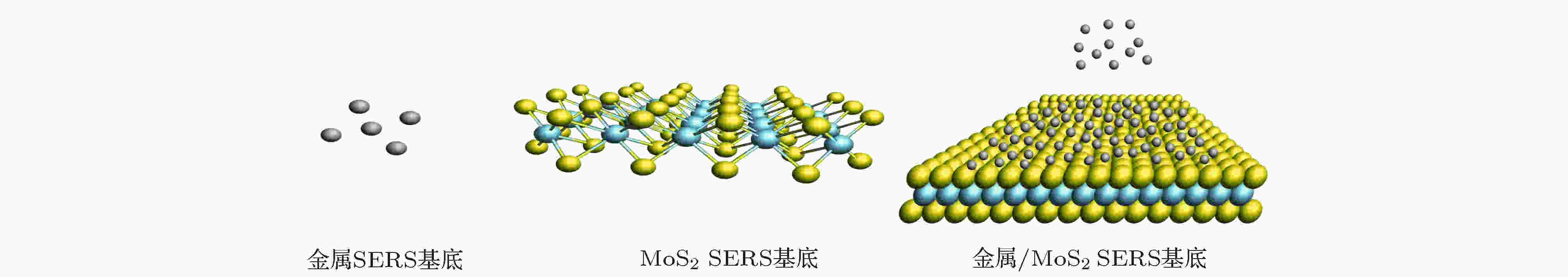 图 1 金属、MoS2、金属/MoS2 SERS基底
图 1 金属、MoS2、金属/MoS2 SERS基底Figure1. Metal, MoS2, metal/MoS2 SERS substrate.
2
2.1.单一金属SERS基底
32.1.1.机 理
V.Raman[19]首次发现了拉曼散射(Raman scattering)现象, 由于可快速分析不同材料的结构及特性, 逐渐成为了重要的分析手段之一, 但检测分子产生的拉曼信号较弱, 难以进行有效的拉曼检测. Fleischmann在粗糙Ag电极表面得到了高信噪比的拉曼信号, Jeanmaire和Van Duyne[20]及Albrecht和Creighton[21]重复以上实验观察到拉曼信号的明显增强, 称这一现象为SERS, 并首次提出电磁增强机理. 电磁增强机理被认为是产生SERS现象的主要因素, 如图2所示, 金属纳米粒子被入射光激发后, 导致其自由电子集体振荡, 当入射光频率与振荡频率相匹配时, 将产生局域表面等离子体共振, 此时, 纳米粒子附近区域的电磁场将大幅度增强, 当检测分子处于此区域时, 拉曼信号将获得增强效果[22].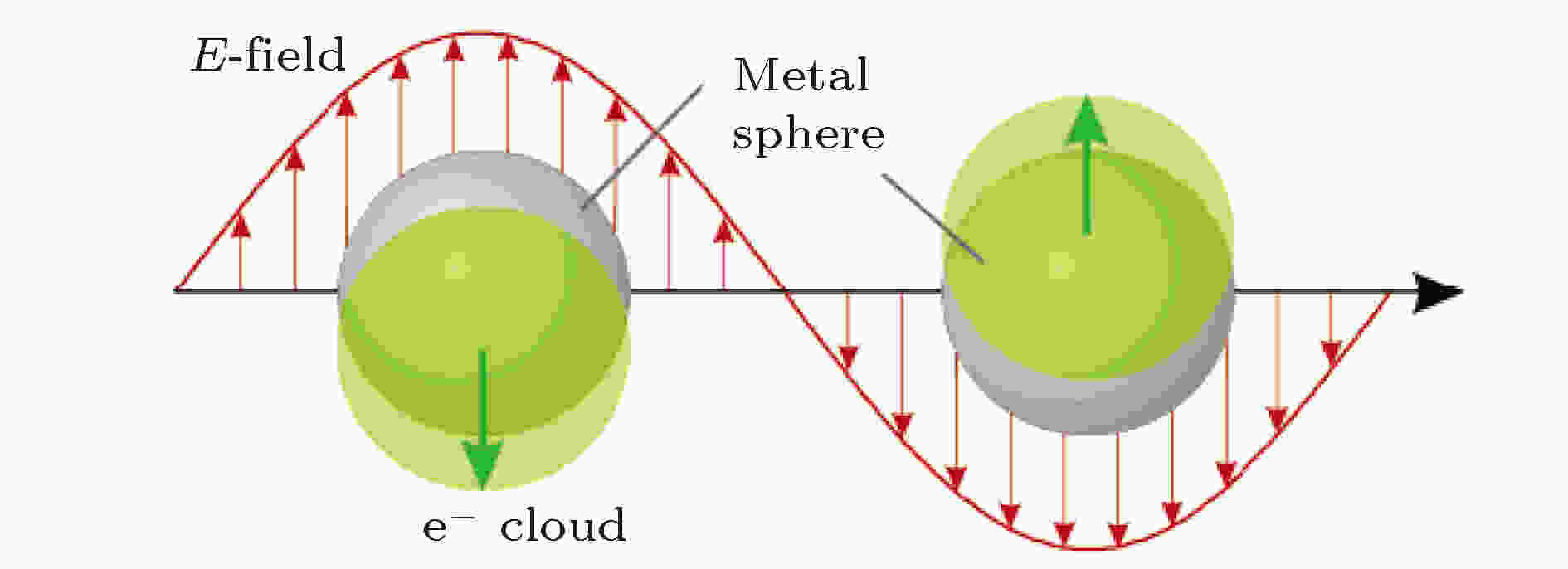 图 2 金属纳米球的局域表面等粒子共振示意图[22]
图 2 金属纳米球的局域表面等粒子共振示意图[22]Figure2. Schematic diagram of local surface isopoly resonance of metal nanospheres[22]
与单个具有SERS性能的金属纳米粒子相比, 由多个金属纳米粒子组成的阵列可产生表面等离子体耦合效应[23], 阵列中纳米粒子的形貌、尺寸及阵列间距、排列方式等将对其产生影响. Kan[24]认为与单个Au纳米棒相比, Au纳米棒阵列将引起纳米棒表面电荷的重新分布, 并在其间距处产生近场耦合效应大幅度提升增强效果. Brawley等[25]通过实验及模拟探究了不同参数Au纳米线阵列对SERS性能的影响, 认为增强效果与衬底表面SiO2厚度、纳米线宽度及线间距有关, 当SiO2厚度为60, 330, 590 nm, 纳米线宽度为50 nm, 线间距为10 nm时, SERS性能最为优越.
3
2.1.2.研究现状
最初研究认为贵金属纳米材料(Au, Ag, Cu)具有良好的拉曼增强效果. Kneipp等[26]在Ag胶上采集了罗丹明6G(R6G)的SERS光谱, 并认为SERS可获得比荧光光谱更低的检测极限; Zhang[27]通过刻蚀法制备Au纳米盘阵列, 可检测低至10–8 mol·L–1的R6G溶液; Chirumamilla等[28]利用电子束光刻技术(electron beam lithography, EBL)制备不同参数的Au矩形阵列, 其中Au纳米矩形尺寸为40—65 nm、间隔为20 nm时, 可获得最大化的信号增强效果; Wu等[29]以Au纳米圆盘及纳米圆环阵列作为SERS基底对4-MBA进行SERS检测及模拟 (图3), 认为Au纳米圆盘阵列中较小的直径以及较小的间距有利于SERS增强, 而Au纳米圆环阵列中较大的直径及较小的间距有利于SERS增强. 随着研究深入, 基底材料逐渐扩展至过渡金属, Tian等[30]发现除贵金属外, 粗糙的过渡金属电极如Pt, Ru, Ni等同样具有良好的增强效果, 扩展了SERS基底材料.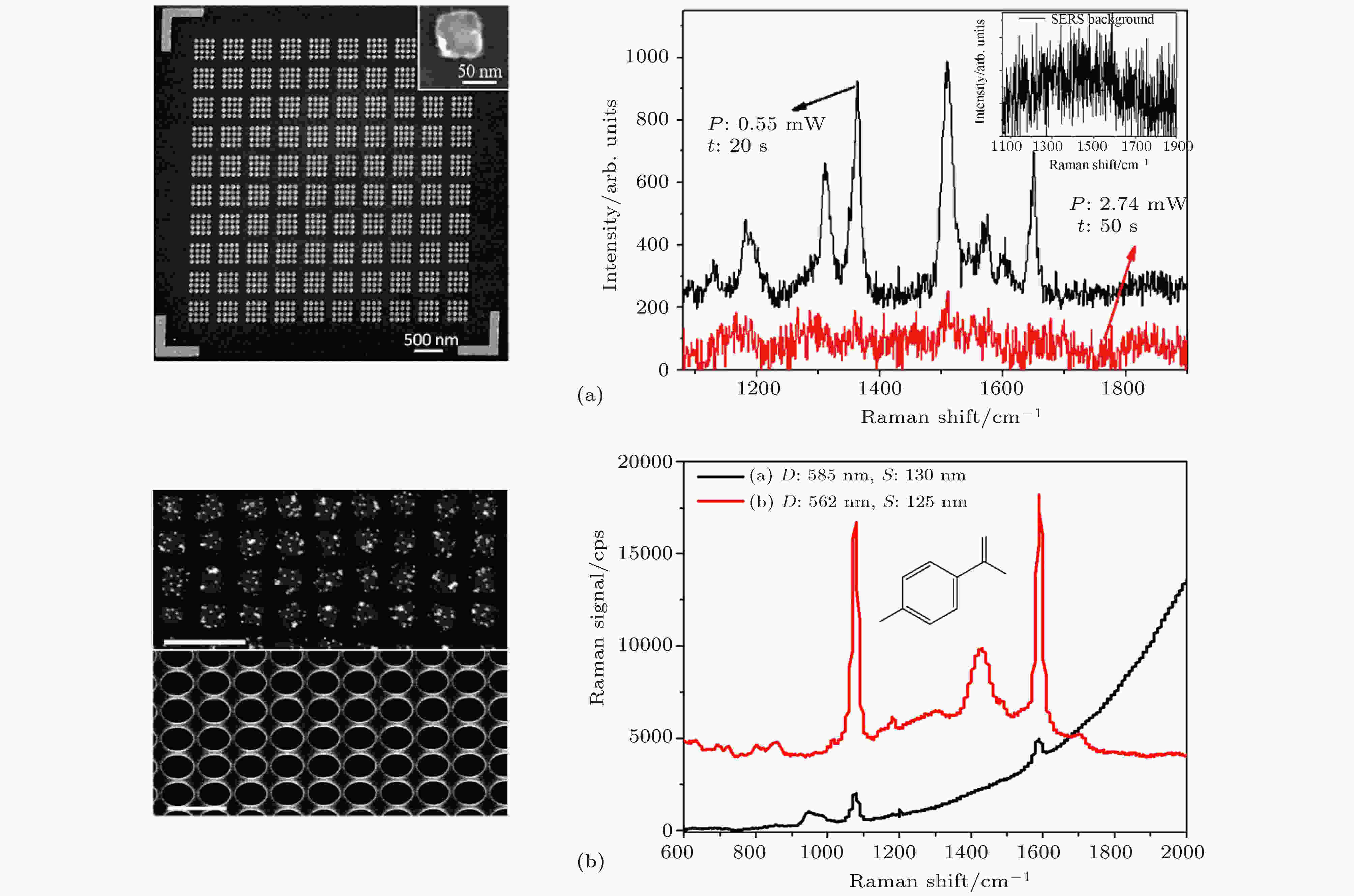 图 3 (a) Au矩形阵列SERS基底对R6G的SERS检测[27]; (b) Au纳米粒子、纳米圆环阵列基底对4-MBA的SERS检测[29]
图 3 (a) Au矩形阵列SERS基底对R6G的SERS检测[27]; (b) Au纳米粒子、纳米圆环阵列基底对4-MBA的SERS检测[29]Figure3. (a) SERS detection of R6G by Au rectangular array SERS substrate[27]; (b) SERS detection of 4-MBA by Au nanoparticles and nanoring array substrates[29]
3
2.1.3.存在的问题
单一金属SERS基底受入射光的作用产生增强效果, 避免了直接与检测分子相互作用, 但检测分子所产生的背景荧光使得拉曼散射信号受到干扰, 同时可能损耗基底造成稳定性下降; 并且单一的金属SERS基底吸附能力较弱, 导致其灵敏度较低, 无法在低浓度环境下获得检测分子的拉曼信号, 使其应用研究陷入了困境.2
2.2.MoS2材料SERS基底
32.2.1.机 理
研究表明, 在诸多实验中仍存在无法通过单一电磁增强机理解释的拉曼增强现象. Moskovits等[31]在采集CO和N2的SERS光谱时发现, CO和N2拉曼峰强相差近200倍, 这一现象表明除电磁增强外, 还存在其他增强机制, 于是提出了化学增强. 化学增强是指检测分子与基底相互作用产生电荷共振跃迁, 从而引起拉曼信号增强[32], 其增强强度由检测分子本身的化学性质决定, 是一种短程效应, 随着检测分子与金属表面距离的增加, 近场增强几乎呈指数衰减. Schlucker[33]认为, 与电磁增强不同的是, 化学增强主要考虑检测分子与基底之间的相互作用, 由于基底的复杂性及检测分子种类的不同, 化学增强远比电磁增强复杂.3
2.2.2.研究现状
随着化学增强机理的发展, SERS基底材料不再局限于金属. 由于MoS2在SERS研究中展现了诸多优点, 使其成为SERS基底材料之一. Zang等[34]合成了单层MoS2作为SERS基底 (图4), 通过检测R6G发现拉曼信号增强了两到三个数量级, 并认为其中化学增强对增强效果起到主要贡献; Muehlethaler等[35]报道了单层MoS2对近场中的4-巯基吡啶的SERS检测, 他认为实验中的增强现象归因于MoS2与有机分子形成的电荷转移, 并且该方式无需将基底图案化. Xia[36]研究了0°堆叠和60°堆叠的双层MoS2的SERS性能, 并认为0°堆叠的双层MoS2比60°堆叠的双层MoS2具有更强的层间电子耦合, 因此其拉曼增强效果更为明显.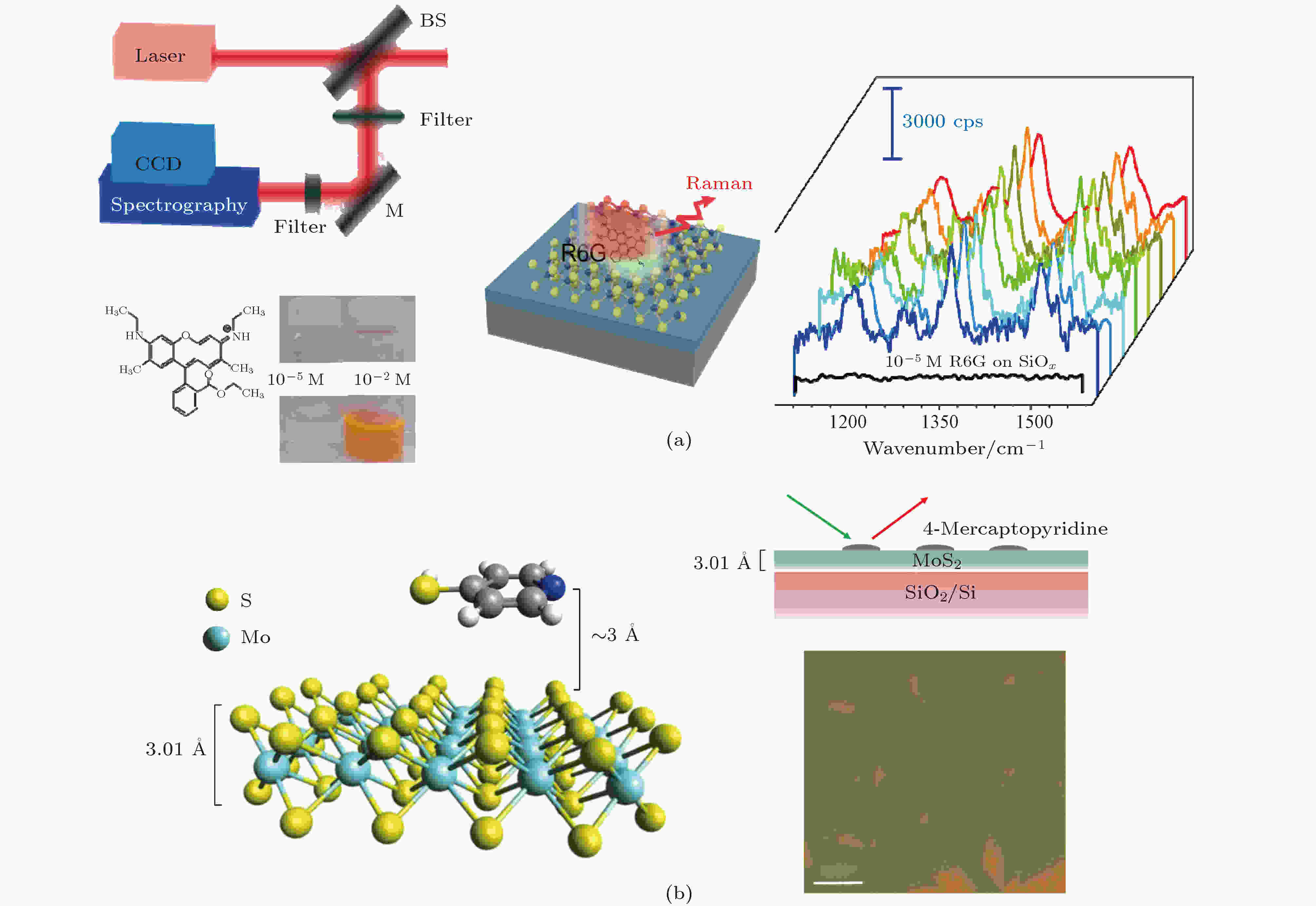 图 4 (a)单层MoS2基底检测R6G流程图及SERS光谱[34]; (b)单层MoS2基底对4-巯基吡啶的SERS检测[35]
图 4 (a)单层MoS2基底检测R6G流程图及SERS光谱[34]; (b)单层MoS2基底对4-巯基吡啶的SERS检测[35]Figure4. (a) Flow chart and SERS spectra of single-layer MoS2 substrate for detecting R6G[34]; (b) SERS detection of 4-mercaptopyridine by single-layer MoS2 substrate[35]
3
2.2.3.存在的问题
相比于单一金属SERS基底, MoS2具有离域

2
2.3.金属/MoS2复合SERS基底
32.3.1.机 理
关于金属/MoS2复合SERS基底的增强机理, 普遍认为电磁增强对增强效果起到主要作用, 化学增强起到次要作用.Liang等[37]利用Ag/MoS2纳米花复合结构进行SERS研究并对其增强机理进行了详细阐述, 他认为Ag的等离子体效应在其表面产生了一个局部增强电磁场(图5灰色区域), 但Ag与MoS2的费米能级不同, 因此在其接触界面形成肖特基势垒, 阻碍电子从金属转移到半导体. 当Ag在激光照射下诱导强等离子体激发, 使电子能够从Ag转移到MoS2的导带(CB), 产生大量的电子空穴对, 之后被激发的电子丧失相干性, 遵循非平衡的费米-狄拉克型分布, 克服金属和半导体之间形成的肖特基势垒后, 成功的转移到价带(VB), 整个过程中强烈的等离子体激发和电子转移过程放大了电磁增强和化学增强.
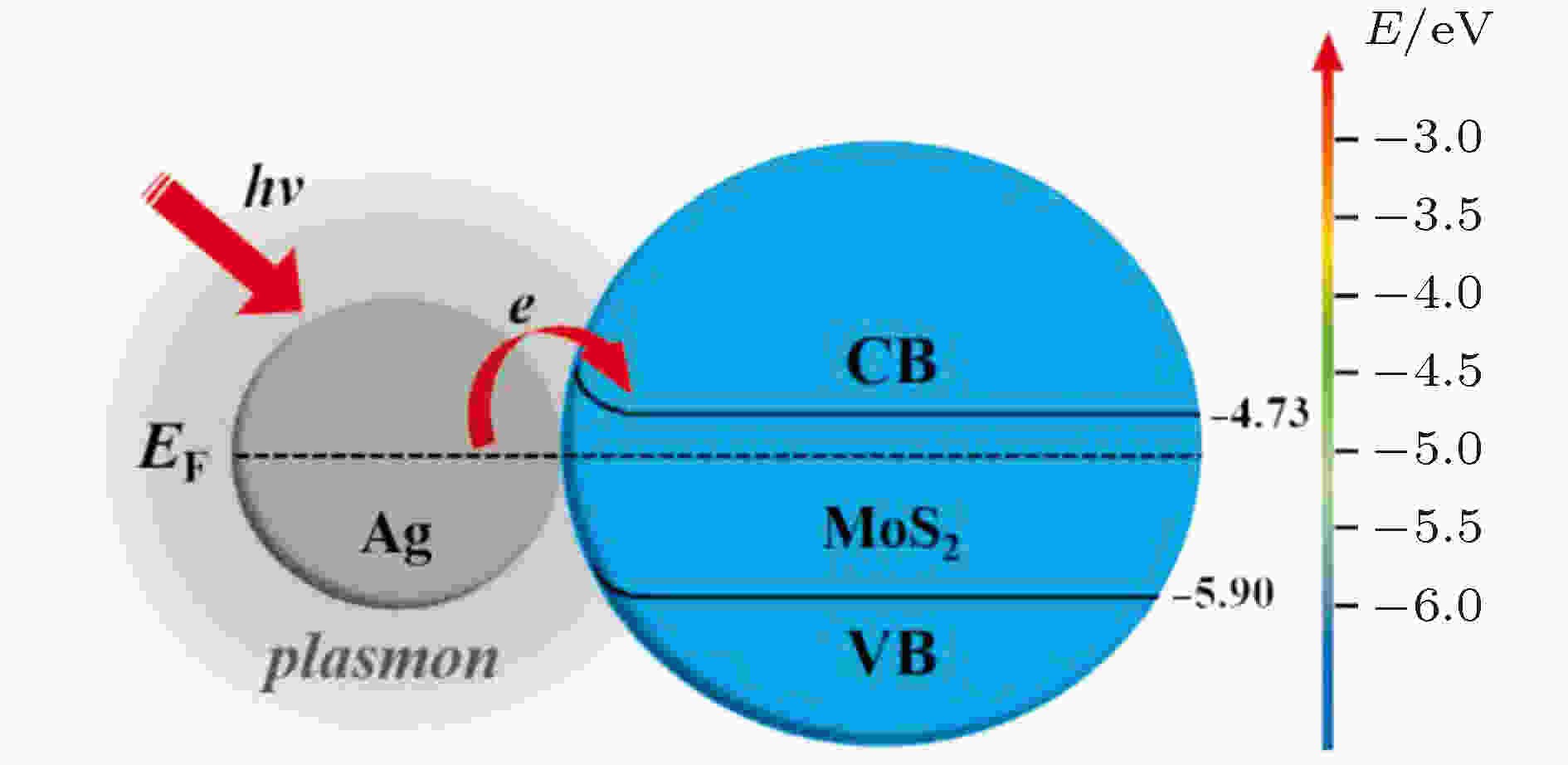 图 5 Ag/MoS2纳米花复合SERS基底机理分析示意图[37]
图 5 Ag/MoS2纳米花复合SERS基底机理分析示意图[37]Figure5. Analysis schematic diagram of Ag/MoS2 nanoflower SERS substrate mechanism[37]
而Shakya等[38]则认为, 由于MoS2的导带能量高于Au纳米粒子的费米能级, 当MoS2被Au纳米粒子的修饰后, Au纳米粒子充当MoS2导带中的电子捕获中心, 电子从MoS2转移到Au, 在MoS2表面产生电位变化, 使得MoS2形成P型掺杂 (图6)[39], 导致MoS2的费米能级逐渐向价带移动, 此过程与Au纳米粒子的电磁增强共同作用使拉曼信号增强.
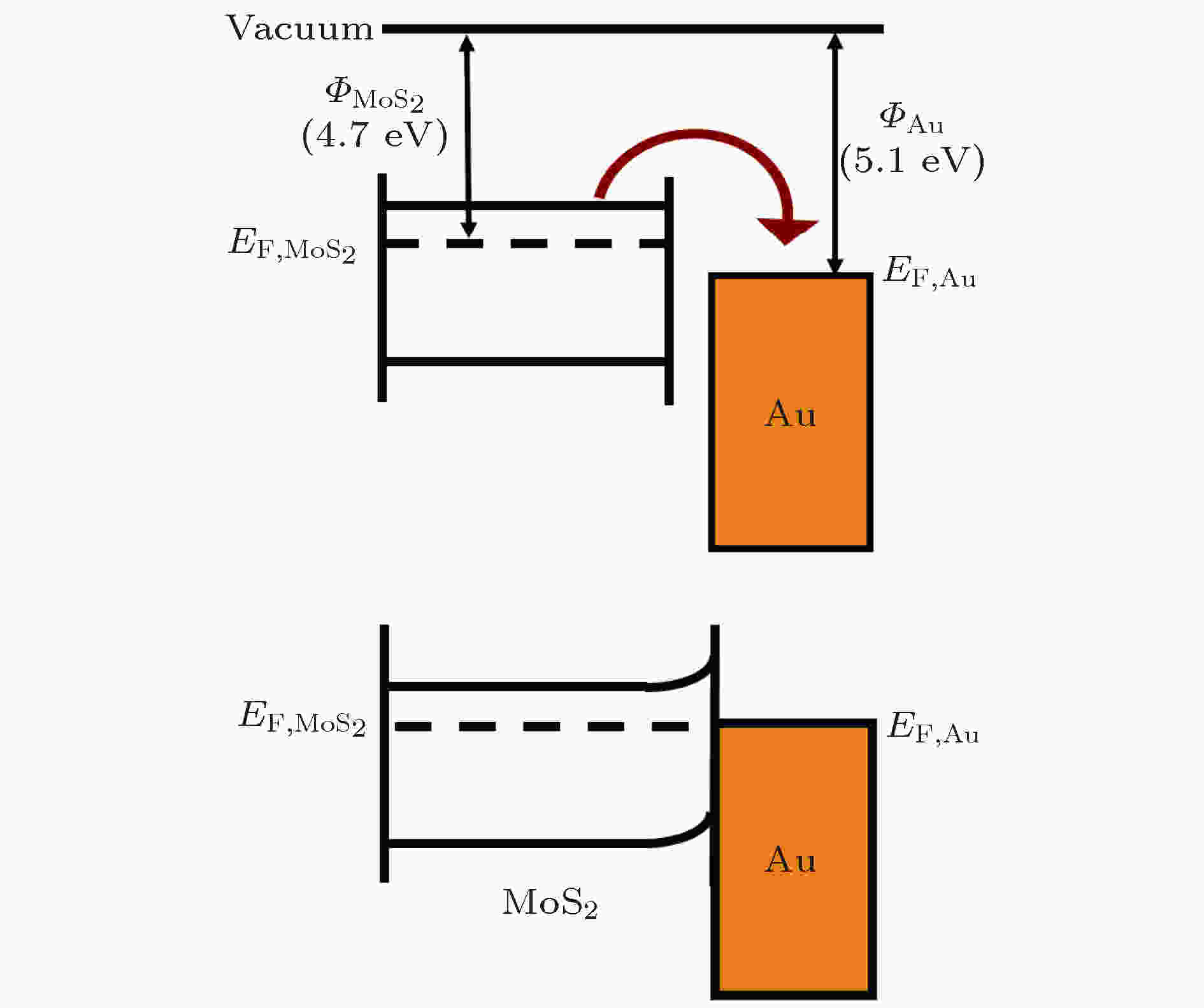 图 6 Au/MoS2复合SERS基底的费米能级移动示意图[39]
图 6 Au/MoS2复合SERS基底的费米能级移动示意图[39]Figure6. Schematic diagram of Fermi level moving of Au/MoS2 composite SERS substrate[39]
金属/MoS2复合SERS基底可有效地将电磁增强机理及化学增强机理相结合, 目前仅探究了二者复合后电荷转移对SERS性能的影响, 而对于MoS2材料自身的

3
2.3.2.研究现状
目前金属/MoS2纳米复合材料作为新型SERS基底已成为研究热点之一. 本研究组中, Zhai等利用EBL技术在单层MoS2薄膜上制备了半径为50 nm、间距为70 nm的Au纳米圆盘阵列, 通过对R6G的SERS检测表明Au/MoS2复合基底增强效果明显优于单一MoS2基底. Lu等[40]制备了超薄MoS2薄膜与Au纳米粒子的复合基底, 实现了不同芳香结构分子的SERS检测; Hwang和Suh[41]制备了卷轴状的金属/MoS2复合基底, 并认为卷轴状复合基底增强效果强于片状复合基底, 其中卷轴状的Ag/MoS2复合基底增强效果最为优越 (图7); Jiang等[42]利用二次退火的方法制备了金字塔形Ag/MoS2复合基底, 成功对10–6—10–11 mol·L–1的R6G溶液进行SERS检测, 增强因子高达1.26 × 1012, 并且此基底在30 d内仍保持良好的SERS性能. Li等[43]在Cu纳米粒子表面包裹MoS2, 实验表明复合基底比单一Cu基底具备更高的灵敏度, 对R6G分子的检测浓度可低至10–9 mol·L–1, 并认为MoS2可有效保护Cu纳米粒子免受氧化, 从而提高其稳定性.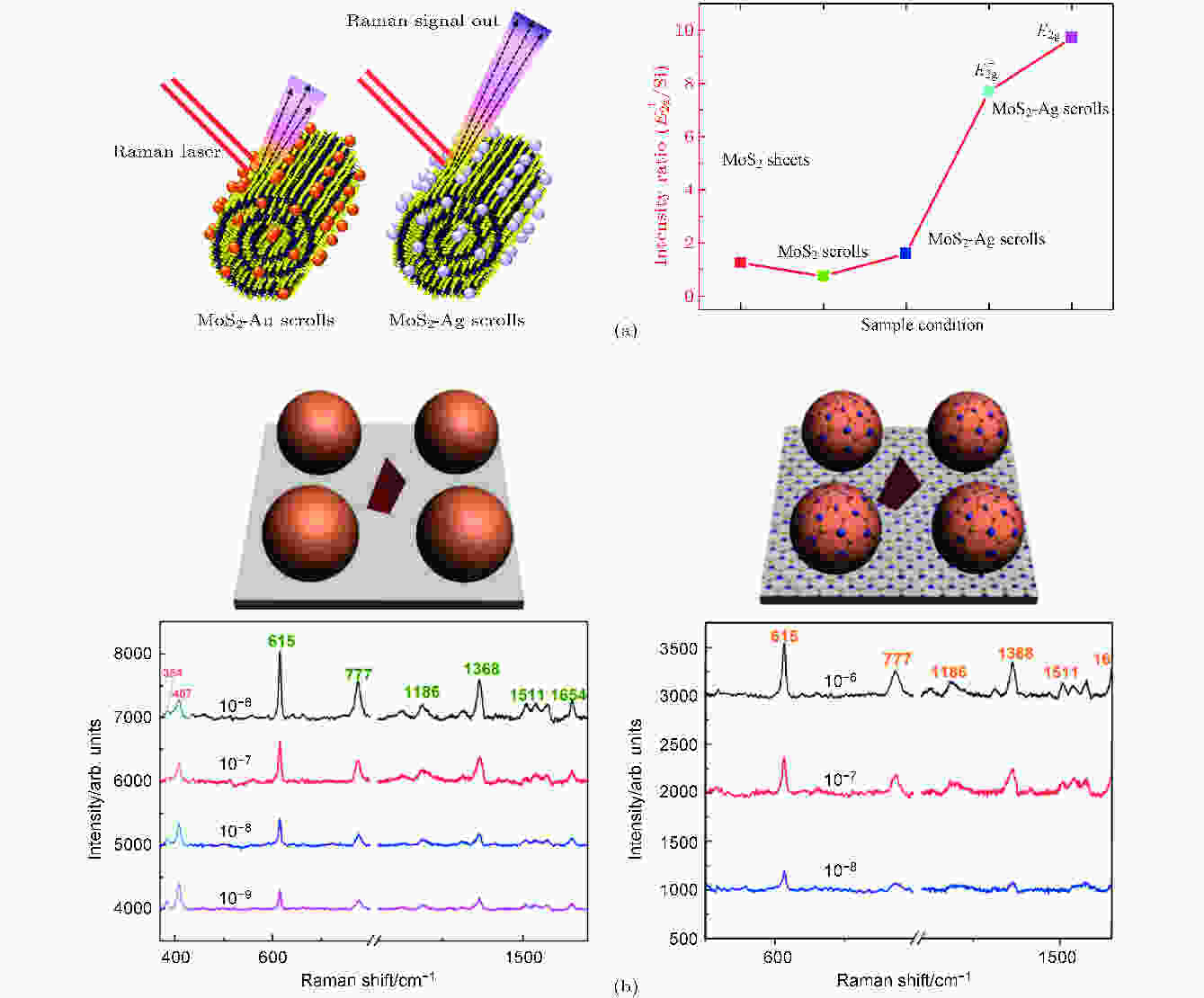 图 7 (a)卷轴形貌的Au/MoS2、Ag/MoS2复合基底增强拉曼强度比[41]; (b) Cu/MoS2复合基底、Cu基底对R6G的SERS检测[43]
图 7 (a)卷轴形貌的Au/MoS2、Ag/MoS2复合基底增强拉曼强度比[41]; (b) Cu/MoS2复合基底、Cu基底对R6G的SERS检测[43]Figure7. (a) Reinforced Raman intensity ratio of Au/MoS2, Ag/MoS2 composite substrate with reel profile[41]; (b) SERS detection of R6G by Cu/MoS2 composite substrate and Cu substrate[43]
3
2.3.3.存在的问题
金属/MoS2复合SERS基底结合了金属基底及MoS2基底的优点, 具有良好的吸附性能及优异的增强效果, 对检测分子的检测浓度可扩展至10–9—10–14 mol·L–1甚至更低, 并且其稳定性得到进一步提升, 可在较长时间内仍保持良好的拉曼增强效果. 但目前MoS2对金属的电磁增强影响以及MoS2与金属的相互作用机理尚不完善, 制备工艺及大范围应用也是未来研究中面临的重要问题.2
3.1.MoS2材料SERS基底的制备
关于MoS2材料SERS基底的制备技术层出不穷, 目前水热/溶剂热法、微机械力剥离法、化学气相沉积法较为成熟常见.3
3.1.1.水热/溶剂热法
水热/溶剂热法是在密闭反应容器中加入钼源及硫源, 以水溶液或有机溶剂作为反应体系, 在高温高压的环境中进行反应. 反应过程中可改变反应时间、反应温度等条件控制其生长, 得到不同形貌的MoS2基底. Shib[44]以水热法制备了MoS2纳米花基底并对Rh6G进行了SERS检测; Fei等[45]采用水热法制备MoS2量子点, 以其为SERS基底成功对CV进行检测.3
3.1.2.微机械力剥离法
微机械力剥离法采用一种特殊的黏性胶带剥离高晶相体材料MoS2, 其原理是通过胶带的黏性附着力, 克服MoS2分子层间的弱范德瓦耳斯力, 从而达到剥离的目的, 随着工艺不断改进, 如今己可剥离至少层甚至单层的MoS2薄膜. Yan等[46]将微机械力剥离法制备的MoS2薄膜进行不同温度的热处理, 认为温度为425 ℃时, MoS2材料SERS基底具有最佳灵敏度, 对R6G分子的最低检测浓度可达10–8 mol·L–1.3
3.1.3.化学气相沉积法
化学气相沉积法通过前驱体在高温气态下发生化学反应, 从而将生成物沉积于衬底表面. Qiu等[47]利用化学气相沉积法在金字塔形Si衬底上生长MoS2薄膜, 并与生长在平面Si基底上的MoS2薄膜相比, 认为金字塔形MoS2薄膜具备更为优异的SERS性能 (图8).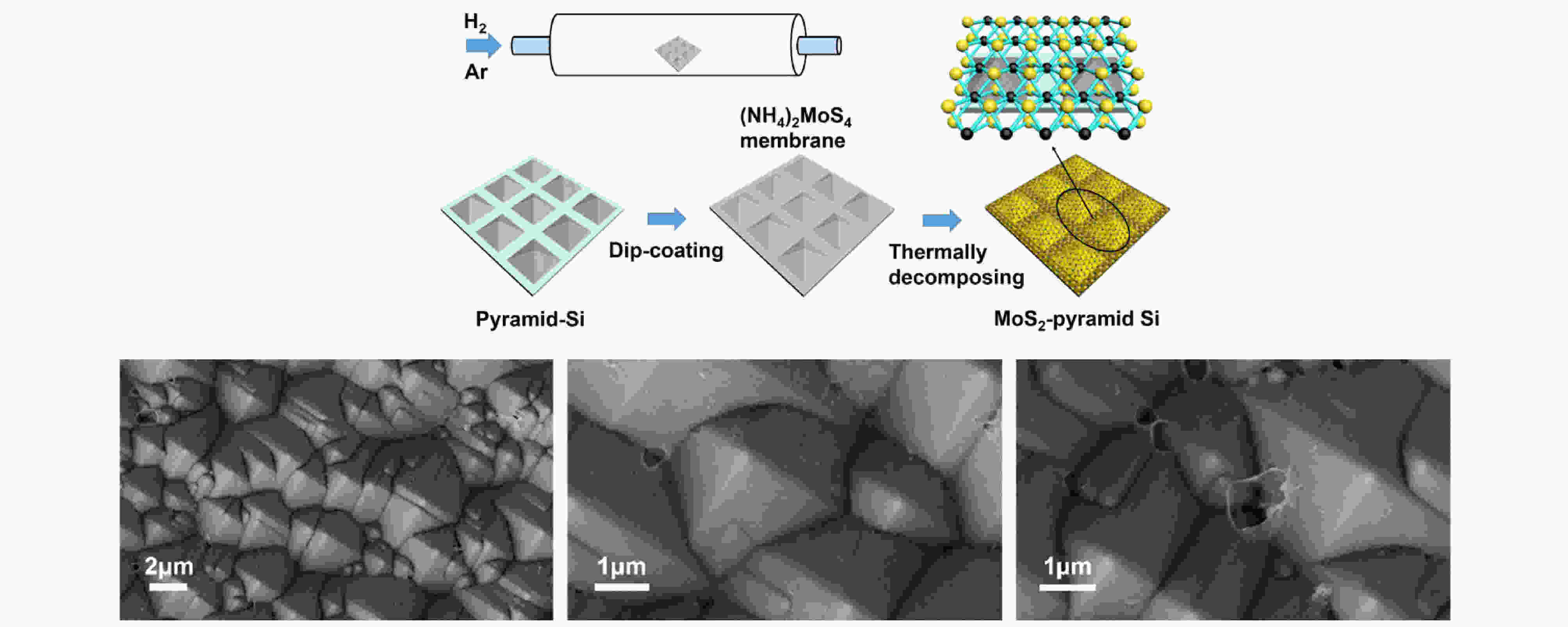 图 8 化学气相沉积法制备的金字塔形MoS2薄膜SERS基底[47]
图 8 化学气相沉积法制备的金字塔形MoS2薄膜SERS基底[47]Figure8. Pyramid-shaped MoS2 film SERS substrate prepared by chemical vapor deposition[47]
综上所述, 水热/溶剂热法制备过程简单、成本低廉、纯度较高, 被广泛应用于多种形貌SERS基底的研究. 而微机械力剥离法及化学气相沉积法均可制备高质量的MoS2薄膜SERS基底, 其中微机械力剥离法所制备的MoS2薄膜结晶度明显优于其他方法制备的同种结构, 但此方法操作过程复杂, 对剥离手法依赖程度高, 且产量较低、重复性差、无法形成大规模生产. 化学气相沉积法可通过调整反应条件, 制备不同厚度、层数的MoS2薄膜, 但制备过程中存在污染环境的风险. 在研究MoS2基底时, 研究人员可根据自身研究内容选择相应制备方式.
2
3.2.金属/MoS2复合SERS基底的制备
制备金属/MoS2复合SERS基底的技术可分为两类, 一类为自组装技术, 一般包括电化学法、热还原法、种子介导生长法等. 另一类为纳米刻蚀技术, 是指利用不同的工具或技术, 对所需纳米结构进行直接加工制备的方法, 一般包括电子束光刻、离子束刻蚀等.3
3.2.1.电化学法
电化学法通过电化学的氧化还原周期, 使贵金属被氧化还原为金属纳米粒子沉积于MoS2, 从而获得SERS性能. Xia等[48]通过电化学法制备了Ag/MoS2复合基底, 并成功对领氨基苯甲酸甲酯香精分子进行了SERS检测, 表明该基底在香精香料分子的检测方面具有潜在的应用价值.3
3.2.2.热还原法
热还原法是在不同的还原条件下, 将金属从其化合物溶液中还原, 同时加入MoS2材料, 金属离子被MoS2表面的不饱和硫吸引形成化学键, 最终得到金属/MoS2复合SERS基底, 此方法多与水热/溶剂热法相配合. Fei利用水热法合成的MoS2量子点作为还原剂, 通过热还原法制备核壳结构的Au/MoS2复合SERS基底, 每隔10 d对CV分子进行SERS检测, 60 d后此基底对CV分子仍保有良好的增强效果, 并成功在活细胞内获得了可区分的SERS图像.3
3.2.3.种子介导生长法
此方法利用水溶液或有机溶剂作为反应体系, 在一定条件下添加相应还原剂, 通过粒子诱导聚集及二次成核技术形成相应化学键, 可改善纳米粒子间的分散性及纵横比, 使金属/MoS2复合结构获得优异的增强效果. Liang以Au/MoS2纳米花复合结构为基础, MoS2表面的Au纳米粒子为晶种, 通过种子介导生长法合成了Ag/MoS2纳米花复合SERS基底, 并对4-MPH进行SERS检测.3
3.2.4.电子束光刻技术
EBL是配合薄膜沉积技术(电子束蒸发、磁控溅射等)将金属通过晶格匹配或静电吸附沉积在光刻后的衬底表面, 最后通过剥离技术在衬底上获得所需图案. 利用EBL技术, 研究人员陆续以MoS2薄膜作为衬底, 制备出多种形貌的金属纳米阵列 (图9), 如领结型阵列、矩形阵列[49]、圆柱状阵列[50]等. Lee等[51]通过EBL在单层MoS2薄膜上制备了Ag领结阵列, 实验表明复合结构SERS活性明显优于单一Ag领结基底及单一MoS2基底, 并认为可通过改变Ag领结与MoS2之间的耦合强度获得更佳增强效果. 图 9 电子束光刻法制备的Au领结/MoS2复合SERS基底 (a)[51], Au矩形/MoS2复合SERS基底[49] (b)和Au圆盘/MoS2复合SERS基底(c)[50]
图 9 电子束光刻法制备的Au领结/MoS2复合SERS基底 (a)[51], Au矩形/MoS2复合SERS基底[49] (b)和Au圆盘/MoS2复合SERS基底(c)[50]Figure9. Au bow tie/MoS2 composite SERS substrate prepared by electron beam lithography(a)[51], Au rectangular/MoS2 composite SERS substrate prepared by electron beam lithography(b)[49] and Au disc/MoS2 composite SERS substrate prepared by electron beam lithography(c)[50]
综上所述, 自组装技术操作方法简便、成本低廉, 可与多种形貌MoS2材料复合成SERS基底, 但此方法所制备的金属/MoS2复合基底的形状及尺寸可控性较低, 需经大量实验摸索. 而纳米刻蚀技术具有高度可控性, 可制备形貌可控、粒子间间距可调、排布高度有序、重现性高的金属阵列/MoS2复合SERS基底, 其中EBL技术较为常见, 但该技术仅适用于二维层状MoS2, 并且由于电子束斑尺寸及邻近效应, 导致制备时间过长, 且阵列参数过于精密时将产生边缘外扩及棱角不分明的情况, 此外, EBL制备SERS基底复杂的操作及较高的成本使其发展受到了限制. 在研究金属/MoS2基底复合基底时, 研究人员可根据研究内容选取合适的制备方案.
2
4.1.食品安全检测
为牟取暴利, 不法商家在食品中添加非法化学添加剂, 严重影响消费者身心健康. 由于大部分非法添加剂具有拉曼活性, 因此可使用SERS技术进行检测. Xu等[52]通过原位生长法成功合成了金字塔形Au-Ag/MoS2复合SERS基底, 实现了对低浓度三聚氰胺溶液的超灵敏检测 (图10); Liang等[53]制备了Au/MoS2纳米花复合SERS基底, 通过环境模拟的方式对牛奶中的三聚氰胺进行了有效的检测, 检测结果符合美国食品药品局规定的三聚氰胺含量.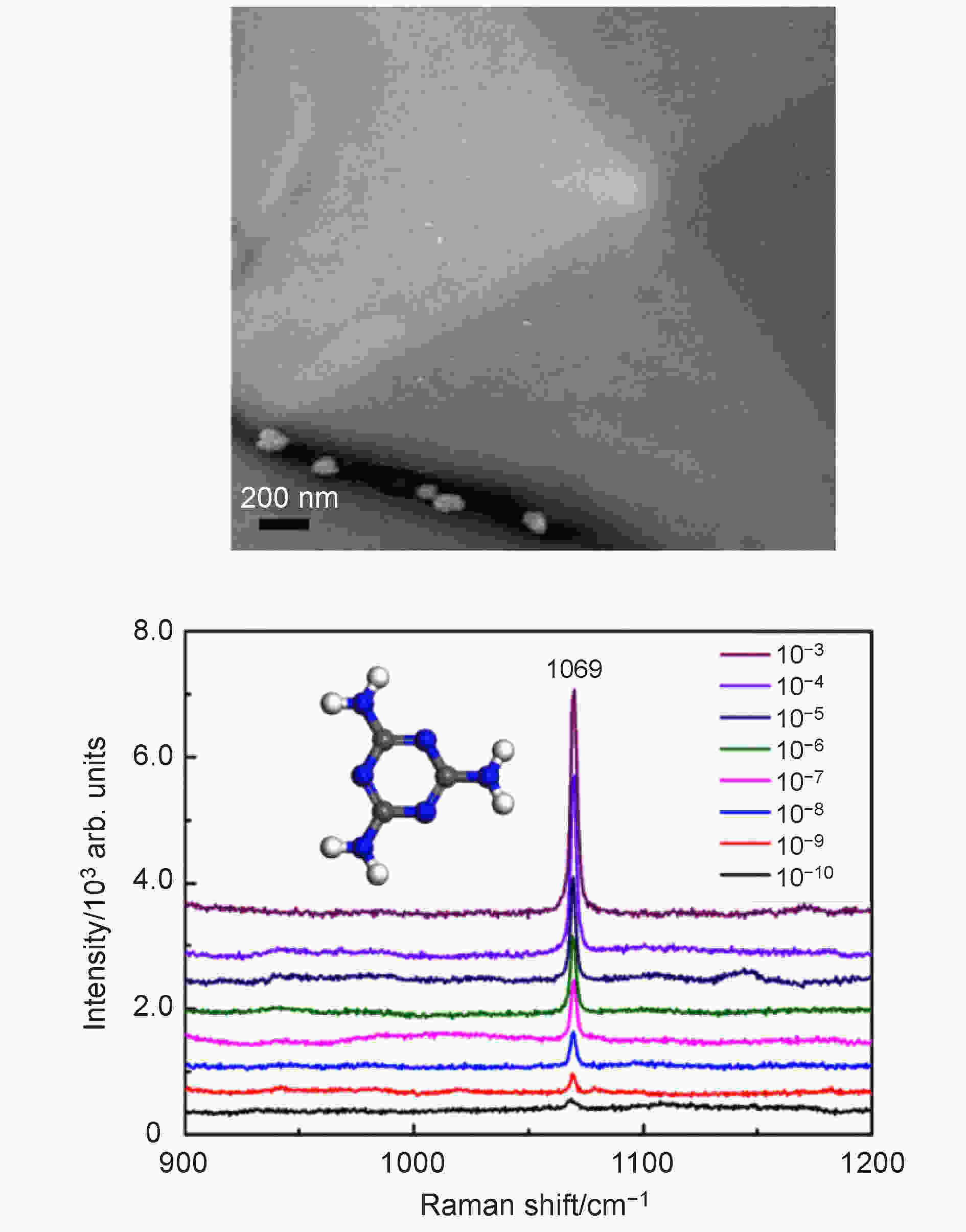 图 10 金字塔形Au-Ag/MoS2复合SERS基底检测三聚氰胺[52]
图 10 金字塔形Au-Ag/MoS2复合SERS基底检测三聚氰胺[52]Figure10. Detection of melamine by pyramidal Au-Ag/MoS2 composite SERS substrate.[52]
2
4.2.生物医学
SERS作为一种高灵敏无损耗的检测技术, 最初应用于生物医学, 随着研究的深入拓展, 到目前为止, 在生物医学方面的应用主要有两个方向: (1)检测生物分子的组成及结构; (2)医学诊断与目标探测. Jin等[54]制备了Au/MoS2复合纳米基底, 将其与标记过的互补DNA相结合, 使用SERS技术快速并具有选择性的对DNA核苷酸长链进行探测; Shib通过以Ag/MoS2纳米花复合结构作为SERS基底成功检测出人体血液内游离的胆红素, 未来将有望应用于关于黄疸的临床检测.2
4.3.环境检测
随着工业的迅速发展, 水污染问题日益严重, 其中各类污染物具有一定毒性, 且不易分解, 被生物体摄入后易致癌、致畸、致突变, 如何精准快速的检测水环境中的污染物, 成为目前的研究重点. 由于一般仪器设备体型过大, 检测时间过长、检测种类较少、前期处理复杂, 限制了其对污染物快速有效的检测, 而SERS因其灵敏度高、检测范围广泛, 响应迅速, 可联用现场快速分离技术(TLC-SERS等)实现快速痕量检测. Zhao等[55]在3D玻璃纤维上合成了Au/MoS2纳米复合材料 (图11), 并以此作为SERS基底对水中的CV分子及TB分子进行无标记筛选和超灵敏检测, 成功将其分离, 在检测水环境污染方面有着极大的应用前景.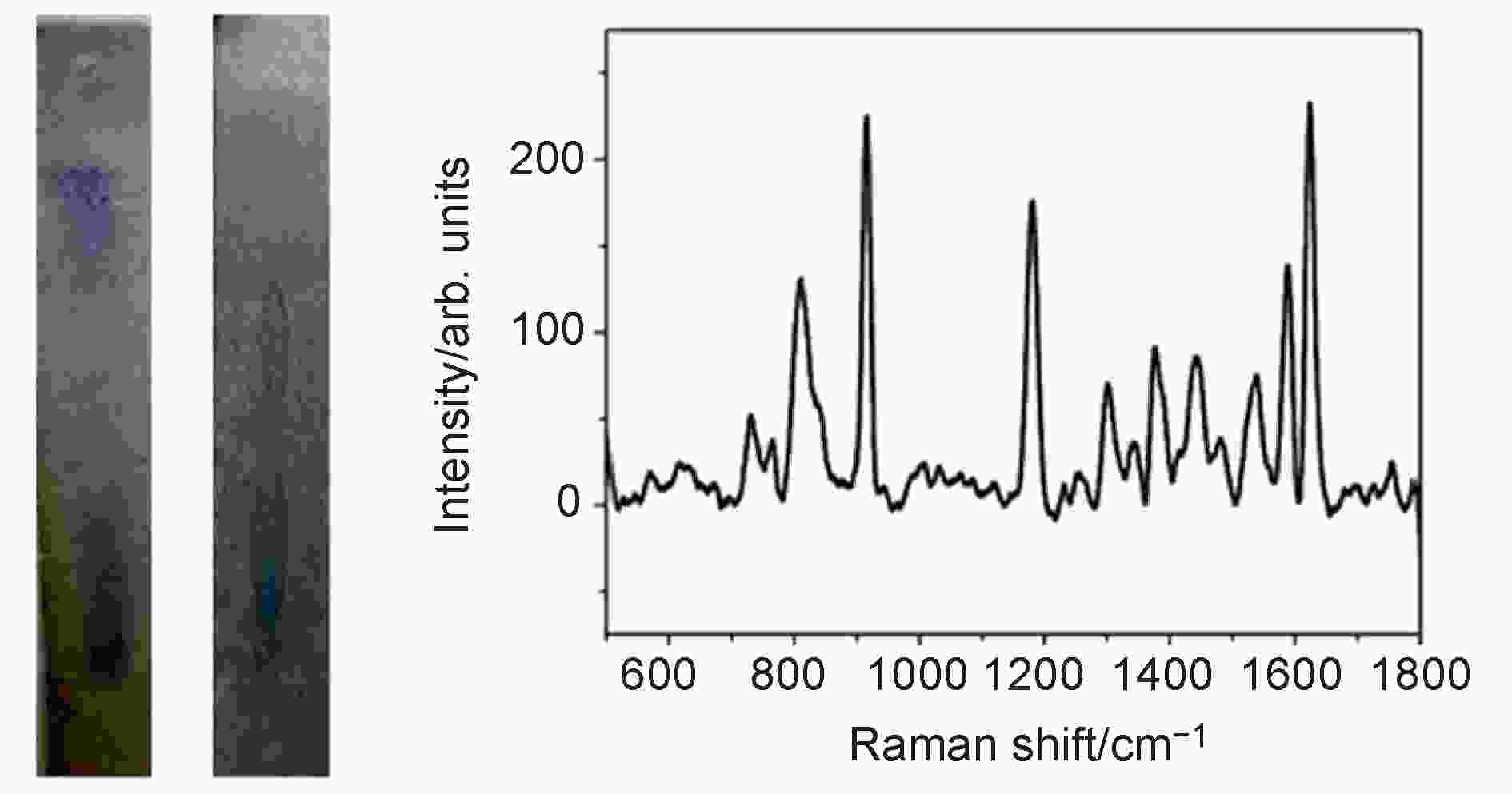 图 11 Au/MoS2作为SERS基底检测水中分离出的CV和TB分子[55]
图 11 Au/MoS2作为SERS基底检测水中分离出的CV和TB分子[55]Figure11. Au/MoS2 as SERS substrate for the detection of CV and TB molecules isolated from water[55]
目前, SERS技术仍在不断发展, MoS2及金属/MoS2复合纳米材料拥有广阔的应用前景值得继续探索. 例如, 在机理方面, 仍不能完善的解释MoS2对金属的电磁增强影响以及MoS2与金属的相互作用机理; 在制备方面, 如何实现降低成本的同时保证金属/MoS2复合基底的重现性及均匀性; 在增强效果方面, 可否通过调整金属阵列的不同参数使金属/MoS2复合基底实现更高的灵敏度等. MoS2及其金属复合SERS基底还需不断创新发展, 未来将有望成为研究纳米科学及表面科学的重要工具, 得到更广泛的应用.
