0 引言
【研究意义】紫茎泽兰(Ageratina adenophora)属菊科多年生恶性毒草,原产于中南美洲,20世纪40年代从中缅边境侵入中国,现已广泛分布于西南地区,给农业、林业、畜牧业和生态环境造成了巨大灾难,是中国危害最严重的外侵植物[1,2]。因此,有效防除与资源化利用紫茎泽兰具有重要意义。【前人研究进展】植物通过植株分解、自然挥发、降雨淋溶和根系分泌等多种途径向周围环境释放化感物质,影响周边其他植物生长[3]。目前,人们已从紫茎泽兰体内分离出100多种化学物质,包括单萜类、倍半萜类、甾体类、三萜类、苯丙素类、黄酮类等各类衍生物[4]。其中,已发现的化感物质有9-β-羰基泽兰酮、泽兰二酮、羟基泽兰酮及2-香豆酸葡萄糖苷等[5,6,7]。大量的研究表明,紫茎泽兰浸提液对白三叶、黑麦草、金毛狗、水稻、番茄、辣椒、茄子和豌豆等多种植物的种子发芽和幼苗生长具有强烈抑制[5,8-11]作用。在紫茎泽兰入侵过程中,枯枝落叶释放的化感物质较多,抑制周边植物生长,迅速形成紫茎泽兰优势种群[12]。在紫茎泽兰利用方面,用于造纸纤维不够长,做饲料有毒,当薪柴热值太低[13]。在农业生产中,施用有机肥和秸秆还田能改良土壤,提供养分,提高产量品质[14]。紫茎泽兰生命力强,根、茎和种子皆可再生繁殖[15],不能用于直接还田,而它繁殖快、生长迅速、生物量大,富含氮、磷、钾和微量元素,去除抑制植物生长的有毒的化感物质后是良好有机肥源[16]。在自然腐解中,紫茎泽兰的毒性抑制微生物的生化反应,导致自然堆腐时间长,效果差,且难于有效杀灭其营养繁殖器官和种子。值得注意的是,有些微生物能降解如苯、萘、菲、蒽等多环芳烃,如假单胞菌属(Pseudomonas)、诺卡氏菌属(Nocardia)、解环菌属(Cycloclasticus)、反硝化产碱菌(Alcaligenes denitrificans)、乙酸不动杆菌(Acinetobacter calcoaceticus)和多色节杆菌(Arthrobacter polychromogenes)等,产黄青霉(Penicllum chrysogenum)能降解香豆素和香草醛,黑曲霉(Aspergillus niger)和焦曲霉(Aspergillus ustus)还能分解丹宁[17,18]。因此,利用这些微生物可降解紫茎泽兰中有毒的化感物质,与腐熟微生物配合堆肥可实现无害化处理与资源化利用[13]。【本研究切入点】前人研究一般限于描述紫茎泽兰的生物学性质和对其他作物的危害。在紫茎泽兰人工防除的过程中,大量堆砌的植物残体亟需科学处理和资源化利用,很有必要选择一种生长周期完整的当地作物,研究紫茎泽兰的化感效应,评价腐熟紫茎泽兰的肥效以及对土壤微生物和作物产量品质的影响。四川省凉山州是紫茎泽兰侵入的重灾区,危害面积占幅员面积的14.1%,紫茎泽兰蚕食农田的现象十分普遍[19]。当地土壤深度风化、板结,有机质缺乏,严重影响作物的生长,需要大量施用有机肥。【拟解决的关键问题】了解紫茎泽兰对小麦的化感作用,评价微生物腐熟紫茎泽兰的肥效,开发有机肥资源,防除与资源化利用紫茎泽兰。1 材料与方法
1.1 供试材料
小麦品种:当地广泛种植的西昌19,购于西昌市种子公司。土壤:田间试验地点位于四川省西昌市西溪乡(东经102.20,北纬27.78),海拔1 680 m,年均气温17.1℃,年日照2 431 h,年降雨1 087.5 mm,属高原亚热带印度洋季风气候。供试土壤类型为紫色土,成土母质是侏罗纪紫色泥岩,质地中壤,肥力中等,pH 6.21、有机质16.01 g·kg-1、全氮1.04 g·kg-1、全磷0.43 g·kg-1、全钾11.62 g·kg-1,有效氮、磷、钾依次为56.32、9.25和117.5 mg·kg-1。
肥料:(1)紫茎泽兰有机肥(organic fertilizer made from A. adenophora,OF):于2015年9月收割营养生长期的紫茎泽兰地上部,用降解紫茎泽兰毒物的恶臭假单胞菌(Pseudomonas putita)和腐熟有机质的热解纤维梭菌(Clostridium thermocellum)制成专用菌剂,野外就地堆制腐熟有机肥[13](表1)。(2)化肥(CF):尿素(N 46%)、过磷酸钙(P2O5 12%)和硫酸钾(K2O 50%),购于当地农资公司。
Table 1
表1
表1紫茎泽兰的pH、有机质、腐植酸和养分含量(干重,%)
Table 1pH, organic matter, humic acid, and nutrients in A. adenophora (dry weight, %)
| 紫茎泽兰 A. adenophora | pH | 有机质 Organic matter | 氮 Nitrogen | 磷 Phosphorus | 钾 Potassium | 腐植酸 Humic acid |
|---|---|---|---|---|---|---|
| 新鲜 Fresh | 6.02 | 94.22 | 2.10 | 0.65 | 1.37 | — |
| 腐熟 Decomposed | 7.63 | 89.47 | 2.79 | 0.80 | 2.70 | 7.83 |
新窗口打开
紫茎泽兰浸提液(extracts of A. adenophora,EA):分别采集新鲜和腐熟紫茎泽兰样品,风干、粉碎、过1.0 mm筛。称取50.0 g样品,加入5 L蒸馏水,37℃浸提48 h,抽滤,获得新鲜(extracts of fresh A. adenophora,EFA)和腐熟紫茎泽兰浸提液(extracts of decomposed A. adenophora,EDA),相当于每1 L溶液含有10.0 g新鲜和腐熟紫茎泽兰。吸取母液分别配制成0(对照)、1.0 mg·L-1(低浓度)、10.0 mg·L-1(高浓度)EFA和EDA溶液。
1.2 试验设计
发芽试验:取均匀一致的供试种子,用1% H2O2消毒1 min,无菌水洗净。分别置于0、1.0、10.0 mg·L-1 EFA和EDA溶液中,(25±1)℃吸涨24 h或浸种至露白。取吸涨24 h的种子50粒,置于底部铺有滤纸的培养皿中(ϕ=10 cm),用相应溶液湿润滤纸,进行种子发芽,培养条件为(25±1)℃、光周期12 h﹕12 h、光照强度5 000 lx、7—10 d。在培养期间,每天适量补充无菌水,重复3次。盆栽试验:每盆装土1 kg,基施尿素0.5 g,过磷酸钙1.0 g,硫酸钾0.4 g,肥土混匀。每盆播种小麦10粒,出苗5 d后留5株均匀一致的健康幼苗。在出苗后第7、14、21天,分别用100 mL 浓度为0、1.0、10.0 mg·L-1 EFA和EDA的溶液灌根,重复6次。在培养期间,用重量法保持土壤含水量(70±2)%,自然温度与光照,持续40 d。
田间试验:设置不施肥(对照,CK)、单施化肥(CF)和化肥配施紫茎泽兰有机肥(CF+OF,无机氮﹕有机氮? 60﹕40)3种处理。在CF处理中,按照当地习惯亩施25 kg尿素,50 kg过磷酸钙和10 kg硫酸钾;在CF+OF处理中,施用15 kg尿素,以及相当于10 kg尿素的OF,并根据OF施入的磷、钾量补施化学磷、钾肥,使之等于CF处理的氮、磷、钾用量。化学磷、钾肥和OF均做基肥,基肥施氮量占全量的60%,剩余的氮肥于播种后40 d施用。小区面积40 m2,重复4次,随机区组排列。
1.3 测定项目与方法
田间和盆栽试验的土壤基本理化性质按常规方法测定[20]。在种子发芽试验中,以胚根长度>1 mm为标准,每隔6 h统计一次种子发芽数,若连续24 h发芽数无增加视为发芽完全,计算发芽率(发芽种子数/种子总数×100),发芽指数(∑Gt/Dt,Dt为发芽日数,Gt在Dt日的发芽数)和种子活力指数 [GI×S,GI为发芽指数,S为苗高(cm)][21]。测定第一片完全展开叶硝酸还原酶活性(磺胺-萘胺比色法)、叶绿素含量(乙醇浸提-分光光度计法)和根系活力(TTC法)[22]。取露白种子,分别用福林酚法、酸解-蒽酮比色法、茚三酮比色法、蒽酮比色法、铁沉淀法和钼蓝比色法分别测定种子蛋白质、淀粉、游离氨基酸、可溶性糖、六磷酸肌醇和水溶性无机磷含量[20,23-24]。
收获盆栽小麦植株,称生物量,105℃杀青,(80±1)℃烘干,H2SO4-H2O2消化,用凯氏法、钼黄比色法和火焰光度法分别测定消化液中的氮、磷、钾含量[20]。
收获田间小麦,记录产量,分别用福林酚法和酸解-蒽酮比色法测定蛋白质和淀粉含量[23]。取新鲜根际土壤,测定微生物生物量(氯仿熏蒸-0.5 mol·L-1 K2SO4提取,K2CrO7氧化法测碳、腚酚蓝比色法测氮)[25]、脱氢酶活性(TTC法)[26]及微生物群落多样性(BIOLOG-ECO法)[27]。
1.4 数据处理与分析
用Excel 2013对原始数据进行基本计算,用SPSS 16.0软件对数据进行Levene方差齐性检验,并进行方差分析,显著性水平为P<0.05。2 结果
2.1 紫茎泽兰浸提液对种子发芽和部分生理指标的影响
随EFA浓度提高,小麦种子发芽率、发芽指数和活力指数降低;EDA则相反,在10.0 mg·L-1的溶液中,发芽率、发芽指数和活力指数比对照分别提高4.73%、13.06%和6.58%(表2)。Table 2
表2
表2紫茎泽兰浸提液对小麦种子发芽特性的影响
Table 2Effects of EA on the germination characteristics of wheat seeds
| 处理 Treatment | 浓度Concentration (mg.L-1) | 发芽率Germination rate (%) | 发芽指数Germination index | 活力指数Vigor index |
|---|---|---|---|---|
| CK | 0 | 88.10±0.64b | 47.18±0.58b | 253.24±7.37b |
| EFA | 1.0 | 90.00±1.34ab | 46.43±1.10bc | 216.63±4.67c |
| 10.0 | 82.12±0.62c | 43.20±1.68c | 204.38±5.16d | |
| EDA | 1.0 | 90.34±0.72ab | 49.92±1.98ab | 258.79±5.61b |
| 10.0 | 92.27±2.01a | 53.34±3.36a | 269.90±5.76a |
新窗口打开
低浓度EFA对苗高、最大根长、硝酸还原酶活性和根系活力无显著影响(1.0 mg·L-1 EFA例外,苗高增加,叶绿素含量降低);在高浓度EFA处理中,上述生理指标显著降低。EDA不同程度地促进生长,在10.0 mg·L-1的溶液中,苗高和最大根长分别增加29.87%和22.81%,叶绿素含量、硝酸还原酶活性和根系活力比对照依次提高17.49%、10.64%和24.55%(表3)。
Table 3
表3
表3紫茎泽兰浸提液对小麦幼苗生长及生理指标的影响
Table 3Effects of EA on wheat seedling growth and physiological indexes
| 处理 Treatment | 浓度 Concentration (mg·L-1) | 苗高 Seedling height (cm) | 根长 Root length (cm) | 根系活力 Root activity (mg TTF·g-1·h-1) | 硝酸还原酶活性 NR activity (μg·g-1·h-1) | 叶绿素含量 Chlorophyll content (μg·g-1) |
|---|---|---|---|---|---|---|
| CK | 0 | 7.70±0.07c | 2.63±0.15b | 1.10±0.00b | 3.29±0.07b | 1.83±0.06b |
| EFA | 1.0 | 8.37±0.51b | 2.47±0.27bc | 1.19±0.29ab | 3.28±0.01b | 1.67±0.05c |
| 10.0 | 7.03±0.40d | 2.20±0.1c | 0.72±0.02c | 2.78±0.04c | 1.55±0.01d | |
| EDA | 1.0 | 8.80±0.12b | 3.57±0.22a | 1.28±0.02ab | 3.63±0.03a | 1.93±0.07b |
| 10.0 | 10.00±0.48a | 3.23±0.16a | 1.37±0.01a | 3.64±0.03a | 2.15±0.07a |
新窗口打开
2.2 紫茎泽兰浸提液对萌发种子内含物的影响
在EFA处理中,抑制小麦胚乳蛋白质、淀粉和六磷酸肌醇水解,其降幅显著低于EDA处理;游离氨基酸显著低于对照,可溶性糖和水溶性无机磷与对照相似。EDA则相反,促进胚乳蛋白质、淀粉和六磷酸肌醇水解,分别比对照提高14.52%—18.55%、14.59%—15.57%和21.54%—27.69%,游离氨基酸、可溶性糖和水溶性无机磷含量显著提高(图1)。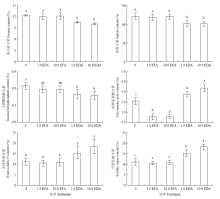 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图1紫茎泽兰浸提液对小麦萌发种子内含物的影响
-->Fig. 1Effects of EA on inclusions in germinating seeds of wheat
-->
2.3 紫茎泽兰浸提液对麦苗生长和养分吸收的影响
EFA抑制小麦生长,生物量降低47.77%—58.70%;EDA则相反,生物量增加17.00%—27.53%。在EFA处理中,植株吸收养分比对照降低69.98%—74.78%(氮)、49.94%—58.55%(磷)和65.50%—70.77%(钾);但与对照相比,EDA处理促进麦苗吸收氮素(10.0 mg·L-1 EDA处理的增幅未达显著水平),对磷、钾吸收无显著影响(表4)。Table 4
表4
表4紫茎泽兰浸提液对小麦生长和养分吸收的影响
Table 4Effect of EA on seedling growth and nutrient uptake of wheat
| 处理 Treatment | 浓度 Concentration (mg·L-1) | 生物量 Biomass (g DW/plant) | 养分吸收量 Nutrient uptake (mg/plant) | ||
|---|---|---|---|---|---|
| N | P | K | |||
| CK | 0 | 2.47±0.34b | 54.09±6.38b | 17.54±2.44a | 45.94±5.02a |
| EFA | 1.0 | 1.29±0.21c | 16.24±2.12c | 8.78±1.22b | 15.85±2.35b |
| 10.0 | 1.02±0.20c | 13.64±1.48c | 7.27±1.05b | 13.43±1.79b | |
| EDA | 1.0 | 3.15±0.28a | 65.21±7.55a | 20.48±4.17a | 45.68±6.16a |
| 10.0 | 2.89±0.24a | 61.13±8.82ab | 17.51±3.03a | 47.07±5.27a | |
新窗口打开
2.4 紫茎泽兰有机肥对根际土壤微生物的影响
在小麦根际土壤中,微生物碳氮含量CF+OF>CF>CK,依次为245.7、215.3和184.5 mg·kg-1(微生物碳),24.84、16.22和13.70 mg·kg-1(微生物氮),微生物碳氮比分别为9.89、13.27和13.47。脱氢酶活性CF与CK无显著差异,但CF+OF比CK和CF分别提高26.47%和34.38%。CF处理的Shannon-Wiener多样性指数与CK无显著差异,但CF+OF处理显著高于CK和CF(图2)。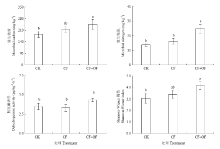 显示原图|下载原图ZIP|生成PPT
显示原图|下载原图ZIP|生成PPT图2紫茎泽兰有机肥对小麦根际微生物的影响
-->Fig. 2Effects of OF on microbes in the rhizosphere of wheat
-->
2.5 紫茎泽兰有机肥对小麦产量品质的影响
小麦籽粒产量CF+OF>CF>CK,CF+OF比CF增产8.87%。施紫茎泽兰有机肥显著提高穗数、穗粒数和粒重;但与CF相比,CF+OF处理的增幅未达显著水平(P<0.05)。此外,籽粒蛋白质含量CF+OF(13.61%)>CF(12.37%)>CK(11.02%),淀粉含量CF+OF、CF(66.22%—68.41%)>CK(61.53%)(表5)。Table 5
表5
表5紫茎泽兰有机肥对小麦产量品质的影响
Table 5Effects of OF on grain yield and quality of wheat
| 处理 Treatment | 穗数 Heads per 667 m2 | 穗粒数 Grains per head | 千粒重 Grain weight per 1000 grains (g) | 产量 Yield (kg/667 m2) | 蛋白质含量 Protein content (%) | 淀粉含量 Starch content (%) |
|---|---|---|---|---|---|---|
| CK | 97595±894b | 31.3±2.76b | 61.02±1.76b | 186.4±7.31c | 11.02±0.16c | 61.53±0.66b |
| CF | 136507±5038a | 41.5±4.51a | 66.89±2.07a | 378.9±10.1b | 12.37±0.09b | 68.41±3.07a |
| CF+OF | 137906±6351a | 43.2±4.02a | 69.24±2.15a | 412.5±11.5a | 13.61±0.11a | 66.22±0.32a |
新窗口打开
3 讨论
研究表明,秸秆直接还田使作物减产,而秸秆整株覆盖还田、秸秆做饲料再以粪肥方式还田,或与化肥配施可改善土壤肥力;换言之,只要具备腐殖化条件,秸秆还田具有明显培肥效果,提高产量[28,29,30]。紫茎泽兰化感物质种类多,毒性强,且其种子、茎、根均可再生繁殖,直接还田不仅不能提高土壤肥力,还会带来生态危害,而紫茎泽兰一旦经微生物腐熟后,可降解化感物质,消除毒性[13]。云贵地区大面积种植的烤烟也含有烟碱等化感物质,不能直接还田,但可利用微生物技术将废弃烟叶腐熟,去除有害物质,制成有机肥料[31]。紫茎泽兰在西南地区分布面积大,生长迅速,生物量大,富含氮、磷、钾及微量元素[16],可作为制备优质有机肥的原料。本研究表明,EFA不同程度地抑制小麦种子发芽,养分吸收和幼苗生长,说明紫茎泽兰内含化感物质,对小麦具有负化感效应不能直接用于翻压还田。前人研究也发现,紫茎泽兰叶片提取液对番茄、辣椒和茄子等14种植物均有毒性,妨碍种子萌发,降低发芽速率、胚轴和胚根长度,抑制幼苗生长[11]。一般植物自然凋零释放化感物质具有明显的毒性动态,前期毒性较强,而后期随着化感物质的分解毒性逐渐减弱[32]。在自然腐解中,紫茎泽兰的有害物质抑制微生物的生化反应,导致自然堆腐时间长,效果差。即植物自然凋落物腐熟周期长,受环境条件影响大。而人为添加专用腐熟剂,可改变和调整其成分和积制环境,加快植物残体的分解,快速降解化感物质,形成优质有机肥料。利用恶臭假单胞菌和热解纤维梭菌制成混合菌剂腐熟紫茎泽兰后,EDA促进小麦种子发芽和幼苗生长,说明微生物腐熟的紫茎泽兰既消除化感毒性,又刺激植物生长,是一种优质的有机肥料。在种子萌发过程中,胚乳中的淀粉、蛋白质和肌醇磷酸盐发生水解,形成单糖、氨基酸和无机磷,然后再经合成作用构建植物体[33]。在EFA抑制小麦种子发芽和幼苗生长的同时,胚乳中的蛋白质、淀粉和六磷酸肌醇的降幅低于腐熟紫茎泽兰浸提液处理,游离氨基酸含量低于对照、可溶性糖和水溶性磷与对照无显著差异,说明在小麦种子发芽过程中,EFA抑制了胚乳中的大分子物质水解,减少可溶性碳水化合物和养分供应,从而降低种子萌发率。相反,EDA则有促进作用,向胚芽提供构建植物体需要的基础物质,提高小麦种子的发芽率和幼苗生长速率。此外,根系活力是根系内多种呼吸酶活性的综合体现,与能量代谢密切相关[34],根系活力强,有益于养分吸收[35]。叶绿素参与光能的吸收与转化,影响光合速率[36],其含量高低通常还能指示植物氮素营养的丰缺状况[37]。在旱地土壤中,无机氮以硝态氮为主,硝酸还原酶催化无机氮同化的原初反应——硝酸盐还原成氨,是植物利用硝态氮的关键酶之一[38]。据报道,植物分泌的化感物质可以改变呼吸酶、硝酸还原酶、谷氨酰合成酶、谷氨酸脱氢酶、吲哚乙酸氧化酶等多种酶的活性,影响能量转化、物质代谢、养分吸收、氮磷同化等,进而抑制周围植物的生长发育[39]。高浓度EFA不同程度地降低根系活力、硝酸还原酶活性和叶绿素含量。在EFA灌根处理中,降低小麦氮、磷、钾吸收量和生物量,推测EFA中的化感物质抑制养分吸收、氮素同化和光合作用,可视为EFA抑制小麦生长的重要原因之一。但是,用浇灌EDA则相反,说明在微生物腐熟紫茎泽兰过程中,降解了化感物质,合成了刺激植物生长腐植酸,并提高了氮、磷、钾等元素的生物有效性。
据报道,紫茎泽兰内含多种对土壤微生物有害的化学物质,抑制其新陈代谢和繁殖生长[19]。因此,紫茎泽兰有机肥对土壤微生物的影响不可忽略。在CF+OF处理中,小麦根际微生物碳氮、脱氢酶活性和多样性指数提高,意味着微生物数量增多,活性增强,种群增加。在稳定良好的生态环境中,多种生物共存,多样性指数提高,是生态系统稳定和健康的重要表现[40],故施用OF改良了土壤生态环境。微生物参与土壤养分转化,活性增强有益于提高土壤养分的生物有效性,增加养分供应[41]。与CF相比,尽管CF+OF的穗数、穗粒数和粒重的增幅未达显著水平,但积微成显,CF+OF比CF增产8.87%,籽粒蛋白质含量显著提高。小麦生育期长,经历冬春两季,土壤温度变化幅度大,需要持续较长时间的养分供应。化肥含速效养分,有机肥肥效持久,CF+OF速缓相济,能满足小麦各生育期对养分的需要,有益于生长发育,提高产量,改善品质。
4 结论
新鲜紫茎泽兰含有抑制小麦种子发芽、养分吸收和幼苗生长的化感物质,利用恶臭假单胞菌和热解纤维梭菌制成的混合菌剂腐熟之后,可消除原生肥源的毒性,刺激小麦种子发芽率,增加氮素吸收,促进幼苗生长,增强根际微生物活性,提高产量品质。微生物腐熟紫茎泽兰生产有机肥兼具无害化处理与资源化利用,值得提倡推广。The authors have declared that no competing interests exist.
