近年来发展起来的CRISPR-Cas9(一种基因编辑技术)系统可以高效地对基因进行编辑。通过向受精卵或卵母细胞共注射Cas9(基因编辑技术之一)和sgRNA(引导核糖核酸),可以有效地产生基因编辑的模式动物。然而,注射的Cas9一旦开始发挥作用即具有持续切割的能力,很难在时间及空间水平上精确地控制Cas9的活性。这限制了Cas9注射方法的应用范围并且突显出了许多弊端。首先,传统的显微注射方法,由于具有持续的Cas9切割活性,其产生的基因编辑胚胎或者动物绝大部分都存在着基因型嵌合,需要经历长时间的繁育纯化过程。其次,目前还没有一种有效的方法可以在胚胎中利用CRISPR-Cas9技术对亲本特异性的位点进行编辑。这些缺陷归根结底是因为不能有效地对Cas9活性进行时空特异性控制。
为了在时空精确调控CRISPR/Cas9的活性并实现精确的单等位位点的基因编辑,研究者们提出了两点假设:第一,在生物体的整个生命周期中,受精卵原核期是能够区分开父母源染色体组的唯一窗口,提供了对不同亲本染色体位点进行操作的空间。第二,受精卵中保留的Cas9/sgRNA可以通过原核互换的方法进行胞质的稀释作用从而终止Cas9的编辑活性,可以用来精确调控CRISPR/Cas9的活性。
基于这两点假设,研究者在MII期卵母细胞中共注射Cas9 mRNA(信使核糖核酸)及靶向目的基因的sgRNA之后,进行体外受精(IVF)。等到受精卵发育到PN3-4阶段(受精后7-9小时),将注射组受精卵的雌原核或者雄原核分别取出,并转移到分别去除雌原核或者雄原核的正常受精卵中重构出二倍体受精卵。理论上,重构受精卵的一套染色体组已经被编辑而另一套染色体组为野生型(Pat-ko/Mat-wt; Mat-ko/Pat-wt)。
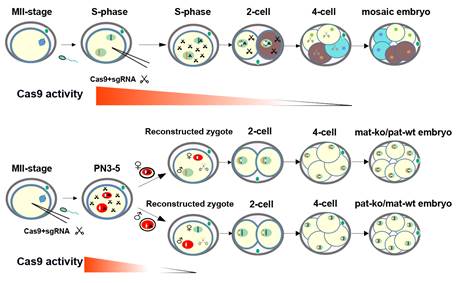
通过利用Past-CRISPR(亲本等位特异性编辑)方法在多个基因位点进行分析验证,发现在保持正常的编辑效率(85.7%)的同时对各基因位点均具有高效的等位特异性的编辑效率(91.7%)。并且该方法能够选择性的对不同亲本等位位点进行编辑。同时,Past-CRIPSR方法与传统的胚胎显微注射方法相比,能够产生更低的基因型嵌合率(7.1% VS 84.6%)。
接下来,研究者利用Past-CRISPR方法进行了多种基因编辑的应用。该方法能够通过一步法对印记基因进行功能及表型的鉴定。该方法能够快速且有效的产生携带有突变致死基因的单等位突变的动物模型,并且证明该致死突变可稳定遗传给后代;同时,该方法可通过一步法得到没有基因型嵌合的完全基因敲除的动物模型。最后,该方法还能用于对显性遗传疾病的治疗,研究人员利用Fgfr3显性突变导致的侏儒症小鼠疾病模型(Gly369Cys),利用Past-CRISPR方法特异性地破坏显性突变等位位点从而纠正子代骨发育异常的病理症状,阻断了该疾病在子代中的传播。
同济大学博士研究生李延鹤为本文第一作者,高绍荣教授和刘文强研究员为本文共同通讯作者。本文的其他作者还包括高绍荣教授实验室的陈嘉瑜副教授,技术员寇晓晨和赵艳红、柏丹丹、贾艳平、刘营东、张亚林、殷吉庆老师、王红老师以及同济大学附属口腔医院王佐林教授和直博生翁雨藤。该研究得到了科技部、基金委和上海市科委等项目支持。
