
桥本甲状腺炎(HT)是最常见的自身免疫性甲状腺疾病(AITD),在女性人群中患病率超过10%。典型的HT以甲状腺组织大量的淋巴细胞浸润、异位淋巴组织的形成,并伴有甲状腺滤泡细胞破坏为特征,同时出现针对甲状腺过氧化物酶抗体(Thyroid peroxidase antibody,TPOAb)和甲状腺球蛋白抗体(Thyroglobulin antibody,TGAb),但到目前为止,导致HT患者甲状腺组织中大量淋巴细胞浸润和甲状腺细胞破坏的机制了解很少。桥本甲状腺炎患者的自然病程多是先出现TPOAb或TGAb阳性,且早期患者甲状腺功能多正常,但随着病程的进展,甲状腺滤泡细胞逐渐被破坏,患者出现亚临床和临床甲减。由于甲状腺自身免疫性抗体测定在临床上的广泛应用,使得大量早期桥本甲状腺炎患者被诊断出来,针对这些患者,目前临床上缺乏有效的可以阻止甲状腺组织破坏及甲状腺功能减退发生的治疗手段。只能等到患者发生甲状腺功能减退后,才能被动给予患者甲状腺激素替代治疗。但即使治疗后患者外周血甲状腺激素浓度完全恢复正常,仍有25%左右的患者存在甲状腺功能减退的症状3。
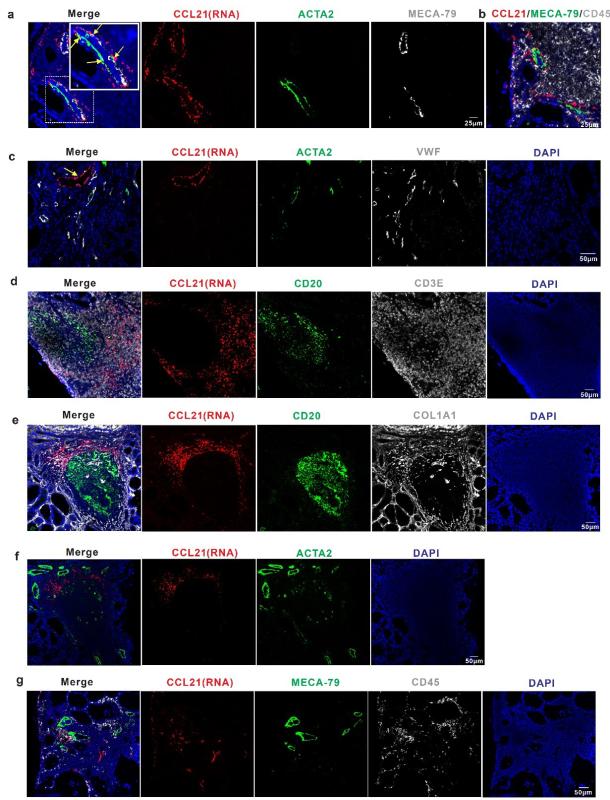
图1. 桥本甲状腺炎患者甲状腺组织切片多色免疫荧光染色显示CCL21+基质细胞分布
HT发病机制尚不清楚且缺乏针对病因的治疗方法。为了进一步探索HT的发病机制,宋怀东课题组通过单细胞测序鉴定了HT患者甲状腺组织基质细胞的多个亚群,其中CCL21+肌成纤维细胞和CCL21+阳性成纤维细胞均高表达CCL19和CCL21。通过多色免疫荧光染色,他们发现CCL21+成纤维细胞在HT患者的甲状腺组织主要呈现三种不同的分布。其一是分布在异常增多的高内皮静脉周围,其二是零散分布在甲状腺的不同区域,且都围绕有聚集的免疫细胞;三是分布在有生发中心形成的三级淋巴组织的T细胞区。而CCL21+肌成纤维细胞分布于高内皮静脉外膜。且体外实验证明CCL21可以在促进T淋巴细胞的迁移。这些结果提示在免疫细胞自高内皮静脉进入到甲状腺组织,浸润到甲状腺组织的不同部位,并在某些部位逐渐形成结构完整的有明显分区的三级淋巴组织的过程中,CCL21+成纤维细胞都发挥着不可或缺的作用(图1)。
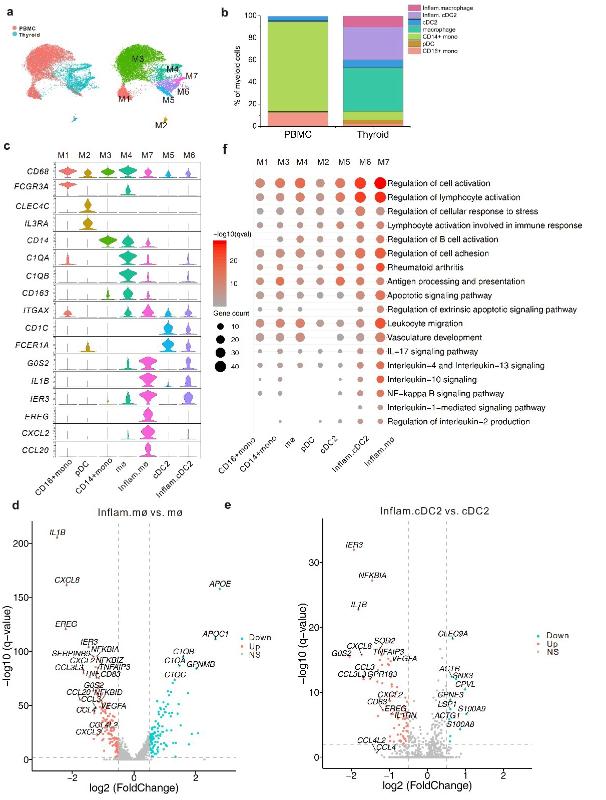
图2. 桥本甲状腺炎患者甲状腺组织存在特异性的高表达IL-1β的炎症性巨噬细胞和炎症性树突细胞亚群
此外,该研究还发现桥本甲状腺炎患者甲状腺组织特异性存在炎症性巨噬细胞和树突细胞亚群,它们均显著高表达多个炎症相关基因,其中,IL-1β在炎症性巨噬细胞中的表达升高最为显著。以往文献表明IL-1β可以促进CD40L介导的树突细胞激活,促进受到抗原刺激后的CD4+ T细胞的激活和增殖, 促进Th17细胞分化, 和诱导甲状腺滤泡细胞异位高表达FAS,进而使甲状腺滤泡细胞凋亡破坏。这些结果提示,炎症性巨噬细胞和炎症性树突细胞可能通过分泌多种炎症因子和趋化因子促进HT甲状腺组织中各类免疫细胞的分化和甲状腺滤泡细胞的破坏(图2)。
该研究提示,CCL19/CCL21在HT发生过程中,对甲状腺组织的免疫细胞浸润和三级淋巴组织形成均可能有重要作用,而浸润到甲状腺组织中的特异性炎症性巨噬细胞和树突细胞亚群,可能通过分泌IL-1β促进甲状腺滤泡的破坏。因此,靶向阻断CCL19/CCL21与CCR7的相互作用有望阻断甲状腺免疫细胞浸润,从而减少甲状腺滤泡破坏,延缓甲状腺功能减退的发生。
近十年,全球自身免疫性甲状腺疾病研究领域在国际著名刊物CNS及其子刊上发表论文仅8篇。这是宋怀东教授团队时隔10年在CNS子刊上发表的第二篇关于自身免疫性甲状腺疾病发病机制的研究论文,也是十年来CNS系列刊物发表的唯一一篇关于桥本甲状腺炎的研究论文。九院宋怀东教授团队的张倩月、叶小萍、周正博士和九院普外科朱晨芳博士为该论文第一作者,团队的宋怀东教授和生物信息学分析专家林建南博士为论文共同通讯作者。
宋怀东上海交通大学医学院附属第九人民医院内分泌代谢病科学术带头人,博士生导师,二级教授,主任医师,研究员,国家基金委二审专家。上海十大****,国务院特殊津贴专家,人事部“新世纪百千万人才工程”国家级人才、教育部“新世纪人才”、上海市优秀学科带头人、上海市“领军人才”。曾获第九届“中国青年科技奖”,上海卫生系统银蛇奖一等奖,上海市教委“曙光****”。长期从事甲状腺基础和临床研究,提出并验证甲亢存在不同的分子亚型,不同的分子亚型由不同的发病机制和临床转归的科学假说,在甲亢和甲减发病机制研究中取得系列性原创成果。发表SCI论著150 余篇,包括《Science》、《Nat Genet》等国际著名刊物,发表论文被引用超5500次。主持包括国家自然基金重点、以及科技部863、重大研发计划等国家级项目12项。获得国家自然科学二等奖、教育部和上海市自然科学一等奖等多项研究成果。
