上海药物研究所围绕近来备受关注的受体酪氨酸激酶c-Met抑制剂,通过在MET基因扩增为分型的肿瘤细胞中构建c-Met抑制剂耐药模型,借助转录组学、激酶芯片等技术及系列细胞生物学实验,发现c-Met抑制剂通过诱发肿瘤细胞激酶组的重编程导致耐药产生。而转录因子c-Myc作为关键下游效应分子,其水平受上游复杂激酶信号通路调控,对c-Met抑制剂敏感及耐药细胞的存活均至关重要。c-Myc蛋白水平的变化与c-Met抑制剂疗效响应及耐药的产生及密切相关,该发现在能高度模拟临床试验的MET基因扩增的PDX动物模型中得到了进一步的验证。
该研究提示,MET基因扩增的肿瘤分子亚型中,c-Myc蛋白水平可以指示疗效、甄别c-Met抑制剂真正有效获益病人;进一步通过监控c-Myc水平的动态变化,则可监测并预警耐药的出现,并协助筛选克服耐药的方案。此项研究首次提出具有区分响应人群、监控耐药发生、指导克服耐药“三位一体”的疗效监控标志物,提示通过开发靶向c-Myc的分子影像学探针,有望在分子水平实现c-Met抑制剂临床使用的全程监控、指导临床方案制定,具有重要的临床转化意义。
该项研究目前已发表在Cancer research杂志上,项目得到了国家自然科学基金,科技部重大专项等基金的资助。
文章链接:http://cancerres.aacrjournals.org/content/early/2015/10/18/0008-5472.CAN-14-2743.long
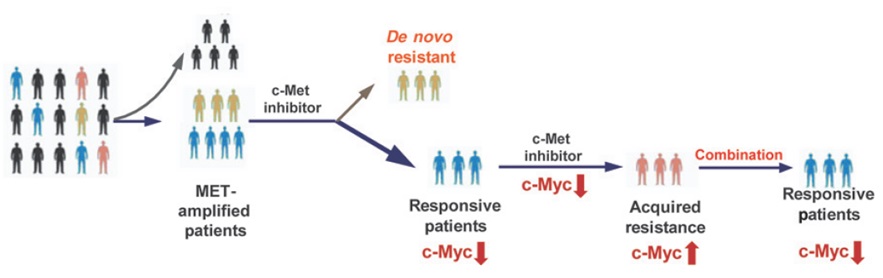
c-Myc参与指导c-Met抑制剂临床用药路线图
(供稿部门:耿美玉课题组;供稿人:黄敏)
