

1. 湖北大学 生命科学学院 省部共建生物催化与酶工程国家重点实验室 湖北省环境微生物工程技术研究中心,湖北 武汉 430062;
2. 湖北工业大学 生物工程与食品学院 发酵工程教育部重点实验室 工业微生物湖北省重点实验室,湖北 武汉 430068;
3. 绿康生化股份有限公司,福建 浦城 353400
收稿日期:2019-10-14;接收日期:2019-11-20
基金项目:国家重点研发计划(No. 2018YFA0900300)资助
摘要:杆菌肽是一种主要由芽胞杆菌产生的广谱性环肽类抗生素,目前广泛应用于兽药领域。能量代谢在微生物高效合成目的代谢产物中具有重要作用。文中以杆菌肽工业生产菌株地衣芽胞杆菌Bacillus licheniformis DW2为出发菌株,首先构建了呼吸链分支途径细胞色素bd泛醇氧化酶基因cydB缺失菌株,发现cydB缺失后杆菌肽效价和胞内ATP浓度相比于对照菌株分别提高了10.97%和22.96%。接着,证实了强化表达另外一条呼吸链分支途径——细胞色素aa3氧化酶基因qoxA能够提高杆菌肽合成水平,其杆菌肽效价和胞内ATP浓度相比于对照菌株分别提高了18.27%和34.00%。强化ADP合成供给也是促进胞内ATP积累的有效策略,结果表明强化表达腺苷激酶DcK和腺苷酸激酶AdK均可以提高杆菌肽效价和胞内ATP浓度,其中强化表达DcK效果较好,其杆菌肽效价相比对照提高16.78%。最后,通过组合代谢工程育种,在基因cydB缺失菌DW2ΔcydB基础上整合表达了qoxA和dck,得到工程菌株DW2-CQD (DW2ΔcydB::qoxA::dck),发酵结果表明,DW2-CQD杆菌肽效价达到954.25 U/mL,相比于对照菌株提高了21.66%,单位菌体杆菌肽效价为2.11 U/CFU,相比对照提高了11.05%。此外,DW2-CQD胞内ATP浓度为39.54 nmol/L,相比于对照提高了49.32%。结果证实能量代谢工程是提高杆菌肽发酵水平的有效策略,提供了一株具有工业化应用前景的杆菌肽生产菌株。
关键词:地衣芽胞杆菌杆菌肽ATP供给代谢工程
Enhanced production of bacitracin via energy metabolism engineering in Bacillus licheniformis DW2
Qing Zhang1, Shan Zhu1, Naixiang Cui1, Bowen Zhang1, Zhi Wang2, Xiaobin Chen3, Jun Liu3, Junhui Li3, Dongbo Cai1, Zhifan Yang1, Shouwen Chen1, Xin Ma1


1. Environmental Microbial Technology Center of Hubei Province, State Key Laboratory of Biocatalysis and Enzyme Engineering, College of Life Sciences, Hubei University, Wuhan 430062, Hubei, China;
2. Hubei Provincial Key Laboratory of Industrial Microbiology, Key Laboratory of Fermentation Engineering (Ministry of Education), School of Food and Biological Engineering, Hubei University of Technology, Wuhan 430068, Hubei, China;
3. Lifecome Biochemistry Co. Ltd, Pucheng 353400, Fujian, China
Received: October 14, 2019; Accepted: November 20, 2019
Supported by: National Key Research and Development Program of China (No. 2018YFA0900300)
Corresponding author: Xin Ma. E-mail: maxin@hubu.edu.cn.
Abstract: Bacitracin is a broad-spectrum cyclic peptide antibiotic, and mainly produced by Bacillus. Energy metabolism plays as a critical role in high-level production of target metabolites. In this study, Bacillus licheniformis DW2, an industrial strain for bacitracin production, was served as the original strain. First, our results confirmed that elimination of cytochrome bd oxidase branch via deleting gene cydB benefited bacitracin synthesis. Bacitracin titer and ATP content were increased by 10.97% and 22.96%, compared with those of original strain, respectively. Then, strengthening cytochrome aa3 oxidase branch via overexpressing gene qoxA was conducive to bacitracin production. Bacitracin titer and ATP content were increased by 18.97% and 34.00%, respectively. In addition, strengthening ADP synthesis supply is also proven as an effective strategy to promote intracellular ATP accumulation, overexpression of adenosine kinase DcK and adenylate kinase AdK could all improve bacitracin titers, among which, dck overexpression strain showed the better performance, and bacitracin titer was increased by 16.78%. Based on the above individual methods, a method of combining the deletion of gene cydB and overexpression of genes qoxA, dck were used to enhance ATP content of cells to 39.54 nmol/L, increased by 49.32% compared to original strain, and bacitracin titer produced by the final strain DW2-CQD (DW2ΔcydB::qoxA::dck) was 954.25 U/mL, increased by 21.66%. The bacitracin titer produced per cell was 2.11 U/CFU, increased by 11.05%. Collectively, this study demonstrates that improving ATP content was an efficient strategy to improve bacitracin production, and a promising strain B. licheniformis DW2-CQD was attained for industrial production of bacitracin.
Keywords: Bacillus licheniformisbacitracinATP supplymetabolic engineering
杆菌肽是一种由12个氨基酸组成的环肽类广谱型抗生素,主要由地衣芽胞杆菌和枯草芽胞杆菌产生[1-2],其组成氨基酸包含Orn、D-Phe、His、D-Asp、Asn、Lys、D-Glu、Cys、Leu、Ile和Val共11种[1-4]。杆菌肽是由多种组分组成的混合物[3],包括杆菌肽A、A1、B1、B2、B3、C、D……G等,其中A、B1、B2组分的生物活性约占其总生物活性的95%以上。杆菌肽由7个氨基酸组成的噻唑环组成,这种独特的氨基酸结构使得其不易被蛋白酶降解,且常以杆菌肽锌盐形式存在,因而在自然界中稳定性较强[1]。杆菌肽络合物可以与细菌细胞壁上的异戊烯焦磷酸结合[5],进而有效抑制细胞壁合成,因此对革兰氏阳性菌和部分革兰氏阴性菌具有显著抑制效果[5-6],现已广泛应用于兽药领域[7-8]。目前,杆菌肽生产水平较低,摇瓶水平一般为700–800 U/mL,限制了杆菌肽的生产及应用推广。
与常规蛋白质合成机制不同,杆菌肽是由非核糖体肽合成酶催化合成[9-11]。杆菌肽合成的前体氨基酸会与腺嘌呤核苷三磷酸(Adenosine triphosphate,ATP)结合,由该酶的A结构域催化生成活性氨酰-AMP,进而生成杆菌肽。此外,ATP是细胞代谢通用的能量载体,在促进细胞生长、代谢产物合成、维持细胞内环境稳定、酶活性调节等多方面发挥着不可或缺的作用[12-13]。目前,能量代谢工程育种也得到人们的广泛关注。通过强化来源于透明颤菌的血红蛋白VHb,人们显著提高了芽胞杆菌中聚-γ谷氨酸[14]、透明质酸[15]等产物的合成水平。鉴于芽胞杆菌高的维持代谢能[16],优化细胞呼吸链分支途径也有利于细胞维持代谢能的降低,进而有利于目的产物的合成。Nicola等[16]通过敲除枯草芽胞杆菌RB50中呼吸链终端细胞色素bd氧化酶,将维持代谢能降低了40%,进而提高了菌体生物量和核黄素产量。采用同样策略,Liu等[17]和Cai等[18]分别显著提高了芽胞杆菌中N-乙酰葡糖胺和聚- γ谷氨酸产量。Zhao等[19]通过优化终端氧化酶表达水平,使得大肠杆菌中β-胡萝卜素产量提升21%。
地衣芽胞杆菌DW2是一株杆菌肽工业生产菌株。之前的研究中,本课题组通过强化底物利用[15]、前体氨基酸(鸟氨酸、赖氨酸、支链氨基酸等)供给[20]、辅因子再生[12]等显著提高了杆菌肽产量,但对于能量供给水平与杆菌肽合成的关系尚不明晰。本研究拟通过优化细胞呼吸链分支途径、强化ATP合成途径等能量代谢工程育种策略获得杆菌肽高产地衣芽胞杆菌工程菌株,进而提高杆菌肽生产水平。
1 材料与方法1.1 菌株与质粒本研究出发菌株为杆菌肽工业生产菌株地衣芽胞杆菌DW2,其由绿康生化股份有限公司提供,菌株保藏号为CCTCC M2011344。本研究所用菌株和质粒见表 1。相关引物见表 2。
表 1 本研究所用的菌株与质粒Table 1 The strains and plasmids used in this study
| Strains or plasmids | Relevant characteristics | Source/reference |
| Strains | ||
| ??E. coli DH5α | F– Φ80d/lacZΔM15, Δ(lacZYA-argF) U169, recA1, endA1, hsdR17 (rK–, mK+), phoA, supE44, λ–, thi-1, gyrA96, relA1 | TaKaRa Co., Ltd |
| ??B. licheniformis DW2 | Bacitracin industrial production strain (CCTCC M2011344) | CCTCC |
| ??DW2ΔcydB | Knockout of gene cydB in DW2 | This study |
| ??DW2ΔqoxA | Knockout of gene qoxA in DW2 | This study |
| ??DW2/pHY300 | DW2 containing plasmid pHY300PLK | This study |
| ??DW2/pHY-qoxA | DW2 containing plasmid pHY-qoxA | This study |
| ??DW2/pHY-dck | DW2 containing plasmid pHY-dck | This study |
| ??DW2/pHY-adk | DW2 containing plasmid pHY-adk | This study |
| ??DW2-CQ | qoxA integrated overexpression in DW2ΔcydB | This study |
| ??DW2-CQD | dck integrated overexpression in DW2-CQ | This study |
| Plasmids | ||
| ??pHY300PLK | E. coli–Bacillus shuttle vector; Ampr in E. coli, Tcr in both E. coli and B. subtilis | Lab collection |
| ??pHY-qoxA | Plasmid pHY300PLK containing P43 promoter, gene qoxA and amyL terminator | This study |
| ??pHY-dck | Plasmid pHY300PLK containing P43 promoter, gene dck and amyL terminator | This study |
| ??pHY-adk | Plasmid pHY300PLK containing P43 promoter, gene adk and amyL terminator | This study |
| ??T2(2)-ori | E. coli-B. licheniformis shuttle vector, for gene konckout | Lab collection |
| ??T2-cydB | T2(2)-ori derivative containing homologous arms for disruption of cydB | This study |
| ??T2-qoxA | T2(2)-ori derivative containing homologous arms for disruption of qoxA | This study |
| ??T2-::dck | T2(2)-ori derivative containing homologous arms and dck expression cluster, to overexpress dck | This study |
| ??T2-::qoxA | T2(2)-ori derivative containing homologous arms and qoxA expression cluster, to overexpress qoxA | This study |
表选项
表 2 本研究所使用的引物Table 2 The primers used in this study
| Primer name | Sequence (5′–3′) |
| pHY-F | GTTTATTATCCATACCCTTAC |
| pHY-R | CAGATTTCGTGATGCTTGTC |
| T2-L | ATGTGATAACTCGGCGTA |
| T2-R | GCAAGCAGCAGATTACGC |
| cydB-KF1 | GGCGAGCTCCACTGCAAAAGCAATATGAAG |
| cydB-KR1 | GCTGACCCGTTTTCTAAAAGAAAGAAAAAACCGATGAACAGC |
| cydB-KF2 | GCTGTTCATCGGTTTTTTCTTTCTTTTAGAAAACGGGTCAGC |
| cydB-KR2 | GCTCTAGACATAAAAGTGATTAAAATCGGC |
| cydB-KYF | TCTGATGAAGAGCCAGCCGATGA |
| cydB-KYR | TTCTTAGTATGTGAACGGCTG |
| qoxA-KF1 | CGGGATCCAAGCACATCCGAACGGCTATCA |
| qoxA-KR1 | CGGAGACAACGGTTTATAGCCCAGCCGCCCAATAAAAAAACG |
| qoxA-KF2 | CGTTTTTTTATTGGGCGGCTGGGCTATAAACCGTTGTCTCCG |
| qoxA-KR2 | GCTCTAGAATCCGCCGATGACGAATGAAAT |
| qoxA-KYF | ATACAATCTCGGAAACGGAAC |
| qoxA-KYR | CAGCGTTGTCCAAGTGAACAT |
| pHY-qoxA-1 | GCTCTAGAGCGGAATTTCCAATTTCATG |
| pHY-qoxA-2 | TAAATGCTCTGAACAAGAGGATCACGTGTACATTCCTCTC |
| pHY-qoxA-3 | GAGAGGAATGTACACGTGATCCTCTTGTTCAGAGCATTTA |
| pHY-qoxA-4 | AAATCCGTCCTCTCTGCTCTTCTAGTGAGAATCTTGGTCTTCAGA |
| pHY-qoxA-5 | TCTGAAGACCAAGATTCTCACTAGAAGAGCAGAGAGGACGGATTT |
| pHY-qoxA-6 | CGGGATCCGATCACCCGCGATACCGTC |
| pHY-dck-1 | GCTCTAGAGCGGAATTTCCAATTTCATG |
| pHY-dck-2 | CTTTCGGAATAGCATATACACTCATGTGTACATTCCTCTC |
| pHY-dck-3 | GAGAGGAATGTACACATGAGTGTATATGCTATTCCGAAAG |
| pHY-dck-4 | AAATCCGTCCTCTCTGCTCTTTTATCTTTGAATAGCTTCACTG |
| pHY-dck-5 | CAGTGAAGCTATTCAAAGATAAAAGAGCAGAGAGGACGGATTT |
| pHY-dck-6 | CGGGATCCGATCACCCGCGATACCGTC |
| pHY-adk-1 | GCTCTAGAGCGGAATTTCCAATTTCATG |
| pHY-adk-2 | GTCCCATTAAGACTAAGTTCATTTCATGTGTACATTCCTCTC |
| pHY-adk-3 | GAGAGGAATGTACACATGAAATGAACTTAGTCTTAATGGGAC |
| pHY-adk-4 | GTCCGTCCTCTCTGCTCTTTCATTTGTCCCGGCCTCCGA |
| pHY-adk-5 | TCGGAGGCCGGGACAAATGAAAGAGCAGAGAGGACGGAC |
| pHY-adk-6 | CGGGATCCGATCACCCGCGATACCGTC |
| T2-dck-1 | CGGGATCCCGTGATAGGTGGTATGTTTTCG |
| T2-dck-2 | CTTTCGGAATAGCATATACACTCATGTGTACATTCCTCTC |
| T2-dck-3 | GAGAGGAATGTACACATGAGTGTATATGCTATTCCGAAAG |
| T2-dck-4 | AAATCCGTCCTCTCTGCTCTTCTAGTGAGAATCTTGGTCTTCAGA |
| T2-dck-5 | CAGTGAAGCTATTCAAAGATAAAAGAGCAGAGAGGACGGATTT |
| T2-dck-6 | GCTCTAGAGCCGCAATAATGCCGTCGCACTGGC |
| T2-dck-KYF | AGCTTCAATGCTACCCAAGCAGC |
| T2-dck-KYR | GCCTTGTCTGAAATACATATA |
| T2-qoxA-1 | GGACTAGTCC TGATAGGTGGTATGTTTTCGC |
| T2-qoxA-2 | TAAATGCTCTGAACAAGAGGATCACGTGTACATTCCTCTC |
| T2-qoxA-3 | GAGAGGAATGTACACGTGATCCTCTTGTTCAGAGCATTTA |
| T2-qoxA-4 | AAATCCGTCCTCTCTGCTCTTCTAGTGAGAATCTTGGTCTTCAGA |
| T2-qoxA-5 | TCTGAAGACCAAGATTCTCACTAGAAGAGCAGAGAGGACGGATTT |
| T2-qoxA-6 | GAAGATCTTCCGCAATAATGCCGTCGCACTGGC |
| T2-qoxA-KYF | GAGATTATTCGTAAAGCCGAGATG |
| T2-qoxA-KYR | CTGTCTCCCGTGTCTTTACCCG |
表选项
1.2 培养基LB液体培养基:蛋白胨10 g/L、酵母提取物5 g/L、氯化钠10 g/L,pH为7.0–7.2。
LB固体培养基:蛋白胨10 g/L、酵母提取物5 g/L、氯化钠10 g/L、琼脂18 g/L,pH为7.0–7.2。
杆菌肽发酵培养基:玉米淀粉45 g/L、轻钙6 g/L、硫酸铵1 g/L、豆粕100 g/L,自然pH。
1.3 主要试剂Taq DNA聚合酶、Pfu DNA聚合酶、dNTPs购自北京全式金生物科技有限公司;DNA限制性内切酶、T4 DNA连接酶、DNA分子量标准购自宝生物工程(大连)有限公司;质粒小提试剂盒、DNA回收纯化试剂盒购自Omega Bio-tek公司;ATP检测试剂盒购置于碧云天生物技术有限公司;引物合成及序列测定均由北京擎科新业生物技术有限公司完成;蛋白胨、酵母提取物、琼脂糖购自Spanish公司;α-淀粉酶、抗生素(Amp、Kan、Tet)购自阿拉丁试剂(上海)有限公司;豆粕、玉米淀粉、轻钙来源于绿康生化股份有限公司;其他普通试剂(国产分析纯)均购自国药集团化学试剂有限公司。
1.4 地衣芽胞杆菌工程菌株构建1.4.1 地衣芽胞杆菌游离表达菌株构建地衣芽胞杆菌游离表达菌株DW2/pHY-qoxA、DW2/pHY-adk和DW2/pHY-dck的构建方法,以DW2/pHY-qoxA为例。首先,以枯草芽胞杆菌168基因组为模板,使用引物pHY-qoxA-1和pHY-qoxA-2,扩增出P43强启动子。以地衣芽胞杆菌DW2为模板,使用pHY-qoxA-3/4和pHY-qoxA-5/6分别扩增出qoxA基因和amyL终止子。重叠延伸PCR连接启动子、qoxA基因和终止子(pHY-dck-1/6)。随后,用限制性内切酶BamHⅠ/XbaⅠ酶切片段与质粒pHY300PLK,经酶连后转化大肠杆菌,得到游离表达载体pHY-qoxA。随后,pHY-qoxA经电转化至地衣芽胞杆菌DW2中,筛选得到的阳性转化子,即为游离表达菌株DW2/pHY-qoxA。采用同样的方法,构建获得游离表达菌株DW2/pHY-dck和DW2/pHY-adk。
1.4.2 地衣芽胞杆菌基因敲除菌株构建地衣芽胞杆菌基因敲除菌株的构建方法,以cydB缺失的地衣芽胞杆菌DW2ΔcydB构建为例。以地衣芽胞杆菌DW2为模板,使用引物cydB-KF1/KR1和cydB-KF2/KR2分别扩增cydB基因的上游和下游同源臂。重叠延伸PCR连接上下游同源臂。随后,采用内切酶SacⅠ/XbaⅠ酶切穿梭载体T2(2)-Ori和上下游同源臂片段,经酶连、转化大肠杆菌,验证并获得敲除载体T2-ΔcydB。将该载体电转化至地衣芽胞杆菌DW2中,经单-双交换,验证并获得阳性转化子,得到地衣芽胞杆菌cydB基因缺失菌株DW2ΔcydB。
1.4.3 地衣芽胞杆菌基因整合表达菌株构建地衣芽胞杆菌基因整合表达菌株的构建方法可参照基因缺失菌株构建流程:以基因qoxA整合表达菌株构建为例,先以地衣芽胞杆菌DW2为模板,分别扩增出整合载体的上下游同源臂以及qoxA基因表达盒。重叠延伸PCR连接上述3个片段,后经过酶切、酶连构成整合表达载体T2-::qoxA。随后,将整合表达载体T2-::qoxA电转至地衣芽胞杆菌中,经过单双交换,验证并获得地衣芽胞杆菌qoxA基因整合表达菌株。
1.5 杆菌肽发酵种子培养:将保存于超低温冰箱中的菌株稀释涂布于带有相应抗性的固体LB平板上,37 ℃培养12 h,随后挑取单菌落重新活化于相应抗性平板上。挑取平板上长好的单菌落接种于含5 mL液体LB培养基的PA瓶中,230 r/min、37 ℃条件下培养12 h。再以5%接种量转接到含20 mL液体LB培养基的250 mL三角瓶中,230 r/min、37 ℃条件下培养6–7 h后转接至发酵培养基中。
摇瓶发酵培养:种子液以5%接种量接至含20 mL杆菌肽发酵培养基的250 mL三角瓶中,230 r/min、37 ℃条件下培养48 h。随后,测定发酵液pH,pH到8.0时即到发酵终点。发酵中每个菌株均设置3个平行。
1.6 分析方法地衣芽胞杆菌生物量采用稀释涂布法测定。杆菌肽效价检测采用安捷伦1260液相色谱仪完成,色谱柱型号:Eclipse Plus C18 column (4.6 mm×250 mm,3.5 μm),流动相甲醇:乙腈:盐相为60.4:4.6:35,进样体积为20 μL;流速为1 mL/min;柱温为30 ℃;紫外检测器波长为254 nm。胞内ATP浓度使用ATP检测试剂盒测定,ATP检测的取样点为24 h。
杆菌肽合成对数期(30 h)的氨基酸浓度使用安捷伦7890A气相色谱仪测定。对于胞外氨基酸检测的预处理:吸取2 mL发酵液于离心管中,12 000 r/min、4 ℃离心10 min,上清液过膜备用。对于胞内氨基酸检测的预处理:吸取15 mL发酵液于离心管中,1 500 r/min、4 ℃离心10 min。吸取8 mL上清液与10 mL预冷2.5% (W/V)氯化钠迅速混匀,10 000 r/min、4 ℃离心5 min,弃上清;沉淀用10 mL预冷2.5% (W/V)碳酸铵溶液洗涤2次,最后用3 mL预冷80% (V/V)甲醇溶液抽提5 min,上清液冻干后加蒸馏水溶解备用。
衍生化处理:取500 μL样品,加入10 μL的7 mol/L氢氧化钠溶液和500 μL无水乙醇与吡啶混合液(体积比4:1),振荡混匀。加入100 μL氯甲酸乙酯后,超声1 min,重复该操作一次;加入500 μL含1% ECF的氯仿溶液以及200 μL饱和碳酸氢钠溶液,振荡1 min后加入40 μL 1%乙酸苯乙酯。混合物静置5 min,随后3 000 r/min离心5 min,将下层溶液转移到含0.1 g硫酸钠的EP管中。3 000 r/min离心5 min,取上清溶液转移到气相瓶中。
气相色谱检测:色谱柱型号Agilent HP-5 column (30 m×0.32 mm×0.25 μm),检测器温度为280 ℃,进样体积1 μL,气体流速为1.5 mL/min。空气、氢气、氮气流速分别为300 mL/min、30 mL/min、30 mL/min。
1.7 统计分析所有的实验均至少重复3次,每次3个平行。采用Origin 8.5和SPSS 18.0进行数据处理和分析(其中,*表示差异显著(P < 0.05),**表示差异极显著(P < 0.01))。
2 结果与分析2.1 基因cydB缺失对杆菌肽合成的影响之前研究报道指出,枯草芽胞杆菌和地衣芽胞杆菌中均含有4种呼吸链末端氧化酶,分别为细胞色素caa3氧化酶(ctaCDEF编码)、细胞色素bd氧化酶(cydABCD编码)、细胞色素aa3氧化酶(qoxABCD编码)、YthAB氧化酶(ythAB编码)[16-17]。其中细胞色素bd氧化酶较为特殊,该酶不含有转运质子的跨膜通道,每转运1个电子仅能向外转移1个质子,H+/e–为1[21-22]。因此,这条分支途径通常被认为是能耗比较高的途径(图 1)。本研究中,我们通过构建cydB基因敲除载体,得到了cydB基因缺失菌株DW2ΔcydB。随后,将DW2和DW2ΔcydB分别接种于LB培养基中,通过检测二者生长曲线发现,cydB缺失后细胞生长速率快于野生菌(图 2A)。结合之前的文献报道,说明cydB缺失降低了菌体维持代谢能,有利于菌体生长。
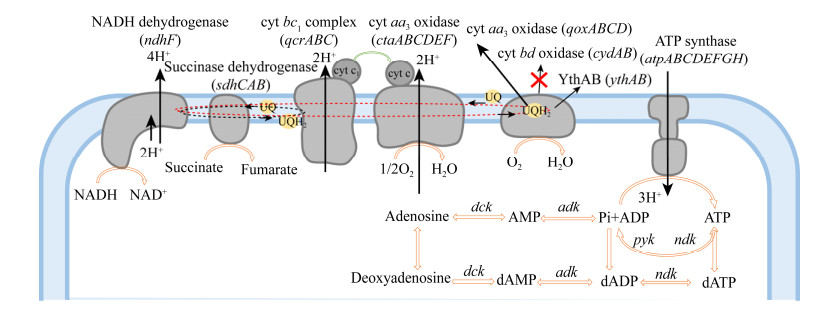 |
| 图 1 地衣芽胞杆菌DW2呼吸电子传递链 Fig. 1 Respiratory electron transport chain of Bacillus licheniformis DW2. |
| 图选项 |
 |
| 图 2 cydB缺失对细胞生长、杆菌肽效价及胞内ATP含量的影响 Fig. 2 Effects of deleting cydB on cell growth, bacitracin titer and intracellular ATP contents. (A) The growth curves in LB medium. (B) Bacitracin titers and biomass. (C) The intracellular ATP contents at 24 h. *P < 0.05; **P < 0.01. |
| 图选项 |
随后,将DW2和DW2ΔcydB分别接种于杆菌肽发酵培养基中。分别检测其最高生物量、杆菌肽效价和胞内ATP浓度。由图 2B可知,DW2最大生物量(24 h)为413.54×108 CFU/mL,cydB缺失菌株生物量为431.35×108 CFU/mL,提高了4.31%。cydB缺失有利于杆菌肽合成,其杆菌肽最高效价(48 h)提高了10.97%。DW2ΔcydB单位菌体杆菌肽效价为2.02×10–8 U/CFU,相比于对照菌株(1.90×10–8 U/CFU)提高了6.87%。此外,通过对二者胞内ATP含量(24 h)检测发现,DW2ΔcydB中胞内ATP浓度达到32.56 nmol/L,相比于对照菌株(26.48 nmol/L)提高了22.96% (图 2C)。由此可见,缺失cydB可以提高胞内ATP供给水平,进而有利于杆菌肽高产。
2.2 强化表达qoxA基因对杆菌肽合成影响之前的研究中,人们指出细胞色素bd氧化酶和aa3氧化酶是芽胞杆菌中主要的两条呼吸链分支途径。人们之前已证实细胞色素bd氧化酶途径是能耗比较高的途径,并通过缺失cydB提高了相关代谢产物的合成水平[16-17, 21]。然而,细胞色素aa3氧化酶与代谢产物合成的关系并未有人研究。本研究中,我们分别构建了qoxA缺失及强化表达菌株DW2ΔqoxA和DW2/pHY-qoxA。
如图 3A所示,缺失qoxA基因后,细胞生物量有所降低,相比于对照菌株下降了11.46%。而强化表达qoxA则能够显著提高菌体生长水平。随后,将上述4种菌分别接种于杆菌肽发酵培养基中,摇瓶发酵结果表明,qoxA缺失菌株杆菌肽最高效价(48 h)为693.24 U/mL,相比于对照降低了11.61%,强化表达qoxA有利于杆菌肽合成,其杆菌肽效价相比于对照提高了18.27%,单位菌体杆菌肽效价提高了11.13%。此外,通过对胞内ATP含量检测发现,qoxA强化表达菌株的ATP浓度(24 h)达到27.67 nmol/L,相比于对照菌株DW2/pHY300 (20.65 nmol/L)提高了34.00% (图 3)。综上,细胞色素aa3氧化酶在地衣芽胞杆菌呼吸链代谢中发挥着重要作用,强化表达qoxA有利于ATP供给和杆菌肽合成。
 |
| 图 3 缺失/强化表达qoxA对细胞生长、杆菌肽效价及胞内ATP浓度的影响 Fig. 3 Effects of deleting or overexpressing qoxA on cell growth, bacitracin titer and intracellular ATP content. (A) The growth curves in LB medium. (B) Bacitracin titers and biomass. (C) ATP contents at 24 h. *P < 0.05; **P < 0.01. |
| 图选项 |
2.3 强化表达dck基因提高杆菌肽合成水平ADP供给水平对于胞内ATP积累及代谢产物合成意义重大。为提高ADP合成水平进而提高胞内ATP浓度,我们通过构建腺苷激酶DcK、腺苷酸激酶AdK游离表达载体,分别构建了dck和adk过表达菌株DW2/pHY-dck和DW2/pHY-adk (图 1)。发酵结果表明,过表达dck和adk均可以增强细胞内ATP供给水平,同时杆菌肽效价相比于对照菌株也有一定提升,其中强化表达dck的效果较好,其杆菌肽效价相比于对照菌株提高了16.78%,单位菌体杆菌肽合成水平提高了12.48% (图 4)。
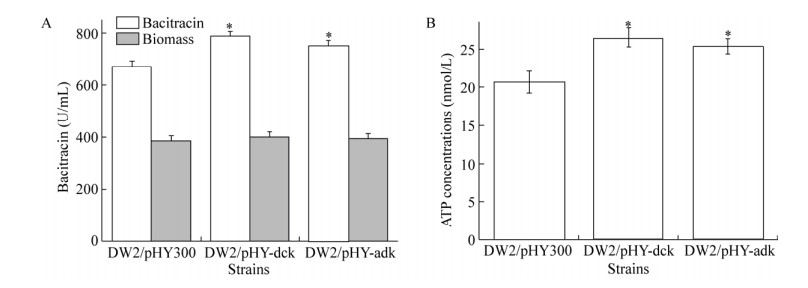 |
| 图 4 强化ATP合成途径对生物量、杆菌肽效价、胞内ATP浓度的影响 Fig. 4 Effects of enhancing ATP supply on biomass, bacitracin titer and intracellular ATP content. (A) Bacitracin titers and biomass. (B) ATP contents. *P < 0.05; **P < 0.01. |
| 图选项 |
2.4 组合代谢工程育种构建杆菌肽高产菌株为进一步提高杆菌肽合成水平,在明确单基因工程菌株发酵效果的基础上,我们通过组合代谢工程育种,进一步构建杆菌肽高产地衣芽胞杆菌工程菌株。首先,通过构建qoxA基因整合表达载体,在DW2ΔcydB中成功整合表达了qoxA,得到工程菌株DW2-CQ (DW2ΔcydB::qoxA)。发酵结果表明,DW2-CQ杆菌肽效价(48 h)达到904.35 U/mL,相比于对照菌株DW2和DW2ΔcydB分别提高了15.30%和3.96%,胞内ATP含量(24 h)分别提高了33.80%和8.81%。随后,在DW2-CQ基础上进一步整合表达了dck,得到工程菌株DW2-CQD (DW2ΔcydB::qoxA::dck)。DW2-CQD杆菌肽效价达到954.25 U/mL,相比于DW2提高了21.66%,DW2-CQD单位菌体杆菌肽效价达到2.11 U/CFU,相比于对照(1.90 U/CFU)提高了11.05%。DW2-CQD最高生物量为451.53×108 CFU/mL,相比于DW2提高了9.19%,DW2-CQD最高ATP浓度为39.54 nmol/L,相比于DW2提高了49.32% (表 3)。
表 3 工程菌株的杆菌肽效价、单位菌体杆菌肽效价、生物量和ATP浓度Table 3 Bacitracin titers, bacitracin titers of per cell, biomass and ATP contents of recombinant strains
| Strains | Bacitracin titers (U/mL) | Bacitracin titers of per cell (U/CFU) | Biomass (108 CFU/mL) | ATP contents (nmol/L) |
| DW2 | 784.34±23.43 | 1.90±0.02 | 413.54±15.43 | 26.48±1.43 |
| DW2△cydB | 874.35±18.76 | 2.02±0.03 | 431.35±16.53 | 32.56±1.52 |
| DW2-BQ | 904.35±21.54 | 2.05±0.02 | 441.54±18.54 | 35.43±1.74 |
| DW2-BQD | 954.25±22.25 | 2.11±0.02 | 451.53±19.34 | 39.54±0.56 |
表选项
随后,我们进一步检测了菌株DW2和DW2-CQD的杆菌肽合成曲线。由图 5可知,DW2-CQD的杆菌肽效价在整个发酵过程中均高于对照菌株,最高值相比对照提高了21.66%。
 |
| 图 5 DW2和DW2-CQD的杆菌肽合成曲线 Fig. 5 The bacitracin synthesis curves of DW2 and DW2-CQD. |
| 图选项 |
紧接着,我们检测了菌株DW2和DW2-CQD在杆菌肽合成对数期(30 h)的胞内外前体氨基酸浓度。如图 6所示,强化ATP供给有利于杆菌肽合成,因此杆菌肽前体氨基酸如异亮氨酸、亮氨酸、半胱氨酸、赖氨酸等胞内浓度均有所下降,此外,其胞外前体氨基酸(异亮氨酸、缬氨酸、亮氨酸、半胱氨酸、赖氨酸)浓度低于对照菌株。由此说明,更多的前体氨基酸被用于杆菌肽的生物合成,导致DW2-CQD中前体氨基酸浓度相比于对照有所降低。
 |
| 图 6 DW2和DW2-CQD的胞内外前体氨基酸浓度 Fig. 6 The intracellular and extracellular concentrations of precursor amino acids of DW2 and DW2-CQD. (A) Intracellular. (B) Extracellular. *P < 0.05; **P < 0.01. |
| 图选项 |
3 结论与展望本研究以工业生产菌株地衣芽胞杆菌DW2为出发菌株,针对目标产物杆菌肽合成过程中ATP供给不足的难题,通过优化呼吸链分支途径、强化ATP合成途径等策略,获得了工程菌株DW2-CQD,与对照菌株DW2相比,该菌株胞内ATP含量和杆菌肽合成水平均显著提高。
芽胞杆菌是一种重要的工业微生物生产菌株,其可以合成具有应用价值的化工产品,如聚γ-谷氨酸、透明质酸、乙偶姻、丁二醇等,也可以作为蛋白表达宿主,用于异源蛋白(酶蛋白和活性多肽等)高效生产。然而,芽胞杆菌高的维持代谢能是限制其代谢产物高效生产的重要限制因素。人们之前的研究已证实,芽胞杆菌呼吸链有4条分支途径,分别为细胞色素bd氧化酶、细胞色素caa3氧化酶、细胞色素aa3氧化酶及通过序列比对获得的YthAB。其中,细胞色素bd氧化酶途径被认为是能耗比较高的途径,之前的研究中,人们通过阻断细胞色素bd氧化酶分支途径,减低芽胞杆菌维持代谢能,进而提高了核黄素、N-乙酰氨基葡萄糖、聚γ-谷氨酸等产物合成水平。然而,另外3条途径在细胞维持能代谢调节方面的功能并不清楚。本研究通过对细胞色素aa3氧化酶的功能进行初步研究,发现细胞色素aa3氧化酶表达对于菌体生长及产物合成十分重要,强化表达细胞色素aa3氧化酶有利于杆菌肽合成和胞内ATP积累。之前研究已证实细胞色素bd氧化酶和aa3氧化酶是芽胞杆菌呼吸链的主要分支途径,而本研究的结果表明,与细胞色素bd氧化酶不同,细胞色素aa3氧化酶则是能耗比较低的分支途径。因此,细胞色素aa3氧化酶可以作为代谢工程改造的靶位点用于目的产物高产菌株的代谢工程育种。此外,尽管本课题之前的研究发现阻断ythAB表达也会使得聚γ-谷氨酸产量下降[18],但YthAB氧化酶与细胞代谢维持能及目的产物合成的关系尚待研究。
本研究通过敲除细胞色素bd泛醇氧化酶亚基cydB、强化表达细胞色素aa3氧化酶亚基qoxA,优化了地衣芽胞杆菌呼吸链途径,通过强化表达腺苷激酶基因dck提高了ADP合成水平。通过上述策略,胞内ATP含量达到39.54 nmol/L,相比于对照提高了49.32%,工程菌株DW2-CQD杆菌肽产量达到954.25 U/mL,相比于对照提高了21.66%。本研究证实能量代谢工程是提高杆菌肽合成水平的有效策略,同时提供了一株具有工业化应用前景的杆菌肽生产菌株。
参考文献
| [1] | Drabl?s F, Nicholson DG, Ronning M. EXAFS study of zinc coordination in bacitracin A. Biochim Biophy Acta, 1999, 1431(2): 433-442. DOI:10.1016/S0167-4838(99)00064-3 |
| [2] | Haavik HI. Studies on the formation of bacitracin by Bacillus licheniformis: effect of glucose. J Gen Microbiol, 1974, 81(2): 383-390. |
| [3] | Lin G. Determination of amino acid and inorganic ions in culture and its application in bacitracin fermentation process[D]. Shanghai: Shanghai Institute of Pharmaceutical Industry, 2006 (in Chinese). 林纲.杆菌肽发酵过程中氨基酸等成分的测定方法研究和应用[D].上海: 上海医药工业研究院, 2006. http://cdmd.cnki.com.cn/Article/CDMD-85901-2007015526.htm |
| [4] | Li Y, Wu F, Cai DB, et al. Enhanced production of bacitracin by knocking out of amino acid permease gene yhdG in Bacillus licheniformis DW2. Chin J Biotech, 2018, 34(6): 916-927 (in Chinese). 李阳, 吴非, 蔡冬波, 等. 地衣芽胞杆菌DW2中敲除氨基酸转运蛋白基因yhdG提高杆菌肽产量. 生物工程学报, 2018, 34(6): 916-927. |
| [5] | Bernard R, El Ghachi M, Mengin-Lecreulx D, et al. BcrC from Bacillus subtilis Acts as an undecaprenyl pyrophosphate phosphatase in bacitracin resistance. J Biol Chem, 2005, 280(32): 28852-28857. DOI:10.1074/jbc.M413750200 |
| [6] | Hancock RE. Mechanisms of action of newer antibiotics for Gram-positive pathogens. Lancet Infect Dis, 2005, 5(4): 209-218. |
| [7] | Zou FQ, Zeng D, Wen B, et al. Illumina Miseq platform analysis caecum bacterial communities of rex rabbits fed with different antibiotics. AMB Express, 2016, 6: 100. DOI:10.1186/s13568-016-0273-1 |
| [8] | Cai DB, Zhu J, Zhu S, et al. Metabolic engineering of main transcription factors in carbon, nitrogen, and phosphorus metabolisms for enhanced production of bacitracin in Bacillus licheniformis. ACS Synth Biol, 2019, 8(4): 866-875. |
| [9] | Konz D, Klens A, Sch?rgendorfer K, et al. The bacitracin biosynthesis operon of Bacillus licheniformis ATCC 10716: molecular characterization of three multi-modular peptide synthetases. Chem Biol, 1997, 4(12): 927-937. |
| [10] | Hur GH, Vickery CR, Burkart MD. Explorations of catalytic domains in non-ribosomal peptide synthetase enzymology. Nat Prod Rep, 2012, 29(10): 1074-1098. DOI:10.1039/c2np20025b |
| [11] | Winn M, Fyans JK, Zhuo Y, et al. Recent advances in engineering nonribosomal peptide assembly lines. Nat Prod Rep, 2016, 33(2): 317-347, doi: 10.1039.C5NP00099H. |
| [12] | Cai DB. Metabolic regulation mechanism and cofactor energy engineering for high-level productionof poly-γ-glutamic acid in Bacillus licheniformis[D]. Wuhan: Hubei University, 2018 (in Chinese). 蔡冬波.地衣芽胞杆菌高产聚γ-谷氨酸的代谢调控及辅酶能量工程[D].武汉: 湖北大学, 2018. http://cdmd.cnki.com.cn/Article/CDMD-10512-1018262975.htm |
| [13] | Wang JY, Zhu SG, Xu CF. Essential biochemistry. Beijing: Higher Education Press, 2008: 624-629 (in Chinese). 王镜岩, 朱圣庚, 许长发. 生物化学教程. 北京: 高等教育出版社, 2008: 624-629. |
| [14] | Lu JF, Zhu Y, Sun HL, et al. Highly efficient production of hyaluronic acid by Streptococcus zooepidemicus R42 derived from heterologous expression of bacterial haemoglobin and mutant selection. Lett Appl Microbiol, 2016, 62(4): 316-322. DOI:10.1111/lam.12546 |
| [15] | Zhu J, Cai DB, Xu HX, et al. Enhancement of precursor amino acid supplies for improving bacitracin production by activation of branched chain amino acid transporter BrnQ and deletion of its regulator gene lrp in Bacillus licheniformis. Synth Syst Biotechnol, 2018, 3(4): 236-243. DOI:10.1016/j.synbio.2018.10.009 |
| [16] | Zamboni N, Mouncey N, Hohmann HP, et al. Reducing maintenance metabolism by metabolic engineering of respiration improves riboflavin production by Bacillus subtilis. Metab Eng, 2003, 5(1): 49-55. |
| [17] | Liu YF, Zhu YQ, Ma WL, et al. Spatial modulation of key pathway enzymes by DNA-guided scaffold system and respiration chain engineering for improved N-acetylglucosamine production by Bacillus subtilis. Metab Eng, 2014, 24: 61-69. |
| [18] | Cai DB, Chen YZ, He PH, et al. Enhanced production of Poly-γ-glutamic acid by improving ATP supply in metabolically engineered Bacillus licheniformis. Biotechnol Bioeng, 2018, 115(10): 2541-2553. DOI:10.1002/bit.26774 |
| [19] | Zhao J, Li QY, Sun T, et al. Engineering central metabolic modules of Escherichia coli for improving β-carotene production. Metab Eng, 2013, 17: 42-50. DOI:10.1016/j.ymben.2013.02.002 |
| [20] | Wang Q, Zheng H, Wan X, et al. Optimization of inexpensive agricultural by-products as raw materials for bacitracin production in Bacillus licheniformis DW2. Appl Biochem Biotechnol, 2017, 183(4): 1146-1157. DOI:10.1007/s12010-017-2489-1 |
| [21] | Von Wachenfeldt C, Hederstedt L. Respiratory cytochromes, other heme proteins, and heme biosynthesis//Sonenshein AL, Hoch JA, Losick R, Eds. Bacillus subtilis and Its Closest Relatives: from Genes to Cells. Washington: ASM Press, 2002: 163-179. |
| [22] | Trumpower BL, Gennis RB. Energy transduction by cytochrome complexes in mitochondrial and bacterial respiration: The enzymology of coupling electron transfer reactions to transmembrane proton translocation. Annu Rev Biochem, 1994, 63: 675-716. DOI:10.1146/annurev.bi.63.070194.003331 |
