 , 罗敏3
, 罗敏3
 , 刘育秀1,2, 谭季1,2, 黄佳芳1,2
, 刘育秀1,2, 谭季1,2, 黄佳芳1,21. 福建师范大学地理科学学院, 福州 350007;
2. 福建师范大学, 湿润亚热带生态地理过程教育部重点实验室, 福州 350007;
3. 福州大学环境与安全工程学院, 福州 350116
收稿日期: 2021-07-04; 修回日期: 2021-09-08; 录用日期: 2021-09-08
基金项目: 国家自然科学基金面上项目(No.32071598, 41877335);福建省自然科学基金(No.2019J02008, 2020J01503);福建省林业科技项目(No.201935, 2021FKJ31)
作者简介: 孙一萍(1997—), 女, E-mail: 995986026@qq.com
通讯作者(责任作者): 罗敏, E-mail: luomin@fzu.edu.cn
摘要:选取中国东南沿海闽江河口潮汐淡水沼泽湿地土壤作为研究对象, 研究不同盐分(淡水对照、低盐处理、高盐处理)和不同淹水(CK、CK+15 cm、CK+30 cm)交互处理对土壤磷形态和磷酸酶活性的影响.结果表明, 在闽江河口潮汐淡水沼泽湿地土壤中, 无机磷是土壤总磷的主要赋存形态, 约占总磷含量的68%~82%, 有机磷含量约占总磷的18%~32%.无机磷以铁铝结合态磷为主(60%~66%), 其次为钙结合态磷和闭蓄态磷.淹水处理对磷的总量和形态的影响有限, 盐分变化对磷的总量和形态影响显著.低盐处理可增加铁铝结合态磷、闭蓄态磷含量及碱性磷酸酶活性, 而高盐处理则对它们表现出抑制作用.随着盐分的增加, 土壤总磷含量逐渐降低, 土壤中钙结合态磷含量和磷酸盐含量将逐渐升高.相关分析表明, 有机磷含量与土壤碱性磷酸酶活性呈负相关, 无机磷含量与土壤碱性磷酸酶活性呈正相关.当盐分由淡水变化至低盐时, 土壤磷的形态主要由有机磷向无机磷转化; 而当盐分由低盐变化至高盐时, 无机磷占比降低, 有机磷占比增加.研究结果表明, 碱性磷酸酶活性在磷形态对盐分和淹水的响应中发挥着重要作用.
关键词:盐分淹水磷形态磷酸酶活性潮汐淡水沼泽湿地闽江河口
Effects of increasing salinity and flooding on soil phosphorus speciation and phosphorus-acquiring enzyme activities in the tidal freshwater wetland soils of the Min River Estuary, southeast China
SUN Yiping1,2
 , LUO Min3
, LUO Min3
 , LIU Yuxiu1,2, TAN Ji1,2, HUANG Jiafang1,2
, LIU Yuxiu1,2, TAN Ji1,2, HUANG Jiafang1,21. School of Geographical Sciences, Fujian Normal University, Fuzhou 350007;
2. Key Laboratory of Humid Subtropical Eco-geographical Process, Ministry of Education, Fujian Normal University, Fuzhou 350007;
3. College of Environment and Safety Engineering, Fuzhou University, Fuzhou 350116
Received 4 July 2021; received in revised from 8 September 2021; accepted 8 September 2021
Abstract: In the present study, we established mesocosms loaded with soil from a tidal freshwater wetland of the Min River Estuary, southeast China, and subjected them to three salinity treatments (fresh control, oligohaline, mesohaline) and three flooding treatments (control, control+15 cm, control+30 cm) treatments. Thereafter, we simultaneously assessed the abundance and speciation of phosphorus (P) and P-acquiring enzyme activities. In general, the contents of organic P accounted for approximately 68%~82% of total P, whereas those of inorganic P accounted for approximately 18%~32% of total P. Moreover, iron/aluminum bound P (Fe/Al-P) was the main component (approximately 60%~66%) of inorganic P, followed by calcium bound P and occluded P. Salinity had remarkable impact on the abundance and speciation of P, whereas flooding treatments revealed limited effect. Oligohaline treatment increased the contents of Fe/Al-P and occluded P and alkaline phosphatase activities, whereas mesohaline treatment decreased these contents. As salinity increased, the total P contents and acid phosphatase activities decreased; however, the calcium bound P contents and porewater phosphate concentrations increased. This study revealed that organic and inorganic P contents exhibited negative and positive correlation with alkaline phosphatase activities, respectively. When the salinity changed from freshwater to oligohaline, few parts of organic P transformed into inorganic P. Furthermore, when the salinity changed from oligohaline to mesohaline, the importance of inorganic P decreased, whereas that of organic P increased. Thus, this study highlighted the importance of phosphorus-acquiring enzyme activities on the feedbacks of abundance and speciation of P toward increasing salinity and flooding in tidal freshwater wetland soils.
Keywords: salinityfloodingphosphorus speciationphosphatase activitytidal freshwater wetlandMin River Estuary
1 引言(Introduction)磷(P)是决定湿地植物初级生产力的关键要素, 并在湿地生态系统服务功能的调节中发挥着重要作用(Vitousek et al., 2010; 张仲胜等, 2016; Lin et al., 2016).湿地土壤中的总磷(TP)可分为有机磷(OP)和无机磷(IP).根据土壤中不同性质的含磷矿物盐, 可将土壤无机磷(IP)进一步划分为铁铝结合态磷(Fe/Al-P)、钙结合态磷(Ca-P)、闭蓄态磷(O-P)和残渣态磷(Hedley et al., 1982; Zhou et al., 2016).不同形态磷的迁移、转化对湿地生态系统健康和邻近区域的水质有着重要的影响.因此, 湿地磷的形态及其变化特征成为当前学界关注和研究的重点(Reddy et al., 2008; Gao et al., 2012; Zhi et al., 2012).
河口沼泽湿地是重要的磷蓄积库, 也是磷的源、汇和转换器(Wu et al., 2008).同时, 河口沼泽湿地位于海陆交界处, 是受海平面上升影响最直接、最敏感的生态系统(Sun et al., 2014).目前, 全球海平面上升速度为3.1~4.3 mm·a-1(IPCC, 2019), 海平面上升带来的盐分和淹水增加将对河口潮汐淡水沼泽湿地土壤磷循环产生重要的影响.
盐分和淹水是河口潮汐淡水沼泽湿地土壤磷循环的关键影响因子(Liu et al., 2002; Jun et al., 2013).盐水中的阴离子(Cl-和SO42-)会与磷酸盐(PO43-)离子竞争土壤颗粒上的结合位, 从而影响土壤磷的吸附能力(Bruland et al., 2009).Liu等(2002)研究发现, 河口潮汐沼泽湿地磷的吸附能力在低盐条件下增加, 而在高盐条件下, 随着盐分的增加, 磷的吸附能力逐渐降低并导致总磷含量下降.在我国黄河三角洲的研究表明, 盐水中的硫化物会减少河口潮汐沼泽湿地土壤中铁矿物对磷的吸附作用, 从而减少土壤无机磷的含量(Bai et al., 2017).淹水条件的改变也会影响土壤有机磷的矿化分解和土壤含磷矿物质的溶解沉淀过程(Reddy et al., 2008).在美国Everglades淡水湿地的研究表明, 淹水增加显著提高了土壤中Ca2+的含量, 从而促进土壤中钙结合态磷及总磷含量的增加(Newman et al., 2001).对水稻田淹水后磷的形态和含量调查研究表明, 淹水后, 氧化还原电位下降促进了土壤中磷的解吸, 导致无机磷含量显著降低(薄录吉等, 2011).目前, 学界对盐分和淹水变化对河口潮汐淡水沼泽湿地土壤磷循环的影响研究, 多关注各形态磷的吸附与解吸过程发生的变化(Price et al., 2010; Sun et al., 2012; Gilbert et al., 2014).盐分和淹水也将影响酸性磷酸酶(ACP)和碱性磷酸酶(AKP)等土壤磷酸酶的活性(Morrissey et al., 2014).磷酸酶的活性与土壤有机磷矿化和无机磷释放密切相关, 从而也能够影响河口潮汐沼泽湿地土壤磷的形态(Quan et al., 2010; Chambers et al., 2012).但目前尚未有文献关注盐分和淹水条件变化下, 磷酸酶活性变化对磷形态迁移和转换产生的影响.因此, 厘清不同形态磷及磷酸酶活性的变化对盐分和淹水的响应, 对进一步了解未来海平面上升背景下河口潮汐淡水沼泽湿地土壤磷的迁移和转换机制有着重要的意义.
受海平面上升的影响, 未来50年和100年时间内, 全球河口潮汐淡水沼泽湿地平均淹水高度将分别增加15 cm和30 cm, 而盐分增幅范围则分别为 < 5‰和5‰~10‰(Woodroffe et al., 2012; Herbert et al., 2015; Tully et al., 2019).盐分和淹水变化对河口潮汐淡水沼泽湿地磷形态的迁移和转换的影响, 目前尚无定论.鉴于此, 本研究选取我国闽江河口潮汐淡水沼泽湿地土壤作为研究对象, 利用模拟潮汐池装置, 研究不同盐分(淡水对照、低盐处理、高盐处理)和淹水处理(CK、CK+15 cm、CK+30 cm)对短叶茳芏(Cyperus malaccensis)沼泽湿地土壤磷形态和磷酸酶活性的影响, 以期明晰未来海平面上升情境下亚热带河口潮汐淡水沼泽湿地土壤磷素的迁移和归趋.
2 材料与方法(Materials and methods)2.1 研究区概况本研究所用土壤和植物均采集自我国东南沿海闽江河口塔礁洲潮汐淡水沼泽湿地(25°56′56″~25°57′36″ N, 119°19′55″~119°22′45″ E).研究区属亚热带海洋性季风气候, 气候温暖湿润, 年均温为21.2 ℃, 潮汐类型为典型半日潮, 每次涨潮淹水时间平均为3~4 h.该地区植物群落优势种为短叶茳芏(Cyperus malaccensis), 该植物具有较强的盐分(盐分耐受范围0~10‰)及淹水耐受性(每日淹水时间可达10 h).研究区土壤盐分为0.4‰±0.2‰, 土壤为粉砂质壤土(粘粒为9.85%~12.02%, 粉粒为46.00%~52.75%, 砂粒为36.36%~42.87%).
2.2 实验设计为揭示盐分和淹水变化对河口潮汐淡水沼泽湿地土壤磷形态和磷酸酶活性的影响, 实验设置3种水平的盐分处理(淡水对照、低盐处理、高盐处理)及3种水平的淹水处理(CK、CK+15 cm、CK+30 cm)交互作用的9种处理(图 1), 每个处理设置3个重复.淹水处理(CK)基于研究区的基本水文特征(日均淹水高度)进行设置.淹水处理(CK+15 cm)和(CK+30 cm)分别模拟3.1 mm·a-1的海平面上升速度下, 未来50年和100年的海平面上升造成的潮汐淡水沼泽湿地淹水增加的高度(IPCC, 2019).淡水对照(0.4‰)以研究区周围土壤盐分为依据进行设置.低盐处理(2.4‰)和高盐处理(8.2‰)分别模拟未来50年和100年全球河口潮汐淡水沼泽湿地因海平面上升可达到的平均盐渍化程度(Woodroffe et al., 2012; Herbert et al., 2015; Tully et al., 2019).
图 1(Fig. 1)
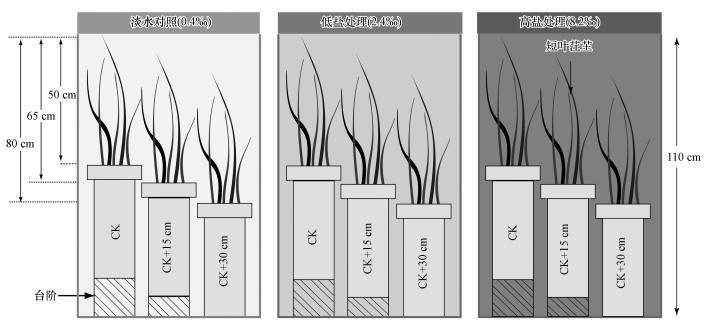 |
| 图 1 模拟潮汐池与实验设计示意图 Fig. 1Illustration of stimulated tidal pool and experiment designs in this study |
2.3 实验装置和实验准备本实验中淹水水位由模拟潮汐池控制.模拟潮汐池由主池、水泵和储水桶组成, 水位控制通过定时开关控制水泵实现, 每日各涨、落潮2次模拟闽江河口半日潮潮汐.在3个潮汐池中, PVC管排成3排, 从高到低分别为处理CK、CK+15 cm、CK+30 cm, 高度差均为15 cm(图 1).盐水由海盐配置(中国海洋生物技术股份有限公司), 含22.5% Cl-、3.9% SO42-、15.3% Na+、1.9% Mg2+、0.5% K+、0.5% Ca2+等, 并利用Salt 6+盐度计(Eutech, 美国)测定其盐分.
于2017年1月原位采集闽江河口塔礁洲潮汐淡水沼泽湿地0~20 cm的表层土壤.所采土壤均过2 mm筛, 剔除其中的根系枯落物和其他杂质, 将土壤充分混匀, 以降低土壤异质性.混匀后土壤装入PVC管中(高度30 cm、内径10 cm).将所有PVC管的顶部覆盖黑色塑料薄膜, 并在水中放置2个月.于2017年3月, 从研究区采集短叶茳芏幼苗(高度均为10~15 cm), 按照短叶茳芏幼苗的天然密度((521±37)株·m-2)种植于PVC管中.模拟潮汐池从2017年3月开始运行, 于2019年7月正式结束.
2.4 测定方法于2019年7月采集土壤和植物样品.植物生物量采用收获法测定.采集后, 将地上和地下部分分别装入孔径为1 mm的尼龙网内洗净, 在105 ℃下杀青30 min, 并在65 ℃下烘干至恒重并称重以计算其生物量.
土壤PO43-浓度使用SKALAR SAN++连续流动分析仪(SKALAR, 荷兰)测定(检测限分别为3 μmol·L-1).土壤SO42-浓度使用ICS-2100离子色谱仪(DIONEX, 美国)测定(检测限为0.09 mg·L-1).土壤Fe(Ⅲ)采用改进的连续浸提法(Bonneville et al., 2009), 其中, 无定形Fe(Ⅲ)和晶质态Fe(Ⅲ)分别利用浓度为0.5 mol·L-1的HCl与10 mg·L-1的羟胺混合液, 以及CBD溶液(0.35 mol·L-1冰醋酸和0.2 mol·L-1柠檬酸钠混合液混合50 mg·L-1连二亚硫酸钠缓冲液)进行浸提(Johnston et al., 2014;Luo et al., 2014).土壤Fe(Ⅲ)含量为无定形Fe(Ⅲ)和晶质态Fe(Ⅲ)含量之和.铁含量利用UV-2450紫外可见分光光度计(岛津, 日本)测定.
土壤总磷含量采用浓H2SO4-HClO4消煮法(Parkinson et al., 1975)测定;无机磷含量采用1 mol·L-1的HCl溶液振荡浸提16 h后离心、过滤并抽取上清液进行测定(Chang et al., 1975);有机磷含量为总磷与无机磷的差值.无机磷采用连续分级法进一步分为铁铝结合态磷、钙结合态磷和闭蓄态磷(Chang et al., 1957).其中, 铁铝结合态磷用1 mol·L-1的NaOH溶液及3.5 mol·L-1的HCl溶液浸提, 剧烈摇晃20 s后静置过夜, 离心、过滤后测定.钙结合态磷(Ca-P)用0.5 mol·L-1的H2SO4溶液浸提, 在室温内振荡、离心后提取.闭蓄态磷用0.3 mol·L-1柠檬酸钠溶液、0.5 mol·L-1NaOH溶液及20 g·L-1连二亚硫酸钠Na2S2O4, 水浴(80~90 ℃)冷却、离心后加入H2SO4:HClO4:HNO3(1:2:7)三酸混合物提取.上述浸提液中的磷含量使用SKALAR SAN++连续流动分析仪(SKALAR, 荷兰)测定(检测限为3 μmol·L-1).
土壤酸性磷酸酶和碱性磷酸酶活性参照Saiya-Cork(2002)的方法测定.使用伞形酮MUB作标示底物, 称取1 g土壤置于内含pH值分别为5.0和11.0的醋酸缓冲液的广口瓶中, 使用磁力搅拌器搅拌5 min后移取200 μL悬浮液至96孔微孔板(PerkinElmer, 美国).在20 ℃下遮光培养4 h后, 向每个微孔板中加入10 μL浓度为1 mol·L-1的NaOH溶液, 使其停止反应.用Synergy H4多功能酶标仪(BioTek, 美国)测定荧光度, 用阴性对照和淬火标准液校正后, 以每克干物质每小时产生底物的摩尔数(nmol·g-1·h-1)计算土壤磷酸酶活性.
2.5 数据处理所有数据均进行方差齐次性检验和正态分布检验, 对不符合正态分布的数据采用log转置处理, 采用SPSS 22.0软件中的双因素方差分析(Two-way ANOVA)检验盐分和淹水对土壤磷形态和磷酸酶活性的影响.对于有显著性差异的结果(p < 0.05), 采用Tukey事后检验分析其组间差异.采用Pearson相关分析检验不同形态磷与磷酸酶活性及土壤理化指标的相关关系.数据分析显著性水平为α=0.05, 相关数据均以平均值(Mean)±标准差(Standard deviation)的形式表示.
3 结果与分析(Results and analysis)3.1 盐分和淹水变化对植物生物量和土壤理化指标的影响由表 1可知, 盐分处理会显著改变沼泽植物生物量.盐分增加显著减少了地上生物量(p < 0.001);相对于淡水对照, 高盐处理降低了地下生物量, 而低盐处理却增加了地下生物量(p < 0.001).淹水处理对地上和地下生物量均无显著影响(p>0.05).
表 1(Table 1)
| 表 1 不同盐分和淹水处理下闽江河口潮汐淡水沼泽湿地植物生物量和土壤理化指标 Table 1 Plant biomass and soil physicochemical properties across salinity and flooding treatments in the tidal freshwater wetland soils of the Min River Estuary, southeast China | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 1 不同盐分和淹水处理下闽江河口潮汐淡水沼泽湿地植物生物量和土壤理化指标 Table 1 Plant biomass and soil physicochemical properties across salinity and flooding treatments in the tidal freshwater wetland soils of the Min River Estuary, southeast China
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
不同处理下, 土壤Fe(Ⅲ)含量由(31.61±2.47) μmol·g-1变化至(61.34±3.18) μmol·g-1(表 1).盐分处理对土壤Fe(Ⅲ)的含量影响显著(p < 0.001), 相对于淡水对照, 低盐处理增加了Fe(Ⅲ)含量, 而高盐处理降低了Fe(Ⅲ)含量.土壤SO42-浓度由(0.09±0.09) mmol·L-1变化至(10.12±0.91) mmol·L-1, 土壤PO43-浓度由(15.73±2.50) mmol·L-1变化至(26.45±5.59) mmol·L-1.随着盐分的增加, 土壤SO42-和PO43-浓度增加(p < 0.05).淹水处理对土壤Fe(Ⅲ)含量及O42-与PO43-浓度的影响不显著(p>0.05).
3.2 盐分和淹水变化对土壤不同形态磷的影响不同处理下, 土壤总磷含量由(663.67±8.08) mg·kg-1变化至(771.33±37.11) mg·kg-1(图 2a).随着土壤盐分的增加, 土壤总磷含量逐渐减少.土壤无机磷占总磷含量的比例为68%~82%, 而土壤有机磷占总磷含量的比例为18%~32%.盐分处理对土壤有机磷和无机磷均有显著影响(p < 0.001)(图 2b和2c), 相对于淡水对照, 低盐处理降低了土壤有机磷含量, 但增加了土壤无机磷含量;高盐处理增加了土壤有机磷含量, 但降低了土壤无机磷含量.淹水处理对土壤总磷、有机磷和无机磷含量的影响不显著(图 2a~2c).
图 2(Fig. 2)
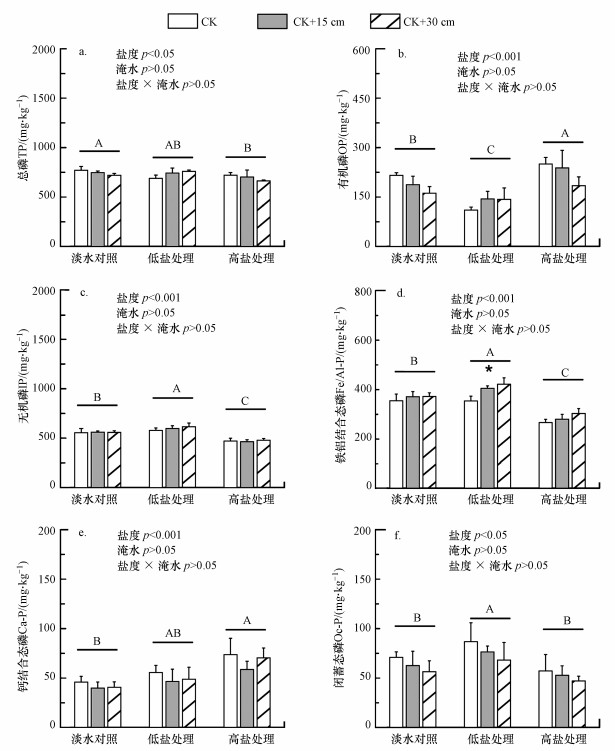 |
| 图 2 不同盐分和淹水处理下闽江河口潮汐淡水沼泽湿地土壤磷形态含量 (不同大写字母表示不同盐分处理下差异显著(p < 0.05);*表示同一盐分处理下不同淹水处理差异显著(***p < 0.001, **p < 0.01, *p < 0.05), 下同) Fig. 2Abundance and speciation of phosphorus across three salinity and three flooding treatments in the tidal freshwater wetland soils of the Min River Estuary, southeast China |
不同处理下, 土壤铁铝结合态磷含量变化范围为(265.33±12.50)~(420.67±26.10) mg·kg-1(图 2d).盐分对铁铝结合态磷Fe/Al-P含量有显著影响(p < 0.001), 相对于淡水对照, 低盐处理增加了铁铝结合态磷含量, 高盐处理降低了土壤铁铝结合态磷含量.土壤钙结合态磷含量为(40.67±12.10)~(73.67±16.65) mg·kg-1, 钙结合态磷含量随着盐分的增加而增加(图 2e).土壤闭蓄态磷(Oc-P)含量从(41.33±4.73) mg·kg-1变化至(86.67±19.14) mg·kg-1, 相对于淡水对照, 低盐处理显著增加了土壤闭蓄态磷含量(图 2f).淹水变化对铁铝结合态磷、钙结合态磷、闭蓄态磷含量均无显著影响(p>0.05).
3.3 盐分和淹水变化对土壤磷酸酶活性的影响土壤酸性磷酸酶活性为(2.08±0.58)~(8.05±1.16) nmol·g-1·h-1(图 3a), 土壤碱性磷酸酶AKP活性为(3.95±0.79)~(50.73±0.57) nmol·g-1·h-1(图 3b).盐分和淹水变化对土壤中酸性磷酸酶及碱性磷酸酶活性皆有显著影响(p < 0.001).盐分增加降低了土壤酸性磷酸酶活性;相对于淡水对照, 低盐处理增加了土壤碱性磷酸酶活性, 高盐处理降低了土壤碱性磷酸酶活性.淹水增加则显著降低了两种磷酸酶的活性(p < 0.001).
图 3(Fig. 3)
 |
| 图 3 不同盐分和淹水处理下闽江河口潮汐淡水沼泽湿地土壤磷酸酶活性 Fig. 3Soil phosphatase activities across three salinity and three flooding treatments in the tidal freshwater wetland soils of the Min River Estuary, southeast China |
3.4 不同形态磷与磷酸酶活性和土壤理化因子的相关性分析不同形态磷与磷酸酶活性和土壤理化因子的相关分析表明, 有机磷含量与碱性磷酸酶活性呈显著负相关(p < 0.05)(图 4a);无机磷含量与碱性磷酸酶活性呈显著正相关(p < 0.05)(图 4b);铁铝结合态磷含量与Fe(Ⅲ)含量(图 4c), 以及钙结合态磷含量与SO42-浓度(图 4d)均呈显著正相关(p < 0.001).
图 4(Fig. 4)
 |
| 图 4 不同形态磷与磷酸酶活性和土壤理化因子的相关性分析 Fig. 4Pearson correlation between different phosphorus speciation and soil phosphatase activities as well as soil physicochemical properties |
4 讨论(Discussion)4.1 盐分变化对河口潮汐淡水沼泽湿地植物生物量和酶活性的影响经过2年多的实验, 9个处理中沼泽植物短叶茳芏长势良好, 但不同盐分处理间植物生物量却出现显著差异(表 1).本研究发现, 高盐处理降低了植物地下生物量, 而低盐处理却增加了地下生物量.在过去的研究中也报道过类似的结果, 即低盐湿地的地下生物量要远高于淡水湿地的地下生物量(Chambers et al., 2012).这主要是由于低盐湿地的盐分并未超过植物的盐分最适耐受域, 而沼泽植物需要增加其地下根系以便从土壤中吸收更多的营养盐而抵抗低盐胁迫(Zhou et al., 2016).高盐处理下, 土壤盐分超出了植物的盐分最适耐受域, 故地下生物量出现了下降趋势(表 1).
碱性磷酸酶(AKP)活性随着盐分的变化与沼泽植物地下生物量一致, 低盐处理增加了碱性磷酸酶活性, 高盐处理降低了碱性磷酸酶活性(图 3b).盐分可通过影响分子稳定性和促进蛋白质的变性, 从而抑制土壤胞外酶活性(Morrisey et al., 2014).低盐处理下碱性磷酸酶的活性增加可能是由于在低盐处理下沼泽植物地下生物量增加, 造成根系分泌物(Root exudates)含量增加.这些根系分泌物使得沼泽植物根际微生物大量富集, 从而提高了土壤碱性磷酸酶活性(Herbert et al., 2015; Tully et al., 2019).与碱性磷酸酶不同, 低盐和高盐处理均降低了酸性磷酸酶(ACP)活性, 这可能是由于当盐分增加时, 土壤环境的pH升高, 从而抑制了土壤酸性磷酸酶的活性(Li et al., 2014).
综上, 沼泽植物生物量和土壤磷酸酶活性与磷的生物地球化学循环密切相关.河口潮汐淡水沼泽湿地植物生物量和磷酸酶活性对低盐和高盐处理的不同响应, 也将引起河口潮汐淡水沼泽湿地磷形态对这两种盐分处理的不同响应.
4.2 盐分变化对河口潮汐淡水沼泽湿地无机磷形态的影响在本研究中, 土壤无机磷(IP)是闽江河口潮汐淡水沼泽湿地土壤总磷的最重要组分, 占潮汐淡水沼泽湿地总磷含量的68%~82%.在各种形态无机磷中, 铁铝结合态磷是潮汐淡水沼泽湿地土壤无机磷的主要形态, 占无机磷含量的60%~66%, 钙结合态磷和闭蓄态磷所占比例分别为8%~14%和11%~13%(表 2).本文研究发现, 闽江河口区域的铁铝结合态磷含量高于一般的滨海地区湿地土壤中铁铝结合态磷含量(表 2).这是由于闽江河口潮汐淡水沼泽湿地土壤磷循环主要受上游地区土壤淋溶的影响.闽江上游丘陵地区分布着大量富含Fe/Al的红壤(Luo et al., 2020), 这些Fe/Al化合物与土壤中的P结合, 生成铁铝结合态磷, 从而使得土壤中铁铝结合态磷的含量较高.
表 2(Table 2)
| 表 2 不同滨海湿地土壤无机磷形态的相对含量 Table 2 Relative importance of each inorganic phosphorus fractions across different coastal wetlands | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 2 不同滨海湿地土壤无机磷形态的相对含量 Table 2 Relative importance of each inorganic phosphorus fractions across different coastal wetlands
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
土壤铁铝结合态磷含量对盐分变化敏感, 相对淡水处理, 高盐处理降低了土壤铁铝结合态磷含量, 但低盐处理增加了土壤铁铝结合态磷含量(图 2d).高盐处理降低铁铝结合态磷含量, 该结果与葡萄牙Mondego河口(Coelho et al., 2004)、美国帕塔克森特河口和切萨皮克湾河口(Hartzell et al., 2010)的研究结果一致.研究认为, 当土壤盐分增加时, 土壤中的硫酸盐还原潜力增强(Weston et al., 2013).硫酸盐还原形成的强还原剂硫氢根离子(HS-)会与铁铝结合态磷竞争Fe形成稳定的Fe-S化合物(Tully et al., 2019).由于Fe-S化合物比铁铝结合态磷更加稳定, 从而降低了土壤中铁铝结合态磷的含量(Herbert et al., 2015).与高盐处理不同, 低盐处理增加了铁铝结合态磷含量(图 2d).在本研究中发现, 铁铝结合态磷含量与土壤中Fe(Ⅲ)含量关系密切(图 4c).土壤Fe(Ⅲ)矿物在形成过程中会固定PO43-, 形成铁铝结合态磷.因此, 在低盐处理下, 由于植物生物量增加, 使得根系泌氧活动达到较高值, 土壤中Fe(Ⅲ)矿物含量增加, 促进土壤中铁铝结合态磷形成, 从而使得相对于淡水对照和高盐处理, 铁铝结合态磷在低盐处理下达到较高值.
土壤闭蓄态磷(Oc-P)含量随着盐分的变化趋势与铁铝结合态磷的情况相似, 低盐处理同时也提高了闭蓄态磷含量(图 2f).闭蓄态磷主要由晶质态Fe(Ⅲ)化合物不溶性胶膜包裹磷酸盐而产生, 受地下生物量和根系泌氧活动影响显著.因此, 低盐处理可提高闭蓄态磷含量(Nguyen, 2000; Ellison et al., 2006).相较于铁铝结合态磷, 闭蓄态磷虽然含量相对较低, 但其化学性质稳定, 不容易受到强还原剂HS-的作用而分解.因此, 高盐处理下土壤闭蓄态磷含量没有显著降低(图 2f).
土壤钙结合态磷含量随着盐分的增加显著增加(图 2e).在本研究中, 钙结合态磷与SO42-浓度呈显著正相关(图 4b).这与过去研究中发现的钙结合态磷在由陆向海方向上含量逐渐增加的结果一致(Hou et al., 2009).这主要是由于当土壤盐分增加时, 有机质矿化潜力由于SO42-的输入迅速增加, 使得水体中的CO2浓度迅速增加(Hyun et al., 2009).盐水中的Ca2+会与溶解的CO2通过沉淀反应生成方解石, 而方解石可吸附P形成钙结合态磷(Coelho et al. 2004; Hartzell et al., 2012), 这也就使得钙结合态磷含量随着盐分的增加显著增加(图 2e).
综上, 由于低盐处理增加了土壤Fe(Ⅲ)含量, 因此, 低盐处理下铁铝结合态磷和闭蓄态磷含量增加;高盐处理下, 土壤Fe(Ⅲ)含量减少, 铁铝结合态磷与闭蓄态磷含量随之减少.钙磷含量随着盐分的增加而增加.
4.3 盐分变化对河口潮汐淡水沼泽湿地有机磷和总磷的影响土壤有机磷含量在低盐处理下减少, 而在高盐处理下增加(图 2b).磷酸酶在土壤有机磷的矿化中具有重要作用, 是衡量环境中有机磷转化潜力与补给机制的重要因素(Chróst et al., 1984; Labry et al., 2013).在本研究中, 土壤有机磷含量与土壤碱性磷酸酶活性呈显著负相关关系(图 4a).因此, 低盐处理下土壤有机磷含量降低的原因是, 有机磷在碱性磷酸酶的作用下迅速分解, 使有机磷含量迅速降低.高盐处理下, 由于土壤碱性磷酸酶活性降低, 从而使得有机磷含量反而高于淡水对照(图 2b).土壤无机磷含量与土壤碱性磷酸酶活性呈正相关关系(图 4d), 说明有机磷被碱性磷酸酶分解后, 绝大多数的有机磷可能转换为无机磷.上述结果表明, 碱性磷酸酶在磷形态对盐分和淹水的响应中发挥着重要的作用.土壤有机磷和无机磷含量与土壤酸性磷酸酶活性没有显著关系(p>0.05), 表明在盐分和淹水增加的背景下, 土壤有机磷和无机磷含量受土壤酸性磷酸酶活性的影响有限.
土壤总磷含量随着盐分的增加而逐渐减少(图 2a).随着盐分的增加, 土壤PO43-浓度不断增加(表 1), 说明随着盐分的增加, 一部分磷将被释放到孔隙水中.受涨落潮的潮泵(tide pumping)作用, 孔隙水中的PO43-将被潮水带至附近水域, 最终引起附近海域的富营养化作用.
通过以上研究结果, 可以预测在未来海平面上升过程中河口潮汐淡水沼泽湿地磷循环发生的改变(图 5).未来50年内, 多数淡水沼泽湿地将转变为低盐沼泽湿地.此时, 沼泽植物地下生物量和土壤碱性磷酸酶活性增加, 土壤中的Fe(Ⅲ)含量增加, 土壤闭蓄态磷、铁铝结合态磷和钙结合态磷含量均显著增加, 有机磷含量将显著减少.这个时期主要存在有机磷向无机磷的转化.而在未来50~100年内, 低盐沼泽湿地将进一步转换为高盐沼泽湿地.此时, 沼泽植物地下生物量和土壤碱性磷酸酶活性减少, 土壤中的Fe(Ⅲ)含量较少, 铁铝结合态磷和闭蓄态磷含量迅速降低, 无机磷的释放速率大于有机磷的分解速率.
图 5(Fig. 5)
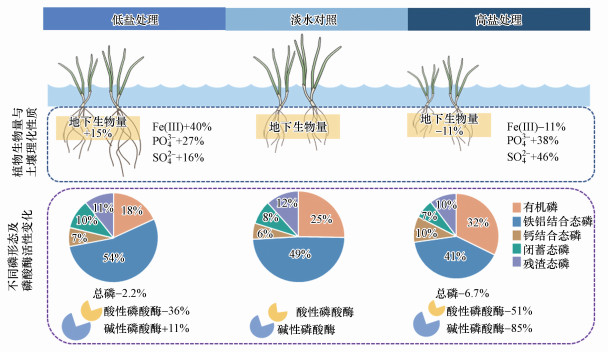 |
| 图 5 闽江河口潮汐淡水沼泽湿地不同盐分处理下土壤不同磷形态的占比变化 Fig. 5Schematic illustration showing partitions of different phosphorus fractions across three salinity treatments in the tidal freshwater wetland soils of the Min River Estuary, southeast China |
5 结论(Conclusions)1) 淹水条件变化对河口潮汐淡水沼泽湿地土壤中磷的形态和含量无显著影响, 但盐分变化对土壤中磷的形态和含量影响显著, 且低盐处理和高盐处理下磷的形态具有明显差异.
2) 土壤无机磷是土壤总磷的主要形态, 其中, 土壤无机磷以铁铝结合态磷为主.铁铝结合态磷含量与土壤Fe(Ⅲ)含量相关, 低盐处理增加了铁铝结合态磷含量, 高盐处理降低了铁铝结合态磷含量.
3) 低盐处理增加了土壤碱性磷酸酶活性, 而高盐处理则降低了土壤碱性磷酸酶活性.土壤碱性磷酸酶活性是土壤有机磷转化为无机磷的关键驱动力.低盐处理减少了土壤有机磷的相对含量, 高盐处理增加了土壤有机磷的相对含量.
4) 随着盐分的增加, 土壤总磷含量将持续下降.低盐处理下, 土壤总磷含量的降低主要以有机磷的分解为主;而高盐处理下, 无机磷的释放速率将大于有机磷的分解速率.
参考文献
| Bai J, Ye X, Jia J, et al. 2017. Phosphorus sorption-desorption and effects of temperature, pH and salinity on phosphorus sorption in marsh soils from coastal wetlands with different flooding conditions[J]. Chemosphere, 188(12): 677. |
| Bonneville S, Behrends T, Cappellen V P. 2009. Solubility and dissimilatory reduction kinetics of iron(Ⅲ) oxyhydroxides: a linear free energy relationship[J]. Geochimica Et Cosmochimica Acta, 73(18): 5273-5282. DOI:10.1016/j.gca.2009.06.006 |
| 薄录吉, 王建国, 王岩, 等. 2011. 淹水时间对水稻土磷素形态转化及其有效性的影响[J]. 土壤, 43(6): 930-934. |
| Bruland G L, DeMent G. 2009. Phosphorus sorption dynamics of Hawaii's coastal wetlands[J]. Estuaries and Coasts, 32(5): 844-854. DOI:10.1007/s12237-009-9201-9 |
| Chambers L G. 2012. The biogeochemical effects of sea level rise on coastal wetland soil carbon[D]. Florida: University of Florida |
| Chang S, Jackson M L. 1957. Fractionation of soil phosphorus[J]. Soil science, 84(2): 133-144. DOI:10.1097/00010694-195708000-00005 |
| Chen R, Twilley R R. 1999. Patterns of mangrove forest structure and soil nutrient dynamics along the Shark River Estuary, Florida[J]. Estuaries, 22(4): 955-970. DOI:10.2307/1353075 |
| Chróst R J, Siuda W, Halemejko G Z. 1984. Long term studies on alkaline phosphatase activity (APA) in a lake with fish-aquaculture in relation to lake eutrophication and phosphorus cycle[J]. Archiv für Hydrobiologie-Supplements, 70(1): 1-32. |
| Coelho J, Flindt M, Jensen H S, et al. 2004. Phosphorus speciation and availability in intertidal sediments of a temperate estuary: relation to eutrophication and annual P-fluxes[J]. Estuarine, Coastal and Shelf Science, 61(4): 583-590. DOI:10.1016/j.ecss.2004.07.001 |
| Ellison M E, Brett M T. 2006. Particulate phosphorus bioavailability as a function of stream flow and land cover[J]. Water Research, 40(6): 1258-1268. DOI:10.1016/j.watres.2006.01.016 |
| Gao H F, Bai J H, Xiao R, et al. 2012. Soil net nitrogen mineralization in salt marshes with different flooding periods in the Yellow River Delta, China[J]. Clean Soil Air Water, 40(10): 1111-1117. DOI:10.1002/clen.201200031 |
| Gilbert J D, Guerrero F, et al. 2014. Sediment desiccation as a driver of phosphate availability in the water column of Mediterranean wetlands[J]. Science of the Total Environment, 466-467: 965-975. DOI:10.1016/j.scitotenv.2013.07.123 |
| Gireeshkumar T R, Deepulal P M, Chandramohanakumar N. 2013. Phosphorous speciation in surface sediments of the Cochin estuary[J]. Environmental Monitoring and Assessment, 185(3): 2535-2552. DOI:10.1007/s10661-012-2729-3 |
| Hartzell J L, Jordan T E, Cornwell J C. 2010. Phosphorus burial in sediments along the salinity gradient of the Patuxent River, a subestuary of the Chesapeake Bay (USA)[J]. Estuaries and Coasts, 33(1): 92-106. DOI:10.1007/s12237-009-9232-2 |
| Hartzell J L, Jordan T E. 2012. Shifts in the relative availability of phosphorus and nitrogen along estuarine salinity gradients[J]. Biogeochemistry, 107(1/3): 489-500. |
| Hedley M J, Stewart J W B, Chauhan B S. 1982. Changes in inorganic and organic soil phosphorus fractions induced by cultivation practices and by laboratory incubations[J]. Soil Science Society of America Journal, 46(5): 970-976. DOI:10.2136/sssaj1982.03615995004600050017x |
| Herbert E R, Boon P A, et al. 2015. Global perspective on wetland salinization: ecological consequences of a growing threat to freshwater wetlands[J]. Ecosphere, 6(10): 1-43. |
| Hou L, Liu M, Yang Y, et al. 2009. Phosphorus speciation and availability in intertidal sediments of the Yangtze Estuary, China[J]. Applied Geochemistry, 24(1): 120-128. DOI:10.1016/j.apgeochem.2008.11.008 |
| Hyun J H, Mok J S, Cho H Y, et al. 2009. Rapid organic matter mineralization coupled to iron cycling in intertidal mudflats of the Han River estuary, Yellow Sea[J]. Biogeochemistry, 92: 231-245. DOI:10.1007/s10533-009-9287-y |
| Johnston S G, Burton E D, Aaso T, et al. 2014. Sulfur, iron and carbon cycling following hydrological restoration of acidic freshwater wetlands[J]. Chemical Geology, 371: 9-26. DOI:10.1016/j.chemgeo.2014.02.001 |
| Jun M, Altor A E, Craft C B. 2013. Effects of increased salinity and inundation on inorganic nitrogen exchange and phosphorus sorption by tidal freshwater floodplain forest soils, Georgia (USA)[J]. Estuaries and Coast, 36(3): 508-518. DOI:10.1007/s12237-012-9499-6 |
| Labry C, Delmas D, Herbland A. 2005. Phytoplankton and bacterial alkaline phosphatase activities in relation to phosphate and DOP availability within the Gironde plume waters (Bay of Biscay)[J]. Journal of Experimental Marine Biology and Ecology, 318(2): 213-225. DOI:10.1016/j.jembe.2004.12.017 |
| 李洁, 张文强, 金鑫, 等. 2015. 环渤海滨海湿地土壤磷形态特征研究[J]. 环境科学学报, 35(4): 1143-1151. |
| 李文华, 邵学新, 吴明, 等. 2013. 杭州湾潮滩湿地土壤碱性磷酸酶活性分布及其与磷形态的关系[J]. 环境科学学报, 33(12): 3341-3349. |
| Lin P, Guo L. 2016. Dynamic changes in the abundance and chemical speciation of dissolved and particulate phosphorus across the river-lake interface in southwest Lake Michigan[J]. Limnology and Oceanography, 61(2): 771-789. DOI:10.1002/lno.10254 |
| Liu M, Hou L, Xu S, et al. 2002. Adsorption of phosphate on tidal flat surface sediments from the Yangtze Estuary[J]. Environmental Geology, 42(6): 657-665. DOI:10.1007/s00254-002-0574-3 |
| Li J G, Pu L J, Han M F, et al. 2014. Soil salinization research in China: Advances and prospects[J]. Journal of Geographical Sciences, 24(5): 943-960. DOI:10.1007/s11442-014-1130-2 |
| 刘敏, 许世远, 侯立军. 2007. 长江口潮滩沉积物—水界面营养盐环境生物地球化学过程[M]. 北京: 科学出版社. |
| 刘越, 胡恭任, 袁栋林, 等. 2011. 晋江感潮河段表层沉积物中磷的分布、赋存形态及环境意义[J]. 环境化学, 9(7): 143-149. |
| Lukawska-Matuszewska K, Bola?ek J. 2008. Spatial distribution of phosphorus forms in sediments in the Gulf of Gdańsk (southern Baltic Sea)[J]. Continental Shelf Research, 28(7): 977-990. DOI:10.1016/j.csr.2008.01.009 |
| Luo M, Zeng C S, Tong C, et al. 2014. Abundance and speciation of iron across a subtropical tidal marsh of the Min River Estuary in the East China Sea[J]. Applied Geochemistry, 45: 1-13. DOI:10.1016/j.apgeochem.2014.02.014 |
| Luo M, Zhai Z F, Ye R Z, et al. 2020. Carbon mineralization in tidal freshwater marsh soils at the intersection of low-level saltwater intrusion and ferric iron loading[J]. Catena, 193: 104644. DOI:10.1016/j.catena.2020.104644 |
| Morrissey E M, Gillespie J L, Morina J C, et al. 2014. Salinity affects microbial activity and soil organic matter content in tidal wetlands[J]. Global Change Biology, 20(4): 1351-1362. DOI:10.1111/gcb.12431 |
| Newman S, Pietro K. 2002. Phosphorus storage and release in response to flooding: implications for Everglades stormwater treatment areas[J]. Ecological Engineering, 18(1): 23-38. |
| Nguyen L M. 2000. Phosphate incorporation and transformation in surface sediments of a sewage- impacted wetland as influenced by sediment sites, sediment pH and added phosphate concentration[J]. Ecological Engineering, 14(1/2): 139-155. |
| Parkinson J, Allen S. 1975. A wet oxidation procedure suitable for the determination of nitrogen and mineral nutrients in biological material[J]. Communications in Soil Science and Plant Analysis, 6(1): 1-11. DOI:10.1080/00103627509366539 |
| P?rtner H O, Roberts D C, Masson-Delmotte V, et al. 2019. IPCC special report on the ocean and cryosphere in a changing climate[R]. Geneva: IPCC Intergovernmental Panel on Climate Change |
| Price R M, Savabi M R, Jolicoeur J L. 2010. Adsorption and desorption of phosphate on limestone in experiments simulating seawater intrusion[J]. Applied Geochemistry, 25(7): 1085-1091. DOI:10.1016/j.apgeochem.2010.04.013 |
| Quan W, Shi L, Han J, et al. 2010. Spatial and temporal distributions of nitrogen, phosphorus and heavy metals in the intertidal sediment of the Chang jiang River Estuary in China[J]. Acta Oceanologica Sinica, 29: 108-115. DOI:10.1007/s13131-010-0013-3 |
| Reddy K R, DeLaune R D. 2008. Biogeochemistry of Wetlands: Science and Applications[M]. CRC Press LLC. |
| Saiya-Cork K R. 2002. Effects of long-term nitrogen deposition on extracellular enzyme activity in an Acer saccharum forest soil[J]. Soil Biology and Biochemistry, 34(9): 1309-1315. DOI:10.1016/S0038-0717(02)00074-3 |
| Samanta S, Debnath D, Maitra N, et al. 2015. Sediment phosphorus forms and levels in two tropical floodplain wetlands[J]. Aquatic Ecosystem Health & Management, 18(4): 467-474. |
| Sun J N, Xu G, Shao H B, et al. 2012. Potential retention and release capacity of phosphorus in the newly formed wetland soils from the Yellow River Delta, China[J]. Acta Hydrochimica Et Hydrobiologica, 40(10): 1131-1136. |
| Sun Z, Wang L, Mou X, et al. 2014. Spatial and temporal variations of nitrous oxide flux between coastal marsh and the atmosphere in the Yellow River estuary of China[J]. Environmental Science and Pollution Research, 21: 419-433. DOI:10.1007/s11356-013-1885-5 |
| Tully K, Keryn G, Rebecca E N, et al. 2019. The invisible flood: the chemistry, ecology, and social implications of coastal saltwater intrusion[J]. BioScience, 69: 368-378. DOI:10.1093/biosci/biz027 |
| Vitousek P M, Porder S, Houlton B Z, et al. 2010. Terrestrial phosphorus limitation: mechanisms, implications, and nitrogen phosphorus interactions[J]. Ecological Applications, 20: 5-15. DOI:10.1890/08-0127.1 |
| Wang L, Ye M, Li Q, et al. 2013. Phosphorus speciation in wetland sediments of Zhujiang (Pearl) River Estuary, China[J]. Chinese Geographical Science, 23(5): 574-583. DOI:10.1007/s11769-013-0627-4 |
| Weston N B, Vile M A, Neubauer S C, et al. 2013. Accelerated microbial organic matter mineralization following salt-water intrusion into tidal freshwater marsh soils[J]. Biogeochemistry, 102: 135-151. |
| Woodroffe C D, Murray-Wallace C V. 2012. Sea-level rise and coastal change: the past as a guide to the future[J]. Quaternary Science Reviews, 54(26): 4-11. |
| Wu M, Shao X X, Hu F, et al. 2008. Effects of reclamation on soil nutrients distribution of coastal wetland in south Hangzhou Bay[J]. Soils, 40(5): 760-764. |
| Zhi W, Ji G. 2012. Constructed wetlands, 1991-2011: A review of research development, current trends, and future directions[J]. Science of the total Environment, 441: 19-27. DOI:10.1016/j.scitotenv.2012.09.064 |
| Zhou M, Butterbach-Bahl K, Vereecken H, et al. 2016. A meta-analysis of soil salinization effects on nitrogen pools, cycles and fluxes in coastal ecosystems[J]. Global Change Biology, 23: 1338-1352. |
| 张仲胜, 吕宪国, 薛振山, 等. 2016. 中国湿地土壤碳氮磷生态化学计量学特征研究[J]. 土壤学报, (5): 1160-1169. |
