 , 吴攀2,3, 查学芳3, 何守阳3, 吴琳娜2, 韩志伟2,3
, 吴攀2,3, 查学芳3, 何守阳3, 吴琳娜2, 韩志伟2,3

1. 贵州大学农学院, 贵阳 550025;
2. 贵州大学资源与环境工程学院, 贵阳 550025;
3. 喀斯特地质资源与环境教育部重点实验室, 贵阳 550025
收稿日期: 2020-08-07; 修回日期: 2020-09-24; 录用日期: 2020-09-24
基金项目: 国家自然科学基金项目(No.41501018,41763019);贵州省地质勘查基金项目(黔国土资地环函[2014]23);贵州省人才基地项目(No.RCJD2018-21)
作者简介: 李学先(1988—), 女, 讲师, E-mail: xxli5@gzu.edu.cn
通讯作者(责任作者): 韩志伟, E-mail: zwhan@gzu.edu.cn
摘要:由于岩溶水文系统的地球化学敏感性和脆弱性,岩溶地下水NO3-污染已成为世界范围普遍存在的环境问题,而岩溶山区地下水硝酸盐来源解析对于保障区域供水安全和人体健康具有重要意义.因此,本文选取贵州中部典型岩溶山区城镇主要供水流域地表水和地下水为研究对象,基于土地利用类型,联合水化学分析及δ15N-NO3-、δ18O-NO3-示踪技术对水体硝酸盐分布特征、来源贡献及迁移转化过程进行研究.结果表明,研究区水体溶解性无机氮以硝态氮为主,水体NO3-含量及分布与区域土地利用方式密切相关,硝酸盐污染主要集中于住宅用地和耕地 & 林地区岩溶地下水中.水体NO3-主要来源于与农业活动和城镇化建设有关的土壤有机氮、化肥及粪便污水,水体氮循环主导过程为硝化作用,反硝化作用基本不存在.稳定同位素模型(SIAR)分析结果显示,区域水体硝酸盐主要受当地农业活动及城镇化过程影响,其中,土壤有机氮、化肥及粪便污水对地表水硝酸盐的贡献率分别为50.24%、27.97%和24.58%,对地下水硝酸盐的贡献率分别为54.58%、24.58%和20.15%,大气降水来源贡献率较低.
关键词:硝酸盐来源氮氧同位素SIAR模型土地利用岩溶山区
Tracing nitrate sources in urban waters of Karst mountainous area using hydrochemistry and stable isotope
LI Xuexian1
 , WU Pan2,3, ZHA Xuefang3, HE Shouyang3, WU Linna2, HAN Zhiwei2,3
, WU Pan2,3, ZHA Xuefang3, HE Shouyang3, WU Linna2, HAN Zhiwei2,3

1. College of Agriculture, Guizhou University, Guiyang 550025;
2. Resource and Environmental Engineering College, Guizhou University, Guiyang 550025;
3. Key Laboratory of Karst Environment and Geohazard Prevention, Ministry of Education, Guiyang 550025
Received 7 August 2020; received in revised from 24 September 2020; accepted 24 September 2020
Abstract: Nitrate (NO3-) contamination in Karst aquifer system has become a worldwide environmental problem.Identification sources of nitrate in Karst groundwater is of great significance for ensuring regional water security and human health.Both surface water and groundwater samples in typical Karst mountainous areas in Central Guizhou were collected.These samples were analyzed by hydrochemistry,environmental isotope tracer technique(δ15N-NO3- and δ18O-NO3-),combing with land-use type analysis to identify distribution,potential sources,contributions,transportation and transformation of nitrate.The results showed that dissolved inorganic nitrogen in surface water and groundwater were dominated as nitrate nitrogen.The concentration and distribution of NO3- in surface water and groundwater were significantly correlated to regional land-use types.Nitrate pollution is mainly occurred in Karst groundwater in residential land and cultivated land & forest areas.NO3- in surface water and groundwater was mainly derived from soil organic nitrogen,chemical fertilizers and manure/sewage related to agricultural activities and urbanization.The nitrogen cycle in surface water and groundwater was nitrification,while denitrification was not significant.The results from stable isotope model (SIAR) analysis showed that nitrate in surface water and groundwater mainly came from agricultural activities related to soil organic nitrogen and fertilizer,followed by manure and sewage related to urban activities.The contributions from soil organic nitrogen,fertilizer and manure and sewage to nitrate were 50.24%,27.97% and 24.58% in surface water and 54.58%,24.58% and 20.15% in groundwater,respectively.The rate of contribution from atmospheric precipitation to nitrate was relatively low.
Keywords: nitrate sourceδ15N-NO3- and δ18O-NO3-SIAR modelland-use typeKarst mountain area
1 引言(Introduction)岩溶地下水作为重要的供水资源, 为全球25%的人口提供饮用水(Ghasemizadeh et al., 2012), 对世界许多国家和地区的社会经济可持续发展起着至关重要的作用(Kalhor et al., 2019).但由于岩溶地下水系统固有的地球化学敏感性和脆弱性, 使得城镇化建设、工农业生产、采矿等人为活动导致的地下水污染在水环境中表现得尤为突出(Sabina et al., 2016;Li et al., 2018;Jia et al., 2020), 目前地下水资源及其环境问题已成为喀斯特地区发展的限制性因素之一.特别是在矿产资源富集、地表干旱、地下水资源丰富的贵州喀斯特山区, 岩溶地下水已成为城镇化发展的重要战略资源(何守阳等, 2019), 对保障城乡居民饮水安全及生态文明建设具有重要的支撑作用.因此, 研究喀斯特地区岩溶地下水环境质量现状及污染物来源对于合理开发利用岩溶地下水资源及保障饮用水安全具有重要意义.
硝酸盐(NO3-)是地下水中常见的污染物, 天然地下水中硝酸盐(以N计)含量通常低于2.5 mg·L-1(Panno et al., 2010), 但由于人类活动不断加剧, 如化肥的过度使用、污水灌溉、畜禽养殖、生活污水排放等, 导致全球许多地区地下水中NO3-含量呈不断上升趋势(Mélida et al., 2017;Zhang et al., 2020), 目前水体硝酸盐污染已成为全球面临的主要环境问题(Zhang et al., 2020).过量硝酸盐进入水环境后不但会引起水生生态系统酸化和富营养化, 影响水生生物生存(Jia et al., 2020), 甚至会威胁人类健康(Fathmawati et al., 2017).喀斯特地区岩溶含水层具有强烈的非均质性, 以喀斯特裂隙和管道网络为主, 常形成开放的地下水系统, 能够快速接受外界污染物输入, 具有高度的地球化学敏感性和污染脆弱性(Bakalowicz, 2005).此外, 岩溶含水层中地下水流动迅速, 硝酸盐在运移和排泄过程中的衰减几乎可以忽略不计, 且在持续污染源输入情况下具有逐渐累积负荷的特征(Mélida et al., 2017), 从而极大地增加了地下水安全利用的隐患.贵州是西南喀斯特地区极具代表性和典型性的区域, 同时又处于社会经济及城镇化进程快速发展时期, 地下水硝酸盐污染问题日益凸显(李耕等, 2019;田永著等, 2020;赵然等, 2020a), 而准确识别岩溶山区地下水硝酸盐来源分配是建立有效防治污染对策的前提和基础.
地下水中硝酸盐来源复杂多样, 通常叠加了面源污染和点源污染, 同时还可能涉及复杂的氮循环和迁移过程(Zhang et al., 2020), 从而给地下水中硝酸盐源解析带来较大难度.传统方法通过硝酸盐与水化学特征离子(如SO42-、Cl-、K+、Ca2+、Na+和Mg2+)之间的相关性统计来定性辨析水体硝酸盐来源(Valiente et al., 2018;Ogrinc et al., 2019), 但只能提供辨别硝酸盐来源和迁移转化过程的常规信息, 难以得到合理、科学的解释(Petitta et al., 2009).近年来, 氮、氧双同位素示踪技术因可以有效弥补水化学分析法的不足而被广泛运用于识别城市化建设、农业活动影响下地表水、地下水中硝酸盐污染来源研究中(Sabina et al., 2016;Zhang et al., 2020;赵然等, 2020b).此外, 硝酸盐氮、氧同位素与贝叶斯混合模型(SIAR)的耦合也为定量识别不同硝酸盐来源的混合比例提供了有力工具, 并在喀斯特地区岩溶地下水系统中得到了成功运用(Yue et al., 2015;田永著等, 2020;赵然等, 2020a).然而, 相关研究主要集中在岩溶地下河流域、岩溶水库流域及农业区域水体硝酸盐来源识别方面, 对岩溶山区受农业生产、城镇化建设等系列人为活动影响的岩溶水体硝酸盐的来源示踪研究鲜有报道.
因此, 本文选取贵州典型岩溶山区城镇供水流域为研究区, 在采样分析基础上, 根据流域水体水化学特征及硝酸盐氮、氧同位素组成, 定性判断流域地表水、地下水中硝酸盐来源、分布特征及转化过程, 并基于SIAR混合模型, 定量识别水中硝酸盐各污染端元的贡献率, 旨在为岩溶山区地下水硝酸盐污染源头防控及区域水环境管理提供科学依据.
2 材料与方法(Materials and methods)2.1 研究区概况织金县位于贵州省中部偏西(105°20′~106°11′E, 26°21′~26°58′N), 是贵州省典型的岩溶山区城镇, 喀斯特分布面积占全县土地总面积的60.8%.境内地势西高东低, 海拔为1400~2400 m, 属亚热带高原季风温润气候, 年降雨量为1400 mm左右.研究区为织金县城主要供水流域, 该区域岩溶洼地、漏斗、溶洞、落水洞及地下暗河分布广泛(图 1), 为区内地表水和地下水转换提供了便捷通道.区内地表发育河流主要为织金河, 属长江流域乌江水系六冲河一级支流, 由西南向东北径流, 流域集水面积为442 km2.
图 1(Fig. 1)
 |
| 图 1 研究区土地利用类型及采样点位置分布 Fig. 1The land-use type and distribution of sampling points in the study arrea |
研究区出露地层主要包括二叠系中统栖霞、茅口组(P2q+m)、上统峨眉山玄武岩组(P3β)、龙潭组(P3l)、长兴、大隆组(P3c+d), 三叠系上统夜郎组(T1y)及第四系(Q), 其中, 二叠系和三叠系碳酸盐岩地层分布较广.区内含水岩组为二叠系中统栖霞-茅口组(P2q+m)碳酸盐岩, 含水层厚度大、富水性强, 是境内主要供水含水层(宋小庆等, 2012).受地形地貌及向斜构造控制, 区域地下水自西南向东北径流, 最终由向斜两翼向织金河槽谷中汇集, 以岩溶大泉或暗河的形式排泄于地表, 形成地下水集中排泄区, 城镇供水以岩溶地下水为主.
研究区人为活动以农业生产、煤矿开采及城镇化建设为主导, 其中, 西南、西北部为主要的农业种植和煤矿集中开采区, 土地利用类型以耕地、林地、草地为主;东北部为县城区域, 近年来城镇化快速发展, 土地利用类型为住宅用地, 同时县城周边农业种植密集, 耕地分布广泛(图 1).研究区煤炭资源丰富, 是贵州省最大的无烟煤产区, 属“织纳煤田”的主体部分, 长期的煤矿开采导致区域水体受到不同程度的影响(Li et al., 2018).此外, 织金县在快速城镇化进程中, 岩溶地下水资源也受到不同程度的影响, 主要表现为地下水水位下降、岩溶大泉断流及水质恶化等(陈登齐等, 2012).但目前还没有关于该地区农业活动、采矿活动及城镇化建设过程对岩溶地下水水质影响的研究报道.
2.2 样品采集与分析于2016年8月(丰水期)采集流域不同水体样品31件(地表水17件、地下水14件), 采样点具体位置见图 1.地下水采自地表排泄泉点及民用水井, 主要为饮用及灌溉用水.现场用便携式水质参数仪(WTW multi 3430, Germany)测定pH、溶解氧(DO)、电导率(EC)、氧化还原电位(Eh)和水温(T)等易变参数, 并用0.01 mol·L-1 HCl滴定HCO3-浓度.水样经0.45 μm醋酸纤维滤膜过滤后分别储存于50 mL聚乙烯瓶中, 用于测定阴、阳离子和硝酸盐氮、氧同位素.其中, 用于阳离子测定的样品现场用优级纯硝酸(HNO3)酸化至pH < 2;用于阴离子和同位素测定的样品直接过滤收集, 并装满整个容器, 确保不留气泡;同时采集500 mL水样储存于预先洗净的聚乙烯瓶中, 并用优级纯硫酸(H2SO4)酸化至pH < 2用于氨氮测定.所有样品均用封口膜封好后, 带回实验室冷藏(4 ℃)保存.
分别用火焰原子吸收光谱仪(ICE3500, Thermo Fisher, USA)和离子色谱(ICS-1100, Dionex, USA)测定水中阳离子(Ca2+、Mg2+、K+、Na+)和阴离子(SO42-、NO3-、Cl-).采用纳氏试剂分光光度法和重氮耦合分光光度法测定水体NH4+-N和NO2--N.数据质量通过空白样、平行样和内标进行控制, 测试误差在5%以内.水体硝酸盐氮、氧同位素在中国科学院地球化学研究所(贵阳)环境地球化学国家重点实验室完成, 采用反硝化细菌法将NO3-反硝化为N2O, 然后利用Trace Gas结合同位素质谱测试, 精度为±0.3‰.测试结果以V-SMOW(Vienna Standard Mean Oceanic Water)千分差的形式表示.
2.3 数据统计与分析采用SPSS21.0对水体理化参数进行描述性统计分析, 采用AqQA进行水化学分析, 同时通过Canoco 5.0进行地表、地下水水化学组分与土地利用类型间冗余分析(Redundancy Analysis, RDA)以指示土地利用类型对水体氮素来源及迁移的影响(张妍等, 2019;孙厚云等 2020).
为定量识别水体硝酸盐污染来源, 采用贝叶斯同位素混合模型(SIAR)估算水体中各硝酸盐来源贡献率.目前, 已有大量研究证实了SIAR模型在计算地表水和地下水中多种硝酸盐来源贡献的可靠性和实用性(Li et al., 2019;Gibrilla et al., 2020;Zhang et al., 2020).SIAR模型通过定义k个来源n个混合物的j个同位素值, 模型可以表示为(Parnell et al., 2010):
 | (1) |
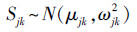 | (2) |
 | (3) |
 | (4) |
3 结果与讨论(Results and discussion)3.1 流域水体水化学特征及演化流域水体水化学组成是岩石风化和外界物质输入的综合结果, 通常是区域水文地质背景及人为活动的直接反映.碳酸盐岩地区水体多呈弱碱性, 水化学离子以Ca2+、Mg2+和HCO3-为主, 体现了岩溶作用为主的地球化学过程和水化学特征(Han et al., 2004).但由于受人为活动的影响, 其水体离子组成、水化学类型会发生演化.由表 1可知, 研究区大部分地表水pH值为7.2~8.5(除R16点pH为3.9外), 属于中性、弱碱性水体.阴离子主要为SO42-和HCO3-, 分别占阴离子总量的58.3%和38.7%, 其次为NO3-和Cl-;阳离子以Ca2+、Na+为主, 分别占阳离子总量的65.3%和23.2%, 其次为Mg2+和K+.地下水pH为6.9~8.1, 为中性-弱碱性水体;DO浓度为2.1~8.16 mg·L-1, 均值为6.48 mg·L-1, 结合地下水中氧化还原电位(Eh=136~339 mV)可知, 区域地下水体大部分处于氧化环境.地下水阳离子主要为Ca2+和Mg2+, 占阳离子总量的80%以上, 阴离子主要为HCO3-, 占阴离子总量的60%以上.
表 1(Table 1)
| 表 1 地表水、地下水物理和化学指标统计特征 Table 1 The statistic characteristics of physical and chemical parameters in surface water and groundwater | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 1 地表水、地下水物理和化学指标统计特征 Table 1 The statistic characteristics of physical and chemical parameters in surface water and groundwater
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
由图 2可知, 地表水水化学类型主要为SO4·Cl-Ca·Mg型, 其次为HCO3-Ca·Mg型, 其中, R14和R16点水化学类型有向SO4·Cl-Na型演化趋势.地下水水化学类型主要为HCO3-Ca·Mg型, 说明地下水离子组成主要来源于流域碳酸岩盐的风化溶解, 个别地下水点(S14)水化学类型有向SO4·Cl-Ca·Mg型演化趋势.整体上, 研究区大部分地表水和地下水SO42-、NO3-、Cl-和Na+含量明显升高(表 1), 水化学类型已发生演化, 说明人类活动已影响到区域水体水质.喀斯特地区水体碳酸盐岩风化溶解主要由H2CO3驱动, 而当H2CO3和HNO3以1∶1共同溶蚀碳酸盐岩, 水中(Ca2++Mg2+)与HCO3-当量比为0.67.研究区地下水中(Ca2++Mg2+)与HCO3-当量比为0.63~1.05, 均值为0.86, 而地表水中(Ca2++Mg2+)与HCO3-当量比明显高于地下水, 均值为1.24, 说明人类活动产生外源酸(HNO3、H2SO4)参与了区域碳酸盐岩风化溶蚀.由图 3可知, 部分地表水和大部分地下水样点集中分布于H2CO3和HNO3共同参与的碳酸盐溶蚀范围内, 说明区域农业活动和/或城镇居民生活产生的NO3-已明显影响到研究区的碳酸盐岩溶蚀过程(段世辉等, 2019).此外, 部分地表水中Ca2++Mg2+含量相对于HCO3-明显过剩, 主要因为研究区西南、西北侧为煤矿集中开采区, 煤矿开采活动及农业活动产生的SO42-(H2SO4)加速了区域碳酸盐岩的溶解, 导致地表水中Ca2+、Mg2+、SO42-、Na+含量明显升高(Li et al., 2018).
图 2(Fig. 2)
 |
| 图 2 研究区水体水化学Piper图 Fig. 2Piper diagram of hydrochemical parameters in study area |
图 3(Fig. 3)
 |
| 图 3 研究区水体(Ca2++Mg2+)与HCO3-关系图 Fig. 3Cross plot of (Ca2++Mg2+) vs.HCO3- in waters of the study area |
3.2 水体溶解性无机氮含量及分布特征研究区不同水体溶解性无机氮含量统计结果见表 2.由表可知, 地表水中溶解性无机氮以NO3--N和NH4+-N为主, 平均含量分别为(1.55±0.42) mg·L-1和(1.30±0.57) mg·L-1, 分别占总溶解性无机氮含量的53.8%和43.4%, 而NO2--N含量较低.其中, 76.4%的地表水NH4+-N含量明显高于《地表水环境质量标准》(GB3838—2002)III类水质标准(1.0 mg·L-1), 超标严重.地下水中溶解性无机氮以硝态氮为主, NO3--N含量为1.34~14.34 mg·L-1, 平均含量为(3.52±3.48) mg·L-1, 明显高于地表水中硝态氮含量, 其中, S14样点NO3--N含量为14.34 mg·L-1, 已超出世界卫生组织(WHO)规定的硝酸盐饮用水标准限值(10 mg·L-1).与地表水相比, 地下水NH4+-N和NO2--N含量相对较低, 其中, NH4+-N含量为(0.56±0.19) mg·L-1, 略高于地下水质量标准(GB/T14848—2017)Ⅲ类水限值(0.5 mg·L-1).以上数据表明, 研究区地表水硝酸盐污染特征不明显, 而地下水存在不同程度的硝酸盐污染, 对区域居民健康具有潜在的风险.
表 2(Table 2)
| 表 2 地表水、地下水中溶解态无机氮素浓度及同位素统计值 Table 2 The statistics on dissolved inorganic nitrogen and isotopes of surface water and groundwater | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 2 地表水、地下水中溶解态无机氮素浓度及同位素统计值 Table 2 The statistics on dissolved inorganic nitrogen and isotopes of surface water and groundwater
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
研究区不同土地利用类型区域水体NO3--N和NH4+-N含量如图 4所示.由图可知, 不同土地利用类型下地表水、地下水中NH4+-N含量变化不大, 而NO3--N含量差异较大, 地表水中NO3--N含量大小排序为住宅用地((1.82±0.32) mg·L-1)>耕地 & 林地((1.38±0.46) mg·L-1)>耕地((1.24±0.24) mg·L-1).地下水中NO3--N含量排序为住宅用地((5.38±4.26) mg·L-1)>耕地((2.14±0.04) mg·L-1)>耕地 & 林地((1.49±0.27) mg·L-1), 说明研究区水体硝酸盐分布受区域土地利用类型的影响.
图 4(Fig. 4)
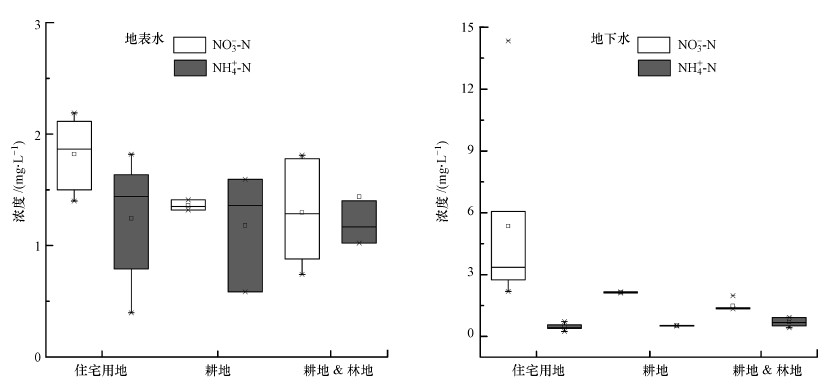 |
| 图 4 不同土地利用类型下水体溶解性无机氮浓度箱型图 Fig. 4Box diagram of dissolved inorganic nitrogen concentrations of waters in different land- use types |
冗余分析(RDA)可以揭示不同土地利用类型对流域水体水质的影响程度, 土地利用类型与水化学组分箭头之间的夹角余弦值可以表征两者之间的相关性, 夹角越小, 表示两者之间相关性越强.如图 5所示, 地表水NO3-、NO2--N及Cl-含量与住宅用地呈正相关关系, 住宅用地土地利用因子对区域地表水NO3-浓度响应的解释程度较高(图 5).地表水SO42-、Ca2+、Na+、Mg2+、NH4+-N与耕地 & 林地及林地之间呈一定的正相关关系, 主要是由于研究区西北、西南部耕地、林地分布广泛, 地表河流发育于沟谷地带, 地表水水质受到地表径流、土壤淋滤等带来的污染物质的影响.同时, 研究区地表河流水质还受上游煤矿开采产生的煤矿废水的影响, 导致地表水中SO42-、Ca2+、Na+、Mg2+、NH4+-N等污染物升高(Li et al., 2018).
图 5(Fig. 5)
 |
| 图 5 研究区水体水化学组分与土地利用类型RDA分析 Fig. 5RDA ordination graph of hydrochemical parameters and land-use types in the study area |
地下水NO3-浓度与住宅用地呈显著正相关, 与林地和耕地的相关程度相对较弱, 且与Ca2+、Mg2+、Cl-、K+、Na+、SO42-、HCO3-的相关性较高(图 5), 说明地下水中硝酸盐来源及分布受多因素影响.地下水中Cl-浓度相对稳定, 常被用于示踪生活污水(含营养盐, 如NaCl等)及农用化肥(KCl)等人为活动对水体的影响(周迅等, 2014).NO3-和Cl-一样具有保守性质, 研究区地下水NO3-与Cl-、Na+呈较强正相关, 表明地下水中NO3-、Cl-和Na+具有相同的来源, 与生活污水输入及农业活动密切相关.研究区地下水样点分布区域位于人类活动较为密集的区域, 且周边农业种植面积较大, 地下水中硝酸盐主要来源于与人类活动有关的农用化肥、生活污水及人畜排泄物等污染源输入(孙厚云等, 2020).地下水中SO42-除来自石膏及硫酸矿物盐的溶解外, 还可能来自区域人类活动所产生的有机质的分解(Kim et al., 2015).研究区为典型喀斯特地区, 地表和地下联通性较好, 岩溶地下水通常处于氧化环境(DO:2.10~8.16 mg·L-1), 使得人类活动产生的污染物进入地下水系统后, 可能通过硝化作用和碳酸盐岩溶解导致地下水NO3-、HCO3-、Ca2+和Mg2+浓度升高, 具体反应方程式见(5)(张英, 2020).由图 5可知, 研究区地下水中NO3-与Ca2+、Mg2+和HCO3-之间较强的相关性也进一步证实了地下水中可能发生硝化作用从而导致水化学组分浓度的升高.
 | (5) |
图 6(Fig. 6)
 |
| 图 6 不同土地利用区域水体δ15N-NO3-及δ18O-NO3-变化特征 Fig. 6Variation characteristics of δ15N-NO3- and δ18O-NO3- in different land use areas |
由图 7可知, 研究区地表水、地下水大多数样点δ15N-NO3-和δ18O-NO3-值不属于特定污染源范围.其中, 地表水δ15N-NO3-和δ18O-NO3-值域主要分布于土壤有机氮范围内, 部分样点分布在与粪便污废水和化肥/降水中氨盐范围重叠区, 说明流域地表水中硝酸盐受多种来源共同影响, 其中, 农业活动是研究区地表水NO3-的重要来源, 而粪便污废水也是不可忽视的来源.通常情况下, 土壤中大部分有机氮会缓慢转化为NH4+, 而NH4+再被硝化细菌转化为NO3-, 其δ15N-NO3-值与土壤有机氮的δ15N-NO3-值相近(张妍等, 2019).研究区地表水δ15N-NO3-值在2.75‰~9.32‰之间, 说明土壤有机氮硝化作用是地表水体中NO3-的主要来源, 主要与研究区河流两侧农业种植活动密切相关.部分地下水样点δ15N-NO3-和δ18O-NO3-值分布在粪便及污废水范围内, 部分与土壤有机氮范围重叠, 地下水中硝酸盐受降水及肥料中氨盐影响较小.结合图 4和6可知, 住宅用地区地下水具有相对高的δ15N-NO3-值和NO3-含量, 且变化幅度较大, 说明城区地下水中硝酸盐来源可能受多种来源混合影响.这与前人研究得出的人口密集地区地下水中硝酸盐δ15N-NO3-值明显高于农业用地区地下水中硝酸盐δ15N-NO3-值的研究结果一致(Matiatos, 2016;Li et al., 2019).根据图 1及野外实际情况可知, 织金县城区位于地势低洼处, 四周环山, 均为城区周边出露地下水的补给区.而城区周边地区及山坡上分布有大量耕地, 以蔬菜、谷物、玉米、经果林种植为主.喀斯特地区耕地土壤土层薄, 大多为坡耕地, 截污能力差, 土壤氮素极易下渗补给地下水(张妍等, 2019;赵然等, 2020a), 导致地下水中硝酸盐含量升高.同时叠加了人为活动密集区污废水排放的影响, 导致城区周边地下水硝酸盐含量明显高于其他地区.研究区耕地、耕地 & 林地区地下水中δ15N-NO3-、NO3-含量偏低(图 4和6), 有研究表明, 地下水中来自土壤有机质腐烂的硝酸盐含量一般在0.06~12.4 mg·L-1之间(Appelo et al., 2007).本研究耕地、耕地 & 林地区地下水中硝酸盐含量通常低于10 mg·L-1, 也说明这些区域地下水硝酸盐主要受农业活动排放源影响.
图 7(Fig. 7)
 |
| 图 7 研究区水体δ15N-NO3- -δ18O-NO3-关系 Fig. 7Relationship between δ15N-NO3- and δ18O-NO3- of waters in the study area |
3.4 硝酸盐转化过程分析水体硝酸盐含量及δ15N-NO3-、δ18O-NO3-组成不仅受硝酸盐来源的影响, 同时还受生物、微生物生物地球化学过程(如硝化、反硝化作用、氨挥发等)的控制(段世辉等, 2019;Zhang et al., 2020).反硝化作用是在反硝化细菌的参与下将NO3-还原为气态产物的过程, 该过程引起的同位素分馏效应较显著(Kendall et al., 2007).在反硝化过程中微生物优先利用较轻的14N和16O同位素, 从而导致剩余NO3-富集重同位素, 且δ15N-NO3-富集值约为δ18O-NO3-富集值的1.5~2.0倍(Bottcher et al., 1990).水体溶解氧(DO)浓度可以作为判断水中是否发生反硝化作用的前提, 研究证实, 水体发生反硝化作用的DO浓度上限为2.0 mg·L-1, 当DO浓度低于2.0 mg·L-1时水体极易发生反硝化作用而造成硝酸盐同位素初始值的改变(Gillham et al., 1978;Ogrinc et al., 2019).研究区地表水DO浓度为6.17~8.29 mg·L-1, 平均值为(7.4±0.53) mg·L-1;地下水DO浓度为2.1~8.16 mg·L-1, 平均值为(6.48±1.86) mg·L-1(表 1), 整体上属于好氧环境.其中, S10和S14地下水样点DO浓度相对较低, 分别为2.1 mg·L-1和3.1 mg·L-1, 具有较高的δ15N-NO3-和δ18O-NO3-值, 但同时NO3-含量也相对较高, 分别为26.9 mg·L-1和63.52 mg·L-1, 不符合反硝化作用发生导致δ15N-NO3-、δ18O-NO3-随NO3-浓度降低而升高的整体趋势(Heaton, 1986).同时, 研究区水体δ15N-NO3-与δ18O-NO3-比值均不在反硝化作用建议的1∶1~2∶1区间内, 表明流域水体硝酸盐的转化过程中反硝化作用不明显, 主要是因为研究区属于典型喀斯特地区, 地表岩溶发育, 地表水和地下水交换频繁, 地下水停留时间短, 一定程度上限制了水中反硝化作用的发生.此外, 有研究表明高浓度的NH4+-N会提高水体硝化速率(Zaman et al., 1999).本研究地表水NH4+-N含量普遍较高(表 1), 为水中硝化作用提供了充足的条件, 也进一步证实硝化作用是研究区水体氮转化的主要过程, 反硝化作用并未对水体δ15N-NO3-和δ18O-NO3-值产生分镏.
硝化作用是硝化细菌在氧化环境中将NH4+转变为NO3-的过程, 属于耗氧反应, 因此, 硝化过程可以通过δ18O-NO3-值来识别(Ogrinc et al., 2019).在没有动力分馏的条件下, 微生物诱导硝化作用产生的NO3-中有1个氧原子来源于水中溶解氧, 另外2个氧原子来源于水体, 预期δ18O-NO3-值可以通过方程式:δ18O-NO3- =2/3 δ18O-H2O + 1/3 δ18O-air来估算(Mayer et al., 2001), 且最终形成的硝酸盐δ18O-NO3-值应基本介于-10‰~10‰之间(Kendall et al., 2007).研究区地表水δ18O-H2O值在-9.24‰~-7.13‰之间, 地下水δ18O-H2O值在-9.11‰~-3.78‰之间(Li et al., 2018), 大气中δ18O-air理论值为23.5‰, 计算得出地表水的δ18O-NO3-理论值为1.66‰~3.08‰, 地下水的δ18O-NO3-理论值为1.76‰~5.31‰.由表 2可知, 地表水中除R9、R11、R12、R15样点δ18O-NO3-值低于理论值外, 其余大部分在理论值范围内, 有的明显高于理论值, 而地下水样点的δ18O-NO3-值总体均在理论值范围内, 表明研究区大部分地表水和地下水中硝酸盐的形成过程以硝化作用为主导.水中氨挥发过程是一个物理化学过程, 受水体pH控制, 当pH值大于临界值9.3时, 可促进水中氨的挥发.研究区地表水和地下水的pH值均未超过9.3, 因此不存在氨挥发的可能性.
3.5 硝酸盐来源定量识别基于各来源氮、氧同位素组成和SIAR混合模型, 对研究区地表水和地下水中硝酸盐来源贡献进行定量识别, 各端元贡献比如图 8所示.由图可知, 地表水硝酸盐来源贡献中, 化肥、土壤有机氮、粪便及污水对硝酸盐来源的贡献率分别达27.97%、50.24%和20.73%, 其中以土壤有机氮贡献比例最高, 大气降水贡献率较低.地下水中硝酸盐来源贡献与地表水相似, 其中, 土壤有机氮贡献比例增加到54.58%, 化肥来源贡献比例降低至24.58%, 粪便及污水贡献比例为20.15%.根据SIAR分析结果可知, 地表水和地下水中硝酸盐来源均以农业源(土壤有机氮和化肥)占主导, 一方面由于研究区农业耕种历史悠久, 随着城市化进程加快, 占用了周边大量耕地, 以往长期种植过程中过量施肥逐渐积累在土壤中;加之研究区岩溶地貌发育, 地表河流和地下水出露泉点分布于地势低洼地带, 土壤中氮素、化肥等极易淋滤、下渗进入区域水体, 导致土壤有机氮和化肥成为区域地表水和地下水硝酸盐的主要来源.另一方面, 织金县城近年来处于城镇化进程中, 城区河道硬化, 污水管网不断完善, 生活污水很难直接进入地下含水层, 从而降低了水体粪便和污水贡献源.此外, 根据当地施肥时节, 春季为农耕施肥高峰期, 采样时为夏季(8月), 频繁的降雨冲刷使土壤中过量的氮素进入地表水和地下水, 加剧了水中硝酸盐污染(张妍等, 2019;Zhang et al., 2020), 因此, 土壤有机氮和化肥来源是该时期水体硝酸盐的主要贡献来源.
图 8(Fig. 8)
 |
| 图 8 基于SIAR模型计算的水体硝酸盐来源贡献比例 Fig. 8Proportional contribution of four nitrate sources estimated by SIAR in surface water and groundwater |
考虑到水体硝酸盐来源贡献可能受不同土地利用方式的影响, 通过SIAR模型定量计算不同土地利用类型区域地表水和地下水中硝酸盐来源贡献比, 具体如图 9所示.结果显示, 不同土地利用方式下地表水中硝酸盐来源贡献以化肥和土壤有机氮为主, 其次为粪便及污水贡献.其中, 粪便及污水来源贡献呈住宅用地(25.52%)>耕地(23.7%)>耕地 & 林地(21.42%)的特征, 化肥来源贡献呈耕地 & 林地(36.23%)>耕地(32.64%)>住宅用地(31.26%)的特点.与地表水相比, 不同土地利用方式对地下水中硝酸盐来源贡献影响更明显, 其中, 化肥来源贡献为耕地 & 林地(34.6%)>耕地(31.9%)>住宅用地(23.41%), 土壤有机氮来源贡献为耕地 & 林地(46.58%)>住宅用地(36.33%)>耕地(31.22%), 粪便及污水来源贡献为住宅用地(38.63%)>耕地(19.04%)>耕地 & 林地(15.96%).以上结果表明, 研究区不同土地利用方式对地表水和地下水中硝酸盐来源贡献有较大影响, 农业源(土壤有机氮、化肥)是区域水体重要的硝酸盐来源, 其次为城镇居民粪便及污水输入源.
图 9(Fig. 9)
 |
| 图 9 研究区水体硝酸盐来源贡献率 Fig. 9Contribution rate of nitrate sources in the study area |
4 结论(Conclusions)1) 研究区地表水和地下水水质特征及硝酸盐含量差异较大, 地表水水化学类型主要为SO4·Cl-Ca·Mg型, 地下水水化学类型主要为HCO3-Ca·Mg型.水中溶解性无机氮以硝态氮为主, 地表水NO3-含量为3.29~9.7 mg·L-1, 而地下水NO3-含量为5.94~63.52mg·L-1, 整体上呈现地下水硝酸盐污染比地表水严重的特征.
2) 水化学及硝酸盐氮、氧同位素结果表明, 水体NO3-含量及分布主要受不同土地利用方式的影响, 总体呈现住宅用地区水体NO3-含量高于耕地 & 林地和耕地的特征.水体硝酸盐主要来源于土壤有机氮、化肥及粪便污水;硝化作用是研究区水体硝酸盐转化的主导过程, 基本不存在反硝化作用.
3) SIAR模型结果显示, 研究区地表水和地下水硝酸盐来源贡献受不同土地利用方式影响明显, 其中, 农业来源(化肥、土壤有机氮)贡献高达75%以上, 城镇化过程中粪便及污水排放来源贡献占20%, 大气降水来源贡献较低.在研究区水污染防治和管控过程中, 应加强区域农业活动的管理、提高化肥的使用效率, 规范城镇建设用地, 加强污废水排放监管, 以减少农业活动和城镇化建设对区域水体水质的影响.
参考文献
| Appelo C A J, Postma D. 2007. Geochemistry, Groundwater and Pollution[M]. (Second Edition). Rotterdam: Balkema. |
| Bakalowicz M. 2005. Karst groundwater: a challenge for new resources[J]. Hydrogeology Journal, 13(1): 148-160. DOI:10.1007/s10040-004-0402-9 |
| Bottcher J, Strebel O, Voerkelius S, et al. 1990. Using isotope fractionation of nitrate-nitrogen and nitrate-oxygen for evaluation of microbial denitrification in a sandy aquifer[J]. Journal of Hydrology, 114: 413-424. DOI:10.1016/0022-1694(90)90068-9 |
| 陈登齐, 宋小庆. 2012. 贵州省织金县四方井岩溶大泉断流原因浅析[J]. 贵州地质, 29(2): 94-98. |
| 段世辉, 蒋勇军, 张远瞩, 等. 2019. 岩溶槽谷区地下河硝酸盐来源及其环境效应: 以重庆龙凤槽谷地下河系统为例[J]. 环境科学, 40(4): 1715-1725. DOI:10.3969/j.issn.1000-6923.2019.04.045 |
| Fathmawati, Fachiroh J, Gravitiani E, et al. 2017. Nitrate in drinking water and risk of colorectal cancer in Yogyakarta, Indonesia[J]. Journal of Toxicology and Environmental Health Part A, 80(2): 120-128. DOI:10.1080/15287394.2016.1260508 |
| Ghasemizadeh R, Hellweger F, Butscher C, et al. 2012. Review: Groundwater flow and transport modeling of karst aquifers, with particular reference to the North Coast Limestone aquifer system of Puerto Rico[J]. Hydrogeology Journal, 20(8): 1441-1461. DOI:10.1007/s10040-012-0897-4 |
| Gibrilla J R, Fianko S, Ganyaglo, et al. 2020. Nitrate contamination and source apportionment in surface and groundwater in Ghana using dual isotopes (15N and 18O-NO3) and a Bayesian isotope mixing model[J]. Journal of Contaminant Hydrology, 233: 103658. DOI:10.1016/j.jconhyd.2020.103658 |
| Gillham R W, Cherry J A. 1978. Field evidence of denitrification in shallow groundwater flow systems[J]. Water Quality Research Journal of Canada, 13(1): 53-71. DOI:10.2166/wqrj.1978.006 |
| Han G, Liu C. 2004. Water geochemistry controlled by carbonate dissolution: a study of the river waters draining karst-dominated terrain, Guizhou Province, China[J]. Chemical Geology, 204(1/2): 1-21. |
| Heaton T H. 1986. Isotopic studies of nitrogen pollution in the hydrosphere and atmosphere: a review[J]. Chemical Geology: Isotope Geoscience Section, 59(1): 87-102. |
| 何守阳, 雷琨, 吴攀, 等. 2019. 贵州岩溶山区城镇化进程中地下水的资源功能评价[J]. 地球科学, 44(9): 2839-2850. |
| Sabina J K, S?awomir S, Rasmus J, et al. 2016. Geochemical and isotopic study to determine sources and processes affecting nitrate and sulphate in groundwater influenced by intensive human activity-carbonate aquifer Gliwice (southern Poland)[J]. Applied Geochemistry, 76: 168-181. |
| Jia H, Howard K W, Qian H, et al. 2020. Use of multiple isotopic and chemical tracers to identify sources of nitrate in shallow groundwaters along the northern slope of the Qinling Mountains, China[J]. Applied Geochemistry, 113: 104512. DOI:10.1016/j.apgeochem.2019.104512 |
| Kalhor K, Ghasemizadeh R, Rajic L, et al. 2019. Assessment of groundwater quality and remediation in karst aquifers: A review[J]. Groundwater for Sustainable Development, 8: 104-121. DOI:10.1016/j.gsd.2018.10.004 |
| Kendall C, Elliott E. M, Wankel S D. 2007. Tracing Anthropogenic Inputs of Nitrogen to Ecosystems//Stable Isotopes in Ecology and Environmental Science[M]. John Wiley & Sons, Ltd |
| Kim H, Kaown D, Mayer B, et al. 2015. Identifying the sources of nitrate contamination of groundwater in an agricultural area (haean basin, korea) using isotope and microbial community analyses[J]. Science of the Total Environment, 533(15): 566-575. |
| Li C, Li S, Yue F, et al. 2019. Identification of sources and transformations of nitrate in the Xijiang River using nitrate isotopes and Bayesian model[J]. Science of the Total Environment, 646: 801-810. DOI:10.1016/j.scitotenv.2018.07.345 |
| Li X, Wu P, Han Z, et al. 2018. Effects of mining activities on evolution of water quality of karst waters in Midwestern Guizhou, China: evidences from hydrochemistry and isotopic composition[J]. Environmental Science and Pollution Research, 25(2): 1220-1230. DOI:10.1007/s11356-017-0488-y |
| 李耕, 韩志伟, 申春华, 等. 2019. 典型岩溶小流域水体中硝酸盐分布特征及成因: 以普定后寨河流域为例[J]. 地球科学, 44(9): 2899-2908. |
| Matiatos I. 2016. Nitrate source identification in groundwater of multiple land-use areas by combining isotopes and multivariate statistical analysis: A case study of Asopos basin (Central Greece)[J]. Science of the Total Environment, 541(15): 802-814. |
| Mayer B, Bollwerk S, Mansfeldt T, et al. 2001. The oxygen isotope composition of nitrate generated by nitrification in acid forest floors[J]. Geochimica et Cosmochimica Acta, 65(16): 2743-2756. DOI:10.1016/S0016-7037(01)00612-3 |
| Mélida G, Richard N B, Maria T A, et al. 2017. An overview of nitrate sources and operating processes in arid and semiarid aquifer systems[J]. Science of the Total Environment, 624: 1513-1522. |
| Ogrinc N, Tamse S, Zavadlav S, et al. 2019. Evaluation of geochemical processes and nitrate pollution sources at the Ljubljansko polje aquifer (Slovenia): A stable isotope perspective[J]. Science of the Total Environment, 646: 1588-1600. DOI:10.1016/j.scitotenv.2018.07.245 |
| Panno S V, Kelly W R, Martinsek A T, et al. 2010. Estimating background and threshold nitrate concentrations using probability graphs[J]. Ground Water, 44(5): 697-709. |
| Parnell A C, Inger R, Bearhop S, et al. 2010. Source partitioning using stable isotopes: coping with too much variation[J]. PLOS ONE, 5(3): 9672. DOI:10.1371/journal.pone.0009672 |
| Petitta M, Fracchiolla D, Aravena R, et al. 2009. Application of isotopic and geochemical tools for the evaluation of nitrogen cycling in an agricultural basin, the Fucino Plain, Central Italy[J]. Journal of Hydrology, 372(1): 124-135. |
| 宋小庆, 彭钦. 2012. 贵州织金县城岩溶地下水脆弱性评价[J]. 贵州地质, 29(2): 99-103. |
| 孙厚云, 卫晓锋, 贾凤超, 等. 2020. 基于多环境介质氮素和同位素的滦平盆地地下水硝酸盐来源示踪[J]. 环境科学, 41(11): 4936-4947. |
| 田永著, 韩志伟, 赵然, 等. 2020. 岩溶流域不同水体硝酸盐的来源解析[J]. 环境科学, 41(7): 3157-3164. |
| Valiente N, Carrey R, Otero N, et al. 2018. A multi-isotopic approach to investigate the influence of land use on nitrate removal in a highly saline lake-aquifer system[J]. Science of the Total Environment, 649: 631-632. |
| Yue F, Li S, Liu C, et al. 2015. Sources and transport of nitrate constrained by the isotopic technique in a karst catchment: an example from Southwest China[J]. Hydrological Processes, 29(8): 1883-1893. DOI:10.1002/hyp.10302 |
| Zaman M, Di H J, Cameron K C, et al. 1999. Gross nitrogen mineralization and nitrification rates and their relationships to enzyme activities and the soil microbial biomass in soils treated with dairy shed effluent and ammonium fertilizer at different water potentials[J]. Biology and Fertility of Soils, 29(2): 178-186. |
| Zhang H, Xu Y, Cheng S, et al. 2020. Application of the dual-isotope approach and Bayesian isotope mixing model to identify nitrate in groundwater of a multiple land-use area in Chengdu Plain, China[J]. Science of the Total Environment, 717: 137134. |
| 张妍, 毕直磊, 张鑫, 等. 2019. 土地利用类型对渭河流域关中段地表水硝酸盐污染的影响[J]. 生态学报, 39(12): 4319-4327. |
| 张英. 2020. 联用地下水年龄和稳定同位素解析硝酸盐污染源的演变[D]. 北京: 中国地质大学(北京) |
| 赵然, 韩志伟, 田永著, 等. 2020a. 岩溶流域地表水和地下水硝酸盐来源定量识别[J]. 中国环境科学, 40(4): 1706-1714. |
| 赵然, 韩志伟, 申春华, 等. 2020b. 典型岩溶地下河流域水体中硝酸盐源解析[J]. 环境科学, 41(6): 2664-2670. |
| 周迅, 朱春芳. 2014. 福建省晋江市浅层地下水硝酸盐含量特征及其水化学指示意义[J]. 地球学报, 35(2): 177-182. |
