 , 任天成, 李珍, 刘冰川, 侯慧杰
, 任天成, 李珍, 刘冰川, 侯慧杰
 , 胡敬平
, 胡敬平

华中科技大学环境科学与工程学院, 武汉 430074
收稿日期: 2018-07-28; 修回日期: 2018-11-06; 录用日期: 2018-11-06
基金项目: 国家自然科学基金(No.51608217)
作者简介: 胡少刚(1992—),男,Email:hsg@hust.edu.cn
通讯作者(责任作者): 侯慧杰,E-mail:houhuijie@hust.edu.cn
胡敬平,E-mail:hujp@hust.edu.cn
摘要: 为提高微生物电解池(MEC)利用剩余污泥产氢气和磷回收的效率,采用Fe3+、原儿茶酸(PCA)和H2O2体系预调理污泥,探究中性PCA/Fe3+/H2O2体系的试剂投加量对污泥液相总磷含量和溶解性化学需氧量(SCOD)的影响.在单因素试验的基础上,通过表面响应法(RSM)优化得到Fe3+和H2O2投加量分别为12.96 mmol·L-1和0.45 mol·L-1,液相总磷含量和SCOD含量实际值分别为(60.14±0.08)mg·L-1和(3357.67±66.37)mg·L-1,模拟效果显著.与未处理的剩余污泥MEC反应器出水相比,经过调理后的剩余污泥MEC反应器出水中的总化学需氧量(TCOD)、多糖和蛋白质的去除率分别提高了30.03%、50.16%和97.31%,氢气转化率提升了1.31倍,有效提升了MEC产氢效率.通过鸟粪石结晶回收MEC污泥上清液中的磷,发现在初始pH值为10、Mg2+浓度为0.056 mol·L-1和NH4+浓度为0.08 mol·L-1时效果最佳.鸟粪石晶体质量浓度最高可达7.6 g·L-1,晶体纯度最大为88.30%,上清液中77.55%的磷以鸟粪石的形式得到回收.在本研究最优化条件下进行中性PCA/Fe3+/H2O2体系调理剩余污泥微生物电解池产氢与磷回收全过程中产出经济价值达到2.36元.实验研究最终表明,经过Fe3+/PCA/H2O2体系调理污泥可促进污泥中磷的释放和MEC处理污泥的产氢效率,为探究污泥资源化提供了新的研究思路.
关键词:剩余污泥中性PCA/Fe3+/H2O2体系微生物电解池鸟粪石芬顿
Study on Fenton-like conditioning of sludge for hydrogen production and phosphorus recovery in microbial electrolysis cells
HU Shaogang
 , REN Tiancheng, LI Zhen, LIU Bingchuan, HOU Huijie
, REN Tiancheng, LI Zhen, LIU Bingchuan, HOU Huijie
 , HU Jingping
, HU Jingping

School of Environmental Science and Engineering, Huazhong University of Science and Technology, Wuhan 430074
Received 28 July 2018; received in revised from 6 November 2018; accepted 6 November 2018
Abstract: In order to improve the efficiency of hydrogen production and phosphorus recovery from excess sludge in microbial electrolysis cell (MEC), sludge was pretreated with Fe3+, protocatechuic acid (PCA) and H2O2. The effects of reagent dosage of PCA/Fe3+/H2O2 under neutral condition on the total phosphorus content and dissolved chemical oxygen demand (SCOD) in sludge liquid phase were investigated by single factor test. The dosages of Fe3+ and H2O2 were optimized by surface response method (RSM), with optimized values of 12.96 mmol·L-1 and 0.45 mol·L-1 respectively. The actual values of total phosphorus and SCOD in liquid phase were (60.14 ±0.08) mg·L-1 and (3357.67±66.37) mg·L-1, respectively, achieving obvious improvement with the optimized simulated parameters. Compared with the untreated effluent from the residual sludge MEC reactor, the removal rates of total chemical oxygen demand (TCOD), polysaccharide and protein in the sludge treated by MEC were increased by 30.03%, 50.16% and 97.31%, respectively. The hydrogen conversion rate was increased by 1.31 times, and the hydrogen production efficiency of MEC was also improved. Phosphorus in the supernatant of MEC sludge was reclaimed by ectopic recovery of struvite crystals under optimum pH value of 10, Mg2+ concentration of 0.056 mol·L-1 and NH4+ concentration of 0.08 mol·L-1. The mass of struvite crystal was up to 7.6 g·L-1 and the highest crystal purity was 88.30%, and 77.55% of the phosphorus in the supernatant was recovered in the form of struvite. The economic value of hydrogen and phosphorus recovered from excess sludge with the proposed system reached 2.36 yuan. The experimental results show that the Fe3+/PCA/H2O2 system can improve phosphorus release from sludge and hydrogen production efficiency in an MEC system, which provides a new research strategy for sludge recycling.
Keywords: excess sludgeneutral PCA/Fe3+/H2O2 systemmicrobial electrolysis cellsstruviteFenton
1 引言(Introduction)市政污泥是污水处理厂在处理污水过程中产生的副产物, 是由可沉淀的颗粒物所组成的固态废弃物(余杰等, 2007).这些固态废弃物含水率高, 难以脱水, 成分复杂, 含有大量的重金属、细菌、病原菌、寄生虫卵等有毒有害污染物, 但也含有丰富的有机物、N、P、K等营养元素(周芊慧, 2018).传统的污泥处理处置方式主要有土地利用、填埋、自然干化、焚烧等(Zhang et al., 2017), 但这些技术主要是将污泥作为一种废弃物进行处理处置, 处理效率较低且存在二次污染问题, 因此, 探究一种较传统处理处置方法更高效、更环保的处置技术是目前亟待解决的难题.
为了提高污泥的处理处置效果, 需要对污泥进行预处理.污泥预处理是通过物理(Banu et al., 2018)、化学(Zhou et al., 2018)和生物(Wu et al., 2018)等方法, 破坏污泥的絮体结构, 释放污泥中的有机质, 一方面使污泥中的大分子物质转化成易被生物降解的小分子物质, 实现污泥的减量化, 另一方面可将预处理后的污泥作为碳源供微生物利用, 回收污泥中的能源和有用物质.近年来, 芬顿反应作为污泥絮体有效的破胞试剂被广泛使用, 可以将污泥絮体中有机物释放到溶液当中(Yu et al., 2016).但传统的芬顿试剂也有较为明显的缺点:pH使用范围较窄(2~3)(Neyens et al., 2003), 以及Fe3+/Fe2+的循环转化率并不理想(Ma et al., 2005)等.使用螯合剂与Fe3+/H2O2构成的类Fenton反应因能够克服传统Fenton反应的缺点而被广泛应用(De Luca et al., 2014; Dong et al., 2016).近年来, 使用对环境友好的试剂原儿茶酸(PCA)作为螯合剂与Fe3+/H2O2构成类Fenton反应逐渐受到重视(Aguiar et al., 2007; Qin et al., 2015).例如, (Qin等2015)通过向Fe3+/H2O2体系中加入螯合剂原儿茶酸(PCA)降解甲草胺, 并与Fe2+/H2O2体系进行降解效果的比较, 发现PCA的加入可促进Fe2+/Fe3+的循环, 减少铁离子的沉淀, 促进· OH的产生, 从而使PCA/Fe3+/H2O2体系在中性条件和酸性条件下都比传统的Fe2+/H2O2效果要好.因此, 本研究为了增强后续微生物电解池产气和磷资源回收的作用, 拟使用芬顿反应作为污泥预处理手段.
微生物电解池(Microbial Electrolysis Cells, MECs)于2005年由Logan等首次提出(Logan et al., 2009), 其通过外加电场的作用强化微生物与电极之间的电子传递, 促进微生物的新陈代谢(Logan et al., 2008; Rozendal et al., 2007; 2008).利用MEC进行污泥中的能源回收相对于传统的污泥厌氧发酵主要有以下优点:解除了厌氧发酵末端产物的限制, 可利用发酵底物产氢, 提高了资源化效率(Lu et al., 2012a);突破了温度限制, 实现了低温制氢.例如, Lu等(2011;2012a;2012b)在4 ℃和9 ℃的条件下成功运行了微生物电解池, 从有机碳水化合物和小分子酸(VFAs)中制得氢气;微生物电解池可降解蛋白质, 相比传统厌氧发酵, 对污泥中有机物的降解更彻底.本研究拟利用MEC处理预调理污泥, 以回收污泥中的氢能源.由于预调理污泥和MEC处理污泥之后, 污泥上清液中富含磷资源, 这部分高浓度的磷资源常被忽略而未能得到合理利用, 在一定程度上造成了磷资源的浪费.
目前, 磷在生物圈的单向流动使之成为一种不可再生的宝贵资源.磷矿石的储量十分有限, 据估计, 全世界的磷矿量只能维持到21世纪中叶(Cordell et al., 2011).世界上可利用的磷资源短缺, 而污泥中含有丰富的有机物、N、P、K等营养元素(Suzuki et al., 2005), 因此, 探究一种将污泥“变废为宝”回收其营养元素磷的技术一直是研究的热点, 这不仅能防止污染, 还能通过磷的循环利用实现污泥的资源化(Song et al., 2006).目前, 从污水污泥中回收磷的方法主要包括化学沉淀法、吸附法、土地利用、生物脱磷、结晶法、离子交换法、电渗析法等(林进南, 2013).鸟粪石是一种优良的缓释肥, 通过鸟粪石结晶回收磷, 可实现污泥的磷资源的高值利用.
因此, 本研究拟用中性PCA/Fe3+/H2O2体系调理污泥, 在单因素试验的基础上, 利用表面响应法探究污泥调理前后污泥中有机物的最佳溶出条件, 并探究污泥中有机物对MEC产氢气的影响.考虑到中性PCA/Fe3+/H2O2体系调理污泥可使污泥固相中的TP释放到液相中, 另外, 为了稳定MEC运行投加的磷酸盐缓冲液(PBS)使得经过MEC运行之后的污泥上清液中富含磷资源, 这部分磷资源经常被忽略, 未得到合理的回收, 在一定程度上造成了磷资源的浪费.针对MEC运行后的污泥上清液, 本文通过鸟粪石异位结晶法探究经过MEC产氢处理之后回收污泥上清液中磷资源的可行性.
2 材料与方法(Materials and methods)2.1 污泥来源与特性本研究所使用的剩余污泥取自湖北省武汉市沙湖污水处理厂二沉池, 该污水处理厂日平均污水处理量为1.5×105 m3, 厂区主体采用厌氧-缺氧-好氧处理工艺(A2/O).经过交替的缺氧和好氧过程, 聚磷菌超量吸收污水中磷, 经过二沉池沉淀, 磷元素从污水中去除, 剩余污泥中含有较高浓度的磷.剩余污泥利用聚丙烯塑料桶采样运回, 放入4 ℃的冰箱冷藏保存.将取回的剩余污泥在4 ℃条件下静置24 h, 去除上清液得到浓缩后的剩余污泥.通过60目的细筛去除剩余污泥中的细石子、杂草等大颗粒杂质后测定剩余污泥基本理化性质(表 1).由表 1可知, 从沙湖污水处理厂取回的剩余污泥pH为6.95, 可不进行pH值的调节, 使剩余污泥保持中性条件.
表 1(Table 1)
| 表 1 浓缩后剩余污泥基本理化性质 Table 1 Characteristics of the raw sludge | ||||||||||||||||||||||||||||||||||||
表 1 浓缩后剩余污泥基本理化性质 Table 1 Characteristics of the raw sludge
| ||||||||||||||||||||||||||||||||||||
2.2 单因素试验设计本试验参考文献(Qin et al., 2018)方法, 选取反应时间、Fe3+投加量、PCA投加量和H2O2投加量进行单因素试验, 以剩余污泥液相中TP含量和SCOD为试验结果.单因素试验设计方案如表 2所示.
表 2(Table 2)
| 表 2 单因素试验设计表 Table 2 Single experimental factor design values | ||||||||||||||||||||||||||||||
表 2 单因素试验设计表 Table 2 Single experimental factor design values
| ||||||||||||||||||||||||||||||
2.3 MEC装置及操作本研究采用微生物电解池反应装置为单室瓶式反应器, 有效容积为250 mL.MEC阳极采用柱状碳刷, 阴极采用不锈钢网, 反应器另设置两个端口分别用来集气和排液, 上部集气口连接气袋以收集反应过程中产生的气体, 下部排液口使用止水夹密封.MEC反应器底部放置磁力搅拌转子, 通过搅拌器控制转速, 使反应器内的电解质混合均匀, 具体装置如图 1所示.
图 1(Fig. 1)
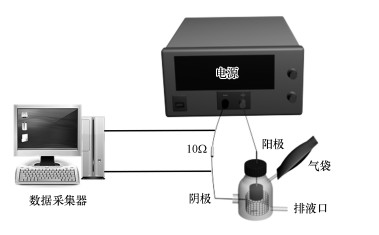 |
| 图 1 MEC实验装置图 Fig. 1A schematic diagram of the MEC reactor |
2.4 MEC的启动与运行本研究中MEC反应器以运行稳定的MFC出水为接种物, 2 g · L-1的乙酸钠溶液作为底物, 100 mmol · L-1的磷酸盐缓冲溶液(Phosphate buffer solution, PBS)为缓冲液, 电解质总体积为200 mL.将MFC出水与磷酸盐缓冲液(PBS)按一定体积比混合, 得到反应液.向反应液中通过高纯氮(纯度达99.999%)15 min, 去除电解质中的氧气.通过恒压直流电源施加的电压为1.0 V, MEC系统外部串联电阻值为10 Ω的电阻, 电阻两端连接数据采集器(型号2750, 美国泰克科技有限公司)以检测采集外接电阻两端电压.
MEC反应器以序批式运行, 当反应装置回路电阻两端电压降至1 mV以下时, 更换新的电解质溶液, 由此驯化并富集阳极微生物, 直到电阻两端电压持续3个批次保持稳定, 说明MEC反应器启动成功.在MEC稳定的条件下, 将剩余污泥与磷酸盐缓冲液(PBS)按一定体积比(3 : 1)混合, 得到反应污泥溶液, 以替换之前启动过程中的反应液, 并于25 ℃的恒温下运行.
2.5 数据检测与分析污泥化学需氧量(COD)采用快速消解分光光度法测定;溶解性多糖采用硫酸苯酚法测定;溶解性蛋白质采用Folin-酚试剂法测定;总悬浮固体(TSS)/挥发性悬浮物(VSS)采用国标称重法测定;污泥中总磷采用钼酸铵分光光度法测定;挥发性脂肪酸(VFAs)用气相色谱仪(GC-2030, 日本Shimadzu)进行测量;利用MEC处理剩余污泥产生的气体通过气袋收集, 通过注射器将气袋中的气体全部抽出, 计算测得气体体积, 用气相色谱仪(GC-2030, 日本Shimadzu)检测气体组分, 色谱柱为毛细管柱Carboxen-1010 PLOT Capillary Column(30 m×0.53 mm)(SUPELCO, Sigma-Aldrich公司).
氢气产率(HY)是通常用来评价MEC产氢能力的指标, 具体是指MEC中阳极微生物菌种降解单位质量有机物(以COD计)所产生的氢气量, 计算公式如下所示:
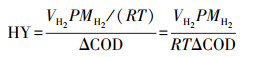 | (1) |
库伦效率(CE)是指在MEC体系中, 阳极微生物降解反应器中有机物的过程中, 转化为电路中的实际电量(Q)与同样底物被氧化转化为电路的理论电量(QT)的比值, 计算过程如下所示:
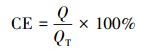 | (2) |
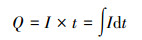 | (3) |
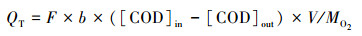 | (4) |
氢气转化率(EH)为单位电路理论电量下实际生成H2的电子总量, 计算过程如式(5)所示, 其中, QH为生成的H2的总电子量, 计算过程见式(6).
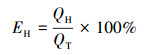 | (5) |
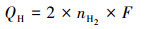 | (6) |
能量转化效率(ηW)为生成的H2的能量与外加电源输入的能量的比值, 计算过程如下所示:
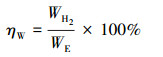 | (7) |
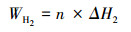 | (8) |
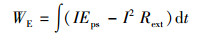 | (9) |
由于自然界中大部分铵盐为可溶性化合物, 一定pH条件下, 结晶中的NH4+只存在于鸟粪石中.因此, 鸟粪石结晶的纯度可通过检测结晶中NH4+的物质的量而确定, 计算过程如下所示:
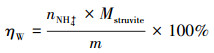 | (10) |
3 结果与讨论(Results and discussion)3.1 中性PCA/ Fe3+/H2O2体系调理剩余污泥试验条件优化3.1.1 影响污泥液相总磷含量和SCOD的污泥调理条件的单因素分析由图 2a可知, 调理开始至120 min时间段内, 液相中总磷(TP)含量先增大后趋于平稳, SCOD随时间的变化趋势在0~120 min内与液相中TP含量的变化趋势一致.反应时间过长会造成成本的增加和时间的浪费, 结合调理剩余污泥液相中TP含量和SCOD的变化趋势, 综合考虑实验成本、能源损耗等因素, 本研究调理反应时间取120 min较为适宜.
由图 2b可知, 调理污泥上清液TP含量和SCOD随着Fe3+投加量的增加先增大后减小.在Fe3+投加量为12 mmol · L-1时, 此时, n(PCA):n(Fe3+)=1.5 : 1, 液相中TP含量和SCOD达到最大, 而Fe3+投加量小于12 mmol · L-1时, 溶液中过量的PCA与· OH反应, 消耗了部分· OH, 从而使污泥破解效果变差;Fe3+投加量大于12 mmol · L-1时, 过量的Fe3+与溶液中的正磷酸盐反应生成难溶的磷酸铁沉淀, 使上清液TP含量降低.
由图 2c可知, 随着H2O2投加量的增加, 上清液TP含量和SCOD呈先增大后减小的趋势.H2O2投加量不足无法产生足够的· OH, 使氧化破解反应不充分;然而过量的H2O2与溶液中的还原性有机质反应, 造成SCOD的降低, 同时, H2O2与溶液中的· OH反应, 消耗了溶液中的H2O2和· OH, 使污泥破解效果变差.结果表明, H2O2投加量为0.4 mol · L-1时调理效果最佳.
图 2(Fig. 2)
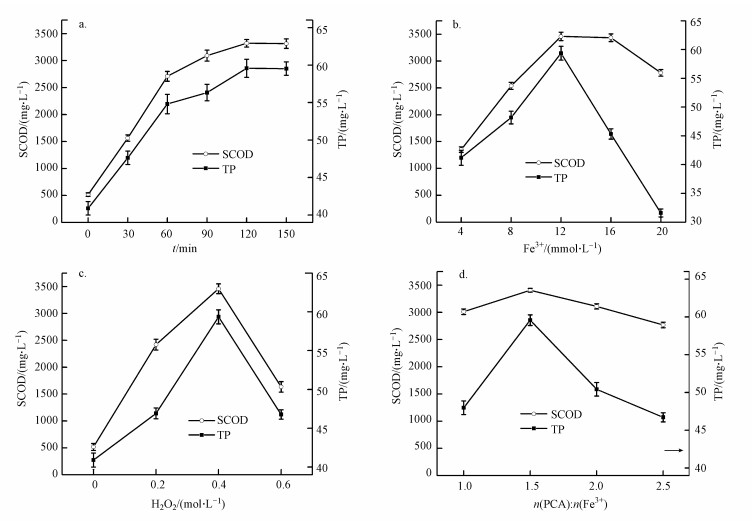 |
| 图 2 不同反应条件对污泥上清液总磷(TP)含量和SCOD的影响(a.时间;b.Fe3+投加量;c.H2O2投加量;d. n(PCA):n(Fe3+)) Fig. 2Effects of different reaction conditions on total phosphorus (TP) content and SCOD in sludge supernatant (a. reaction time; b. amount of Fe3+ addition; c. amount of H2O2 addition; d. molar ratio of n(PCA):n(Fe3+)) |
不同n(PCA):n(Fe3+)值对剩余污泥液相中TP含量和SCOD的影响规律见图 2d.当n(PCA) : n(Fe3+)=1.5 : 1时, 剩余污泥液相中TP含量和SCOD达到峰值, 分别为59.57 mg · L-1和3406.33 mg · L-1.PCA在反应中作为一种螯合剂, 与Fe3+反应生成络合物(Nam et al., 2001), 并与H2O2反应, 使H2O2分解产生· OH, 从而氧化分解污泥中的有机物.但过量的PCA与剩余污泥中的有机物质争夺· OH, 剩余污泥中的一部分· OH与PCA反应(Rivas et al., 2005), 使PCA矿化生成CO2和H2O, 从而消耗剩余污泥中一部分的· OH, 导致污泥破胞效果变差.因此, PCA/Fe3+比对实验效果有重要影响, 结果表明, n(PCA) : n(Fe3+)=1.5 : 1时调理效果最佳.
3.1.2 表面响应法最优化试验条件及分析为得到PCA/Fe3+/H2O2体系调理剩余污泥最佳效果的优化条件, 在反应时间为120 min和n(PCA):n(Fe3+)=1.5 : 1的条件下, 利用表面相应法对Fe3+投加量和H2O2投加量进行优化.响应曲面模型选取中心复合设计(Central Composite Design, CCD), 以Fe3+投加量(X1)和H2O2投加量(X2)为自变量, 剩余污泥液相中TP含量(Y1)和SCOD(Y2)作为响应值.Fe3+投加量和H2O2投加量中间值选择单因素试验最佳数值.表 3为实验因素和水平设计值.
表 3(Table 3)
| 表 3 试验因素和水平设计值 Table 3 Experimental factors and horizontal design values | ||||||||||||||||||
表 3 试验因素和水平设计值 Table 3 Experimental factors and horizontal design values
| ||||||||||||||||||
用Design Expert 8.0软件将表 3中数据通过CCD模拟和试验, 得到表 4所示试验结果.将表 4中的试验结果进行回归方程分析, 建立剩余污泥液相中TP含量与Fe3+投加量和H2O2投加量之间的二次回归方程:
 | (11) |
| 表 4 CCD优化的预测值与实际值 Table 4 Composite Design matrix and the actual and predicted response results | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 4 CCD优化的预测值与实际值 Table 4 Composite Design matrix and the actual and predicted response results
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
式中, Y1为剩余污泥液相中TP含量(mg · L-1);X1为Fe3+投加量(mmol · L-1);X2为H2O2投加量(mol · L-1).
由表 4可知, 剩余污泥液相中TP含量的实际值与预测值一致性良好, 回归系数R2=0.9062.模型的F值为9.66, p值(Prob>F)= 0.0132 <0.05, 说明该二次方程模型显著, 能很好地模拟Fe3+投加量和H2O2投加量对剩余污泥液相中TP含量(响应值Y1)的影响.
同时,本研究建立了剩余污泥液相中SCOD与Fe3+投加量和H2O2投加量之间的二次回归方程:
 | (12) |
由表 4可知, 剩余污泥液相中SCOD的实际值与预测值一致性良好, 回归系数R2=0.8431.模型的F值为5.37, p值(Prob>F)=0.0443 < 0.05, 说明该二次方程模型显著, 能很好地模拟2个因素对SCOD(响应值Y2)的影响.
综上可以得到, Fe3+投加量和H2O2投加量对上清液总磷含量交互影响作用显著, 上清液总磷含量随Fe3+投加量和H2O2投加量的增大呈先增大后减少.其中, 随着H2O2投加量的增大, 上清液总磷含量先增大后小幅下降, 与Fe3+投加量的趋势几乎一致.
依照上述试验结果进行优化, 优化条件见表 5, 优化目标为在剩余污泥液相中TP含量和SCOD达到最大值的条件下, 使Fe3+投加量和H2O2投加量最小化.
表 5(Table 5)
| 表 5 CCD模型优化条件 Table 5 The optimization conditions of the CCD model | |||||||||||||||||||||||||
表 5 CCD模型优化条件 Table 5 The optimization conditions of the CCD model
| |||||||||||||||||||||||||
最终得到的试验结果见表 6, 剩余污泥液相中TP含量为(60.14±0.08) mg · L-1, SCOD为(3357.67±66.37) mg · L-1, 剩余污泥液相中TP实际值与预测值的相对标准偏差(RSD)为1.79%, 剩余污泥液相中SCOD实际值与预测值的RSD为5.19%, 在可接受范围内, 这说明此次RSM优化结果可信度较高.
表 6(Table 6)
| 表 6 CCD优化结果 Table 6 Optimization results of the CCD model | ||||||||||||||||||||||||||||||||||
表 6 CCD优化结果 Table 6 Optimization results of the CCD model
| ||||||||||||||||||||||||||||||||||
3.2 调理剩余污泥对MEC性能的影响利用响应面法得到的最优化条件对剩余污泥进行调理, 调理完成后剩余污泥的基本理化特性见表 7.中性PCA/Fe3+/H2O2体系调理剩余污泥后上清液中SCOD、溶解性多糖和溶解性蛋白质含量显著增加, 分别是未处理生物污泥的5.49、15.15和3.03倍, TSS和VSS则分别减少了21.42%和45.98%.这表明经过中性PCA/Fe3+/H2O2体系调理后剩余污泥结构和胞外聚合物被破坏, 为后续MEC回收氢气和磷元素提供了有利条件, 这与文献中(Xiao et al., 2018)通过将污泥调成碱性并加热预处理, 释放污泥中的有机物, 能够增强MEC对有机物的利用, 使MEC的产甲烷量最高能提高79.3%的结论一致.
表 7(Table 7)
| 表 7 调理后剩余污泥基本性质 Table 7 The characteristics of the waste activated sludge and after pretreatments | ||||||||||||||||||||||||||||||||||||
表 7 调理后剩余污泥基本性质 Table 7 The characteristics of the waste activated sludge and after pretreatments
| ||||||||||||||||||||||||||||||||||||
从表 1可以得到原泥中溶解性蛋白质为(493.53±12.66) mg · L-1, 溶解性多糖为(24.58±2.37) mg · L-1.原泥进入MEC装置之后, MEC处理剩余污泥有机物的去除率结果如图 3a所示, 污泥中多糖去除率为45.39%, 蛋白质去除率为29.41%.因为MEC中的微生物更加容易利用多糖(Montpart et al., 2015), 因此, 多糖去除率大于蛋白质去除率.当中性PCA/Fe3+/H2O2体系调理污泥之后, 从表 7可以得到污泥中的溶解性蛋白质为(1988.18±45.98) mg · L-1, 溶解性多糖为(445.5±34.15) mg · L-1, 污泥溶液中的蛋白质含量大幅增加, 因此, MEC中的微生物能够更加容易地利用蛋白质, 蛋白质去除率从29.41%增加到58.03%, 提高了97.31%.但污泥经过中性PCA/Fe3+/H2O2体系调理之后的多糖增加量相对蛋白质增加量较少, 因此, 进入MEC处理之后的多糖去除率从45.39%增加到68.16%, 只提高了50.16%.总体而言, 中性PCA/Fe3+/H2O2体系调理污泥之后, 由于污泥固相中蛋白质与多糖的释放, 以及污泥的水溶性提高, MEC系统中的微生物更容易吸收利用污泥中的有机物进行反应, 使污泥中蛋白质和多糖的利用率明显提高, 从而改善了MEC系统中微生物产氢效果.
图 3(Fig. 3)
 |
| 图 3 MEC对调理污泥中有机物的影响(a.有机物的变化; b.挥发性脂肪酸的变化; R-S:原污泥;F-S:调理过的剩余污泥) Fig. 3Effects of MEC on organic matter in conditioned sludge (a.the changes of organic matter; b.the changes of VFAs) |
MEC处理的剩余污泥的VFAs含量(以COD计)与组分如图 3b所示.由图可知, 反应污泥内主要含有乙酸、丙酸、异丁酸、正丁酸等小分子有机酸, 其中, 乙酸的含量最高, 丙酸的含量明显较少, 仅为原泥的45.57%, 调理污泥中异丁酸和丁酸总含量为原泥的83.57%, MEC对污泥中有机酸的利用率增加了25.83%.MEC反应器内的微生物更容易利用污泥中的有机酸, 使得更多的有机酸被微生物降解利用, 从而使污泥中的有机物能够更好地转换成氢气.
调理剩余污泥对MEC产氢性能的影响如表 8所示.由表可知, 污泥调理对MEC产氢具有明显的促进效果, 污泥的氢气产率和氢气转化率均增加了1.31倍, 使得更多的有机质被产氢菌利用产生氢气, 从而提高了污泥的资源化利用.同时, 污泥是一个极其复杂的系统, 产电菌与发酵细菌的共同作用使得污泥被有效降解利用, 随着大量有机物被产氢菌所降解, 导致电子的供体出现不足, 进而使得反应器的库伦效率不高, 调理污泥作为底物时, 库伦效率仅为38.09%, 而原泥作为底物时, 库伦效率更低, 只有33.5%.文献中报道(Wang et al., 2010), 通过优化反应器结构, 在阳极添加颗粒状的活性炭减小反应器的电阻可使MEC的氢气转换率从11.6%提高到35.5%, 后续可通过改变反应器构造来进一步增加氢气转换率.
表 8(Table 8)
| 表 8 调理剩余污泥对MEC产氢性能的影响 Table 8 The effects of conditioned sludge on hydrogen production performance of MEC | |||||||||||||||
表 8 调理剩余污泥对MEC产氢性能的影响 Table 8 The effects of conditioned sludge on hydrogen production performance of MEC
| |||||||||||||||
3.3 鸟粪石异位结晶回收MEC污泥上清液中的磷经测量, MEC处理剩余污泥出水上清液的基础理化性质见表 9.MEC出水中NH4+和Mg2+的含量不能将原有的PO43-全部以鸟粪石的形式沉淀.为了提高剩余污泥中磷的回收率, 最大程度地回收磷元素, 可取MEC出水上清液50 mL并通过向MEC出水上清液中添加适量镁源和氮源, 使合成鸟粪石各组分达到最适比值, 实现MEC处理剩余污泥出水上清液中磷的最大化利用.
表 9(Table 9)
| 表 9 MEC处理剩余污泥后出水上清液基础理化性质 Table 9 The physicochemical properties of effluent from MEC treated sludge | ||||||||||
表 9 MEC处理剩余污泥后出水上清液基础理化性质 Table 9 The physicochemical properties of effluent from MEC treated sludge
| ||||||||||
图 4a为初始pH对鸟粪石异位结晶回收MEC处理剩余污泥中磷效果的影响.由图可知, pH=9.5时, 鸟粪石晶体质量达到0.47 g, 纯度为56.16%;当pH为10时, 鸟粪石结晶纯度达到最大, 而晶体质量反而偏小;pH增至11时, 鸟粪石晶体质量迅速增大, 结晶纯度却只有15.94%.推测原因为pH=11时, 上清液中的NH4+与OH-反应生成NH3逸出, 同时在试验时亦能闻到NH3刺鼻的气味, 使得上清液中NH4+浓度下降, 从而造成结晶中鸟粪石纯度下降.因此, 为得到较纯的鸟粪石结晶, 上清液初始pH不应超过11.图 4b所示为不同初始pH条件下得到的鸟粪石晶体的XRD图.通过对比鸟粪石标准卡片分析可知, 不同初始pH条件下的产物中均发现了鸟粪石和磷酸镁(Mg3(PO4)2·22H2O), 但未发现其他晶体物质.在pH为9.5~10.5时, 结晶XRD图谱中的强峰改变, 第2个标记的特征峰与标准卡片相比差异明显, 说明结晶的主要物相发生了改变;在pH=11时, 与标准卡片对比, 结晶XRD图谱中标记的3条鸟粪石特征峰出现了左偏, 说明结晶中鸟粪石纯度不高.过大的pH反而会降低鸟粪石纯度, 但其中也可能受NH4+浓度的制约, 因此, 为提高结晶中鸟粪石纯度和质量, 调节适宜的pH和添加适量的NH4+是必要的.综合考虑, 初始pH为10时污泥中磷的回收效果最佳.
图 4(Fig. 4)
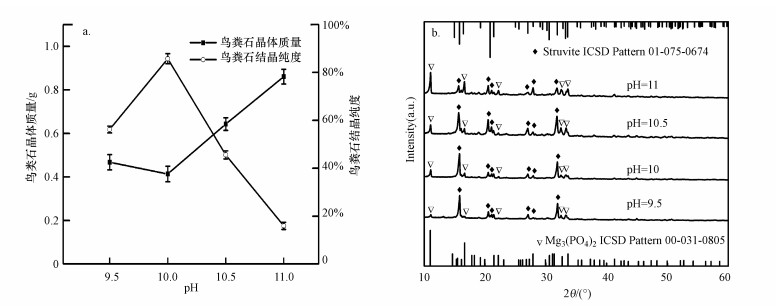 |
| 图 4 不同初始pH下鸟粪石的质量与纯度的变化(a)及鸟粪石晶体的XRD图(b) Fig. 4The changes in quality and purity(a) and XRD patterns (b) of struvite under different initial pH |
图 5a为Mg2+投加量对鸟粪石异位结晶回收MEC处理剩余污泥中磷效果的影响.由图可知, Mg2+投加量由0.044 mol · L-1增至0.056 mol · L-1时, 鸟粪石结晶质量缓慢增加, 但纯度没有明显提升.随着Mg2+投加量继续增加, 鸟粪石结晶纯度下降明显, 由87.36%下降至40.39%, 下降了53.77%, 鸟粪石晶体质量却增加了85.37%.结合图 5b中不同Mg2+投加量下鸟粪石晶体的XRD图分析可知, 晶体中皆检测到磷酸镁结晶(Mg3(PO4)2·22H2O)和碳酸镁(MgCO3), 由此造成了鸟粪石晶体纯度偏低.在Mg2+投加量为0.056 mol · L-1时, 结晶中鸟粪石的质量达到最高.综合考虑, 当Mg2+投加量为0.056 mol · L-1时, 对鸟粪石异位结晶回收剩余污泥中磷效果最佳.
图 5(Fig. 5)
 |
| 图 5 不同Mg2+投加量下鸟粪石的质量与纯度的变化(a)及鸟粪石晶体的XRD图(b) Fig. 5The changes in quality and purity (a) and XRD patterns(b) of struvite under different initial Mg2+ dosage |
不同NH4+投加量下鸟粪石的质量与纯度的变化及XRD图见图 6, 通过补充NH4+量, 鸟粪石结晶的纯度明显提高, 鸟粪石结晶纯度皆大于60%, 相比于不添加NH4+时鸟粪石结晶纯度不高于50%的结果, 有着明显的区别.当NH4+投加量为0.08 mol · L-1时, 鸟粪石晶体质量最高可达0.38 g, 上清液中鸟粪石晶体质量浓度可达7.6 g · L-1, 鸟粪石结晶纯度更是达到了最大值88.3%, 上清液中77.55%的磷以鸟粪石的形式得到回收.Almotouq等(2017)用双室MEC处理污泥, 在阴极添加一定量的磷酸盐缓冲液, 在最佳条件下, 鸟粪石结晶最大效率可达95%, 表明MEC可有效回收磷资源.之后, 随着NH4+投加量的增加, 鸟粪石纯度开始下降至62.5%.以上结果表明, NH4+投加量对鸟粪石纯度有着显著的影响, 在一定范围内, 当NH4+投加量增加时, 纯度增大;同时, 在鸟粪石晶体质量方面, 随着NH4+投加量的增加, 鸟粪石晶体质量降低.这可能是因为NH4+含量的增加可使上清液pH下降, 导致鸟粪石溶解度增大, 析出的鸟粪石结晶质量减少, 进而使结晶纯度下降, 结晶质量减少.通过沉淀结晶的XRD图谱与鸟粪石标准卡片ICSD Pattern 01-075-0674对比发现, 结晶XRD图谱与标准卡片拟合度较高, 图中标记出5条强度明显的特征谱线, 与卡片中的特征谱线一一对应, 图谱的特征峰峰形明显且未出现偏移, 说明此时沉淀物中物相为鸟粪石, 鸟粪石晶体的纯度较高.综合考虑鸟粪石晶体的质量和结晶纯度, NH4+投加量为0.08 mol · L-1时, 对鸟粪石回收MEC处理剩余污泥中磷效果最佳.
图 6(Fig. 6)
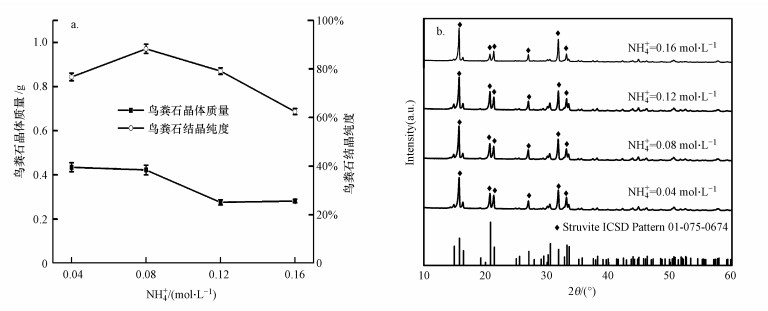 |
| 图 6 不同氨氮投加量下鸟粪石的质量与纯度的变化(a)及鸟粪石晶体的XRD图(b) Fig. 6Changes in quality and purity(a) and XRD patterns(b) of struvite under different initial NH4+ dosage |
3.4 经济效益分析以本研究中固体含量为11.81 g · L-1、体积为250 mL的剩余污泥作为处理对象, 回收其中的能源与磷资源进行经济性分析.以本研究得到的中性PCA/Fe3+/H2O2体系调理剩余污泥最优化条件为标准, 核算中性PCA/ Fe3+/H2O2体系调理剩余污泥的投入成本.同时, 以本研究得到的鸟粪石异位结晶回收所得到的最优化条件核算鸟粪石异位合成的成本.试剂单价为从供货商处的实际购买金额, 电费取武汉市居民用电的平均值.本文经济效益分析中不考虑烧杯等试验容器和测试仪器的购置成本, 只考虑在本研究的基础上, 从剩余污泥调理到MEC产氢和异位结晶回收鸟粪石的全过程中物料和能源消耗及产出价值.本研究的投入与产出经济分析见表 10.由表 10可知, 在本研究最优化条件下进行中性PCA/ Fe3+/H2O2体系调理剩余污泥微生物电解池产氢与磷回收全过程中, 物料消耗和能源消耗的总成本为0.53元, 而总产出经济价值达到2.89元, 大大高于成本.在实际情况下, 氢气热值转化率不会到100%, 实际经济价值稍微小于理论计算值.虽然本研究中需要加入一些化学试剂, 但这些试剂的使用量和成本均比较低, 成本主要来自电能的消耗.本研究中所产出的能源和物质属于高附加值的产物, 具有较高的经济价值, 可以实现盈利, 对实际工程应用具有较好的指导意义.在产业化应用中, 微生物电解池中制取的高纯度氢气转化成电能可以减少电能的消耗, 实现能源供给.鸟粪石作为优质的磷肥出售, 获得的经济价值可以保证项目良好的运营并实现盈利.
表 10(Table 10)
| 表 10 最优化条件下经济效益分析 Table 10 Economic benefit analysis under optimum conditions | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
表 10 最优化条件下经济效益分析 Table 10 Economic benefit analysis under optimum conditions
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
本研究由于前期思考的不足和实验室条件的限制, 在试验过程中仍然存在一些不足.鸟粪石异位结晶的方式在后续试验中也可改为微生物电解池原位回收的方式, 外加氨氮和镁源的方式也需要更进一步探索成本更加低廉的方式, 如利用垃圾渗滤液来提供氨氮, 利用富含镁元素的矿渣来提供镁源等方式, 使成本进一步降低.同时, 还需要探索提高生物污泥在微生物电解池体系中同步产氢与磷回收的更加高效的方式.
4 结论(Conclusions)1) 单因素试验结果表明, 各因素独立作用时得到PCA/Fe3+/H2O2体系调理剩余污泥效果较佳的条件为:反应时间为120 min, n(PCA):n(Fe3+)=1.5 : 1, Fe3+和H2O2投加量分别为12 mmol · L-1和0.4 mol · L-1.RSM最优化条件分析试验结果表明, Fe3+和H2O2投加量分别为12.96 mmol · L-1和0.45 mol · L-1时对剩余污泥破胞效果最佳.
2) 污泥经中性PCA/Fe3+/H2O2体系调理再通过微生物电解池(MEC)处理后, 调理污泥中TCOD、多糖和蛋白质的去除率分别提高了30.03%、50.16%和97.31%, 且MEC对污泥中有机酸的利用率增加, 同时, MEC中利用调理后的剩余污泥的氢气转化率提升了1.31倍.
3) 通过鸟粪石异位结晶回收MEC污泥上清液中磷的方式可行, 且在初始pH值为10、Mg2+浓度为0.056 mol · L-1和NH4+浓度为0.08 mol · L-1时效果最佳.鸟粪石晶体质量浓度最高可达7.6 g · L-1上清液, 晶体纯度最大为88.30%, 上清液中77.55%的磷以鸟粪石的形式得到回收.
4) 本研究对中性PCA/ Fe3+/H2O2体系调理剩余污泥微生物电解池产氢与磷回收全过程中经济效益进行了计算, 结果显示, 产出的经济效益大大高于投入的成本.
参考文献
| Aguiar A, Ferraz A. 2007. Fe3+ and Cu2+ reduction by phenol derivatives associated with Azure B degradation in Fenton-like reactions[J]. Chemosphere, 66(5): 947–954.DOI:10.1016/j.chemosphere.2006.05.067 |
| Almatouq A, Babatunde A O. 2017. Concurrent hydrogen production and phosphorus recovery in dual chamber microbial electrolysis cell[J]. Bioresource Technology, 237: 193–203.DOI:10.1016/j.biortech.2017.02.043 |
| Cordell D, Rosemarin A, Schroder J J, et al. 2011. Towards global phosphorus security:a systems framework for phosphorus recovery and reuse options[J]. Chemosphere, 84(6): 747–758.DOI:10.1016/j.chemosphere.2011.02.032 |
| De Luca A, Dantas R F, Esplugas S. 2014. Assessment of iron chelates efficiency for photo-Fenton at neutral pH[J]. Water Research, 61: 232–242.DOI:10.1016/j.watres.2014.05.033 |
| Dong H, Sans C, Li W, et al. 2016. Promoted discoloration of methyl orange in H2O2/Fe(Ⅲ) Fenton system:Effects of gallic acid on iron cycling[J]. Separation & Purification Technology, 171: 144–150. |
| 林进南.2013.利用硫酸亚铁去除污水中的磷酸盐[D].哈尔滨: 哈尔滨工业大学http://cdmd.cnki.com.cn/Article/CDMD-10213-1013038454.htm |
| Logan B, Call D, Cheng S, et al. 2008. Microbial electrolysis cells for high yield hydrogen gas production from organic matter[J]. Environmental Science & Technology, 42(23): 8630–8640. |
| Logan B, Grot S, Mallouk T E, et al.2009.Bio-electrochemically assisted microbial reactor that generates hydrogen gas and methods of generating hydrogen gas[P].U.S. Patent 7491453.2009-2-17.https://www.deepdyve.com/search?query=bio+electrochemically+assisted+microbial+reactor+that+generates&docNotFound=true |
| Lu L, Ren N, Zhao X, et al. 2011. Hydrogen production, methanogen inhibition and microbial community structures in psychrophilic single-chamber microbial electrolysis cells[J]. Energy & Environmental Science, 4(4): 1329–1336. |
| Lu L, Xing D, Ren N. 2012a. Bioreactor performance and quantitative analysis of methanogenic and bacterial community dynamics in microbial electrolysis cells during large temperature fluctuations[J]. Environmental Science & Technology, 46(12): 6874–6881. |
| Lu L, Xing D, Ren N, et al. 2012b. Syntrophic interactions drive the hydrogen production from glucose at low temperature in microbial electrolysis cells[J]. Bioresource Technology, 124(3): 68–76. |
| Ma J, Song W, Chen C, et al. 2005. Fenton degradation of organic compounds promoted by dyes under visible irradiation[J]. Environmental Science & Technology, 39(15): 5810–5815. |
| Montpart N, Rago L, Baeza J A, et al. 2015. Hydrogen production in single chamber microbial electrolysis cells with different complex substrates[J]. Water Research, 68(68C): 601–615. |
| Nam S, Renganathan V, Tratnyek P. 2001. Substituent effects on azo dye oxidation by the Fe(Ⅲ)-EDTA-H2O2 system[J]. Chemosphere, 45(1): 59–65.DOI:10.1016/S0045-6535(00)00599-3 |
| Neyens E, Baeyens J. 2003. A review of classic Fenton's peroxidation as an advanced oxidation technique[J]. Journal of Hazardous Materials, 98(1/3): 33–50. |
| Qin Y, Song F, Ai Z, et al. 2015. Protocatechuic acid promoted alachlor degradation in Fe(Ⅲ)/H2O2 fenton system[J]. Environmental Science & Technology, 49(13): 7948–7956. |
| Rajesh B J, Kannah R Y, Kavitha S, et al. 2018. Novel insights into scalability of biosurfactant combined microwave disintegration of sludge at alkali pH for achieving profitable bioenergy recovery and net profit[J]. Bioresource Technology, 267: 281–290.DOI:10.1016/j.biortech.2018.07.046 |
| Rivas F, Frades J, Alonso M, et al. 2005. Fenton's oxidation of food processing wastewater components.Kinetic modeling of protocatechuic acid degradation[J]. Journal of Agricultural & Food Chemistry, 53(26): 10097–10104. |
| Rozendal R A, Hamelers H V, Molenkamp R J, et al. 2007. Performance of single chamber biocatalyzed electrolysis with different types of ion exchange membranes[J]. Water Research, 41(9): 1984–1994.DOI:10.1016/j.watres.2007.01.019 |
| Rozendal R A, Sleutels T H, Hamelers H V, et al. 2008. Effect of the type of ion exchange membrane on performance, ion transport, and pH in biocatalyzed electrolysis of wastewater[J]. Water Science & Technology, 57(11): 1757–1762. |
| Song Y, Weidler P G, Berg U, et al. 2006. Calcite-seeded crystallization of calcium phosphate for phosphorus recovery[J]. Chemosphere, 63(2): 236–243.DOI:10.1016/j.chemosphere.2005.08.021 |
| Suzuki K, Tanaka Y, Kuroda K, et al. 2005. Recovery of phosphorous from swine wastewater through crystallization[J]. Bioresource Technology, 96(14): 1544–1550.DOI:10.1016/j.biortech.2004.12.017 |
| Wang A, Liu W, Ren N, et al. 2010. Reduced internal resistance of microbial electrolysis cell (MEC) as factors of configuration and stuffing with granular activated carbon[J]. International Journal of Hydrogen Energy, 35(24): 13488–13492.DOI:10.1016/j.ijhydene.2009.11.124 |
| Wu Y, Wang K, He C, et al. 2018. Effects of bioleaching pretreatment on nitrous oxide emission related functional genes in sludge composting process[J]. Bioresource Technology, 266: 181–188.DOI:10.1016/j.biortech.2018.06.049 |
| Xiao B, Chen X, Han Y, et al. 2017. Bioelectrochemical enhancement of the anaerobic digestion of thermal-alkaline pretreated sludge in microbial electrolysis cells[J]. Renewable Energy, 115: 1177–1183. |
| 余杰, 田宁宁, 王凯军, 等. 2007. 中国城市污水处理厂污泥处理、处置问题探讨分析[J]. 环境工程学报, 2007, 1(1): 82–86.DOI:10.3969/j.issn.1673-9108.2007.01.021 |
| Yu W, Yang J, Shi Y, et al. 2016. Roles of iron species and pH optimization on sewage sludge conditioning with Fenton's reagent and lime[J]. Water Research, 95: 124–133.DOI:10.1016/j.watres.2016.03.016 |
| Zhang Q, Hu J, Lee D J, et al. 2017. Sludge treatment:Current research trends[J]. Bioresource Technology, 243: 1159–1172.DOI:10.1016/j.biortech.2017.07.070 |
| Zhou L, Zhuang W Q, Costa Y G D. 2018. In situ and short-time anaerobic digestion coupled with alkalization and mechanical stirring to enhance sludge disintegration for phosphate recovery[J]. Chemical Engineering Journal, 351: 878–885.DOI:10.1016/j.cej.2018.06.156 |
| 周芊慧. 2018. 城市污泥处置技术探析[J]. 科技风, 2018(1): 113–113. |
