细胞衰老是器官乃至个体衰老的基础,这一过程受到遗传和环境等多种复杂因素的影响。尽管已有研究报道了一系列细胞衰老相关基因,但仍可能存在大量未知的衰老调控基因,且其调控衰老的具体分子机制尚不明确。此外,能否针对这些衰老调控基因发展干预个体衰老进程的基因靶向操控手段也缺乏系统研究。
2021年1月7日,中国科学院动物研究所刘光慧研究组、曲静研究组,中国科学院北京基因组研究所张维绮研究组及北京大学汤富酬研究组合作在Science Translational Medicine杂志在线发表题为“A genome-wide CRISPR-based screen identifies KAT7 as a driver of cellular senescence”的研究论文。该研究首次利用全基因组CRISPR/Cas9筛选体系在人间充质干细胞中鉴定出新的衰老调控基因,并在此基础上开发了可以延缓机体衰老的新型“基因疗法”。这项工作大大扩展了人们对于衰老基因的认识,为延缓衰老、防治衰老相关疾病提供了重要的干预靶标与新型策略。
在该项研究中,来自中国科学院和北京大学的研究团队联合攻关,经过六年多的不懈努力,利用全基因组CRISPR/Cas9筛选技术及人早衰症间充质干细胞研究体系,鉴定了百余个新的人类细胞衰老促进基因(图1),并对排名前50的基因进行了功能验证,证实了敲除这些基因均可延缓人间充质干细胞的衰老。其中,组蛋白乙酰转移酶的编码基因KAT7是排名最高的候选基因。研究人员发现KAT7在生理性和病理性衰老的人间充质干细胞中均上调表达,敲除KAT7可有效延缓细胞衰老,而过表达KAT7则会促进细胞衰老。进一步的机制研究表明,KAT7能通过选择性催化H3K14的乙酰化促进p15INK4b表达并诱导细胞衰老(图2)。
以往的研究表明,个体衰老伴随着组织器官中衰老细胞的持续累积,而清除衰老细胞或实现衰老细胞年轻化可以减轻组织退行性病变并延长小鼠的健康寿命。在该项工作中,研究人员发现静脉注射靶向敲低KAT7的Cas9/sgRNA慢病毒载体,可以减少衰老小鼠肝脏中衰老细胞的比例,显著降低血液中促炎因子的水平,改善小鼠的健康状态,延长生理性衰老小鼠和早衰症小鼠的寿命。这些结果表明基于单因子失活的“基因疗法”有望实现延长哺乳动物的自然寿命和健康寿命(图2)。在此基础上,研究人员还发现利用Cas9/sgRNA敲低KAT7或利用KAT7抑制剂WM-3835处理均可延缓人肝细胞衰老,并且导致衰老相关炎症因子的表达和分泌水平降低,提示这些干预手段在人类衰老转化医学中的潜在应用价值。
该研究通过CRISPR/Cas9全基因组筛选产生了迄今为止国际上最大的人类衰老促进基因名录,从概念上首次证明了基于单因子失活的基因治疗策略有助于延缓衰老、延长健康寿命。审稿专家们对这项工作给予了高度评价,认为“这项高质量的工作为衰老生物学领域提供了宝贵的资源”,“为衰老机制的理解做出了重要贡献”,“为开发促进人类健康、延长人类寿命的疗法明确了路径”。该成果不仅加深了人们对衰老规律的认识,也为干预衰老及衰老相关疾病提供了全新的靶标和思路。
该研究由中国科学院动物研究所、中国科学院北京基因组研究所、中国科学院干细胞与再生医学创新研究院、北京大学、首都医科大学宣武医院等多家机构合作完成。中国科学院动物研究所刘光慧研究员、北京大学汤富酬研究员、中国科学院动物研究所曲静研究员以及中国科学院北京基因组研究所张维绮研究员为文章的共同通讯作者。中国科学院动物研究所博士研究生汪伟、北京大学博士研究生郑宇轩以及中国科学院动物研究所助理研究员孙淑慧和首都医科大学宣武医院助理研究员李维为并列第一作者。该研究得到了中国科学院动物研究所周琪院士、首都医科大学宣武医院陈彪教授、中国科学院动物研究所宋默识研究员及王思副研究员的指导与支持。获得了国家科技部、国家自然科学基金委、中国科学院及北京市等项目的资助。相关测序数据已上传至衰老多组学数据库Aging Atlas。
文章链接:https://stm.sciencemag.org/content/13/575/eabd2655
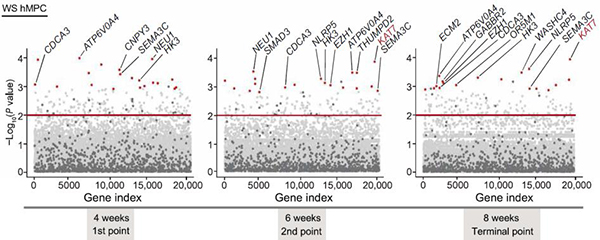
图1. 全基因组CRISPR/Cas9筛选鉴定新的人类衰老基因
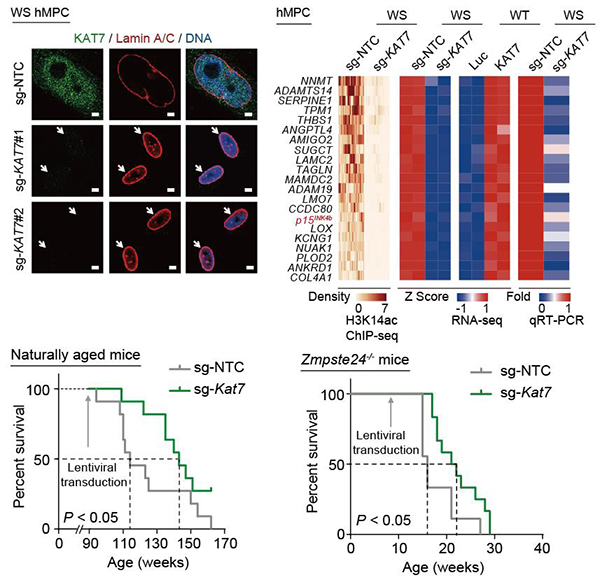
图2. 基于Cas9/sg-KAT7的基因治疗可延长生理性衰老和早衰症小鼠的寿命
| 附件下载: | |
