L-瓜氨酸是一种高附加值氨基酸,在医药和食品工业中具有广阔的应用前景。L-瓜氨酸生物合成途径受严格的反馈调控,同时需多种前体物及辅因子的参与,为L-瓜氨酸的高效生产带来了严峻的挑战。另外,由于L-瓜氨酸并非细胞终端代谢产物,很容易被argG基因编码的精氨酸琥珀酸合成酶转化为L-精氨酸,因此为实现L-瓜氨酸的大量积累通常会敲除argG基因构建L-精氨酸营养缺陷型菌株,但是在培养过程中需要外源添加L-精氨酸以弥补细胞生长不足,这无疑会增加L-瓜氨酸的生产成本和过程的复杂性。
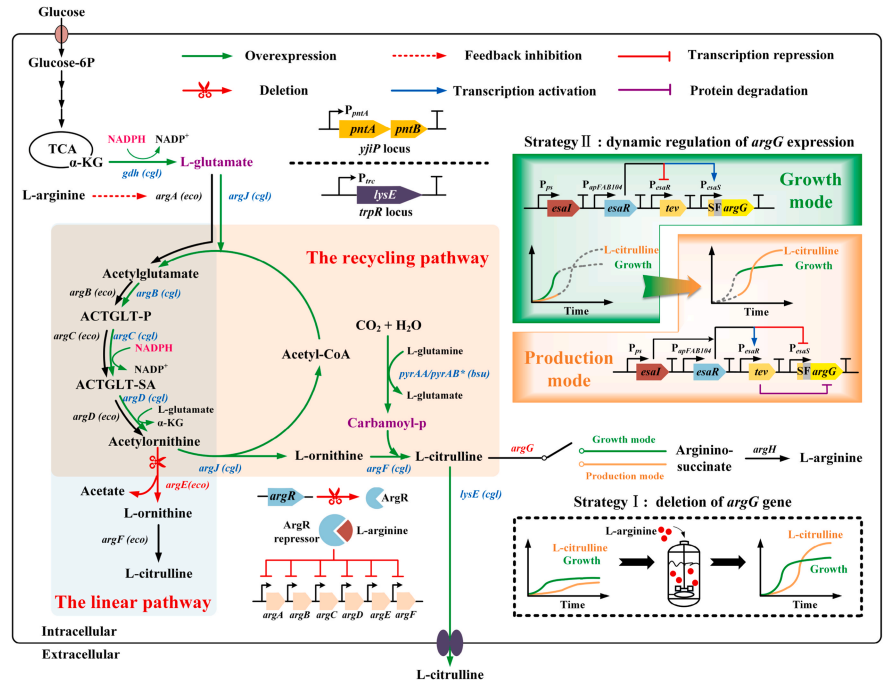
针对上述问题,研究团队采用系统代谢工程策略,首先阻断大肠杆菌中L-瓜氨酸降解途径并引入来源于谷氨酸棒状杆菌的L-瓜氨酸合成基因簇,以强化L-瓜氨酸合成途径代谢通量。通过失活大肠杆菌中乙酰鸟氨酸脱乙酰基酶构建了一条性能更优的L-瓜氨酸循环合成途径,以取代本源的线性合成途径。随后,对氨甲酰磷酸和L-谷氨酸合成模块、NADPH再生模块和L-瓜氨酸转运模块进行修饰,以进一步提高L-瓜氨酸积累量。虽然系统化模块工程改造后,L-瓜氨酸产量增高,但是改造菌的生产过程仍然依赖L-精氨酸的添加,为了解决这个问题,研究团队设计一个响应细胞密度的切换开关动态控制argG基因的表达,以实现内源L-精氨酸的供应。在不添加L-精氨酸的发酵过程中,CIT24菌株在5 L生物反应器中可生产82.1 g/L的L-瓜氨酸,糖酸转化率为0.34 g/g,生产强度为1.71 g/(L ×h),这是目前报道的微生物发酵法生产L-瓜氨酸的最高水平。该研究不仅成功设计了高效合成L-瓜氨酸的微生物细胞工厂,而且为理性代谢工程改造和动态调控策略生产高附加值中间代谢产物提供了重要参考。
多年以来,天津科技大学代谢工程研究团队致力于氨基酸菌种选育和发酵控制研究,编制或修订国家标准(行业标准)21项,建立了基于合成生物学与高通量筛选技术相结合的育种体系,构建了产酸率高、发酵周期短的高效优质工程菌株;结合代谢网络定量分析,通过多尺度优化与现代分离技术集成,实现了多种氨基酸高效生产。其中组氨酸、精氨酸、谷氨酸、色氨酸、酪氨酸、亮氨酸等氨基酸的主要技术指标方面均位于行业前列,突破了高值氨基酸合成瓶颈。相关研究成果获得黑龙江省科学技术进步奖一等奖、内蒙古自治区科学技术一等奖、中国轻工业联合会科学技术进步奖一等奖、天津市科学技术进步奖二等奖等省市级以上科技成果奖进步奖10余项。有25余项成果实现产业化,打破国外大公司的技术垄断,行业新增经济效益年超过160亿元,有力地推动了我国氨基酸等生物发酵行业的整体技术进步和产业升级,同时带动了上下游相关产业的健康发展。
论文链接:https://doi.org/10.1016/j.ymben.2021.10.009
