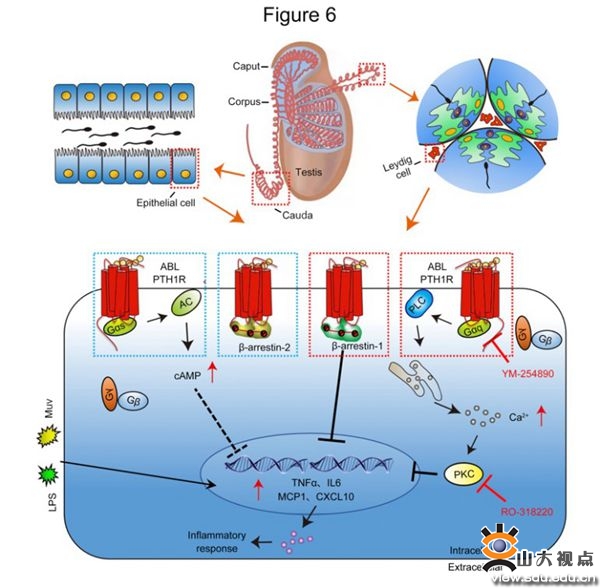
目前,男性不孕不育已成为威胁人类健康和生活质量的重大问题,其中由附睾-睾丸炎症导致的不育患者占比达到6-15%,该疾病因而受到广泛关注。附睾-睾丸炎症的临床治疗主要依靠抗生素疗法,然而抗生素往往引起不良反应,并对病毒感染或者其他非细菌感染引发的附睾-睾丸炎症疗效较差,因此亟需开发新的治疗策略。为探索有临床意义的附睾-睾丸炎症新型疗法,研究团队分别建立了腮腺炎病毒(MuV)和脂多糖(LPS)诱导的小鼠附睾-睾丸炎症模型,结合临床样本发现甲状旁腺激素受体PTH1R及其内源性配体PTH/PTHrP在睾丸间质细胞和附睾上皮细胞中异常表达,提示PTH1R的内源性环路可能参与调控附睾-睾丸免疫稳态。PTH1R的激动剂阿巴洛肽(FDA批准的骨质疏松症治疗药物)可以显著缓解MuV或LPS引起的附睾-睾丸炎症,同时提升小鼠精子活力。联合使用药理学手段和多种基因敲除小鼠,研究团队发现阿巴洛肽主要通过激活PTH1R下游的Gq和βarr1信号通路发挥抑炎作用。本工作发现了PTH1R内源性环路在男性生殖系统中的免疫调节作用,提示选择性靶向PTH1R下游Gq和βarr1信号通路可有效抑制附睾-睾丸炎症,为附睾-睾丸炎症的治疗提供了全新靶点和思路。
孙金鹏教授团队和于晓教授团队在GPCR偏好性信号转导领域连续取得进展,先后发现了肾上腺素受体下游βarr1在压力应激下调控学习记忆的分子机制(Biol Psychiatry, 2017),揭示了血管紧张素受体AT1R通过βarr1偏好性信号激活离子通道的全新快速机制(Nat Commun,2017),阐明了ADGRG2通过Gq和βarr1偶联CFTR调控输出小管重吸收和附睾微环境稳态的机制(Elife,2018)。孙金鹏、于晓、许文明和林浩成团队多年来长期合作,并同浙江大学张岩教授团队在PTH1R研究领域密切合作。张岩教授团队前期解析了PTH1R-Gs复合物的冷冻电镜结构(Science,2019),为本工作奠定了良好研究基础。本研究获得了北医三院姜辉教授以及国家计划生育重点实验室李建远教授的指导,得到了国家重点基础研发项目和国家****科学基金等多项基金的资助。
