上海药物所杨财广课题组前期合作研究描述了金黄色葡萄球菌ClpP蛋白酶的晶体结构以及分子动力学基础(J. Biol. Chem. 2013, 288, 17643-17653; J. Biol. Chem. 2011, 286, 37590-37601)。该研究成功设计并充分表征了具有功能获得性自激活的ClpP突变体ClpPN42AY63A,从分子机制和表型上,突变体的特征与ADEP紊乱激动ClpP水解酶的特征极其相似。首先研究表征了突变体蛋白质的生化活性、聚集状态及热稳定性,揭示Tyr63对于ClpP功能激动起到启动开关的作用。其次,解析了ClpPY63A突变体的晶体结构,发现具有多米诺效应的Asn42在功能激动中发挥促进增强的作用。
利用冷冻电镜技术展示ClpPY63AN42A的N端底物入口的口径变大,是实现功能激活的结构基础。利用扫描电镜实验确证了表达ClpPY63AN42A突变体的菌株生长缓慢是由于分裂蛋白FtsZ被降解,表现出金黄色葡萄球菌个体变大的表型,该结果也为评价ClpP小分子激动剂的表型研究提供实验模型。最后,由周虎课题组利用基于质谱的蛋白质组学技术,发现在表达ClpPY63AN42A的突变体菌株中有500多个蛋白质的丰度发生了显著性改变,尤其是FtsZ等蛋白质显著减少,与ADEP处理的野生菌株的蛋白质组分析结果一致。
该研究构建获得了具有非特异性自激活的ClpP突变水解体系,深入描述了ClpP功能激活的结构基础和分子机制,奠定了基于ClpP结构和功能发展小分子激动剂控制持留菌感染的基础。
该研究得到了浙江理工大学、上海光源、蛋白质设施、上海中医药大学、复旦大学以及上海药物所等合作课题组的大力支持,获得了国家自然科学基金、上海药物所自主部署项目等资助。研究成果于2016年5月在线发表于美国化学会化学生物学期刊ACS Chemical Biology上。
论文链接:http://pubs.acs.org/doi/abs/10.1021/acschembio.6b00390
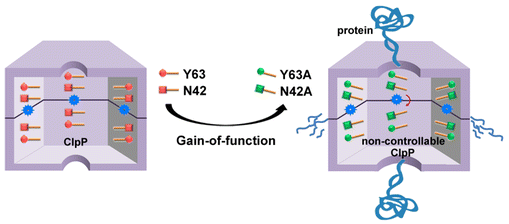
ClpP功能获得性突变体的作用示意图
(供稿部门:杨财广课题组)
