
 , 李有才, 王兆文, 石忠宁
, 李有才, 王兆文, 石忠宁 东北大学 冶金学院,辽宁 沈阳 110819
收稿日期:2020-05-07
基金项目:国家自然科学基金资助项目(51804069);中央高校基本科研业务费专项资金资助项目(N2025033)。
作者简介:杨酉坚(1987-), 男, 山东烟台人, 东北大学讲师, 博士;
王兆文(1964-), 男, 辽宁沈阳人, 东北大学教授, 博士生导师;
石忠宁(1975-), 男, 广西都安人, 东北大学教授, 博士生导师。
摘要:利用邱氏高温透明槽实验平台的高速温度采集模块结合原位重量分析法研究了冶金级氧化铝在冰晶石电解质中的溶解过程,尤其是结壳的形成与溶解过程,测定了结壳的溶解速率并分析了结壳的主要物理化学性质.通过对氧化铝溶解结壳过程的热量计算,分析了氧化铝加料过程中的热量平衡,以及加料量、氧化铝预热温度、电解液温度、过热度对溶解过程的影响.研究发现,在热平衡重新建立的过程中,氧化铝从体系中吸收的热量,首先由电解液降温来快速补充;当电解质大幅降温仍满足不了氧化铝的热量需求时,便由电解质冷凝放热来提供热量.相对于较高的电解温度、过热度而言,少量、多频次的氧化铝加料能够获得更加稳定的电解条件.
关键词:冶金级氧化铝氧化铝结壳溶解速率热量平衡过热度
Dissolution and Agglomeration Behavior of Alumina in Aluminum Electrolysis
YANG You-jian

 , LI You-cai, WANG Zhao-wen, SHI Zhong-ning
, LI You-cai, WANG Zhao-wen, SHI Zhong-ning School of Metallurgy, Northeastern University, Shenyang 110819, China
Corresponding author: YANG You-jian, E-mail: yangyj@smm.neu.edu.cn.
Abstract: The agglomerating behavior and heat transfer process upon the addition of smelting grade alumina into cryolite electrolyte were studied using the see-through cell platform, especially the formation and dissolution of the agglomerate. The dissolution rate of the alumina agglomerate was measured, and physicochemical properties of the alumina agglomerate was analyzed. The influence factors, such as the electrolyte temperature, alumina feeding amount, alumina preheating temperature and superheat during the dissolution and formation of the agglomerate were investigated through heat balance calculation. The results show that during the re-establishment of a new heat balance after alumina feeding, the absorbed heat for alumina dissolution is firstly supplied by electrolyte cooling. When the temperature drop is above the liquidus temperature of the electrolyte, which cannot provide enough heat for the dissolution, electrolyte condensation would take place and release more heat. In contrast to a relatively high electrolyte temperature and high superheat, a high frequent and small amount of alumina feeding would benefit the electrolysis process.
Key words: smelting grade aluminaalumina agglomeratedissolution rateheat balancesuperheat
铝电解工业是国民经济的基础产业,为我国的国防建设和经济发展提供了大量的金属铝材原料.氧化铝作为铝电解的原料,其在冰晶石电解质中的溶解过程是至关重要的[1].氧化铝能否顺畅地溶解于电解质中,并且在短时间内均匀扩散到阴、阳极之间,关系到核心电解反应是否能够顺利进行、电解过程是否能够保持稳定.工业实践表明,在氧化铝加料时,氧化铝颗粒在溶解过程中团聚、结壳的现象在很大程度上降低了氧化铝的溶解速度,并且氧化铝沉淀还会对电解槽产生一系列负面影响[2-3].
在工业电解槽中,氧化铝的溶解问题主要体现在:①电解槽下料区域过热度控制不良时氧化铝溶解受阻[4].在电解质过热度较低的区域,电解质无法迅速提供足够的热量满足预热物料和保证氧化铝持续溶解的反应热焓[5].过早凝结的电解质与大量未溶解的氧化铝颗粒发生团聚,由此引起的氧化铝溶解不良通常被归因于电解槽的热平衡问题.②我国低温复杂电解质对中间状氧化铝溶解性不良[6].初晶温度较低的电解质中,氧化铝溶解度较低[7].国产氧化铝中细颗粒含量较高,物料流动性不好,使氧化铝在最初加料溶解阶段无法在电解质液面上快速铺展,导致参与溶解和热量传递的有效电解质量大幅降低,也是造成氧化铝溶解过程受阻的重要原因之一[8].因此,从考虑溶解过程电解质-氧化铝多相热量平衡的角度,深入分析氧化铝的颗粒团聚行为规律,揭示氧化铝溶解机理和传质特征,是解决工业氧化铝溶解问题的有效手段.
1 实验材料和实验方法实验中使用的电解质有两种,编号为1#电解质和2#电解质.1#电解质成分为90%Na3AlF6-5%CaF2-5%LiF(其中氟化钠和氟化铝的摩尔比为2.9),电解质温度960 ℃.2#电解质成分为77.5%Na3AlF6-5%CaF2-10%KF-7.5%LiF(其中氟化钠和氟化铝的摩尔比为2.9),实验温度900 ℃.本实验采用邱氏高温透明槽实验平台与升降装置、分析天平(精度为0.1 mg)、摄像机、计算机、温度高速采集设备、铂托架等来研究氧化铝的溶解和结壳行为.实验装置简图如图 1所示.
图 1(Fig. 1)
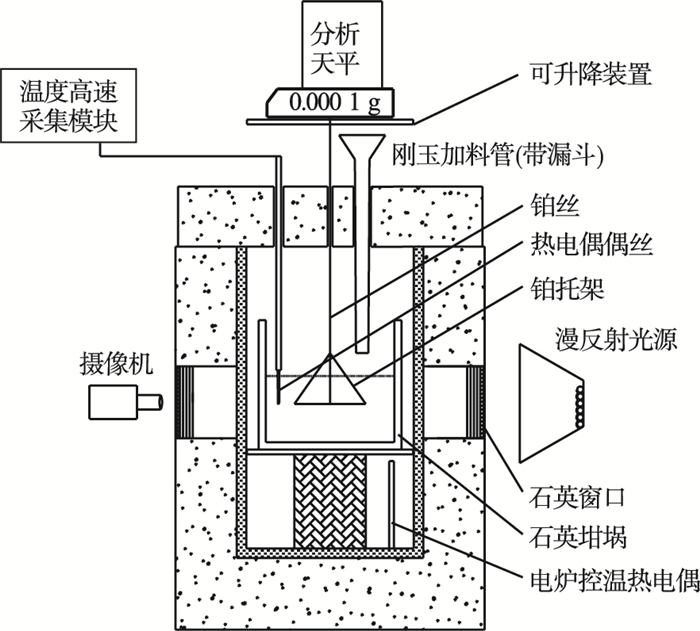 | 图 1 改装后的透明电解槽实验平台装置示意图Fig.1 Schematic diagram of the updated see-through cell |
实验中使用的透明石英坩埚的材质是高纯α石英,内部尺寸为65 mm×70 mm×90 mm,壁厚3 mm.铂托架由两部分组成:一是以?2 mm的铂丝制成的直径为50 mm的圆(以下称之为铂盘);二是吊装铂圆的3根?2 mm的铂丝.铂托架由细铂丝和镍铬丝吊装于分析天平(精度为0.000 1 g)用来实时获得结壳的质量变化.天平放在可水平和垂直方向移动的升降装置上,通过调整分析天平的位置使得铂托架位于石英坩埚正中央并且在垂直方向移动时不触碰坩埚壁和热电偶偶丝.分析天平通过数据线与计算机相连,使用赛多利斯软件实时自动采集天平示数.热电偶采用S型热电偶,采用补偿导线与计算机相连,可以高速采集温度数据,实时获得电解液的温度变化.
每次实验需要在石英坩埚中盛装500 g的电解质.当炉温升至初晶温度以上时,电解质开始融化为澄清透明状熔盐.通过刚玉加料管向电解液中加入5 g或10 g的不同温度的冶金级氧化铝.加料后,氧化铝粉末迅速在电解液表面扩散铺开,一部分冶金级氧化铝在加料后数秒内快速溶解进入电解液,剩余的氧化铝颗粒在氟盐的催化下其中的γ相氧化铝转化为片状的α相氧化铝,并与冷凝的电解液混合形成结壳.加料60 s后,将铂盘下降10 mm,使得结壳和铂架完全浸入电解液.下沉约30 s后,提升铂托架,将之完全提出液面.此时可以获得结壳的总质量,也可取出结壳分析其物理化学性质,或者30 s后沉降铂架和结壳至完全浸入到液面之下的位置,直至结壳完全溶解,获得结壳溶解速率.结壳的密度亦可通过铂架在不同位置时的天平读数,依据阿基米德定律得出.利用透明电解槽装置拍摄到的氧化铝结壳见图 2.
图 2(Fig. 2)
 | 图 2 透明电解槽获得的氧化铝溶解实验图像Fig.2 The images obtained by the see-through cell during alumina dissolution (a)—加料前铂架位置,-10 s;(b)—加料瞬间,4 s; (c)—铂架降低至液面之下,80 s; (d)—结壳大部分溶解,910 s. |
2 结果与讨论2.1 氧化铝加料后铝电解质熔盐的温度变化当实验使用的冶金级氧化铝被加入到高温熔融电解质中,它从电解液中吸收大量的热使自身温度升高到电解液的温度.这个过程中,氧化铝中含有的大量γ,γ',θ相氧化铝会在氟盐的催化下迅速转变为α相[9].伴随着晶型转变,羟基和氧化铝中的附着水/结晶水以水蒸气的形式快速释放.这个过程中氧化铝相变放出热量,灼减释放过程吸收热量.加入到电解液中的氧化铝一部分快速溶解进入电解液,一部分与冷凝的冰晶石混合形成结壳.氧化铝快速溶解的过程中要吸收大量的热,这使得局部电解液温度急剧下降放出热量.部分电解液的温度下降至初晶温度以下时,就会发生冷凝,转化为固态电解质,释放热量.结壳形成后漂浮在电解液表面,并随着铂架的下降而沉浸在电解液中,最终缓慢溶解在电解液中或者被取出分析结壳的物理化学性质[10-11].
图 3所示为将温度为20 ℃的10 g氧化铝加入500 g的1#电解质熔盐后所测得的电解液温度曲线,加料前电解质中的初始氧化铝质量分数为0.冷的氧化铝加入后从电解液中吸收大量的热量,热电偶处的电解液温度迅速下降至最低点a.加料后8 s(a点)到12 s(b点),冷、热电解液之间发生对流,热的电解质补充到局部过冷区域,温度迅速回升到b点.12 s(b点)到26 s(c点),一部分氧化铝快速溶解,从电解液中吸收大量的热,电解液温度再次下降到c点,此时电解液温度与加料前相比下降了10.21 ℃.26 s(c点)以后,氧化铝进入缓慢溶解阶段,电解液从高温炉内吸热量大于氧化铝溶解所需的热量,570 s后(d点)电解液温度缓慢回升到加料前的水平.
图 3(Fig. 3)
 | 图 3 加料前30 s到加料后700 s时间段内电解液的温度变化Fig.3 The electrolyte temperatures from 30 s before alumina feeding to 700 s after alumina feeding |
2.2 冰晶石-氧化铝冷凝结壳的物理化学性质分析结壳中氧化铝含量通过氯化铝(AlCl3)溶解法(GBT 6609.2—2004)进行测定,表面形貌采用德国蔡司显微镜有限公司生产的场发射扫描电镜(ULTRA PLUS)进行观察.
冶金级氧化铝加入到电解液后会在氟盐的催化下发生晶型转变,颗粒状的氧化铝崩裂为片状的α相氧化铝.大量的片状氧化铝与冷凝电解质联结而形成结壳.对960 ℃电解质成分下,初始氧化铝质量分数为2.91%时加入5 g 20 ℃的氧化铝所形成的结壳进行SEM分析,如图 4a所示.图 4b为图 4a局部放大照片,图 4b中对应打点位置的EDS能谱分析结果见表 1,由表 1可看出,打点位置1的主要成分为氧化铝和少量的冰晶石;打点位置2的主要成分为冰晶石.位置1中含有少量的冰晶石的原因是液态冰晶石冷凝在氧化铝的表面.由打点位置图像可知,结壳之中的氧化铝以片状形式存在,这与Less[12]的研究结果相符合;结壳中的电解质的形态比较圆润,呈柱状、水滴状等.由图 4b可以看到片状的α相氧化铝与冷凝电解质相互交织,联结紧密.
图 4(Fig. 4)
 | 图 4 氧化铝结壳的表面形貌SEM显微照片Fig.4 SEM images of the alumina agglomerate (a)—氧化铝结壳的表面形貌;(b)—局部放大照片. |
表 1(Table 1)
| 表 1 图 4b中对应的EDS能谱打点元素分析结果 Table 1 The EDS analysis results in Fig. 4b | ||||||||||||||||||||
据化学成分分析和密度测试,冷凝结壳中的氧化铝质量分数约为30%~50%,结壳的密度为2.3~2.4 g/cm3,结壳的孔隙率约为6%~10%.
2.3 氧化铝结壳的溶解速率分析根据结壳在电解质中的质量变化曲线的斜率计算出的结壳溶解速率随已溶氧化铝质量分数变化曲线如图 5所示,氧化铝质量分数与电解液过热度的对应关系见表 2.
图 5(Fig. 5)
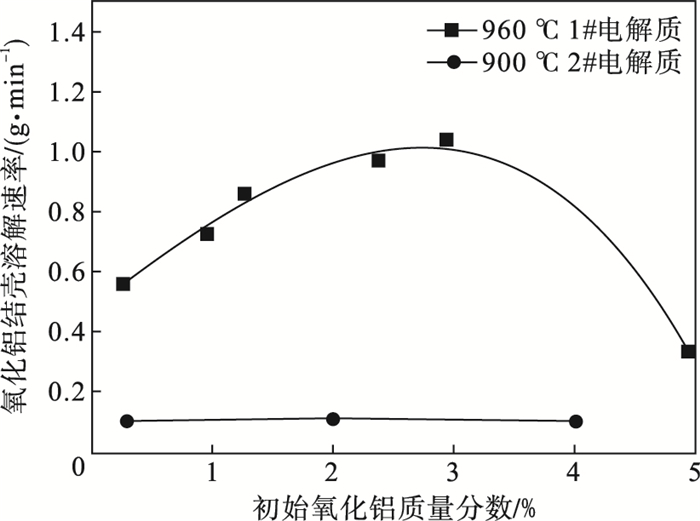 | 图 5 结壳溶解速率与氧化铝质量分数的关系Fig.5 Relationship between the crust dissolution rate and the alumina concentration |
表 2(Table 2)
| 表 2 电解质氧化铝质量分数与电解液过热度的对应关系 Table 2 The relationship between the alumina concentrationand electrolyte superheat | ||||||||||||||||||||||||||||||||
从图 5可以发现,在960 ℃的电解质中初始氧化铝质量分数低于3%时,结壳的溶解速率随着过热度的增大而增大.当氧化铝质量分数达到2.93%时,过热度为25.8 ℃,结壳的溶解速率为1.03 g/min,约为氧化铝质量分数为0(过热度为7.2 ℃)时溶解速率的2倍.在这个区间内,较大的过热度使得结壳和电解液之间的热传导速率增加,进而促进了结壳的溶解.
在电解液中氧化铝质量分数低于3%时,相对于氧化铝初始质量分数对溶解的作用,过热度对结壳溶解的提升作用占主导地位,结壳的溶解过程是传热控制的过程[13].根据Haverkamp和Welch[14]的传热控制方程,溶解速率与过热度成正比增加,考虑到氧化铝质量分数对结壳溶解速率的影响,认为它与本实验结果相符合.
在初始氧化铝质量分数增加到3.84%时,结壳溶解速率急剧降低,仅为0.31 g/min.这是由于电解质中氧化铝质量分数的增加使得溶解过程为扩散控制过程.可以推测,初始氧化铝质量分数越接近电解质中氧化铝的饱和浓度,结壳的溶解速率越慢.然而,在900 ℃电解质中,结壳的溶解速率稳定地保持在0.1 g·min-1的极低水平,它并不随着氧化铝质量分数或者电解液过热度的变化而变化.这表明,电解液的温度也是影响结壳溶解的一个重要因素.
2.4 氧化铝溶解过程的热量平衡分析假设加料后60 s的时间段内石英透明槽内是一个绝热体系,分析这个时间段内体系的热量支出与收入平衡情况.
热量平衡以物料平衡为基础,主要包括结壳过程中氧化铝的热量变化和电解液的热量变化两个方面.其中,氧化铝的热量变化包括氧化铝升温吸热Q1、氧化铝溶解吸热Q2、氧化铝灼减释放吸热Q3、氧化铝相变放热Q4;电解液的热量变化主要包括液态电解质降温放热Q5、电解质冷凝相变放热Q6.
各热力学数据的选取依据如下:
1) 氧化铝升温吸热Q1.加到电解液表面的氧化铝从电解液中吸收热量使自身温度升高到电解液的温度,这个过程中用于加热氧化铝热量为Q1,J:
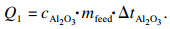 | (1) |
2) 氧化铝溶解吸热Q2.当氧化铝溶解在冰晶石熔体中时,冰晶石熔体的各种物理化学性质会发生很大的变化,伴随着溶解会产生热效应,这表明氧化铝在冰晶石中的溶解并非物理溶解,而是化学溶解.Phan-Xuan等使用一种名为“Tian-Colvet”的高温微热量仪测量了α相氧化铝在冰晶石熔体中的溶解热[16-17].
由于氧化铝的相变热单独计算,因此计算Q2使用的氧化铝的溶解热焓取α相的溶解热焓.对Phan-Xuan的测量结果[16]进行拟合,可得ΔHα-Al2O3与已溶氧化铝质量分数x的数值关系为
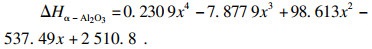 | (2) |
每次加料后,部分氧化铝快速溶解在冰晶石熔体中,这部分氧化铝溶解时吸收的热量为Q2,J:
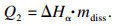 | (3) |
3) 氧化铝灼减释放吸热Q3.实验中所使用的冶金级氧化铝中仍然含有0.88%的结晶水.这部分水在氧化铝接触高温熔盐的瞬间汽化,这个过程中吸收的热量为Q3,J:
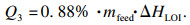 | (4) |
4) 氧化铝相变放热Q4.当实验使用的冶金级氧化铝被加入到高温熔融电解质中,氧化铝中含有的大量的γ,γ',θ相氧化铝,会在氟盐的催化下迅速转变为最稳定的α相[18].该氧化铝中α相的质量分数为1.51%.这个过程中,氧化铝的放出热量为Q4,J:
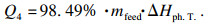 | (5) |
5) 液态电解质降温放热Q5.加料后,液态电解质中的热量被冷的氧化铝吸收,电解液温度降低,但是仍保持熔融状态[19].保持熔融态的电解液因为自身温度降低所释放的热量为Q5,J:
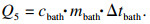 | (6) |
6) 电解质冷凝相变放热Q6.加入冷的氧化铝之后,温度降到初晶温度以下的电解质冷凝发生相变,相变过程中释放的热量为电解质的相变热Q6,J:
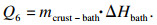 | (7) |
本文考察了两种电解质条件下温度、过热度、氧化铝质量分数、氧化铝加料量、氧化铝预热温度对氧化铝溶解过程中热量平衡的影响.表 3中列举了5个典型的热量平衡计算实例,5个实例分别对应的柱状分布图见图 6,图 6中Q1,Q2,Q3为溶解吸热过程;Q4,Q5,Q6为溶解放热过程;δ为吸热总量和放热总量的百分差值.
表 3(Table 3)
| 表 3 氧化铝溶解过程热量平衡计算的5个实例 Table 3 The five cases for thermal balance calculation in different alumina dissolution conditions |
图 6(Fig. 6)
 | 图 6 不同条件下的氧化铝溶解过程中的热量平衡对比Fig.6 Comparison of heat balance during alumina dissolution under different conditions |
图 6中,对比实例2和实例1,降低加料氧化铝的预热温度,则溶解过程需要传递更多的热量,预热较冷的氧化铝物料所需的热量基本由电解质降温提供;对比实例3和实例1,960 ℃时加料量从5 g增加至10 g,溶解过程的总热量传递加倍,但加料后迅速溶解的氧化铝量增加了超过一倍,同时电解质降温所提供的热量也增加了一倍多;对比实例4和实例2,当电解质的温度从960 ℃降低至900 ℃,传递的总热量变化不大,但更多的氧化铝在加料后迅速溶解,此时由电解质冷凝提供额外的热量;对比实例5和实例4,900 ℃时加料量增加一倍,溶解过程的总热量并没有加倍,同时加料后快速溶解的氧化铝也没有对应加倍,即更多的氧化铝在加料后进入了团聚结壳.
3 结论1) 氧化铝溶解过程中的颗粒团聚结壳是由于过早凝结的电解质与大量未溶解的氧化铝发生黏结团聚.当氧化铝加料导致体系热量失去平衡,在热平衡重新建立的过程中,氧化铝从体系中吸收的热量首先由电解液降温来快速补充.当电解质大幅降温仍满足不了氧化铝的热量需求时,便由电解质冷凝放热来提供热量,这时结壳的总质量(或者说加料后参与形成结壳的氧化铝量)便会上升.
2) 在较高的电解温度下(例如960 ℃,初晶温度较高的电解质成分)加料时,会有更大比例的氧化铝快速发生溶解反应,且电解液对冷物料的容忍度更大.而在较低的电解温度下(例如900 ℃,初晶温度较低的电解质成分),加料后更多的氧化铝形成了结壳.
3) 相对于加料前将氧化铝预热至500 ℃,或改变电解质温度(900 ℃至960 ℃),提高单次氧化铝加料量所引起的体系热量变化是最大的,包括电解液温度的波动和氧化铝结壳的增加量.因此,为了获得更加稳定的电解槽运行条件,少量、多次添加氧化铝的策略更为有效.
参考文献
| [1] | 邱竹贤. 铝电解原理与应用[M]. 徐州: 中国矿业大学出版社, 1998: 404-406. (Qiu Zhu-xian. Theory and application of aluminium electrolysis[M]. Xuzhou: China University of Mining and Technology Press, 1998: 404-406.) |
| [2] | Lavoie P, Taylor M, Metson J. A review of alumina feeding and dissolution factors in aluminum reduction cells[J]. Metallurgical and Materials Transactions B, 2016, 47(4): 2690-2696. DOI:10.1007/s11663-016-0680-3 |
| [3] | 徐君莉, 石忠宁, 高炳亮, 等. 氧化铝在熔融冰晶石中的溶解[J]. 东北大学学报(自然科学版), 2003, 24(9): 832-834. (Xu Jun-li, Shi Zhong-ning, Gao Bing-liang, et al. Dissolution of alumina in molten cryolite[J]. Journal of Northeastern University(Natural Science), 2003, 24(9): 832-834. DOI:10.3321/j.issn:1005-3026.2003.09.005) |
| [4] | Wang X.Alumina dissolution in cryolitic melts: a literature review[C]//TMS Proceedings—Light Metals.Nashville: Springer-Verlag, 2000: 41-54. |
| [5] | Bagshaw A N, Kuschel G I, Taylor M P, et al.Effect of operating conditions on the dissolution of primary and secondary (reacted) alumina powders in electrolytes[C]//TMS Proceedings—Light Metals.New Orleans: Springer-Verlag, 1985: 649-659. |
| [6] | Lyu Xiao-jun, Shuang Ya-jing, Li Jie, et al. Physicochemical properties of industrial aluminum electrolytes enriching Li and K:the liquidus temperature[J]. Metallurgical and Materials Transactions B, 2017, 48(2): 1315-1320. DOI:10.1007/s11663-016-0908-2 |
| [7] | 吕晓军, 双亚静, 胡凌云, 等. 铝电解质初晶温度和氧化铝溶解度的理论计算[J]. 轻金属, 2015(9): 27-31. (Lyu Xiao-jun, Shuang Ya-jing, Hu Ling-yun, et al. Theoretical calculation of primary crystallization temperature and alumina solubility of alumina electrolyte[J]. Light Metals, 2015(9): 27-31.) |
| [8] | Raahauge B E.Smelter grade alumina quality in 40+ year perspective: where to from here?[C]//TMS Proceedings—Light Metals.Orlando: Springer-Verlag, 2015: 73-78. |
| [9] | 付雪冰, 李志坚, 李心慰, 等. 煅烧温度对工业氧化铝相变及活性的影响[J]. 耐火材料, 2016, 50(3): 177-180. (Fu Xue-bing, Li Zhi-jian, Li Xin-wei, et al. Influence of calcining temperature on phase transformation and activity of industrial alumina[J]. Refractories, 2016, 50(3): 177-180. DOI:10.3969/j.issn.1001-1935.2016.03.006) |
| [10] | Thonstad J, Nordmo N, Paulsen J B. Dissolution of alumina in molten cryolite[J]. Metallurgical Transactions, 1972, 2: 403-408. |
| [11] | Gerlach J, Hennig U, Kern K. The dissolution of aluminum oxide in cryolite melts[J]. Metallurgical and Materials Transactions B, 1975, 3: 83-86. |
| [12] | Less L N. The crusting behavior of smelter aluminas[J]. Metallurgical Transactions B, 1977, 8: 219-225. |
| [13] | 李茂, 高玉婷, 白晓, 等. 300 kA铝电解槽中氧化铝颗粒的溶解模拟[J]. 中国有色金属学报, 2017, 27(8): 1738-1747. (Li Mao, Gao Yu-ting, Bai Xiao, et al. Simulation of alumina particle dissolution in 300 kA aluminum electrolytic cell[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(8): 1738-1747.) |
| [14] | Haverkamp R G, Welch B J. Modelling the dissolution of alumina powder in cryolite[J]. Chemical Engineering and Processing, 1998, 37(2): 177-187. DOI:10.1016/S0255-2701(97)00048-2 |
| [15] | Gurvich L V, Veyts I V, Alcock C B. Thermodynamic properties of individual substances[M]. 4th ed. New York: CRC Press, 1996: 448-707. |
| [16] | Phan-Xuan D, Castanet R, Laffitte M.Microcalorimetric study of alumina dissolution in cryolitic baths[C]//TMS Proceedings—Light Metals.Hoboken: Springer-Verlag, 1975: 159-177. |
| [17] | Wai-Poi N, Welch B J.Comparing alumina quality specifications and smelter expectations in cells[C]//TMS Proceedings—Light Metals.Hoboken: Springer-Verlag, 1994: 345-350. |
| [18] | Wilkening S, Reny P, Murphy B.Anode cover material and bath level control[C]//TMS Proceedings—Light Metals.San Francisco: Springer-Verlag, 2005: 367-372. |
| [19] | Dando N, Wang X, Sorensen J, et al.Impact of thermal pretreatment on alumina dissolution rate and HF evolution[C]//TMS Proceedings—Light Metals.Seattle: Springer-Verlag, 2010: 541-546. |
