����,�Խ�,������
(�Ͼ����պ����ѧ �Զ���ѧԺ,�Ͼ� 210006)
ժҪ:
����RNA��һ��㷺���������ϸ������Դ��RNA,����ǰ��RNA��������γ�,�ʱջ��ṹ,û��5����ñ�ӽṹ��3����polyAβ�͡�һֱ����,����RNA����Ϊû�б�������,���ܱ��뵰����,ֻ����ΪmicroRNA�����ࡱ�ȷ�ʽ,���ӵ��ع��ܡ�Ȼ��,���������ŶԻ���RNA�о��IJ�������,���ֻ���RNA�����ֿ�ͨ����ñ����������ʼ���Ʊ��뵰���ʡ�����,����RNA����ĵ����ʱ�֤ʵ�ڶ��ϸ�������з�����������Ҫ�����á���Ŀǰ����RNA���뵰���о���״��������,����Ŀǰ����RNA���뵰�����������Ϣѧ���߽������ܽᡣ
�ؼ���: ����RNA ����DZ�� �ڲ����������λ�� m6A��������
DOI��10.12113/201910002
�����:Q74
���ױ�ʶ��:A
������Ŀ:������Ȼ��ѧ������Ŀ(No.61973155,No.61571223)
Review on circular RNA with protein-coding ability in eukaryotes
WANG Cong, ZHAO Jian, SONG Xiaofeng
(College of Automation Engineering, Nanjing University of Aeronautics and Astronautics, Nanjing 210006, China)
Abstract:
Circular RNA (circRNA) is a type of endogenous RNA widely expressed in eukaryotic cells, which is formed by back-splicing of pre-RNA without 5��cap and 3��tail. circRNA has long been considered to be without coding ability, for it cannot encode protein and just regulates gene expression as microRNA sponge. However, with more and more research results on circRNA over the years, a small number of circRNAs has been proved able to encode protein or peptides in cap-independent manner. These proteins or peptide have been shown to play a vital role in cellular processes. This paper reviews the current circRNA research, and summarizes some bioinformatics methods related to circRNA protein coding ability.
Key words: circRNA Coding potential Internal ribosome entry site m6A modification
����, �Խ�, ������. ������ﻷ��RNA���뵰���о���չ[J]. ������Ϣѧ, 2020, 18(1): 1-7. DOI: 10.12113/201910002.

WANG Cong, ZHAO Jian, SONG Xiaofeng. Review on circular RNA with protein-coding ability in eukaryotes[J]. Chinese Journal of Bioinformatics, 2020, 18(1): 1-7. DOI: 10.12113/201910002.

������Ŀ ������Ȼ��ѧ������Ŀ(No.61973155, No.61571223) ͨ������ �����壬�У����ڣ���ʿ����ʦ���о�����������Ϣѧ. E-mail: xfsong@nuaa.edu.cn ����� �������У�˶ʿ�о������о�����������Ϣѧ. E-mail: wangcong@nuaa.edu, cn ������ʷ �ո�����: 2019-10-21 ������: 2019-12-02
Contents Abstract Full text Figures/Tables PDF
������ﻷ��RNA���뵰���о���չ
����
 , �Խ�, ������
, �Խ�, ������

�Ͼ����պ����ѧ �Զ���ѧԺ���Ͼ� 210006
�ո�����: 2019-10-21; ������: 2019-12-02
������Ŀ: ������Ȼ��ѧ������Ŀ(No.61973155, No.61571223)
�����:�������У�˶ʿ�о������о�����������Ϣѧ. E-mail: wangcong@nuaa.edu, cn
ͨ������: �����壬�У����ڣ���ʿ����ʦ���о�����������Ϣѧ. E-mail: xfsong@nuaa.edu.cn
ժҪ: ����RNA��һ��㷺���������ϸ������Դ��RNA������ǰ��RNA��������γɣ��ʱջ��ṹ��û��5����ñ�ӽṹ��3����polyAβ�͡�һֱ����������RNA����Ϊû�б������������ܱ��뵰���ʣ�ֻ����ΪmicroRNA�����ࡱ�ȷ�ʽ�����ӵ��ع��ܡ�Ȼ�������������ŶԻ���RNA�о��IJ������룬���ֻ���RNA�����ֿ�ͨ����ñ����������ʼ���Ʊ��뵰���ʡ����ң�����RNA����ĵ����ʱ�֤ʵ�ڶ��ϸ�������з�����������Ҫ�����á���Ŀǰ����RNA���뵰���о���״��������������Ŀǰ����RNA���뵰�����������Ϣѧ���߽������ܽᡣ
�ؼ���: ����RNA ����DZ�� �ڲ����������λ�� m6A��������
Review on circular RNA with protein-coding ability in eukaryotes
WANG Cong
 , ZHAO Jian, SONG Xiaofeng
, ZHAO Jian, SONG Xiaofeng

College of Automation Engineering, Nanjing University of Aeronautics and Astronautics, Nanjing 210006, China
Abstract: Circular RNA (circRNA) is a type of endogenous RNA widely expressed in eukaryotic cells, which is formed by back-splicing of pre-RNA without 5'cap and 3'tail. circRNA has long been considered to be without coding ability, for it cannot encode protein and just regulates gene expression as microRNA sponge. However, with more and more research results on circRNA over the years, a small number of circRNAs has been proved able to encode protein or peptides in cap-independent manner. These proteins or peptide have been shown to play a vital role in cellular processes. This paper reviews the current circRNA research, and summarizes some bioinformatics methods related to circRNA protein coding ability.
Key Words: circRNA Coding potential Internal ribosome entry site m6A modification
����RNA��һ������ijʷ�ջ�״�ṹ��RNA���ӣ���û��5����ñ�ӽṹ��3����PolyAβ�ͣ���ǰ��RNA(pre-mRNA)ͨ����������γɡ������о����ֻ���RNAҲ���Ա��뵰�ף��ҹ��ƴ�Լ10%�Ļ���RNA���е��ױ������������ܽ����������뵰�Ļ���RNA�����֣�����Щ����RNA�����С���ڶ����������з�������Ҫ�����ã����뼲�����й�����Ŀǰ���д����Ļ���RNA�ȴ�������ȥ���֣���˱��ĶԻ���RNA���뵰������о�����������������Ŀǰ���еĿ����ڱ��뵰����RNAʶ������������Ϣѧ���ߺͷ����������ܽᡣ����RNAͨ�����뵰����һ���ƣ��������뼲����ص�һЩ���á���˶��ڻ���RNA���뵰���о�������Ҫ�����塣
1 ����RNA���뵰��DZ�ܵķ���1976�������״��ڲ����й۲쵽����RNA�Ĵ���[1]��1979���о���Ա�ڵ��������¹۲쵽���ϸ���еĻ���RNA[2]�����Ŷ����������Ŀ��ٷ�չ��������Ϣѧ���ߵĿ���������RNA�����㷺��������������С��������С������֯�ֱ��65 731��15 849������RNA [3]��2015�꣬Wang����ͨ�����ڲ����������λ��(Internal Ribosome Entry Site, IRES)�˹����뻷��RNA��ʵ�鷽�������������˹������Ļ���RNA���Է���[4]�����������о����ǵ�ע�⡣
һֱ����������RNA����Ϊ���ܱ��뵰���ʣ���һ���µķDZ���RNA��ͨ�������Խ��microRNA���ػ�����Ȼ�����˹������Ŀɱ��뵰����RNA�ij���ʹ�����ǿ�ʼ�����Ƿ������Դ�ԵĿɱ��뵰����RNA��2015��Chen���˶������RNA�ı������������˷����������൱��Ļ���RNAת¼�����е����ʱ���DZ�ܣ���ͨ���������ݴ��м�����21�����뵰�Ļ���RNA����2017�꣬Ivano����ͨ��northern blot���������ȷ�����֤�˻���RNA(circ-ZNF609)�ܹ����뵰���ʣ��Ӷ����ؼ�ϸ����ֳ��������֤�˸û���RNA�ķǷ�����(Un-translated region, UTR)����IRES�ṹ[5]��Yang����ͨ�������⡢�����������Circ-FBXW7�ܹ���������Խ���������������صĵ���FBXW7-185aa[6]��Zhang������֤��circ-SHPRH�ܹ��������͵�����SHPRH-146aa���õ����ܹ������������ķ���[7]��2018��Zhang���˻���֤��circ-PINT�ܹ��������͵���PINT87aa�����ƶ��ְ�����ת¼����[8]��2019��Liang���˷�����circ��-catenin�ܹ�����ȫ�µ��צ�-Catenin-370aa������Wnt/�����������ź�ͨ·[9]��Heesch������������֯�з���40�ֻ���RNA�ܱ����룬����6����������еõ���֤[10]��
�ۺ������Ѿ���������֤����RNA���뵰�����£���֤�Ĺ��̴������£�Ԥ���RNA�Ŀ����Ķ���(Open reading frame��ORF)�������˿�Խ��ͷλ��(Junction site)����������п����Ķ���Ļ���RNA���б��뵰���ʵ�DZ������; ����������Ϣѧ�ķ���Ԥ���RNA���Ƿ�����ڲ����������λ��(Internal ribosome entry site��IRES)�ṹ������У���һ��ͨ��˫˳����ʵ����֤IRES�ṹ�Ļ���; ���Ԥ��Ŀ����Ķ����Խ�������λ�㣬Ԥ������ܱ���ĵ��������У�ͨ�������(MS)������֤�Ƿ��л���RNA�����γɵ��ض�С��Ƭ�Σ��������֤ʵ�û���RNA���뵰���ʡ�
2 ����RNA���뵰����ص��ػ����ڻ������У�mRNA����������ʼ�����ӱ�Ȼ����ֹ������֮ǰ��Ȼ�������ڻ���RNA������ջ��ṹ�������������ʼ�������ڻ������е�λ�ÿ�������ֹ������֮���ұ������ij��ȿ��ܴ��ڻ���RNA���������⣬��ջ��ṹ������RNA����5����ñ�ӽṹ�����������ñ�ӽṹ��ļ��������ʼ���뵰�ף���ֻ��ͨ����ñ�������ڲ�������ʼ���Ʊ��뵰�ס�IRESԪ����Ϊһ��RNA�ڲ����У���ֱ����ļ�������ϣ���RNA�ڲ���ʼ���뵰�ף����IRESԪ������Ϊ����RNA���뵰��ǰ������֮һ��m6A������ΪRNA�з����ߵ�ת¼�����Σ������ڵĶ����п���ΪIRESԪ����������RNA���뵰�ף��ɴ�m6A����Ҳ����������RNA���뵰�ı�־����ˣ����½��ӱ��������ʶ������ʼ����������ܻ���RNA���뵰����ص��ػ��ơ�
2.1 ����RNA�б��뵰�������ʶ����ƻ���RNA���뵰���Ⱦ������DZ���Ҫ��һ�����ȵĿ����Ķ���(ORF)�������Ķ�����ָ����ʼ������(AUG)��ʼ����������ֹ������(UAA, UAG, UGA)��һ������������С����������ӵĶ�д��ʼλ�ò�ͬ��RNA���п��ܰ����ֿ����Ķ����Ķ��ͷ��롣���������ʼ�����ӿ�ʼ���룬����RNA���кϳɶ��������������죬������ֹ�����ӷ�����ֹ��Ȼ�������ڻ���RNA��һ���ֻ�״������RNA�����������ͬ����ͬ������mRNA������RNA�Ŀ����Ķ�����ܿ�Խ�������λ��(Junction site)�������Ķ�������ƻ���RNAһȦ������Ȧ�������������ڻ���RNA��������˾��п����Ķ���Ļ���RNA�ſ��ܱ��뵰���ʡ�
2.2 �ڲ����������λ��(IRES)�鵼�Ļ���RNA�ڲ�������ʼ����RNA�ķ�����ʼ�ɷ�Ϊñ��������ͷ�ñ�����������ַ�ʽ������ñ����������Ҫ����5���˵�ñ�ӽṹ��ļ��ʼ���Ӹ�����ͺ������ǻ�������ʼ���ӵĸ����£���RNA��40 S�������ǻ���ϣ�����������ʼ�����ڷ�ñ������������У�IRES�鵼���ڲ�������ʼռ�˺ܴ�һ���֣����ڷ�ʽ�������ӵ�������ֱ����ļ40 S�������ǻ���RNA��ϣ���������������̡���ˣ����ܻ���RNA��һ���ջ��ṹ��û��5��ñ�ӽṹ��������RNA����ͨ���ڲ���IRESԪ����ʼ�����ʷ�����̡�
���뵰���ʵĻ���RNA�ڲ�������IRESԪ��������ʵ�����IRESȷʵ�����˻���RNA�ķ�����ʼ[5-9]��IRESʵ����֤����Ҫ�ֶ���ͨ��˫˳����ʵ�飬ͨ��ʹ��ӫ����ø������Ϊ���壬����5��UTR������������У��������ӫ����ø������������֤���������о���IRES���ԡ�IRESԪ��������5���Ƿ�����(5��Un-translated region, UTR)�зֲ�����CDS����3��UTR��ͬ������IRESԪ��[11]�����ң��о����ִ�Լ10%������mRNA��5��UTR������IRESԪ��������RNA�����Դ��mRNA�������ӣ�������㹻���������൱һ���ֵĻ���RNA����IRESԪ����һ����˵������IRESԪ���ṹ�Ļ���RNA�����Ǹ���������б��뵰���ʵ���������ΪIRESԪ���ܹ���ļ�������ǻ������ϴӶ��������롣
2.3 m6A(N6)�������������Ļ���RNA�������N6�������δٽ�����RNA�ķ�����ʼ��N6�������Σ���������6��N�������������¼����ֳ�m6A��m6A�����ϸ������㷺��һ��RNA��������[12-13]������������ܳ��ֵĹ��л���(Consensus motif)�ǡ�RRm6ACH��������R��A��G��H��A, C��U[14-15]��m6A��3���DZ�����(UTR)ͨ����YTHDF1����ϣ���߷���Ч��[16]��Ȼ������5��UTR����m6Aͨ��YTHDF2������û��ƣ��ٽ���ñ����������ʼ[17-18]��YTHDF3����������嵰������ôٽ�mRNA�ķ���[19]��
����mRNA�ɺ�����ɨ����ʼ���룬Ȼ������RNA�ķ�����ʼ������ȫ��ͬ��������ﳣ�浰������ʼ��eIF4�����↑ʼ������eIF4E���5��ñ�ӽṹ��eIF4G�ṩ������ʼ��������װ����֧�ܣ�ļ�����������ʼ������̡��о���Աͨ��һϵ��ʵ�����eIF4G2��eIF3A���λ����m6A����λ���غϽϸ�[20]��Yang����ͨ��circRNA-m6A-seq(m6A�������߹�������Ӧ��Ȳ���)��ʵ���ֶ�֤ʵ��Դ�Ի���RNA�к��д�����m6A����λ�㣬����������������������m6A���ξ���������eIF4G2���λ�����Σ�˵�������߿��ܴ���Эͬ���ط��������á�����m6A����������ȫ������RNA������������, ��Լ��13%����RNA����m6A�����¼�����ˣ�����m6A���εĻ���RNA���п��ܾ��з����������ܹ����뵰���ʡ�
3 ����RNA���뵰�����������ϢѧԤ���3.1 ���뵰����RNA��Ԥ������Ԥ����뵰����RNA�����̴������£�(1)����Ԥ���RNA�Ŀ����Ķ����п����Ķ���Ļ���RNA���б��뵰���ʵ�DZ��������(2)�Կ����Ķ�������б����Խ��м��㣻(3)ͨ��һЩ���й��������÷֣�(4)����������Ϣѧ�ķ�������Ԥ���RNA���Ƿ����IRES�ṹ��(5)���Ž���m6A���ε�Ԥ�⣻(6)���ribo-seq���ݣ�����rRNA���Σ�ȥ��ƥ��������RNA�IJ��֣�������RNA��ͷ����ƥ����ribo-seq���ݣ������������Ż���RNA�����˷��룻(7)���Ԥ��Ŀ����Ķ����Խ�������λ�㣬Ԥ������ܱ���İ��������У�ͨ�������(MS)������֤�Ƿ��л���RNA�����γɵ��ض�С��Ƭ�Σ��������֤ʵ�û���RNAȷʵ�ܹ�����С�ġ�����ͼ��ͼ 1��
ͼ 1(Figure 1)
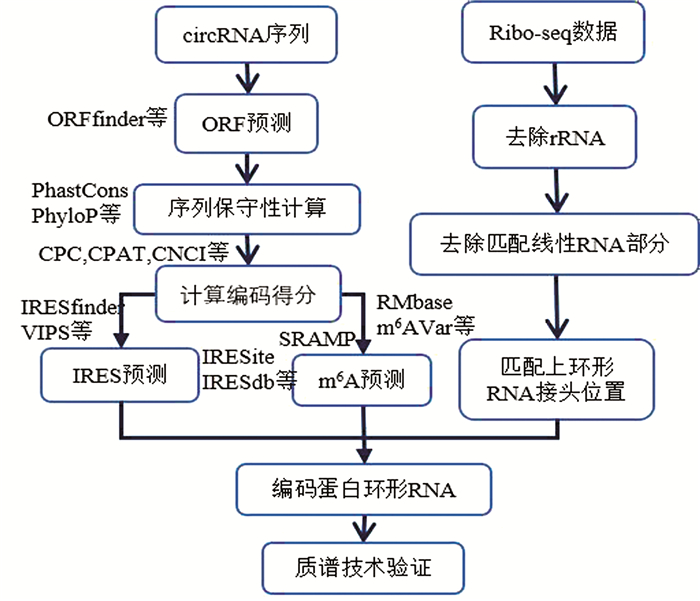 ͼ 1 ���뵰����RNAԤ������ͼFigure 1 Flow chart pipeline for predicting protein-coding circRNAs
ͼ 1 ���뵰����RNAԤ������ͼFigure 1 Flow chart pipeline for predicting protein-coding circRNAs3.2 �����Ķ���Ԥ���ORFԤ��������Ҫ��ORFfinder, ORF Investigator, ORF Predictor��ORFik��ORFfinder��һ��ͼ�η������ߣ����Բ����û����������д���һ�����ȵ����п����Ķ��������������ݿ��д��ڵ����У���ͨ��BLAST�����������ݿ��м������������С�ORF Investigator�ǻ���perl���Ա�д�ij����ܹ���Ч���ҵ���Ӧ���������е�ORF��������ת�������ǵĵ���ĸ��������룬�����������ṩ���ǵ�λ�ã����������м����ȫ�ֱȶԣ���ⵥ�������̬�ԡ�ORF Predictorʹ�����ֲ�ͬORF�������ϣ�����������ʼ�����ӿ�ʼ����ֹ�����ӽ��������졣��Ϊ����ı�������5'�Ƿ�����(UTR)��������ֹ�����ӡ�ORFik��Bioconductor�е�R��������Ѱ�ҿ����Ķ���ܲ�ʹ����һ����������֤��ORF�ĺ����ԡ�Ȼ��������RNA�ʱպϻ�״�ṹ�������Ķ����ܹ���Խ��ͷλ�ã��ƻ�һ�����ϣ�������Щ���߶���̫�ʺϻ���RNA�����Ķ����Ԥ�⣬��Ҫ�Ա����ʵ�֡�
3.3 IRESԤ���������ݿ�ĿǰԤ��IRESԪ���Ĺ�����Ҫ��IRSS[21]��VIPS[22], IRESpred[23]��IRESfinder[24]�����У�IRSS��VIPSͨ������֪IRES�Ķ����ṹ�������ƶȱȶԣ��ó���������ΪIRESԪ�������Ŷȡ�IRESpredͨ��֧��������ģ�ͣ������˲�����ϸ��IRESԪ����35������������27���������ڴ�������5'UTR����С�ǻ������嵰��ϵĿ����ԣ�������������UTR�������кͽṹ������IRESfinderͨ��������֤[11]��583��IRESԪ�����л���ѧϰѵ��������10�ν�����֤��ROC���߷�����AUCֵ�ﵽ��0.825�����У�VIPS����֪����IRES�����ṹ���бȶԣ�����ʱ��֪����IRESֻ��4����������ʱ��ϳ���IRESfinder������������Ԥ�����IRESԪ���Ŀ����ԣ��������ڻ���RNA��IRES��Ԥ�⡣
Ŀǰ��¼IRESԪ�������ݿ���Ҫ��IRESdb[25], IRESite[26]��Rfam[27]��IRESdb������2002�꣬�ṩ��30�����Բ�����IRES��50���������ϸ��IRES���mRNA��Ϣ��IRESite������2005�꣬���ݿ���¼��125��IRES������Ϣ������43��������70�����mRNA��Rfam�ռ���IRES_RhPV, IRES_cyp24a1���������IRES���ṩ����Դ�����Ͳο����������Ϣ������IRES���ݿ���¼��Ϣ���ȽϾ�Զ��Ŀǰ����֤��IRESԪ����Զ�������������ݿ⡣
3.4 m6AԤ���������ݿ����л�������Ԥ��m6A����λ���������Ҫ��SRAMP(Sequence-based RNA adenosine methylation site predictor)[28]��SRAMP�����������ɭ�ַ�����(����λ�÷�����������K���ڽ��㷨�����������ں�����Է�����)�����ۺϴ�֡���������ǻ��������л��Ǻ���DNA����(cDNA)���ֱ��Ӧ����ģʽ��SRAMP�ڽ�����֤�Ͷ�����֤���涼�������ƣ�ѵ����������������ƪ��֤���鶯�ﵥ������ֱ��ʵ�m6Aλ�������[29-30]��������������ͬ����(DRACH)��ͬ�����ݼ��е����ѡȡ����Ϊm6A���β����������[31]��SRAMP����������ҳ����������ʽ�ṩ���û�ʹ�á����ڻ���RNA��m6A����λ���Ԥ�⣬��������Ԥ��Ĺ���SRAMP�ܹ�ʤ�Ρ�
Ŀǰ��¼m6A����λ������ݿ���Ҫ��RMbase[32]��m6Avar[33]��RMbaseͨ��m6A-CLIP��ʵ�鼼�����ռ�������12����ͬ���ִ�Լ1 373 000��m6A����λ����Ϣ��m6Avarͨ��7��miCLIP��2��PA-m6A-Seqʵ�飬244��MeRIP-Seqʵ���Լ�����Ԥ��������ռ�������m6A����λ�����ݣ���414 241��m6A��ر���λ�㣬�������Ͱ�����lincRNA, miRNA, piRNA�ȡ�
3.5 ת¼�����ױ���Ԥ���Ŀǰ����ת¼�����뵰��Ԥ�����Ҫ��CPC[34], CPAT[35]��CNCI [36]��������Ҫ��Ϊ���࣬�������бȶ�(Alignment-based)�Ͳ���Ҫ�������бȶ�(Alignment-free)������CPC�������бȶԣ�����ʶ�����ԽϺõĵ��ױ������CPAT��CNCI����Ҫ���бȶԣ���Ҫ�������ּ䱣���Խϲ��ת¼����
2007�꣬Kong���˿���������ת¼�����뵰��DZ�ܵĹ���CPC[34]��CPC����֧����������������ͨ����ȡ������Ҫ����ѧ����������������������������з�Ϊ�������л�DZ������в�������Ӧ�÷֡�ѵ������ͨ��ʮ��������֤���ڴ������ݼ���չʾ��CPC���кܸߵ�ȷ��(95.77%)��CPC��ȡ����������ǰ�������Ԥ��Ŀ����Ķ���(ORF)����framefinder��������(����The Log-odds score, Coverage of the predicted orf, Integrity of the predicted orf)������������ͨ���ٶ�ORF����ĵ�����UniProt���ݿ⾭��blast�ȶԽ������(����Number of hits, hit score, frame score)��CPCѵ��������������EMBL��121 914��������(CDS)���У�����������Rfam��RNADB��34 766���DZ������С�
��ͬ��CPC���ǣ�CPAT����Ҫ�������бȶ�(Alignment-free)������ͨ������ͷDZ���ת¼����������������������[35]��CPAT�������ع�����������������������������ֱ�����DZ���ת¼�����ֱ��ǣ�(1)�����Ķ���(Open reading frame size)��(2)�����Ķ��Ƕ�(Open reading frame coverage)��(3)Fickettͳ�ƣ����ڼ����ɺ������ӷֲ�(Fickett TESTCODE statistic)��(4)������Ƶ��(Hexamer usage bias)�������������������ܽϺ����ֱ�����DZ���ת¼��������������RefSeq���ݿ��10 000�����뵰��ת¼��������������GENCODE���ݿ��10 000�����ѡȡ�ķDZ���RNA��ͨ��ʮ�ν�����֤AUC���ߴﵽ0.992 7��
��CNCI���ڼ�������ӵĹ��������ֱ�����DZ���ת¼���������������С��ת¼������֧��������ģ�ͣ����ڶԼ�������з���[36]��ѵ��������������RefSeq���ݿ⣬����������GENCODE�����Լ��������ְ�����С��ȼ������ֲ������������ͷDZ���ת¼��������ʮ�ν�����֤����ȷ�ʴﵽ97.3%��
��Ի���RNA���뵰��Ԥ�⣬��Ҫ�Ƚ�����RNA����Ԥ��������֤ORF�������ԣ������Խ��ͷλ�õ�ORF���ָ���ܽ�����RNA����������������ת¼�����뵰��Ԥ��߽��з�����
3.6 ���뵰����RNAԤ���������ݿ����Ŷ����������Ŀ��ٷ�չ�������Ļ���RNA�����֣�����һ�����뵰�Ļ���RNA�����ݿ�dz��б�Ҫ��2016��Chen���˹������������RNA���ݿ�circRNAdb�����Ի���RNA�ĵ����ʱ���DZ�ܽ����˷���[37]���о�����Ҫͨ�������Ķ���Ԥ�⣬IRESԪ��Ԥ�⣬�Լ������������ݱȶԵȼ������棬��32 914�������RNA�����У�ɸѡ��6 608�����б��뵰��DZ�ܵĻ���RNA������21���õ����������ݵ���֤��Yang���˺�Zhang����ͨ��circRNAdb�ṩ�IJο���Ϣ��ʵ����֤��Circ-FBXW7��circ-SHPRH�ܹ����뵰���ʣ�ORF�����ݿ���Ԥ�����Ϣһ�£�IRES����֤Ҳ�����ݿ��е���Ϣ�кܴ��ص����ɴ˿ɼ���circRNAdb������֤����RNA���뵰���ʾ��кܴ�IJο����塣
Ŀǰ����RNA���뵰��DZ��Ԥ�����Ҫ��CircPro��CircCode��2017�꣬Meng���˿�����������RNA-seq��Ribo-seq����ʶ����뵰����RNA�Ĺ���CircPro[38]���о�������ʹ��ת¼���������(RNA-seq)��Ϊ���룬���.GTF����ע���ļ����������ļ������û���RNA����CIRI2Ԥ����������еĻ���RNA[39]����Σ���ȡCIRI2���ý���Ļ���RNA���У�������ƴ�Ӻ����CPC(Coding potential calculator)Ԥ���RNA���������÷֡����ʹ�÷������������(Ribo-seq)��Ϊ���룬Ѱ�ұȶԲ�������RNA��reads�������뻷��RNA�������λ��(Junction sites)��reads���ȶԣ����ܱȶ��ϣ�����Ϊ�û���RNA�ķ���DZ���ṩ֧�֡�CircPro�ܹ������4���ļ�������Ҫ���ݷֱ�Ϊ��(a)Ԥ��Ļ���RNA���У�(b)ÿ��circRNA�ı���DZ�ܵ÷�(CPCԤ��)��(c)ÿ��circRNA��RNA-seq reads֧������Ribo-seq reads֧������(d)���뵰���ʵ�circRNAs��
2019�꣬Sun���˿����˻���RNA�����Ԥ������CircCode������һ�ֻ��ڻ���ѧϰ�ķ���[40]�������������£�����Ӧ��Ribo-seq�������ݣ������ȶԲ��ϻ������reads������ӳ�䵽����RNA�Ľ�ͷλ�ã�����ӳ����������Ϊ�ɷ���ĺ�ѡ����RNA(�ù�����CircPro���һ������)������ͨ������ѧϰ����BASiNETԤ���Խ��ͷ���ֵ�ribo-seq reads�Ƿ���Է��룬ȷ�����Է���Ļ���RNA�����Ԥ���RNA��ORF������ܱ���Ķ��ġ�
CircPro��CircCode�л���ribo-seq���ݷ����ķ������ƣ��нϸ߿��Ŷȣ���֮ͬ������CircCode���ڻ���ѧϰ��Ԥ����Щ�ȶ��Ϸ������λ���ribo-seq reads�Ƿ�ɷ��룬��CircPro���ȶ��ϵ�reads����Ϊ����RNA�ɱ��뵰��һ��֤�ݡ����⣬CircCodeʹ��FragGeneScanԤ���RNA�����Ķ���CircProͨ��CPCԤ���RNA���뵰��DZ�ܡ�
4 �ܽ���չ��һֱ����������RNA������Ϊ�DZ���RNA��Ȼ���������о����֣��൱һ���ֵĻ���RNA���б��뵰���ʵ�DZ�ܡ�Ŀǰ�����ڱ��뵰����RNA�������в���ȷ�����������ϢѧԤ�⼰����������ΪǷȱ�������谭��������ﻷ��RNA���뵰������о�������RNA����DZ�ܵ�Ԥ��ߴ��ǻ�������RNA(mRNA��lncRNA)�������ɣ�������RNA����mRNA���ص����֣���������ԵĻ�״�ṹ�������ؽ��������й��߶Ի���RNA����DZ�ܵ�Ԥ��������
����RNA�ڵ�IRES��m6A����λ���ѱ�֤ʵ�ɽ鵼���ñ����������ʼ���̣����IRES��m6A����λ��ʶ����������߱��뵰����RNA��ʶ�����������⣬����Խ��Խ��ı��뵰����RNA�����֣��Լ�����RNA���뵰���Ƶ������о������Ż��и������Ч�ı��뵰����RNA���������Ϣѧ�������ݿ���֣���������һ���ٽ����뵰����RNA�ķ��ּ����������ʼ���Ƶ������о���
�����
[1] SANGER H L, KLOTZ G, RIESNER D, et al. Viroids are single-stranded covalently closed circular RNA molecules existing as highly base-paired rod-like structures[J]. Proceedings of the National Academy of Sciences, 1976, 73(11): 3852-3856. DOI:10.1073/pnas.73.11.3852 (
 0)
0)[2] HSU M T, MIGUEL C P. Electron microscopic evidence for the circular form of RNA in the cytoplasm of eukaryotic cells[J]. Nature, 1979, 280(5720): 339-340. DOI:10.1038/280339a0 (
 0)
0)[3] RYBAK-WOLF A, STOTTMEISTER C, GLA?AR P, et al. Circular RNAs in the mammalian brain are highly abundant, conserved, and dynamically expressed[J]. Molecular Cell, 2015, 58(5): 870-885. DOI:10.1016/j.molcel.2015.03.027 (
 0)
0)[4] WANG Y, WANG Z. Efficient backsplicing produces translatable circular mRNAs[J]. Rna, 2015, 21(2): 172-179. DOI:10.1261/rna.048272.114 (
 0)
0)[5] LEGNINI I, DI T G, ROSSI F, et al. Circ-ZNF609 is a circular RNA that can be translated and functions in myogenesis[J]. Molecular Cell, 2017, 66(1): 22-37.e9. DOI:10.1016/j.molcel.2017.02.017 (
 0)
0)[6] YANG Y, GAO X, ZHANG M, et al. Novel role of FBXW7 circular RNA in repressing glioma tumorigenesis[J]. JNCI: Journal of the National Cancer Institute, 2017, 110(3): 304-315. DOI:10.1093/jnci/djy116 (
 0)
0)[7] ZHANG M, HUANG N, YANG X, et al. A novel protein encoded by the circular form of the SHPRH gene suppresses glioma tumorigenesis[J]. Oncogene, 2018, 37(13): 1805. DOI:10.1038/s41388-017-0019-9 (
 0)
0)[8] ZHANG M, ZHAO K, XU X, et al. A peptide encoded by circular form of LINC-PINT suppresses oncogenic transcriptional elongation in glioblastoma[J]. Nature Communications, 2018, 9(1): 4475. DOI:10.1038/s41467-018-06862-2 (
 0)
0)[9] LIANG W C, WONG C W, LIANG P P, et al. Translation of the circular RNA circ��-catenin promotes liver cancer cell growth through activation of the Wnt pathway[J]. Genome Biology, 2019, 20(1): 84. DOI:10.1186/s13059-019-1685-4 (
 0)
0)[10] VAN HEESCH S, WITTE F, SCHNEIDER-LUNITZ V, et al. The translational landscape of the human heart[J]. Cell, 2019, 178(1): 242-260. DOI:10.1016/j.cell.2019.05.010 (
 0)
0)[11] WEINGARTEN-GABBAY S, ELIAS-KIRMA S, NIR R, et al. Systematic discovery of cap-independent translation sequences in human and viral genomes[J]. Science, 2016, 351(6270): aad4939. DOI:10.1126/science.aad4939 (
 0)
0)[12] LI S, MASON C E. The pivotal regulatory landscape of RNA modifications[J]. Annual Review of Genomics and Human Genetics, 2014, 15: 127-150. DOI:10.1146/annurev-genom-090413-025405 (
 0)
0)[13] WEI C M, GERSHOWITZ A, MOSS B. Methylated nucleotides block 5' terminus of HeLa cell messenger RNA[J]. Cell, 1975, 4(4): 379-386. DOI:10.1016/0092-8674(75)90158-0 (
 0)
0)[14] CSEPANY T, LIN A, BALDICK C J, et al. Sequence specificity of mRNA N6-adenosine methyltransferase[J]. Journal of Biological Chemistry, 1990, 265(33): 20117-20122. DOI:10.1093/nar/18.19.5735 (
 0)
0)[15] HARPER J E, MICELI S M, ROBERTS R J, et al. Sequence specificity of the human mRNA N6-adenosine methylase in vitro[J]. Nucleic Acids Research, 1990, 18(19): 5735-5741. DOI:10.1093/nar/18.19.5735 (
 0)
0)[16] WANG X, ZHAO B S, ROUNDTREE I A, et al. N6-methyladenosine modulates messenger RNA translation efficiency[J]. Cell, 2015, 161(6): 1388-1399. DOI:10.1016/j.cell.2015.05.014 (
 0)
0)[17] ZHOU J, WAN J, GAO X, et al. Dynamic m6A mRNA methylation directs translational control of heat shock response[J]. Nature, 2015, 526(7574): 591. DOI:10.1038/nature15377 (
 0)
0)[18] MEYER K D, PATIL D P, ZHOU J, et al. 5' UTR m6A promotes cap-independent translation[J]. Cell, 2015, 163(4): 999-1010. DOI:10.1016/j.cell.2015.10.012 (
 0)
0)[19] LI A, CHEN Y S, PING X L, et al. Cytoplasmic m6A reader YTHDF3 promotes mRNA translation[J]. Cell Research, 2017, 27(3): 444. DOI:10.1038/cr.2017.10 (
 0)
0)[20] YANG Y, FAN X, MAO M, et al. Extensive translation of circular RNAs driven by N6-methyladenosine[J]. Cell Research, 2017, 27(5): 626. DOI:10.1038/cr.2017.31 (
 0)
0)[21] WU T Y, HSIEH C C, HONG J J, et al. IRSS: A web-based tool for automatic layout and analysis of IRES secondary structure prediction and searching system in silico[J]. BMC Bioinformatics, 2009, 10(1): 160. DOI:10.1186/1471-2105-10-160 (
 0)
0)[22] HONG J J, WU T Y, CHANG T Y, et al. Viral IRES prediction system-A web server for prediction of the IRES secondary structure in silico[J]. PLoS One, 2013, 8(11): e79288. DOI:10.1371/journal.pone.0079288 (
 0)
0)[23] KOLEKAR P, PATASKAR A, KULKARNI-KALE U, et al. IRESPred: Web server for prediction of cellular and viral internal ribosome entry site (IRES)[J]. Scientific Reports, 2016, 6: 27436. DOI:10.1038/srep27436 (
 0)
0)[24] ZHAO J, WU J, XU T, et al. IRESfinder: Identifying RNA internal ribosome entry site in eukaryotic cell using framed k-mer features[J]. Journal of Genetics and Genomics= Yi Chuan Xue Bao, 2018, 45(7): 403. DOI:10.1016/j.jgg.2018.07.006 (
 0)
0)[25] BONNAL S, BOUTONNET C, PRADO-LOUREN?O L, et al. IRESdb: The internal ribosome entry site database[J]. Nucleic Acids Research, 2003, 31(1): 427-428. DOI:10.1093/nar/gkg003 (
 0)
0)[26] MOKREJ? M, MA?EK T, VOP��LENSKy V, et al. IRESite��A tool for the examination of viral and cellular internal ribosome entry sites[J]. Nucleic Acids Research, 2009, 38(suppl_1): D131-D136. DOI:10.1093/nar/gkp981 (
 0)
0)[27] KALVARI I, ARGASINSKA J, QUINONES-OLVERA N, et al. Rfam 13.0: Shifting to a genome-centric resource for non-coding RNA families[J]. Nucleic Acids Research, 2017, 46(D1): D335-D342. DOI:10.1093/nar/gkx1038 (
 0)
0)[28] ZHOU Y, ZENG P, LI Y H, et al. SRAMP: Prediction of mammalian N6-methyladenosine (m6A) sites based on sequence-derived features[J]. Nucleic Acids Research, 2016, 44(10): e91-e91. DOI:10.1093/nar/gkw104 (
 0)
0)[29] LINDER B, GROZHIK A V, OLARERIN-GEORGE A O, et al. Single-nucleotide-resolution mapping of m6A and m6 Am throughout the transcriptome[J]. Nature Methods, 2015, 12(8): 767. DOI:10.1038/nmeth.3453 (
 0)
0)[30] KE S, ALEMU E A, MERTENS C, et al. A majority of m6A residues are in the last exons, allowing the potential for 3' UTR regulation[J]. Genes & Development, 2015, 29(19): 2037-2053. DOI:10.1101/gad.269415.115 (
 0)
0)[31] MEYER K D, JAFFREY S R. The dynamic epitranscriptome: N6-methyladenosine and gene expression control[J]. Nature Reviews Molecular Cell Biology, 2014, 15(5): 313. DOI:10.1038/nrm3785 (
 0)
0)[32] SUN W J, LI J H, LIU S, et al. RMBase: A resource for decoding the landscape of RNA modifications from high-throughput sequencing data[J]. Nucleic Acids Research, 2015, 44(D1): D259-D265. DOI:10.1093/nar/gkv1036 (
 0)
0)[33] ZHENG Y, NIE P, PENG D, et al. m6A Var: A database of functional variants involved in m6A modification[J]. Nucleic Acids Research, 2017, 46(D1): D139-D145. DOI:10.1093/nar/gkx895 (
 0)
0)[34] KONG L, ZHANG Y, YE Z Q, et al. CPC: Assess the protein-coding potential of transcripts using sequence features and support vector machine[J]. Nucleic Acids Research, 2007, 35(suppl_2): W345-W349. DOI:10.1093/nar/gkm391 (
 0)
0)[35] WANG L, PARK H J, DASARI S, et al. CPAT: Coding-potential assessment tool using an alignment-free logistic regression model[J]. Nucleic Acids Research, 2013, 41(6): e74-e74. DOI:10.1093/nar/gkt006 (
 0)
0)[36] SUN L, LUO H, BU D, et al. Utilizing sequence intrinsic composition to classify protein-coding and long non-coding transcripts[J]. Nucleic Acids Research, 2013, 41(17): e166-e166. DOI:10.1093/nar/gkt646 (
 0)
0)[37] CHEN X, HAN P, ZHOU T, et al. circRNADb: A comprehensive database for human circular RNAs with protein-coding annotations[J]. Scientific Reports, 2016, 6: 34985. DOI:10.1038/srep34985 (
 0)
0)[38] MENG X, CHEN Q, ZHANG P, et al. CircPro: An integrated tool for the identification of circRNAs with protein-coding potential[J]. Bioinformatics, 2017, 33(20): 3314-3316. DOI:10.1093/bioinformatics/btx446 (
 0)
0)[39] GAO Y, WANG J, ZHAO F. CIRI: An efficient and unbiased algorithm for de novo circular RNA identification[J]. Genome Biology, 2015, 16(1): 4. DOI:10.1186/s13059-014-0571-3 (
 0)
0)[40] SUN Peisen, LI Guanglin. CircCode:A powerful tool for identifying circRNA coding ability[J]. Frontiers in Genetics, 2019, 10: 981. DOI:10.3389/fgene.2019.00981 (
 0)
0)