
 , 张瑜芬
, 张瑜芬 , 胡俊, 姚志伟, 黄武, 汤露
, 胡俊, 姚志伟, 黄武, 汤露浙江工业大学环境学院, 杭州 310032
收稿日期: 2020-07-02; 修回日期: 2020-08-10; 录用日期: 2020-08-10
基金项目: 浙江省科技计划项目-公益技术(No.LGF20B070002)
作者简介: 姜理英(1977-), 女, 教授(博士), E-mail: jiangly@zjut.edu.cn
通讯作者(责任作者): 姜理英
摘要:以TiO2为载体,采用共沉淀法制备了3种双金属催化剂(Co-Mn/TiO2、Ce-Mn/TiO2和Nb-Mn/TiO2),与低温等离子体(NTP)协同对氯苯进行降解,并通过XRD、SEM、TEM、BET、XPS、H2-TPR和O2-TPD手段表征其物化性质,以阐明不同催化剂对氯苯的等离子体催化降解差异.结果显示,与单独的NTP相比,双金属催化剂耦合NTP可显著提高氯苯的降解效率和矿化率,减少有毒副产物的产生.Co-Mn/TiO2的催化活性优于Ce-Mn/TiO2和Nb-Mn/TiO2,在氯苯初始浓度为300 mg·m-3,气体停留时间为2 s,放电电压为15 kV的工况条件下,Co-Mn/TiO2耦合的NTP系统对氯苯的降解效率和CO2选择性分别达78.14%和51.02%,其O3的排放浓度为211 mg·m-3.表征结果也验证了以上结论,3种催化剂的金属氧化物均在TiO2表面高度分散,催化剂的比表面积为51~64 m2·g-1.Co-Mn/TiO2催化剂表面的高Mn4+/Mn3+比和Oads含量呈现出更多的氧空位,增大了氧迁徙率,因而表现出最高的催化活性和催化氧化性能.研究表明,双金属锰基催化剂耦合NTP降解氯苯具有很好的应用前景.
关键词:低温等离子体双金属锰基催化剂氯苯降解特性副产物
Removal of chlorobenzene by non-thermal plasma combined with bimetallic manganese-based catalyst
JIANG Liying

 , ZHANG Yufen
, ZHANG Yufen , HU Jun, YAO Zhiwei, HUANG Wu, TANG Lu
, HU Jun, YAO Zhiwei, HUANG Wu, TANG LuCollege of Environmental, Zhejiang University of Technology, Hangzhou 310032
Received 2 July 2020; received in revised from 10 August 2020; accepted 10 August 2020
Abstract: Bimetallic manganese-based catalysts (Co-Mn/TiO2, Ce-Mn/TiO2 and Nb-Mn/TiO2) were supported on TiO2 by co-precipitation method and combined with non-thermal plasma (NTP) catalytic degradation of chlorobenzene (CB). The physicochemical properties of the catalysts were characterized by XRD、SEM、TEM、BET、XPS、H2-TPR and O2-TPD to clarify the differences between the various catalysts during the plasma catalytic degradation of CB. The experimental results showed that the bimetallic catalysts combined with NTP significantly improved the CB removal efficiency and mineralization rate compared with the NTP alone. Meanwhile, it greatly reduced the production of poisonous by-products (O3 and NOx). Co-Mn/TiO2 exhibited better catalytic activity than Ce-Mn/TiO2 and Nb-Mn/TiO2 in the NTP-catalysis reactor. At the initial concentration of 300 mg·m-3, residence time of 2 s and discharge voltage of 15 kV, the degradation efficiency and CO2 selectivity were 78.14% and 51.02% respectively in the Co-Mn/TiO2 coupled NTP reactor, and the emissions of O3 reached the minimum of 211 mg·m-3. The characterization results also verified that the metal oxides were highly dispersed on the surface of TiO2 for the catalysts, and the specific surface area was 51~64 m2·g-1. The high Mn4+/Mn3+ ratio and Oads content on the surface of the Co-Mn/TiO2 catalyst presented more O-vacancies and increased the oxygen migration rate, exhibiting the highest catalytic activity and redox property. Therefore, bimetallic manganese-based catalyst combined with NTP has a good application prospect for the degradation of CB.
Keywords: non-thermal plasmabimetallic manganese-based catalystchlorobenzenedegradation characteristicsby-product
1 引言(Introduction)挥发性有机物化合物(Volatile Organic Compounds, VOCs)是大气中的主要污染物, 由于对生态环境和人类健康有害而受到广泛关注(Sultana et al., 2015; Zhang et al., 2018).其中, 氯化有机物由于其高毒性且难以降解, 因而在《斯哥德尔持久性有机污染物公约》中被列入有限控制有机污染物(Qian et al., 2004).近年来, 应用于VOCs污染控制的技术主要包括:高温焚烧、催化氧化(Qu et al., 2012)、生物氧化(Wang et al., 2010)和低温等离子体技术等, 其中, 低温等离子体(Nonthermal Temperature Plasma, NTP)凭借其在常温和大气压下对VOCs表现出的良好去除能力, 现已被广泛应用于VOCs的治理, 特别是在处理低浓度VOCs方面(Bahri et al., 2014; Thevenet et al., 2014).除此之外, NTP处理技术还具有设备简单、热损失少和对污染物耐受性高等有优点.尽管如此, NTP技术仍然存在一些缺陷从而限制其进一步应用, 如能量效率低和产生不必要的副产物等(Dang et al., 2016).
目前大量研究表明, NTP协同催化剂可有效提高能量效率并减少副产物的形成(Assadi et al., 2014).过渡金属Mn因价格低廉且性能优越而被广泛应用于NTP催化中, 同时Mn基催化剂活性组分分散, 能够将O3分解为活性氧, 进一步提升NTP降解VOCs的性能(Sivachandiran et al., 2015).一些新的研究表明, 通过向Mn基催化剂中掺杂其他金属可以提高VOCs的去除效率且将副产物产量最小化(Yao et al., 2019).金属在Mn基催化剂中掺杂是通过改变放电特性、增加电子交换, 来提供更多的活性物质和氧空位来促进污染物的分解, 同时还可以提高酸耐受性, 加强O3在室温下的分解(Huang et al., 2015; Wang et al., 2017; Sun et al., 2018).催化剂中支撑材料的引入可以为催化剂提供有序的孔径结构, 提升催化剂的吸附能力并改善催化特征(Yao et al., 2018).研究发现, TiO2性质稳定, 孔径结构良好, 具有光催化活性, 有助于O3的分解, 是很好的催化剂支撑材料(Maciuca et al., 2012).
氯苯是一种典型的氯化有机污染物, 化学性质稳定, 难于降解, 已被广泛应用于工业过程中(Jose et al, 2019).氯苯在NTP催化解离中会发生C—Cl键的解离, 产生的氯化的环己二烯酮类等化合物会造成催化剂孔径活性位点氯化失活(He et al., 2012; 2019).而目前在NTP耦合催化系统中针对氯苯降解的双金属催化剂研究尚不充分, 从而影响了双金催化剂在该领域的广泛应用.
基于此, 本研究采用共沉淀法制备以TiO2为支撑材料的3种双金属催化剂, 并耦合NTP反应器催化降解氯苯, 从氯苯去除效率、CO2选择性和副产物(O3和NOx)产量方面评估双金属催化剂降解氯苯的催化活性.同时, 使用XRD、SEM、TEM、BET、XPS、H2-TPR和O2-TPD等方法对双金属催化剂进行物化表征, 以阐明不同双金属催化剂对氯苯的NTP催化降解差异, 从而选取最具NTP催化降解氯苯应用前景的催化剂.
2 材料与方法(Materials and methods)2.1 材料制备3种双金属催化剂参考之前的文献采用共沉淀法制备(Song et al., 2018), 所有试剂均为分析纯级别, 均购自阿拉丁试剂有限公司.用P25 TiO2作为Mn基催化剂支撑材料.具体操作为:将0.29 g金属硝酸盐Mn(NO3)2·5H2O与等物质的量的乙酸钴(C4H6CoO4·4H2O)、草酸铌(C10H5NbO20·xH2O)和硝酸铈(CeN3O9·6H2O)一并溶于50 mL去离子水中并搅拌形成均匀溶液;将P25 TiO2粉末(n(金属)∶n(Mn)∶n(Ti)=1∶1∶20)缓慢加入上述溶液中搅拌2 h, 再缓慢加入25 mL的Na2CO3溶液(0.2 mol·L-1);然后将沉淀物搅拌4 h, 过滤并用去离子水洗涤至中性;最后将得到的残余物在80 ℃下干燥过夜, 并用马弗炉在350 ℃(3 ℃·min-1)下煅烧5 h, 分别得到Mn-Co/TiO2、Mn-Nb/TiO2和Mn-Ce/TiO2催化剂.
2.2 材料表征X射线衍射(XRD)使用德国BrukerAXS D8 Advance型X射线衍射仪测定, 配备Cu Kα射线, 波长为0.154056 nm, 并在2θ为10°~80°范围下扫描搜集XRD图谱, 扫描速度为5°·min-1, 之后用X′Pert HighScore Plus和Origin软件进行XRD能谱处理.扫描电子显微镜图(SEM)和透射电子显微镜图(TEM)分别使用SU8010和FEI Verios 460扫描电镜观测.比表面积及孔结构分析(BET)使用Micromeritics Tristar 3000型比表面测定仪进行测定, 并采用Barrett Joyner Halenda(BJH)计算多孔体积和孔径分布.X射线光电子能谱(XPS)在Thermo ESCALAB 250XI型X射线光电子能谱仪中完成, 采用Al Kα为X射线光源并经过单色化处理, 以结合能为284.6 eV的C 1s峰进行校准, 之后用Casaxps和Origin软件进行XPS能谱处理.程序升温还原(H2-TPR和O2-TPD)在装备TCD检测的AutoChem1 Ⅱ 2920装置中进行, 首先将100 mg催化剂预热至300 ℃, 并用He吹扫60 min, 以除去水分和其他吸附的气体, 再冷却至50 ℃;然后在50 ℃下分别用5%H2/He和5%O2/He(50 mL·min-1)以10 ℃·min-1的升温速率升温至800 ℃.
2.3 等离子体催化性能评价该设备由混合气体系统、反应器系统和分析仪器组成, 具体工艺流程见图 1.使压缩空气通过干燥剂以除去空气中的水, 然后使用温控浴(40 ℃)混合挥发的氯苯.通过控制质量流量控制器(MFC)的气流速率和氯苯的注入速率, 可以确定氯苯的进口浓度.在装有催化剂(0.3 g)的反应器中进行等离子体放电实验, 该催化剂包裹在石英棉中并置于放电间隙.NTP反应器与以前使用的相同, 由浙江大学制造(Jiang et al., 2017).反应器由内径为1.75 cm、外径为2.61 cm、长度为39.8 cm的石英玻璃制成, 用长度为10 cm的铜片包裹并接地, 用直径为0.6 cm的不锈钢棒作为高压电极, 由南京苏曼公司制造的CTP-2000K为NTP装置提供高压电.采用杭州华南电子技术公司生产的DPO3012示波器测定放电电压.采用美国安捷伦生产的6890N气相色谱仪(GC, 配备FID和TCD检测器)测量氯苯和CO2浓度.采用Thermo Scientific公司生产的42i-HL NO-NO2-NOx气体分析仪确定NOx浓度, 并通过碘量法测量O3浓度.
图 1(Fig. 1)
 |
| 图 1 NTP处理氯苯的工艺流程图 Fig. 1Schematic diagram of NTP for degradation of chlorobenzene |
为了比较不同双金属催化剂对氯苯的催化氧化性能, NTP反应器的反应条件控制为:氯苯在放电区停留时间为2 s, 进气浓度为300 mg·m-3, 保持进气干燥.催化剂的性能通过计算氯苯降解率(η)和CO2选择性(SCO2)进行评价, 公式如下:
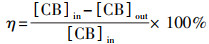 | (1) |
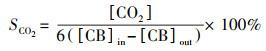 | (2) |
3 结果与讨论(Results and discussion)3.1 催化剂对氯苯的降解性能分析3.1.1 吸附效率图 2a所示为3种不同双金属催化剂对氯苯吸附效果的评估, 其中, 氯苯的进气浓度为300 mg·m-3, 通过检测氯苯的出口浓度绘制了3种双金属催化剂对氯苯的吸附量随时间变化的折线图.由图 2a可知, 不同催化剂对氯苯的吸附在20 min后几乎都达到饱和, 氯苯的出口浓度均在297 mg·m-3以上, 与氯苯的进口浓度几乎一致, 且对氯苯的吸附效率均低于2%.与单独的TiO2载体对氯苯的吸附相比, 负载金属后催化剂对氯苯的吸附能力减弱, 这是因为金属离子在TiO2孔径中的掺杂造成的.同时数据表明, 催化剂对氯苯的吸附作用不明显, 在协同等离子体过程中可忽略不计.为排除吸附作用对实验的影响, 实验前均进行30 min的氯苯吸附, 并在等离子体稳定后进行数据记录.
图 2(Fig. 2)
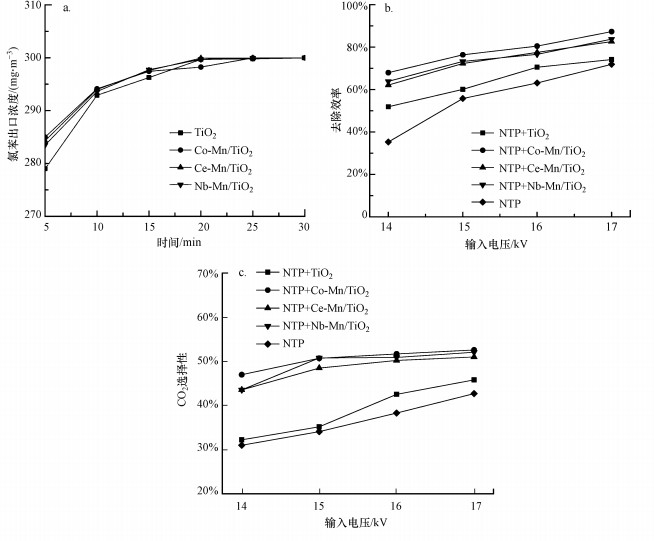 |
| 图 2 不同催化剂对氯苯的吸附效率(a)、氯苯等离子体催化降解效率(b)及CO2选择性(c)的影响 Fig. 2Influence of different catalysts on the adsorption efficiency for chlorobenzene (a), the plasma catalytic degradation efficiency of chlorobenzene(b) and selectivity of CO2(c) |
3.1.2 降解效率图 2b为不同双金属催化剂协同NTP放电时, 氯苯降解效率随输入电压变化的折线图, 并以单独的等NTP放电和支撑材料TiO2协同NTP作为对照试验, 试验控制氯苯在放电区停留时间为2 s, 进气浓度为300 mg·m-3.根据斜率变化可知, 提高放电电压在一定范围内有利于氯苯降解, 随着电源输入功率的增加, NTP系统中产生的活性颗粒(O·、HO·和HO2·)也增加, 但当电压过高时反应器温度会升高, 可能导致火花放电, 不利于活性颗粒的产生(Li et al., 2015).NTP反应器中载体TiO2的添加能够延长氯苯的停留时间和介电常数, 这导致观察到高于单独NTP的氯苯转化率(Mei et al., 2015).双金属催化剂的耦合也能够提高NTP对氯苯的降解效率, 体现了催化剂与NTP的协同作用, 且在相同输入电压下(15 kV)的氯苯去除性能不同, 排序为Co-Mn/TiO2(78.14%)>Nb-Mn/TiO2(73.51%)>Ce-Mn/TiO2(71.33%), 该结果与催化剂的比表面BET并不一致, 但与氧化还原性质的表征一致, 这说明催化剂的表面结构不是催化剂性能的决定性因素.在Co-Mn/TiO2催化剂协同NTP的情况下基本保持了78%以上的氯苯去除率, 氯苯的出气浓度可降低至60 mg·m-3左右, 而工业条件下废气中的氯苯浓度普遍低于较低300 mg·m-3, 从理论上来说, NTP的Co-Mn/TiO2催化体系能够使氯苯出气浓度低于GB16297—1996规定的最高允许排放浓度(60 mg·m-3).Co-Mn/TiO2催化剂耦合NTP对氯苯的去除效果具有一定优势, 高于研究报道中采用CuO/MnO2协同NTP催化的70.7%的氯苯降解率(Zhu et al., 2015).
3.1.3 CO2选择性图 2c显示了不同双金属与NTP协同降解氯苯时的CO2选择性, 其结果与氯苯的去除率表现出的规律相似.CO2选择性也随着输入电压的增加而增加, 这是因为随着施加电压的增加平均电场增强, 产生具有较高能量的电子并轰击高键能结构物质(如苯环), 促使深度氧化降解(Karatum et al., 2016).仅含TiO2的NTP反应器的CO2选择性略低, TiO2上负载双金属使氯苯的矿化率更高, 一方面是因为金属催化剂的加入可以改变介电系数, 增加微放电, 对电子密度的增加产生一定影响, 从而进一步通过电子撞击产生更多的活性物质, 来驱动氯苯发生化学反应(Kim et al., 2011; Snoeckx et al., 2013);另一方面, 在NTP放电中过渡金属通过电子转移引起的价态变化更易产生更多的活性位点, 这些活性位点可以增强TiO2的吸附作用, 更容易与催化剂表面的活性物质接触反应(Trinh et al., 2015).
3.1.4 副产物NTP反应器的高压电场不可避免的会产生O3, 同时随着不间断的污染物与空气混合物的涌入也产生了NOx, 且从理论上分析这些副产物的产量随着电压的升高而增加, O3和NOx的产生过程如式(3)~(5)所示(Ghorbani et al., 2017).
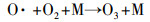 | (3) |
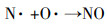 | (4) |
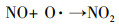 | (5) |
图 3(Fig. 3)
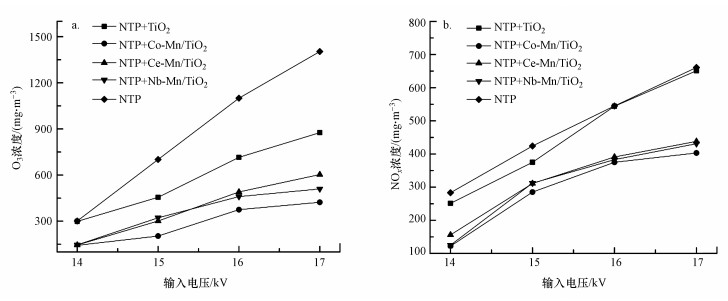 |
| 图 3 不同催化剂对O3(a)和NOx(b)产生量的影响 Fig. 3Effects of different catalysts on the production of O3(a) and NOx(b) |
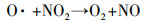 | (6) |
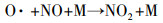 | (7) |
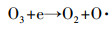 | (8) |
图 4(Fig. 4)
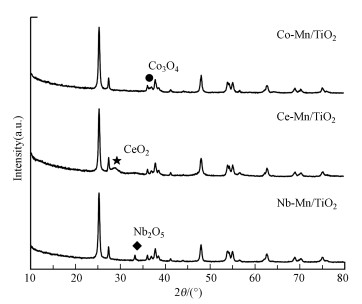 |
| 图 4 各种催化剂的XRD图谱 Fig. 4XRD spectra of synthesized catalysts |
3.2.2 SEM-TEM图 5是3种催化剂的形貌特征, 扫描电镜(SEM)和透射电镜(TEM)图像以200 nm的尺度进行捕捉拍摄.通过SEM图像可以看出(图 5a、5c、5e), 3种催化剂都具备均一的粒径和形状, 整体以光滑的球状颗粒聚集, 双金属的引入未改变TiO2载体的基础形状, 这进一步证明双金属氧化物高度分散地负载于TiO2的表面.TEM表征结果(图 5b、5d、5f)进一步证实了3种催化剂形状的相似性, 催化剂的粒径差距微小, 颗粒的平均直径约为20~30 nm.TEM图像显示出Co-Mn/TiO2催化剂的颗粒聚集度较低, 空间分布均匀.
图 5(Fig. 5)
 |
| 图 5 Co-Mn/TiO2(a, b)、Ce-Mn/TiO2(c, d)和Nb-Mn/TiO2(e, f)催化剂的SEM图(上)和TEM图(下) Fig. 5SEM(up) and TEM(bottom) images of Co-Mn/TiO2(a, b), Ce-Mn/TiO2(c, d) and Nb-Mn/TiO2(e, f) |
3.2.3 BET样品的表面积、孔体积和孔径等物理性质(表 1)与上述表征结果吻合, 催化剂的孔径结构性质差距不大, 负载后催化剂的孔径相较于纯TiO2都有所减小.其中, Co-Mn/TiO2催化剂的孔径结构性质与纯TiO2最相近, 这表明相较于金属Nb和Ce, 金属Co的负载对TiO2表面性质的变化影响最小.Ce-Mn/TiO2和Nb-Mn/TiO2催化剂比表面积和孔容的增加可能与双金属的强相互作用团聚成更小的纳米颗粒有关.
表 1(Table 1)
| 表 1 不同催化剂的孔结构性质 Table 1 Pore structure properties of different catalysts | ||||||||||||||||||||
表 1 不同催化剂的孔结构性质 Table 1 Pore structure properties of different catalysts
| ||||||||||||||||||||
3.2.4 XPS图 6中给出的XPS数据用于研究催化剂的化学成分和缺陷, 表 2在XPS表征结果的基础上列出了催化剂表面的原子含量.在制备的3种双金属催化剂表面均观察到Mn 2p3/2光谱在结合能为644.3 eV和641.1 eV处分解为两个组分(图 6a), 它们分别可代表表面Mn4+和Mn3+(Bai et al., 2016).催化剂表面的MnOx的还原顺序为:MnO2/Mn2O3→Mn3O4→MnO, MnO2/Mn2O3更容易形成氧自由基(O·), Mn4+和Mn3+的取代为氯苯降解提供了更多的氧空位, 表现出更高的催化活性(Lin et al., 2018).换言之, Co-Mn/TiO2催化剂表现出较高的Mn4+/Mn3+, 它的催化活性就越高.同时也观察到O 1s光谱可分解为两个以531.3 eV和529.6 eV为中心的特征峰(图 6b), 前者主要是由表面吸附氧(Oads)引起的, 而后者归因于表面晶格氧(Olatt)的存在(Kan et al., 2017).在3种双金属催化剂中, Co-Mn/TiO2的Oads含量最高, Nb-Mn/TiO2其次, Co-Mn/TiO2的Oads含量最低.研究表明, Oads可以改善催化作用的氧化过程(Jha et al., 2014).Co-Mn/TiO2催化剂的Co 2p图谱可分为两个以781.1 eV和779.4 eV为中心的特征峰(图 6c), 分别代表Co2+和Co3+.Ce-Mn/TiO2催化剂的Ce 3d能谱中(图 6d), 结合能在887.2 eV和895.4 eV的特征峰为Ce4+, 结合能在880.1 eV和883.5 eV的特征峰为Ce3+.图 6e为Nb-Mn/TiO2催化剂的Nb 3d能谱, 其中, Nb 3p光谱中出现以207.1 eV和206.5 eV为中心的特征峰, 分别代表Nb5+和Nb4+.催化剂表面高价态的金属离子可以被还原为低价态, 然后再次被Oads氧化为高价态, 也就是说催化剂表面的金属氧化物之间存在着电子转移(Xn+1+e-→ Xn+Oads → Xn+1, 其中, X代表掺杂的金属), 因此, Co-Mn/TiO2催化剂中Co3+的高比存在体现了较好的催化性能(Wang et al., 2018).
图 6(Fig. 6)
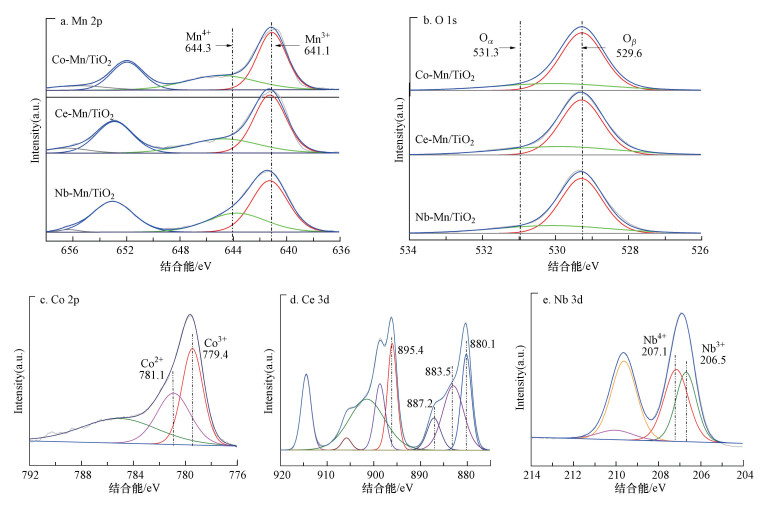 |
| 图 6 各种催化剂的XPS图谱 Fig. 6XPS spectra of synthesized catalysts |
表 2(Table 2)
| 表 2 催化剂的XPS结果 Table 2 XPS results of the catalysts | ||||||||||||||||||||||||
表 2 催化剂的XPS结果 Table 2 XPS results of the catalysts
| ||||||||||||||||||||||||
3.2.5 H2-TPR图 7a显示了不同双金属催化剂的氧化还原性, H2-TPR曲线显示3种催化剂在180~400 ℃范围内均出现了还原峰, 这主要是MnOx的还原.其中, Co-Mn/TiO2和Nb-Mn/TiO2在该范围内显示出明显的两个峰, 还原温度为230~260 ℃的还原峰与Mn4+还原为Mn3+有关(Kim et al., 2010), 还原温度为300~370 ℃的还原峰与Mn3+还原为Mn2+有关(Lu et al., 2014).Co-Mn/TiO2与Nb-Mn/TiO2相比, Co-Mn/TiO2的还原峰出现在更低的温度, 证明Co-Mn/TiO2催化剂具有更高的还原性;而Ce-Mn/TiO2催化剂的还原峰在290~400 ℃范围内重叠且不突出, 这可能归因于Ce-Mn共存的较少, 是以CeO2和MnOx的形式单独存在(Yu et al., 2010).Co-Mn/TiO2催化剂在474 ℃处出现的还原峰与氧化钴的还原有关, 而氧化铌和氧化铈还原需要更高的温度(Xu et al., 2017a).
图 7(Fig. 7)
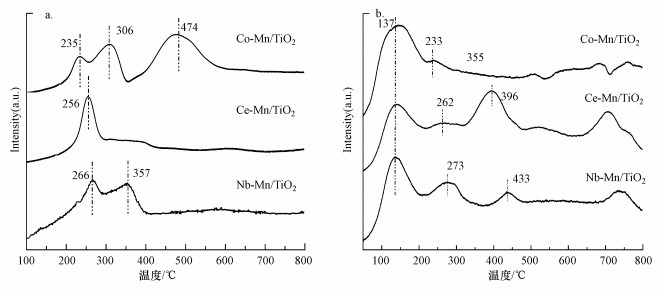 |
| 图 7 各种催化剂的H2-TPR(a)及O2-TPD(b) Fig. 7H2-TPR(a) and O2-TPD(b) spectra of synthesized catalysts |
3.2.6 O2-TPD为了解催化剂表面的氧的迁徙, 对双金属催化剂进行了O2-TPD测试, 结果如图 7b所示.催化剂表面的氧种类分为两类:表面吸附氧(包括分子氧O2(ads)、原子氧O2-(ads)和原子氧O-(ads))和晶格氧(O2-(latt)), 这些种类的氧是通过以下顺序变化的:O2(ads)→O2-(ads)→O-(ads)→O2-(latt)(Wang et al., 2017).在图 7b中, Co-Mn/TiO2、Ce-Mn/TiO2和Nb-Mn/TiO2催化剂均具有4种氧, O2(ads)和O2-(ads)在较低温度下(300 ℃以下)释放, O-(ads)出现在350~450 ℃之间, 而O2-(latt)在较高温度(600 ℃以上)释放.Co-Mn/TiO2催化剂的O-(ads)代表峰的出现温度(355 ℃)低于Ce-Mn/TiO2(396℃)和Nb-Mn/TiO2(433 ℃)催化剂, 因而提高了O2-(ads)与O-(ads)的迁徙率(Song et al., 2018).双金属催化剂的氧析出峰出现温度不同, 因为金属离子部分取代Mn4+和Mn3+的位置, 产生的氧空位致使氧析出峰向更低的温度移动, 其中, Co的掺杂能够产生更多的氧空位(Zhang et al., 2006).另外, 大量的O2(ads)和O2-(ads)及较高的O(ads)/O(latt)比率也证明了Co-Mn/sTiO2催化剂的优越性.O2-TPD曲线显示的催化剂活性与氯苯催化活性一致.
以上结果表明, 双金属的负载催化剂表面存在不同价态的金属离子, 以Co-Mn/TiO2催化剂为例, 金属Co离子(Co3+和Co2+)与金属Mn离子(Mn4+和Mn3+)存在电子传递, 引起了活性位点的替换从而产生了氧空位, 增加了催化剂表面的活性物质;同时, 催化条件下O3的产生和分解能够产生更多的活性物质(O·), 从而促进氯苯降解, 提高矿化率, 抑制副产物的产生.Co-Mn/TiO2相较于Ce-Mn/TiO2和Nb-Mn/TiO2, 其表面的化学缺陷更突出, 拥有更多的氧空位来吸附氯苯, 同时还具备较高的氧迁徙率和还原性, 从而增强了对O3和NOx的抑制作用, 促进氯苯氧化分解为CO2、H2O和HCl.
4 结论(Conclusions)1) 用共沉淀法制备的3种双金属催化剂中, Co-Mn/TiO2催化剂在协同NTP系统处理氯苯时表现出优秀的氯苯降解性和CO2选择性, 分别可达78.14%和51.02%.
2) NTP反应器中副产物的热解和O原子的竞争可降低副产物的产生速率, 双金属催化剂协同增加了表面活性物质(O·), 同时催化O3分解产生O·, 促进了氯苯深度氧化.
3) 双金属催化剂呈现表面光滑的球形分布, 金属氧化物高度分散于TiO2表面, 掺杂金属分别以Co3O4、CeO2和Nb2O5的形式存在.
4) 催化剂表面存在化学缺陷, Co-Mn/TiO2催化剂表现出较高的Mn4+/Mn3+, 与Oads更易形成氧自由基(O·), 从而改善氧化过程, 同时还具备更高的氧化还原性和氧迁徙率.
参考文献
| Assadi A A, Bouzaza A, Merabet S, et al. 2014. Modeling and simulation of VOCs removal by nonthermal plasma discharge with photocatalysis in a continuous reactor: Synergetic effect and mass transfer[J]. Chemical Engineering Journal, 258: 119-127. DOI:10.1016/j.cej.2014.07.050 |
| Bahri M, Haghighat F. 2014. Plasma-based indoor air cleaning technologies: The state of the art-review[J]. Clean-Soil, Air, Water, 42(12): 1667-1680. DOI:10.1002/clen.201300296 |
| Bai B, Qiao Q, Arandiyan H, Li J, et al. 2016. Three-dimensional ordered mesoporous MnO2-supported Ag nanoparticles for catalytic removal of formaldehyde[J]. Environmental Science and Technology, 50(5): 2635-2640. DOI:10.1021/acs.est.5b03342 |
| Dang X, Qin C, Huang J, et al. 2016. Adsorbed benzene/toluene oxidation using plasma driven catalysis with gas circulation: Elimination of the byproducts[J]. Journal of Industrial and Engineering Chemistry, 37: 366-371. DOI:10.1016/j.jiec.2016.03.051 |
| Ghorbani S F, Bahrami A, Alimohammadi I, et al. 2017. Chlorobenzene degeradation by non-thermal plasma combined with EG-TiO2/ZnO as a photocatalyst: Effect of photocatalyst on CO2 selectivity and byproducts reduction[J]. Journal of Hazardous Materials, 324(8): 544-553. |
| He C, Li J, Zhang X, et al. 2012. Highly active Pd-based catalysts with hierarchical pore structure for toluene oxidation: Catalyst property and reaction determining factor[J]. Chemical Engineering Journal, 180: 46-56. DOI:10.1016/j.cej.2011.10.099 |
| He F, Jiao Y, Wu L, et al. 2019. Enhancement mechanism of Sn on the catalytic performance of Cu/KIT-6 during the catalytic combustion of chlorobenzene[J]. Catalysis Science and Technology, 9(21): 6114-6123. DOI:10.1039/C9CY01169B |
| Huang Y, Dai S, Feng F, et al. 2015. A comparison study of toluene removal by two-stage DBD-catalyst systems loading with MnOx, CeMnOx, and CoMnOx[J]. Environmental Science and Pollution Research, 22(23): 19240-19250. DOI:10.1007/s11356-015-5121-3 |
| Jha A, Mhamane D, Suryawanshi A, et al. 2014. Triple nanocomposites of CoMn2O4, Co3O4 and reduced graphene oxide for oxidation of aromatic alcohols[J]. Catalysis Science and Technology, 4(6): 1771-1778. DOI:10.1039/c3cy01025b |
| Jiang L, Nie G, Zhu R, et al. 2017. Efficient degradation of chlorobenzene in a non-thermal plasma catalytic reactor supported on CeO2/HZSM-5 catalysts[J]. Journal of Environmental Sciences, 55: 266-273. DOI:10.1016/j.jes.2016.07.014 |
| Jose J, Philip L. 2019. Degradation of chlorobenzene in aqueous solution by pulsed power plasma: Mechanism and effect of operational parameters[J]. Journal of Environmental Chemical Engineering, 7(6): 103476. DOI:10.1016/j.jece.2019.103476 |
| Kan J, Deng L, Li B, et al. 2017. Performance of co-doped Mn-Ce catalysts supported on cordierite for low concentration chlorobenzene oxidation[J]. Applied Catalysis A: General, 530: 21-29. DOI:10.1016/j.apcata.2016.11.013 |
| Karatum O, Deshusses M A. 2016. A comparative study of dilute VOCs treatment in a non-thermal plasma reactor[J]. Chemical Engineering Journal, 294: 308-315. DOI:10.1016/j.cej.2016.03.002 |
| Kim H H, Ogata A. 2011. Nonthermal plasma activates catalyst: From current understanding and future prospects[J]. European Phusical Journal Applied Physics, 55(1): 532-542. |
| Kim S C, Shim W G. 2010. Catalytic combustion of VOCs over a series of manganese oxide catalysts[J]. Applied Catalysis B: Environmental, 98(3/4): 180-185. |
| Li S, Ma X, Liu L, et al. 2015. Degradation of 2, 4-dichlorophenol in wastewater by low temperature plasma coupled with TiO2 photocatalysis[J]. Royal Society of Chemistry, 5(3): 1902-1909. |
| Lin X, Li S, He H, et al. 2018. Evolution of oxygen vacancies in MnOx-CeO2 mixed oxides for soot oxidation[J]. Applied Catalysis B: Environmental, 223: 91-102. DOI:10.1016/j.apcatb.2017.06.071 |
| Lu Y, Dai Q, Wang X. 2014. Catalytic combustion of chlorobenzene on modified LaMnO3 catalysts[J]. Catalysis Communications, 54: 114-117. DOI:10.1016/j.catcom.2014.05.018 |
| Maciuca A, Batiot-Dupeyrat C, Tatibou?t J M. 2012. Synergetic effect by coupling photocatalysis with plasma for low VOCs concentration removal from air[J]. Applied Catalysis B: Environmental, 125: 432-438. DOI:10.1016/j.apcatb.2012.06.012 |
| Mei D, Zhu X, He Y L, et al. 2015. Plasma-assisted conversion of CO2 in a dielectric barrier discharge reactor: Understanding the effect of packing materials[J]. Plasma Sources Science and Technology, 24(1): 015011. |
| Pekárek S. 2011. Effect of catalysts on dc corona discharge poisoning[J]. European Physical Journal D, 61(3): 657-662. DOI:10.1140/epjd/e2010-10246-4 |
| Qian Y, Yin D, Li Y, et al. 2004. Effects of four chlorobenzenes on serum sex steroids and hepatic microsome enzyme activities in crucian carp, Carassius auratus[J]. Chemosphere, 57(2): 127-133. DOI:10.1016/j.chemosphere.2004.04.044 |
| Qu Z, Bu Y, Qin Y, et al. 2012. The effects of alkali metal on structure of manganese oxide supported on SBA-15 for application in the toluene catalytic oxidation[J]. Chemical Engineering Journal, 209: 163-169. DOI:10.1016/j.cej.2012.07.138 |
| Sivachandiran L, Thevenet F, Rousseau A. 2015. Isopropanol removal using MnXOY packed bed non-thermal plasma reactor: Comparison between continuous treatment and sequential sorption/regeneration[J]. Chemical Engineering Journal, 270: 327-335. DOI:10.1016/j.cej.2015.01.055 |
| Snoeckx R, Aerts R, Tu X, et al. 2013. Plasma-based dry reforming: A computational study ranging from the nanoseconds to seconds time scale[J]. The Journal of Physical Chemisry, 4: 4957-4970. |
| Song H, Hu F, Peng Y, et al. 2018. Non-thermal plasma catalysis for chlorobenzene removal over CoMn/TiO2 and CeMn/TiO2: Synergistic effect of chemical catalysis and dielectric constant[J]. Chemical Engineering Journal, 347: 447-454. DOI:10.1016/j.cej.2018.04.018 |
| Sultana S, Vandenbroucke A M, Leys C, et al. 2015. Abatement of VOCs with alternate adsorption and plasma-assisted regeneration: A review[J]. Catalysts, 5(2): 718-746. DOI:10.3390/catal5020718 |
| Sun P, Huang S X, Guo R, et al. 2018. The enhanced SCR performance and SO2 resistance of Mn/TiO2 catalyst by the modification with Nb: A mechanistic study[J]. Applied Surface Science, 447: 479-488. DOI:10.1016/j.apsusc.2018.03.245 |
| Thevenet F, Sivachandiran L, Guaitella O, et al. 2014. Plasma-catalyst coupling for volatile organic compound removal and indoor air treatment: A review[J]. Journal of Physics D: Applied Physics, 47(22): 224011. DOI:10.1088/0022-3727/47/22/224011 |
| Trinh Q H, Lee S B, Mok Y S. 2015. Removal of ethylene from air stream by adsorption and plasma-catalytic oxidation using silver-based bimetallic catalysts supported on zeolite[J]. Journal of Hazardous Materials, 285: 525-534. DOI:10.1016/j.jhazmat.2014.12.019 |
| Wang B, Chi C, Xu M, et al. 2017. Plasma-catalytic removal of toluene over CeO2-MnOx catalysts in an atmosphere dielectric barrier discharge[J]. Chemical Engineering Journal, 322: 679-692. DOI:10.1016/j.cej.2017.03.153 |
| Wang P, Chen S, Gao S, et al. 2018. Niobium oxide confined by ceria nanotubes as a novel SCR catalyst with excellent resistance to potassium, phosphorus, and lead[J]. Applied Catalysis B: Environmental, 231(2): 299-309. |
| Wang X, Jia X, Wen J. 2010. Transient modeling of toluene waste gas biotreatment in a gas-liquid airlift loop reactor[J]. Chemical Engineering Journal, 159(1): 1-10. |
| Xu H, Yan N, Qu Z, et al. 2017a. Gaseous heterogeneous catalytic reactions over Mn-based oxides for environmental applications: A critical review[J]. Environmental Science and Technology, 51(16): 8879-8892. DOI:10.1021/acs.est.6b06079 |
| Xu X, Wu J, Xu W, et al. 2017b. High-efficiency non-thermal plasma-catalysis of cobalt incorporated mesoporous MCM-41 for toluene removal[J]. Catalysis Today, 281: 527-533. DOI:10.1016/j.cattod.2016.03.036 |
| Yao X, Zhang J, Liang X, et al. 2019. Niobium doping enhanced catalytic performance of Mn/MCM-41 for toluene degradation in the NTP-catalysis system[J]. Chemosphere, 230: 479-487. DOI:10.1016/j.chemosphere.2019.05.075 |
| Yao X, Zhang J, Liang X, et al. 2018. Plasma-catalytic removal of toluene over the supported manganese oxides in DBD reactor: Effect of the structure of zeolites support[J]. Chemosphere, 208: 922-930. DOI:10.1016/j.chemosphere.2018.06.064 |
| Yu D, Liu Y, Wu Z. 2010. Low-temperature catalytic oxidation of toluene over mesoporous MnOx-CeO2/TiO2 prepared by sol-gel method[J]. Catalysis Communications, 11(8): 788-791. DOI:10.1016/j.catcom.2010.02.016 |
| Zhang S, You J, Kennes C, et al. 2018. Current advances of VOCs degradation by bioelectrochemical systems: A review[J]. Chemical Engineering Journal, 334: 2625-2637. DOI:10.1016/j.cej.2017.11.014 |
| Zhang R, Villanueva A, Alamdari H, et al. 2006. Reduction of NO by CO over nanoscale LaCo1-xCuxO3 and LaMn1-xCuxO3 perovskites[J]. Journal of Molecular Catalysis A Chemical, 258(1/2): 22-34. |
| Zhu R, Mao Y, Jiang L, et al. 2015. Performance of chlorobenzene removal in a nonthermal plasma catalysis reactor and evaluation of its byproducts[J]. Chemical Engineering Journal, 279: 463-471. DOI:10.1016/j.cej.2015.05.043 |
