
 , 吴豪1
, 吴豪1
 , 胡志德2, 边凤霞1
, 胡志德2, 边凤霞11. 重庆工商大学环境与资源学院, 重庆高校催化理论与应用技术市级重点实验室, 催化与环境新材料重庆市重点实验室, 重庆 400067;
2. 陆军勤务学院军事设施系, 重庆 401331
收稿日期: 2020-06-30; 修回日期: 2020-07-25; 录用日期: 2020-07-25
基金项目: 重庆市自然科学基金(No.cstc2018jcyjAX0735,cstc2019jcyj-msxmX0641);国家自然科学基金(No.21201184);重庆市教委自然科学基金(No.KJQN201900811);重庆工商大学自然科学基金(No.950119090);催化与环境新材料重庆市重点实验室项目(No.KFJJ2019082);重庆市高等学校“十三五”市级化学工程与技术重点学科资助项目
作者简介: 蒋和雁(1981-), 男, E-mail: orgjiang@163.com
通讯作者(责任作者): 蒋和雁
吴豪, E-mail: wuhbvb@163.com
摘要:以镁铁尖晶石MgFe2O4为磁核,在磁核表层包覆MgAl水滑石后经高温焙烧形成MgAl(O)复合氧化物包覆的磁性载体MgFe2O4/MgAl(O),进而负载纳米金属Pd制成磁性催化剂Pd-MgFe2O4/MgAl(O).通过X射线衍射(XRD)、X射线光电子能谱分析(XPS)、傅里叶红外光谱(FT-IR)、透射电镜(TEM)、扫描电子显微镜(SEM)、选区电子衍射(SAED)、比表面积(SBET)和振动样品磁强计(VSM)等手段对催化材料进行表征.结果表明,MgFe2O4-LDH转化为磁性MgFe2O4/MgAl(O)载体有利于催化材料比表面积的增加、结构稳定性的提升及相应催化活性位点的增加,进而有利于提升4-氯苯酚高效加氢脱氯效率.研究进一步考察了催化剂负载量、催化剂用量、底物浓度、反应温度、反应溶剂等条件对4-氯苯酚降解效率的影响.结果发现,在优化反应条件下催化反应的转换频率TOF(0.04 s-1)可媲美常温、常压、无碱性添加剂等温和条件下4-氯苯酚高效加氢脱氯反应的最佳文献报道水平.磁性催化剂Pd-MgFe2O4/MgAl(O)循环使用4次后仍保持很好的催化活性.
关键词:磁性MgFe2O4/MgAl(O)4-氯苯酚加氢脱氯纳米Pd
Magnetic Pd-MgFe2O4/MgAl(O) catalyzed highly efficient hydrodechlorination of 4-chlorophenol under mild conditions
JIANG Heyan1

 , WU Hao1
, WU Hao1
 , HU Zhide2, BIAN Fengxia1
, HU Zhide2, BIAN Fengxia11. Key Laboratory of Catalysis Science and Technology of Chongqing Education Commission, Chongqing Key Laboratory of Catalysis and New Environmental Materials, College of Environmental and Resources, Chongqing Technology and Business University, Chongqing 400067;
2. Department of Military Facilities, Army Logistics University of PLA, Chongqing 401331
Received 30 June 2020; received in revised from 25 July 2020; accepted 25 July 2020
Abstract: The MgFe2O4 was used as the magnetic core, which was coated with MgAl hydrotalcite.After high-temperature calcination, MgAl(O) compound oxide based magnetic carrier MgFe2O4/MgAl(O) was formed.Magnetic catalyst Pd-MgFe2O4/MgAl(O) was prepared by nano-metal Pd loading.The material were characterized by X-ray diffraction(XRD), X-ray photoelectron spectroscopy (XPS), fourier infrared spectroscopy(FT-IR), transmission electron microscopy(TEM), scanning electron microscopy(SEM), selected area electron diffraction(SAED), brunauer emmett teller method(SBET) and vibrating sample magnetometer(VSM) measurement.The study showed that the specific surface area, the structural stability and the corresponding catalytic active site of the catalytic material was enhanced by the transformation of MgFe2O4-LDH into the magnetic MgFe2O4/MgAl(O) carrier, which was beneficial to improve the efficiency of the hydrodechlorination of 4-chlorophenol.The removal efficiency of 4-chlorophenol was investigated under different conditions of catalyst loading, catalyst concentration, substrate concentration, reaction temperature as well as solvent.In comparison with literature, the TOF (0.04 s-1) of the catalytic 4-chlorophenol hydrodechlorination reaction under optimal reaction conditions approach one of the best efficiency under mild conditions such as room temperature, ambient pressure and no base additive.The catalytic efficiency of the magnetic catalyst Pd-MgFe2O4/MgAl(O) was well maintained after 4 recycle times.
Keywords: magnetisumMgFe2O4/MgAl(O)4-chlorophenolhydrodechlorinationPd nanoparticle
1 引言(Introduction)氯酚类化合物(Chlorophenols, CPs)是一类具有持久性毒性的有机化合物, 在被人们广泛应用于橡胶、染料、杀虫剂、木材防腐剂、塑料、药品和化妆品等行业的化工原料和中间体的同时, 也从各种工业污染源排入自然环境中, 不断威胁着人类的健康和自然环境(秦洪伟等, 2017).研究表明, CPs的毒性极高, 且对人和动物具有强烈的致畸、致癌、致突变效应(Deng et al., 2014).这类化合物较为稳定, 可以在自然环境中长距离、持久性迁移, 因而其在全球范围内分布极为广泛(Wu et al., 2018).中国生态环境部(周文敏等, 1991)和美国环保局(U.S.EPA)已将氯酚类化合物列入优先控制的毒性污染物名单, 而且在自然环境下有可能转化为毒性更大的化学物质(Kwean et al., 2018), 因此, 研究如何消除环境中的氯酚类化合物具有重要意义.
目前, 较为常见和传统的氯酚类化合物处理方法包括: 生物降解法(Domenica et al., 2017;Concetta et al., 2017)、光催化法(Sripriya et al., 2018;Tomasz et al., 2019)、电化学氧化法(Zhu et al., 2013)、生物膜法(Zhang et al., 2017;Zhao et al., 2018)和催化加氢脱氯法(Lan et al., 2019;Corina et al., 2020).其中, 催化加氢脱氯法(Hydrodechlorination, HDC)是利用催化剂吸附活化氯酚类有机物, 并加入还原剂使其转化为危害性小、易被生物降解的有机物的方法(Ruiz-Garcia et al., 2020).催化加氢脱氯法具有许多优势, 如反应高效(Huang et al., 2016)、反应条件温和(Xia et al., 2004)、绿色清洁等, 可以在不破坏苯环的基础上温和地将氯原子移除, 而且降解后的产物还可重新用于工业生产.这不仅对环境保护具有很重要的价值, 而且在有机合成领域也体现出巨大的发展前景, 因此, 近年来国内外****对催化加氢脱氯法进行了深入而广泛的研究.传统的催化加氢脱氯法在反应过程中通常还需添加碱性物质(Li et al., 2015), 且在常温、常压、无碱性添加剂催化加氢脱氯体系中氯酚类化合物的转换频率(Turnover Frequency, TOF)仍有待提高(Xu et al., 2019), 如何避免传统催化体系中碱添加剂的使用及进一步提高催化效率仍是后续研究努力的方向.传统的催化加氢脱氯法中常用的催化活性组分有Ni(Bharati et al., 2017)、Pd(Jiang et al., 2016)、Rh(Ming et al., 2017)、Pt(Li et al., 2015)等, 相比之下, Ni催化剂的反应条件较为苛刻且不耐腐蚀, Pd的催化活性较好.
层状双氢氧化物(Layered Double Hydroxide, LDH)是一系列二维层状化合物, 由带正电的水镁石层、层间阴离子和水分子组成(Zhang et al., 2020).作为水滑石最常见的代表, MgAl水滑石自身具有碱性, 高温焙烧后会形成比表面积增大、结构更加稳定且保持一定碱性的MgAl(O)复合氧化物(Li et al., 2015), 故MgAl(O)复合氧化物成为多相催化反应体系的理想载体.
本研究以MgFe2O4作为便于催化剂分离回收的磁核, 磁核表层包覆MgAl水滑石并高温焙烧后形成具有大比表面积且稳定的磁性载体MgFe2O4/MgAl(O), 进一步负载纳米金属Pd后制得用于4-氯苯酚加氢脱氯催化研究的磁性催化剂.在常压、无碱添加剂等温和条件下, 深入考察催化剂负载量、催化剂用量、底物浓度、反应温度、反应溶剂等反应条件对4-氯苯酚降解效率的影响.
2 材料与方法(Materials and methods)2.1 催化剂的制备磁核MgFe2O4的制备: 取1.997 g(0.01 mol) FeCl2·4H2O、2.702 g(0.01 mol) FeCl3·6H2O、5.125 g(0.02 mol) Mg(NO3)2·6H2O, 使Fe2+、Fe3+、Mg2+三者的物质的量之比为1∶1∶2, 溶于100 mL水中, 制成混合盐溶液A1;取7.420 g(0.07 mol) Na2CO3和6.000 g(0.15 mol) NaOH, 溶于100 mL水中, 制成混合碱溶液B1;将混合碱溶液B1快速滴入混合盐溶液A1中至酸碱度为11, 在40 ℃水浴条件下晶化10 h;然后对混合液进行抽滤, 依次用水和无水乙醇洗涤, 放入真空干燥箱中干燥24 h后取出, 将其研磨成粉末, 再于马弗炉中焙烧8 h, 焙烧温度为800 ℃, 制得磁核MgFe2O4.
磁性载体的制备: 取0.963 g(0.003 mol) Al(NO3)3·9H2O、2.304 g(0.009 mol) Mg(NO3)2·6H2O、0.518 g MgFe2O4, 使Mg2+与MgFe2O4物质的量之比为2.4, 溶于100 mL水中, 制成混合盐溶液A2;取0.400 g (0.01 mol) NaOH和2.120 g (0.02 mol) Na2CO3溶于100 mL水中, 制成混合碱溶液B2;将混合盐溶液A2和混合碱溶液B2迅速混合后剧烈搅拌2 min, 在100 ℃油浴条件下晶化6 h;然后对混合液进行抽滤, 依次用水和无水乙醇洗涤, 放入真空干燥箱中干燥24 h后取出, 将其研磨成粉末, 制得磁性水滑石MgFe2O4/MgAl-LDH, 再于马弗炉中焙烧6 h, 焙烧温度为500 ℃, 制得磁性载体MgFe2O4/MgAl(O).
磁性催化剂的制备: 取一定量的PdCl2和磁性载体MgFe2O4/MgAl(O)使得金属Pd的质量比为3%, 溶于少量蒸馏水中, 并放置于高压反应釜中, 在30 ℃、1 MPa H2的条件下反应1 h;依次用水和无水乙醇洗涤反应液后离心, 放入真空干燥箱中干燥24 h后取出, 将其研磨成粉末, 制得磁性催化剂Pd-MgFe2O4/MgAl(O).
2.2 实验方法与表征磁性催化剂Pd-MgFe2O4/MgAl(O)对4-氯苯酚的加氢脱氯实验在100 mL的玻璃具塞支试管中进行.试管口用橡胶塞封闭, 侧面连接三通玻璃接头, 接口上方和气球连通.用真空泵将反应装置中的空气抽尽, 再通入高纯氮气, 反复循环抽真空、充氮气3次以上, 再向实验装置中充入高纯氢气.然后向试管中加入10 mL配置好的4-氯苯酚溶液.将恒温水浴锅加热至30 ℃后, 再将实验装置固定于恒温水浴锅中, 开始搅拌, 记录反应时间.每隔一段时间从反应装置中抽取少量反应溶液, 萃取后取上清液用于气相色谱分析.ICP-OES分析表明, 复合催化剂在反应过程中没有金属离子的溶出和释放.
分别采用X-射线衍射仪(XRD)、X射线光电子能谱分析仪(XPS)、傅里叶红外光谱仪(FT-IR)、透射电子显微镜(TEM)、扫描电子显微镜(SEM)、选区电子衍射仪(SAED)、比表面积(SBET)和振动样品磁强计(VSM)等对催化材料的结构、形貌和性质进行表征分析研究.
3 结果与分析(Results and analysis)3.1 催化剂表征对磁核MgFe2O4、磁性水滑石MgFe2O4-LDH、磁性载体MgFe2O4/MgAl(O)、磁性催化剂Pd-MgFe2O4-LDH、Pd-MgFe2O4/MgAl(O)样品进行XRD表征, 结果如图 1A所示.磁核MgFe2O4(图 1A-a)的特征衍射峰明显, 在2θ=30.3°、35.4°、42.8°、55.1°、56.8°、60.7°、62.7°等位置均有较明显的特征峰, 分别与(220)、(311)、(400)、(422)、(511)、(440)、(531)晶面相对应, 这与磁核MgFe2O4晶体的标准卡片(JCPDS 17-0406)一致, 表明成功制备了磁核MgFe2O4, 并且磁核MgFe2O4样品具有较高的纯度和结晶度.磁性水滑石MgFe2O4-LDH(图 1A-b)在2θ=11°、23°、35°、61°和63.5°处出现了水滑石所特有的(003)、(006)、(009)、(110)和(113)等晶面的特征衍射峰(Liu et al., 2013), 表明材料具有理想的层状结构, 符合水滑石的结构特征.经过500 ℃高温焙烧, 磁性载体MgFe2O4/MgAl(O)的谱图见图 1A-c, 可以看出水滑石的特征衍射峰基本消失, 在2θ=42.8°、62.7°附近出现的衍射峰对应于MgO的(200)、(220)晶面, 与磁核MgFe2O4的(400)、(531)晶面的特征衍射峰发生叠加, 表明焙烧后的磁性载体中的磁核与MgAl(O)复合氧化物共同存在.对比谱图 1A-d和1A-e, 可以看出谱图 1A-d在2θ=40°附近出现金属Pd的(111)晶面, 而谱图 1A-e中并没有在相应位置出现明显的特征衍射峰, 这表明金属Pd在磁性载体MgFe2O4/MgAl(O)中的分布比在磁性水滑石MgFe2O4-LDH中更均匀.磁性载体MgFe2O4/MgAl(O)更有利于活性金属Pd的分散, 相比磁性水滑石MgFe2O4-LDH具有更好的结构优势.
图 1(Fig. 1)
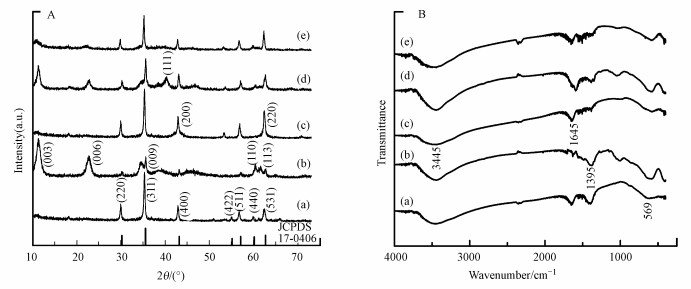 |
| 图 1 MgFe2O4(a)、MgFe2O4-LDH(b)、MgFe2O4/MgAl(O)(c)、Pd-MgFe2O4-LDH(d)和Pd-MgFe2O4/MgAl(O)(e)的XRD(A)及FT-IR谱图(B) Fig. 1XRD(A) and FT-IR(B) spectra of MgFe2O4(a), MgFe2O4-LDH(b), MgFe2O4/MgAl(O)(c), Pd-MgFe2O4-LDH(d) and Pd-MgFe2O4/MgAl(O)(e) |
磁核MgFe2O4、磁性水滑石MgFe2O4-LDH、磁性载体MgFe2O4/MgAl(O)、磁性催化剂Pd-MgFe2O4-LDH、Pd-MgFe2O4/MgAl(O)的FT-IR谱图如图 1B所示.谱图中3445 cm-1和1645 cm-1附近各有一宽的吸收峰, 分别是由缔合羟基的伸缩振动v-OH和弯曲振动δ-OH引起的, 在100~500 cm-1范围内出现了水滑石的骨架M—O振动特征吸收峰(Sotoudeh et al., 2019);图 1B-b、1B-d中1395 cm-1处的吸收峰代表的是样品中含有碳酸根离子, 进一步证明所制得的催化材料是水滑石类物质(Dos Santos et al., 2013), 569 cm-1处出现的很强的吸收峰属于MgFe2O4中Mg—O和Fe—O的伸缩振动(Davood et al., 2015).综上表明, 磁核MgFe2O4与MgAl(O)复合氧化物表面形成了很好的复合, 且图 1B-e中并没有出现明显的金属Pd的特征吸收峰, 这表明金属Pd在磁性载体MgFe2O4/MgAl(O)中分散均匀.
利用扫描电子显微镜(SEM)对磁核MgFe2O4、磁性载体MgFe2O4/MgAl(O)和磁性催化剂Pd-MgFe2O4/MgAl(O)进行表征分析.从图 2a中可以清晰地看出, 磁核MgFe2O4呈圆球状, 颗粒大小较为均一.从图 2b可以看出, MgAl(O)复合氧化物已成功包覆磁核MgFe2O4微粒, 高温焙烧后的磁性载体MgFe2O4/MgAl(O)依然保留了类似于水滑石的层状结构, 且形成更加稳定的包覆结构(Lefèvre et al., 2019).图 2c中金属Pd负载于磁性载体MgFe2O4/MgAl(O)后其形貌结构相比于图 2b没有发生明显改变, 这表明金属Pd的负载对载体结构没有明显影响.
图 2(Fig. 2)
 |
| 图 2 MgFe2O4(a)、MgFe2O4/MgAl(O)(b)、Pd-MgFe2O4/MgAl(O)(c)的SEM图和Pd-MgFe2O4/MgAl(O)的TEM图(d)、HRTEM图(e)和SAED图(f) Fig. 2SEM images of MgFe2O4(a), MgFe2O4/MgAl(O)(b), Pd-MgFe2O4/MgAl(O)(c) and TEM image(d), HRTEMimage(e) and SAED pattern(f) of Pd-MgFe2O4/MgAl(O) |
图 2d为Pd-MgFe2O4/MgAl(O)的TEM图, 图中黑色颗粒为磁核MgFe2O4, 且MgAl(O)复合氧化物成功包覆磁核MgFe2O4, 这与SEM图中观察到的现象一致.此外, 在图 2e中时常可以清晰地看到间距为0.23 nm的晶格条纹, 对应于金属Pd的(111)晶面(Hong et al., 2007);周围出现间距为0.241 nm的晶格条纹, 对应于MgAl(O)复合氧化物中MgO的(220)晶面(Aravind et al., 2017).以上结果表明, 金属Pd成功负载于磁性载体MgFe2O4/MgAl(O)上, 形成了稳定的催化剂结构.图 2f的SAED图谱显示同心圆是由方向不同的小颗粒组成, 说明Pd-MgFe2O4/MgAl(O)是多晶结构, 相应的环对应于金属Pd的(111)晶面(Maurizio et al., 2014)、MgO的(220)晶面(Aravind et al., 2017)和MgFe2O4的(311)晶面(Timm et al., 2019).
为进一步研究加氢脱氯效果最佳的催化剂中, 活性金属Pd与磁核、磁性载体的相互作用关系, 采用XPS表征了3%Pd-MgFe2O4/MgAl(O)催化剂中主要元素的价态.XPS全扫描结果如图 3a所示, 可以看出催化剂中含有Pd、Mg、Fe、Al、O、C等6种元素, 表明金属Pd已成功负载于磁性载体MgFe2O4/MgAl(O)上.但Fe 2p的谱峰相对较弱, 表明磁核相MgFe2O4大部分处于催化材料内部, 焙烧后形成的MgAl(O)复合氧化物则是处于催化材料表面, 形成了较好的包覆结构.
图 3(Fig. 3)
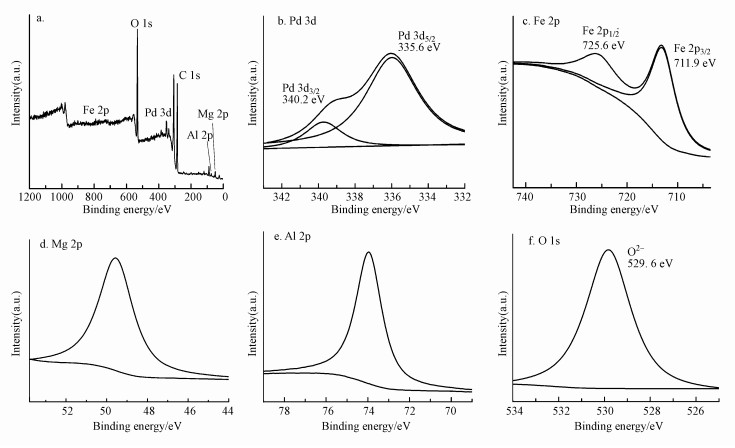 |
| 图 3 3%Pd-MgFe2O4/MgAl(O)的XPS谱图 (a.总谱, b.Pd 3d, c.Fe 2p, d.Mg 2p, e.Al 2p, f.O 1s) Fig. 3XPS pattern of 3%Pd-MgFe2O4/MgAl(O) (a.survey spectra, b.Pd 3d, c.Fe 2p, d.Mg 2p, e.Al 2p, f.O 1s) |
Pd 3d轨道的XPS谱图如图 3b所示, 结合能为335.6 eV和340.2 eV处分别归属于金属Pd(0)的Pd 3d5/2和Pd 3d3/2(Yu et al., 2020), 表明成功负载于磁性载体上的金属Pd被充分还原.Fe 2p轨道的XPS谱图如图 3c所示, 在MgFe2O4结构特征的711.9 eV和725.6 eV处, Fe 2p轨道的XPS谱图出现两个峰, 分别对应于Fe 2p3/2和Fe 2p1/2(Sun et al., 2020).图 3d和3e分别为Mg 2p和Al 2p的XPS谱图, 结合能为49.5 eV和74.0 eV分别归属于MgAl(O)复合氧化物中的Mg和Al元素(Hernandez-Moreno et al., 1985;Chao et al., 2018).对比文献(Andreeva et al., 2018), 从O 1s轨道的XPS分峰图(图 3f)可以看出, 结合能为529.6 eV对应的是磁性催化剂表面的O2-.
对MgFe2O4、MgFe2O4-LDH、MgFe2O4/MgAl(O)和Pd-MgFe2O4/MgAl(O)进行比表面积分析(表 1), 磁核MgFe2O4颗粒的比表面积(SBET)为3.73 m2·g-1, 经过高温焙烧后的磁性载体MgFe2O4/MgAl(O)(SBET=76.28m2·g-1)相较于MgFe2O4/MgAl-LDH(SBET=54.24 m2·g-1)比表面积提高了近40%;此外, MgFe2O4/MgAl(O)相较于MgFe2O4/MgAl-LDH孔容(VP)也呈现出较大幅度的提高, 这可能归因于在焙烧过程中, 水滑石中的碳酸根分解为二氧化碳排出, 使催化材料中的小孔转变为大孔, 比表面积和孔容均有一定程度的提高(陈银飞等, 2001).这种现象会增强结构的稳定性, 增加相应的催化活性位点(Sotoudeh et al., 2019), 有利于Pd的负载.负载金属Pd后形成的催化剂Pd-MgFe2O4/MgAl(O), 其比表面积与磁性载体MgFe2O4/MgAl(O)的比表面积相比略有增加, 而孔容则出现一定程度的降低, 这可能是因为金属Pd负载到材料的内部, 但没有堵塞磁性载体的孔隙结构.
表 1(Table 1)
| 表 1 各种催化材料的比表面积和孔容 Table 1 Specific surface area and pore volume of various kinds of catalytic materials | |||||||||||||||
表 1 各种催化材料的比表面积和孔容 Table 1 Specific surface area and pore volume of various kinds of catalytic materials
| |||||||||||||||
图 4为磁核MgFe2O4、磁性载体MgFe2O4/MgAl(O)和磁性催化剂Pd-MgFe2O4/MgAl(O)的磁滞回线图.从图 4中可以看出, 磁核MgFe2O4的比饱和磁化强度较高, 为12.6 emu·g-1, 这可能是因为磁核发生聚集所致;磁性载体和磁性催化剂的比饱和磁化强度均为8.0 emu·g-1, 说明没有磁性的MgAl(O)复合氧化物包裹磁核后, 减弱了复合物的磁性, 但金属Pd的负载并没有影响催化剂载体原有的磁性.此外, 从图 4中还可以看出, 3条磁滞回线对应的磁矫顽力几乎可以忽略, 这表明磁核、磁性载体和磁性催化剂都具备超顺磁特性(Habiby et al., 2020), 因此, 在外界磁场的作用下, 催化剂更容易发生定向移动, 从反应体系中分离, 便于循环利用.
图 4(Fig. 4)
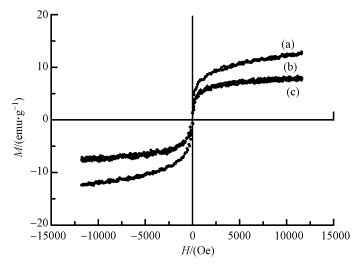 |
| 图 4 MgFe2O4(a)、MgFe2O4/MgAl(O)(b)和Pd-MgFe2O4/MgAl(O)(c)的磁滞回线 Fig. 4Magnetic hysteresis curves of MgFe2O4(a), MgFe2O4/MgAl(O)(b) and Pd-MgFe2O4/MgAl(O)(c) |
3.2 加氢脱氯实验为了考察不同催化材料对4-氯苯酚的催化加氢脱氯效果, 选取多种材料进行实验, 结果如表 2所示.从表 2可以看出, 磁核MgFe2O4、磁性水滑石MgFe2O4-LDH和磁性载体MgFe2O4/MgAl(O)作为催化剂时, 4-氯苯酚的转化率几乎为0.当X(X=Ru、Rh、Pd)-MgFe2O4/MgAl(O)作为催化剂时, 4-氯苯酚均有转化, 表明金属Ru、Rh、Pd是起到催化作用的活性组分, 其中, Pd-MgFe2O4/MgAl(O)的催化效果最佳, 反应40 min后4-氯苯酚就可完全转化.而当金属Pd负载于磁性水滑石MgFe2O4-LDH时, 其催化效果不及Pd-MgFe2O4/MgAl(O), 这可能是因为焙烧后的MgFe2O4-LDH转化为具有更大比表面积、结构更加稳定的磁性MgFe2O4/MgAl(O)载体, 更有利于金属Pd的负载.
表 2(Table 2)
| 表 2 不同催化剂对4-氯苯酚的加氢脱氯影响 Table 2 Hydrodechlorination of 4-chlorophenol catalyzed by different catalysts | ||||||||||||||||||||||||||||||||||||
表 2 不同催化剂对4-氯苯酚的加氢脱氯影响 Table 2 Hydrodechlorination of 4-chlorophenol catalyzed by different catalysts
| ||||||||||||||||||||||||||||||||||||
3.2.1 金属Pd负载量的影响催化剂中活性金属Pd的负载量对催化反应速率有较大的影响(杨慧等, 2018).不同负载量的金属Pd对4-氯苯酚催化加氢脱氯反应的影响见图 5a, 在相同的实验条件下(催化剂用量为1.0 g·L-1, 4-氯苯酚初始浓度为2.0 g·L-1, 反应温度为30 ℃, 氢气压力为常压), 随着金属Pd负载量的增加, 4-氯苯酚的转化率也逐渐增大.当金属Pd的负载量为3%和5%时, 4-氯苯酚完全转化所用的时间分别为40 min和30 min, 但当金属的负载量为1%时, 60 min内4-氯苯酚的转化率只有68%.这可能是因此随着Pd负载量的增大, 可催化4-氯苯酚的金属Pd纳米颗粒不断增多, 进而提高了4-氯苯酚的转化率.但当Pd的负载量超出一定范围时, 金属Pd纳米粒子容易聚集长大, 造成反应活性位的增幅减少, 因此, 4-氯苯酚转化率的增加幅度下降.
图 5(Fig. 5)
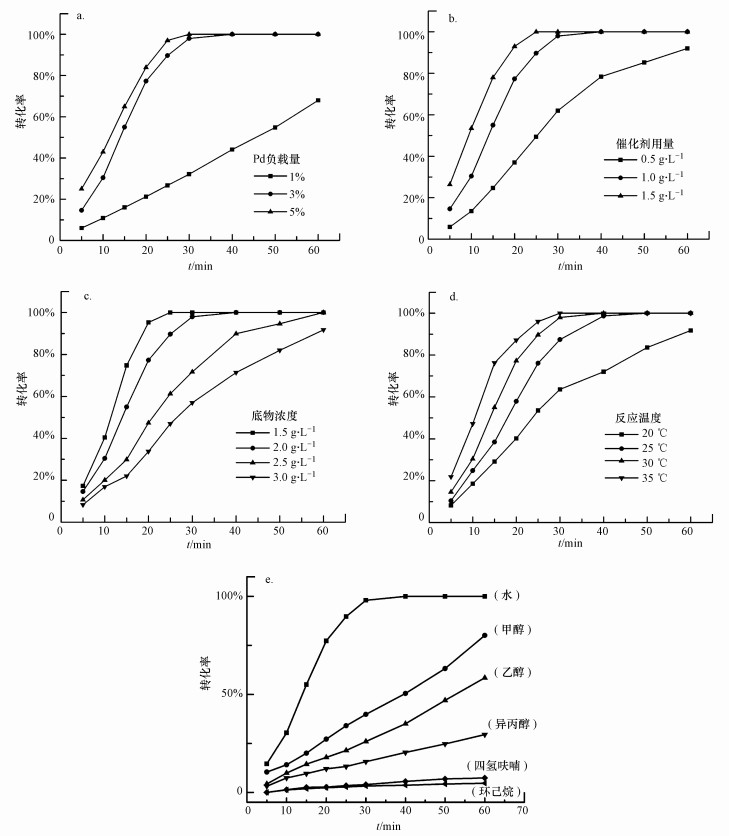 |
| 图 5 Pd负载量(a)、催化剂用量(b)、底物浓度(c)、反应温度(d)及反应溶剂(e)对4-氯苯酚加氢脱氯的影响 Fig. 5Effect of Pd loading(a), catalyst concentration(b), 4-CP concentration(c), reaction temperature(d) and solvents(e) on the hydrodechlorination of 4-CP |
3.2.2 催化剂用量的影响催化加氢脱氯反应中, 催化剂用量是影响催化反应的重要因素之一, 对转化率的高低有很大的影响(Peng et al., 2018).催化剂用量对4-氯苯酚加氢脱氯反应的影响如图 5b所示, 在相同的实验条件下(金属Pd的负载量为3%, 4-氯苯酚初始浓度为2.0 g·L-1, 反应温度为30 ℃, 氢气压力为常压), 随着催化剂投加量的增加, 4-氯苯酚的转化率逐渐增加, 反应速率也逐渐加快.当催化剂投加量从0.5 g·L-1增加到1.0 g·L-1时, 4-氯苯酚加氢脱氯反应的转化率和反应速率有了较大的提升.当催化剂投加量为0.5 g·L-1时, 4-氯苯酚反应60 min仍未完全转化;当提高催化剂的投加量到1.0 g·L-1时, 4-氯苯酚在40 min内就可完全转化, 转化率显著提高, 说明增加催化剂投加量会为反应提供更多的表面反应位.但当继续增加催化剂用量为1.5 g·L-1时, 4-氯苯酚的转化率持续增加, 但增加的幅度并不是很明显.
3.2.3 底物浓度的影响底物4-氯苯酚的浓度对催化加氢脱氯反应速率有很大影响(Divya et al., 2018).如图 5c所示, 在相同的实验条件下(催化剂用量为1.0 g·L-1, 金属Pd负载量为3%, 反应温度为30 ℃, 氢气压力为常压), 4-氯苯酚初始浓度分别为1.5、2.0、2.5、3.0 g·L-1, 相同时间内, 随着底物浓度的增加, 4-氯苯酚的转化率有所下降, 底物浓度从2.0 g·L-1增加到2.5 g·L-1时, 4-氯苯酚的转化率下降幅度最大.当反应时间为25 min时, 底物浓度从1.5 g·L-1逐步增加到3.0 g·L-1, 每次增加幅度为0.5 g·L-1, 相对应的4-氯苯酚转化率依次下降.出现这种现象的原因可能是定量的催化剂活性位点不足以催化逐步增加的4-氯苯酚, 这就会造成部分4-氯苯酚不能及时参加反应, 最终表现为4-氯苯酚转化率的下降.
3.2.4 反应温度的影响及反应动力学反应温度不仅会影响反应速率, 而且对催化反应历程有较大的影响, 在化工生产中温度的控制显得极为重要(Hannah et al., 2018).由图 5d可以看出, 催化剂用量为1.0 g·L-1, 金属Pd负载量为3%, 4-氯苯酚初始浓度为2.0 g·L-1, 分别在20、25、30、35 ℃的条件下反应, 4-氯苯酚的转化率随着反应温度的升高逐渐增加.
根据文献报道(Lien et al., 2007), 4-氯苯酚的加氢脱氯反应为一级反应.按一级反应Arrhenius公式(式(1))对实验数据进行拟合, 求得不同温度对应的反应速率常数.当温度为20、25、30、35 ℃时, 对应的速率常数分别为0.1388、0.213、0.3023和0.5948 min-1.可以看出随着温度的升高, 反应速率常数逐渐变大.
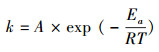 | (1) |
以lnk对1/T作图, 如图 6a所示, 可决系数大于0.99, 其斜率为-7365.7, 故反应的活化能Ea为61.24 kJ·mol-1, 与文献(Vondrackova et al., 2015;Ding et al., 2018)中所报道的数据几乎一致.
图 6(Fig. 6)
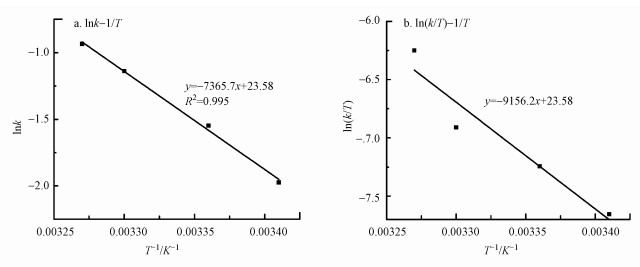 |
| 图 6 293~308 K温度下拟合的lnk-1/T(a)图和ln(k/T)-1/T(b)图 Fig. 6The plots of lnk vs 1/T(a) and ln(k/T) vs 1/T(b) at the temperature from 293 K to 308 K |
反应的焓变ΔH和熵变ΔS对化学反应的方向都有着重要影响, 可以根据Eyring公式(式(2))进行计算.
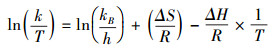 | (2) |
以ln(k/T)对1/T作图, 如图 6b所示, 其斜率为-(ΔH/R)=-9156.2, 截距为ln(kB/h)+(ΔS/R)=23.5, 由此可以求出ΔH=76.13 kJ·mol-1, ΔS=-2.16 J·mol-1·K-1.
3.2.5 反应溶剂的影响反应溶剂不仅会影响催化剂的催化性能, 而且对反应物的选择性也有一定的影响(Gómez-Quero et al., 2010).由图 5e可见, 在相同的反应条件下, 选取水、甲醇、乙醇、异丙醇、四氢呋喃和环己烷等几种常见溶剂作为4-氯苯酚加氢脱氯反应的溶剂, 考察不同反应溶剂对4-氯苯酚加氢脱氯反应的影响.当质子性溶剂甲醇、乙醇、异丙醇作为反应溶剂时, 反应速率明显下降;非质子性溶剂四氢呋喃、环已烷作为反应溶剂时, 4-氯苯酚的转化率大幅降低.而当去离子水作为反应溶剂时, 4-氯苯酚则表现出高的转化率.以上结果表明, 溶剂的极性对4-氯苯酚的加氢脱氯活性有直接影响.
3.2.6 Pd-MgFe2O4/MgAl(O)对不同底物的加氢脱氯进一步研究催化剂的催化性能, 考察了催化剂Pd-MgFe2O4/MgAl(O)对不同底物的加氢脱氯的性能, TOF的计算公式见式(3).
 | (3) |
计算出各反应底物加氢脱氯的TOF值, 结果如表 3所示.由表 3可知, 催化剂不仅在单氯酚(4-氯苯酚、3-氯苯酚、2-氯苯酚)的加氢脱氯反应中催化性能优异, 且在二氯酚(2, 4-二氯苯酚、2, 6-二氯苯酚)及三氯酚(2, 4, 6-三氯苯酚)的加氢脱氯中也显示出了良好的催化活性.由于氯取代基的电子效应和位阻效应(Qasim et al., 2020), 氯酚完全反应所需的时间不同.单氯酚的加氢脱氯反应速率大小为: 4-氯苯酚>3-氯苯酚>2-氯苯酚, 不同数目氯取代基的氯酚加氢脱氯的反应速率大小为: 单氯酚>二氯酚>三氯酚.
表 3(Table 3)
| 表 3 催化剂对不同底物的催化加氢脱氯 Table 3 Catalytic hydrodechlorination of different substrates by Pd-MgFe2O4/MgAl(O) | ||||||||||||||||||||||||||||||||
表 3 催化剂对不同底物的催化加氢脱氯 Table 3 Catalytic hydrodechlorination of different substrates by Pd-MgFe2O4/MgAl(O)
| ||||||||||||||||||||||||||||||||
近年来, 4-氯苯酚降解的研究主要集中在光催化降解法和催化加氢脱氯法.对比相关文献(Ren et al., 2014;Jiang et al., 2016)可知, 催化加氢脱氯法(编号3、4、5、6、7)相对于光催化降解法(编号1、2)在催化效率方面具有显著优势(表 4).而在催化加氢脱氯反应中, 大部分反应仍需添加碱性添加剂(编号3、4、5), 添加碱的催化体系中4-氯苯酚的转化率相比于无碱性添加剂的反应速率更快.只有少部分催化加氢脱氯反应体系不需要添加碱性添加剂, 目前文献中报道的不需添加碱性添加剂的4-氯苯酚催化加氢脱氯反应的最快TOF值为0.04 s-1 (编号6), 本研究在未添加碱性添加剂的情况下, 实现了相当的催化效率(编号7).
表 4(Table 4)
| 表 4 相关文献中各催化剂对4-氯苯酚降解的催化活性对比 Table 4 The catalytic activity of 4-CP degradation by various catalysts were compared with related literature | ||||||||||||||||||||||||||||||||||||
表 4 相关文献中各催化剂对4-氯苯酚降解的催化活性对比 Table 4 The catalytic activity of 4-CP degradation by various catalysts were compared with related literature
| ||||||||||||||||||||||||||||||||||||
3.2.7 催化剂的循环利用在最佳实验条件下(金属Pd负载量为3%, 催化剂用量为1.0 g·L-1, 底物4-氯苯酚浓度为2.0 g·L-1, 反应温度为30 ℃, 常压, 反应溶剂为去离子水), 进行了催化剂的循环利用实验(图 7).实验结束后的催化剂经过去离子水和无水乙醇多次洗涤, 然后放置于60 ℃真空干燥箱中干燥后用于下一次的循环实验.
图 7(Fig. 7)
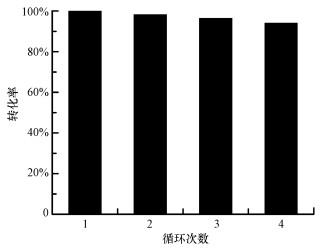 |
| 图 7 催化剂Pd-MgFe2O4/MgAl(O)的循环利用 Fig. 7Reusability of the Pd-MgFe2O4/MgAl(O) catalyst |
磁性催化剂Pd-MgFe2O4/MgAl(O)的循环实验结果如图 7所示, 催化剂循环利用4次, 其催化活性依然保持在90%以上.此外, 由于催化剂自身的磁性, 在外加磁场的作用下可以很容易地将催化剂从反应体系中分离出来.这体现了磁性催化剂Pd-MgFe2O4/MgAl(O)在循环利用方面较好的应用前景.
4 结论(Conclusions)1) 4-氯苯酚高效加氢脱氯的最佳反应条件为: 金属Pd负载量为3%, 催化剂用量为1.0 g·L-1, 底物4-氯苯酚浓度为2.0 g·L-1, 反应温度30 ℃, 常压, 反应溶剂为去离子水.
2) 磁性催化剂Pd-MgFe2O4/MgAl(O)对4-氯苯酚催化加氢脱氯反应可以在常温、常压、无碱性添加剂的条件下获得媲美常温、常压、无碱条件下4-氯苯酚高效加氢脱氯反应的最佳文献报道的TOF水平(0.04 s-1).
3) MgAl水滑石经过高温焙烧后形成MgAl(O)复合氧化物过程中比表面积的提升、结构稳定性的增强及相应的催化活性位点的增加有利于提升4-氯苯酚高效加氢脱氯效率.
4) 催化剂具有良好的磁性, 在外加磁场的作用下即可快速实现固液分离, 磁性催化剂循环利用4次, 其催化4-氯苯酚的转化率仍在90%以上, 具有良好的循环再利用效率.
致谢:本实验的表征分析工作得到重庆工商大学环境与资源学院贺有周老师的协助, 在此表示感谢.
参考文献
| Andreeva A Y, Sukhikh T S, Kozlova S G, et al. 2018. Exchange interactions and XPS O1s spectra in polynuclear lanthanide complexes with dibenzoylmethanide and 4-hydroxy-2, 1, 3-benzothiadiazole[J]. Journal of Molecular Structure, 1166: 190-194. DOI:10.1016/j.molstruc.2018.04.047 |
| Aravind L G, Takehiko S, Bhalchandra M B. 2017. Mechanistic aspects of formation of MgO nanoparticles under microwave irradiation and its catalytic application[J]. Advanced Powder Technology, 28(4): 1185-1192. DOI:10.1016/j.apt.2017.02.004 |
| Bharati D, Bhattacharyya K G. 2015. Using coal fly ash as a support for Mn(Ⅱ), Co(Ⅱ) and Ni(Ⅱ) and utilizing the materials as novel oxidation catalysts for 4-chlorophenol mineralization[J]. Journal of Environmental Management, 150: 479-488. DOI:10.1016/j.jenvman.2014.12.037 |
| Chao H P, Wang Y C, Hai N T. 2018. Removal of hexavalent chromium from groundwater by Mg/Al-layered double hydroxides using characteristics of in-situ synthesis[J]. Environmental Pollution, 8(33): 1-25. |
| Concetta T, Domenica M A, Andrew J, et al. 2017. A novel continuous two-phase partitioning bioreactor operated with polymeric tubing: Performance validation for enhanced biological removal of toxic substrates[J]. Journal of Environmental Management, 187: 265-272. |
| Corina B, Constantin C, Florica P, et al. 2020. Pd-Cu catalysts supported on anion exchange resin for the simultaneous catalytic reduction of nitrate ions and reductive dehalogenation of organochlorinated pollutants from water[J]. Applied Catalysis A, General, 570: 120-129. |
| 陈银飞, 葛忠华, 吕德伟. 2001. MgAlFe复合氧化物氧化吸附SO2的性质[J]. 环境科学学报, 21(3): 307-311. |
| Davood G, Masoud S N. 2015. Hydrothermal synthesis of different morphologies of MgFe2O4 and magnetic cellulose acetate nanocomposite[J]. Korean Journal of Chemical Engineering, 32(5): 903-910. DOI:10.1007/s11814-014-0306-x |
| Deng H Y, Fan G Y, Wang C Y, et al. 2014. Aqueous phase catalytic hydrodechlorination of 4-chlorophenol over palladium deposited on reduced graphene oxide[J]. Catalysis Communications, 46: 219-223. DOI:10.1016/j.catcom.2013.12.025 |
| Ding X F, Yao Z Q, Xu Y H, et al. 2018. Aqueous-phase hydrodechlorination of 4-chlorophenol on palladium nanocrystals: Identifying the catalytic sites and unraveling the reaction mechanism[J]. Journal of Catalysis, 368: 336-344. DOI:10.1016/j.jcat.2018.10.008 |
| Divya S N, Manju K. 2018. Chromium-zinc ferrite nanocomposites for the catalytic abatement of toxic environmental pollutants under ambient conditions[J]. Journal of Hazardous Materials, 344: 925-941. DOI:10.1016/j.jhazmat.2017.11.045 |
| Domenica M A, Valentina S, Andrew J, et al. 2017. Treatment of synthetic tannery wastewater in a continuous two-phase partitioning bioreactor: Biodegradation of the organic fraction and chromium separation[J]. Journal of Cleaner Production, 152: 321-329. DOI:10.1016/j.jclepro.2017.03.135 |
| Dos Santos R M M, Goncalves R G L, Constantino V R L, et al. 2013. Removal of acid green 68:1 from aqueous solutions by calcined and uncalcined layered double hydroxides[J]. Applied Clay Science, 81: 189-195. |
| Fan G Y, Li X J, Xu C L, et al. 2018. Palladium supported on titanium carbide: A highly efficient, durable and recyclable bifunctional catalyst for the transformation of 4-chlorophenol and 4-nitrophenol[J]. Nanomaterials, 8: 141:1-3. |
| Gómez-Quero S, Díaz E, Cárdenas-Lizana F, et al. 2010. Solvent effects in the catalytic hydrotreatment of haloaromatics over Pd/Al2O3 in water+organic mixtures[J]. Chemical Engineering Science, 65(12): 3786-3797. DOI:10.1016/j.ces.2010.03.018 |
| Habiby S R, Esmaeili H, Foroutan R. 2020. Magnetically modified MgO nanoparticles as an efficient adsorbent for phosphate ions removal from wastewater[J]. Separation Science and Technology, 55(11): 1910-1921. DOI:10.1080/01496395.2019.1617744 |
| Hannah M, Kwinten V E, Raf D. 2018. Degradation of 4-chlorophenol by microwave-enhanced advanced oxidation processes: Kinetics and influential process parameters[J]. Water, 10(3): 247. DOI:10.3390/w10030247 |
| Hong S, Rahman T S. 2007. Adsorption and diffusion of hydrogen on Pd(211) and Pd(111): Results from first-principles electronic structure calculations[J]. Physical Review B Condensed Matter, 75(15): 1418-1428. |
| Huang B B, Qian W T, Yu C X, et al. 2016. Effective catalytic hydrodechlorination of o-, p- and m-chloronitrobenzene over Ni/Fe nanoparticles: Effects of experimental parameter and molecule structure on the reduction kinetics and mechanisms[J]. Chemical Engineering Journal, 306: 607-618. DOI:10.1016/j.cej.2016.07.109 |
| Jiang W D, Xiang Z, Xu B, et al. 2016. Convenient preparation of Pd/RGO catalyst for the efficient hydrodechlorination of various chlorophenols[J]. New Journal of Chemistry, 40: 372-376. DOI:10.1039/C5NJ02349A |
| Kwean O S, Cho S Y, Yang J W, et al. 2018. 4-Chlorophenol biodegradation facilitator composed of recombinant multi-biocatalysts immobilized onto montmorillonite[J]. Bioresource Technology, 259: 268-275. DOI:10.1016/j.biortech.2018.03.066 |
| Lan L J, Liu Y, Liu S J, et al. 2019. Effect of the supports on catalytic activity of Pd catalysts for liquid-phase hydrodechlorination/hydrogenation reaction[J]. Environmental Technology, 40(12): 1615-1623. DOI:10.1080/09593330.2018.1426645 |
| Lefèvre Grégory, Julie L, Makolana Aurélie. 2019. Extraction of tungsten as polyoxometalate anion using a layered double hydroxide: Selectivity and regeneration[J]. Separation Science and Technology, 54(4): 549-558. DOI:10.1080/01496395.2018.1505911 |
| Li C, Tan P J, Li X D, et al. 2015. Effect of the addition of Ce and Zr on the structure and performances of Ni-Mo/CeZr-MgAl(O) catalysts for CH4-CO2 reforming[J]. Fuel Processing Technology, 140: 39-45. DOI:10.1016/j.fuproc.2015.08.020 |
| Li K X, Zeng Z X, Yan L S, et al. 2015. Fabrication of platinum-deposited carbon nitride nanotubes by a one-step solvothermal treatment strategy and their efficient visible-light photocatalytic activity[J]. Applied Catalysis B: Environmental, 165: 428-437. DOI:10.1016/j.apcatb.2014.10.039 |
| Lien H L, Zhang W X. 2007. Nanoscale Pd/Fe bimetallic particles: Catalytic effects of palladium on hydrodechlorination[J]. Applied Catalysis B: Environmental, 77(1/2): 110-116. |
| Liu X F, Fan B B, Gao S C, et al. 2013. Citral-acetone condensation over catalysts from C/MgAl hydrotalcite hybrids[J]. Chinese Journal of Inorganic Chemistry, 29(3): 345-349. |
| Liu Y S, Li X L, Le X D, et al. 2015. Catalysis of the hydro-dechlorination of 4-chlorophenol by Pd(0)-modified MCM-48 mesoporous microspheres with an ultra-high surface area[J]. New Journal of Chemistry, 39: 4519-4525. DOI:10.1039/C5NJ00617A |
| Hernandez-Moreno M J, Ulibarri M A, Rendon J L, et al. 1985. IR characteristics of hydrotalcite-like compounds[J]. Physics and Chemistry of Minerals, 12(1): 34-38. DOI:10.1007/BF00348744 |
| Maurizio M M, Cristina G, Patrizia C, et al. 2014. SERS and catalytically active Ag/Pd nanoparticles obtained by combining laser ablation and galvanic replacement[J]. Journal of Alloys and Compounds, 615: S352-S356. DOI:10.1016/j.jallcom.2013.12.064 |
| Ming M, Ren Y L, Hu M, et al. 2017. Promoted effect of alkalization on the catalytic performance of Rh/alk-Ti3C2X2(X=O, F) for the hydrodechlorination of chlorophenols in base-free aqueous medium[J]. Applied Catalysis B: Environmental, 210: 462-469. DOI:10.1016/j.apcatb.2017.04.017 |
| Peng W, Liu J, Li C X, et al. 2018. A multipath peroxymonosulfate activation process over supported by magnetic CuO-Fe3O4 nanoparticles for efficient degradation of 4-chlorophenol[J]. Korean Journal of Chemical Engineering, 35(8): 1662-1672. DOI:10.1007/s11814-018-0074-0 |
| Qasim M, Tan C, Chen C L. 2020. Concerted steric and electronic effects on α-diimine nickel- and palladium-catalyzed ethylene polymerization and copolymerization[J]. Science Bulletin, 65(4): 300-307. DOI:10.1016/j.scib.2019.11.019 |
| 秦洪伟, 闫彬, 尤国红, 等. 2017. 双信号细胞电化学法检测氯酚类的毒性[J]. 环境科学学报, 37(4): 1594-1600. |
| Ren Y L, Zhao Q D, Li X Y, et al. 2014. 2D Porous graphitic C3N4nanosheets/Ag3PO4nanocomposites for enhanced visible-light photocatalytic degradation of 4-chlorophenol[J]. Journal of Nanoparticle Research, 16(8): 2532. DOI:10.1007/s11051-014-2532-x |
| Ruiz-Garcia C, Heras F, Calvo L, et al. 2020. Improving the activity in hydrodechlorination of Pd/C catalysts by nitrogen doping of activated carbon supports[J]. Journal of Environmental Chemical Engineering, 8(2): 1-19. |
| Sotoudeh S H, Mansoor A. 2019. ZnO impregnated MgAl(O) catalyst with improved properties for biodiesel production: The influence of synthesis method on stability and reusability[J]. Particulate Science & Technology, 37(7): 897-903. |
| Sripriya R C, Samson A F, Anand S, et al. 2018. Comparative studies of structural, magnetic and photocatalytic degradation on 4-chlorophenol by ZnFe2O4 nanostructures prepared via cost effective combustion methods[J]. Journal of Materials Science: Materials in Electronics, 29(16): 14084-14092. DOI:10.1007/s10854-018-9540-z |
| Sun Y B, Peng D K, Li Y, et al. 2020. A robust prediction of U(Ⅵ) sorption on Fe3O4/activated carbon composites with surface complexation model[J]. Environmental Research, 185: 109467. DOI:10.1016/j.envres.2020.109467 |
| Timm J, André B, Zhang S, et al. 2019. Stabilization of nanosized MgFe2O4 nanoparticles in phenylene-bridged KIT-6-type ordered mesoporous organosilica (PMO)[J]. Microporous and Mesoporous Materials. DOI:10.1016/j.micromeso.2019.109783 |
| Tomasz ?, Kamila Z, Kamil S, et al. 2019. Photocatalytic degradation of 4-chlorophenol with the use of FTO/TiO2/SrTiO3 composite prepared by microwave-assisted hydrothermal method[J]. Applied Surface Science, 470: 991-1002. DOI:10.1016/j.apsusc.2018.11.200 |
| Vondrackova M, Hejda S, Stavarek P, et al. 2015. Combined effect of temperature and dissolved oxygen on degradation of 4-chlorophenol in photo microreactor[J]. Chemical Engineering & Processing: Process Intensification, 94: 35-38. |
| Wu Y F, Gan L, Zhang S P, et al. 2018. Carbon-nanotube-doped Pd-Ni bimetallic three-dimensional electrode for electrocatalytic hydrodechlorination of 4-chlorophenol: Enhanced activity and stability[J]. Journal of Hazardous Materials, 356: 17-25. DOI:10.1016/j.jhazmat.2018.05.034 |
| Xia C H, Xu J, Wu W D, et al. 2004. Pd/C-catalyzed hydrodehalogenation of aromatic halides in aqueous solutions at room temperature under normal pressure[J]. Catalysis Communications, 5(8): 383-386. DOI:10.1016/j.catcom.2004.04.006 |
| Xu J, Zhang S S, Liu X Y, et al. 2019. Rh/polymeric carbon nitride porous tubular catalyst: visible light enhanced chlorophenol hydrodechlorination in base-free aqueous medium[J]. Catalysis Science & Technology, 9: 6938-6945. |
| Yu Y C, Wang X, Liu C P, et al. 2020. Surface interaction between Pd and nitrogen derived from hyperbranched polyamide towards highly effective formic acid dehydrogenation[J]. Journal of Energy Chemistry, 40(1): 212-216. |
| 杨慧, 吕小凡, 陈海, 等. 2018. CeO2负载型双金属Pd/Fe催化还原四氯化碳的实验研究[J]. 环境科学学报, 38(1): 226-233. |
| Zhang C F, Fu L, Xu Z G, et al. 2017. Contrasting roles of phenol and pyrocatechol on the degradation of 4-chlorophenol in a photocatalytic-biological reactor[J]. Environmental Science and Pollution Research, 24(31): 24725-24731. DOI:10.1007/s11356-017-0245-2 |
| Zhang S S, Xu J, Cheng H M, et al. 2020. Highly efficient one-pot multi-directional selective hydrogenation and Nalkylation catalyzed by Ru/LDH under mild conditions[J]. Applied Catalysis A, General, 596: 117536. DOI:10.1016/j.apcata.2020.117536 |
| Zhao M Y, Shi J L, Zhao Z Q, et al. 2018. Enhancing chlorophenol biodegradation: Using a co-substrate strategy to resist photo-H2O2 stress in a photocatalytic-biological reactor[J]. Chemical Engineering Journal, 352: 255-261. DOI:10.1016/j.cej.2018.07.018 |
| Zhu Y Y, Wu M M, Liu S T. 2013. Self-assembly of Ag-phosphotungstic acid composite nanoparticles on a modified ITO electrode for the electrochemical detection of 4-chlorophenol[J]. Journal of Applied Electrochemistry, 43(10): 1035-1041. DOI:10.1007/s10800-013-0592-8 |
| 周文敏, 傅德黔, 孙宗光. 1991. 中国水中优先控制污染物黑名单的确定[J]. 环境科学研究, 4(6): 9-12. |
