 , 夏磊, 丁杰
, 夏磊, 丁杰

哈尔滨工业大学环境学院, 哈尔滨 150090
收稿日期: 2020-09-15; 修回日期: 2020-09-17; 录用日期: 2020-09-17
基金项目: 国家重点研发计划项目(No.2016YFC0401105)
作者简介: 钟乐(1994-), 男, 博士, E-mail:19b929047@stu.hit.edu.cn
通讯作者(责任作者): 丁杰(1972—), 女, 教授, 博士生导师, 主要研究方向为:废水生物处理及资源化综合技术. E-mail:dingjie123@hit.edu.cn
摘要:针对人工湿地对低碳氮污水处理效果差这一问题,本研究构建了电解强化潮汐流人工湿地系统,通过对比电解强化前后湿地系统脱氮除磷的效果,从微生物群落结构及污染物电化学去除机制等角度揭示电解潮汐流人工湿地强化脱氮脱磷的机制.研究结果表明:电解潮汐流人工湿地对废水中NH4+-N、TN和TP的去除率(分别为88.30%、82.10%和87.74%)均高于未强化的湿地系统.纯电解过程对氨氮的去除没有影响,但是对硝态氮具有还原作用.相比于未强化的湿地系统,电解潮汐流人工湿地阳极附近基质中含有更多的铁氧键、磷氧键、羟基聚合铁等含磷沉淀物,细菌群落结构更为丰富多样,异养反硝化细菌和基于氢气的自养反硝化细菌(Rhodoblastus)丰度都较高,从而实现氮磷的高效同步去除.
关键词:电解潮汐流人工湿地低碳氮比脱氮除磷自养异养反硝化
Efficiency and mechanism on low C/N ratio sewage treatment by electrolysis-integrated constructed wetland
ZHONG Le
 , XIA Lei, DING Jie
, XIA Lei, DING Jie

School of Environment, Harbin Institute of Technology, Harbin 150090
Received 15 September 2020; received in revised from 17 September 2020; accepted 17 September 2020
Abstract: Constructed wetlands(CWs) are less effective in treating low carbon and nitrogen sewage. In order to solve this problem,the electrolysis tidal flow CWs (ETFCW) were built to compare the effects of nitrogen and phosphorus removal efficiency,and the mechanism of nitrogen and phosphorus removal in the ETFCW was revealed from microbial community structure and electrochemical effect. The results showed that the removal efficiency of NH4+-N,TN and TP by the ETFCW was higher than that of the non- electrolysis wetland system,which is 88.30%,82.10% and 87.74%,respectively. The pure electrolysis process had no effect on the ammonia nitrogen removal,but produced a reducing effect on nitrate nitrogen. Compared with the non-electrolysis wetland system,the precipitates near the anode region of the ETFCW were rich in ferrite bonds,phosphorus-oxygen bonds,hydroxyl-polymerized iron and other structures. And the bacterial community structure was richer and more diverse in ETFCW system. Both heterotrophic denitrifying bacteria and H2-based autotrophic denitrifying bacteria (Rhodoblastus) had high abundance,therefore,the efficient simultaneous nitrogen and phosphorus removal could be achieved.
Keywords: electrolysis-integrated tidal flow constructed wetlandlow C/N rationitrogen and phosphorus removalautotrophic and heterotrophic denitrification
1 引言(Introduction)近年来, 人工湿地作为一种生态处理技术, 由于其成本低、处理性能好和便于管理, 目前已经被广泛地用来处理生活污水、污水厂尾水、城市暴雨径流以及污染的河流湖泊等(Li et al., 2018).其中潮汐流人工湿地能够形成好氧缺氧的环境, 提供更多的氧气, 同时具有较大的污染负荷、不宜堵塞等优点, 克服了传统人工湿地氧气不足限制氮去除的问题, 在污水处理领域得到了广泛的研究与应用(Wu et al., 2011).柳明慧等(2014)研究发现采取潮汐流的进水模式, 人工湿地的复氧能力达到450 g·m-2·d-1, 远高于其他种类的人工湿地.但是潮汐流人工湿地在去除硝态氮的过程中也存在有机碳源不足影响反硝化过程的问题, 尤其是低碳氮比污水, 从而导致总氮去除率下降(Zhu et al., 2014).
低碳氮比废水通过外加有机碳源可以显著提高脱氮性能, 目前外加的有机碳源主要包括液体碳源、固体碳源(陆松柳等, 2011)以及工业废水, 但是液体碳源成本比较高, 不适合大规模应用, 固体碳源释放碳源不稳定, 工业废水成分复杂, 可能会造成二次污染(陈宏来等, 2016).基质吸附是传统人工湿地除磷的主要方式, 但存在吸附饱和问题.电化学强化人工湿地处理低碳氮比污水, 无需外加碳源, 可以实现自养反硝化脱氮, 而且电化学可以有效去除污水中磷元素.Gao等(2017)构建了电解-水平潜流人工湿地系统, 研究发现该方法可以提高系统对硝态氮和总磷的去除.Ju等(2014)将电化学应用于潮汐流人工湿地, 研究了极板间距和电解时间对污染物去除性能的影响, 结果表明铁作为阳极时总磷的去除率高达98%以上, 同时可以有效控制硫化物和硝态氮的累积.王皓等(2020)采用电解强化人工湿地处理农村生活污水, 也发现该系统可以高效的去除氮磷等污染物质.
上述研究表明, 采用电解强化与潮汐流人工湿地结合处理污水, 可以实现自养反硝化脱氮的同时有效地去除污水中磷元素.然而, 电解强化潮汐流人工湿地去除污染物的机理还不是特别清晰, 尤其针对低碳氮比废水.因此, 本研究在构建电解强化潮汐流人工湿地(Electrolysis-integrated tidal flow constructed wetland, ETFCW)的基础上, 从电解对污染物去除过程以及湿地微生物群落结构等方面解析了系统处理低碳氮比污水的脱氮除磷机制.
2 材料与方法(Materials and methods)2.1 人工湿地的构建实验构建了两个人工湿地系统如图 1a所示, 分别为电解强化潮汐流人工湿地(ETFCW)和潮汐流人工湿地系统(TFCW).由有机玻璃制成, 高为70 cm, 下部基质为30 cm椰壳活性炭(2~4 mm), 上部基质为30 cm沸石(2~4 mm).填充总体积为10 L, 有效空隙容积为2 L.在活性炭区域等距铺设3个圆形电极, 铺设方式为一个阳极两个阴极, 上下两个电极为阴极, 中间电极为阳极, 电极间隔5 cm, 最下部极板距湿地底部10 cm.极板直径12 cm, 厚度3 mm, 表面设置半径为5 mm的若干圆孔.铁电极与直径2 mm的铜线连接, 连接处用防水胶密封采用直流稳压电源(汉晟普源公司型号为HSPY-36-03)供电, 中心及底部安装溶解氧仪和ORP检测仪原位测定湿地系统内部的溶解氧、ORP等参数, 湿地植物选择美人蕉(Canna indica L.).实验过程中室内温度保持在25 ℃左右.
电解小试装置见图 1b, 内径为14 cm, 内部水平等距固定3个电极, 电极种类、间距设置和电压设置与ETFCW系统完全一致.电解过程中采用磁力搅拌, 确保污染物物质混合均匀.
图 1(Fig. 1)
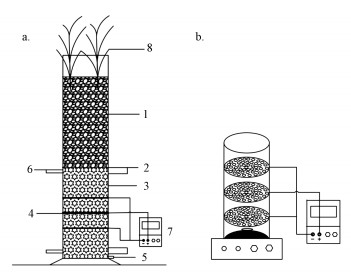 |
| 图 1 实验装置示意图(a.湿地装置, b.电解小试装置)(1.沸石, 2.ORP电极, 3.椰壳活性炭, 4.电极板, 5.出水口, 6.DO电极, 7.电源, 8.植物) Fig. 1Experiment apparatus(a. wetland system, b. electrolysis device)(1. zeolite, 2.ORP electrode, 3. coconut shell activated carbon, 4. electrode plate, 5. outlet, 6.DO electrode, 7. power, 8. plant) |
2.2 实验设计与启动人工湿地启动前接种取自哈尔滨某污水处理厂的活性污泥.进水采用实验室模拟的城市黑臭水体水质, 用生活污水和氯化铵以及磷酸二氢钾配置而成, 使进水COD、氨氮以及总磷的浓度分别为100、35、4 mg·L-1左右, 进水溶液pH约为7.水力停留时间为24 h, 水力负荷为130 L·m-2·d-1;模拟自然潮汐形式, 采用瞬时进水和排水方式, 淹没和排空的时间比为1 : 1.电解参数采用前期研究优化后的数据:电压为15 V, 电解时间为5 h, 系统进水3.5 h后开始电解.电解小试实验的废水用氯化铵或硝酸钠实验室配置而成, 浓度都约为35 mg·L-1.
2.3 样品的收集与测定水样的测试指标主要包括:COD、TP、NH4+-N、NO3--N、NO2--N、溶解氧(DO)、氧化还原电位(ORP)和pH等, 具体测试方法见表 1.利用傅里叶红外光谱仪分析阳极附近产生的沉淀, 即实验结束后取阳极区域的沉淀物, 用冷冻干燥器干燥后测定红外光谱图, 设定波峰范围为400~4000 cm-1, 分辨率为0.09 cm-1, 精度为0.01 cm-1.
表 1(Table 1)
| 表 1 水质测试方法 Table 1 Water quality testing methods | ||||||||||||||||||
表 1 水质测试方法 Table 1 Water quality testing methods
| ||||||||||||||||||
2.4 基质微生物的测定与分析采用高通量测序来表征湿地系统微生物的种群结构, 收集约250 g阴极区域的湿地基质, 加入磷酸缓冲液(PBS, K2HPO4 9.3 g·L-1, KH2PO4 1.8 g·L-1)在振荡器中振荡30 min左右, 然后用离心机离心取沉淀物, 保存于-80 ℃的冰箱.微生物的16S rDNA用V3片段的515F和907R引物来扩增, PCR扩增参考Xu等(2016)的方法, PCR结束后上机分析.测序结果通过上海美吉生物测序的云平台进行分析.
3 结果与讨论(Results and discussion)3.1 电解强化潮汐流人工湿地污染物去除效能3.1.1 COD去除效果人工湿地系统进水COD为100 mg·L-1, 出水COD见图 2a, 两个系统出水COD均呈现先增加后降低的趋势, 进水初期由于吸附作用比较强, 出水浓度比较低, 当基质达到吸附饱和后出水浓度升高, 之后随着微生物逐渐适应新的环境并开始繁殖, 微生物的降解作用增强, 出水COD又降低.两个湿地系统出水COD的趋势基本相同, 可见电解作用对COD的影响较小.两个系统出水COD最终稳定在20.3 mg·L-1左右, 去除效率为79.7%.
图 2(Fig. 2)
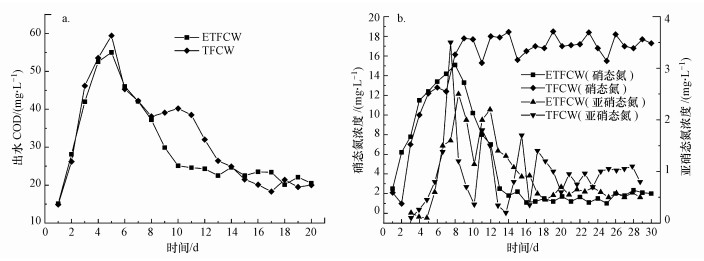 |
| 图 2 两个湿地出水COD (a)及硝态氮与亚硝态氮的累积(b) Fig. 2The effluent COD concentration(a) and accumulation of nitrate nitrogen and nitrite nitrogen(b) in CWs |
由图 2b可知, ETFCW系统和TFCW系统出水中硝态氮的浓度分别为2.03 mg·L-1和17.42 mg·L-1, 亚硝态氮浓度分别为0.58 mg·L-1和0.83 mg·L-1.湿地系统中的硝态氮和亚硝态氮是由氨氮氧化形成, 主要通过反硝化作用来去除.然而进水BOD低, 不能为异养反硝化微生物提供足够的有机碳源(Li et al., 2017), 从而致使TFCW系统硝态氮的累积量大.要实现高效的反硝化, 常常需要外加碳源, 外加碳源的多少成为关注的热点, 碳源投加过多, 不仅增加成本, 亦造成二次污染, 投加过少, 处理效果不理想.硝酸盐的电催化还原被认为是去除氮磷污染物去除的有效方法(Garcia-Segura et al., 2018), 人工湿地与电解耦合系统有利于硝酸盐的去除, ETFCW系统中硝酸盐和亚硝酸盐的累积量低于TFCW系统.原因可能是:系统下部DO在0.5 mg·L-1以下, 为反硝化细菌提供良好的生存环境(Sasikala et al., 2009).底部的ORP为-493.2 mV, 表现为强还原性(表 2), 硝态氮在阴极区域被产生的电子还原, 还原的产物可能有氮气、一氧化二氮、亚硝态氮和氨氮等(刘蕾等, 2013).此外, 阴极和阳极之间的电势差大于1.23 V, 阴极表面会析出氢气.本实验中外加电压为15 V, 大于1.23 V, 阴极表面会产生氢气, 为氢气自养反硝化细菌提供电子供体, 原位将硝态氮和亚硝态氮转化为氮气(王建超等, 2016).因此, ETFCW系统的亚硝态氮和硝态氮的累积量都低于TFCW系统.
3.1.2 脱氮效果人工湿地的进水氨氮浓度为35 mg·L-1左右, 出水氨氮浓度如图 3a所示, 呈先增大后减少的趋势.湿地系统启动的初始阶段, 氨氮出水浓度比较低, 原因可能是沸石和活性炭对氨氮的吸附性能强.但吸附达到饱和后, 出水氨氮的浓度又逐渐增加, ETFCW系统和TFCW系统的出水氨氮浓度分别达到13.86 mg·L-1和14.86 mg·L-1.随着系统的运行, 细菌在基质表面生长繁殖, 微生物脱氮的过程得到强化.而且潮汐流的运行模式使得系统的复氧能力大幅度提高, DO的增加为好氧微生物提供了生存繁殖的条件(张东晓等, 2011).进水氨氮在微生物的作用下转化为亚硝态氮和硝态氮, 最终两个系统的出水氨氮浓度维持在较低的水平, 分别为4.24 mg·L-1(ETFCW)与5.65 mg·L-1(TFCW).因此, ETFCW系统对氨氮的去除率略高于TFCW系统.
表 2(Table 2)
| 表 2 人工湿地系统进水和出水指标 Table 2 The indexes of influent and effluent in CW systems | ||||||||||||||||||||||||||||
表 2 人工湿地系统进水和出水指标 Table 2 The indexes of influent and effluent in CW systems
| ||||||||||||||||||||||||||||
两个系统出水TN的浓度随运行周期有相同的变化趋势, 在运行初期, 两个系统TN去除率没有差异.但是在运行后期, TFCW系统和ETFCW系统的出水TN浓度分别稳定在24 mg·L-1和7 mg·L-1.整个过程中, ETFCW系统对总氮的去除效率是TFCW系统的2.51倍(图 3b).
图 3(Fig. 3)
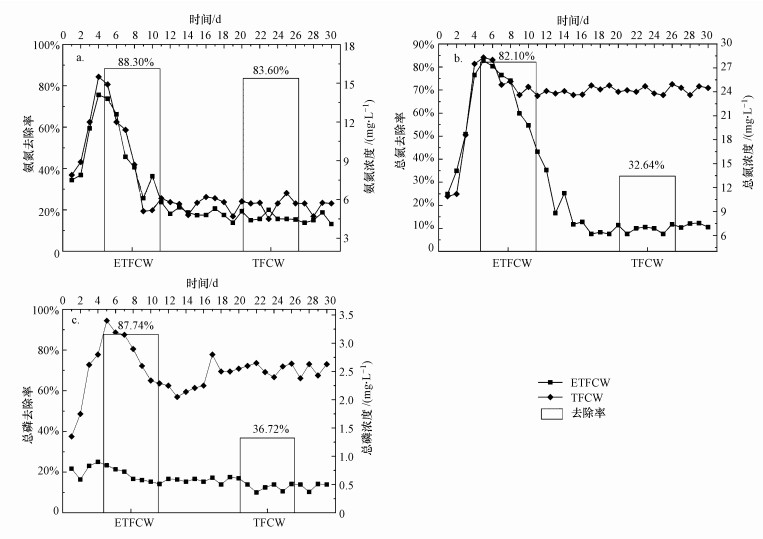 |
| 图 3 湿地出水氨氮(a)、总氮(b)及总磷(c)浓度及去除率 Fig. 3The effluent NH4+-N(a), TN(a) and TP(b) concentration and removal efficiency in CWs |
3.1.3 除磷效果实验进水总磷浓度在4 mg·L-1左右, 出水总磷浓度的变化见图 3c, TFCW系统出水总磷在初期比较低, 原因是活性炭和沸石对磷酸盐吸附性能强, 但当吸附达到饱和后, 出水TP浓度又急剧增加, 最终出水浓度稳定在2.5 mg·L-1.而ETFCW系统出水总磷的浓度变化比较小, 出水总磷浓度接近0.5 mg·L-1.ETFCW系统对总磷的去除率远高于TFCW系统, 原因是ETFCW系统中存在着电化学作用, 铁作为阳极时会产生亚铁离子和铁离子, 可以与水体中的OH-结合生成Fe(OH)2或Fe(OH)3, 实现了电絮凝作用除磷.范军辉等的研究也表明, 铁离子的存在, 有助于系统除磷的效果(范军辉等, 2016).
3.2 ETFCW系统脱氮除磷机制分析3.2.1 纯电解脱氮除磷机制为了研究纯电解对体系中污染物的去除, 考察了单独电解的作用.如图 4所示, 当进水为NH4+-N时, 体系中出现少量的NO2--N, 导致NH4+-N和TN的浓度略有降低.当进水为NO3--N时, 在电解作用下NO3--N的浓度降低, 但却出现NH4+-N的累积, 同时也发现少量的NO2--N, 出水TN的含量随着时间的延长而减少.原因是电化学产生的还原性物质, 与受体NO3--N结合, 发生还原反应, 具体过程见式(1).
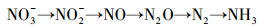 | (1) |
电化学还原NO3--N的动力学方程:
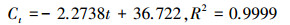 | (2) |
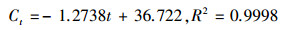 | (3) |
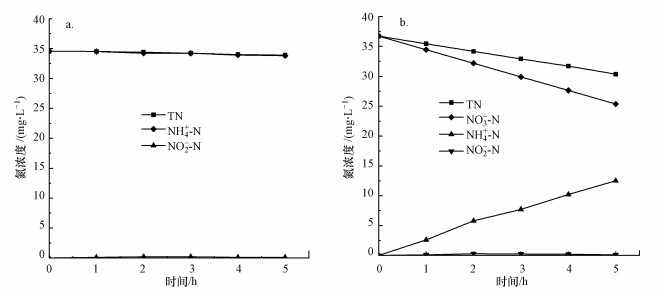 |
| 图 4 模拟电化学体系对氮的去除(a.氮源为氨氮, b.氮源为硝态氮) Fig. 4The removal of nitrogen by simulated electrochemical system (a. ammonia nitrogen as nitrogen source, b.nitrate nitrogen as nitrogen source) |
为了验证ETFCW系统中电解除磷机制, 测定了阳极区域沉淀物, 结果表明沉淀物在470~540、1030~1090、1400~1640、320~3420和3700 cm-1附近有较强的吸收峰(图 5).474 cm-1和538 cm-1的峰归属于Fe—O振动(Zhang et al., 2020), 而波长1030~1090 cm-1的尖锐吸收峰主要是磷氧键振动产生的, 证明了溶液中的磷酸盐通过沉淀作用得以去除(李安玉等, 2020).波长1400~1640 cm-1的峰由Fe—OH的振动产生, 而3412 cm-1处的峰是羟基聚合物伸缩振动形成的.ETFCW系统阳极产生Fe2+/Fe3+, 参与体系磷的转化, 可能的反应见公式(4)~(7).可见铁磷直接沉淀以及FeOOH的混凝作用是电化学体系除磷的主要方式.
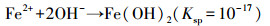 | (4) |
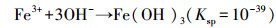 | (5) |
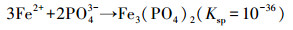 | (6) |
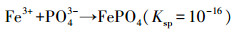 | (7) |
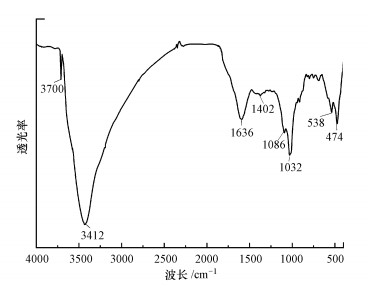 |
| 图 5 ETFCW系统阳极附近沉淀物的红外光谱 Fig. 5The infrared spectrum of precipitates near the anode in the ETFCW system |
3.2.2 微生物群落分析表 3描述了湿地系统微生物的多样性和丰富度, 量化的指标包括:Sobs、Shannon、Simpson、Ace和Chao等指数.Sobs和Shannon指数越大, 微生物多样性就越高, 而Simpson指数刚好相反.ETFCW系统的Sobs指数和Shannon指数分别为877, 4.725, 均高于TFCW系统, Simpson指数低于TFCW系统, 说明电解人工湿地系统增加了微生物的多样性.Ace和Chao指数表征微生物的丰富度, ETFCW系统的Ace指数(893.857)和Chao指数(898.022)均高于TFCW系统, 表明电解人工湿地系统也使微生物的丰富度增加.
表 3(Table 3)
| 表 3 两个湿地系统微生物多样性指数 Table 3 Microbial diversity index of two wetland systems | ||||||||||||||||||
表 3 两个湿地系统微生物多样性指数 Table 3 Microbial diversity index of two wetland systems
| ||||||||||||||||||
电解使得人工湿地系统内微生物的菌群发生明显变化(图 6).两个人工湿地系统丰度最高的菌属为Saccharibacteria, 丰度分别为22.83%(ETFCW)和32.15%(TFCW), 该菌属的微生物可以利用环境中的丁酸、氨基酸和油酸等来降解有机物(Kindaichi et al., 2016).然而, 电化学作用使得该菌属细菌的丰度降低.在电化学作用下, Nitrospira、Rhizomicrobium、Gammaproteobacteria、Rhodoblastus、Rhodanobacter、Afipia和Alcaligenaceae等细菌菌属的丰度增加, 其中, Nitrospira属于硝化细菌菌属, 可以将NO2--N氧化为NO3--N(Deng et al., 2020), 可见系统硝化过程比较强, 这也与ETFCW系统出水氨氮浓度低的结果相一致.Rhizomicrobium、Gammaproteobacteria、Rhodanobacter、Afipia和Coxiella等都是异养反硝化细菌菌属, 在好氧条件或者厌氧条件下进行反硝化脱氮过程(Zhang et al., 2011;Yao et al., 2013).Xanthomonadaceae是一种即使在碳源不足的条件下, 仍可以进行反硝化作用的兼性自养反硝化菌属(Miao et al., 2017).Rhodoblastus只在ETFCW系统中检测到, 该类细菌可以以氢气作为电子供体, 是一种厌氧的自养反硝化细菌(Imhoff et al., 2001; Wu et al., 2015), 这表明电解系统除了异养反硝化脱氮, 自养反硝化脱氮也占有很大的比例.与反硝化作用相关菌属的丰度在ETFCW系统高于TFCW系统, 这也是电解强化人工湿地系统脱氮性能强的原因.
图 6(Fig. 6)
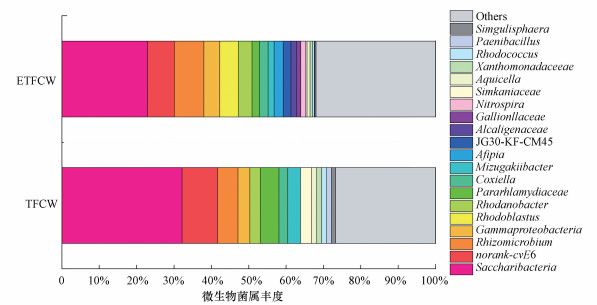 |
| 图 6 人工湿地系统基质微生物在属水平上的丰度 Fig. 6The substrate microbial richness in CW systems at the genus level |
3.2.3 ETFCW系统脱氮除磷机制潮汐流人工湿地对氮去除途径主要有微生物反应、植物吸收、基质吸附和氨挥发等物理化学以及生物过程.其中氨挥发对氮的去除作用较小, 氨挥发受pH影响, 当pH低于7.5时, 氨挥发可以不考虑(Reddy et al., 2009).本研究中出水pH小于7(表 2), 氨挥发忽略.基质吸附污染物主要是通过离子交换、物理吸附等(Yang et al., 2018), 在初期的吸附效率相对较高, 但是随着时间的推移, 达到吸附饱和后对氮去除率较低.植物对于人工湿地氮的去除具有重要的作用, 研究表明植物对于氮的去除贡献率大约为0.5%~40%, 不同植物以及生长状态下去除率存在显著性差别(Saeed et al., 2012), 本研究中植物属于幼苗, 但对氮的去除贡献较小.微生物的硝化作用和反硝化作用是湿地系统去除氮的主要途径, 本研究中, ETFCW系统对氮的去除比TFCW系统高约33.07%, 出水总氮少11 mg·L-1, 而纯电解作用对氮去除的贡献最多为6 mg·L-1.因此, ETFCW系统存在其他的脱氮途径.微生物的分析可知, 电解强化后微生物的异养反硝化过程增强.此外, 体系存在利用氢气的自养反硝化细菌, 以硝态氮作为电子受体, 实现自养反硝化脱氮.ETFCW系统对氨氮的去除率高于TFCW系统, 这源于电解强化后硝化细菌的丰度增加.此外, 阳极产生的Fe3+, 水解形成Fe(OH)3, 现有的文献发现Fe(OH)3在酸性和偏中性的厌氧环境中, 可以与NH4+发生厌氧氨氧化铁还原(Feammox), 实现氨氮的去除(Yang et al., 2012), 反应公式见式(8)~(10).本研究中出水pH为弱酸性(表 2), 同时可以满足厌氧环境.因此, 体系中也可能存在Feammox过程, 但需要进一步验证.
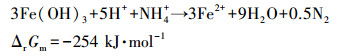 | (8) |
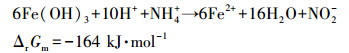 | (9) |
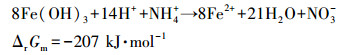 | (10) |
4 结论(Conlusions)1) ETFCW系统对低碳氮比污水中污染物去除效果明显优于TFCW系统.电化学强化极大提高了人工湿地系统对NH4+-N、TN和TP的去除率, 去除率分别为88.30%、82.10%和87.74%.
2) 电解强化使人工湿地的细菌群落发生了演替, 细菌的多样性和丰度都增加.其中, 与硝化和反硝化过程相关的细菌丰度都增加.此外, 电解系统出现以H2作为电子供体的自养反硝化细菌(Rhodoblastus), 实现自养和异养反硝化同步脱氮.
3) ETFCW系统的电解实现了对硝态氮的还原, 同时也强化了微生物的硝化和反硝化过程.电解强化除磷主要通过阳极产生的Fe2+/Fe3+与磷酸盐的直接沉淀以及Fe2+/Fe3+水解产生FeOOH的混凝沉淀作用.
参考文献
| 陈宏来. 2016. 高浓度有机工业废水补充反硝化碳源的试验研究[J]. 工业用水与废水, 47(4): 42-46. |
| Deng S, Xie B, Kong Q, et al. 2020. An oxic/anoxic-integrated and Fe/C micro-electrolysis-mediated vertical constructed wetland for decentralized low-carbon greywater treatment[J]. Bioresource Technology, 315: 123802. DOI:10.1016/j.biortech.2020.123802 |
| 范军辉, 郝瑞霞, 李萌, 等. 2016. 基于反硝化脱氮的硫铁复合填料除磷机制[J]. 环境科学, 37(11): 4275-4281. |
| Gao Y, Xie Y W, Zhang Q, et al. 2017. Intensified nitrate and phosphorus removal in an electrolysis-integrated horizontal subsurface-flow constructed wetland[J]. Water Research, 108: 39-45. DOI:10.1016/j.watres.2016.10.033 |
| Garcia-Segura S, Lanzarini-Lopes M, Hristovski K, et al. 2018. Electrocatalytic reduction of nitrate:Fundamentals to full-scale water treatment applications[J]. Applied Catalysis B-Environmental, 236: 546-568. DOI:10.1016/j.apcatb.2018.05.041 |
| Imhoff J F. 2001. Transfer of Rhodopseudomonas acidophila to the new genus Rhodoblastus as Rhodoblastus acidophilus gen.nov., comb. nov.[J]. International Journal of Systematic and Evolutionary Microbiology, 51: 1863-1866. DOI:10.1099/00207713-51-5-1863 |
| Ju X X, Wu S B, Zhang Y S, et al. 2014. Intensified nitrogen and phosphorus removal in a novel electrolysis-integrated tidal flow constructed wetland system[J]. Water Research, 59: 37-45. DOI:10.1016/j.watres.2014.04.004 |
| Kindaichi T, Yamaoka S, Uehara R, et al. 2016. Phylogenetic diversity and ecophysiology of Candidate phylum Saccharibacteria in activated sludge[J]. Fems Microbiology Ecology, 92(6). |
| Li M, Wu H, Zhang J, et al. 2017. Nitrogen removal and nitrous oxide emission in surface flow constructed wetlands for treating sewage treatment plant effluent:Effect of C/N ratios[J]. Bioresource Technology, 240: 157-164. DOI:10.1016/j.biortech.2017.02.054 |
| Li X Y, Ding A Z, Zheng L, et al. 2018. Relationship between design parameters and removal efficiency for constructed wetlands in China[J]. Ecological Engineering, 123: 135-140. DOI:10.1016/j.ecoleng.2018.08.005 |
| 李安玉, 李双莉, 余碧戈, 等. 2020. 镁浸渍生物炭吸附氨氮和磷:制备优化和吸附机理[J]. 化工学报, 71(4): 1683-1695. |
| 刘蕾, 张冬梅, 褚衍洋. 2013. 电化学法去除水中的硝酸根[J]. 环境工程学报, 7(11): 4195-4200. |
| 柳明慧, 吴树彪, 鞠鑫鑫, 等. 2014. 潮汐流人工湿地污水强化处理研究进展[J]. 水处理技术, 40(5): 10-15. |
| 陆松柳, 张辰, 王国华. 2011. 碳源强化对人工湿地反硝化过程的影响研究[J]. 环境科学学报, 31(9): 1949-1954. |
| Miao J, Zhao Y F, Wu G X. 2017. Effect of organic carbons on microbial activity and structure in denitrifying systems acclimated to nitrite as the electron acceptor[J]. International Biodeterioration & Biodegradation, 118: 66-72. |
| Reddy K R, Patrick W H, Broadbent F E. 2009. Nitrogen transformations and loss in flooded soils and sediments[J]. CRC Critical Reviews in Environmental Control, 13(4): 273-309. |
| Saeed T, Sun G Z. 2012. A review on nitrogen and organics removal mechanisms in subsurface flow constructed wetlands:Dependency on environmental parameters, operating conditions and supporting media[J]. Journal of Environmental Management, 112: 429-448. DOI:10.1016/j.jenvman.2012.08.011 |
| Sasikala S, Tanaka N, Wah H S Y W, et al. 2009. Effects of water level fluctuation on radial oxygen loss, root porosity, and nitrogen removal in subsurface vertical flow wetland mesocosms[J]. Ecological Engineering, 35(3): 410-417. |
| Wu S B, Zhang D X, Austin D, et al. 2011. Evaluation of a lab-scale tidal flow constructed wetland performance:Oxygen transfer capacity, organic matter and ammonium removal[J]. Ecological Engineering, 37(11): 1789-1795. DOI:10.1016/j.ecoleng.2011.06.026 |
| Wu X H, Ge T D, Wang W, et al. 2015. Cropping systems modulate the rate and magnitude of soil microbial autotrophic CO2 fixation in soil[J]. Frontiers in Microbiology, 6. |
| 王皓, 钱琪卉, 丁瑞睿, 等. 2020.电解强化人工湿地对农村生活污水中氮磷的去除性能[J].环境工程学报: 1-12.https://kns.cnki.net/kcms/detail/11.5591.X.20200720.1818.030.html |
| 王建超, 郝瑞霞, 周彦卿. 2016. 电流对MEC-3DBER-S脱氮除磷效果的影响及机理分析[J]. 中国环境科学, 36(8): 2388-2394. |
| 王振, 齐冉, 李莹莹, 等. 2017. 潮汐流人工湿地中生物蓄磷的强化及其稳定性[J]. 中国环境科学, 37(2): 534-542. |
| Xu N, Tan G, Wang H, et al. 2016. Effect of biochar additions to soil on nitrogen leaching, microbial biomass and bacterial community structure[J]. European Journal of Soil Biology, 74: 1-8. DOI:10.1016/j.ejsobi.2016.02.004 |
| Yang W H, Weber K A, Silver W L. 2012. Nitrogen loss from soil through anaerobic ammonium oxidation coupled to iron reduction[J]. Nature Geoscience, 5(8): 538-541. |
| Yang Y, Zhao Y Q, Liu R B, et al. 2018. Global development of various emerged substrates utilized in constructed wetlands[J]. Bioresource Technology, 261: 441-452. DOI:10.1016/j.biortech.2018.03.085 |
| Yao S, Ni J R, Chen Q, et al. 2013. Enrichment and characterization of a bacteria consortium capable of heterotrophic nitrification and aerobic denitrification at low temperature[J]. Bioresource Technology, 127: 151-157. DOI:10.1016/j.biortech.2012.09.098 |
| Zhang J B, Wu P X, Hao B, et al. 2011. Heterotrophic nitrification and aerobic denitrification by the bacterium Pseudomonas stutzeri YZN-001[J]. Bioresource Technology, 102(21): 9866-9869. DOI:10.1016/j.biortech.2011.07.118 |
| Zhang X, Gang D D, Sun P, et al. 2020. Goethite dispersed corn straw-derived biochar for phosphate recovery from synthetic urine and its potential as a slow-release fertilizer[J]. Chemosphere, 262: 127861. |
| Zhu H, Yan B, Xu Y, et al. 2014. Removal of nitrogen and COD in horizontal subsurface flow constructed wetlands under different influent C/N ratios[J]. Ecological Engineering, 63: 58-63. DOI:10.1016/j.ecoleng.2013.12.018 |
| 张东晓, 吴树彪, 宋玉丽, 等. 2011. 潮汐流人工湿地床污水处理效果试验研究[J]. 中国农业大学学报, 16(6): 110-116. |
