 , 孙梦强, 林加奖
, 孙梦强, 林加奖
 , 陈祖亮
, 陈祖亮福建师范大学环境科学与工程学院, 福州 350007
收稿日期: 2018-07-28; 修回日期: 2018-10-26; 录用日期: 2018-10-26
基金项目: 国家自然科学基金(No.41501349)
作者简介: 苏炳林(1993-), 男, E-mail:1528602805@qq.com
通讯作者(责任作者): 林加奖, E-mail:jjlin@fjnu.edu.cn
摘要: 虽然绿色合成纳米材料已成功地用于去除废水中的重金属,但利用绿色合成纳米材料钝化土壤中重金属的报道很少.本文利用植物叶提取液制备纳米氧化铁(GION),并将其用于钝化土壤中重金属镉的研究,观察中、短培养周期下对镉钝化的稳定性.实验室条件下设置50%田间最大持水量培养,对照、1%、3%、9% GION 4个处理.分别于第60、120 d采样分析土壤中镉、pH、铁、酶等相关指标的变化.结果表明,GION对土壤中镉有较好的钝化效果,60 d与120 d之间有效态镉的含量无显著差异,说明GION对土壤中镉的钝化作用随时间增长相对稳定.120 d的数据显示,相比对照组,1%、3%、9% GION处理下有效态Cd(0.1 mol·L-1 CaCl2)分别降低了19.1%、16.7%、66.7%,交换态Cd(Tessier法)分别降低了12.5%、18.8%、56.3%.GION能够显著提高土壤的pH和铁的含量.pH提高能够显著降低Cd的有效性.(NH4)C2O4-Fe则分别增加了0.7、1.1、1.9倍,DCB-Fe分别增加了0.4、2.9、6.0倍.另外,随培养时间的延长,(NH4)C2O4-Fe和DCB-Fe增加而HCl-Fe2+含量降低.说明GION影响土壤中铁物种的活性,增强其生物化学过程而转化为更加稳定的形态,该过程将改变镉在土壤中的赋存形态.通过扫描电镜-能谱(SEM-EDS)发现,GION处理残渣态中Fe的含量远高于对照组,说明镉可能随铁进入残渣态.土壤中脲酶和转化酶活性升高而过氧化氢酶则没有显著的变化.该结果说明GION降低了土壤中镉的生物有效性,土壤得以恢复,从而提升了土壤酶活性.综上所述,GION具有环境友好的特点,且对镉具有稳定的钝化作用,可作为一种良好的中低污染重金属污染土壤的修复剂.
关键词:绿色合成纳米氧化铁镉原位钝化
Immobilization of cadmium in soil by green synthesized iron oxide nanoparticles
SU Binglin
 , SUN Mengqiang, LIN Jiajiang
, SUN Mengqiang, LIN Jiajiang
 , CHEN Zuliang
, CHEN Zuliang School of Environmental Science and Engineering, Fujian Normal University, Fuzhou 350007
Received 28 July 2018; received in revised from 26 October 2018; accepted 26 October 2018
Abstract: Green synthesized nanomaterials have been successfully used to remove heavy metals in wastewater, immobilizing heavy metals in soils is still unclear.In this study, iron oxide nanoparticles (GION) were prepared from euphorbia cochinchinensis extract and following used to immobilize cadmium (Cd) in soil, where soil was tested under after 60 and 120 d incubation with a 50% water hold capacity with control.Results show 1the Cd in soil were immobilized effectively by GION, and there was no significantly difference between 60 and 120 d, indicating that the immobilization of Cd by GION was stability in 60 d and 120 d incubation.At 120 d, the available Cd (0.1 mol·L-1 CaCl2) in the 1%, 3% and 9% GION treatments decreased by 19.1%, 16.7%, 66.7%, and he exchangeable Cd (Tessier) decreased by 12.5%, 18.8%, 56.3% respectively.2the pH and Fe species in soil increased with increasing GION dosage, resulting in decreasing the available of Cd effectively.With increasing in pH.The (NH4)C2O4-Fe and DCB-Fe increased by 0.4, 2.9, 6.0 times and 0.7, 1.1 and 1.9 times, respectively.In addition, in the GION treatments, (NH4)C2O4-Fe and DCB-Fe increased, while HCl-Fe2+ decreased with incubation time, indicating that GION affected the activity of iron species in soil, and enhancing its biochemical process and transform it into a more stable fractions, leading to further change the fraction of Cd in soil by SEM-EDS. Furthermore, the abundance of Fe in the 9% GION treatment was much higher than that of the control.3the activity of urease and invertase activity increased, while catalase did not change significantly, revealing that GION immobilized Cd by reducing the bioavailability of cadmium in soil, resulting in the increasing enzyme activity.Since GION is environmentally friendly and in the stable immobilizing Cd.GION could be potentially used to Cd in contaminated soil.
Keywords: green synthesisiron oxidecadmiumin situ immobilization
1 引言(Introduction)随着工业的迅速发展, 重金属污染使我国的耕地受到了严重的威胁, 土壤污染面积达到了2×107 hm2, 其中, 重金属Cd污染是一类常见的问题(向倩等2014;周琴等, 2018).镉主要来源有电镀、采矿、冶炼、燃料、电池和化学工业等排放的废水(崔红标等, 2016).镉在环境中不能被降解, 沉积到土壤之中被植物吸收通过食物链进入人体和动物体内, 会导致痛痛病、高血压、脑血管疾病和肝脏损害等.国内外的许多****对镉污染的修复进行了一系列的研究, 主要有物理化学修复、化学修复、生物修复及电动修复等, 每种修复方法有各自的优势, 这些方法对修复土壤中的Cd具有潜在的应用价值(陈卫平等, 2018).
化学钝化修复是通过金属与钝化剂发生吸附、沉淀、氧化还原和螯合作用等反应而降低其生物有效性的一种高效方法(Gueye et al., 2016).目前, 常见的钝化材料有磷酸盐和碳酸盐、生物炭、黏土矿物钝化材料膨润土、煤粉灰颗粒、海泡石、沸石等.如Huang等(2016)利用磷酸盐和碳酸盐等钝化材料修复污染土壤中Cd;Zhang等(2016)利用生物炭钝化剂修复农田中的Cd;周莉娜等(2016)利用膨润土钝化污泥中的重金属.近年来, 纳米氧化铁因其环境友好、比表面积大、活性高的优点, 被广泛用于水体和土壤的修复研究.然而, 在土壤中的绝大多数研究为纳米铁对重金属的钝化(Xue et al., 2018), 而纳米氧化铁的研究则集中在对类金属砷的修复应用, 对重金属阳离子的研究则相对较少(Hartley et al., 2004).少有的报道中证明磁铁矿和赤铁矿纳米粒子能够成功地用于土壤中镉和铅的钝化(Shipley et al., 2011).另外, 综合诸多文献报道纳米氧化铁在水体中去除重金属的能力(Hua et al., 2012), 也能够证明它在土壤中具有较大的应用潜力.
纳米氧化铁因其自身的一些缺点限制了它在环境中的应用, 如稳定性、合成成本高及试剂的环境友好性问题.近年来, 利用植物叶提取液制备纳米氧化铁解决了这些问题.绿色合成纳米氧化铁也被成功用于水体中重金属、持久性有机污染物及氮磷去除(Weng et al., 2016; Lin et al., 2018).绿色合成纳米氧化铁富含丰富的碳氧官能团和铁氧表面对阴阳离子均有显著的吸附作用(Luo et al., 2016).然而, 将绿色合成纳米氧化铁用于土壤重金属污染的修复则尚未见报道.因土壤环境的复杂性及土壤重金属污染的严峻性, 开展相关研究具有重要的意义.
本研究通过绿色合成方法制备纳米氧化铁(GION), 并研究GION对土壤中镉的钝化作用.主要内容包括通过Tessier和CaCl2两种方法来探究GION对镉的钝化效率和稳定性.进一步通过土壤pH和铁形态的变化分析Cd钝化的可能机制.最后分析土壤Cd污染在经GION修复后, 关键酶活性的响应, 以此来分析GION用于土壤重金属钝化的可行性.
2 材料与方法(Materials and methods)2.1 材料和仪器材料:Cd污染土壤选自湖南湘潭金属矿区周边农田0~20 cm深度的表层土壤.污染土壤放置在阴凉通风处, 经过自然风干, 研磨过2 mm筛, 备用.过氧化氢酶、脲酶、转化酶试剂盒购买于江苏科铭科技有限公司;重金属Cd2+溶液用氯化镉配制(CdCl2·5/2H2O, 福晨化学试剂厂)、氯化铁、无水乙酸钠、无水乙醇等药品均为分析纯.红背桂叶采摘于福建师范大学校区内.
仪器:ICP-OES测量(PerkinELmer Optima 8000)、超声波清洗器(KQ-250E, 昆山市超声波仪器有限公司)、台式恒温振荡器(THZ-320上海精宏实验设备有限公司)、重金属消解仪(SH230N山东海能科学仪器有限公司)、电子天平(BS-224S北京赛多利斯仪器系统有限公司).
2.2 纳米氧化铁(GION)的制备取30 g干燥的植物叶片(红背桂)剪碎后倒入1000 mL的烧杯中, 加入500 mL的蒸馏水, 让蒸馏水浸没树叶, 在水浴锅中恒温80 ℃煮1 h后取出, 真空抽滤过0.45 μm滤膜得到植物叶片提取液, 装入棕色瓶中置于冰箱保存备用.
绿色合成纳米氧化铁的具体操作为:将恒温水浴锅温度设定为70 ℃, 固定好烧杯和机械搅拌棒, 用量筒量取120 mL植物液提取液置于250 mL烧杯或锥形瓶中, 再去分析天平上依次称取19.68 g NaAc, 6.48 g FeCl3·6H2O加到提取液中, 搅拌反应2 h, 反应后生成黑色产物, 用真空抽滤泵抽滤, 先用水洗3次再用无水乙醇洗3次, 得到的黑色产物置于真空干燥器中烘干, 设定温度为45 ℃, 干燥过夜, 取出, 过110目的筛, 即得GION.最终通过表征可知, GION为30~80 nm大小富含碳氧官能团的纳米氧化铁颗粒, 其中各主要元素含量分别为O(42.9%)、C(32.03%)、Fe(23.19%).
2.3 土壤理化性质土壤理化性质均采用常规方法检测(鲁如坤, 2000), pH值以1:2.5的土壤-水比率测定;总有机质采用重铬酸钾氧化方法测定;土壤金属总量采用HNO3-HF-HClO4消解后, 电感耦合等离子发射光谱仪(ICP-OES)测定.结果见表 1.
表 1(Table 1)
| 表 1 土壤基本理化性质 Table 1 The physiochemical properties of soil | ||||||||||||||||||||||||||
表 1 土壤基本理化性质 Table 1 The physiochemical properties of soil
| ||||||||||||||||||||||||||
2.4 试验设计平行取100 g过2 mm尼龙筛网的污染土3份置于250 mL广口瓶中, 调节其水分含量达到50%最大田间持水量(WHC), 使其处于好氧状态.设立对照组(无GION)与1%、3%、9%按照质量比添加GION作为实验组, 60 d和120 d共8个处理.每个处理设置3组平行.放置于(25±1) ℃恒温培养箱培养, 每两天用去离子水补充损失水分, 分别于第60、120 d破坏性取样分析, 新鲜土壤样品保存在-40 ℃的环境中, 并称取一部分待测样品冷冻干燥, 研磨过100目尼龙筛待用.
2.5 分析方法2.5.1 土壤镉的提取方法分别采用Tessier五步连续提取法(Tessier, et al)和CaCl2溶液提取有效态镉.
提取Tessier法的前两步形态.可交换态:将1.00 g土壤样品加入到50 mL的离心管后, 再往离心管中加入8 mL 1 mol·L-1的MgCl2, 常温下200 r·min-1振荡1 h, 9000 r·min-1离心10 min, 移出的上清液用0.22 μm的滤膜过滤至25 mL的容量瓶中, 用去离子水定容, ICP-OES测定镉含量.碳酸盐结合态:经可交换态处理后的残余土样在离心管中再加入8 mL 1 mol·L-1的乙酸钠(用冰醋酸把pH调至5.0)浸提, 常温下200 r·min-1振荡8 h, 9000 r·min-1离心10 min, 将移出的上清液用0.22 μm的滤膜过滤至25 mL的容量瓶中, 用去离子水定容, ICP-OES测定镉含量.另外, 按照迟荪琳等(2017)的方法, 采用0.1 mol·L-1 CaCl2一步法提取有效态镉, 提取步骤同可交换态.
2.5.2 扫描电子显微镜-能谱(SEM-EDS)采用日本JEOL公司的JSM-7500型扫描电子显微镜观察在GION作用下残渣态的微观结构的SEM图.采用英国Oxford公司的INCA EDS与扫描电子显微镜连接起来检测样品的表面微区成分元素种类.其中, 残渣态为经过Tessier分级提取最后一步的固体产物.
2.5.3 土壤铁形态的分析HCl可提取态铁(HCl-Fe), 称取0.1 g土壤鲜样至50 mL离心管内, 加入5 mL的0.5 mol·L-1 HCl溶液, 25 ℃下, 200 r·min-1振荡1 h, 然后9000 r·min-1离心10 min. HCl-Fe2+的测定, 取0.05 mL上清液至5 mL离心管内, 加入2.45 mL 10 g·L-1菲啰啉, 在510 nm处测定吸光度.总HCl-Fe的测定, 取0.05 mL上清液至5 mL离心管内, 加入2 mL 10%的盐酸羟胺溶液, 加入2.5 mL乙酸钠数分钟后, 再加入2.45 mL 10 g·L-1菲啰啉, 在510 nm处测吸光度.
(NH4)2C2O4提取态铁, 称取0.5 g土样至50 mL离心管内, 加入0.2 mol·L-1 (NH4)2C2O4溶液, 25 ℃下, 200 r·min-1振荡4 h, 然后9000 r·min-1离心10 min, 取0.05 mL上清液加入2 mL 10%的盐酸羟胺溶液, 加入2.5 mL乙酸钠数分钟后再加入2.45 mL 10 g·L-1菲啰啉显色, 在510 nm处测吸光度.
DCB提取态铁, 称取0.5 g土壤样品, 置于50 mL离心管中, 加入20 mL 0.3 mol·L-1柠檬酸钠和2.5 mL 1 mol·L-1重碳酸钠, 水浴锅内加热至80 ℃, 加入0.5 g连二亚硫酸钠, 不断搅拌15 min后, 9000 r·min-1离心过滤, 取0.05 mL上清液加入2 mL 10%的盐酸羟胺溶液, 加入2.5 mL乙酸钠数分钟后再加入2.45 mL 10 g·L-1菲啰啉显色, 在510 nm处测吸光度.
2.5.4 酶的提取分析按照转化酶、过氧化氢酶、脲酶等试剂盒流程.
2.6 数据分析使用Excel 2017或Origin 8.5对所有实验数据进行分析和作图.采用SPSS 16软件对差异显著性进行检验.差异有显著性, p < 0.05, 字母abcde用于表达图表中的数据是否具有显著性差异.钝化率的计算公式见式(1).
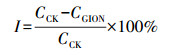 | (1) |
3 结果与讨论(Results and discussion)3.1 镉的钝化效率采用Tessier连续提取来分析GION对Cd的钝化效果.图 1a和图 1b分别为Tessier法的可交换态Cd和碳酸结合态Cd的结果.从图 1a中可以看出, 培养到60 d, 1%、3%、9% GION处理后的土壤中交换态Cd含量分别降低了14.3%、23.7%、61.2%.从第60~120 d, 可交换态Cd的含量基本趋于稳定并且1%、3%、9%的GION的钝化效率与60 d的基本持平, 1%、3%、9% GION处理后土壤中交换态Cd含量分别降低了12.5%、18.8%、56.3%, 这也再次验证了GION能长久有效的钝化土壤中的Cd, 降低了Cd的迁移性和有效性.从图 1b中可以看出, 随着培养时间的延长, 所有处理中碳酸结合态Cd总量呈增加的趋势, 但GION处理组仍明显低于对照组.以对照组为参考, 1%、3%、9% GION处理后碳酸结合态Cd的含量降低了3.69%~11.13%、14.81%~25.01%、33.33%~40.70%, 与可交换态Cd的变化趋势相似.GION添加到土壤第60 d后, 碳酸结合态Cd降低, 但处理之间的差距没有可交换态Cd之间明显.说明可交换态Cd更容易被GION钝化而进入最稳定的形态.
图 1(Fig. 1)
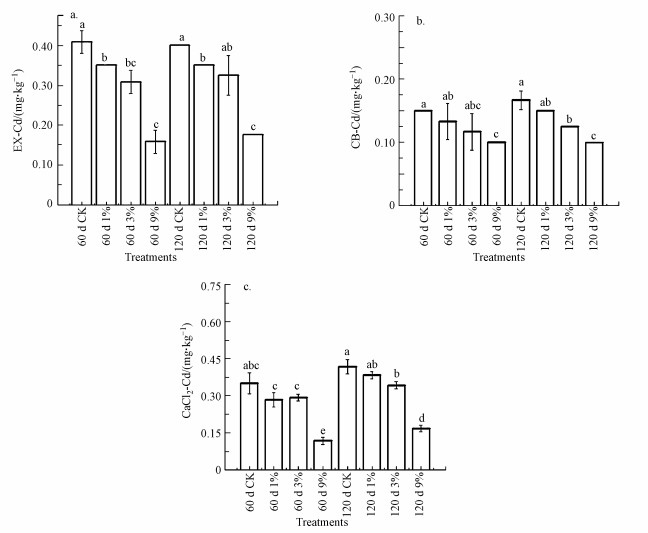 |
| 图 1 镉的形态(a.交换态;b.碳酸结合态;c.CaCl2可提取态) Fig. 1Cd fractions (a. exchangeable, b. carbonate-bound, c. CaCl2 extractable) |
另外, 再采用0.1 mol·L-1 CaCl2提取方法来分析GION对Cd的钝化效果.图 1c反映了在有GION培养下, 土壤中有效镉的变化.培养到第60 d后, 所有GION处理的土壤中生物有效性Cd的含量均降低, 1%、3%、9% GION处理土壤中Cd相比对照组含量分别降低了19.1%、16.7%、66.7%.培养至第120 d, 与对照组相比, 1%、3%、9% GION处理土壤中Cd的含量都有明显的下降.但与60 d培养对比, 120 d处理下有效镉略有上升, 说明在土壤中的其他金属离子跟Cd存在竞争关系, 所以Cd含量在后期略有上升(Shahriar et al., 2015).0.1 mol·L-1 CaCl2提取态Cd可以代表有效态Cd.总体而言, GION添加到Cd污染土壤并经过60、120 d的培养后, 不同添加量的GION均有明显的钝化效果, 特别是3%和9%处理, 达到了显著水平.有效态Cd浓度的波动可能受GION或土壤中固有组分的生物地球化学循环影响(Qasim et al., 2015; Bhattacharya et al., 2018).
3.2 残渣态SEM-EDS分析对Tessier提取残渣态进行SEM-EDS分析, 结果如图 2所示.图 2a是对照组第120 d土样Tessier提取残渣态的SEM-EDS结果, 图 2b是9% GION处理残渣态的SEM-EDS.结果显示对照组中的C、O、S、Cd、Fe元素比重分别为2.31%、42.60%、0.05%、未检出、2.40%, 而GION处理土壤中C、O、S、Cd、Fe 5种元素比重分别为2.50%、39.18%、0.10%、0.54%、4.96%.其中, GION处理下Fe含量显著增加, S和Cd也有增加的趋势.当GION进入土壤, 可通过络合作用、胶结作用固定Cd.另外Cd和Fe的增加则进一步证明了土壤在经过120 d的培养周期后, 部分Cd随Fe的生物化学过程进入到有效性较低的残渣态中, 从而达到被钝化的目的.
图 2(Fig. 2)
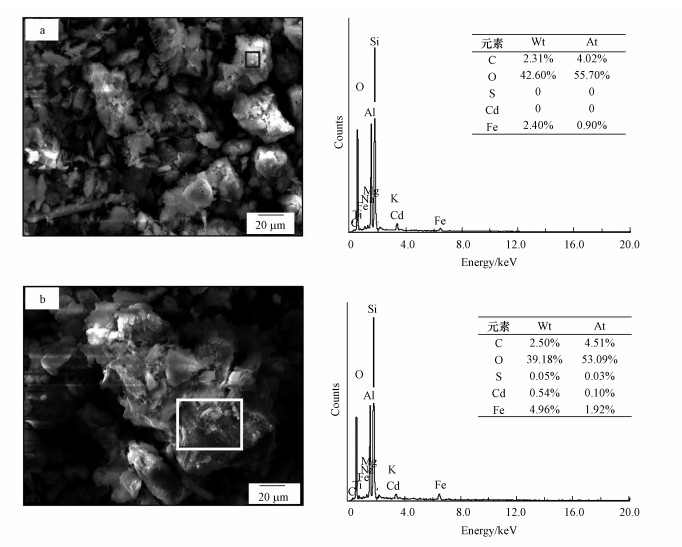 |
| 图 2 Tessier残渣态SEM-EDS(a.对照组放大5000倍EDS; b.9%GION处理放大5000倍EDS) Fig. 2The SEM-EDS images of (a.untreated residual fraction, b.GION treated residual fraction) |
3.3 pH的变化由图 3可知, 使用GION改变了土壤pH.培养到第60 d, 对照组、1%、3%、9% GION处理土壤的pH分别为4.98、5.07、5.86、6.92.培养到120 d时, 发现土壤的pH有所下降, 但GION处理组仍然高于对照组, 其中3%、9% GION处理土壤pH分别高出对照组0.62、1.87个单位, 达到显著水平.首先, GION添加使pH升高, 可能是由于GION中氧化铁发生氧化还原反应释放的铁离子发生水解反应而释放OH-(Tang et al., 2010; Huan et al., 2016).其次, 随着培养时间延长pH下降, 这可能是由于GION加入激活了一些土壤微生物, 土壤含水50%的状态下, 有机质被好氧微生物分解导致可溶性有机酸消耗了OH-, 导致pH值下降(Lefevre et al., 2014).土壤pH的变化对土壤环境中金属离子的溶解与固定起着至关重要的作用(Carla et al., 2018; Sima et al., 2018).pH升高离子态重金属减少而络合态增加, 另外, pH的降低会导致重金属碳酸结合态的溶出(Zeng et al., 2011).总体而言, 当GION投加量在3%以上时, 能够显著(p < 0.05)提高土壤pH, 使其中镉的有效性降低, 这是GION对土壤中镉钝化的解释之一.
图 3(Fig. 3)
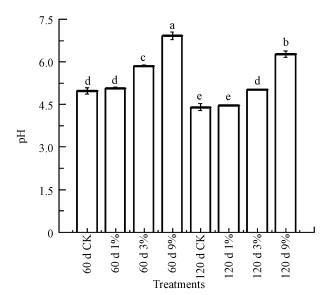 |
| 图 3 pH变化 Fig. 3The variation of pH |
3.4 铁形态的变化图 4a为(NH4)C2O4提取态Fe的变化, 由图可知, 与60 d相比, 培养120 d后, GION处理土壤中的(NH4)C2O4-Fe的含量(p < 0.05)升高, 而对照组没有显著变化.总体而言, 随GION的添加, 无定形铁的含量显著增加, 1%、3%、9% GION处理土壤无定形铁相比对照组升高了0.69、1.10、1.95倍.
图 4(Fig. 4)
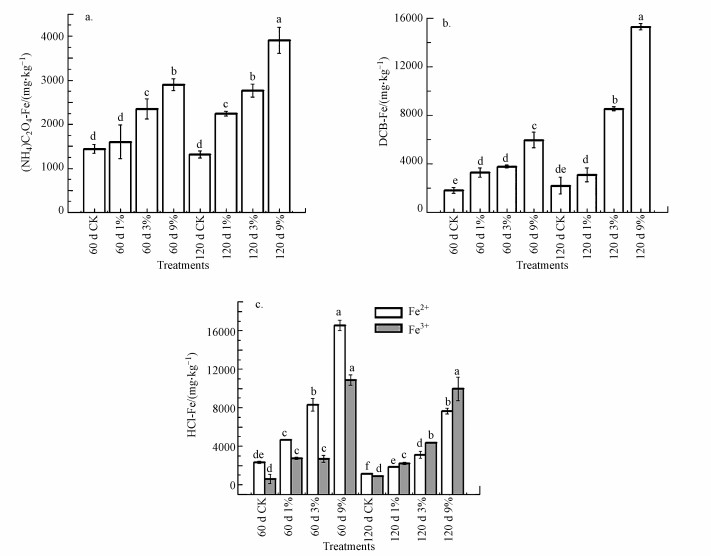 |
| 图 4 铁在土壤中的变化(a.草酸铵提取铁;b.DCB提取铁;c.HCl提取态Fe2+和Fe3+) Fig. 4The variation of Fe in soil (a.oxalate extractable Fe; b.DCB extractable Fe; c.HCl extractable Fe2+ and Fe3+) |
由图 4b可知, GION的添加改变了DCB-Fe的含量.第60 d, 1%、3%、9% GION处理土壤中DCB-Fe比对照组高出0.80、1.10、2.33倍.培养120 d后, 1%、3%、9% GION处理土壤中DCB-Fe相比于对照组分别升高了1.05、2.91、6.01倍.培养120 d中, 3%和9% GION处理较60 d的DCB-Fe显著(p < 0.05)增加.
图 4c为HCl提取态Fe的变化.培养120 d后, GION处理土壤中HCl提取态总Fe的含量明显降低.进一步对比铁的价态, 发现HCl-Fe2+的含量显著(p < 0.05)降低, 相对而言, HCl-Fe3+的含量无显著变化.
Fe(NH4)C2O4提取态Fe用于表示无定形氧化铁;DCB-Fe代表晶型、弱晶型游离氧化铁, 包含无定形氧化铁;0.5 mol·L-1 HCl-Fe则常被用于表征土壤中具有微生物活性的铁形态(Liu et al., 2015; Sulu et al., 2016), 可能包括游离和部分结构态铁矿物.显然, 在GION处理下, 随培养时间延长, (NH4)C2O4提取态Fe和DCB-Fe增加而HCl-Fe2+减少.Fe(NH4)C2O4提取态Fe作为微生物活性最高的铁形态, 它的浓度随培养时间的增加而增加, 说明GION加强了土壤微生物的活性, 其中包括铁氧化还原菌(Poulain et al., 2009;Calvarro et al., 2014). DCB-Fe含量增加进一步说明在GION添加后60~120 d培养时间段, 铁在土壤中仍然发生形态转化, 不仅包括无定形铁, 还包括晶形和弱晶形铁.这种现象随GION投加量增加而更明显.另外, 观察3种形态铁的总量可知, HCl-Fe包含范围更广的铁形态.Fe2+减少而Fe3+没有显著变化, 说明Fe2+被氧化而结合进入更加稳定的形态.重金属在土壤环境中钝化的重要环节是矿物溶解和重结晶, 以上3种铁形态的结果说明GION在进入土壤之后, 激活了铁氧化还原微生物, 经历了生物化学过程, 对镉的钝化具有重要意义.
3.5 酶活性的变化图 5a反映了土壤脲酶活性的变化, 培养第60 d, 土壤中GION含量越多则脲酶的活性越高, 这可能是由于GION的投加增强了对Cd的钝化能力, 进而降低了Cd与羟基、疏基等对酶活性位点的竞争(Li et al., 2013; Bhattacharya et al., 2018).当培养至120 d时, 对照组中脲酶活性明显降低, 这主要是随着培养时间的增加, 土壤中营养物质被消耗造成的, 继而导致土壤脲酶活性的降低, 然而, 1%、3%、9% GION处理土壤脲酶活性也有略微降低, 但仍高于对照组.同时, 从对应的雷达图可以看出, 9% GION处理土壤的脲酶活性明显高于其它两种剂量, 与对照组相比, 1%、3%、9% GION处理土壤中的脲酶活性分别提高了105.75%、130.42%、187.07%, 并且酶的变化达到了显著水平(p < 0.05).
图 5(Fig. 5)
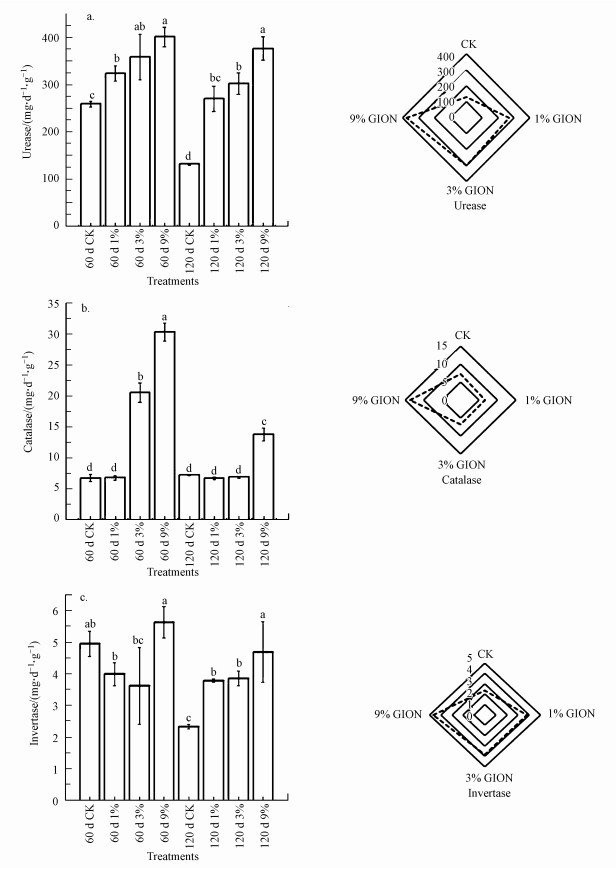 |
| 图 5 酶活性变化(a.脲酶;b.过氧化氢酶;c.转化酶) Fig. 5The changes of soil enzymatic activities. (a.Urease; b.Catalase; c.Invertase) |
图 5b为土壤过氧化氢酶活性的变化, 当处理至第60 d时, 1%、3%、9% GION处理土壤中过氧化氢酶活性分别为6.7、20.49、30.28 μmol·d-1·g-1.当处理到第120 d时, 1%、3%、9% GION处理的过氧化氢酶活性均有明显的降低, 这可能是由于土壤pH的降低导致H2O2分解(Li et al., 2013).另外, GION进入土壤环境后, 土壤环境进入稳定阶段, 导致其活性降低.从对应的雷达图可以看出, 9% GION处理相比1%、3% GION处理有明显的优势.
图 5c反映土壤中转化酶活性随时间的变化, 当培养至120 d时, GION处理土壤中转化酶活性均高于对照组土壤, 即1%、3%、9% GION处理相比于对照组分别提高了62.67%、65.04%、101.33%.由对应的雷达图可知, 9% GION处理土壤的转化酶活性明显高于1%和3% GION处理土壤.
当外源性重金属进入土壤系统后, 土壤环境中的酶表现出抑制作用、促进作用或不相关性, 因此, 一些酶的活性强弱可作为反映土壤受重金属污染状况的重要指标, 如脲酶、过氧化氢酶和转化酶(Li et al., 2013; Achuba et al., 2008).总之, GION处理过的Cd污染土壤, 土壤过氧化氢酶、脲酶、转化酶的活性得到相应地提高, 且有随着GION剂量的增加而增强的趋势.一方面, 说明GION对Cd的钝化而降低其对微生物的毒性, 另一方面则说明GION对土壤相对友好, 从酶活的角度分析并未产生破坏性的影响.
4 结论(Conclusions)1) 0.1 mol·L-1 CaCl2提取有效态Cd的含量, 发现9% GION处理下有效态Cd降低了66.7%, 交换态Cd(Tessier法)降低了56.3%.结果证明, 在经过长达120 d的培养周期之后, GION对土壤中Cd仍然具有较好的钝化效果.
2) GION的添加使污染土壤的pH显著升高, 9% GION处理土壤pH保持在6.0~7.0之间.
3) GION处理显著提高了土壤中DCB-Fe、HCl-Fe、(NH4)C2O4-Fe的含量.另外, 随着培养时间的延长, 铁的形态发生显著的变化.根据结果推测铁形态之间的转化, 最终生成稳定的晶形铁被认为是Cd在土壤中钝化的重要机制.
4) GION处理后土壤中的脲酶、转化酶的活性较比对照组显著提高.总而言之, 50% WHC条件下, GION能够钝化土壤中的Cd, 并且钝化作用稳定.土壤酶活性的响应说明GION的添加使土壤环境在一定程度上得以恢复, 绿色合成纳米氧化铁作为重金属钝化剂具有一定的应用前景.
参考文献
| Achuba F I, Peretiemo-Clarke B O. 2008. Effect of spent engine oil on soil catalase and dehydrogenase activities[J]. International Agrophysics, 22: 1. |
| Bhattacharya A, Naik S N, Khare S K. 2018. Harnessing the bio-mineralization ability of urease producing Serratia marcescens and Enterobacter cloacae EMB19 for remediation of heavy metal cadmium (Ⅱ)[J]. Journal of Environmental Management, 215: 143–152.DOI:10.1016/j.jenvman.2018.03.055 |
| Carla E R, Rufus L C, Carmen E M. 2018. Soil geochemical factors regulate Cd accumulation by metal hyperaccumulating Noccaea caerulescens (J. Presl & C. Presl) F.K. Mey infield-contaminated soils[J]. Science of the Total Environment, 616-617: 279–287.DOI:10.1016/j.scitotenv.2017.11.016 |
| 陈卫平, 杨阳, 谢天, 等. 2018. 中国农田土壤重金属污染防治挑战与对策[J]. 土壤学报, 2018, 55(2): 1–12. |
| 迟荪琳, 徐卫红, 熊仕娟, 等. 2017. 不同镉水平下纳米沸石对土壤p H、CEC及Cd形态的影响[J]. 环境科学, 2017, 38(4): 1654–1666. |
| 崔红标, 范玉超, 周静, 等. 2016. 改良剂对土壤铜镉有效性和微生物群落结构的影响[J]. 中国环境科学, 2016, 36(1): 197–205.DOI:10.3969/j.issn.1000-6923.2016.01.033 |
| Gueye M T, Di P L, G A, et al. 2016. The influence of heavy metals and organic matter on hexavalent chromium reduction by nano zero valent iron in soil[J]. Chemical Engineering Transactions, 47: 289–294. |
| Hartley W, Edwards R, Lepp N W. 2004. Arsenic and heavy metal mobility in iron oxide-amended contaminated soils as evaluated by short-and long-term leaching tests[J]. Environmental Pollution, 131: 495–504.DOI:10.1016/j.envpol.2004.02.017 |
| Hua M, Zhang S, Pan B, Zhang W, et al. 2012. Heavy metal removal from water/wastewater by nanosized metal oxides:A review[J]. Journal of Hazardous Materials, 211-212: 317–331.DOI:10.1016/j.jhazmat.2011.10.016 |
| Huang D, Xue W, Zeng G, et al. 2016. Immobilization of Cd in river sediments by sodium alginate modified nanoscale zero-valent iron:Impact on enzyme activities and microbial community diversity[J]. Water Research, 106: 15–25.DOI:10.1016/j.watres.2016.09.050 |
| Huang G Y, Su X J, Rizwan M S, et al. 2016. Chemical immobilization of Pb, Cu, and Cd by phosphate materials and calcium carbonate in contaminated soils[J]. Environmental Science & Pollution Research International, 23(16): 1–12. |
| Lefevre E, Bossa N, Wiesner M R, et al. 2016. A review of the environmental implications of in situ remediation by nanoscale zero valent iron (nZVI):behavior, transport and impacts on microbial communities[J]. Science of the Total Environment, 565: 889–901.DOI:10.1016/j.scitotenv.2016.02.003 |
| Li M, Cheng X, Guo H. 2013. Heavy metal removal by biomineralization of urease producing bacteria isolated from soil[J]. International Biodeterioration & Biodegradation, 76: 81–85. |
| Lin J, Su B, Sun M, et al. 2018. Biosynthesized iron oxide nanoparticles used for optimized removal of cadmium with response surface methodology[J]. Science of the Total Environment, 627: 314–321.DOI:10.1016/j.scitotenv.2018.01.170 |
| Liu C, Yu H Y, Liu C, et al. 2015. Arsenic availability in rice from a mining area:is amorphous iron oxide-bound arsenic a source or sink[J]. Environmental Pollution, 199: 95–101.DOI:10.1016/j.envpol.2015.01.025 |
| Luo F, Chen Z, Megharaj M, et al. 2016. Simultaneous removal of trichloroethylene and hexavalent chromium by green synthesized agarose-Fe nanoparticles hydrogel[J]. Chemical Engineering Journal, 294: 290–297.DOI:10.1016/j.cej.2016.03.005 |
| 鲁如坤. 2000. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社. |
| Poulain A J, Newman D K. 2009. Rhodobacter capsulatus catalyzes light-dependent Fe (Ⅱ) oxidation under anaerobic conditions as a potential detoxification mechanism[J]. Applied and Environmental Microbiology, 75: 6639–6646.DOI:10.1128/AEM.00054-09 |
| Qasim B, Motelica-Heino M, Bourgerie S, et al. 2015. Effect of nitrate and ammonium fertilization on Zn, Pb, and Cd phytostabilization by Populus euramericana Dorskamp in contaminated technosol[J]. Environmental Science & Pollution Research, 22(23): 18759–18771. |
| Shipley H J, Engates K E, Guettner A M. 2011. Study of iron oxide nanoparticles in soil for remediation of arsenic[J]. Journal of Nanoparticle Research, 13(6): 2387–2397.DOI:10.1007/s11051-010-9999-x |
| Sima B, Ronald J, Smernik, et al. 2018. The application of a spectrophotometric method to determine pH in acidic (pH < 5) soils[J]. Talanta, 186: 421–426.DOI:10.1016/j.talanta.2018.04.074 |
| Sulu G, Dorina S, Filip J R, et al. 2016. Cable bacteria control iron-phosphorus dynamics in sediments of a coastal hypoxic basin[J]. Environmental Science & Technology, 50(3): 1227–1233. |
| Tang X, Shen C, Shi D, et al. 2010. Heavy metal and persistent organic compound contamination in soil from Wenling:an emerging e-waste recycling city in Taizhou area, China[J]. Journal of Hazardous Materials, 173: 653–660.DOI:10.1016/j.jhazmat.2009.08.134 |
| Tessier A, Campbell P G C, Bisson M. 1979. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 51(7): 844–851.DOI:10.1021/ac50043a017 |
| Weng X, Jin X, Lin J, et al. 2016. Removal of mixed contaminants Cr(Ⅵ) and Cu(Ⅱ) by green synthesized iron based nanoparticles[J]. Ecological Engineering, 97: 32–39. |
| Xue W, Huang D, Zeng G, et al. 2018. Nanoscale zero-valent iron coated with rhamnolipid as an effective stabilizer for immobilization of Cd and Pb in river sediments[J]. Journal of Hazardous Materials, 341: 381–389.DOI:10.1016/j.jhazmat.2017.06.028 |
| 向倩, 许超, 张杨, 等. 2014. 控释尿素对污染土壤镉有效性的影响[J]. 中国环境科学, 2014, 34(12): 3150–3156. |
| Zeng F, Ali S, Zhang H, et al. 2011. The influence of pH and organic matter content in paddy soil on heavy metal availability and their uptake by rice plants[J]. Environmental pollution, 159(1): 84–91.DOI:10.1016/j.ecoleng.2016.08.003 |
| Zhang W M, Li Q X, Wen F C, et al. 2016. Remediation effects of maize-straw-derived biochar on rice grown in cadmium-contaminated soil in North China[J]. Fresenius Environmental Bulletin, 25: 602–611. |
| 周莉娜, 蔡函臻, 李荣华. 2017. 膨润土调质对污泥堆肥的脱毒及重金属钝化和雌酮消除作用[J]. 环境科学, 2017, 38(7): 3061–3069. |
| 周琴, 姜军, 徐仁扣. 2018. Cu(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)在红壤胶体和非胶体颗粒上吸附的比较[J]. 土壤学报, 2018, 55(1): 131–138. |
