听力障碍可因遗传和环境及其相互作用等多种因素导致。线粒体是真核细胞能量代谢的中心,也是细胞信号的调控中心,tRNA作为蛋白质合成过程中氨基酸的转运载体起着关键性作用。线粒体tRNA存在大量的转录后修饰(8.7%),目前已知的18种修饰位于137个不同位点,在tRNA成熟、折叠、降解及蛋白质翻译中发挥着重要功能。线粒体tRNA反密码子环37位包含i6A,t6A,ms2i6A,m1G等多种修饰,其中YRDC/OSGEPL1负责人线粒体tRNAIle、tRNAAsn、tRNALys、tRNASer(AGY)和tRNAThr的t6A修饰,TRMT5负责线粒体tRNAAla、tRNAGln、tRNALeu(CUN)、和tRNAPro的m1G修饰。
管敏鑫教授团队前期研究发现,与原核生物中负责tRNA m1G37修饰的TrmD相比,TRMT5表现出对反密码子环序列识别的宽泛性,即不要求保守的G36,仅仅识别G37,且当原有的A37突变为G37时,TRMT5也同样识别并催化修饰反应的进行,这意味着细胞内m1G37修饰可能存在tRNA反密码子环37位特异性的调节平衡(Nucleic Acids Res2016,J Biol Chem2017)。同时tRNAThrG15927A突变导致t6A37修饰水平的降低也严重影响了tRNAThr的稳态水平和氨基酰化水平,再次证明了37位修饰对维持tRNA结构与功能的重要性(Nucleic Acids Res2019)。
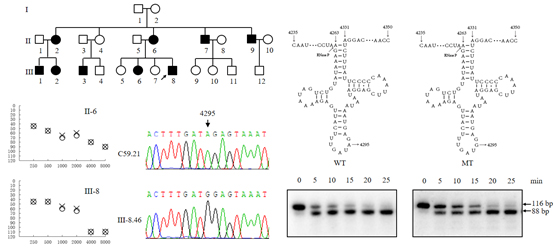
本研究针对中国汉族2651个耳聋病人以及574个正常对照进行线粒体基因测序分析,鉴定了位于线粒体tRNAIle反密码子环37的m.4295A>G突变。该家系呈现明显的母系遗传模式,14个母系成员中9人表现出不同程度的听力损伤,发病年龄23-50岁,未发现其他临床表现。序列分析表明母系成员中m.4295A>G突变均为同质性突变。Primer extention实验和体外修饰酶Trm5催化实验表明m.4295A>G引入了新的m1G37修饰,改变了原有的t6A37修饰,同时导致tRNAIle反密码子环的构象变化(Molecular Dynamics)。线粒体tRNA前体5’端体外酶切实验分析表明,该突变影响了RNase P催化的线粒体tRNAIle前体的5’末端加工效率。此次研究发现也是管敏鑫教授围绕“线粒体tRNA转录后剪切加工异常导致母系遗传性耳聋分子机制”相关研究(Nucleic Acids Res2020)的另一重大突破,是对该理论补充的又一强有力的证据。
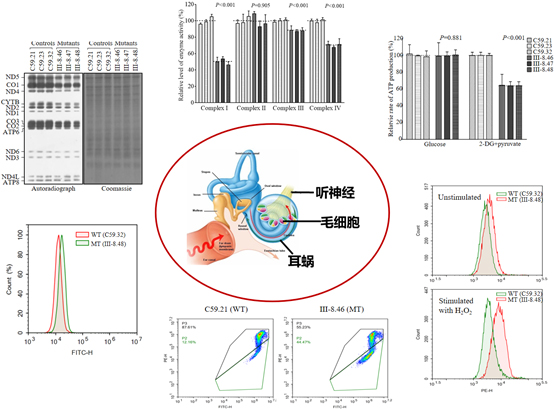
转线粒体融合细胞模型进一步研究发现该突变导致tRNAIle稳态水平和氨基酰化水平的明显下降。作为蛋白质合成中氨基酸的转运载体,tRNA结构和功能障碍导致的蛋白质合成受阻引起线粒体内蛋白稳态失衡,呼吸链复合体氧化磷酸化活性降低,氧耗速率下降,线粒体ATP合成减少,线粒体膜电位降低,活性氧水平增加及细胞凋亡水平增高。内耳的毛细胞能量代谢水平需求较高,且毛细胞对内环境离子的稳定比较敏感,突变导致的线粒体供能不足和ROS增加加剧了内耳毛细胞损伤和凋亡,影响内耳功能,最终引发耳聋。
管敏鑫教授长期从事线粒体遗传学和母系遗传性疾病的基础研究和临床转化,尤其在母系遗传性和药物性耳聋领域做出了重大贡献,在分子致病机制研究中取得了一系列具有国际领先水平的创新性成果。该成果也是管敏鑫教授全职回国加盟浙江大学后发表在顶级生物化学与分子生物学期刊《核酸研究》(Nucleic Acids Research)上的第八篇学术论文。
该研究获得国家自然科学基金和科技部重点研发计划、浙江省自然科学基金和重点研发计划等的支持。浙江大学医学院附属儿童医院孟飞龙博士和博士后周觅(现在美国德克萨斯州西南医学中心)为本文的第一作者,浙江大学医学院遗传学研究所/浙江大学医学院附属儿童医院管敏鑫教授和王猛副教授为本文通讯作者。
