研究揭示了大肠癌易感位点通过上调长非编码RNA,激活肿瘤细胞糖代谢,从而促进大肠癌发生的分子机制,为结直肠癌的治疗和预防提供了理论依据。

既往研究表明,遗传因素及环境因素均参与大肠癌发生发展。全基因组关联研究(GWAS)已发现50多个与大肠癌发生相关的单核苷酸多态性(SNP)位点,但其背后机制仍未阐明。肿瘤微环境中糖酵解的异常激活和乳酸积累与大肠癌患者预后不良相关。然而,遗传因素与肿瘤糖代谢如何共同参与大肠癌发生尚无深入研究。房静远教授、洪洁和陈豪燕研究员团队的成果正是聚焦于遗传相关lncRNA如何通过调节肿瘤糖代谢影响大肠癌的进展和治疗。
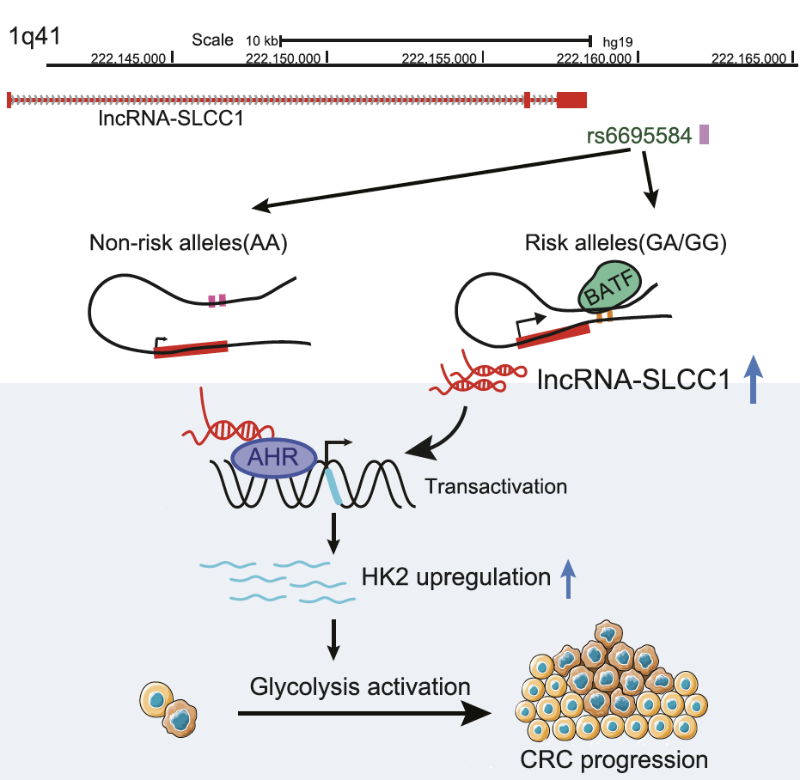
该团队利用e-QTL分析及3C实验发现SNP rs6695584位点A>G变异后lncRNA-SLCC1表达显著上调,且大肠癌组织中高表达lncRNA-SLCC1与大肠癌预后不良相关。机制研究发现,lncRNA-SLCC1通过转录激活糖酵解关键酶HK2的表达,上调大肠癌细胞糖代谢水平,进而影响大肠癌的发生发展。
该文第一作者为房静远教授博士生严婷婷,并列第一作者是洪洁研究员博士生沈超琴,张俊芳研究员博士生姜蓬垒,通讯作者为房静远教授,陈豪燕、洪洁及上海海洋大学的张俊芳研究员。
近年来,房静远教授团队在肠癌非编码RNA研究,以及表观遗传修饰和代谢紊乱参与大肠癌发生发展的基础研究和临床转化等领域均取得了令人瞩目的成绩,在Cell、Cancer Discovery、Cell Res、Clin Cancer Res、Mol Cancer、Gut和Nat Commun等期刊发表了多篇论文。
论文链接:https://www.nature.com/articles/s41392-020-00446-7
