近日,复旦大学生物医学研究院黄鑫欣课题组和美国印第安纳大学Hal Broxmeyer课题组合作在《白血病》(Leukemia)杂志上发表文章“Pharmacological activation of nitric oxide signaling promotes human hematopoietic stem cell homing and engraftment”,首次报道了一氧化氮通路在促进人源脐带血造血干细胞归巢和移植方面的作用,以及进一步运用靶向该信号通路的小分子增进临床造血干细胞移植的潜在策略。

一氧化氮是一类气体小分子,也是哺乳动物细胞中一种重要的信号分子,参与调控各种生理过程,例如突触可塑性、内皮细胞松弛和免疫反应。一氧化氮可以自由穿过细胞膜,并激活细胞质中的鸟苷基环化酶(soluble guanylate cyclase, sGC)。sGC进一步把三磷酸鸟苷(GTP)转变成环磷酸鸟苷(cGMP),cGMP充当重要的第二信使,再激活cGMP依赖性蛋白激酶(PKG),从而广泛的调节下游过程。cGMP特异性的磷酸二酯酶5(PDE5)参与降解细胞内的cGMP,使信号减弱,是一氧化氮通路的负调控因子。
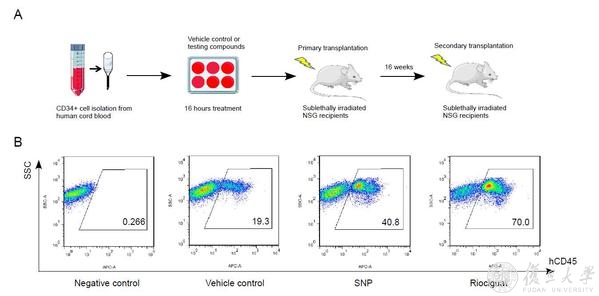
研究团队先从脐带血中分离得到富含造血干细胞和前体细胞的CD34阳性细胞,预处理SNP(一氧化氮供体)和Riociguat(sGC激动剂),再通过免疫缺陷小鼠的移植模型分析不同处理组之间在体移植的效果差异。研究发现预处理SNP和Riociguat相比对照组能够增加造血干细胞的在体移植效率,促进干细胞的长期植入。同时,运用PDE5的抑制剂Sildenafil也具有相同的效果,验证了一氧化氮通路的激活能够促进CD34阳性细胞在小鼠的骨髓中的植入效果。
通过转录组分析,研究团队发现一氧化氮信号的激活能够促进细胞迁移相关基因的表达,其中CXCR4的转录水平有显著增加。研究团队进一步验证了造血干细胞表面CXCR4蛋白水平也同样显著增加,并运用体外的细胞迁移实验发现激活一氧化氮信号通路可以促进CD34阳性细胞向SDF1的趋化迁移(chemotaxis)。最后,研究团队用在体实验证明了一氧化氮的激活能够促进造血干细胞的归巢。
该研究丰富了促进造血干细胞归巢和移植的机制,并充分阐明了一氧化氮信号通路在造血干细胞归巢过程中的重要作用,为进一步的临床应用提供理论依据。据介绍,研究团队下一步的研究目标将是临床验证这一方法的可行性。
据悉,黄鑫欣课题组的研究助理徐丹华和复旦大学附属妇产科医院主治医师杨旻为论文的共同第一作者,生物医学研究院青年研究员黄鑫欣和印第安纳大学教授Hal Broxmeyer为论文的共同通讯作者。该工作还得到了上海交通大学医学院研究员郭滨及印第安纳大学教授Maegan Capitano、万钧的大力支持。
论文链接:https://www.nature.com/articles/s41375-020-0787-z
