香港城市大學(城大)及香港大學(港大)共同領導的研究團隊,在研發基因改造人體神經幹細胞用以治療脊髓損傷方面,取得重大進展。
由於缺乏有效的臨床管理和治療方案,現時脊髓損傷的病人須忍受終身行動不便之苦。不過,聯合研究團隊發現通過修飾人體神經幹細胞中的特定基因,可改變其特性,有效激發神經再生修復的能力,令病人恢復活動機能,帶來新的治療曙光。
脊髓損傷通常由跌倒、撞車或運動意外而導致。正常情況下,脊髓神經元通過上下行通路接收傳遞來自大腦的信息。這些通路由長軸突組成,軸突將信號從大腦傳遞到脊髓,在脊髓中與中間神經元或運動神經元發生突觸傳遞,調控肌肉肢體活動和感覺機能。受損後的脊髓神經元及幼長軸突組成的通路往往產生不可逆的損傷,無法自行修復,中斷上下行信號傳輸令病人喪失活動及肢體感覺機能。
城大神經科學系助理教授兼研究團隊共同領導人劉艾佳教授說:「雖然最近通過移植人體多能性幹細胞誘導產生的神經幹細胞,在治療方面取得一定進展,但病人活動機能的復原程度有限。主要原因在於損傷部位出現惡性的微環境,促進星形膠質細胞傷疤的障礙結構形成,且成人環境缺乏神經營養因子,阻礙神經幹細胞存活、分化成為成熟的具有長軸突神經元,由此無法有效的重新建立脊髓通路,傳遞信號,從而限制了病人的活動和感覺機能復原。」
早前的研究發現高表達的SOX9基因與損傷後的惡性微環境有密切關係,是導致神經膠質形成及阻礙神經元存活、分化成功能性神經元的主要原因。聯合研究團隊發現,改造移植的神經幹細胞中SOX9基因的表達降低約50%,可有效增強人體神經幹細胞在惡性微環境中的耐受性和神經元分化能力,並在較短時間内重新建立脊髓通路。
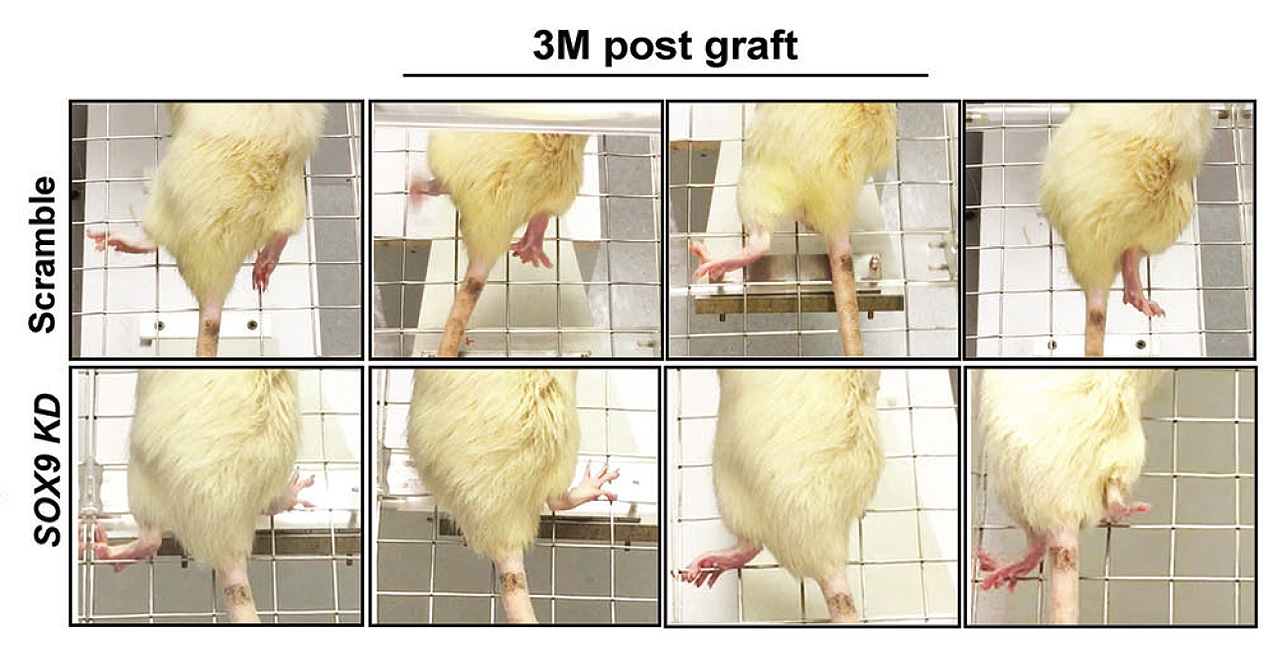
為進一步了解移植SOX9基因修飾的人體神經幹細胞是否有助恢復活動機能,團隊採用脊髓嚴重損傷大鼠模型,並利用網格步行、持續步行和感覺刺激等,測試移植後大鼠各項運動感覺能力。其中,網格步行測試是要觀察老鼠的肢體協調能力,如左右前後腳是否能正確的抓着網格;持續步行測試則是要記錄老鼠的踏步模式以了解步態和指尖末端運動能力。
相比於移植未經SOX9修飾神經幹細胞治療的大鼠,接受SOX9基因修飾神經幹細胞移植的大鼠可將受損後腳掌正確放在網格,並出現較少的錯誤。此外,這些大鼠步行通過一米長的狹窄通道時,具有良好的步態,並清楚顯示其腳掌位置及腳趾的移動,證明指尖末端運動能力恢復。
劉教授說:「我們的研究運用基因修飾的方法,改變人體神經幹細胞在活體內對損傷後惡性微環境的反應,提升細胞的耐受力和自行分化潛能,為利用神經幹細胞修復脊髓損傷帶來了新的治療方向。」
劉教授補充:「這種基因改造神經幹細胞由人體多能性幹細胞產生,可以從患者自身的細胞(如皮膚細胞或血細胞)中生成,這消除了對胚胎幹細胞的需求,也消除了與使用胚胎幹細胞相關的倫理問題。這也降低了細胞用於移植時的免疫排斥風險。」
研究論文的共同第一作者及通訊作者是劉教授及港大李嘉誠醫學院生物醫學學院副教授張知恒博士,團隊其他成員包括港大醫學院陳應城教授及城大研究員。項目獲香港研究資助局撥款資助。