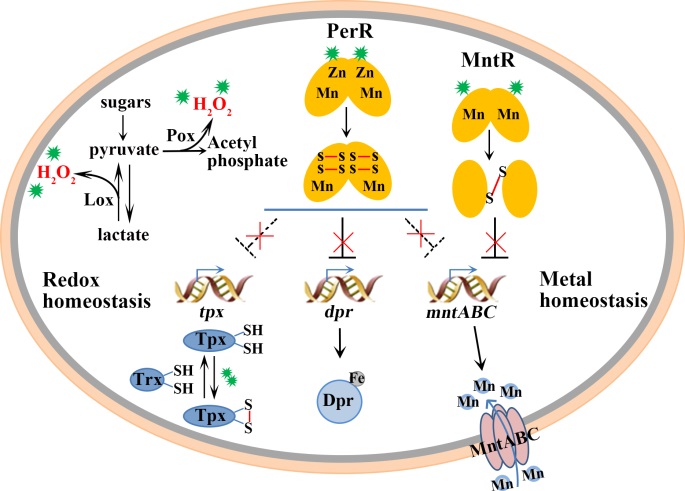
2020年3月17日,美国微生物学会权威期刊mSystems在线发表了该课题组最新研究成果“Redox-regulated adaptation ofStreptococcus oligofermentansto hydrogen peroxide stress”。该研究揭示了链球菌中独特的、H2O2敏感的半胱氨酸巯基所介导的H2O2自诱导防御的分子机制:过氧化物响应抑制蛋白PerR及锰转运抑制蛋白MntR的半胱氨酸感应胞内低浓度的H2O2,并被氧化失活从而解除对所抑制的抗氧胁迫基因(巯基氧化还原及金属离子平衡蛋白)的表达,发挥抗氧化功能(如图)。我们先前的研究证明40μMH2O2氧化锰转录调控蛋白MntR的半胱氨酸使之失活(Chen et al., J Biol Chem, 2017),本研究通过氧化还原蛋白质组学技术、Redox Western blotting、Cys点突变、免疫沉淀结合质谱分析,证实40 μMH2O2可氧化过氧化物响应抑制蛋白PerR的Cys139及Cys142残基。而PerR的半胱氨酸氧化导致其结构性锌离子丢失,使之可逆性失活,解除对其调控的巯基氧化还原(trx和tpx)及金属离子平衡等基因(dpr及mntABC)的抑制。我们的研究结果揭示链球菌为适应其胞内独特的高锰环境,PerR蛋白利用半胱氨酸氧化感应H2O2,并调控巯基氧化还原蛋白及金属离子平衡蛋白的表达,帮助触酶阴性的链球菌抵抗H2O2胁迫。
东秀珠研究员课题组长期致力于链球菌抗氧胁迫的分子机制研究,最近发现链球菌利用碳代谢物抑制蛋白CcpA同时调控葡萄糖的优先利用及H2O2产生。同时,CcpA还在转录后水平,通过调控转录通读而调控自然感受态的最适形成,使寡发酵链球菌摄取外界DNA从而增强对氧化损伤的修复,增加基因组稳定性而贡献抗氧胁迫(Wang et al., Mol Microbiol, 2019)。东秀珠团队还发现原核生物的膜整合蛋白-水通道蛋白在链球菌中与抗氧胁迫及致病性密切相关。水通道蛋白(Aquaporin,AQPs)是广泛存在于三域生命的一类跨膜蛋白,协助水及其他小分子物质,如甘油,尿素等双向扩散。1998年Peter Agre首次发现人红细胞膜上的AQP协助水分子跨膜扩散,并因此而获得2003年的诺贝尔化学奖。真核生物的AQPs协助转运H2O2及NO等,发挥信号分子作用,调控细胞的凋亡以及疾病发生。而目前原核生物AQPs的生理功能绝大部分未知。东秀珠课题组首次表明寡发酵链球菌的水通道蛋白AqpA协助H2O2双向渗透;重要的是,aqpA基因缺失显著削弱了寡发酵链球菌高氧压力下的生长,并减弱其种内及种间竞争生存能力。因此AqpA特化为一个H2O2转运蛋白,帮助触酶阴性的链球菌脱毒细胞内的H2O2,抵御氧化压力(Tonget al., J Biol Chem, 2019)。该课题组还发现肺炎链球菌的非典型甘油型水通道蛋白Pn-AqpC缺失显著影响肺炎链球菌的抗氧胁迫能力及致病性和毒力,其分子机制正在研究中。
以上所揭示的链球菌抗氧胁迫的新机制,不仅丰富了对原核生物抗氧胁迫的认识,同时对利用和控制链球菌提供了思路,尤其是低浓度H2O2介导的H2O2免疫机制及水通道蛋白新的生理功能的认知,使得口腔有益菌更好地抑制龋齿致病菌,并可为致病链球菌,如肺炎链球菌的控制提供新的作用靶点。
东秀珠课题组的副研究员佟卉春、博士生东雨竹、王新慧为论文的共同第一作者,东秀珠研究员和佟卉春副研究员为论文的共同通讯作者。该研究得到了国家自然科学基金的资助。
原文链接
