最近,研究人员通过基因组挖掘,证实来源于生防菌Trichoderma virens 的一个HRPKS基因簇(vir基因簇)负责合成环氧环己醇类新天然产物trichoxide(化合物1)。在研究该化合物的生物合成过程中,解析了一种合成芳香类聚酮化合物的新策略(图1):由HRPKS负责合成高度还原的线性聚酮产物,然后经由不同短链脱氢酶家族蛋白催化特定位置β-羟基的选择性氧化重新转变成β-酮,从而实现分子内的缩合环化,并最终芳构化形成6-取代水杨醛(化合物4)。
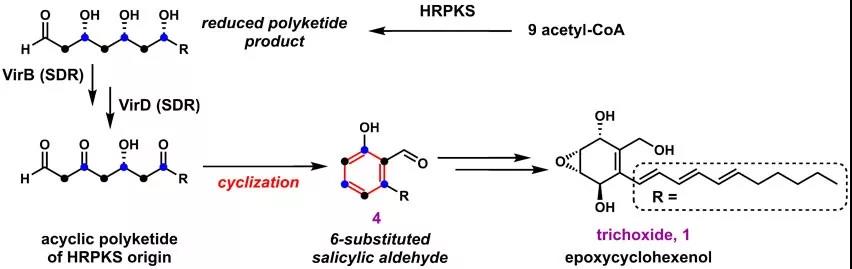
图1. 芳香类聚酮化合物的生物合成新策略
研究人员首先利用负责合成6-取代水杨醛sordarial的srd基因簇为模板对已测序真菌基因组进行生物信息学分析,搜寻到一个在许多木霉属真菌中保守的HRPKS基因簇,并选取了来自Trichoderma virens中的vir基因簇作为研究对象(图2)。通过在构巢曲霉(Aspergillus nidulans)中异源表达,确定了vir基因簇负责合成环氧环己醇类化合物1。活性测试结果显示,1具有较好的抗白色念珠菌活性。同时,vir基因簇的异源表达还产了1的生物合成中间体,即芳香类化合物2-4。
为揭示2-4的生物合成机制,研究人员先表征了HRPKS VirA的功能,其负责合成含有多羟基结构的线性聚酮化合物5(图2)。进一步,他们通过不同后修饰基因与virA的组合,先后确定了参与将5转变成4的基因,即virB和virD。体内共表达实验以及体外的生化实验均证实,VirB催化5中7-位羟基的选择性氧化形成7-位羰基化合物6,而VirD则催化6中3-位羟基的选择性氧化,形成化合物8,并经分子内aldol缩合与脱水,生成6-取代水杨醛4(图2)。有趣的是,VirD在有还原性辅因子NADH存在下可以快速将6还原成7。
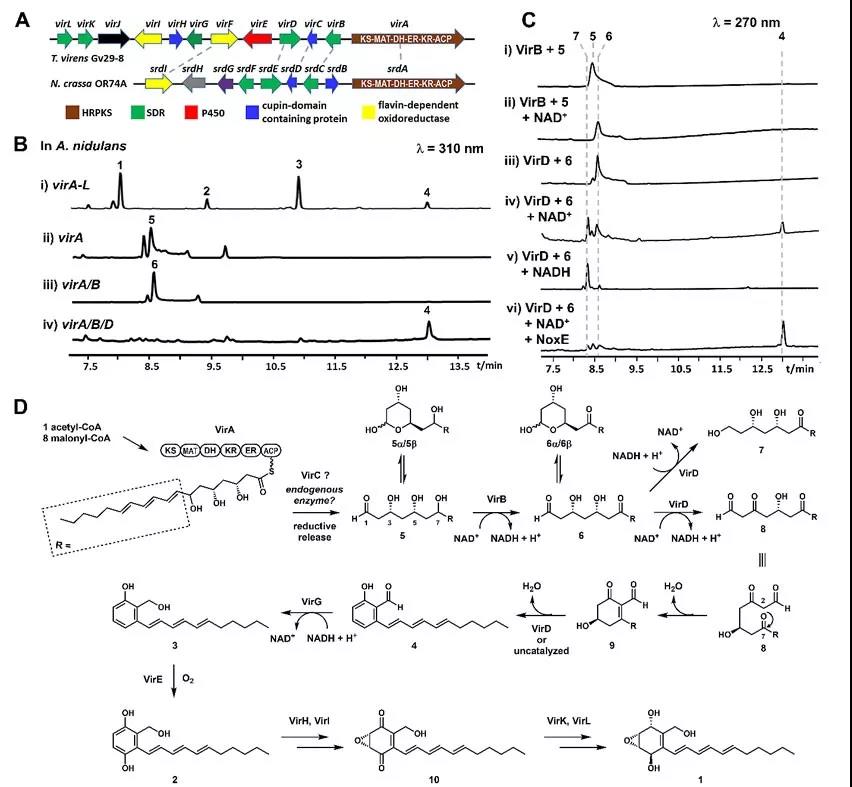
图2. Trichoxide1的生物合成
在此基础上,研究人员也对vir基因簇中其他基因的功能展开了相应的研究,并证实短链脱氢酶VirG负责4到3的转化,细胞色素P450 VirE负责3中苯环上的羟化形成2,而其他氧化还原酶VirH/I/K/L则负责2的去芳构化并将其转化成最终产物1。
该研究成果,不仅展示了一种全新的经由高度还原的线性聚酮化合物前体合成芳香类聚酮化合物的生物合成逻辑,而且也扩展了经由HRPKS途径可获得的天然产物的化学空间。
该工作主要由中科院微生物所真菌室刘玲研究员完成,美国加州大学洛杉矶分校(UCLA)的唐奕教授和上海交通大学生命科学技术学院的唐满成副教授为共同通讯作者。
