 , 马晓吉, 尚志国, 吕汪洋
, 马晓吉, 尚志国, 吕汪洋
 , 陈文兴
, 陈文兴浙江理工大学材料科学与工程学院, 杭州 310018
收稿日期: 2021-01-22; 修回日期: 2021-03-08; 录用日期: 2021-03-08
基金项目: 国家自然科学基金(No.22006136);浙江省自然科学基金(No.LQ19E090023)
作者简介: 竺哲欣(1989-), 男, E-mail: zzx@zstu.edu.cn
通讯作者(责任作者): 吕汪洋, E-mail: luwy@zstu.edu.cn
摘要:研究了氯离子存在条件下模拟太阳光活化过一硫酸盐(PMS)催化氧化模型污染物卡马西平(CBZ)的效果及机理.结果表明,无氯离子存在时,光活化PMS在30 min内只能转化25%左右的CBZ;随着氯离子浓度的增加,PMS/氯离子光催化体系对CBZ的氧化速率也迅速增加.通过电子顺磁共振(EPR)测试、活性种捕获实验等方式确定了氯离子/PMS光催化体系是以HClO为主要的氧化活性种.在无氯离子存在时,光活化PMS以1O2活性种为主.随着氯离子浓度的增加,1O2的EPR信号强度逐渐减弱,表明PMS在光照下生成的1O2易与氯离子反应生成HClO.结合超高效液相色谱-质谱法对不同反应时间的中间产物进行分析,发现CBZ转化为氯代有机副产物.
关键词:氯离子过一硫酸盐光催化反应中间产物催化机理
Effect of chloride ion on oxidation of carbamazepine by simulated sunlight activation of peroxymonosulfate
ZHU Zhexin
 , MA Xiaoji, SHANG Zhiguo, Lü Wangyang
, MA Xiaoji, SHANG Zhiguo, Lü Wangyang
 , CHEN Wenxing
, CHEN WenxingSchool of Materials Science & Engineering, Zhejiang Sci-Tech University, Hangzhou 310018
Received 22 January 2021; received in revised from 8 March 2021; accepted 8 March 2021
Abstract: The activation of peroxomonosulfate (PMS) by simulated sunlight to oxidize model pollutant carbamazepine (CBZ) in the presence of chloride ions was studied. The results showed that the photoactivated PMS could only oxidize about 25% of CBZ in 30 minutes. With increase of chloride ion concentration, the oxidation rate of CBZ enhanced obviously. It was determined that the main reaction species in chloride ion/PMS photocatalytic system was HClO by electron paramagnetic resonance (EPR) test and active species capture experiment. 1O2 played the primary role in the system without chloride ion. When the chloride ion concentration increased, the EPR intensity of 1O2 gradually weakened, indicating that PMS easily reacted with chloride ions to generate HClO. Combined with ultra-high performance liquid chromatography-mass spectrometry analysis in different reaction time, the intermediates, chlorinated organic by-products were detected.
Keywords: chloride ionperoxomonosulfatephotocatalytic reactionintermediatescatalytic mechanism
1 引言(Introduction)随着工业化的快速推进和人们生活水平的提高, 水资源的消耗和污染也日趋严重, 特别是工业废水具有成分复杂、浓度高、毒性大等特点, 因此, 有效去除工业废水中的难降解有机污染物越来越受到重视(Li et al., 2019; Sun et al., 2019; Luo et al., 2019; Zhou et al., 2019).近年来, 基于过一硫酸盐(PMS)作为氧化剂的高级氧化技术成为处理难生物降解有机污染物的重要方法之一, 并被广泛用于水处理和土壤修复领域(闫松等, 2020; Chen et al., 2020; Peng et al., 2021; Chen et al., 2021).PMS是一种在水中溶解度较高、相对稳定、无二次污染的绿色氧化剂, 可通过光、热、电等方式活化PMS产生具有强氧化能力的硫酸根自由基(·SO4-)、羟基自由基(·OH)和单线态氧(1O2)来去除有机污染物(许芬等, 2018; Wang et al., 2019; Wang et al., 2019).
在工业废水中除具有难降解有机污染物外, 还普遍存在大量的无机盐离子, 其中, 氯离子的存在对氧化去除有机污染物具有较大的影响(Huang et al., 2019; Zhang et al., 2019).研究发现, 氯离子具有较强的捕获自由基的能力, 能够与·SO4-和·OH反应生成活性氯, 如式(1)和(2)所示(Wang et al., 2020).此外, PMS也能够与氯离子直接反应生成次氯酸(HClO)来降解有机污染物(式(3))(Guo et al., 2018).在较高的氯离子浓度下, 氯离子与PMS反应直接生成氯自由基(·Cl)和HClO(式(4))(Wang et al., 2017), 其中, ·Cl具有较高的氧化还原电位(2.41 eV), 因此, ·Cl和HClO也能够有效氧化降解有机污染物.例如, Huang等(2019)通过紫外光活化PMS降解染料副产物香豆素, 发现随着氯离子浓度的增加, 体系对污染物的降解速率也逐渐增加.徐蕾等(2013)在对钴/PMS体系的研究中发现, 在较低氯离子浓度下体系对三氯苯酚的降解有一定抑制作用, 随着氯离子浓度的增加, 体系对三氯苯酚的降解速率也随之增加.尽管氯离子存在下能够增强PMS的氧化效率, 但目前对降解产物的形成、变化趋势和降解历程研究相对较少.因此, 还需要深入探究氯离子对以PMS为氧化剂的催化氧化体系的影响规律.
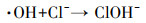 | (1) |
 | (2) |
 | (3) |
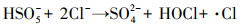 | (4) |
2 实验部分(Experimental section)2.1 试剂与仪器试剂: 卡马西平(CBZ, 分析纯)、过一硫酸氢钾(PMS, 分析纯)购于上海阿拉丁试剂有限公司; 氯化钠(NaCl, 分析纯)购于百灵威科技有限公司; 乙腈、甲醇(色谱级)购于默克化工有限公司; 5, 5-二甲基-吡咯啉-N-氧化物(DMPO, 分析纯)、2, 2, 6, 6-四甲基哌啶氧化物(TMPO, 分析纯)购于东京化成工业株式会社; 组氨酸(L-His, 分析纯)购于上海麦克林生化科技有限公司; 氢氧化钠、硫酸、叔丁醇(TBA)、硫酸铵均为分析纯, 购于高晶精细化工有限公司.
仪器: Q-Sun Xe-1型太阳光模拟反应仪(美国Westlake公司); UPLC/Synapt G2-S HDMS型超高效液相色谱-高分辨质谱联用仪(美国Waters公司); A300型电子顺磁共振波谱仪(德国Bruker公司); pH计(美国Mettler公司); 总有机碳TOC分析仪(德国Elementar公司).
2.2 光催化实验以CBZ作为模型污染物, 将20 mL 0.025 mmol·L-1的CBZ溶液置于40 mL样品瓶中, 设置氧化剂PMS浓度分别为0.2、0.3、0.4、0.5、0.6 mmol·L-1, NaCl浓度分别为0、10、50、100、300 mmol·L-1.所有反应实验均在Q-Sun Xe-1型光反应装置中进行.反应一定时间后取一定量的反应液, 经0.22 μm的聚四氟乙烯过滤头过滤后进行进一步测试.
2.3 自由基捕获实验在自由基捕获实验中, 将20 mL 0.025 mmol·L-1 CBZ溶液置于40 mL样品瓶中, 氧化剂PMS浓度为0.4 mmol·L-1, NaCl浓度为10 mmol·L-1, 分别加入浓度为10 mmol·L-1的叔丁醇、甲醇、组氨酸和硫酸铵, 分别作为羟基自由基(·OH)、羟基自由基(·OH)/硫酸根自由基(·SO4-)、单线态氧(1O2)和次氯酸的捕获剂.反应条件、取样时间间隔及取样方法与光催化降解实验相同.
2.4 光催化氧化污染物分析方法CBZ在氧化过程中的剩余浓度随反应时间的变化情况通过超高效液相色谱-高分辨质谱联用仪(UPLC-HDMS)进行分析.CBZ在一定色谱条件下, 其特征峰处的峰面积与其浓度成正比关系, 所以可通过内标法计算其剩余率:
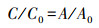 | (5) |
其中, 样品测试条件为: 毛细管电压3 kV, 锥孔电压40 V, 离子源温度130 ℃, 脱溶剂温度500 ℃, 高纯氮作为锥孔和脱溶剂气体, 流速分别为50和500 L·h-1;样品进样量为5 μL;色谱柱为HSS T3柱(1.8 μm, 2.1 mm×100 mm), 柱温35 ℃, 流速为0.3 mL·min-1.
CBZ测试的流动相及方法为: 初始为90%A(超纯水)和10%B(乙腈), 持续0.2 min, 随后8 min内流动相从10%B持续增加至90%B.
2.5 光催化氧化中间产物分析方法CBZ氧化的中间产物通过正离子模式检测, 检测条件同2.4节中的样品测试条件.测定CBZ氧化中间产物的流动相及方法同2.4节.
3 结果与讨论(Results and discussion)3.1 PMS/氯离子光催化体系氧化CBZ3.1.1 氯离子浓度的影响图 1a为不同氯离子浓度下太阳光活化PMS氧化CBZ曲线.从图中可以发现, 不存在氯离子的情况下, 反应30 min内CBZ氧化率只有25%左右.当加入氯离子浓度分别为10、50、100、300 mmol·L-1时, CBZ氧化速率明显提升, 并通过动力学拟合可得相应氯离子浓度下k值分别为0.011、0.568、1.093、4.969、5.644 min-1(图 1c).氯离子浓度为10 mmol·L-1时, 30 min内就能将CBZ氧化完全.氯离子浓度增加至50 mmol·L-1时, CBZ在10 min内就能完全氧化.随着氯离子浓度的继续增加, 体系对CBZ的氧化效果持续提高, 在100、300 mmol·L-1氯离子浓度条件下, CBZ在3 min内就能氧化完全.上述结果表明, PMS/氯离子光催化体系中少量氯离子的存在就能够显著提高太阳光活化PMS氧化CBZ的性能, 而且氯离子浓度越高, CBZ的氧化效率越快.然而氧化效率过快不利于研究其反应过程, 因此, 本文氯离子浓度取10 mmol·L-1.
图 1(Fig. 1)
 |
| 图 1 不同氯化钠浓度(a)、PMS浓度(b)对CBZ氧化效果的影响及对应的动力学拟合(c、d) (如无特殊说明, NaCl浓度为10 mmol·L-1, PMS浓度为0.4 mmol·L-1, CBZ浓度为0.025 mmol·L-1) Fig. 1Effect of NaCl concentration(a) and PMS concentration(b) on the oxidation of CBZ and corresponding kinetic fit(c, d) |
3.1.2 PMS浓度的影响PMS在太阳光活化下可分解产生具有强氧化能力的自由基, 因此, PMS浓度是影响体系氧化CBZ的重要参数之一.本文通过加入不同初始浓度的PMS来考察不同PMS用量下PMS/氯离子光催化体系对CBZ氧化性能的影响, 结果如图 1b所示.由图可知, 在10 mmol·L-1氯离子存在条件下, 随着PMS初始浓度的增加(0.2~0.6 mmol·L-1), 体系对CBZ的氧化率逐渐增加.当PMS浓度为0.2、0.3、0.4 mmol·L-1时, 30 min内CBZ的氧化率分别为33%、83%、100%.当PMS浓度达到0.5、0.6 mmol·L-1时, CBZ在10 min内就能被氧化完全.通过动力学拟合可得当PMS浓度分别为0.2、0.3、0.4、0.5、0.6 mmol·L-1时, 对应k值分别为0.013、0.162、0.568、2.182、4.189 min-1(图 1d).因此, 本研究PMS浓度取0.4 mmol·L-1.
3.1.3 pH的影响在不同废水环境下, pH值是影响催化氧化反应的重要因素之一.为研究pH值对PMS/氯离子光催化体系氧化CBZ的影响, 调节溶液初始pH分别为3.0、7.0和10.0, 分别测试在酸性、中性及碱性条件下PMS/氯离子光催化体系对CBZ的氧化性能(其中, PMS浓度为0.4 mmol·L-1, NaCl浓度为10 mmol·L-1).如图 2a所示, 在酸性、中性及碱性条件下, PMS/氯离子光催化体系均能有效氧化CBZ, 并通过动力学拟合得出在初始pH为3、7、10时, 对应的k值分别为0.757、0.568、0.381 min-1(图 2b).可见在酸性条件下该光催化体系的氧化反应速率较中性及碱性条件下高, 且碱性条件下反应速率相对较低.这可能是由于酸性条件下水溶液中含有大量氢离子, 促进了次氯酸的形成, 从而提高了氧化反应速率.
图 2(Fig. 2)
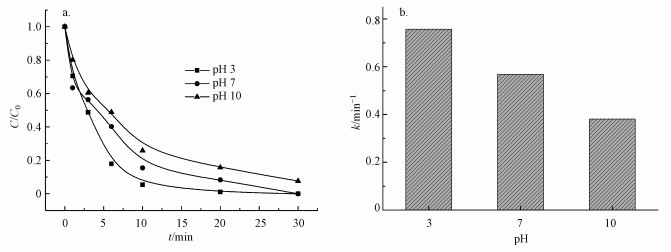 |
| 图 2 初始pH对PMS/氯离子光催化体系氧化CBZ的影响(a)及动力学拟合(b) Fig. 2Effect of pH on the oxidation of CBZ in PMS/chloride ion photocatalytic system(a) and kinetic fit(b) |
3.2 PMS/氯离子光催化体系的催化机理分析为了确定PMS/氯离子光催化体系中究竟是哪些活性种在催化CBZ过程中起主要作用, 本研究进行了捕获剂实验和EPR测试.在反应溶液中分别加入10 mmol·L-1的L-His、TBA和MeOH, 分别用于捕获1O2(肖彤等.2021)、·OH和·OH/·SO4-.为了明确体系中是否产生HClO活性种, 在反应体系中加入10 mmol·L-1的(NH4)2SO4作为HClO的捕获剂, 这是因为HClO能够与NH4+反应生成氯胺, 而氯胺的氧化能力要远远弱于HClO(Dodd et al., 2008).由图 3可知, 当加入L-His和(NH4)2SO4时, 反应体系的催化速率明显受到抑制, 30 min内CBZ的转变率只有20%左右.当加入TBA、MeOH时, 反而促进了反应体系的催化速率, 这可能是由于TBA和MeOH捕获了·OH和·SO4-, 减少了ClOH-和·Cl的生成, 使PMS与氯离子反应生成更多的HClO, 从而加速了反应的进行.
图 3(Fig. 3)
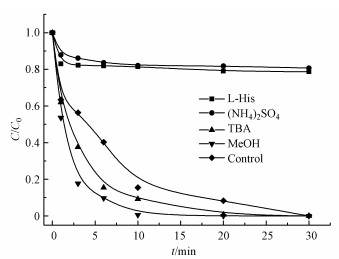 |
| 图 3 不同自由基捕获剂对PMS/氯离子光催化体系氧化CBZ的影响 Fig. 3Effect of different scavengers on the oxidation of CBZ by PMS/chloride ion photocatalytic system |
为了进一步证实PMS/氯离子光催化体系中的活性种, 以DMPO和TMPO分别作为·OH和1O2的自旋捕捉剂, 通过EPR波谱检测两者的自由基加合物.如图 4a所示, TMPO作为1O2的捕获剂, 当催化体系中仅加入PMS不加入氯离子时, 检测到较强的TMPO的加合物TMPO-1O2的峰型(Kang et al., 2020).随着氯离子浓度的增加, 加合物TMPO-1O2的强度逐渐减弱.图 4b所示为不加入氯离子时检测到较弱的DMPO与·OH加合物的峰型(Chen et al., 2020), 由于自由基强度较弱, DMPO与·SO4-加合物的峰型不明显.随着氯离子浓度的增加, DMPO-·OH加合物的峰型消失, 在较高氯离子浓度下出现了一些不规则的加合物的峰型, 可能是由于氯离子浓度高导致DMPO被过度氧化所致.
图 4(Fig. 4)
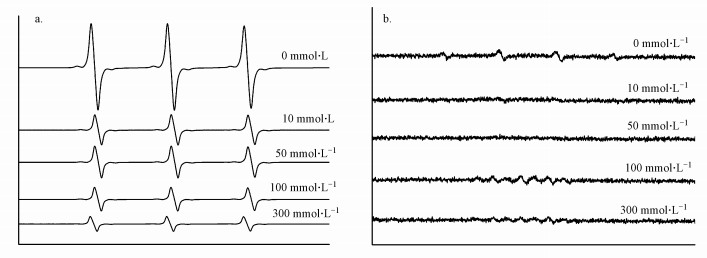 |
| 图 4 不同氯离子浓度下PMS/氯离子光催化体系中1O2(a)和自由基(b)的EPR检测 Fig. 4EPR identification of 1O2 (a) and free radical (b) of PMS/chloride ion photocatalytic system in different NaCl concentration |
结合捕获剂实验及EPR测试结果表明, 不存在氯离子时, 太阳光活化PMS主要生成1O2(式(6))(Wang et al., 2017)和少量的·OH和·SO4-, 然而1O2对CBZ的氧化能力较弱, 因此, 只存在PMS时体系对CBZ的氧化率较低.随着氯离子的加入, 所生成的1O2与氯离子反应生成具有较强氧化能力的HClO(式(7))(Wang et al., 2020), 因此, 随着氯离子浓度的增加, 1O2的强度逐渐减弱.当加入1O2捕获剂L-His时, 抑制了1O2与氯离子的反应, 减少了HClO的生成, 因此, 催化体系的反应速率明显受到抑制.同时, (NH4)2SO4作为HClO捕获剂的加入也使得催化体系的反应速率明显受到抑制, 说明PMS/氯离子光催化体系以HClO作为主要的氧化活性种.
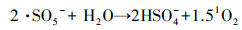 | (6) |
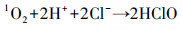 | (7) |
表 1(Table 1)
| 表 1 PMS/氯离子光催化体系氧化CBZ的产物 Table 1 Oxidation of CBZ products by PMS/chloride ion photocatalytic system | ||||||||||||||||||||||||||||||||||||
表 1 PMS/氯离子光催化体系氧化CBZ的产物 Table 1 Oxidation of CBZ products by PMS/chloride ion photocatalytic system
| ||||||||||||||||||||||||||||||||||||
图 5(Fig. 5)
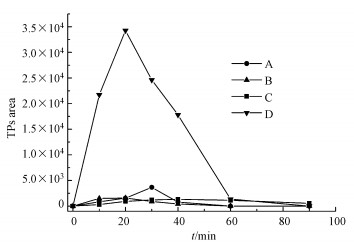 |
| 图 5 PMS/氯离子光催化体系中间产物变化趋势 (可完全去除的产物) Fig. 5Trend of transportation products over time on PMS/chloride ion photocatalytic system(Completely removed) |
图 6(Fig. 6)
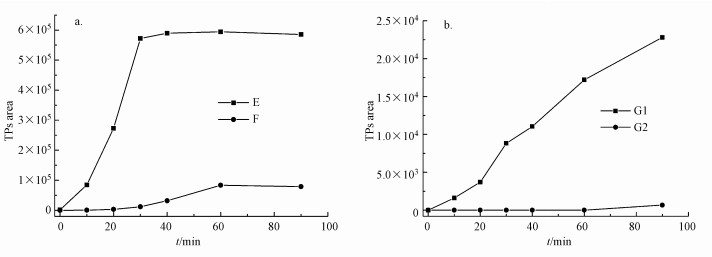 |
| 图 6 PMS/氯离子光催化体系中间产物变化趋势 (不可完全去除的产物) Fig. 6Trend of transportation products over time on PMS/chloride ion photocatalytic system(Cannot be completely removed) |
3.4 CBZ光催化氧化历程分析根据所检测到的CBZ中间产物, 推测PMS/氯离子光催化体系氧化CBZ可能的催化氧化反应历程(图 7).从催化机理部分可知, PMS/氯离子光催化体系主要以1O2和HClO为主要活性种.CBZ分子被1O2和HClO氧化, 其中, CBZ中心杂环的烯属双键容易被氧自由基进攻, 发生加氧反应生成化合物A, 而HClO进攻CBZ上的苯环结构生成氯代化合物B.因此, 在PMS/氯离子光催化体系中CBZ被迅速转化.化合物A接着发生环缩合反应形成化合物C(Chiron et al., 2006).化合物D则是通过化合物C脱去一个CONH2基团所形成, 然后继续被氧化为化合物E.随后化合物E经1O2和HClO分别氧化生成化合物F和G(Zhu et al., 2016; Zhu et al., 2020), 其中, 化合物G也可通过化合物B进一步分解得到.
图 7(Fig. 7)
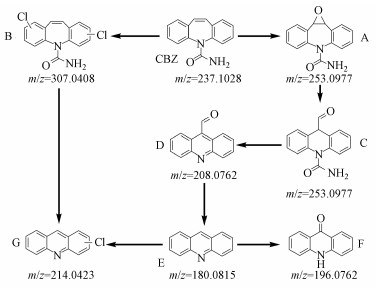 |
| 图 7 PMS/氯离子光催化体系催化CBZ的历程分析 Fig. 7Possible catalysis pathway of CBZ on PMS/chloride ion photocatalytic system |
3.5 PMS/氯离子光催化体系对污染物的矿化率为研究氯离子对PMS/氯离子光催化体系氧化CBZ矿化度的影响, 本文对比了无氯离子存在和有氯离子存在下体系对CBZ的矿化率.如图 8所示, PMS浓度为0.4 mmol·L-1时, 将反应时间延长至90 min, 未加入氯离子时TOC去除率为26%, 在氯离子存在下(10 mmol·L-1)TOC去除率为28%, 矿化率并没有随着氯离子的加入而显著提升.表明尽管氯离子的存在能够加速CBZ的氧化, 然而所生成的氧化中间产物并未能进一步有效矿化.
图 8(Fig. 8)
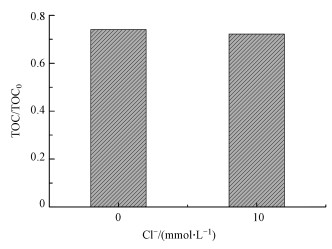 |
| 图 8 PMS/氯离子光催化体系对CBZ的TOC去除率 Fig. 8TOC removal efficiency of CBZ on PMS/chloride ion photocatalytic system |
4 结论(Conclusions)在PMS/氯离子光催化体系中, 随着氯离子浓度的增加, 模型污染物CBZ的浓度快速下降, 而无氯离子存在时30 min内CBZ只能转变25%左右.通过EPR及捕获剂实验可知, 氯离子存在下其催化机理主要是1O2和HClO的共同作用, 且随着氯离子浓度的增加, 1O2的强度逐渐降低, HClO的含量增加, 从而对CBZ的氧化率也快速增加.尽管CBZ在PMS/氯离子光催化体系中能够被快速氧化, 但生成的氧化中间产物中含有具有潜在毒性的氯代副产物, 且浓度随着反应的进行持续增加.在有氯离子存在条件下, TOC去除率也并未显著提升.因此, 在设计以PMS作为氧化剂的催化体系时, 应考虑催化体系在氧化含氯有机废水时避免氯代副产物的产生或将生成的氯代副产物继续降解矿化.
参考文献
| Anipsitakis G P, Dionysiou D D, Gonzalez M A, et al. 2006. Cobalt-Mediated activation of peroxymonosulfate and sulfate radical attack on phenolic compounds.Implications of chloride ions[J]. Environmental Science & Technology, 40: 1000. |
| Chen M, Huang Z, Liang S, et al. 2021. Immobilized Co2+ and Cu2+ induced structural change of layered double hydroxide for efficient heterogeneous degradation of antibiotic[J]. Journal of Hazardous Materials, 403: 123554. DOI:10.1016/j.jhazmat.2020.123554 |
| Chen P, Gou Y, Ni J, et al. 2020. Efficient ofloxacin degradation with Co(Ⅱ)-doped MoS2 nano-flowers as PMS activator under visible-light irradiation[J]. Chemical Engineering Journal, 401: 125978. DOI:10.1016/j.cej.2020.125978 |
| Chen T, Zhu Z, Zhang H, et al. 2020. Facile construction of a copper-containing covalent bond for peroxymonosulfate activation: Efficient redox behavior of copper species via electron transfer regulation[J]. ACS Applied Material & Interfaces, 12: 42790-42802. |
| Chiron S, Minero C, Vione D, et al. 2006. Photodegradation processes of the antiepileptic drug carbamazepine, relevant to estuarine waters[J]. Environmental Science & Technology, 40: 5977-5983. |
| Dodd M C, Von G U. 2008. Reactions of chlorine with inorganic and organic compounds during water treatment-Kinetics and mechanisms: A critical review[J]. Water Research, 42: 13-51. DOI:10.1016/j.watres.2007.07.025 |
| Guo Y, Zeng Z, Zhu Y, et al. 2018. Catalytic oxidation of aqueous organic contaminants by persulfate activated with sulfur-doped hierarchically porous carbon derived from thiophene[J]. Applied Catalysis B: Environmental, 220: 635-644. DOI:10.1016/j.apcatb.2017.08.073 |
| Huang Y, Sheng B, Yang F, et al. 2019. Chlorine incorporation into dye degradation by-product (coumarin) in UV/peroxymonosulfate process: A negative case of end-of-pipe treatment[J]. Chemosphere, 229: 374-382. DOI:10.1016/j.chemosphere.2019.05.024 |
| Kang J, Zhou L, Duan X, et al. 2020. Catalytic degradation of antibiotics by metal-free catalysis over nitrogen-doped graphene[J]. Catalysis Today, 357: 341-349. DOI:10.1016/j.cattod.2018.12.002 |
| 李坤, 刘佳蒙, 宋弼尧, 等. 2017. 高锰酸盐复合药剂预氧化对摇蚊幼虫DBPsFP的去除控制研究[J]. 环境科学学报, 37(1): 249-253. |
| Li X, Bai J, Li J, et al. 2019. Efficient TN removal and simultaneous TOC conversion for highly toxic organic amines based on a photoelectrochemical-chlorine radicals process[J]. Catalysis Today, 335: 452-459. DOI:10.1016/j.cattod.2019.01.066 |
| Luo J, Liu T, Zhang D, et al. 2019. Combining solar irradiation with chlorination enhances the photochemical decomposition of microcystin-LR[J]. Water Research, 159: 102-110. DOI:10.1016/j.watres.2019.05.019 |
| Peng G, Qi C, Wang X, et al. 2021. Activation of peroxymonosulfate by calcined electroplating sludge for ofloxacin degradation[J]. Chemosphere, 266: 128944. DOI:10.1016/j.chemosphere.2020.128944 |
| Sun P, Meng T, Wang Z, et al. 2019. Degradation of organic micropollutants in UV/NH2Cl advanced oxidation process[J]. Environmental Science & Technology, 53: 9024-9033. |
| Wang S, Liu Y, Wang J, et al. 2019. Peroxymonosulfate activation by Fe-Co-O-Codoped graphite carbon nitride for degradation of sulfamethoxazole[J]. Environmental Science & Technology, 54: 10361-10369. |
| Wang S, Xu L, Wang J, et al. 2019. Nitrogen-doped graphene as peroxymonosulfate activator and electron transfer mediator for the enhanced degradation of sulfamethoxazole[J]. Chemical Engineering Journal, 375: 122041. DOI:10.1016/j.cej.2019.122041 |
| Wang S, Wang J. 2020. Peroxymonosulfate activation by Co9S8@S and N co-doped biochar for sulfamethoxazole degradation[J]. Chemical Engineering Journal, 385: 123933. DOI:10.1016/j.cej.2019.123933 |
| Wang Z, Feng M, Fang C, et al. 2017. Both degradation and AOX accumulation are significantly enhanced in UV/peroxymonosulfate/4-chlorophenol/Cl-system: two sides of the same coin?[J]. RSC Advances, 7: 12318-12321. DOI:10.1039/C7RA01294B |
| 肖彤, 马捷, 王雁, 等. 2021. 铁改性掺氮碳纤维活化过一硫酸盐降解双酚A[J]. 环境科学学报. DOI:10.13671/j.hjkxxb.2020.0543 |
| 徐蕾, 袁瑞霞, 郭耀广, 等. 2013. 氯离子对钴/单过氧硫酸盐体系降解2, 4, 6-三氯苯酚的影响[J]. 武汉大学学报(理学版), 59: 51-56. |
| 许芬, 陈家斌, 张书源, 等. 2018. 丙酮活化过一硫酸盐性能及非自由基机制[J]. 环境科学学报, 38(11): 4333-4339. |
| 闫松, 张成武, 袁芳, 等. 2020. 氮掺杂碳纳米管的合成及活化过一硫酸盐的性能与机理[J]. 高等学校化学学报, 41(11): 2503-2510. |
| Zhang X, He J, Lei Y, et al. 2019. Combining solar irradiation with chlorination enhances the photochemical decomposition of microcystin-LR[J]. Water Research, 159: 324-332. DOI:10.1016/j.watres.2019.05.030 |
| Zhou S, He J, Bi X, et al. 2019. Kinetics of inhibition of dichlorophenol oxidation by NaCl over Fe-Cu-pillared clay[J]. Journal of Environmental Engineering, 145: 04019053. DOI:10.1061/(ASCE)EE.1943-7870.0001550 |
| Zhu Z, Chen Y, Gu Y, et al. 2016. Catalytic degradation of recalcitrant pollutants by Fenton-like process using polyacrylonitrile-supported iron(Ⅱ) phthalocyanine nanofibers: Intermediates and pathway[J]. Water Research, 93: 296-305. DOI:10.1016/j.watres.2016.02.035 |
| Zhu Z, Lu W, Xu T, et al. 2020. High-valent iron-oxo complexes as dominant species to eliminate pharmaceuticals and chloride-containing intermediates by the activation of peroxymonosulfate under visible irradiation[J]. Catalysis Letters, 150: 1355-1367. DOI:10.1007/s10562-019-03047-4 |
